Неходжкинская лимфома яичка - клиника, прогноз
Добавил пользователь Владимир З. Обновлено: 10.01.2026
Лимфома Ходжкина (лимфогранулематоз) — это онкологическое заболевание, поражающее лимфоциты и разрушающее иммунную систему пациента. При своевременном начале лечения стойкой ремиссии удаётся добиться почти в 90% случаев.
Акции
Полное обследование на онкологические заболевания для мужчин и женщин.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Содержание статьи:
Лимфомы – это группа злокачественных опухолей, поражающих лимфатическую систему, отвечающую в здоровом организме за иммунитет. Одним из первых и типичных признаков этих опухолевых патологий является безболезненное увеличение лимфатических узлов до 20 мм и более в разных частях тела.
Лимфомы, аналогично другим злокачественным образованиям, обладают способностью к метастазированию как с током крови либо лимфы, так и прорастая контактным путем в неповрежденные ткани, где затем размножаются раковые клетки. Диагноз любого вида лимфомы устанавливается только по результатам морфологического исследования ткани, взятой из опухоли в ходе биопсии.
Лимфома Ходжкина: что это за болезнь
Это злокачественное заболевание получило свое название по имени первооткрывателя. Впервые Томас Ходжкин описал эту лимфому еще в 1832 году. Сегодня в научном мире ее называют лимфогранулематозом – это процесс злокачественной гиперплазии (разрастания) лимфоидной ткани. Ключевым признаком патологии считают образование гранулем, в которых находят клетки Березовского-Штернберга.
При лимфогранулематозе увеличиваются пакеты лимфоузлов в разных частях тела: чаще страдают надключичные группы, нижнечелюстные узлы или медиастенальные. Также типично увеличение в объеме селезенки, постоянное повышение температуры, зуд кожи, потеря веса и выраженная слабость.
На сегодня лимфома Ходжкина – одно из наиболее изученных злокачественных новообразований. С 70-х годов прошлого века она утратила статус неизлечимой патологии. Если лечение начато своевременно, выживает до 98% пациентов, рецидивирует опухоль крайне редко.
По данным общемировой статистики ходжкинская лимфома возникает с частотой 2,2 на 100 тысяч населения. Обычно болеют молодые люди в возрасте до 30 лет или лица старше 60 лет. Мужчины почти в два раза чаще, нежели женщины. После лейкемии лимфогранулематоз занимает второе место по встречаемости.
Причины развития Лимфомы Ходжкина
Аргументы, которые приводятся в пользу вирусного происхождения лимфомы – при ней часто выявляется ранее перенесенный мононуклеоз (в крови есть антитела к вирусу Эпштейна-Барр и около 20% клеток Березовского-Штернберга также содержат частицы вируса). Также рассматривается влияние ретровирусов, включая ВИЧ.
В пользу наследственной теории говорит тот факт, что выявлены семейные случаи лимфомы Ходжкина с выявление определенных генетических маркеров.
По данным иммунологической теории считается, что при переносе материнских лимфоцитов через плаценту к плоду, у него развиваются реакции иммунопатологического типа.
Возможно влияние внешних мутагенов – токсинов, излучений, препаратов в патогенезе этой формы лимфомы.
Считается, что лимфогранулематоз возникает при дефиците Т-клеточного иммунитета, так как при ее развитии страдают клетки и меняется соотношение Т-клеток хелперов с супрессорами. Ключевыми признаками, точно определяющими болезнь, считаются клетки Березовского-Штернберга или их предшественники – клетки Ходжкина в сочетании с поликлональными лимфоцитами, эозинофилами и плазматическими клетками.
Изначально опухоль имеет один очаг в лимфоузлах, но затем метастазирует, формируя поражения легких, пищеварения, костного мозга или почек.
Классификация лимфомы Ходжкина
Гематологами различаются различные типы лимфомы:
- локальная (либо изолированная) – поражается только одна группа лимфоузлов;
- генерализованная – злокачественное прорастание в ткани (печень, селезенка, кожа, желудок, легкие).
По локализации можно соответственно выделить несколько форм лимфогранулематоза:
- периферический;
- легочный;
- медиастенальный;
- костный;
- кожный;
- абдоминальный;
- желудочно-кишечный;
- нервный вариант патологии.
По скорости развития патологии лимфома Ходжкина может иметь острое течение (развивается всего за несколько месяцев до терминального состояния), либо хроническое (с затяжным развитием симптомов, чередованием обострений с периодами ремиссии).
Также в современных клинических рекомендациях выделяют 4 основных гистологических формы болезни, которые определяют по данным биопсии и подсчета соотношения клеток. Это:
- преобладание лимфоцитов (или лимфогистиоцитарная стадия);
- нодулярный склероз;
- смешанноклеточная;
- истощение лимфоцитов.
Стадирование лимфомы Ходжкина
По клинической классификации, в основе которой лежит распространенность опухоли, можно делать прогноз относительно эффективности лечения. Согласно этой классификации лимфогранулематоз делят на четыре стадии:
- Стадия I или локальная: поражение расположено только в одной группе лимфоузлов или поражает один орган.
- Стадия II или регионарная: поражаются две группы лимфоузлов или больше, либо страдает один орган с прилегающими к нему лимфоузлами.
- Стадия III или генерализованная: лимфоузлы поражены с обеих сторон от области диафрагмы. Также поражается один из органов, ткань селезенки.
- Стадия IV или диссеминированная: поражения расположены в нескольких органах и одновременно страдают их лимфоузлы.
Если имеются общие симптомы лимфомы в течение последнего полугода (потеря веса, лихорадка, потливость), к стадии добавляют букву А, если нет – В.
Симптомы лимфогранулематоза
Одним из типичных симптомов считается увеличение в размерах лимфоузлов, которые расположены под кожей и доступны для прощупывания. Чаще всего увеличиваются лимфоузлы в области подмышек, паха, бедренные. Сами лимфоузлы плотные по консистенции, они подвижны, не болят, не спаяны друг с другом, с кожными покровами и тканями, имеют вид цепочек.
Примерно у пятой части пациентов изначально увеличиваются лимфоузлы в грудной клетке (медиастенальные). Тогда может возникать нарушение глотания, одышка, сухой кашель. При поражении узлов в забрюшинном пространстве или мезентериальных, будет боль в животе, отек ног.
У четверти пациентов страдает легочная ткань. Могут возникать явления пневмонии, образуются полости, а при захвате плевры – признаки плеврита с экссудацией (скопление жидкости в полости плевры).
Если поражаются кости, чаще всего страдает грудина, позвоночник, ребра или тазовые кости, реже вовлекаются черепа и трубчатые кости. Возникают боль в костях, изменения позвонков. Поражение костного мозга ведет к понижению тромбоцитов, анемии и лейкопении.
Лимфома в области пищеварительной системы ведет к повреждению мышечного слоя кишки, образованию язвенных дефектов слизистой с кровотечениями. Это может приводить к образованию отверстий в стенке кишки и перитониту. Если поражается печень, повышается уровень ферментов, увеличивается размер органа. Если вовлекается спинной мозг, возможны параличи. При терминальной стадии возможны поражения кожи, груди, яичников или яичек, сердца, матки, щитовидной железы, глаз.
Диагностика лимфомы Ходжкина
При наличии типичных признаков – увеличенных лимфоузлов, печени с селезенкой, похудением, лихорадкой, необходимо проведение полного обследования. Основу постановки диагноза составляет исследование биопсийного материала – забора материала из лимфоузлов, выполнение торако-, лапароскопии с забором образцов.
Диагноз подтверждается обнаружением типичных изменений и клеток Березовского. Если выявлены клетки Ходжкина, это может стать предположением лимфомы, но не дает повода для начала лечения.
При лимфоме Ходжкина необходимо исследование анализа крови, биохимии, чтобы оценить работу костного мозга и печени. Они не подтверждают диагноз, но могут определить отклонения в работе внутренних органов. В общем анализе определяются:
- сниженный уровень гемоглобина;
- понижение количества тромбоцитов;
- увеличен уровень лейкоцитов за счет моноцитоза, эозино-и базофилии;
- количество лимфоцитов легко снижено;
- СОЭ ускорено до 20-25 мм/ч и выше.
В биохимическом анализе отмечает повышение воспалительных маркеров, в том числе количества СРБ, фибриногена, альфа-два-глобулина. В поздней стадии повышаются уровни билирубина и АЛТ, АСТ.
Также показано выполнение стернальной пункции (при подозрении на поражение костного мозга), выполнение рентгенографии груди, КТ брюшной полости, средостения, сцинтиграфии костей, лимфографии.
Методы лечения лимфомы Ходжкина
Современные методы лечения этой болезни позволяют добиться стойкой ремиссии. Терапия проводится поэтапно, с учетом стадии лимфогранулематоза. Применяют комбинацию лучевой терапии, циклы полихимиотерапии, таргетную терапию.
При стадиях I-IIА применяется только лучевая терапия, позволяющая устранить опухолевые клетки в области единичных пораженных узлов или органа. Также предварительно пораженные узлы и селезенку удаляют. Облучают как пораженные узлы, так и неизмененные, для профилактики рецидивов.
При стадии IIВ – IIIА применяют комбинацию лучевого лечения и химиотерапии. Сначала делают вводную полихимиотерапию, затем облучают только пораженные лимфоузлы, после этого – остальные узлы и применяют поддерживающую химиотерапию в течение 2-3 лет.
В стадии IIIВ – IV показаны циклы полихимиотерапии, а в стадии ремиссии циклы облучения или медикаментов. Все лечение проводится согласно специальным онкологическим протоколам.
Современные разработке в онкологии позволили сегодня применять в лечении лимфомы Ходжкина таргетную терапию. Это соединения, которые блокируют у опухоли ключевые молекулы, отвечающие за ее размножение, рост и сопротивление иммунной системе. Таргетные препараты более избирательны в сравнении с обычно химиотерапией, они влияют только на раковые клетки, не трогая собственные. Применяют несколько вариантов препаратов:
- ингибиторы протеасом;
- блокаторы гистондеацетилазы;
- блокаторы киназ;
- другие препараты.
Препараты вводят курсами с последующей оценкой изменений по данным обледований.
После лечения возможны определенные результаты:
- Наступление полной ремиссии – в течение месяца исчезают все признаки болезни (субъективные и объективные);
- Наступление частичной ремиссии – устраняются признаки болезни, уменьшаются лимфоузлы и очаги вне узлов на 50% и более.
Также возможно клиническое улучшение, отсутствие динамики, тогда курс лечения корректируют.
Врачи в ходе лечения делают все возможное, чтобы предотвратить возможные осложнения.
Прогноз при лимфоме Ходжкина
В стадии 1-2 пятилетняя выживаемость достигает 90% и более. При выявлении лимфомы на стадии III A выживаемость в течение пяти лет и шансы на безрецидивную жизнь составляют по оценкам экспертов примерно 80%. Если это стадия лимфомы III Б стадии — шансы на безрецидивное течение и выживание на протяжении пятилетия снижаются до 60%. На IV стадии после проведения полного курса терапии – полихимиотерапии в сочетании с облечением, процент выживания снижается до 45%.
Среди неблагоприятных признаков можно выделить острый лимфогранулематоз, образование участков пораженных лимфоузлов более 5 см, поражение большого объема узлов и органов, селезенки и печени.
Рецидивы бывают редко, обычно они возникают из-за нарушения циклов поддерживающего лечения, после беременности или тяжелых нагрузок. Пациентам нужно постоянно находиться на учете у онколога.
Профилактика
Эффективных вариантов профилактики при развитии лимфомы на сегодняшний день не разработано. Это связано с тем, что не определены точные причинные факторы, которые провоцируют развитие опухоли.
Михайлов Алексей Геннадьевич оперирующий онколог, врач высшей квалификационной категории, к.м.н. стаж: 21 год
Информация в статье предоставлена в справочных целях и не заменяет консультации квалифицированного специалиста. Не занимайтесь самолечением! При первых признаках заболевания необходимо обратиться к врачу.
Мантийноклеточная лимфома ( Лимфомой из клеток мантийной зоны )
Мантийноклеточная лимфома – это зрелая В-клеточная неходжкинская лимфома, которая возникает из мелких и средних клеток с неправильными контурами ядер. Основной причиной заболевания называют генную транслокацию CCND1. Клинические проявления включают малоболезненное увеличение лимфоузлов, гепатоспленомегалию, неспецифический интоксикационный синдром. Диагностика мантийноклеточной опухоли основана на результатах цитологического и иммуногистохимического анализа биоптатов. Лечение болезни предполагает интенсивные схемы химио- и иммунотерапии, трансплантацию костного мозга, симптоматическую терапию.
МКБ-10
Общие сведения
Диагноз «мантийноклеточная лимфома» (МКЛ), которую также называют лимфомой из клеток мантии, впервые появился в 1994 г. в «Пересмотренной Европейско-Американской классификации лимфоидных опухолей». Она составляет 3-10% от всех неходжкинских лимфом. Частота встречаемости заболевания варьирует от 0,5-0,7 случаев на 100 тыс. населения младше 65 лет до 3,9 случая в старшей возрастной группе. В России такой диагноз ежегодно обнаруживают примерно у 2500 пациентов. Чаще всего патологию выявляют у мужчин после 60 лет.
Причины
В 95% случаев развитие МКЛ связывают с транслокацией гена CCND1 в область конституционально гиперэкспресированных на В-лимфоцитах генов IgVH. Молекулярно-генетическое описание классического переноса – (11;14) (q13;q32), реже встречаются варианты t(2;11)(p11;q13) и t(11;22)(q13;q11). Оставшиеся 5% случаев заболевания вызваны перестройкой протоонкогена в гены легких цепей иммуноглобулинов.
Факторы риска
Значимую роль в развитии лимфопролиферативных процессов играют провоцирующие факторы. К наиболее известным из них относятся вирусные агенты: возбудитель гепатита С, вирус иммунодефицита человека, вирус Эпштейна-Барр. Вероятность мантийноклеточной лимфомы повышается среди пациентов с первичными иммунодефицитами и больных, которые длительное время получают иммуносупрессивную терапию в отделениях трансплантологии. Вклад экзогенных канцерогенов пока недостаточно изучен.
Патогенез
Основу заболевания составляет злокачественная трансформация нормальных В-лимфоцитов, которая возникает на фоне транслокации генов и гиперэкспрессии отдельных вариантов циклинов. Современные данные показывают, что повреждение гена CCND1 – не единственное онкогенное событие при МКЛ. В 80% случаев наблюдаются дополнительные цитогенетические поломки и усиление активности комплекса Cyclin D1-CDK4, который стимулирует переход клеток в фазу деления.
Вторым звеном патогенеза при мантийноклеточной лимфоме является усиление синтеза транскрипционного фактора SOX11. Он регулирует деление и рост злокачественных клеток, стимулирует ангиогенез, является прогностически неблагоприятным маркером. Экспрессия SOX11 важна для дифференциальной диагностики различных вариантов неходжкинских лимфом, когда не удается определить типичную для МКЛ транслокацию генов.

Классификация
Изучение молекулярной структуры опухолей позволяет разделить МКЛ на классический и индолентный варианты. Классическая лимфома составляет 80-90% случаев, происходит из В-клеток прегерминального этапа дифференцировки. Индолентный тип имеет мутации генов IGHV и является SOX11-негативным, в отличие от предыдущего варианта. В практической онкогематологии широко применяется модифицированная классификация Ann Arbor, в которой выделяют 4 стадии:
- СтадияI. Характеризуется вовлечением лимфатических узлов одной зоны или единичным поражением экстралимфатической ткани.
- СтадияII. Диагностируется при патологии более двух групп лимфоузлов с одной стороны от диафрагмы, либо при сочетанном поражении одного экстралимфатического органа и соседних лимфатических узлов.
- СтадияIII. Проявляется вовлечением лимфоидной ткани по обе стороны от диафрагмы, в том числе с единичным или множественным поражением экстранодулярных образований.
- СтадияIV. Устанавливается при диссеминированных поражениях экстралимфатических органов, независимо от вовлечения в процесс лимфоузлов.
Большое значение для врача-онколога имеет оценка прогностического индекса мантийноклеточной лимфомы. Для расчета этого показателя учитывают возраст пациента, уровень лактатдегидрогеназы крови, число лейкоцитов и обще состояние здоровья. Низкий риск прогрессирования устанавливается при сумме 0-3 балла, промежуточный – 4-5 баллов, высокий – 6-11 баллов.
Симптомы мантийноклеточной лимфомы
Основным проявлением заболевания является увеличение лимфатических узлов в одной или нескольких зонах тела. Периферическая лимфаденопатия на начальных этапах болезни протекает бессимптомно. Узлы имеют плотноэластическую консистенцию и остаются подвижными, по мере прогрессирования мантийноклеточной лимфомы они сливаются в обширные конгломераты. Кожа над увеличенными лимфоузлами не изменена, болевой синдром встречается редко.
Вторым типичным симптомом МКЛ является интоксикация. Больные жалуются на повышение температуры тела, обильное потоотделение вечером и ночью, слабость и снижение работоспособности. Беспокоит кожный зуд, из-за чего на теле остаются множественные следы расчесов. Опухолевый процесс сопровождается резким снижением массы тела: многие пациенты худеют на 10 кг за 2-3 месяца. Вследствие увеличения печени возможна тяжесть и дискомфорт в правом подреберье.
Осложнения
Основной проблемой мантийноклеточной лимфомы считается ее рецидивирование, которое не всегда удается предупредить даже интенсивными схемами фармакотерапии. Увеличение глубоких лимфоузлов чревато компрессией трахеи, пищевода, кишечника и мочеточников. Сдавление органов вызывает дыхательную недостаточность, кишечную непроходимость, задержку мочи. Иммуносупрессия повышает риск бактериальных, вирусных и грибковых инфекций.
Диагностика
Пациенты с симптомами лимфопролиферативных заболеваний проходят обследование у врача-онкогематолога. При первичном осмотре обращают внимание на количество и размеры увеличенных лимфоузлов, наличие гепатоспленомегалии, антропометрические показатели и внешние признаки белково-энергетической недостаточности. Для постановки диагноза назначаются следующие методы исследования:
- УЗИ лимфатических узлов. С помощью сонографии обнаруживают увеличение периферических и внутрибрюшных лимфоузлов, изменение их структуры. Дополнительно проводится ультразвуковая визуализация печени и селезенки, чтобы определить линейные размеры и структуру паренхимы органов.
- Биопсия лимфоузлов. Инвазивная диагностика показана всем пациентам с подозрением на МКЛ перед назначением противоопухолевого лечения. Для исследования необходим образец ткани увеличенного лимфоидного образования или пораженного экстралимфатического органа.
- Компьютерная томография. Исследование шеи, грудной и брюшной полости рекомендовано для оценки размеров и степени распространения лимфаденопатии. По показаниям выполняется МРТ, ПЭТ-КТ, радиоизотопное сканирование с галлием.
- Гистологическое исследование. При мантийноклеточном типе лимфомы определяется зрелоклеточная опухоль с нодулярным, диффузным или смешанным характером роста. При осмотре под микроскопом клетки имеют ядра неправильной формы и ободок бледной цитоплазмы.
- Иммуногистохимический анализ. Для клеток МКЛ характерна фиксация поверхностных иммуноглобулинов M и D, которые позитивны по CD20, CD79a, CD5, CD43. Наблюдается положительное окрашивание на ядерный циклин D1. По результатам иммуногистохимии верифицируется морфологическая форма опухоли.
- Анализы крови. В гемограмме определяют повышение СОЭ, снижение числа эритроцитов и гемоглобина, умеренный тромбоцитоз. В биохимическом анализе крови особое внимание обращают на показатели ЛДГ, общего белка, электролитов, чтобы выявить синдром опухолевого лизиса и сопутствующие поражения внутренних органов. В коагулограмме наблюдается рост Д-димера.
Дифференциальная диагностика
Мантийноклеточную лимфому дифференцируют с более распространенными причинами лимфаденопатии:
- лимфогранулематозом;
- инфекционным мононуклеозом;
- специфическими инфекционными лимфаденитами при бруцеллезе, сифилисе, туберкулезе.
При локализации опухоли в области средостения необходимо исключить тимому. В рамках иммуногистохимического исследования проводится дифференциальная диагностика разных типов неходжкинских лимфом.

Лечение мантийноклеточной лимфомы
Консервативная терапия
Основу лечения заболевания составляет интенсивная схема иммунохимиотерапии с последующей консолидацией. Выбор терапевтической программы зависит от молекулярно-генетических особенностей опухоли, возраста и соматического статуса пациента, тяжести сопутствующих заболеваний. Учитывая агрессивное течение классической МКЛ, терапию рекомендовано начинать в максимально ранние сроки. При индолентной форме возможна выжидательная тактика.
Оптимальным вариантом признана высокодозная химиотерапия, которая проводится по общепринятым протоколам. Она включает один или несколько противоопухолевых препаратов с разными механизмами действия. У пациентов до 65 лет без значимых коморбидных состояний фармакотерапию дополняют трансплантацией аутологичных гемопоэтических стволовых клеток. ТГСК предшествует кондиционирование, которое требует сочетания лучевой терапии и химиотерапии.
Для облегчения состояния больных во время курса иммунохимиотерапии назначается симптоматическое лечение. Обязательно используют обезболивающую терапию, в том числе с применением опиоидных анальгетиков. Важную роль имеет профилактика тошноты и рвоты препаратами центрального действия. Проводится коррекция уровня форменных элементов крови, устраняются проявления нутритивного дефицита.
Экспериментальное лечение
Особое внимание уделяется терапии пациентов старше 65 лет, когда необходимо найти баланс между противоопухолевым действием препаратов и допустимыми побочными эффектами. Большой интерес представляют режимы «chemo-free», которые включают индукционный этап и поддерживающую терапию. Длительность протоколов не превышает 3 года. В клинических исследованиях схема «chemo-free» показывает общую 5-летнюю выживаемость на уровне 77%.
Стандартные схемы химиотерапии дополняются новыми иммунотерапевтическими препаратами. Хорошие перспективы имеют ингибиторы протеасомы 26S, которая взаимодействует с комплексом Cyclin D1–CDK4. В комплексном лечении применяются ингибиторы В-клеточного рецептора, которые угнетают пролиферацию опухолевых клеток. Для терапии рецидивирующей МКЛ используются препараты из группы ингибиторов mTOR-киназы.
Прогноз и профилактика
Появление новых лекарственных средств позволяет снять «печать фатальности» с мантийноклеточной лимфомы. Однако общая 5-летняя выживаемость составляет не более 71%, выживаемость без прогрессирования – 45%. Более благоприятный прогноз для больных с индолентным вариантом патологии, который отличается невысокой опухолевой нагрузкой и низкой пролиферативной активностью (уровень ядерного белка Ki67 менее 10%). Меры профилактики МКЛ пока не разработаны.
2. Мантийноклеточная лимфома: история, современные принципы диагностики, лечение (обзор литературы)/ Г.С. Тумин// Клиническая онкогематология. – 2020. – №13.
3. Мантийноклеточная лимфома: программное лечение первичных больных в возрасте до 65 лет/ В.И. Воробьев, С.К. Кравченко, Э.Г. Гемджян, Ю.Ю. Лорие// Клиническая онкогематология. – 2013. – №3.
Лимфома ЦНС
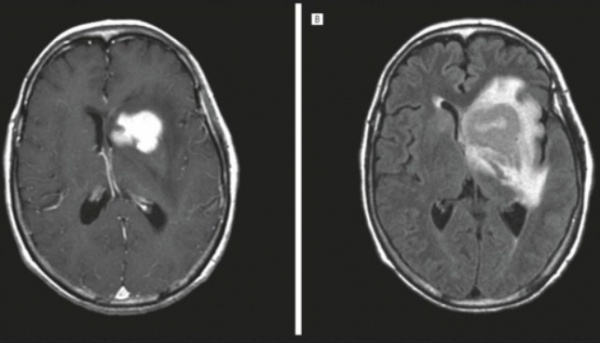
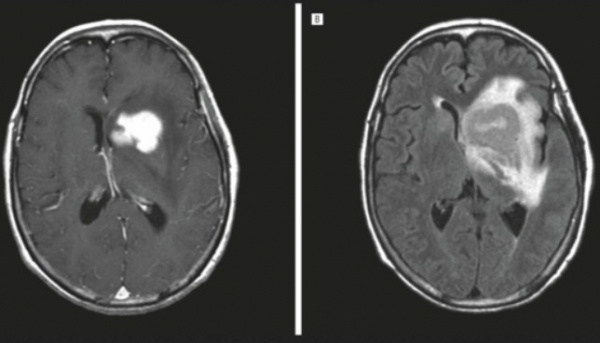
Лимфома центральной нервной системы — редкое новообразование, поражающее ткани головного и спинного мозга, заднюю стенку глаза. Клиническая картина зависит от локализации процесса, включает общемозговые симптомы, парезы, нарушения координации, расстройства зрения. Диагностика осуществляется с применением методов нейровизуализации, анализа спинномозговой жидкости, гистологического исследования биоптата. В лечении активно используется терапия химиопрепаратами, облучение мозга и их сочетание. При одиночном характере опухоли возможно нейрохирургическое вмешательство.

Лимфома ЦНС впервые выделена в отдельную нозологию в 1974 г. Относится к злокачественным новообразованиям, составляет около 4% опухолей центральных органов нервной системы. По статистическим данным, распространенность патологии находится на уровне 0,5-0,75 случая на 100 тысяч пациентов. Последнее время наблюдается увеличение заболеваемости, связанное с ростом иммуносупрессивных состояний. Риск возникновения лимфомы ЦНС у больных СПИДом составляет 4-6%, при врожденном иммунодефиците — 4%. Средний возраст заболевших среди иммунокомпетентных лиц — 62 года. Возрастная медиана у пациентов с врожденным иммунодефицитом составляет 10 лет. Гендерная предрасположенность не наблюдается.

Этиология возникающих в ЦНС лимфом не определена. У иммунокомпрометированных пациентов выявляют следы вируса Эпштейна-Барр и герпеса VI типа, также характерных для лимфоидных опухолей другой локализации. Однако роль данных вирусов в возникновении заболевания не доказана. Ведется дальнейший поиск триггеров, обуславливающих появление патологических, активно делящихся лимфоцитов. Среди установленных факторов риска выделяют следующие иммуносупрессивные состояния:
- Наследственные иммунодефициты: синдром Луи-Бар, синдром Вискотта–Олдрича, селективный дефицита Ig A и другие.
- ВИЧ-инфекция: у больных поражается Т-клеточная составляющая иммунитета.
- Аутоиммунная патология: системная красная волчанка, ревматоидный артрит.
- Состояния после трансплантации: иммуносупрессия создается медикаментозно для предотвращения реакции отторжения трансплантата.
Большинство лимфом ЦНС являются экстранодулярными, первично развивающимися в церебральных тканях без предварительного образования в лимфатическом узле. С целью объяснения их возникновения в нервной ткани, не имеющей лимфоидных образований, были выдвинуты 2 гипотезы. Первая предполагает проникновение лимфоцитов в мозговые структуры под действием неких триггеров, которыми могут служить вирусные инфекции. Попадая в нервные структуры, лимфоциты изменяют свои свойства и дают начало патологическому клеточному клону. Вторая гипотеза предполагает формирование опухолевого лимфоцитарного клона в отдалении, с последующей миграцией в ЦНС.
90% лимфом ЦНС состоят из трансформированных В-лимфоцитов. В большинстве случаев предшественниками опухолевых клеток являются В-лимфоциты герминогенного центра, реже — постгерминогенные активированные лимфоциты. В ряде случаев патологические лимфоциты пропитывают стенки церебральных сосудов, давая картину васкулита.

Единая классификация лимфом ЦНС не разработана. В современной клинической нейроонкологии новообразования разделяют морфологически, по характеру распространения и расположению.
- По иммунофенотипу подавляющее большинство образований представляют собой неходжкинские лимфомы. Лимфома Ходжкина, лимфобластные и Т-клеточные лимфомы наблюдаются значительно реже.
- По распространенности процесса в ЦНС образования могут быть одиночными, инфильтративными и множественными.
- По локализации различают церебральные и спинномозговые лимфомы. Первые составляют подавляющее большинство и классифицируются на полушарные, лептоменингеальные, лимфомы мозолистого тела. Поражения спинного мозга составляют менее 1%.
Симптомы лимфомы ЦНС
Клиническими проявлениями выступают неспецифические общемозговые и очаговые симптомы. У большинства больных заболевание манифестирует признаками поражения ЦНС в виде головных болей, психоневрологических изменений, сонливости и расстройств сознания. Возможны когнитивные нарушения, дискоординация. Эписиндром возникает в 10% случаев. У трети больных отмечаются симптомы интракраниальной гипертензии: интенсивные цефалгии, тошнота, чувство «тяжести» на глазах. Расположение очагов в задних отделах глазного яблока сопровождается зрительной дисфункцией, экзофтальмом, офтальмоплегией.
Спинномозговая форма проявляется мышечной слабостью, выпадением двигательной функции с последующим присоединением сенсорных нарушений и болевого синдрома. Лептоменингеальное поражение протекает с сенсомоторными расстройствами лицевой области, корешковым синдромом с локализацией в люмбосакральном отделе. Наблюдается нижний парапарез, расстройство мочеиспускания, гидроцефалия. Типичные для лимфом другой локализации подъемы температуры тела, потливость, снижение массы тела не наблюдаются.
Являясь объемным образованием, лимфома ЦНС по мере роста приводит к масс-эфекту с повышением ликворного давления и гидроцефалией. Последняя опасна дислокацией мозга с ущемлением его тканей. Локализуясь по ходу мозговых сосудов и прорастая их, опухоль может приводить к нарушению целостности сосудистой стенки и геморрагическому инсульту. Возможна диссеминация опухолевых клеток с образованием вторичных очагов в ЦНС.
Выявление общемозговых симптомов и очаговых выпадений в неврологическом статусе позволяет врачу-неврологу заподозрить новообразование ЦНС и его предположительную локализацию. Подтверждение диагноза возможно по результатам нейровизуализирующих обследований, для верификации опухоли требуется морфологическое исследование. В перечень необходимых обследований при подозрении на лимфому входит:
- Нейровизуализация. Церебральная КТ или МРТ позволяют оценить размер и расположение новообразования, степень дислокации серединных структур. В пользу лимфомы ЦНС говорит многоочаговость процесса, кольцевидное контрастирование, значительный перифокальный отек.
- Офтальмологическое обследование. Необходимо больным, имеющим зрительные расстройства. Выявляет экзофтальм, повышенное внутриглазное давление, застойные явления при офтальмоскопии.
- КТ всего тела. Необходимо для поиска первичного очага, локализующегося вне ЦНС. Его обнаружение свидетельствует о вторичном характере мозговой лимфомы.
- Исследование цереброспинальной жидкости. Забор материала производиться путем спинномозговой пункции. В половине случаев в ликворе определяется повышение белка, плеоцитоз с большим количеством реактивных лимфоцитов, наличием опухолевых клеточных элементов.
- Гистологическое исследование. Забор тканей опухоли предпочтительно производить путем стереотаксической биопсии, позволяющей минимизировать опасность диссеминации. При микроскопии типичная цитологическая картина представлена скоплением патологически трансформированных лимфоидных клеток со светлыми ядрами, окруженных зрелыми лимфоцитами. Иммунофенотипирование лимфомы ЦНС позволяет установить ее гистологический тип, степень зрелости клеток, спрогнозировать развитие заболевания.
Необходимо дифференцировать лимфому ЦНС с другими объемными образованиями:
- глиобластомой;
- абсцессом;
- церебральными метастазами.
Дифференцировка осуществляется по характерным особенностям МРТ. Для глиобластомы типичны некротические очаги центральной локализации, отсутствующие у лимфомы. С целью исключения метастатического характера новообразования производится поиск первичной опухоли экстраневральной локализации. Церебральный абсцесс характеризуется четким контуром. Лимфому ЦНС следует также отличать от нейросаркоидоза, лейкоэнцефалопатии, демиелинизирующих заболеваний, в пользу которых будет свидетельствовать диффузно-многоочаговый характер поражения.

Лечение лимфомы ЦНС
Лимфомы чувствительны к химиотерапии и облучению. Текущие рекомендации по лечению основаны на нескольких проспективных исследованиях, однако в связи с редкой встречаемостью опухоли последние имеют небольшой размер выборки. Терапия осуществляется индивидуально в соответствии с характером поражения, возрастом пациента, преморбидным фоном. К наиболее популярным методикам относятся:
- Монотерапия цитостатиками. Проводится одним цитостатическим препаратом. Приводит к полной ремиссии у 30-40% больных. Побочными эффектами выступает почечная, печеночная недостаточность, гематологические нарушения, пневмонит.
- Комбинированная химиотерапия. Применение сочетания двух цитостатиков, способных проникать через гематоэнцефалический барьер, дает лучший ответ на терапию. К недостаткам метода относится его высокая токсичность.
- Лучевая терапия. Фракционное облучение мозга у большинства больных приводит к быстрой ремиссии. Однако, характерно раннее возникновение рецидивов. Средняя продолжительность жизни пациентов составляет 1-1,5 года.
- Сочетанная терапия. Лечение включает химио- и радиотерапию. Данное сочетание позволяет продлить жизнь пациента, но обладает высокой нейротоксичностью, приводящей к лейкоэнцефалопатии с кортикальной атрофией. В таких случаях наблюдаются тяжелые когнитивные нарушения, нарушения походки, недержание мочи, возникает необходимость ухода за больным.
Хирургическое лечение
Резекция может улучшить выживаемость без прогрессирования у пациентов с одиночными поражениями. Диффузное прорастание лимфомы ЦНС в окружающие ткани, ее локализация в глубинных церебральных структурах делает нейрохирургическое лечение малоэффективным. Оперативное вмешательство может способствовать распространению опухолевых лимфоцитов с возникновением множественных рецидивов. Медиана выживаемости таких больных после оперативного лечения без применения других методов не превышает 4 месяца.
Возможно применение иммунотерапии ингибиторами контрольных точек. В современной нейроонкологии рассматривается использование препаратов, препятствующих передаче сигналов В-клеточного рецептора и таким образом влияющих на пролиферацию клеток лимфомы, Препараты первой группы были связаны со значительной токсичностью у некоторых пациентов. Пришедшие им на смену средства менее токсичны, но и менее активны. В настоящее время ведется поиск способов повышения их активности.
Лимфома ЦНС представляет собой высокозлокачественное новообразование со средней выживаемостью от недель до месяцев, если лечение является только симптоматическим. При противоопухолевой терапии 5-летняя выживаемость составляет 31%. Пожилой возраст, плохое клиническое состояние, повышенный уровень белка в спинномозговой жидкости, вовлечение глубоких церебральных отделов, спинальное поражение связаны с более неблагоприятным прогнозом. Профилактика сводится к предупреждению и своевременному лечению приводящих к иммунодефициту заболеваний.
1. Первичные лимфопролиферативные заболевания центральной нервной системы/ Губкин А.В., Звонков Е.Е., Кременецкая В.А. и др.// Клиническая онкогематология. - 2008. - 4(1).
2. Современные представления об этиологии, патогенезе, диагностике и методах лечения первичной диффузной В-клеточной крупноклеточной лимфомы центральной нервной системы/ С.В. Волошин, Ю.А. Криволапов, А.В. Шмидт, В.А. Шуваев, М.С. Фоминых, К.М. Абдулкадыров// Онкогематология. - 2013. - 2.
3. The Diagnosis and Treatment of Primary CNS Lymphoma/ von Baumgarten L, Illerhaus G, Korfel A, Schlegel U, Deckert M, Dreyling M.// Deutsches Arzteblatt international. - 2018. - 115(25).
4. Primary CNS Lymphoma/ Grommes, C., DeAngelis, L. M.// Journal of clinical oncology : official journal of the American Society of Clinical Oncology. - 2017. - 35(21).
Неходжкинские лимфомы ( Лимфосаркома )
Неходжкинские лимфомы – опухолевые заболевания лимфатической системы, представленные злокачественными B- и T-клеточными лимфомами. Первичный очаг может возникать в лимфатических узлах либо других органах и в дальнейшем метастазировать лимфогенным или гематогенным путем. Клиника лимфом характеризуется лимфаденопатией, симптомами поражения того или иного органа, лихорадочно-интоксикационным синдромом. Диагностика основывается на клинико-рентгенологических данных, результатах исследования гемограммы, биоптата лимфоузлов и костного мозга. Противоопухолевое лечение включает курсы полихимиотерапии и лучевой терапии.
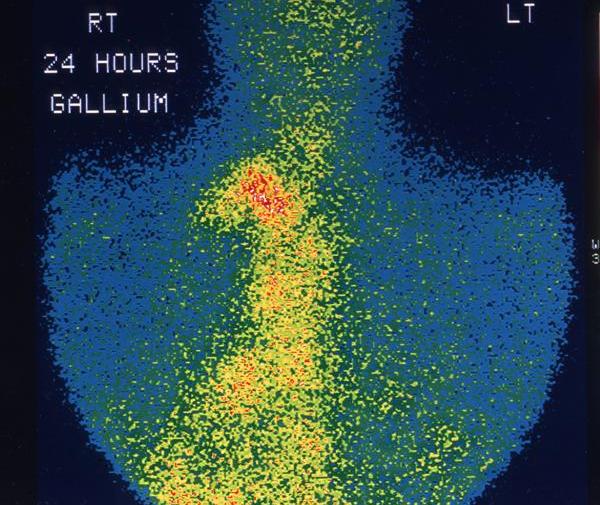
Неходжкинские лимфомы (НХЛ, лимфосаркомы) – различные по морфологии, клиническим признакам и течению злокачественные лимфопролиферативные опухоли, отличные по своим характеристикам от лимфомы Ходжкина (лимфогранулематоза). В зависимости от места возникновения первичного очага гемобластозы делятся на лейкозы (опухолевые поражения костного мозга) и лимфомы (опухоли лимфоидной ткани с первичной внекостномозговой локализацией). На основании отличительных морфологических признаков лимфомы, в свою очередь, подразделяются на ходжкинские и неходжкинские; к числу последних в гематологии относят В- и Т-клеточные лимфомы. Неходжкинские лимфомы встречаются во всех возрастных группах, однако более половины случаев лимфосарком диагностируется у лиц старше 60 лет. Средний показатель заболеваемости среди мужчин составляет 2-7 случая, среди женщин – 1-5 случаев на 100 000 населения. В течение последних лет прослеживается тенденция к прогрессирующему увеличению заболеваемости.
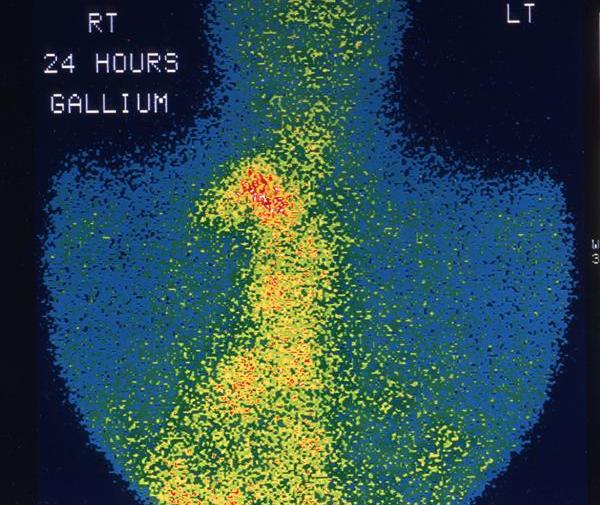
Этиология лимфосарком достоверно неизвестна. Более того, причины лимфом различных гистологических типов и локализаций существенно варьируются. В настоящее время правильнее говорить о факторах риска, повышающих вероятность развития лимфомы, которые на данный момент хорошо изучены. Влияние одних этиофакторов выражено значительно, вклад других в этиологию лимфом весьма несущественен. К такого рода неблагоприятным предпосылкам относятся:
- Инфекции. Наибольшим цитопатогенным эффектом на лимфоидные клетки обладает вирус иммунодефицита человека (ВИЧ), гепатита С, Т-лимфотропный вирус 1 типа. Доказана связь инфицирования вирусом Эпштейна-Барр с развитием лимфомы Беркитта. Известно, что инфекция Helicobacter pylori, ассоциированная с язвенной болезнью желудка, может вызывать развитие лимфомы той же локализации.
- Дефекты иммунитета. Риск возникновения лимфом повышается при врожденных и приобретенных иммунодефицитах (СПИДе, синдроме Вискотта-Олдрича, Луи-Бар, Х-сцепленном лимфопролиферативном синдроме и др.). У пациентов, получающих иммуносупрессивную терапию по поводу трансплантации костного мозга или органов, вероятность развития НХЛ увеличивается в 30-50 раз.
- Сопутствующие заболевания. Повышенный риск заболеваемости НХЛ отмечается среди пациентов с ревматоидным артритом, красной волчанкой, что может быть объяснено как иммунными нарушениями, так и использованием иммуносупрессивных препаратов для лечения данных состояний. Лимфома щитовидной железы обычно развивается на фоне аутоиммунного тиреоидита.
- Токсическое воздействие. Прослеживается причинно-следственная связь между лимфосаркомами и предшествующим контактом с химическими канцерогенами (бензолом, инсектицидами, гербицидами), УФ-излучением, проведением лучевой терапии по поводу онкологического заболевания. Прямое цитопатическое действие оказывают цитостатические препараты, применяемые для химиотерапии.
Патологический лимфогенез инициируется тем или иным онкогенным событием, вызывающим нарушение нормального клеточного цикла. В этом могут быть задействованы два механизма - активация онкогенов либо подавление опухолевых супрессоров (антионкогенов). Опухолевый клон при НХЛ в 90% случаев формируется из В-лимфоцитов, крайне редко – из Т-лимфоцитов, NK- клеток или недифференцированных клеток.
Для различных типов лимфом характерны определенные хромосомные транслокации, которые приводят к подавлению апоптоза, утрате контроля над пролиферацией и дифференцировкой лимфоцитов на любом этапе. Это сопровождается появлением клона бластных клеток в лимфатических органах. Лимфоузлы (периферические, медиастинальные, мезентериальные и др.) увеличиваются в размерах и могут нарушать функцию близлежащих органов. При инфильтрации костного мозга развивается цитопения. Разрастание и метастазирование опухолевой массы сопровождается кахексией.
Лимфосаркомы, первично развивающиеся в лимфоузлах называются нодальными, в других органах (небной и глоточных миндалинах, слюнных железах, желудке, селезенке, кишечнике, головном мозге, легких, коже, щитовидной железе и др.) - экстранодальными. По структуре опухолевой ткани НХЛ делятся на фолликулярные (нодулярные) и диффузные. По темпам прогрессирования лимфомы классифицируются на индолентные (с медленным, относительно благоприятным течением), агрессивные и высоко агрессивные (с бурным развитием и генерализацией). При отсутствии лечения больные с индолентными лимфомами живут в среднем 7 – 10 лет, с агрессивными – от нескольких месяцев до 1,5-2 лет.
Современная классификация насчитывает свыше 30 различных видов лимфосарком. Большая часть опухолей (85%) происходит из В-лимфоцитов (В-клеточные лимфомы), остальные из Т-лимфоцитов (Т-клеточные лимфомы). Внутри этих групп существуют различные подтипы неходжкинских лимфом. Группа В-клеточных опухолей включает:
- диффузную В-крупноклеточную лимфому – самый распространенный гистологический тип лимфосарком (31%). Характеризуется агрессивным ростом, несмотря на это почти в половине случаев поддается полному излечению.
- фолликулярную лимфому – ее частота составляет 22% от числа НХЛ. Течение индолентное, однако возможна трансформация в агрессивную диффузную лимфому. Прогноз 5-летней выживаемости – 60-70%.
- мелкоклеточную лимфоцитарную лимфомуи хронический лимфоцитарный лейкоз – близкие типы НХЛ, на долю которых приходится 7% от их числа. Течение медленное, но плохо поддающееся терапии. Прогноз вариабелен: в одних случаях лимфосаркома развивается в течение 10 лет, в других – на определенном этапе превращается в быстрорастущую лимфому.
- лимфому из мантийных клеток– в структуре НХЛ составляет 6%. Пятилетний рубеж выживаемости преодолевает лишь 20% больных.
- В-клеточные лимфомы из клеток маргинальной зоны – делятся на экстранодальные (могут развиваться в желудке, щитовидной, слюнных, молочных железах), нодальные (развиваются в лимфоузлах), селезеночную (с локализацией в селезенке). Отличаются медленным локальным ростом; на ранних стадиях хорошо поддаются излечению.
- В-клеточную медиастинальную лимфому – встречается редко (в 2% случаев), однако в отличие от других типов поражает преимущественно молодых женщин 30-40 лет. В связи с быстрым ростом вызывает компрессию органов средостения; излечивается в 50% случаев.
- макроглобулинемию Вальденстрема (лимфоплазмоцитарную лимфому) – диагностируется у 1% больных с НХЛ. Характеризуется гиперпродукцией IgM опухолевыми клетками, что приводит к повышению вязкости крови, сосудистым тромбозам, разрывам капилляров. Может иметь как относительно доброкачественное (с выживаемостью до 20 лет), так и скоротечное развитие (с гибелью пациента в течение 1-2 лет).
- волосатоклеточный лейкоз– очень редкий тип лимфомы, встречающийся у лиц пожилого возраста. Течение опухоли медленное, не всегда требующее лечения.
- лимфому Беркитта – на ее долю приходится около 2% НХЛ. В 90% случаев опухоль поражает молодых мужчин до 30 лет. Рост лимфомы Беркитта агрессивный; интенсивная химиотерапия позволяет добиться излечение половины больных.
- лимфому центральной нервной системы – первичное поражение ЦНС может затрагивать головной или спинной мозг. Чаще ассоциируется с ВИЧ-инфекцией. Пятилетняя выживаемость составляет 30%.
Неходжкинские лимфомы Т-клеточного происхождения представлены:
- Т-лимфобластной лимфомой или лейкозом из клеток-предшественников – встречается с частотой 2%. Различаются между собой количеством бластных клеток в костном мозге: при 25% - как лейкоз. Диагностируется преимущественно у молодых людей, средний возраст заболевших – 25 лет. Худший прогноз имеет Т-лимфобластный лейкоз, показатель излечения при котором не превышает 20%.
- периферическими Т-клеточными лимфомами, включающими кожную лимфому (синдром Сезари, грибовидный микоз), ангиоиммунобластную лимфому, экстранодальную лимфому из естественных киллеров, лимфому с энтеропатией, панникулитоподобную лимфому подкожной клетчатки, крупноклеточную анапластическую лимфому. Течение большей части Т-клеточных лимфом быстрое, а исход неблагоприятный.

Симптомы
Варианты клинических проявлений НХЛ сильно варьируются в зависимости от локализации первичного очага, распространенности опухолевого процесса, гистологического типа опухоли и пр. Все проявления лимфосарком укладываются в три синдрома: лимфаденопатии, лихорадки и интоксикации, экстранодального поражения. В большинстве случаев первым признаком НХЛ служит увеличение периферических лимфоузлов. Вначале они остаются эластичными и подвижными, позднее сливаются в обширные конгломераты. Одновременно могут поражаться лимфоузлы одной или многих областей. При образовании свищевых ходов необходимо исключить актиномикоз и туберкулез.
Такие неспецифические симптомы лимфосарком, как лихорадка без очевидных причин, ночная потливость, потеря веса, астения в большинстве случаев указывают на генерализованный характер заболевания. Среди экстранодальных поражений доминируют неходжкинские лимфомы кольца Пирогова-Вальдейера, ЖКТ, головного мозга, реже поражаются молочная железа, кости, паренхима легких и др. органы. Лимфома носоглотки при эндоскопическом исследовании имеет вид опухоли бледно-розового цвета с бугристыми контурами. Часто прорастает верхнечелюстную и решетчатую пазуху, орбиту, вызывая затруднение носового дыхания, ринофонию, снижение слуха, экзофтальм.
Первичная лимфосаркома яичка может иметь гладкую или бугристую поверхность, эластическую или каменистую плотность. В некоторых случаях развивается отек мошонки, изъязвление кожи над опухолью, увеличение пахово-подвздошных лимфоузлов. Лимфомы яичка предрасположены к ранней диссеминации с поражением второго яичка, ЦНС и др.
Лимфома молочной железы при пальпации определяется как четкий опухолевый узел или диффузное уплотнение груди; втяжение соска нехарактерно. При поражении желудка клиническая картина напоминает рак желудка, сопровождаясь болями, тошнотой, потерей аппетита, снижением веса. Абдоминальные лимфосаркомы могут проявлять себя частичной или полной кишечной непроходимостью, перитонитом, синдромом мальабсорбции, болями в животе, асцитом. Лимфома кожи проявляется зудом, узелками и уплотнением красновато-багрового цвета. Первичное поражение ЦНС более характерно для больных СПИДом – течение лимфомы данной локализации сопровождаются очаговой или менингеальной симптоматикой.
Наличие значительной опухолевой массы может вызывать сдавление органов с развитием жизнеугрожащих состояний. При поражении медиастинальных лимфоузлов развивается компрессия пищевода и трахеи, синдром сдавления ВПВ. Увеличенные внутрибрюшные и забрюшинные лимфатические узлы могут вызвать явления кишечной непроходимости, лимфостаза в нижней половине туловища, механической желтухи, компрессии мочеточника. Прорастание стенок желудка или кишечника опасно возникновением кровотечения (в случае аррозии сосудов) или перитонита (при выходе содержимого в брюшную полость). Иммуносупрессия обусловливает подверженность пациентов инфекционным заболеваниям, представляющим угрозу для жизни. Для лимфом высокой степени злокачественности характерно раннее лимфогенное и гематогенное метастазирование в головной и спинной мозг, печень, кости.
Вопросы диагностики неходжкинских лимфом находятся в компетенции онкогематологов. Клиническими критериями лимфосаркомы служат увеличение одной или нескольких групп лимфоузлов, явления интоксикации, экстранодальные поражения. Для подтверждения предполагаемого диагноза необходимо проведение морфологической верификации опухоли и инструментальной диагностики:
- Исследование клеточного субстрата опухоли. Выполняются диагностические операции: пункционная или эксцизионная биопсия лимфоузлов, лапароскопия, торакоскопия, аспирационная пункция костного мозга с последующими иммуногистохимическими, цитологическими, цитогенетическими и другими исследованиями диагностического материала. Кроме диагностики, установление структуры НХЛ важно для выбора тактики лечения и определения прогноза.
- Методы визуализации. Увеличение медиастинальных и внутрибрюшных лимфоузлов обнаруживается с помощью УЗИ средостения, рентгенографии и КТ грудной клетки, брюшной полости. В алгоритм обследования по показаниям входят УЗИ лимфатических узлов, печени, селезенки, молочных желез, щитовидной железы, органов мошонки, гастроскопия. С целью стадирования опухоли проводится МРТ внутренних органов; в выявлении метастазов информативны лимфосцинтиграфия, сцинтиграфия костей.
- Лабораторная диагностика. Направлена на оценку факторов риска и функции внутренних органов при лимфомах различных локализаций. В группе риска производится определение ВИЧ-антигена, анти-HCV. Изменение периферической крови (лимфоцитоз) характерно для лейкемизации. Во всех случаях исследуется биохимический комплекс, включающий печеночные ферменты, ЛДГ, мочевую кислоту, креатинин и др. показатели. Своеобразным онкомаркером НХЛ может служить b2-микроглобулин.
Дифференцировать неходжкинские лимфомы приходится с лимфогранулематозом, метастатическим раком, лимфаденитами, возникающими при туляремии, бруцеллезе, сифилисе, туберкулезе, токсоплазмозе, инфекционном мононуклеозе, гриппе, СКВ и др. При лимфомах конкретных локализаций проводятся консультации профильных специалистов: оториноларинголога, гастроэнтеролога, маммолога и т.д.

Лечение
Варианты лечения неходжкинских лимфом включают оперативный метод, лучевую терапию и химиотерапию. Выбор методики определяется морфологическим типом, распространенностью, локализацией опухоли, сохранностью и возрастом больного. В современной онкогематологии приняты протоколы лечения лимфосарком, базирующиеся на использовании:
- Химиотерапии. Наиболее часто лечение лимфом начинают с курса полихимиотерапии. Этот метод может являться самостоятельным или сочетаться с лучевой терапией. Комбинированная химиолучевая терапия позволяет достичь более длительных ремиссий. Лечение продолжается до достижения полной ремиссии, после чего необходимо проведение еще 2-3 консолидирующих курсов. Возможно включение в циклы лечения гормонотерапии.
- Хирургических вмешательств. Обычно применяется при изолированном поражении какого-либо органа, чаще - ЖКТ. По возможности операции носят радикальный характер – выполняются расширенные и комбинированные резекции. В запущенных случаях, при угрозе перфорации полых органов, кровотечения, непроходимости кишечника могут выполняться циторедуктивные вмешательства. Хирургическое лечение обязательно дополняется химиотерапией.
- Лучевой терапии. В качестве монотерапии лимфом применяется только при локализованных формах и низкой степени злокачественности опухоли. Кроме этого, облучение может быть использовано и в качестве паллиативного метода при невозможности проведения других вариантов лечения.
- Дополнительных схем лечения. Из альтернативных методов хорошо себя зарекомендовала иммунохимиотерапия с применением интерферона, моноклональных антител. С целью консолидации ремиссии применяется трансплантация аутологичного или аллогенного костного мозга и введение периферических стволовых клеток.
Прогноз при неходжкинских лимфомах различен, зависит, главным образом, от гистологического типа опухоли и стадии выявления. При местнораспространенных формах долгосрочная выживаемость в среднем составляет 50-60%, при генерализованных - всего 10-15%. Неблагоприятными прогностическими факторами служат возраст старше 60 лет, III-IV стадии онкопроцесса, вовлечение костного мозга, наличие нескольких экстранодальных очагов. Вместе с тем, современные протоколы ПХТ во многих случаях позволяют добиться долгосрочной ремиссии. Профилактика лимфом коррелирует с известными причинами: рекомендуется избегать инфицирования цитопатогенными вирусами, токсических воздействий, чрезмерной инсоляции. При наличии факторов риска необходимо проходить регулярное обследование.
2. Эпидемиология и биология неходжкинских лимфом/ Хансон К.П., Имянитов Е.Н.// Практическая онкология. – 2004 - Т.5, №3.
4. Современные подходы к терапии неходжкинских лимфом/ Поддубная И. В.// Русский медицинский журнал. – 2011. - №22.
Читайте также:
- Гистероскопическая стерилизация. Современная гистероскопия
- Лучевая диагностика послеоперационной деформации позвоночника
- Показания для реконструкции слуховых косточек и отбор пациентов
- Остеосаркома глазницы (остеогенная саркома глазницы): признаки, гистология, лечение, прогноз
- Псориатический артрит: причины, симптомы и лечение
