Отравление золотом и его побочные эффекты
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Пищевое отравление (интоксикация) — тяжелое функциональное расстройство со стороны желудочно-кишечного тракта, которое провоцируют болезнетворные микроорганизмы и продукты их жизнедеятельности (токсины), а также факторы, не имеющие отношение к патогенной микрофлоре. Среди населения чаще встречаются пищевые отравления, вызванные употреблением некачественной и термически необработанной пищи животного и растительного происхождения. Опасен не только любой из видов отравления в разгар болезни, но и последствия, с которыми сталкивается человек уже после выздоровления.
Симптомы пищевого отравления
Сами болезнетворные микроорганизмы, продукты их жизнедейятельности или другие токсические вещества, агрессивно воздействуют на желудочно-кишечный тракт на всей его протяженности. Пищевое отравление сопровождается дегидратацией (обезвоживанием), повреждением слизистой оболочки желудка и кишечника, нарушением баланса кишечной микрофлоры.
Выделяют такие распространенные симптомы пищевого отравления:
- ; (частота позывов к дефекации и консистенция стула зависит от тяжести отравления);
- боль в околопупочной, левой или правой подвздошной области;
- привкус горечи во рту;
- мышечная слабость;
- общее недомогание;
- бледность кожных покровов;
- головная боль;
- повышение температуры тела;
- одышка;
- сонливость.
Токсины, выделяемые патогенными микроорганизмами, негативно влияют на центр терморегуляции, находящийся в гипоталамусе. Результатом такого влияния становится озноб и лихорадочное состояние. Понос при пищевом отравлении имеет профузный характер. Диарея и рвота приводят к значительной потере жидкости организмом и развитию обезвоживания. Дегидратация или обезвоживание сопровождается учащением пульса и повышением артериального давления.
Первые симптомы интоксикации дают о себе знать в течение 24 часов с момента попадания в организм болезнетворных микроорганизмов и других токсических соединений. В зависимости от тяжести отравления, температура тела может находиться в пределах от 37,3-40 градусов.
Классификация пищевых отравлений
Пищевые токсикоинфекции подразделяются на 2 основные группы:
- Микробного происхождения. Пищевые интоксикации микробного происхождения развиваются при попадании в организм с пищей микроорганизмов бактериальной или грибковой природы. Спровоцировать отравление могут энтерококки, стафилококки, ботулиновая палочка, бициллы, вибрионы, кишечная палочка, аспергиллы, микроскопические грибы, пенициллы.
- Немикробного происхождения. Эта разновидность токсикоинфекций бывает спровоцирована природными ядами как растительного, так и животного происхождения. Такие компоненты содержаться в сердцевине абрикосовых косточек, ядовитых дикорастущих ягодах и грибах, некоторых сорных растениях, проросшем картофеле, икре налима, мидиях.
Также, пищевое отравление может развиваться при попадании в организм солей тяжелых металлов, пестицидов, нитрозаминов и циклических углеводородов.
Первая помощь при пищевом отравлении
При возникновении симптомов пищевой токсикоинфекции, необходимо действовать по такому алгоритму:
- Человеку следует дать выпить 3-5 стаканов чистой воды, после чего вызвать рвотный рефлекс нажатием двумя пальцами на корень языка. Повторять процедуру следует до тех пор, пока вода на выходе не будет чистой.
- После очищения желудка, 4 раза подряд с интервалом 15 минут необходимо давать пострадавшему энтересорбент.
- Больного следует укутать и обеспечить полный покой. В первые 24 часа пострадавшему необходимо отказаться от употребления пищи.
Питание после отравления
Для того чтобы не ухудшить общее состояние, важно знать, что можно есть после отравления, а от чего лучше отказаться. Начинать прием пищи, рекомендовано на вторые сутки после отравления. Начинать следует с не крепкого куриного бульона, переходя на протертые супы из риса. В рацион включают слабый черный чай без сахара, вчерашний белый хлеб, сухари и сушки, запеченные яблоки без сахара, манную, овсяную, гречневую каши на воде, нежирную рыбу, приготовленную на пару или в отварном виде.
Из рациона исключают полуфабрикаты, жареную и жирную пищу, жирные сорта мяса и рыбы, овощи и фрукты в свежем виде, кондитерские изделия, выпечку, соусы, приправы, специи, фастфуд. Употребляемая пища не должна создавать дополнительную нагрузку на пищеварительную систему, не должна провоцировать диарею и раздражение слизистой оболочки ЖКТ. После перенесенной пищевой токсикоинфекции очень важно позаботиться о восстановлении микрофлоры кишечника, так как в 75% случаев, после отравления развивается кишечный дисбиоз.
Для самостоятельного восстановления нормальной микрофлоры организму потребуется много времени, и он не сможет осуществить это в полной мере. Возникает вопрос о том, как восстановить микрофлору кишечника, прибегнув к помощи извне. Метапребиотики это настоящая скорая помощь для организма, ослабленного пищевым отравлением и его последствиями.
Стимбифид Плюс — принципиально новое средство, в состав которого входят фруктополисахариды и фруктоолигосахариды, а также лактат кальция. В совокупности эти компоненты активно восстанавливают баланс кишечной микрофлоры, обеспечиваюи ее натуральным питательным субстратом и препятствуют размножению болезнетворных микроорганизмов.
Клинически доказано, что даже лучший пребиотик из числа современных наименований, не конкурирует по уровню эффективности с метапребиотиками. Метапребиотик Стимбифид Плюс не только предупреждает и лечит дисбактериоз после пищевого отравления, но и помогает бережно восстановить эпителий желудочно-кишечного тракта, который был поврежден продуктами жизнедеятельности бактерий и другими токсическими компонентами.
Кроме того, при тяжелых пищевых отравления могут назначаться антибиотики. Стимбифид Плюс поможет избежать последствий антибиотикотерапии. Начинать прием метапребиотика необходимо как можно раньше, и продолжать пить Стимбифид Плюс в течение 1,5-2 недель после нормализации общего состояния.
Отравление золотом и его побочные эффекты
Все противоревматические соединения золота содержат золото в окисляемом (I) состоянии. Неблагоприятное действие золотосодержащих противоревматических средств, по-видимому, обусловлено золотом III, продуктом окисления золота.
а) Клиника отравления золотом. 53-летнему мужчине по ошибке была сделана внутримышечная инъекция 450 мг ауротиомалата натрия. В течение 30 мин наблюдались отек век и сыпь. Концентрации золота в крови достигали 2970 мкг/100 мл, без значительных проявлений токсичности. Для лечения пациента применили БАЛ, пациент выздоровел.
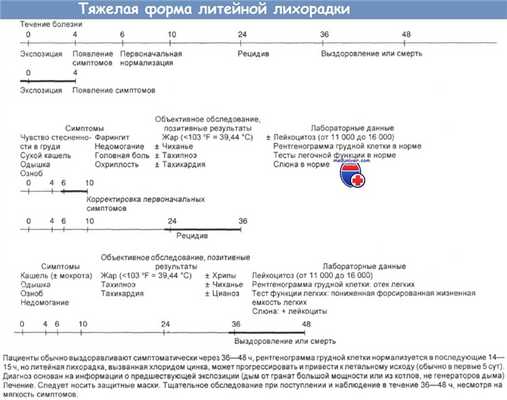
б) "Золотые легкие". "Золотые легкие" — редкий токсический побочный эффект, наблюдаемый при проведении лечения с применением золота, который может появиться после введения суммарной дозы от 300 до 1000 мг. За период от 2 до 10 сут внезапно начинается одышка. На рентгенограмме грудной клетки обнаруживают двусторонние диффузные затемнения в легких.
Может отмечаться умеренная эозинофилия. Утолщения кончиков пальцев ("барабанные палочки") не происходит. Исследования трансформации лимфоцитов позволяют предположить наличие гиперчувствительности к золоту. Для благоприятного прогноза достаточно отменить лечение золотом. Тесты функции легких выявляют рестрикционный дефект с пониженным коэффициентом переноса окиси углерода. Ухудшение функции легких может быть перманентным.
в) Нитритоидная реакция. Нитритоидная реакция представляет собой побочный эффект лечения ауротиомалатом натрия и включает кратковременное покраснение лица, тошноту, головокружение и в некоторых случаях гипотензию. Эта реакция наблюдается редко, начинается через несколько минут после внутримышечной инъекции и возникает неожиданно на протяжении первой недели после начала лечения золотом.
Нитритоидная реакция возникает чаще, если в схему лечения золотом вводят ангиотензин-преобразующий фермент.

- Влияние на желудочно-кишечный тракт. При лечении золотом, вводимым посредством инъекций или перорально, может развиться энтероколит, затрагивающий любой сегмент желудочно-кишечного тракта. В число симптомов могут входить лихорадка, тошнота, рвота и спазмы в брюшной полости с диареей. Эта болезнь чревата летальным исходом. Лечение начинают с немедленного прекращения применения золота. Может помочь пероральное применение кромолина.
- Влияние на печень. После инъекций золота может наблюдаться интрагепатический холестаз с эозинофилией. Это заболевание проходит без лечения. После прекращения терапии золотом тесты функции печени становятся нормальными примерно через 3 мес.
- Влияние на кровь. Сообщалось, что лечение золотом сопровождается развитием идиосинкразического агранулоцитоза и гипопла-стической анемии. Спонтанное восстановление нейтро-филов может произойти через 15—30 сут после прекращения приема лекарства. Филгастрин в дозе 10 мкг/сут (ГКСФ — гранулоцитарный колониестимулирующий фактор) может интенсифицировать миелоидное восстановление.
- Лимфаденопатия. После продолжительного лечения с применением золота в увеличенных регионарных лимфатических узлах могут обнаруживаться отложения золота.
- Влияние на почки. У 2—20 % пациентов, которых лечили инъекциями золота, отмечается протеинурия, и у 10—30 % из них она может быть достаточно тяжелой и вызвать нефротический синдром. Почечная биопсия выявляет мембранозный гломерулонефрит. При прекращении инъекций протеинурия обычно проходит. Функция почек не нарушается. В применении кортикостероидов, как правило, необходимости нет.
У пациентов с нарушенной способностью к сульфоокислению (пониженная способность окислять соединения, содержащие сульфгидрильные группы) может отмечаться предрасположенность к интоксикации ауротиомалатом натрия.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление железом и его побочные эффекты
а) Препараты. Предполагается, что клиническая токсичность развивается после приема внутрь по меньшей мере 20 мг/кг элементарного железа. Доля элементарного железа в фумарате железа равна 33 %, в хлориде — 28 %, в сульфате (наиболее распространенный источник) — 20 %, в хлориде — 20 % и в глюконате — 12 %. Проглатывание всего 5 или 6 таблеток высокоактивного препарата может привести к смерти ребенка с массой тела 10 кг.
- Жевательные препараты с железом. Передозировка железосодержащих жевательных витаминов остается одной из наиболее распространенных причин отравлений железом у детей. Дозы около 10 мг/кг элементарного железа, часто считающиеся нетоксичными, могут обусловить приближение концентрации железа в сыворотке к границе общей железосвязывающей способности (ОЖСС).
Кинетика абсорбции железа после проглатывания жевательных витаминов не совсем ясна. В одном контролируемом исследовании с участием добровольцев, которые принимали 6 мг элементарного железа на 1 кг массы тела в виде жевательных поливитаминов с железом (ПВЖ), было показано, что железо очень хорошо абсорбируется из жевательных ПВЖ. Жевательные витамины могут усилить абсорбцию железа — таким образом, "низкие" дозы могут вызвать системный эффект. Пока мало данных, подтверждающих целесообразность применения рентгенографии брюшной полости с целью идентификации железа, остающегося в желудочно-кишечном тракте после передозировки жевательных поливитаминов с железом.
Исследования на животных позволили установить 4 признака тяжелого отравления собак железом. Первый — снижение минутного сердечного выброса и среднего артериального давления независимо от применения интенсивной инфузионной реанимационной терапии. Второй — снижение частоты сердечных сокращений, которое, по меньшей мере частично, обусловлено снижением уровня СО. Третий: для поддержания внутрисосудистого объема необходимы внутривенные вливания больших количеств жидкости. Четвертый: развивается и сохраняется метаболический ацидоз вопреки неизмененному потреблению кислорода, при этом предполагается, что ацидоз обусловлен эффектами интоксикации железом, которые изолированы от ге-модинамических изменений.

б) Клиника отравления железом:
I. Начинается сразу после проглатывания. Могут наблюдаться рвота, диарея, боли в животе, гипотензия, бледность, летаргическое состояние, метаболический ацидоз, лейкоцитоз и гипергликемия.
II. Начинается через 6—24 ч и продолжается 12—24 ч. Признаки гиповолемии, летаргического состояния, гипотензии и метаболического ацидоза. Уровень железа в сыворотке не достигает пика.
III. Начинается через 12—24 ч после проглатывания. Множественные поражения органов (желудочно-кишечный тракт, центральная нервная система, сердечно-сосудистая система, функции почек и печени, метаболическая коагулопатия, гипогликемия). Быстро развивающаяся печеночная недостаточность обычно приводит к летальному исходу.
IV. Начинается через 4—6 нед. Шрамы в желудке, закупоривание привратника.
- Желудочно-кишечный тракт. Коррозионные эффекты железа (раздражение слизистой оболочки, геморрагический гастрит, изъязвление, кровотечение, ишемия, инфаркт и перфорация) могут вызывать значительные желудочно-кишечные симптомы, даже в дозах, значительно более низких, чем те, о которых известно, что они индуцируют системную токсичность.
- Коагулопатия. Типичные аномалии — подавление активности факторов V, VII, IX и X и фибриногена. Увеличиваются протромбиновое и частичное тромбопластиновое время. Коагулопатия может быть двухфазной, при этом наступает через несколько часов после передозировки. Она обратима и зависит от концентрации в сыворотке. Вторая, более поздняя фаза характеризуется гепатотоксичностью, которая сопровождается коагулопатией обычно через 24 ч после проглатывания. Коагулопатия обратима и зависит от железа в сыворотке.
в) Лабораторные данные отравления железом:
- Уровни в сыворотке. Нормальные уровни железа в сыворотке составляют 50—150 мкг/100 мл. Максимальные уровни железа в сыворотке отмечаются примерно через 4 ч после проглатывания. Токсическое действие железа не исключается при концентрациях в сыворотке, более низких, чем 350 мкг/100 мл. Общая железосвязывающая способность (ОЖСС) (в норме от 300 до 435 мкг/100 мл) усиливается при наличии высоких концентраций железа или дефероксамина в сыворотке. Уровень железа в сыворотке, более низкий, чем ОЖСС, не исключает острого отравления железом. Менее чем у 10 % пациентов с концентрациями железа в сыворотке ниже 500 мкг/100 мл развиваются сердечно-сосудистый коллапс или кома.
Дефероксамин, обеспечивая участки связывания железа, может привести к ошибочно завышенным результатам измерения ОЖСС. Ненадежность ОЖСС как показателя, определяющего принятие решения при назначении дефероксаминовой терапии, может быть обусловлена искажениями лабораторных определений в случаях отравлений железом . Даже если уровень железа в сыворотке превышает 300 мкг/100 мл и развивается клиническая интоксикация, уровень ОЖСС в действительности может оказаться непревышенным, он, по-видимому, повышается посредством неустановленного механизма.
У 22-месячного ребенка, отравившегося таблетками сульфата железа, уровень железа в сыворотке составлял 16 700 мкг/100 мл. После применения дефероксамина и интенсивной поддерживающей терапии ребенок выздоровел.
Что касается жевательных таблеток, уровни железа в сыворотке через 2 ч после проглатывания — слишком ранний показатель, чтобы по нему прогнозировать максимальные концентрации и оценивать потенциал системной токсичности. Значимость уровня железа в сыворотке после проглатывания жевательных таблеток еще предстоит установить.
- Кровь. Chyka и Butler рассмотрели 128 случаев отравления железом и не смогли подтвердить, что рвота, диарея, лейкоцитоз, гипергликемия и рентгеноконтрастность сами по себе свидетельствуют о том, что концентрация железа в сыворотке превышает 300 мкг/100 мл (54 мкмоль/л). При концентрациях, превышающих 500 мкг/100 мл (90 мкмоль/л), наблюдаются кома или совокупность следующих симптомов: лейкоцитоз, рентгеноконтрастность и повышенный анионный дефицит. Для выявления пациентов с отравлением железом нельзя полагаться только на такие показатели, как рвота, диарея, лейкоцитоз, гипергликемия и рентгеноконтрастность. Отсутствие всех этих признаков или симптомов, вероятно, обусловлено тем, что концентрация железа в сыворотке ниже 500 мкг/100 мл. Если при подозрении на отравление железом наблюдаются кома, рентгеноконтрастность, лейкоцитоз и повышенный анионный дефицит, целесообразны дополнительные тесты. Широкий разброс величин уровней железа в группах пациентов с сердечно-сосудистыми симптомами и в группах без таковых значительно затрудняет интерпретацию отдельных показателей. Наличие концентраций железа в сыворотке, превышающих общую железосвязывающую способность, не сопровождалось клиническими симптомами или окрашиванием мочи в винно-розовый цвет после применения дефероксамина. Концентрации глюкозы, превышающие 150 мг/100 мл, и число белых кровяных телец, превышающее 15 000, не свидетельствуют о том, что концентрации железа превышают 300 мкг/100 мл.
Лечение отравления железом и его антидот
Лечение отравления железом:
1. Собрать полный анамнез и провести физикальное обследование.
2. Обеспечить адекватное функционирование дыхательных путей, вентиляцию и кровообращение.
3. Провести лаваж желудка пациентам в случаях намеренного приема железа внутрь, положительных результатов при рентгенографии почек, мочеточников и мочевого пузыря и когда содержание элементарного железа в проглоченном продукте превышает 20 мг/кг. Нельзя применять бикарбонат натрия или фосфосоду.
4. Если у детей, проглотивших поливитамины, количество проглоченного элементарного железа ниже 20 мг/кг и показатели рентгенограмм почек, мочеточников и мочевого пузыря отрицательны, достаточно просто ограничиться наблюдениями.
5. Симптоматичным пациентам вводят ударную дозу 20 мл/кг изотонического раствора.
6. Необходимо определить уровни железа в сыворотке, креатинина, электролитов, концентрации гемоглобина в крови, продолжительность протромбинового времени, исходные показатели функции печени и газовый состав артериальной крови у пациентов с тяжелым отравлением.
7. Активированный уголь неэффективен.
8. Пероральное введение препаратов магния может снизить абсорбцию железа сывороткой.
Лечение тяжелобольных пациентов (необъяснимое изменение психического состояния, кровотечение или гипотензия) с подозрением на интоксикацию железом должно быть экстренным (дефероксамин), и не следует ждать, когда концентрация железа в сыворотке нормализуется.
а) Очистка желудочно-кишечного тракта — усиление выведения:
- Экстракорпоральное лечение. Полное промывание кишечника при лечении острого отравления железом, по-видимому, является безопасным эффективным средством очистки желудочно-кишечного тракта при отравлениях железом, но не проводилось ни одного контролируемого исследования, которое подтвердило бы это. Поскольку железо оказывает хорошо известное прямое коррозионное действие на слизистую оболочку желудочно-кишечного тракта, запоздалая госпитализация после острого отравления железом может привести к значительному повреждению желудочно-кишечного тракта. Поэтому следует соблюдать осторожность при полном промывании кишечника в тех случаях, когда у пациента повреждена слизистая оболочка. Противопоказаниями к полному промыванию кишечника являются серьезные желудочно-кишечные дисфункции, включая непроходимость и закупорку кишечника, перфорацию или значительное кровотечение в желудочно-кишечном тракте. Для документального подтверждения элиминации больших количеств таблеток железа из кишечника целесообразно сделать серию рентгенограмм брюшной полости .
Исходя из данных исследования на животных, можно предположить, что непрерывная артериально-веноз-ная гемофильтрация способна обеспечить удаление железа в случаях тяжелой интоксикации, особенно при почечной недостаточности.
б) Антидот железа - дефероксамин (Desferal). Окрашивание мочи в винно-розовый цвет — нечувствительный маркер при сильном повышении концентраций железа в сыворотке или при тяжелом отравлении железом. Отсутствие винно-розовой мочи после применения дефероксамина не исключает острой интоксикации железом или необходимости дефероксаминовой терапии. Поэтому применять провокационный ДФО-тест нецелесообразно. При остром отравлении железом предпочтительно внутривенное введение ДФО. При непрерывной внутривенной инфузии рекомендуемая доза дефероксамина составляет 15 мг/кг в час, хотя проводилось мало контролируемых исследований, в которых была подтверждена целесообразность применения этой дозы. Cheney и соавт. с успехом применяли вливания по 25 мг/кг в час в течение 12 ч в сутки в течение 3 сут ребенку с концентрацией железа 2687 мкмоль/л (выше 15 000 мкг/100 мл). Пероральный прием дефероксамина не снижает всасывание низких доз железа в организме человека.
- Применение. Хелатирующая терапия с применением дефероксамин-мезилата (ДФО: Desferal) показана в любом из перечисленных случаев.
1. Всем симптоматичным пациентам со значимыми симптомами (например, более 1 эпизода рвоты или диареи).
2. Пациентам с признаками летаргии, сильных болей в брюшной полости, гиповолемии или ацидоза.
3. Пациентам, у которых на рентгенограммах брюшной полости видны множественные рентгеноконтрастные участки. У огромного большинства этих пациентов будет развиваться симптоматическое отравление железом.
4. Любому симптоматичному пациенту с концентрацией железа в сыворотке выше 300—350 мкг/100 мл независимо от уровня ОЖСС. Bosse полагает, что в тех случаях, когда у бессимптомных пациентов концентрации железа в сыворотке находятся в пределах от 300 до 500 мкг/100 мл, а также в случаях проходящей без лечения некровавой рвоты или диареи в отсутствие других симптомов следует рекомендовать консервативный подход без дефероксаминовой терапии или провокационной стимуляции.
Дефероксамин, обеспечивающий участки связывания железа, способен обусловить завышение показателей ОЖСС, которые воспринимаются как показатели, отражающие уровень железосвязывающих белков (например, трансферрина, лактоферрина). Это чревато преждевременным прекращением дефероксаминовой терапии в случаях острой интоксикации железом.

- Другие способы применения. Дефероксамин применим в качестве антипролифератив-ного, противовоспалительного и иммуносупрессивного средства. Он подавляет пролиферацию Т-лимфоцитов и блокирует синтез ДНК посредством ингибирования рибонуклеотидредуктазы.
- Токсикокинетика. В организме человека общий клиренс дефероксамина составляет 0,296 л/ч на 1 кг. Почечный клиренс составляет примерно 1/3 от общего. Период полувыведения дефероксамина варьирует от 10 до 30 мин. Дефероксамин быстро метаболизируется главным образом в плазме, вероятно, ферментом, относящимся к альфа-глобулинам.
- Ферриоксамин. Комплекс железо + дефероксамин, ферриоксамин, плохо всасывается в желудочно-кишечном тракте. Его объем распределения составляет примерно 20 % массы тела, что соответствует внеклеточному пространству. Он не разлагается в той степени, которая поддается определению, и быстро выводится в неизмененном виде с мочой. Период его полувыведения составляет примерно 5,9 ч, а почечный клиренс варьирует от 516 до 1766 л/кг в час.
- Неблагоприятные эффекты:
Анафилактические и анафилактоидные реакции. Вызываемая дефероксамином IgE-опосредованная анафилаксия встречается редко. Введение болюса и/или быстрое вливание дозы выше 15 мг/кг в час вызывают выделение гистамина и гипотензию, особенно при гиповолемии.
Инфекции. После лечения передозировки железа дефероксамином может развиться обусловленная Yersinia enterocolitica септицемия, вызываемая энтеритом, который индуцирован железом или стимуляцией роста под воздействием железа и дефероксамина. По-видимому, есть взаимосвязь между передозировками железа в организме и бактериальными инфекциями при проведении диализа с применением дефероксамина или без него.
Зрение и слух. Описаны случаи ретробульбарной оптической невропатии; слабой, высокочастотной перцептивной тугоухости и катаракт.
Почечные и другие токсические эффекты. Могут наблюдаться острая почечная недостаточность, нарушение функции почек, тромбоцитопения и задержка роста.
Влияние на легкие. У 4 пациентов, которых после острого отравления железом лечили внутривенным введением дефероксамина в дозе 15 мг/кг в час в течение 5—92 ч, развился летальный респираторный дистресс-синдром взрослых. Авторы предупреждают, что дефероксамин не следует вводить внутривенно дольше 24 ч. Такой вывод был подвергнут сомнению, поскольку отравление железом само по себе может вызвать поражение легких; смерть могла наступить вследствие неправильного или запоздалого лечения, ежедневного применения дефероксамина (57— 120 г в течение 65—90 ч) и чрезмерного превышения обычно рекомендуемой дозы (примерно 6 г за 24 ч). Ранее сообщалось о поражении легких, вызванном высокими дозами дефероксамина, у пациентов с талассемией и запущенной злокачественной опухолью. Обусловленное дефероксамином поражение легких может наблюдаться после применения высоких доз. В основе поражающего действия лежит или индуцированное дефероксамином образование свободных радикалов, или нарушение синтеза каталазы и гема и индуцированное железом образование опасных оксидантов. Максимальная безопасная доза введения ДФО не установлена.

в) Показания. Выбор метода лечения обусловлен тяжестью симптомов и уровнем железа в сыворотке.
г) ОЖСС. Определение ОЖСС — трудоемкая процедура. Этот показатель ненадежен во время острой гиперферремии, а его воспроизводимость в разных лабораториях в нормо-ферремических условиях неприемлема. Взаимосвязь между превышением ОЖСС относительно концентрации железа в сыворотке и клинической токсичностью железа не установлена. Исходя из ОЖСС не следует определять начало дефероксаминовой терапии для пациентов с отравлением железом. Если окраска мочи неизменна, может помочь такой показатель, как уровень железа в сыворотке ниже 100—150 мкг/100 мл. При решении вопроса о прекращении курса лечения врач должен учитывать совокупность следующих факторов: отсутствие симптомов, осветление мочи и относительно нормальный уровень железа.
д) Критерии для прекращения терапии дефероксамином. Предложены следующие критерии для принятия решения о прекращении лечения. Вводится внутрисосудистая доза дефероксамина (15 мг/кг в час). Спустя 2 ч определяют соотношение содержащегося в моче железа и креатинина. Если оно выше 12,5, тест считается положительным и служит критерием для прекращения дефероксаминовой терапии, однако эти данные необходимо проверить.
е) Трансплантация печени. В случае молниеносно развивающейся печеночной недостаточности, индуцированной острой передозировкой железа, в качестве лечения может быть проведена трансплантация печени.
ж) Деферипрон. Деферипрон — перорально принимаемое хелатообразующее средство, связывающее железо, целесообразность применения которого в случаях передозировок железа не была систематически изучена.
XIII Международная студенческая научная конференция Студенческий научный форум - 2021

БИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ СОЕДИНЕНИЙ ЗОЛОТА НА ОРГАНИЗМ ЧЕЛОВЕКА
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке "Файлы работы" в формате PDF
В организме взрослого человека содержится около 10 мг золота, примерно половина от этого количества сконцентрировано в костях. Распределение золота в организме зависит от растворимости его соединений. Коллоидные соединения в большей степени накапливаются в печени, тогда как растворимые – в почках.
Механизм биологического действия соединений золота до конца не ясен, однако в настоящее время известно, что золото может входить в состав металлопротеидов, взаимодействовать с медью и с протеазами, гидролизующими коллаген, также как и с эластазами и другими активными компонентами соединительной ткани. Золото может вовлекаться в процессы связывания гормонов в тканях.
Токсическая и летальная дозы доза для человека не определены. Металлическое золото нетоксично, в отличие от органических производных, используемых как лекарственные препараты. Некоторые органические соединения золота токсичны, накапливаются в почках, печени, селезёнке и гипоталамусе, что может привести к органическим заболеваниям и дерматитам, стоматитам, тромбоцитопении.
Отравление золотом явление очень редкое. Механизм токсичности золота основан на большом сродстве этого элемента к сульфгидрильным группам SH-содержащих белков, в результате чего золото ингибирует SH-ферменты. Этот механизм реализуется, например, при лечении больных ревматоидным артритом, когда длительное введение препаратов золота приводит к снижению активности сульфгидрильных систем и энзимных комплексов лейкоцитов, в конечном итоге обеспечивая уменьшение концентрации ревматоидного фактора. Однако негативное действие избыточного количества золота легко снимается введением 2,3-димеркаптопропранола, SH-группа которого, отрывает золото от SH-содержащих белков, восстанавливая их нормальные свойства
Определение золота в организме проводят на основе изучения биосубстратов (кровь и биоптаты). В случаях отравления золотом в моче повышается содержание копропорфирина, ДАЛК (дельта-аминолевуленовая кислота).
Несмотря на то, что золото является инертным металлом, у части обладателей золотых ювелирных украшений развивается контактный дерматит. В ряде случаев золото может вызывать сенсибилизацию организма, что подтверждается при использовании этого металла в стоматологической практике, применении золотых нитей для армирования лица и тела и ряда других случаев.
Выраженным раздражающим действием на кожу обладают золота хлорид, трихлорид, цианид, калия дицианоаурат (который используется в электронной и химической промышленности, а также при производстве фаянса).
Значительные количества золота потребляет стоматология: коронки и зубные протезы изготовляют из сплавов золота с серебром, медью, никелем, платиной, цинком. Такие сплавы сочетают коррозионную стойкость с высокими механическими свойствами.
Золото усиливает бактерицидное действие серебра и оказывает антисептическое действие на бактерии и вирусы. Возможно участие золота в нормализации иммунных процессов в организме.
Органические соединения золота (препараты кризанол и ауранофин) применяются в медицине при лечении аутоиммунных заболеваний, в частности ревматоидного артрита. Радиоактивное золото используют при лечении злокачественных опухолей.
Читайте также:
- Лечение опухоли стромы полового тяжа у беременной - тактика
- Лечение посттрансфузионных реакций. Гемотрансфузионные осложнения переливания крови
- Дифференциальная диагностика заболеваний. Воспаление в медицине.
- Должное поглощение кислорода. Спирография
- Диагностика внематочной беременности. Дифференциация кишечной инфекции и внематочной беременности
