Ревматизм при пороках сердца. Аномалия развития сердца
Добавил пользователь Валентин П. Обновлено: 30.01.2026
Частота болей в сердце при врожденных пороках. Ревмокардит при врожденных пороках сердца
Мы проанализировали истории болезни всех больных, находившихся на обследовании в Институте хирургии. Оказалось, что жалобы на боли за грудиной и в области сердца — не столь редки. Лишь маленькие дети до 4—5 лет не предъявляли их, что, вероятно, связано с тем, что дети в этом возрасте вообще не могут локализовать своих ощущений. Дети школьного возраста отчетливо указывали на боли в области сердца, особенно при физической нагрузке.
По нашим данным, 20% больных с врожденными пороками сердца жаловались на боли в области сердца. При этом мы не смогли установить зависимости между состоянием миокарда (по данным электрокардиограм мы и баллистокардиограммы) и частотой возникновения болей.
Новейшие морфологические и биохимические исследования дают возможность предположить причину развития инфарктов у маленьких детей. Несмотря на резкое увеличение количества новообразованных интрамуральных сосудистых ветвей в гипертрофированном миокарде, обмен веществ, особенно при цианотичных пороках сердца, резко нарушен, что и приводит к развитию инфарктов. Боли в области сердца, на которые жалуются больные с врожденными пороками сердца уже с 5—6-летнего возраста, — один из показателей нарушения обменных процессов и, возможно, развития инфаркта миокарда.
Таким образом, при врожденных пороках сердца у маленьких детей могут наблюдаться инфаркты миокарда без поражения коронарных сосудов, обусловленные нарушением обменных процессов миокарда. Морфологически наблюдаются как микроинфаркты, так и обширные. Клинически они протекают бессимптомно, без типичного при этом состоянии болевого синдрома. При обширных участках поражения инфаркта миокарда они могут быть причиной смерти. Боли в области сердца, столь частые при врожденных пороках сердца, можно расценивать как один из показателей нарушения обменных процессов в миокарде.
Эти больные нуждаются в длительной предоперационной подготовке сердечными средствами (АТФ, кокарбоксилазой, витаминами) с целью нормализации обменных процессов в миокарде.
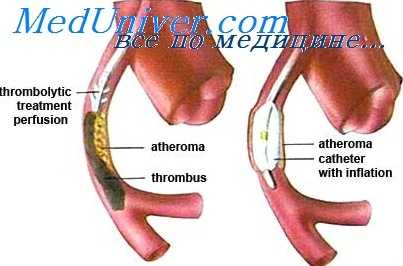
Ревмокардит при врожденных пороках сердца
Литературные данные о частоте ревматизма при врожденных пороках сердца весьма противоречивы. Большинство авторов указывают, что ревматизм наблюдается редко, однако White (1945), Taussig (1947) относят его к одному из частых осложнений.
Ревматизм чаще описывают при дефекте межпредсердной перегородки. Сочетание митрального стеноза и дефекта межпредсердной перегородки известно в литературе как синдром Лютембаше. Лютембаше, подробно описавший такое сочетание, считал митральный стеноз врожденным. Установлено, что у больных с дефектом межпредсердной перегородки он может быть как врожденным, так и приобретенным.
Большинство авторов считают митральный стеноз, сопутствующий дефекту межпредсердной перегородки, ревматическим. Частота его, по литературным данным, составляет 18—78%.
По мнению Edwards с соавторами (1955), разный процент находок митрального стеноза при дефектах межпредсердной перегородки объясняется различной оценкой авторами секционных и операционных находок. Даже при отсутствии ревматической инфекции в некоторых случаях митральный клапан при дефектах межпредсердной перегородки заметно утолщен, а левое венозное устье, будучи в норме уже правого, кажется еще более узким.
В таких случаях может создаться впечатление наличия митрального стеноза там, где его в действительности нет.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Ревматизм при пороках сердца. Аномалия развития сердца
Ревматизм при открытом артериальном протоке. Диагностика и течение ревматизма при врожденном пороке сердца
Опубликованы единичные описания сочетания ревматического и врожденного пороков сердца при открытом артериальном протоке (И. С. Богословский, 1930; В. Ф. Зеленин, 1952; К. Ф. Ширяева, 1965); тетраде Фалло (П. Н. Юренев и А. В. Буковская, 1952; Collins с соавт., 1960); коарктации аорты (Reifenstein, Gross, Levin, 1947; Н. Ф. Брижаненко, 1962); дефекте межжелудочковой перегородки (К. Ф. Ширяева, 1965; А. М. Спектор, 1966); изолированном стенозе легочной артерии (Shubin, Levinson, 1957); субаортальном стенозе (А. М. Спектор, 1966). Описан также случай острого ревмокардита у больного с sit. vise, inversus в сочетании с дефектом межпредсердной перегородки (Jennings, Kleiber, Levin, 1961).
Патологоанатомические данные также весьма противоречивы. По секционным данным Golfman, Levin (1942), на 181 аутопсию умерших в возрасте старше 2 лет ревматические изменения наблюдались в 25 (14%), при этом в 8 случаях ревматический порок сочетался с подострым септическим эндокардитом.
Durlacher, Beyer (1948) отметили ревматизм в 22 из 55 секционных случаев врожденных пороков сердца у умерших старше 2 лет, причем 4 умерли от ревматического миокардита.
Мы лишь в 1 случае наблюдали сочетание ревматического митрального и врожденного порока сердца — открытого артериального протока. Кроме того, у 106 (3,25%) больных в анамнезе имелось указание на перенесенный ревматизм. Кардиологическое обследование этих больных не выявило сочетания врожденного и приобретенного порока сердца.
Присоединение ревматического порока сердца к врожденному значительно отягощает течение последнего, ухудшает работу сердца, раньше приводит к декомпенсации. Диагностика ревматизма при наличии врожденного порока сердца трудна, так как симптомы, указывающие на изменение в состоянии больного, можно оценить как проявление ранней декомпенсации у больного с врожденным пороком и активного ревматического процесса.
Taussig (1947) указывает, что диагностика ревмаизма при наличии врожденного порока сердца затрудняется еще и тем, что у этих больных часто наблюдается подострый септический эндокардит. В связи с этим она рекомендует вначале проводить лечение антибиотиками и, если это окажется недостаточным, назначить антиревматическую терапию.
Для диагностики активного ревматического процесса у больных, страдающих врожденными пороками сердца, имеют значение все иммунологические реакции, применяемые в настоящее время.
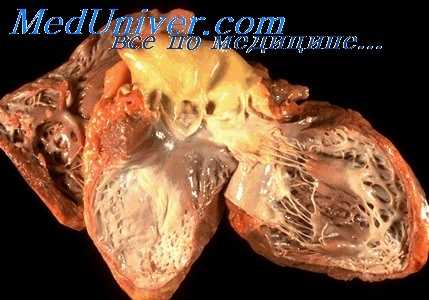
При сочетании врожденного и ревматического порока сердца диагноз устанавливается при помощи обычных клинических и инструментальных методов исследования (ЭКГ, ФКГ, БКХ, рентгенография и рентгенокимография, внутрисердечные исследования) и при выраженной клинической картине обоих пороков не представляет трудностей.
Опубликованы единичные описания хирургического лечения сочетанных пороков сердца (Bedford с соавт., 1957; В. С. Савельев, И. Г. Костенко, 1961). Мы диагностировали сочетанный врожденный и ревматический пороки сердца только у одной больной.
Некоторые наши больные указывали, что перенесли суставную форму ревматизма. Однако ревматическая атака у них не сопровождалась ни повышением температуры, ни изменением конфигурации суставов. Больных лишь беспокоили боли в суставах. Можно полагать, что у некоторых они связаны с нарушением солевого обмена и ранним развитием подагры. В литературе имеются указания, что у больных с врожденными пороками сердца «синего» типа рано (с 16—18 лет) развивается подагра (Sommervill, 1967; Bernheim, Chabot, 1963).
Причиной болей в суставах может быть кардиотонзиллярный синдром. Известно, что у больных с врожденным пороком сердца часто наблюдается хронический тонзиллит (С. А. Серебрякова, 1965; Н. А. Вишневская, 1966).
В ряде случаев врачи длительное время не диагностировали врожденный порок сердца, полагая, что изменения в сердце обусловлены ревмокардитом. Больные в течение нескольких лет лечились по поводу ревматизма и обращались в наш институт для оперативного лечения митрального порока сердца. При амбулаторном и стационарном обследовании у них устанавливали диагноз врожденного порока сердца.
Таким образом, ревматизм при врожденных пороках сердца — осложнение чрезвычайно редкое. Диагностика его трудна. Ревмокардит необходимо дифференцировать от подострого септического эндокардита. При сочетании ревматического и врожденного пороков сердца диагностика также сложна. В этих случаях целесообразно производить коррекцию обоих пороков одновременно.
Ревматизм (в частности, хорея) является этиологическим моментом в 80% пороков сердца.
Здесь следует отметить, что поражение миндалин, зубов, придаточных полостей носа, а также осенне-весенние катарры верхних дыхательных путей играют определенную роль в возникновении и обострениях ревматического процесса. В какой мере перечисленные органы являются «входными воротами» для ревматической инфекции, статистические исследования точно не выяснили, однако роль ангины можно считать в настоящее время вполне установленной.
Наш материал, в котором мы учли два момента — перенесенные заболевания и период, с которым сами больные связывают появление порока сердца, показал, что перенесли суставной ревматизм 42,6% больных, связывают начало заболевания с суставным ревматизмом 22,6%.
Обращает на себя внимание то, что 47% больных могли указать момент начала заболевания, 8,8% больных связывали его с ангиной, в то время как большинство авторов эту причину обходит молчанием или указывает низкие цифры. Мы полагаем, что роль ангины недооценивается, так как среди наших больных острый тонзиллит в анамнезе отмечается в 26%.
Сифилис в анамнезе чаще всего отмечается у больных с аортальными пороками, в то время как больные с поражениями двустворчатого клапана имели в своем анамнезе сифилис лишь в небольшом числе.
Сепсис (затяжной септический эндокардит) после излечения может оставить порок. Статистических данных пока нет.
Склеротические изменения клапанного аппарата на почве атероматоза встречаются чаще у мужчин в пожилом возрасте и не превышают 5—10% общего количества случаев пороков сердца.
Различные острые инфекции также иногда обусловливают развитие пороков клапанов. В. И. Молчанов придает особое значение скарлатине.
Травматические повреждения клапанов встречаются не чаще чем в 2%.
Аномалия развития сердца обнаруживается еще реже — в 0,2—0,5%.
По статистике Черногубова (1950), основанной на изучении 1 121 секционного случая с пороками сердца, они распределяются следующим образом по этиологии, возрасту и локализации поражения клапанов. Комбинированные пороки ревматической этиологии встречаются более чем в 2 раза чаще, чем простые (простыми пороками Черногубов называет изолированные пороки— сужение отверстия или недостаточность клапана, а также сочетание стеноза отверстия и недостаточности клапана того же отверстия; комбинированными — поражение нескольких отверстий); во-вторых, что при простых пороках септический эндокардит поражает преимущественно аортальные клапаны (по обоим полам в 7 раз чаще, чем ревматизм, а у женщин более чем в 15 раз чаще); в-третьих, что септический эндокардит почти никогда не встречается на трехстворчатом клапане; в-четвертых, что при комбинированном пороке у женщин почти во всех случаях (99,4%) имеет место митральный порок и, наконец, в-пятых, что наличие порока трехстворки почти всегда указывает и на наличие митрального порока.
При этом следует отметить, что при ревматизме и септическом эндокардите чаще встречаются комбинированные пороки (70,6% и 61,2%), а при сифилисе и атеросклерозе — чаще простые пороки.
Следует еще добавить, что при малом количестве пороков сифилитической (56 человек) и атеросклеротической (64 человека) этиологии процентные отношения по категории порока мало убедительны.
Опухоли сердца являются лишь редкой, казуистической находкой.
Ревмокардит
Ревмокардит – это поражение различных слоев сердца (эндокарда, миокарда, перикарда) и клапанного аппарата, вызванное острой ревматической лихорадкой. Основные симптомы ревмокардита включают повышение температуры, слабость, ощущения сердцебиения или неправильной работы сердца, явления недостаточности кровообращения. В диагностике имеют значение анамнестические данные, наличие маркеров воспаления и увеличение титра антистрептококковых антител в крови, данные электро- и эхокардиографии. Консервативное лечение проводится с помощью антибиотиков и противовоспалительных средств; при формировании сердечного порока показана кардиохирургическая операция.
МКБ-10
Общие сведения
Ревмокардит (ревматический кардит) является не самостоятельным заболеванием, а ведущим компонентом острой ревматической лихорадки (ОРЛ), определяющим тяжесть состояния пациента. Поражение сердца может протекать как изолированно, так и вместе с другими проявлениями ревматизма (боли в суставах, высыпания, подкожные узелки, гиперкинезы). После первичной ревматической атаки ревмокардит возникает у 79-83% детей и 90-93% взрослых, при рецидиве ревматической лихорадки развивается у 100% пациентов, являясь ведущей причиной приобретенных пороков сердца. Встречаемость кардита у лиц мужского и женского пола одинакова.
Причины ревмокардита
Ревматический кардит служит проявлением системного ревматического воспаления, которое, в свою очередь, развивается как осложнение перенесенной стрептококковой инфекции глотки (хронического тонзиллита, острой ангины). Ведущая роль в каскаде патологических реакций отводится определенным штаммам бета-гемолитического стрептококка группы А (БГСА). Благодаря уникальным антигенным свойствам строения клеточной оболочки (факторам ревматогенности) они способны запускать в организме человека реакции иммунной аутоагрессии против собственных соединительных тканей, в т. ч. образующих сердечные оболочки.
Однако стрептококковая инфекция вызывает ревматическую лихорадку не у всех людей, а только у 3%, которые имеют к этому наследственную предрасположенность. Это связано с индивидуальной реактивностью иммунной системы. В ходе многолетних клинических исследований было обнаружено, что у 90-100% больных ревматизмом имеются специфические аллоантигены D8/17 на В-лимфоцитах, которые могут служить маркерами генетической детерминированности заболевания. Также доказана корреляция ОРЛ с определенными антигенами гистосовместимости, в частности, поражение клапанного аппарата обычно ассоциировано с HLA-A3 и HLA-В15. Еще одним важнейшим фактором развития ОРЛ и ревмокардита является сенсибилизация макроорганизма, т. е. повторное перенесение стрептококковой инфекции. Именно поэтому ревматизм чаще развивается у взрослых и детей 7-15 лет и не встречается среди младшей возрастной группы.
Патогенез
Наиболее важную патогенетическую роль играет М-протеин, который обладает сильной иммуногенностью, т. е. способностью вызывать иммунный ответ. Этот белок входит в состав мембраны стрептококка и имеет ту же молекулярную структуру, что и мембраны кардиомиоцитов (феномен молекулярной мимикрии). Благодаря такому феномену возникает перекрестная аутоиммунная реакция, при которой Т-лимфоциты наряду с бактериями атакуют собственные клетки сердца. В патогенезе также принимают участие экзоферменты стрептококка, которые обладают прямым повреждающим действием на клетки соединительной ткани (стрептолизин О, стрептолизин S, гиалуронидаза, стрептокиназа).
Патоморфологически ревмокардит протекает в 4 стадии, каждая из которых продолжается 1-2 месяца: мукоидное набухание, фибриноидное набухание, образование ревматической гранулемы, склероз. В процессе этих стадий происходит разрушение основного вещества соединительной ткани, образуются очаги некроза и ревматические гранулемы. Исходом является склероз, т. е. рубцевание. Наиболее пагубное влияние эти процессы оказывают на сердечные клапаны, которые деформируются, что приводит к формированию сердечных пороков. Именно пороки сердца в исходе ревматического воспаления и являются чрезвычайно актуальной проблемой.
Классификация
В клинической кардиологии ревмокардит подразделяется на первичный (дебютная атака) и возвратный (последующие атаки); сопровождающийся формированием клапанного порока или протекающий без поражения клапанов. При ревмокардите поражаются различные отделы сердца. По степени вовлечения в воспалительный процесс стенок сердца различают:
- Эндокардит. Инфекционный эндокардит встречается практически в 100% случаев, т. е. является обязательным компонентом ревмокардита. Может сочетаться с вальвулитом - воспалением клапанов.
- Миокардит. При воспалении сердечной мышцы увеличиваются размеры сердца и ухудшается его сократительная функция. В основном именно миокардит определяет тяжесть заболевания. Для ревмокардита наиболее типично сочетание воспаления клапанов и сердечной мышцы – эндомиокардит.
- Перикардит. Воспаление сердечной сумки (перикардит) наблюдается достаточно редко ‒ в 2-3% случаев. Вовлечение всех стенок сердца (панкардит) также происходит нечасто.
Существуют специальные клинические критерии для определения степени тяжести ревмокардита: органический шум в сердце, увеличение размеров сердца (кардиомегалия), признаки сердечной недостаточности (выраженная одышка, цианоз, отеки нижних конечностей, увеличение размеров печени, расширение вен шеи, влажные хрипы в легких), шум трения перикарда или признаки перикардиального выпота. Учитывая эти критерии, в течении ревмокардита выделяют три степени тяжести:
- Легкая. Диагностируется при наличии только органического шума.
- Средняя. Определяется при наличии органического шума и кардиомегалии.
- Тяжелая. Выставляется при наличии шума, кардиомегалии, недостаточности кровообращения и перикардиального выпота.
Симптомы ревмокардита
Клинические проявления начинают развиваться через 2-3 недели после стрептококковой инфекции верхних дыхательных путей. В начале заболевания симптоматика неспецифична – утомляемость, повышение температуры тела до субфебрильных или фебрильных цифр, потливость. Примерно через неделю присоединяются симптомы со стороны сердца - затруднение дыхания, ощущение сильного сердцебиения и перебоев в работе сердца, боли в области сердца неопределенного характера. В случае тяжелого течения ревмокардита наряду с вышеперечисленными симптомами возникают выраженная одышка, кашель, отеки ног, тяжесть в правом подреберье из-за увеличенной печени. Период атаки ревмокардита продолжается от 2-х до 6-ти месяцев, после чего либо наступает выздоровление, либо формируется порок сердца.
Осложнения
Основная опасность ревмокардита ‒ развитие сердечных пороков. Частота этого явления составляет 20-25%. При длительном течении пороки сердца приводят к сердечной недостаточности, повышению давления в сосудах малого круга кровообращения, расширению полостей сердца, образованию в них тромбов и ишемическому инсульту. Еще одно осложнение ‒ миокардиосклероз, т. е. замещение сердечной мышцы рубцовой тканью. При этом развиваются различные нарушения ритма сердца и снижение его сократительной функции. Все эти патологии вынуждают пациента прибегать к постоянной лекарственной терапии, ухудшают качество и уменьшают продолжительность его жизни.
Диагностика
Ревмокардит является основным проявлением ОРЛ, для диагностирования которой используются специально разработанные клинические и лабораторные критерии. Они включают кардит, артрит, малую хорею, кольцевидную эритему, подкожные узелки, лихорадку и данные, свидетельствующие о наличии стрептококковой инфекции в организме. Диагностика непосредственно ревмокардита проводится следующими методами:
- Аускультативными. При ревмокардите аускультативная картина разнообразна. У пациентов выслушиваются шумы в проекции митрального и аортального клапанов (наиболее специфичны протодиастолический шум и мезосистолический шум Кера-Кумбса), ослабление и глухость тонов сердца, дополнительные тоны, трение перикарда, изменение частоты сердечных сокращений, неритмичное сердцебиение, ритм галопа.
- Лабораторными. В общем и биохимическом анализе крови выявляется наличие воспалительных маркеров (нейтрофильный лейкоцитоз, сдвиг лейкоцитарной формулы влево, увеличение скорости оседания эритроцитов, С-реактивного белка). Также обнаруживаются высокие титры антител к стрептококку - антистретолизин-О (АСЛО), антистрептогиалуронидаза (АСГ), антистрептокиназа (АСК), антидезоксирибонуклеаза-В (АДНК-В).
- Инструментальными. На ЭКГ обнаруживаются нарушения ритма и проводимости сердца – тахи- или брадикардия, удлинение интервала PQ, экстрасистолия, предсердно-желудочковая блокада I или II степени, признаки перегрузки левых отделов сердца. Эхо-КГ – наиболее точный визуализирующий метод. Выявляет утолщение или деформацию створок клапанов, признаки регургитации (обратного тока крови), снижение сократительной функции сердца (фракции выброса), расширение полостей сердца, утолщение листков перикарда, выпот в перикардиальную полость.
Ревмокардит дифференцируют со следующими заболеваниями: инфекционный эндокардит, кардиомиопатии, поражения клапанов сердца при серонегативных спондилоартропатиях и системной красной волчанке, антифосфолипидный синдром, вирусные миокардиты. В дифференциальной диагностике обязательно принимают участие кардиолог и ревматолог.
Лечение ревмокардита
Первым условием успешного лечения является госпитализация в кардиологический стационар или отделение ревматологии. Необходимо соблюдать постельный режим минимум 4 недели. При тяжелом ревмокардите обязателен строгий постельный режим до исчезновения симптомов недостаточности кровообращения. Рекомендуется питание с повышенным содержанием белка и витаминов. Лечение ревмокардита следующее:
- Этиотропная терапия. Так как основной причиной ревмокардита является стрептококковая инфекция, этиотропная терапия направлена на ее эрадикацию. Для этого применяются антибиотики пенициллинового ряда – бензилпенициллин, феноксиметилпенициллин. При развитии аллергических реакций на пенициллины их заменяют другими группами антибиотиков – макролидами (азитромицин), цефалоспоринами (цефуроксим), линкозамидами (линкомицин).
- Патогенетическая терапия. Подразумевает лечение непосредственного ревматического воспаления. Обычно применяются нестероидные противовоспалительные средства (в основном, это диклофенак). Однако при тяжелом течении ревмокардита необходимы препараты, обладающие мощным противовоспалительным действием. В таких случаях используют глюкокортикостероиды (преднизолон).
- Симптоматическая терапия. Заключается в коррекции сердечной недостаточности. Обязательно нужно ограничить употребление поваренной соли (менее 3 грамм в сутки). Лекарственные средства применяют у пациентов с уже имеющимся пороком сердца и тяжелой недостаточностью кровообращения. Это ингибиторы АПФ, диуретики, бета-блокаторы, сердечные гликозиды, антагонисты альдостерона.
- Хирургическое лечение. Показано при сформировавшихся тяжелых пороках сердца, вызывающих грубые гемодинамические нарушения и резистентных к лекарственной терапии. В зависимости от вида порока (стеноз или недостаточность), а также от пораженного клапана применяются коммисуротомия, вальвулопластика или протезирование клапана искусственными или биологическими протезами.
При выписке из стационара необходимо постоянное диспансерное наблюдение у кардиолога или ревматолога, периодическое проведение эхокардиографии для оценки состояния клапанов сердца. Обязательно посещение оториноларинголога, который проводит промывание лакун миндалин. При неэффективности промывания прибегают к радикальному методу ‒ тонзиллэктомии. Ее следует выполнять при стихании активного ревматического процесса и стабильном состоянии пациента.
Прогноз и профилактика
Прогноз при ревмокардите напрямую зависит от формирования порока сердца. Люди с ревматическим пороком имеют повышенный риск развития инфекционного эндокардита. Им показана антибиотикопрофилактика при различных хирургических манипуляциях – стоматологических процедурах, операциях на ЛОР-органах и т. д. Первичная профилактика подразумевает правильное и своевременное лечение тонзиллита. С этой целью применяются те же антибиотики, что и для лечения ревмокардита. Для предупреждения рецидива ревмокардита существует так называемая вторичная профилактика. Она заключается в ежемесячном внутримышечном введении антибиотиков пенициллинового ряда пролонгированного действия (бензатина бензилпенициллин). Продолжительность такой профилактики зависит от того, сформировался после ревмокардита порок сердца или нет.
3. Исходы первичного ревматизма по данным проспективного клинико-эпидемиологического обследования/ Крюкова Т.В. – 1997.
4. Кардиологические аспекты ревматологии в работах сотрудников ИВГМА/ Мясоедова С.Е.// Вестник Ивановской медицинской академии. – 2009.
Ревматизм у детей
Ревматизм у детей – инфекционно-аллергическое заболевание, протекающее с системным поражением соединительной ткани сердечно-сосудистой системы, синовиальных оболочек суставов, серозных оболочек ЦНС, печени, почек, легких, глаз, кожи. При ревматизме у детей может развиваться ревматический полиартрит, ревмокардит, малая хорея, ревматические узелки, кольцевидная эритема, пневмония, нефрит. Диагностика ревматизма у детей основана на клинических критериях, их связи с перенесенной стрептококковой инфекцией, подтвержденных лабораторными тестами и маркерами. В лечении ревматизма у детей применяются глюкокортикоиды, НПВС, препараты хинолинового и пенициллинового ряда.
Ревматизм у детей (ревматическая лихорадка, болезнь Сокольского-Буйо) – системное заболевание воспалительного характера, характеризующееся поражением соединительной ткани различных органов и этиологически связанное со стрептококковой инфекцией. В педиатрии ревматизм диагностируется преимущественно у детей школьного возраста (7-15 лет). Средняя популяционная частота составляет 0,3 случая ревматизма на 1000 детей. Ревматизм у детей характеризуется острым началом, нередко длительным, на протяжении многих лет, течением с чередованием периодов обострений и ремиссий. Ревматизм у детей служит распространенной причиной формирования приобретенных пороков сердца и инвалидизации.
Причины ревматизма у детей
Накопленный в ревматологии опыт позволяет отнести ревматизм у детей к инфекционно-аллергическому заболеванию, в основе которого лежит инфекция, вызванная β-гемолитическим стрептококком группы А (М-серотип), и измененная реактивность организма. Таким образом, заболеваемости ребенка ревматизмом всегда предшествует стрептококковая инфекция: тонзиллит, ангина, фарингит, скарлатина. Этиологическое значение β-гемолитического стрептококка в развитии ревматизма у детей подтверждено обнаружением в крови большинства больных противострептококковых антител – АСЛ-О, антистрептокиназы, антистрептогиалуронидазы, антидезоксирибонуклеазы В, обладающих тропностью к соединительной ткани.
Важная роль в развитии ревматизма у детей отводится наследственной и конституциональной предрасположенности. В ряде случаев прослеживается семейный анамнез ревматизма, а тот факт, что ревматической лихорадкой заболевает только 1–3% детей и взрослых, перенесших стрептококковую инфекцию, позволяет говорить о существовании так называемого «ревматического диатеза».
Ведущими факторами вирулентности β-гемолитического стрептококка выступают его экзотоксины (стрептолизин-О, эритрогенный токсин, гиалуронидаза, протеиназа), обусловливающие пирогенные, цитотоксические и иммунные реакции, вызывающие повреждение сердечной мышцы с развитием эндомиокардита, нарушений сократимости и проводимости миокарда.
Кроме этого, протеины клеточной стенки стрептококка (липотейхоевая кислота пептидогликан, полисахарид) инициируют и поддерживают воспалительный процесс в миокарде, печени, синовиальных оболочках. М-протеин клеточной стенки подавляет фагоцитоз, оказывает нефротоксическое действие, стимулирует образование антикардиальных антител и т. п. В основе поражения кожи и подкожной клетчатки при ревматизме у детей лежит васкулит; ревматическая хорея обусловлена поражением подкорковых ядер.
Классификация ревматизма у детей
В развитии ревматизма у детей выделяют активную и неактивную фазы. Критериями активности ревматического процесса выступают выраженность клинических проявлений и изменения лабораторных маркеров, в связи с чем выделяют три степени:
- I (минимальная активность) - отсутствие экссудативного компонента воспаления; слабая выраженность клинических и лабораторных признаков ревматизма у детей;
- II (умеренная активность) – все признаки ревматизма у детей (клинические, электрокардиографические, рентгенологические, лабораторные) выражены нерезко;
- III (максимальная активность) – преобладание экссудативного компонента воспаления, наличие высокой лихорадки, признаков ревмокардита, суставного синдрома, полисерозита. Присутствие отчетливых рентгенологических, электро- и фонокардиографических признаков кардита. Резкие изменения лабораторных показателей – высокий нейтрофильный лейкоцитоз. Резко положительный СРБ, высокий уровень сывороточных глобулинов, значительное повышение титров антистрептококковых антител и пр.
Неактивная фаза ревматизма у детей отмечается в межприступный период и характеризуется нормализацией самочувствия ребенка, инструментальных и лабораторных показателей. Иногда между приступами ревматической лихорадки сохраняется субфебрилитет и недомогание, отмечается прогрессирование кардита с формированием клапанных пороков сердца или кардиосклероза. Неактивная фаза ревматизма у детей может продолжаться от нескольких месяцев до нескольких лет.
Течение ревматизма у детей может быть острым (до 3-х месс.), подострым (от 3 до 6 мес.), затяжным (более 6 мес.), непрерывно-рецидивирующим (без четких периодов ремиссии длительностью до 1 года и более), латентным (скрыто приводящим к формированию клапанного порока сердца).
Симптомы ревматизма у детей
Клинические проявления ревматизма у детей многообразны и вариабельны. К основным клиническим синдромам относят ревмокардит, полиартрит, малую хорею, анулярную эритему и ревматические узелки. Для всех форм ревматизма у детей характерна клиническая манифестация спустя 1,5-4 недели после предшествующей стрептококковой инфекции.
Поражение сердца при ревматизме у детей (ревмокардит) происходит всегда; в 70-85% случаев – первично. При ревматизме у детей может возникать эндокардит, миокардит, перикардит или панкардит. Ревмокардит сопровождается вялостью, утомляемостью ребенка, субфебрилитетом, тахикардией (реже брадикардией), одышкой, болями в сердце.
Повторная атака ревмокардита, как правило, случается через 10-12 месяцев и протекает тяжелее с симптомами интоксикации, артритами, увеитами и т. д. В результате повторных атак ревматизма у всех детей выявляются приобретенные пороки сердца: митральная недостаточность, митральный стеноз, аортальная недостаточность, стеноз устья аорты, пролапс митрального клапана, митрально-аортальный порок.
У 40-60% детей с ревматизмом развивается полиартрит, как изолированно, так и в сочетании с ревмокардитом. Характерными признаками полиартрита при ревматизме у детей являются преимущественное поражение средних и крупных суставов (коленных, голеностопных, локтевых, плечевых, реже - лучезапястных); симметричность артралгии, мигрирующий характер болей, быстрое и полное обратное развитие суставного синдрома.
На долю церебральной формы ревматизма у детей (малой хореи) приходится 7-10% случаев. Данный синдром, главным образом, развивается у девочек и проявляется эмоциональными расстройствами (плаксивостью, раздражительностью, сменой настроения) и постепенно нарастающими двигательными нарушениями. Вначале изменяется почерк и походка, затем появляются гиперкинезы, сопровождающиеся нарушением внятности речи, а иногда – невозможностью самостоятельного приема пищи и самообслуживания. Признаки хореи полностью регрессируют через 2-3 месяца, однако имеют склонность к рецидивированию.
Проявления ревматизма в виде анулярной (кольцевидной) эритемы и ревматических узелков типично для детского возраста. Кольцевидная эритема представляет собой разновидность сыпи в виде колец бледно-розового цвета, локализующихся на коже живота и груди. Зуд, пигментация и шелушение кожи отсутствуют. Ревматические узелки можно обнаружить в активную фазу ревматизма у детей в затылочной области и в области суставов, в местах прикрепления сухожилий. Они имеют вид подкожных образований диаметром 1-2 мм.
Висцеральные поражения при ревматизме у детей (ревматическая пневмония, нефрит, перитонит и др.) в настоящее время практически не встречаются.
Диагностика ревматизма у детей
Ревматизм у ребенка может быть заподозрен педиатром или детским ревматологом на основании следующих клинических критериев: наличия одного или нескольких клинических синдромов (кардита, полиартрита, хореи, подкожных узелков или кольцевидной эритемы), связи дебюта заболевания со стрептококковой инфекцией, наличия «ревматического анамнеза» в семье, улучшения самочувствия ребенка после специфического лечения.
Достоверность диагноза ревматизма у детей обязательно должна быть подтверждена лабораторно. Изменения гемограммы в острую фазу характеризуются нейтрофильным лейкоцитозом, ускорением СОЭ, анемией. Биохимический анализ крови демонстрирует гиперфибриногенемию, появление СРБ, повышение фракций α2 и γ-глобулинов и сывороточных мукопротеинов. Иммунологическое исследование крови выявляет повышение титров АСГ, АСЛ-О, АСК; увеличение ЦИК, иммуноглобулинов А, М, G, антикардиальных антител.
При ревмокардите у детей проведение рентгенографии грудной клетки выявляет кардиомегалию, митральную или аортальную конфигурацию сердца. Электрокардиография при ревматизме у детей может регистрировать различные аритмии и нарушения проводимости (брадикардию, синусовую тахикардию, атриовентрикулярные блокады, фибрилляцию и трепетание предсердий). Фонокардиография позволяет зафиксировать изменения тонов сердца и шумы, свидетельствующие о поражении клапанного аппарата. В выявлении приобретенных пороков сердца при ревматизме у детей решающая роль принадлежит ЭхоКГ.
Дифференциальную диагностику ревмокардита проводят с неревматическими кардитами у детей, врожденными пороками сердца, инфекционным эндокардитом. Ревматический полиартрит необходимо отличать от артритов другой этиологии, геморрагического васкулита, СКВ. Наличие у ребенка церебрального синдрома требует привлечения к диагностике детского невролога и исключения невроза, синдрома Туретта, опухолей мозга и др.
Лечение ревматизма у детей
Терапия ревматизма у детей должна быть комплексной, непрерывной, длительной и поэтапной.
В острой фазе показано стационарное лечение с ограничением физической активности: постельный режим (при ревмокардите) или щадящий режим при других формах ревматизма у детей. Для борьбы со стрептококковой инфекцией проводится антибактериальная терапия препаратами пенициллинового ряда курсом 10-14 дней. С целью подавления активного воспалительного процесса назначаются нестероидные (ибупрофен, диклофенак) и стероидные противовоспалительные препараты (преднизолон). При затяжном течении ревматизма у детей в комплексную терапию включаются базисные препараты хинолинового ряда (гидроксихлорохин, хлорохин).
На втором этапе лечение ревматизма у детей продолжается в ревматологическом санатории, где проводится общеукрепляющая терапия, ЛФК, грязелечение, санирование очагов инфекции. На третьем этапе наблюдение ребенка специалистами (детским кардиологом-ревматологом, детским стоматологом, детским отоларингологом) организуется в условиях поликлиники. Важнейшим направлением диспансерного наблюдения служит антибиотикопрофилактика рецидивов ревматизма у детей.
Прогноз и профилактика ревматизма у детей
Первичный эпизод ревмокардита сопровождается формированием пороков сердца в 20-25% случаях; однако возвратный ревмокардит не оставляет шансов избежать повреждения клапанов сердца, что требует последующего кардиохирургического вмешательства. Летальность от сердечной недостаточности, обусловленной пороками сердца, доходит до 0,4-0,1%. Исход ревматизма у детей во многом определяется сроками начала и адекватностью терапии.
Первичная профилактика ревматизма у детей предполагает закаливание, полноценное питание, рациональную физическую культуру, санацию хронических очагов инфекции (в частности, своевременную тонзиллэктомию). Меры вторичной профилактики направлены на предупреждение прогрессирования ревматизма у детей, перенесших ревматическую лихорадку, и включают введение пенициллина пролонгированного действия.
Читайте также:
- Тактика при фиброваскулярной пролиферации стекловидного тела. Регматогенная отслойка сетчатки
- Диагностика туберкулеза предстательной железы. Обследование при туберкулезном простатите
- Лечение брадиаритмий. Тактика при блокадах сердца.
- Когда посетить врача
- Осложнения применения катетера Свана-Ганса. Ценность катетера Свана-Ганса
