Секвестрация легких. Эмфизема легких
Добавил пользователь Евгений Кузнецов Обновлено: 20.01.2026
Эмфизема. Гемоторакс
Скопление воздуха в тканях является частым спутником травмы груди. Подкожная эмфизема развивается, как правило, вследствие возникновения пневмоторакса. Обязательным условием при этом является повреждение париетальной плевры (открытые ранения, переломы ребер). Попавший в плевральную полость воздух при кашле или дыхании через дефект плевры проникает в подкожную клетчатку, откуда легко распространяется на грудь, шею, живот и другие участки тела. Особенно выраженной подкожная эмфизема бывает при напряженном пневмотораксе, когда воздух буквально накачивается в клетчатку, межфасциальные и межмышечные пространства. Этот механизм иногда является спасительным для пострадавшего, ибо таким, путем компенсируется клапанный пневмоторакс.
Сама по себе подкожная эмфизема не представляет опасности для больного. Положение становится тревожным только в том случае, если воздух проникает на шею и в средостение. Сдавление магистральных сосудов и трахеи может привести к тяжелым дыхательным и гемодинамическим нарушениям. В большинстве случаев специального лечения подкожная эмфизема не требует. При очень больших ее размерах в области наибольшего скопления воздуха можно ввести в подкожиую клетчатку несколько коротких толстых (типа Дюфо) игл и через них «сцедить» воздух.
Медиастинальная эмфизема является очень серьезным осложнением травмы груди. Возникновение ее связано с поступлением воздуха через надрыв медиастинальной плевры при разрыве трахеи или крупных бронхов, а также ткани легкого при наличии плевральных сращений. Клетчатка средостения обладает присасывающим действием во время вдоха, поэтому воздух очень быстро проникает не только в средостение, но и нашею, откуда распространяется на туловище, и конечности. Тяжесть клинической картины связана прежде всего со сдавленнем сердца и сосудов средостения попавшим туда воздухом. Наиболее чувствительны венозные магистрали (полые, легочные, подключичные вены), сдавление которых быстро приводит к венозному застою. Следствием этого являются уменьшение сердечного выброса и прогрессирование гемодинамических нарушений.
Лечение эмфиземы средостения обязательно требует мероприятий по устранению ее первопричины (ликвидация клапанного пневмоторакса, ушивание разрыва бронха и пр.). Для уменьшения компрессии средостения производят разрез длиной 4—5 см над рукояткой грудины; таким путем вскрывают клетчатку средостения впереди трахеи и вводят в нее дренажи. Кожу вокруг дренажей сшивают, дренажи подключают к вакуумному аппарату.
Гемоторакс
Скопление крови в полости плевры наблюдается почти при каждой травме груди. Источником кровотечения чаще всего бывают межреберные - сосуды, сосуды легких, реже сердцами средостения. Объем гемоторакса варьирует в широких пределах — от нескольких миллиметров до нескольких литров. Небольшое количество крови (менее 150—200 мл) не удается диагностировать ни клиническими, ни рентгенологическими методами.
Излившаяся в плевральную полость кровь обычно свертывается, а затем вследствие фибринолиза вновь становится жидкой. Однако при большом гемотораксе часто образуются сгустки (свернувшийся гемоторакс), которые препятствуют расправлению легкого и могут нагнаиваться. Патологическое влияние гемоторакса двоякое: кровопотеря как таковая и сдавленис органов груди. В зависимости от объема кровопотери в той или иной мере выражена гиповолемия, которая всегда усугубляет дыхательные и циркуляторные расстройства. Это следует обязательно учитывать при составлении плана лечебных мероприятий. Быстрое на-растанисгемоторакса и повторное появление крови после ее аспирации всегда свидетельствуют о продолжающемся кровотечении н могут служить показанием к торакотомии.
Массивный гемоторакс приводит к коллапсу легкого и смешению средостения. Как и пневмоторакс, это обусловливает выраженные нарушения дыхания и работы сердца. Гемопневмоторакс представляет собой синдром сочетанного повреждения воздухоносных и кровеносных путей. Его роль в патогенезе травмы груди такая же, как и каждого из его компонентов в отдельности.
Лечебная тактика при гемотораксе сводится к возможно более раннему удалению излившейся крови, так как это является самым надежным средством профилактики нагноения. В ранние сроки после травмы целесообразно аспирнрованную кровь влить больному, соблюдая при этом правила реинфузии аутокрови. Некоторую помощь в диагностике инфицированного гемоторакса могут оказать пробы Петрова и Эфсндиева.
Проба Петрова. Пунктат из плевральной полости разбавляют ведой. Если кровь не инфицирована, она гемолизируется и жидкость остается прозрачной. При наличии инфекции жидкость мутная.
Проба Эфендцева. Пуиктат из плевральной полости центрифугируют или отстаивают. Образуются два слоя: верхний — плазма, нижний — форменные элементы. При отсутствии инфекции их соотношение равно 1:1, в инфицированной крови объем осадка уменьшается.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Пороки развития легких
Пороки развития легких – грубые изменения нормальной анатомической структуры легких, возникающие на этапе эмбриональной закладки и развития бронхолегочной системы и вызывающие нарушение или потерю ее функций. Пороки развития легких могут проявиться в детстве или взрослом возрасте, сопровождаясь цианозом, одышкой, кашлем с выделением гнойной мокроты, кровохарканьем, деформацией грудной клетки и др. С целью диагностики пороков развития легких выполняется рентгенография, КТ, бронхоскопия и бронхография, АПГ. Лечение пороков развития легких может быть хирургическим (резекция легкого, пульмонэктомия) или консервативным (медикаменты, ФТЛ, массаж, санация бронхиального дерева).
МКБ-10
Общие сведения
Пороки развития легких – врожденные анатомические аномалии и дефекты функционирования легких, бронхов и легочных сосудов. Частота выявления пороков развития легких у детей варьирует от 10 до 20%. Среди врожденных дефектов легких и бронхов встречаются аномалии их развития, которые, в отличие от пороков, не проявляются клинически и не влияют на функцию измененного органа (например, аномалии деления крупных и средних бронхов). Пороки развития легких, сопровождающиеся дыхательной недостаточностью, проявляются уже в раннем детском возрасте и сопровождаются задержкой в физическом развитии ребенка.
На фоне пороков развития легких нередко развиваются воспалительные и нагноительные процессы, вызывающие клинику острых или хронических неспецифических заболеваний, которые могут принимать очень тяжелое течение. Более половины хронических неспецифических заболеваний легких патогенетически связаны с имеющимися пороками развития легких.
Причины
Формирование аномалий и пороков развития легких в пренатальном периоде может происходить под влиянием ряда экзогенных и эндогенных тератогенных (повреждающих плод) факторов. К экзогенным факторам, оказывающим тератогенное воздействие на эмбрион, относятся физические (механическая или термическая травма, электромагнитное или радиоактивное излучение), химические (любые яды), биологические (вирусные или иные инфекции, бактериальные токсины) повреждающие механизмы.
К числу эндогенных тератогенных факторов принадлежат наследственность, аномалии генов и хромосом, эндокринные патологии, биологически неполноценные половые клетки (при поздней беременности у женщин или пожилом возрасте у мужчин). Вид развивающегося порока легкого зависит не столько от характера тератогенного фактора, сколько от срока беременности, на котором организм женщины испытывает его воздействие.
Если воздействие тератогенного фактора приходится на первые 3-4 недели беременности, когда происходит закладка трахеи и главных бронхов, возможно развитие пороков эти структур вплоть до нарушения формирования целого легкого. Тератогенное воздействие на эмбрион в период с 6 по 10 недели беременности может вызвать пороки формирования сегментарных и субсегментарных бронхов по типу кистозной или простой гипоплазии, а также развитие врожденных бронхоэктазов. Поздние пороки развития легких у плода могут сформироваться на 6-8 месяце беременности, когда закладывается альвеолярная ткань.
Классификация
По степени недоразвития легкого или его отдельных анатомических, тканевых, структурных элементов в пульмонологии различают:
- Агенезию – порок развития, характеризующийся полным отсутствием легкого и соответствующего ему главного бронха.
- Аплазию – порок развития, при котором отсутствует легкое или его часть при наличии культи рудиментарного главного бронха.
- Гипоплазию – одновременное недоразвитие элементов легкого (бронхов, легочной паренхимы, сосудов), встречающееся на уровне сегмента, доли или всего легкого. Простая гипоплазия характеризуется равномерным уменьшением размеров легкого без существенного нарушения его структуры с сохранением отчетливой редукции бронхиального дерева. Кистозная гипоплазия (кистозное или сотовое легкое, поликистоз) встречается среди всех пороков развития легкого наиболее часто (в 60-80% случаев) и сопровождается одновременным недоразвитием бронхов, легочной паренхимы и сосудов с формированием бронхогенных полостей в дистальных отделах субсегментарных бронхов, где обычно развивается хронический воспалительно-нагноительный процесс.
Среди пороков развития стенок трахеи и бронхов выделяют:
- Трахеоброхомегалию (трахеоцеле, мегатрахея, синдром Мунье-Куна) – расширение просвета трахеи и крупных бронхов вследствие врожденного недоразвития мышечных и эластических волокон их стенок. Наличие трахеобронхомегалии сопровождается упорным течением трахеобронхита.
- Трахеобронхомаляцию – несостоятельность хрящей трахеи и бронхов, вызывающую их аномальное спадание в процессе дыхания. Проявляется стридорозным дыханием, грубым кашлем, приступами апноэ.
- Синдром Вильямса-Кемпбелла – гипоплазия хрящей и эластических тканей бронхов III -VI-го порядков, проявляющаяся генерализованным развитием бронхоэктазов на уровне средних бронхов и бронхообструктивным синдромом.
- Бронхиолоэктатическую эмфизему Лешке – врожденную слабость стенок бронхиол, сопровождающуюся бронхиолоэктазиями и центрилобулярной эмфиземой.
Ограниченные (локализованные) дефекты строения стенок бронхов и трахеи включают:
К врожденным порокам развития легких, связанным с наличием добавочных (избыточных) дизэмбриогенетических структур, относят:
Среди пороков развития легких, характеризующихся аномальным расположением анатомических структур, наиболее часто встречаются:
- Синдром Картагенера – обратное расположение внутренних органов, в т. ч. и легких. Обычно сочетается с хроническим бронхитом, бронхоэктазами и хроническим синуситом, протекает с частыми обострениями гнойного бронхолегочного процесса. Возможны видоизменения концевых фаланг и ногтей по типу «часовых стекол», «барабанных палочек».
- Трахеальный бронх – наличие аномального бронха, отходящего от трахеи выше верхнедолевого бронха.
- Доля непарной вены – часть верхней доли правого легкого, отделенная непарной веной.
К наиболее распространенным порокам развития кровеносных сосудов легких относятся:
Симптомы пороков развития легких
Многообразию видов пороков развития легких соответствует полиморфность их возможных клинических проявлений. Скрытое течение многих пороков легких обусловливает вариабельность сроков их выявления. В первое десятилетие жизни обнаруживается 3,8% всех встречающихся пороков развития легких, во второе десятилетие - 18,2%, в третье - 26,6%, в четвертое - 37,9%, у лиц после 40 лет -14%.
Бессимптомное течение пороков развития легких встречается у 21,7% пациентов, симптомами нагноения проявляется 74,1% пороков, осложнениями других заболеваний - 4,2%.
Наиболее рано, в первые дни жизни ребенка, проявляются пороки развития легких, сопровождающиеся признаками дыхательной недостаточности: лобарная эмфизема, выраженный стеноз главных бронхов и трахеи, бронхо- и трахеопищеводные свищи, агенезия, аплазия и выраженная гипоплазия легкого. Они характеризуются стридорозным дыханием, приступами асфиксии, цианозом.
Кисты легкого, легочная секвестрация, гипоплазия легкого, бронхоэктазы могут впервые проявить себя развитием острого воспалительного процесса и нагноения. Характер воспалительных процессов при пороках развития легких носит затяжное рецидивирующее течение и сопровождается кашлем с выделением значительного количества гнойной мокроты, эпизодами кровохарканья, интоксикацией, нарушением самочувствия в периоды обострений. Тяжелые пороки развития легких вызывают отставание физического развития детей, асимметрию и деформацию грудной клетки.
Диагностика пороков развития легких
Диагностирование пороков развития легких требует комплексного специализированного обследования. Заподозрить пороки развития легких следует у пациентов, с детства страдающих стойкими хроническими бронхолегочными процессами. Решающее значение в диагностике пороков легких занимают рентгенологическое и бронхологическое исследования.
Рентгенологическое исследование позволяет выявить пороки развития легких даже при их бессимптомном течении. По данным рентгенографии и КТ легких можно определить изменения сосудистого и бронхиального рисунка (при гипоплазии), повышение прозрачности (при лобарной эмфиземе), смещение органов средостения (при гипоплазии или агенезии), контуры теней (при гамартоме или секвествации), обратную топографию легких (при синдроме Картагенера) и др. При бронхоскопии и бронхографии проводится оценка анатомического строения трахеи и бронхов, выявляются деформации (стеноз, свищи и др.) и изменения бронхиального дерева. При пороках развития сосудов легкого целесообразно проведение ангиопульмонографии.
Лечение пороков развития легких
Выбор адекватной тактики лечения пороков развития легких осуществляется пульмонологоми и торакальными хирургами. Он диктуется оценкой состояния пациента, степенью выраженности имеющихся нарушений и возможным прогнозом. Неотложная операция показана при выраженной дыхательной недостаточности в случаях лобарной эмфиземы, аплазии и агенезии легких, при трахеопищеводном свище и стенозах трахеи и бронхов.
При бронхоэктазах и кистозной гипоплазии выбор хирургического или консервативного лечения определяется количеством измененных сегментов в обоих легких, частотой рецидивов и характером изменений легочной ткани. Как правило, при таких пороках развития легких проводят резекцию измененного участка легкого.
При распространенных изменениях в легких проводится консервативная терапия, направленная на предупреждение обострений гнойного процесса. Она включает в себя ежегодные курсы противовоспалительной терапии, улучшение дренажа бронхиального дерева (бронхоальвеолярный лаваж, отхаркивающие, муколитические препараты, массаж, ингаляции, ЛФК), санаторно-курортную реабилитации.
Прогноз и профилактика пороков развития легких
При пороках развития легких, не связанных с развитием дыхательной недостаточности и не сопровождающихся гнойно-воспалительными осложнениями, прогноз удовлетворительный. Частые обострения бронхолегочного процесса могут вызывать ограничение трудоспособности пациентов. Меры профилактики врожденных пороков развития легких включают: исключение неблагоприятных тератогенных воздействий на протяжении беременности, медико-генетическое консультирование и обследование пар, планирующих рождение ребенка.
1. Пороки развития, наследственные и интерстициальные болезни легких у детей: учеб.-метод. пособие/ Самаль Т. Н. – 2014.
2. Клинико-эпидемиологические особенности врожденных кистозно-аденоматозных пороков развития легких в Нижегородской области/ Галягина Н.А., Халецкая О.В., Удалова О.В., Царева Л.А.// Медицинский альманах. – 2013 - №3 (30).
3. Пороки развития и наследственные заболевания легких/ Бородулина Е.А., Суворова Г.Н., Бородулин Б.Е. – 2016.
4. Врожденные заболевания легких плода (течение беременности, диагностика и исходы): Автореферат диссертации/ Кохно Н. И. – 2005.
Эмфизема легких
Эмфизема легких – это хроническое неспецифическое заболевание легких, в основе которого лежит стойкое, необратимое расширение воздухоносных пространств и повышенное вздутие легочной ткани дистальнее концевых бронхиол. Эмфизема легких проявляется экспираторной одышкой, кашлем с небольшим количеством слизистой мокроты, признаками дыхательной недостаточности, рецидивирующими спонтанными пневмотораксами. Диагностика патологии проводится с учетом данных аускультации, рентгенографии и КТ легких, спирографии, анализа газового состава крови. Консервативное лечение эмфиземы легких включает прием бронхолитиков, глюкокортикоидов, кислородотерапию; в некоторых случаях показано резекционное хирургические вмешательство.
Эмфизема легких (от греч. emphysema - вздутие) – патологическое изменение легочной ткани, характеризующееся ее повышенной воздушностью, вследствие расширения альвеол и деструкции альвеолярных стенок. Эмфизема легких выявляется у 4% пациентов, причем у мужчин встречается в 2 раза чаще, чем у женщин. Риск развития эмфиземы легких выше у пациентов с хроническими обструктивными заболеваниями легких, особенно после 60 лет. Клиническая и социальная значимость эмфиземы легких в практической пульмонологии определяется высоким процентом развития сердечно-легочных осложнений, нетрудоспособности, инвалидизации больных и возрастающей летальностью.
Любые причины, приводящие к хроническому воспалению альвеол, стимулируют развитие эмфизематозных изменений. Вероятность развития эмфиземы легких повышается при наличии следующих факторов:
- врожденной недостаточности α-1 антитрипсина, приводящей к разрушению протеолитическими ферментами альвеолярной ткани легких;
- вдыхании табачного дыма, токсичных веществ и полютантов;
- нарушениях микроциркуляции в тканях легких;
- бронхиальной астме и хронических обструктивных заболеваниях легких;
- воспалительные процессы в респираторных бронхах и альвеолах;
- особенностей профессиональной деятельности, связанных с постоянным повышением давления воздуха в бронхах и альвеолярной ткани.
Патогенез
Под воздействием данных факторов происходит повреждение эластической ткани легких, снижение и утрата ее способности к воздухонаполнению и спадению. Переполненные воздухом легкие приводят к слипанию мелких бронхов при выдохе и нарушениям легочной вентиляции по обструктивному типу. Формирование клапанного механизма при эмфиземе легких вызывает вздутие и перерастяжение тканей легкого и формирование воздушных кист – булл. Разрывы булл могут вызывать эпизоды рецидивирующего спонтанного пневмоторакса.
Эмфизема легких сопровождается значительным увеличением легких в размерах, которые макроскопически становятся похожими на крупнопористую губку. При исследовании эмфизематозной легочной ткани под микроскопом наблюдается деструкция альвеолярных перегородок.
Эмфизема легких подразделяется на первичную или врожденную, развивающуюся как самостоятельная патология, и вторичную, возникшую на фоне других заболеваний легких (чаще бронхита с обструктивным синдромом). По степени распространенности в легочной ткани выделяют локализованную и диффузную формы эмфиземы легких.
По степени вовлечения в патологический процесс ацинуса (структурно-функциональной единицы легких, обеспечивающей газообмен, и состоящей из разветвления терминальной бронхиолы с альвеолярными ходами, альвеолярными мешками и альвеолами) различают следующие виды эмфиземы легких:
- панлобулярную (панацинарную) - с поражением целого ацинуса;
- центрилобулярную (центриацинарную) – с поражением респираторных альвеол в центральной части ацинуса;
- перилобулярную (периацинарную) – с поражением дистальной части ацинуса;
- околорубцовую (иррегулярную или неравномерную);
- буллезную (буллезную болезнь легких при наличии воздушных кист - булл).
Особо выделяют врожденную долевую (лобарную) эмфизему легких и синдром Маклеода – эмфизему с неясной этиологией, поражающую одно легкое.
Симптомы эмфиземы легких
Ведущим симптомом эмфиземы легких является экспираторная одышка с затрудненным выдохом воздуха. Одышка носит прогрессирующий характер, возникая сначала при нагрузке, а затем и в спокойном состоянии, и зависит от степени дыхательной недостаточности. Пациенты с эмфиземой легких делают выдох через сомкнутые губы, одновременно надувая щеки (как бы «пыхтят»). Одышке сопутствует кашель с выделение скудной слизистой мокроты. О выраженной степени дыхательной недостаточности свидетельствуют цианоз, одутловатость лица, набухание вен шеи.
Пациенты с эмфиземой легких значительно теряют в весе, имеют кахектичный вид. Потеря массы тела при эмфиземе легких объясняется большими энергозатратами, расходуемыми на интенсивную работу дыхательных мышц. При буллезной форме эмфиземы легких возникают повторные эпизоды спонтанного пневмоторакса.
Осложнения
Прогрессирующее течение эмфиземы легких приводит к развитию необратимых патофизиологических изменений в сердечно-легочной системе. Спадение мелких бронхиол на выдохе приводит к нарушениям легочной вентиляции по обструктивному типу. Деструкция альвеол вызывает уменьшение функциональной легочной поверхности и явления выраженной дыхательной недостаточности.
Редукция сети капилляров в легких влечет за собой развитие легочной гипертензии и возрастание нагрузки на правые отделы сердца. При нарастающей правожелудочковой недостаточности возникают отеки нижних конечностей, асцит, гепатомегалия. Неотложным состоянием при эмфиземе легких является развитие спонтанного пневмоторакса, требующее дренирования плевральной полости и аспирации воздуха.
Диагностика
В анамнезе пациентов с эмфиземой легких отмечаются большой стаж курения, профессиональные вредности, хронические или наследственные заболевания легких. При осмотре пациентов с эмфиземой легких обращает внимание увеличенная, бочкообразная (цилиндрической формы) грудная клетка, расширенные межреберные промежутки и эпигастральный угол (тупой), выпячивание надключичных ямок, поверхностное дыхание с участием вспомогательной дыхательной мускулатуры.
Перкуторно определяется смещение нижних границ легких на 1-2 ребра книзу, коробочный звук по всей поверхности грудной клетки. Аускультативно при эмфиземе легких выслушивается ослабленное везикулярное («ватное») дыхание, глухие сердечные тона. В крови при выраженной дыхательной недостаточности выявляется эритроцитоз и повышение гемоглобина.
- Рентгендиагностика. При рентгенографии легких определяется повышение прозрачности легочных полей, обедненный сосудистый рисунок, ограничение подвижности купола диафрагмы и ее низкое расположение (спереди ниже уровня VI ребра), почти горизонтальное положение ребер, сужение сердечной тени, расширение загрудинного пространства. С помощью КТ легких уточняется наличие и расположение булл при буллезной эмфиземе легких.
- Исследование ФВД. Высокоинформативно при эмфиземе легких исследование функции внешнего дыхания: спирометрия, пикфлоуметрия и др. На ранних этапах развития эмфиземы легких выявляется обструкция дистальных отрезков дыхательных путей. Проведение теста с ингаляторами-бронходилататорами показывает необратимость обструкции, характерную для эмфиземы легких. Также при ФВД определяется снижение ЖЕЛ и пробы Тиффно.
- Лабораторные тесты. Анализ газового состава крови выявляет гипоксемию и гиперкапнию, клинический анализ – полицитемию (увеличение Hb, эритроцитов, вязкости крови). В план обследования необходимо включать анализ на α -1-ингибитор трипсина.
Лечение эмфиземы легких
Консервативная терапия
Специфическое лечение отсутствует. Первостепенным является устранение предрасполагающего к эмфиземе фактора (курения, вдыхания газов, токсических веществ, лечение хронических заболеваний органов дыхания).
Лекарственная терапия при эмфиземе легких симптоматическая. Показано пожизненное применение ингаляционных и таблетированных бронхолитиков (сальбутамола, фенотерола, теофиллина и др.) и глюкокортикоидов (будесонида, преднизолона). При сердечной и дыхательной недостаточности проводят оксигенотерапию, назначают диуретики. В комплекс лечения эмфиземы легких включают дыхательную гимнастику.
Хирургическое лечение
Хирургическое лечение эмфиземы легких заключается в проведении операции по уменьшению объема легких (торакоскопической буллэктомии). Суть метода сводится к резекции периферических участков легочной ткани, что вызывает «декомпрессию» остальной части легкого. Наблюдения за пациентами после перенесенной буллэктомии показывают улучшение функциональных показателей легких. Пациентам с эмфиземой легких показана трансплантация легких.
Прогноз и профилактика
Отсутствие адекватной терапии эмфиземы легких приводит к прогрессированию заболевания, нетрудоспособности и ранней инвалидизации вследствие развития дыхательной и сердечной недостаточности. Несмотря на то, что при эмфиземе легких происходят необратимые процессы, качество жизни пациентов можно повысить постоянно применяя ингаляционные препараты. Оперативное лечение буллезной эмфиземы легких несколько стабилизирует процесс и избавляет пациентов от рецидивирующих спонтанных пневмотораксов.
Существенным моментом профилактики эмфиземы легких является антитабачная пропаганда, направленная на предупреждение и борьбу с курением. Также необходимы раннее выявление и лечение пациентов с хроническим обструктивным бронхитом. Пациенты, страдающие ХОБЛ, подлежат наблюдению пульмонолога.
Секвестрация легкого
Секвестрация легкого – порок формирования легких, заключающийся в обособлении от основного органа рудиментарного участка легочной ткани с автономным кровотоком, не участвующего в процессе газообмена. Клиника при секвестрации легкого может быть скудной; при обострении инфекционного воспаления включает лихорадку, слабость, одышку, кашель со слизисто-гнойной мокротой, кровохарканье; при сдавлении пищевода и желудка - нарушение прохождения пищи. Диагноз основан на данных рентгенографии и КТ легких, бронхографии, бронхоскопии, ангиопульмонографии. При секвестрации легкого лечение только оперативное – секвестрэктомия, сегментэктомия или лобэктомия.
Секвестр легочной ткани не участвует в дыхательной функции, имеет небольшую величину и обычно представлен кистовидным образованием (единичной бронхогенной кистой или скоплением мелких кист). Участок секвестрации не связан с сосудами малого круга кровообращения (легочной артерией), а имеет аномальное кровоснабжение через дополнительные сосуды, идущие от нисходящей дуги грудной или брюшной аорты или ее ветвей (подключичной и селезеночной артерий). Основной венозный отток от порочного участка реализуется через систему верхней полой вены, реже - через легочные вены. Иногда секвестрированная ткань может сообщаться с бронхами пораженного легкого.
Причины секвестрации легкого
Секвестрация легкого является сложным пороком, вызванным комбинированным нарушением формирования различных бронхолегочных структур. Аномалия развивается в результате тератогенных влияний в раннюю внутриутробную фазу. Источником развития легочного секвестра являются добавочные выпячивания первичной кишки, рудименты дивертикула пищевода, отделившиеся от организующихся легких и затем теряющие связь с первичной кишкой и бронхиальным деревом. Иногда может оставаться связь рудимента легкого с пищеводом или желудком с помощью соустья-тяжа (бронхолегочно-кишечная мальформация).
Согласно теории тракции, развитию секвестрации легкого способствует нарушение редукции ветвей первичной аорты с трансформацией их в аномальные сосуды. Через эти сосудистые ветви зачаточные фрагменты легкого отграничиваются от нормальной легочной закладки.
Секвестрация легкого часто комбинируется с другими пороками развития: ЭЛС - с неиммунной водянкой плода, анасаркой, гидротораксом новорожденного; ИЛС – с врожденной аденоматоидной мальформацией легкого 2-го типа, рабдомиоматозной дисплазией, трахео- и бронхопищеводными свищами, воронкообразной деформацией грудной клетки, открытым средостением, диафрагмальной грыжей, гипоплазией почки, дефектами позвоночника и тазобедренных суставов.
Различают 2 формы секвестрации легкого: внутридолевую (интралобарную – ИЛС) и внедолевую (экстралобарную – ЭЛС). При интралобарной легочной секвестрации кистозный участок располагается среди функционирующей паренхимы легкого в границах висцерального листка плевры (чаще всего в области медиально-базальных сегментов нижней доли левого легкого) и васкуляризуется одним или несколькими аберрантными сосудами. ИЛС можно рассматривать как врожденную кисту с аномальным кровообращением. Секвестрированные легочные кисты имеют эпителиальную выстилку и жидкое или слизистое содержимое, часто первично не связаны с бронхиальным деревом. В кистозно-измененном участке секвестрации легкого рано или поздно возникает нагноение.
При экстралобарной форме легочный секвестр имеет отдельный плевральный листок и изолирован от основного органа, являясь полностью эктопированной тканью (добавочной легочной долей). ЭЛС чаще наблюдается в левой половине грудной клетки (в 48% случаев), в правой (20%), в переднем (8%) или заднем (6%) средостении, поддиафрагмально (18%), в брюшной полости (10%), интраперикардиально (единичные случаи). ЭЛС обеспечивается кровью исключительно через артерии большого круга кровообращения (грудную или брюшную аорту). Микроскопически ткань ЭЛС включает множество неразвитых одинаковых бронхиол, ацинусов, состоящих из альвеолярных ходов неправильной формы и обычных или расширенных альвеол. В четверти случаев ЭЛС диагностируется пренатально, в 2/3 случаев - в первые 3 месяца жизни ребенка.
Встречаемость внутридолевой секвестрации легкого примерно в 3 раза выше, чем внедолевой, иногда возможно их одновременное присутствие у одного больного. ЭЛС в 3–4 раза чаще выявляется у мальчиков, чем у девочек.
По клиническим критериям выделяют 3 формы секвестрации легкого:
Симптомы секвестрации легкого
Клиническая картина секвестрации легкого определяется локализацией секвестра, наличием или отсутствием его связи с дыхательными путями, степенью развития гипоплазии легочной ткани и воспалительных изменений. Симптомы интралобарной секвестрации легкого редко проявляются на этапе новорожденности и раннего детства, развиваясь обычно в более старшем возрасте при инфицировании, воспалении, нагноении и прорыве кистозного секвестра.
При нагноении кисты и абсцессе порочной доли легкого заболевание начинается остро с лихорадки, слабости, потливости, умеренного болевого синдрома, одышки при нагрузке, непродуктивного кашля, а при прорыве гнойника - с выделения значительного объема гнойной мокроты. Иногда возможно кровохарканье и легочные кровотечения, часты плевральные осложнения. Течение секвестрации легкого обычно приобретает хронический характер с повторяющимися вялыми обострениями и ремиссиям. При ИЛС может иметь место клиника рецидивирующей пневмонии.
Экстралобарная секвестрация легкого часто протекает асимптомно и начинает беспокоить больного только в подростковом и более позднем возрасте. Внедолевые секвестры могут провоцировать сдавление пищевода, желудка и других органов, что может проявляться одышкой, цианозом, нарушением эвакуации пищи. Риск инфекционного процесса крайне низок.
Секвестрация легкого может осложниться пневмомикозом, туберкулезом, профузным легочным кровотечением и массивным гемотораксом, формированием опухоли, развитием острой сердечной недостаточности по причине объемной перегрузки сердца за счет артериовенозного шунтирования в секвестрированной кисте.
Ранняя диагностика секвестрации легкого затруднена из-за схожести ее клинико-рентгенологических симптомов с таковыми при другой легочной патологии. Диагноз устанавливают по совокупности данных обзорной рентгенографии и КТ легких, бронхографии, бронхоскопии, УЗИ брюшной полости, аортографии, ангиопульмонографии.
Рентгенологически интралобарная секвестрация легких (в отсутствии связи с бронхом и воспаления) определяется как затенение неправильной формы разной степени интенсивности с просветлением в толще или как полостное образование с горизонтальным уровнем жидкости или без него. При обострении вокруг секвестра в нижней доле легкого отмечается выраженная деформация сосудисто-бронхиального рисунка, умеренная перифокальная инфильтрация легочной ткани. При бронхографии наблюдается деформация и смещение бронхов, соседних с пораженным сегментом легкого. Бронхоскопическая картина секвестрации легкого, сообщающейся с дыхательными путями, соответствует катарально-гнойному эндобронхиту на стороне пораженного легкого.
Брюшнополостная ЭЛС выявляется на УЗИ как четко отграниченное образование однородной эхогенности с кровоснабжением через ветви крупных артерий. Диагноз окончательно подтверждается МСКТ легких и ангиопульмонографией с установлением наличия, количества и топографии аномальных сосудов, питающих область секвестрации. Радиоизотопное сканирование печени и перитонеография помогают отграничить правостороннюю секвестрацию легких от патологии органов ЖКТ. Секвестрация легкого нередко выявляется в ходе хирургического вмешательства по поводу хронического гнойного процесса в легком. Дифференциальный диагноз при секвестрации легкого проводится с деструктивной пневмонией, туберкулезным процессом, кистой или абсцессом легкого, бронхоэктазами, опухолью грудной полости.
Лечение секвестрации легкого
При секвестрации легких требуется проведение оперативного вмешательства – удаление аномального участка легочной ткани. При выявлении бессимптомной внутридолевой секвестрации легких возможно выполнение сегментэктомии, однако чаще всего требуется удаление всей пораженной легочной доли (обычно нижней) – лобэктомия. Тактика хирургического лечения внедолевой формы заключается в удалении секвестрированного участка (секвестрэктомии). Наличие при секвестрации легких аномальных крупных артериальных сосудов нетипичной локализации делает важным тщательную предварительную диагностику во избежание их интраоперационного повреждения и развития тяжелого угрожающего жизни кровотечения.
Прогноз при интралобарной форме в отсутствие гнойно-септических процессов – удовлетворительный, при экстралобарной секвестрации легкого брюшнополостной локализации, как правило, лучше, чем при ее внутригрудном расположении.
1. Секвестрация легкого как интраоперационная находка/ Зеленский И.В., Оспанов М.А., Кали Д.Е., Аманжолов Е.У., Баширов М.Ш.// Вестник Казахстана – 2014 - №4.
2. Внутридолевая секвестрация легкого. Клиническое наблюдение/ Ворончихин В. В., Волкова Н. В., Санников О. Р.// Актуальные вопросы эндоскопии. – 2015.
3. Внелегочная секвестрация легкого/ Дубова Е.А., Павлов К.А., Кучеров Ю.И., Жиркова Ю.В., Кулабухова Е.А., Щёголев А.И.// Российский вестник детской хирургии, анестезиологии и реаниматологии. – 2011.
4. Случай диагностики и лечения внутрилегочной секвестрации у женщины 34 лет/ Шулутко А.М. , Ясногородский О.О. , Талдыкин М.В., Качикин А.С. , Гандыбина Е.Г. , Винарская В.А., Мороз Н.Г., Катанэ Ю.А.К.// Русский медицинский журнал. – 2014.
Секвестрация легких. Эмфизема легких
Секвестрированный участок может располагаться внутри доли легкого (внутридолевая секвестрация) или вне основной части легкого, с которым он связан посредством фиброзной перемычки. Во втором случае говорят о добавочной доле, или внелегочной секвестрации. Данный порок обычно локализуется в заднемедиальном отделе нижних долей, чаще слева.
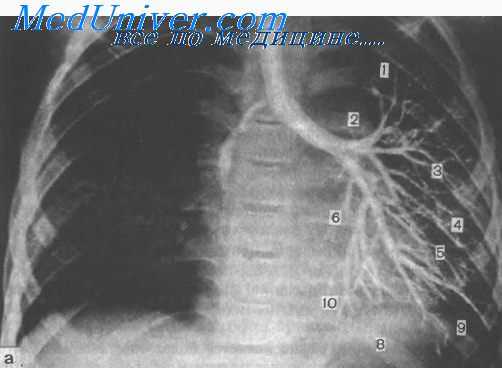
Клиническое течение порока различно и зависит от осложняющих его процессов, чаще всего инфицирования. Более типичны рентгенологические данные. В заднемедиальных отделах верхней доли выявляется округлое иегомогеиное затемнение, на фоне которого можно видеть одну или несколько кистозиых полостей. При бронхографии контрастное вещество обычно не проникает в этот участок. Достоверный дооперационный диагноз секвестрации может быть установлен при аортографии, когда выделяется тень аберрантного сосуда, отходящего от аорты.
Лечение состоит в удалении пораженной части легкого.
Эмфизема легких
Врожденная эмфизема обычно поражает долю легкого» поэтому ее называют лобарной. Известны и другие синонимы: обструктивная, гипертрофическая, гигантская эмфизема, сверхпрозрачнос легкое. В основе заболевания лежит дефект развития хрящевых колец долевого или сегментарного бронха. Возможны перегиб бронха, сдапление его сосудом, гипертрофия слизистой оболочки. Возникающий при этом вентильный механизм приводит к резкому вздутию паренхимы легкого, что и определяет клинико-рентгенологическую картину порока.
Клиническая картина порока может проявиться сразу после рождения или в первые недели жизни новорожденного. Она характеризуется одышкой, сухим кашлем, приступами асфиксии при кормлении. Присоединяющаяся пневмония усугубляет тяжесть клинической картины и может привести к летальному исходу.
Острое вздутие паренхимы вызывает коллапс прилежащих отделов легкого н смешение органов средостения. В этой стадии процесса возможны диагностические ошибки. Повышенную прозрачность легкого принимают за напряженный пневмоторакс или напряженную солитар-ную кисту. Дифференцируют эти состояния главным образом рентгенологически. Некоторую помошь в дифференциальном диагнозе может оказать бронхологическое исследование. Однако при наличии „синдрома напряжения" это исследование опасно, так как введение в бронхи контрастной массы может усугубить дыхательную недостаточность.
Хронически текущая врожденная эмфизема имеет другую клиническую картину. Вздутый участок легкого, достигая определенного объема, не имеет тенденции к дальнейшему увеличению. Наступает адаптация к возникшим условиям вентиляции и гемодинамики и малом круге кровообращения. В покое одышка исчезает. Она возникает только при напряжении или не беспокоит вообще. При осмотре обращают на себя внимание некоторое выбухание грудной клетки на стороне порока и отставание ее при дыхании. Аускультативно над эмфизематозной частью легкого дыхание значительно ослаблено.
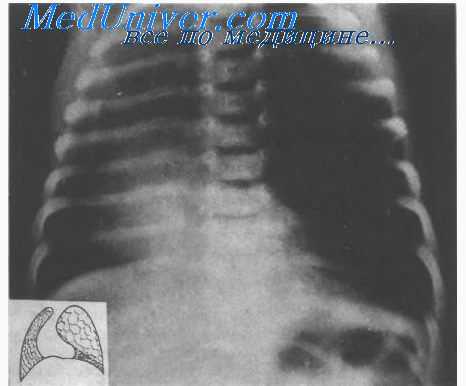
Рентгенологическая картина достаточно типична. На прямой рентгенограмме определяется повышенная прозрачность пораженной части легкого. Органы средостения смещены в здоровую сторону в большей пли меньшей степени, в зависимости от вздутия паренхимы. Легочный рисунок н области эмфиземы обеднен или отсутствует, в коллабированных отделах, наоборот, усилен. Бронхологическое исследование и контрастирование сосудов легких позволяют установить точный диагноз н определить степень нарушения функции пораженного легкого.
В большинстве случаев при врожденной эмфиземе показано оперативное лечение. При „синдроме напряжения" оно является экстренным. В стадии стабилизации процесса показания к операции зависят от степени сдавления прилежащих отделов легкого н средостения. В раннем возрасте не следует торопиться с вмешательством при отсутствии при знаков дыхательной недостаточности. Возможно самоизлечение за счет постепенной нормализации хрящевого каркаса бронхов. С другой стороны, известны рецидивы процесса после операции.
Эти обстоятельства заставляют сдержанно относиться к операции у больных с отсутствием клинических симптомов порока. Во всех остальных случаях резекция пораженного отдела легкого является единственно радикальным вмешательством.
Читайте также:
