Шваннома симпатического ствола - лучевая диагностика
Добавил пользователь Morpheus Обновлено: 29.01.2026
(Акустическая неврома; акустическая невринома; опухоль VIII нерва)
, MD, Columbia University Medical Center and New York Presbyterian Hospital
Вестибулярные шванномы происходят из вестибулярной порции VIII пары черепных нервов и на ее долю приходится около 7% всех внутричерепных опухолей. Акустическая невринома происходит из вестибулярной порции 8 пары черепных нервов и по мере роста сдавливает 7 и 8 пары черепных нервов в области мостомозжечкового угла. По мере роста происходит сдавление мозжечка, спинного мозга, близлежащих черепных нервов (5, 9 и 12 пары).
Двусторонняя вестибулярная шваннома характерна для нейрофиброматоза Нейрофиброматоз Нейрофиброматоз - это группа заболеваний, которые имеют однотипные клинические проявления, но, как предполагают в настоящее время, вызваны различными генетическими причинами. Это заболевание. Прочитайте дополнительные сведенияСимптомы и признаки невриномы слухового нерва
Основным симптомом вестибулярной шванномы является медленно прогрессирующая односторонняя нейросенсорная тугоухость ПатофизиологияДиагностика невриномы слухового нерва
При асимметричной тугоухости МРТ с контрастированием гадолинием
Наиболее часто аудиограмма Обследование Во всем мире около полумиллиарда человек (почти 8% мирового населения) страдают от потери слуха ( 1). У более 10% жителей США отмечается тугоухость определенной степени, которая создает им проблемы. Прочитайте дополнительные сведенияДругие данные включают в себя наличие затухания акустического рефлекса при тимпанометрии. Тестирование ответа ствола мозга на слуховые раздражители позволяет выявить отсутствие сигнала и/или увеличение задержки 5-й волны. Хотя при стандартном обследовании по поводу асимметричной нейросенсорной тугоухости калорическую пробу обычно проводить не требуется, ее результаты показывают выраженную вестибулярную гипоактивность (парез канала) на пораженной стороне.
Лечение невриномы слухового нерва
В отобранных случаях хирургическое удаление или стереотаксическая лучевая терапия
Мелкие бессимптомные (т.е. обнаруженные случайно) и не растущие вестибулярные шванномы лечения не требуют; за такими опухолями можно проводить динамическое наблюдение с помощью МРТ и лечить в случае, если они начинают расти или вызывают симптомы. Выбор между стереотаксической лучевой терапией (например, гамма-нож или кибернож радиотерапия) и консервативной микрохирургией зависит от многих факторов, включая степень снижения слуха, размер опухоли, возраст и общее состояние больного. Стереотаксическую лучевую терапию применяют у более молодых пациентов, при небольших размерах опухоли либо при наличии противопоказаний к операционному вмешательству. Микрохирургия может проводиться через подход, сохраняющий слух (подход через среднюю черепную ямку или ретросигмоидальный подход) или, если слух полностью утерян, то используют транслабиринтный микрохирургический подход.
Основные положения
Обычно, вестибулярная шваннома односторонняя, однако при фиброматозе 2 типа может быть билатеральной.
Часто развивается односторонняя тугоухость, иногда с шумом в ушах и головокружением.
При больших размерах опухоли или тяжелом течении заболевания используют стереотаксическую радиохирургию или микрохирургию.
На серийных МРТ-снимках могут выявляться небольшие асимптоматические или нерастущие опухоли.
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Шваннома симпатического ствола - лучевая диагностика
Телефон регистратуры поликлиники:
Телефон регистратуры лучевой диагностики:
Гамма-нож
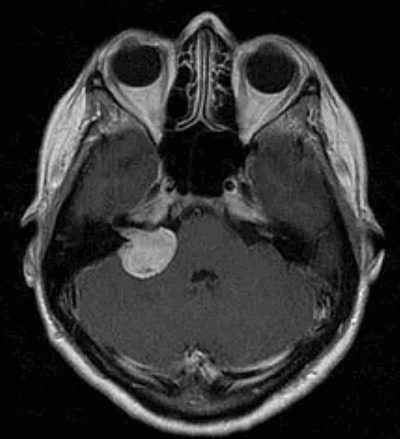 |
Вестибулярная шваннома (невринома VIII нерва, акустическая невринома) представляет собой доброкачественное новообразование, возникающее из шванновских клеток вестибулярной порции VIII нерва.
Заболеваемость невриномами слухового нерва составляет примерно 1 случай на 100000 населения в год. Каждый год в Российской Федерации появляется 1500 новых случаев неврином слухового нерва. Среди первичных интракраниальных опухолей вестибулярные шванномы вестибулярные шванномы занимают 4-е место (после глиом, менингиом и аденом гипофиза), составляя до 6-10% всех верифицированных опухолей мозга и поражая преимущественно лиц работоспособного возраста (30-60 лет), на который приходится более 80% случаев. Вестибулярные шванномы составляют около 30% опухолей задней черепной ямки и до 90% новообразований мосто-мозжечкового угла. Несколько чаще встречаются у женщин, чем у мужчин, примерное соотношение 3:2.
Клиническая картина зависит от размеров опухоли. При небольших размерах симптоматики может не быть вовсе. По мере увеличения опухоли в размерах появляется симптоматика, зависящая от того, какие структуры сдавливает опухоль:
- Поражения нервов.
- Нарушение слуховой и вестибулярной функции.
- Расстройства функции вкуса на передней 2/3 языка и слюноотделения (XIII нерв).
- Расстройства функций каудальной группы нервов.
- Расстройства функции мимической мускулатуры.
- Глазодвигательные нарушения.
- Симптомы раздражении/компрессии ствола головного мозга.
- Различные виды нистагма.
- Пирамидная симптоматика.
- Мозжечковая симптоматика.
- Гипертензионно-дислокационный синдром.
Диагностика
Наиболее информативным методом выявления вестибулярных шванном является МРТ головного мозга с контрастным усилением в режиме Т1 и Т2. Это исследование позволяет определить размеры опухоли, наличие перитуморозного отека, наличие признаков окклюзионной гидроцефалии, которая может быть следствием сдавления опухолью IV желудочка. Кроме этого МРТ позволяет провести дифференциальную диагностику с другими опухолями схожей локализации (чаще с менингиомой задней грани пирамиды височной кости). Еще одним стандартом диагностики является КТ в костном режиме. Независимо от снижения слуха стандартом является проведение аппаратной аудиографии.
Классификация KOOS
I стадия: опухоль находится в пределах внутреннего слухового прохода, диаметр экстраканальной части составляет 1-10 мм.
II стадия: опухоль вызывает расширение канала внутреннего слухового прохода, и выходит в мостомозжечковый угол, ее диаметр составляет, 11-20 мм.
III стадия: опухоль распространяется до ствола головного мозга без его компрессии, диаметр составляет 21 - 30 мм.
IV стадия: опухоль вызывает компрессию ствола головного мозга, ее диаметр более 30 мм.
Классификация M. Samii
Т1 – интрамеатальная опухоль.
Т2 – интра-экстрамеатальная опухоль.
Т3а – опухоль заполняет мостомозжечковую цистерну.
Т3b – опухоль распространяется до ствола головного мозга.
Т4а – опухоль вызывает компрессию ствола.
Т4b – опухоль грубо деформирует ствол мозга и IV желудочек.
Тактика лечения
В зависимости от размеров опухоли, клинической симптоматики, возраста больного, тяжести его состояния, наличия сопутствующей патологии возможны 3 варианта тактики лечения:
- динамическое наблюдение;
- хирургическое лечение;
- стереотаксическая радиохирургия.
Динамическое наблюдение
Учитывая, что вестибулярная шваннома является доброкачественной опухолью с невысокими темпами роста, при небольших ее размерах, отсутствии или минимальном неврологическом дефиците возможен выбор выжидательной тактики. Особенно такой подход оправдан у пожилых людей, или у пациентов с выраженной декомпенсированной соматической патологией. Однако, в большинстве случаев, учитывая риски, связанные с возможным ростом опухоли, более оправданным считается выбор активной тактики.
Хирургическое лечение
Наличие у пациента вестибулярной шванномы является показанием к хирургическому лечению. Большие и гигантские размеры опухоли (более 3,5 см.) являются абсолютным показанием к хирургическому лечению. При меньших размерах возможно проведение радиохирургического лечения.
Для удаления вестибулярных шванном в настоящее время используются три основных доступа: транслабиринтный, ретросигмовидный (наиболее часто используемый) и доступ через среднюю черепную ямку. Каждый из них обладает своими преимуществами и своими же недостатками. В последние годы в связи с развитием микрохирургической техники результаты хирургического лечения пациентов значительно улучшились. Летальность после удаления вестибулярных шванном колеблется в пределах (0-3%), рецидивы опухоли наблюдаются в 5-10%.
В настоящее время превалирующим фактором результативности хирургического лечения считается качество жизни пациента, поэтому интраоперационная тактика в большей степени должна быть нацелена на достижение именно этой цели. Такие послеоперационные осложнения как паралич лицевого нерва (до 25%), нарушения глотания, глазодвигательные нарушения, несут существенную угрозу инвалидизации, поэтому проведение таких операций диктуют высокие требования к профессиональной подготовке оперирующего нейрохирурга. Из послеоперационных осложнений также следует отметить ликворею у 2-20% пациентов, которая иногда может потребовать проведение повторной операции для закрытия ликворного свища; кровоизлияние в ложе операции (1-2%); отек мозжечка и ствола мозга; гемипарез; менингит (1,2%); раневую инфекцию (1,2%); парез VI черепного нерва (1-2%) и парезы других, ниже расположенных черепных нервов; подкожную гематому (3%).
Стереотаксическая радиохирургия
Целью радиохирургического метода является контроль роста опухоли. Стабилизация процесса и даже уменьшение размеров наблюдается в 85-94% случаев, что соответствует мировым данным. Другим критерием эффективности лучевой терапии является высокий (до 98%) показатель отсутствия операции после проведения облучения. Важным также является сохранение функции улиткового и других черепных нервов в случаях, когда это возможно, а также улучшение неврологического статуса пациента. Эффективность применения Гамма-ножа при лечении больных с вестибулярными шванномами создало реальную альтернативу хирургическому лечению при опухолях, размеры которых не превышают 3,5 см, при этом метод радиохирургии лишен недостатков хирургического метода лечения.
После облучения опухоли гамма-ножом возможно как уменьшение ее размеров, так и временное их увеличение. Третьим возможным вариантом развития событий может быть продолженный рост опухоли, однако, это происходит нечасто (от 0 до 7% в течение 10 лет).
Версия для слабовидящих Карта сайта
Кисты и опухоли забрюшинного пространства
Забрюшинные внеорганные опухоли относятся к редкой патологии и составляют 0,2% по отношению ко всем опухолям человека. Забрюшинные опухоли чаще встречаются у женщин. Наибольшее число больных молодого и среднего возраста (21 — 50 лет).
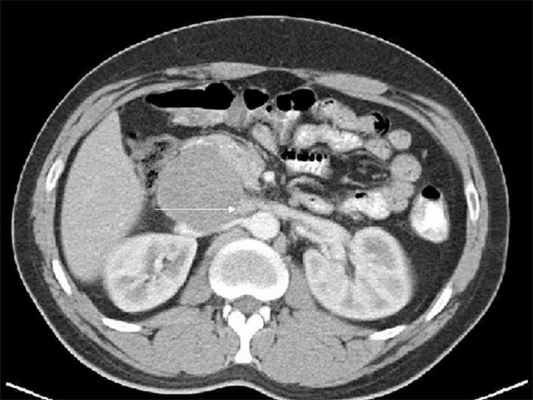
Классификация опухолей забрюшинного пространства.
Наибольшее распространение получила классификация Ассегmann (1954), который называет разделение опухолей данной локализации условным и в основу его кладет гистогенетический принцип:
Опухоли мезодермального происхождения
A. Опухоли из жировой ткани: 1) доброкачественные — липомы, 2) злокачественные — липосаркомы.
B. Опухоли из гладких мышц: 1) доброкачественные — лейомиома, 2) злокачественные — лейомиосаркома.
C. Опухоли из соединительной ткани: 1) доброкачественные-фиброма, 2) злокачественные — фибросаркома.
D. Опухоли из поперечных полосатых мышц: 1) доброкачественные — рабдомиома, 2) злокачественные — рабдомиосаркома.
E. Опухоли из кровеносных сосудов: 1) гемангиома и ангиосаркома, 2) гемангиоперицитома — доброкачественная и злокачественная.
F. Опухоли из лимфатических сосудов: 1) доброкачественные — лимфангиома, 2) злокачественные — лимфангиосаркома.
G. Опухоли из первичной мезенхимы: 1) доброкачественные — миксома, 2) злокачественные — миксосаркома.
H. Опухоли недифференцированные, неясного происхождения — ксантогранулемы.
II. Опухоли нейрогенного происхождения
A. Опухоли из закладок нервных влагалищ: 1) нейрофиброма, без капсулы, 2) инкапсулированная нейролеммома, 3) злокачественная нейролеммома (злокачественная шваннома).
B. Опухоли из тканей симпатической нервной системы: 1) ганглионеврома, 2) симпатобластома, 3) нейробластома.
C. Опухоли из гетеротопных тканей коры надпочечников и хромаффинных тканей: 1) рак из клеток надпочечника, 2) злокачественная нейромаффинная парагангиома, 3) парагангиома, 4) активная феохромоцитома.
III. Опухоли из эмбриональных остатков почки
A. Злокачественные и доброкачественные тератомы.
IV. Злокачественные опухоли метастатического характера
Клиническое течение внеорганных забрюшинных опухолей.
Анатомические особенности забрюшинного пространства с наличием жировой клетчатки обусловливают длительный бессимптомный период. Развиваясь в свободной клетчатке забрюшинного пространства, эти новообразования постепенно могут достигать значительных размеров без каких-либо клинических проявлений, сдавливая прилегающие органы. В одних случаях развиваются расстройства мочеиспускания, в других — явления кишечной непроходимости, поражения нервов в виде стойкой боли в брюшной полости, поясничном отделе, нижних конечностях.
Иногда первыми признаками заболевания является лимфовенозный стаз в одной или обеих нижних конечностях, вторичное варикоцеле.
Общее состояние больных, даже при наличии больших опухолей, остается длительное время удовлетворительным. Быстрая утомляемость, слабость, потеря массы тела, повышения температуры тела, явления интоксикации свидетельствуют о длительном процессе.
Боль в животе является одним из ранних симптомов, наиболее характерна для опухолей небольших размеров, расположенных паравертебрально, в полости малого таза. Боль возникает в случае сдавливания опухолью нервов, которые идут от поясничного или крестцового сплетения, а также при условии растяжения париетального листка брюшины.
Определение опухоли во время пальпации живота является очень ценным клиническим симптомом, который чаще выявляется в случае злокачественных опухолей.
Нарушения венозного и лимфатического оттока клинически проявляются увеличением объема нижней конечности на стороне поражения, болью, расширением подкожных вен передней брюшной стенки. Сдавливание и деформация вен чаще влекут нейрогенные опухоли. Забрюшинные опухоли не сдавливают артериальные стволы, а смещают их.
Расстройство функции пищеварительного тракта проявляются тошнотой, тяжестью в животе, запором; расстройство мочевыделительной системы — дизурией, болью в поясничном отделе (в случае сдавливания и сдвига мочеточников, почки), затруднением во время мочеиспускания. Иногда может наблюдаться олигоурия (если сдавлены оба мочеточника).
Опухоли, которые локализуются в правой половине забрюшинного пространства, дают более раннюю клиническую картину венозного застоя.
В случае локализации опухоли в эпигастральной области (справа или слева), больные чаще жалуются на ощущение тяжести и боль, не связанную с приемом пищи. Симптомы кишечной непроходимости, предопределенные экстраорганным сдавлением, проявляются раньше на фоне новообразований, которые располагаются в нижних отделах левой половины забрюшинного пространства. В случае опухолей этой локализации наблюдается боль, которая иррадиирует в поясничную область, прямую кишку, паховую область и нижние конечности.
Для опухолей тазовой локализации характерно длительное и чаще бессимптомное начало развития заболевания, в связи с чем ранняя диагностика имеет значительные трудности. Неорганные забрюшинные опухоли малого таза не имеют специфических диагностических признаков, которые отличают их от опухолей или неопухолевых заболеваний этой же локализации.
Одним из самых ранних симптомов первичных неорганных опухолей малого таза есть боль внизу живота, которая наблюдается приблизительно в 50% случаев и чаще имеет постоянный характер. Ранними клиническими симптомами являются также нарушения дефекации и мочеиспускания. Отеки и расширения подкожных вен нижних конечностей наблюдаются обычно на фоне злокачественных опухолей.
Иррадиация боли в одну или обе нижние конечности предопределена давлением опухоли на корешки пояснично-крестцового сплетения, что необходимо учитывать во время дифференциальной диагностики неорганных опухолей малого таза и пояснично-крестцового радикулита.
Симптомом, который наблюдается почти у всех больных с первичными неорганными опухолями малого таза, является определение опухоли во время пальпации через прямую кишку или влагалище. Забрюшинные опухоли тазовой локализации могут способствовать возникновению промежностных грыж
Диагностика опухолей
Жалобы и анамнез заболевания, а также осмотр с перкуссией и пальпацией имеют важное значение для того, чтобы заподозрить наличие забрюшинной опухоли.
Диагноз заболевания уточняется после рентгеновского исследования, потому необходимо начинать с обзорной рентгенографии органов грудной и брюшной полостей, что может подтвердить наличие опухоли, но не дает возможности уточнить локализацию и отношение к органам. В связи с этим считают обязательным рентгеноконтрастное исследование органов пищеварительного тракта и мочевыделительной системы. Смещение желудка, толстой или тонкой кишки, почки, мочеточника свидетельствует о забрюшинной локализации опухоли и помогает определить функциональные нарушения этих органов. Особенное место в диагностике забрюшинных новообразований занимает ультрасонография, а также аортография, ангиография, каваграфия, внутривенная экскреторная урография, ирригоскопия, компьютерная томография, ядерномагнитнорезонансная томография, рентгенография грудной полости для исключения метастазов в легких.
На основании прямых и непрямых признаков отмеченные рентгенологические методы исследования позволяют уточнять биологический характер заболевания и расположения опухоли, определить ее взаимоотношение с соседними органами и магистральными сосудами, что необходимо для решения вопроса относительно плана лечения и характера хирургического вмешательства.
Ультразвуковая эхография помогает определить размеры и глубину расположения опухоли, выяснить ее связь с сосудами; компьютерная томография позволяет определить опухоли диаметром начиная с 1,5-2,0 см, точное их распространение, топографию, обнаружить увеличение лимфатических узлов.
К менее распространенным методам относят ангиосканирование опухолей забрюшинного пространства. Однако ни один из перечисленных методов исследования не позволяет определить гистологическую структуру новообразования, что необходимо для выбора метода лечения, особенно лучевого и химиотерапевтического.
В случае забрюшинних неорганных опухолях обязательно выполняют биопсию для цитологического и гистологического исследований. Чрезкожную аспирационную пункционную биопсию осуществляют в случае расположения забрюшинной опухоли на боковых стенках таза. В случае тазового расположения опухоли применяют пункционную биопсию через заднюю стенку влагалища или путем прокола ишиоректального участка. Помогают проводить прицельную биопсию эхография и компьютерная томография.
Пункционная биопсия позволяет уточнить характер процесса и определить морфологическое строение новообразования. Чаще пункционная биопсия является завершающим этапом обследования больного после уточнения локализации, размеров и взаимоотношения опухоли с соседними органами.
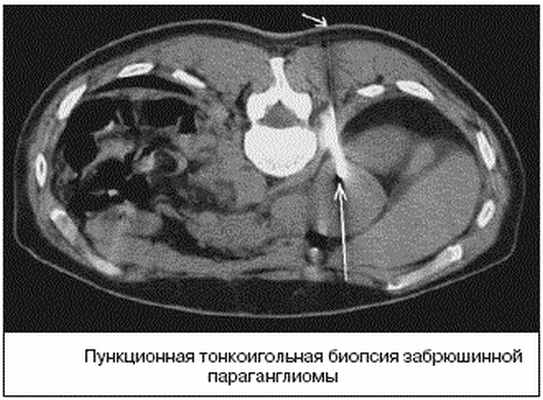
Лечение опухолей забрюшинного пространства
Основным методом лечения является хирургический. Операбельность при неорганных забрюшинных опухолях остается низкой. Операции удается выполнить лишь у 20 — 30% больных. Рецидивы возникают часто — у 35 — 50% оперированных.
Лучевая терапия. Лучевой метод лечения применяют у неоперированных больных в поздних стадиях заболевания результаты лечения малоутешительные. Для применения лучевой и комбинированной терапии необходима уверенность в злокачественной природе опухоли.
В настоящее время показания к лучевой терапии забрюшинных опухолей значительно расширены. Рентгенотерапия фибросарком, оперативное удаление которых было невозможным, значительно продлевает жизнь больным. Предварительная лучевая терапия кажущихся неоперабельными опухолей (типа фибросарком, липосарком, миксосарком) может в некоторых случаях уменьшить их настолько, что они становятся доступными удалению. Это объясняется различной степенью зрелости клеточных элементов упомянутых опухолей, что и является, в сущности, показанием к лучевой терапии. Предварительная лучевая терапия показана у тех больных, у которых по клиническим данным радикальное удаление является сомнительным, а природа злокачественности доказана.
Отдаленные результаты лечения при первичных злокачественных опухолях малоутешительны, 5-летний срок переживают не более 10% перенесших радикальные операции.
При доброкачественных опухолях результаты более стабильные, но возможны рецидивы, требующие повторных операций.
Государственная клиническая больница №29 им. Н.Э.Баумана – это современная многопрофильная высокотехнологичная больница с уникальной полуторавековой историей и традицией, оказывающая высококачественную медицинскую помощь в круглосуточном режиме.
Ганглиоцитома (ганглионеврома)
Ганглиоцитома (ганглионеврома) – доброкачественная опухоль из элементов нервных тканей с участием нервных клеток (ганглиев). Может развиваться в любых отделах головного мозга, но чаще в области дна III желудочка. Встречается достаточно редко.
Ганглиоцитома имеет безкапсульную структуру, размеры опухоли обычно не превышают 4 см. Ганглионевромы, развивающиеся из симпатического ствола, нередко прорастают в заднее средостение или в позвоночный канал. В последнем случае опухоль имеет вид песочных часов, т.е. состоит из двух узлов – паравертебрального (расположенного рядом с позвоночником) и экстрамедуллярного (расположенного в пределах спинномозгового канала).
Лечение
Решение о лечении ганглионевромы (ганглиоцитомы), обнаруженной случайно, без клинических проявлений необходимо принимать крайне взвешенно, оценивая возможные риски. В случае, если наблюдается динамика роста или нарастание симптомов без увеличения опухоли в размерах, пациентам показано радикальное лечение, в качестве которого могут применяться как традиционное нейрохирургическое вмешательство, так и радиохирургия на КиберНоже (предпочтительнее), при которой риск повреждения здоровых тканей практически отсутствует (КибнрНож воздействует дистанционно, без разрезов).
Как проводится лечение на системе КиберНож?

Радиохирургическая система КиберНож
Преимущество КиберНожа состоит в неинвазивности лечения ганглиоцитомы — операция в общепринятом понимании не проводится: нет повреждения ни кожных покровов, ни нарушения целостности мозговых оболочек. Высокая доза ионизирующего излучения, которая приводит к разрушению тканей опухоли либо остановке ее роста, подается точно в область расположения опухоли, оставляя нетронутыми (в пределах безопасных, легко переносимых, доз) здоровые ткани, через которых тонкие пучки излучения проходят на пути в опухоль.
В процессе выбора метода лечения ганглиоцитомы следует помнить, что отсутствие чётких очертаний патологического образования в глубине полушарий мозжечка составляет огромную техническую проблему для нейрохирурга при выполнении традиционной операции. Это значительно повышает риск осложнений во время традиционного нейрохирургического вмешательства и после него.
Тем не менее, каждая ганглионеврома — уникальна, и тактика лечения должна приниматься с учетом всех особенностей конкретного случая. Решение о том, показано ли пациенту с ганглиоцитомой лечение на КиберНоже принимается после проведения междисциплинарного консилиума. На нем также определяется методика сочетанной терапии новообразования, и, соответственно, стоимость лечения ганглиневромы (ганглиоцитомы) у данного пациента.
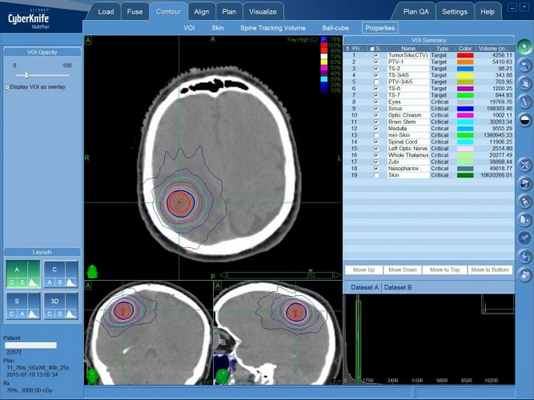
Ганглиоцитома (ганглионеврома) — план лечения на КиберНоже. Красным контуром отмечено пространство, подлежащее облучение разовой высокой дозой ионизирующего излучение, которое остановит биологическую активность опухолевых клеток.
В случае, если размеры опухоли превышают допустимый размер для эффективного лечения методом радиохирургии, может применяться высокоточная лучевая терапия IMRT на современном линейном ускорителе.
Диагностика
Диагностика осложнена тем, что у ганглиоцитом отсутствует характерная симптоматика. Как правило, диагноз устанавливается после гистологического исследования. Иногда опухоль случайно обнаруживают при рентгенологических исследованиях, компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ), хирургических операциях.
Причины
Как и в большинстве случаев возникновения новообразований, точные причины появления ганглиоцитомы не известны. Большинство специалистов в этой сфере утверждают, что появлению этого вида рака способствуют нарушения в период развития симпатической нервной системы. Риск развития ганглиоцитомы возрастает при наличии других патологий, таких как заячья губа, волчья пасть, врожденная базиллярная импрессия. Выделяют ряд причин, которые могут спровоцировать развитие новообразования:
Материалы конгрессов и конференций
Термин «опухоли основания черепа», являясь собирательным, объединяет разнообразные опухолевые процессы, характеризующиеся поражением весьма специфического анатомического образования. Основание черепа представляет собой анатомо-топографический комплекс, состоящий из множества разнородных органов и тканей, вследствие чего опухоли этой локализации вызывают, как правило, комбинированное поражение нескольких анатомических зон, и приводят к развитию выраженной клинической симптоматики.
Анатомическими границами основания черепа считается комплекс костных структур, располагающихся ниже линии, соединяющей место пересечения лобно-носового шва и срединной линии (nasion) с наружным затылочным выступом (inion). При этом необходимо отметить, что существует наружное и внутреннее основания черепа. Учитывая это обстоятельство, мы относим к опухолям основания черепа не только те из них, которые проявляются поражением внутреннего основания, но и опухоли, локализованные в структурах, составляющих наружное основание, таких как клетки решетчатого лабиринта, орбита, подвисочная и крылонебная ямки, шейно-затылочное сочленение.
Определить поражение непосредственно основания черепа клинически невозможно без таких диагностических процедур как компьютерная рентгеновская и магнитно-резонансная томографии. Это связано с тем, что даже небольшие по размерам опухоли с минимальными клиническими проявлениями, нередко имеющие вообще немое течение, могут сразу поражать основание черепа и, наоборот, опухоли с обширным поражением соседних с основанием черепа анатомических образований, имеющие выраженную клиническую симптоматику, могут не распространяться непосредственно на основание, что значительно облегчает технически выполнение хирургического вмешательства и улучшает прогноз жизни. Поэтому рождение такой неординарной нозологической единицы как «опухоли основания черепа» и основные успехи в её лечении связаны именно с появлением этих революционных методик визуализации опухолей.
В чем же клиническая значимость поражения опухолью основания черепа? Как известно, основание черепа выполняет весьма специфическую физиологическую функцию связующего звена мозгового скелета с лицевым и черепа в целом с позвоночным столбом. Несмотря на успехи современной химиолучевой терапии, когда некоторые виды опухолей, например, рак носоглотки, успешно лечатся консервативно, основным методом лечения опухолей основания черепа является хирургический. При определении объема хирургического вмешательства необходимо учитывать то обстоятельство, что в ходе вмешательств на основании черепа по поводу онкологических заболеваний возникают слишком обширные комбинированные дефекты, которые сами по себе могут приводить к развитию несовместимых с жизнью осложнений, среди которых наиболее грозные – менингоэнцефалит, инсульт, тромбоз мозговых синусов, воздушная эмболия, травматическое повреждение спинного мозга.
Экспериментальные основы хирургии основания черепа были заложены ещё в конце XIX века знаменитыми нейрохирургами Виктором Хорсли и Харви Кушингом. Однако толчком к бурному развитию этого направления стали результаты исследования американского хирурга A.S. Ketcham, опубликованные в начале 60-х гг. прошлого века, в которых впервые у больных с рецидивными опухолями околоносовых пазух с поражением основания черепа, считавшихся ранее обреченными, удалось достичь 3-х летней выживаемости, равной 61%, благодаря применению комбинированных краниофациальных резекций.
В настоящее время наиболее целесообразным в лечении больных с поражением основания черепа считается комплексный метод, комбинирующий химиолучевую терапию с операцией. Комбинированное поражение обеих глазниц, зрительного перекреста, поражение ствола мозга, поперечного и сигмовидного синусов, протяженное поражение внутренней сонной артерии являются факторами, колоссально ограничивающими радикализм выполняемого вмешательства. Большинство авторов в подобных случаях склоняются к необходимости проведения предоперационной химиолучевой терапии с целью уменьшения размеров опухолевого очага до рубежа возможности выполнения функционально-сохранного хирургического вмешательства без ущерба для радикализма. Пожалуй, единственным ограничением в проведении подобной методики лечения является устойчивость опухоли к химиолучевому воздействию (остеогенные саркомы, хондросаркомы, менингиомы и т.д.). В таких случаях, а также тогда, когда после проведения химиолучевого этапа не удается достичь выраженной регрессии опухоли целесообразно проведение курса послеоперационной лучевой терапии с целью девитализации микроскопических остаточных очагов – зон развития потенциальных рецидивов. Основным критерием при этом является морфологически подтвержденное наличие опухолевых клеток в крае резекции.
На сегодня не существует универсальной классификации опухолей основания черепа, т.к. в большинстве случаев основание вовлекается в опухолевый процесс вторично местно-распространенными опухолями соседних локализаций, либо метастазами злокачественных опухолей из отдаленных органов. Оптимальным, на наш взгляд, является условное разделение опухолей, поражающих основание черепа соответственно проекции трех черепных ямок, так как оно весьма удобно в планировании объема хирургического вмешательства, играющего основную роль в лечении этой патологии. Например, в проекции передней черепной ямки располагаются опухоли, исходящие из верхнечелюстных и лобных пазух, клеток решетчатого лабиринта, глазниц; средней – опухоли основной пазухи, носоглотки, подвисочной и крылонебной ямок, среднего уха; задней – тканей, составляющих шейно-затылочное сочленение.
Клинические проявления опухолей, поражающих основание черепа, разнообразны и неспецифичны и, в основном, зависят от первичной локализации опухоли и вовлечения в процесс соседних структур: черепно-мозговых нервов, магистральных сосудов, тканей головного и спинного мозга. Первое место по частоте поражения основания черепа занимают опухоли околоносовых пазух, которые примерно в 15% случаев распространяются в область передней черепной ямки. Чаще всего это эпителиальные опухоли, среди которых в большинстве случаев (50-80%) встречается плоскоклеточный рак. Нередко опухоли околоносовых пазух принимают за различные воспалительные процессы (гаймориты, фронтиты и т.д.) из-за чего большинство пациентов (70-90%) поступают в клинику с уже распространенным опухолевым процессом. Среди основных симптомов при этом - заложенность и периодические кровянистые выделения из носа, снижение слуха на стороне поражения, нередко при инфильтративных опухолях носоглотки - комбинированное поражение n. abducens (VI) и n. facialis (VII), проявляющееся приводящим косоглазием и парезом мимической мускулатуры, снижение чувствительности кожи лица, невралгии, экзофтальм. Опухоли подвисочной ямки клинически протекают как парафарингеальные и чаще всего проявляются смещением боковой стенки глотки к срединной линии, дисфагией, затрудненным дыханием; при злокачественных опухолях с инфильтративным ростом могут присоединиться прогрессирующие головные боли, связанные с вовлечением в процесс внутренней сонной артерии, парез гортани вследствие поражения блуждающего нерва, синдром Горнера при поражении симпатического ствола. В тех случаях, когда опухоли располагаются в проекции задней черепной ямки, клиническая картина напоминает шейный остеохондроз – боли в шейном отделе позвоночника, периодические головные боли, головокружения, вестибулярные расстройства. При распространении опухоли в полость черепа на первый план выходят проявления очаговой неврологической симптоматики, которые зависят от локализации поражения.
За период с 1980 г. в клинике опухолей верхних дыхательно-пищеварительных путей ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России находились на лечении 366 пациентов с различными патологическими процессами в области основания черепа. Среди них 140 (38,2%) больных с опухолями, локализованными в области околоносовых пазух и полости носа, 176 (48,1%) - с опухолями подвисочной ямки, 40 (10,9%) пациентов - с распространенными патологическими процессами, исходящими из костей основания черепа, 8 (2,2%) - с первичным либо вторичным метастатическим поражением орбиты, 2 (0,5%) - с местно-распространенными опухолями кожи, поражающими основание черепа. Многообразие опухолей, поражающих основание черепа, требует тщательной морфологической верификации перед началом лечения; нередко окончательный диагноз можно получить лишь после проведения иммуноморфологического исследования. В исследуемой группе 196 (53,6%) пациентов имели злокачественные новообразования, среди которых преобладали эпителиальные опухоли: плоскоклеточный рак – у 65 (33,2%), аденокистозный рак – у 16 (8,2%), аденокарцинома – у 8 (4,1%), эстезионейробластома – у 18 (9,2%), поражающие, в основном (54,1%), придаточные пазухи и полость носа; встречались также различные виды сарком (55 больных - 28,1%), исходящие из костных структур основания черепа; кроме того, встречались такие опухоли как злокачественная шваннома (6 больных - 3,1%), меланома (3 больных - 1,5%), базально-клеточный рак (2 больных - 1%) и т.д.
170 (46,4%) больных имели доброкачественные опухоли. В этой группе преобладали опухоли подвисочной ямки (75,9%), среди которых чаще всего встречались доброкачественные шванномы (34 больных - 20%), исходящие из оболочек черепно-мозговых нервов и чувствительных корешков шейного сплетения, плеоморфная аденома глоточного отростка околоушной слюнной железы (30 больных - 17,6%), вагальные параганглиомы (28 больных - 16,5%), невриномы (14 больных - 8,2%), менингиома (7 больных - 4,1%); кроме этого ангиофибромы носоглотки (8 больных -8,2%), фиброзная дисплазия верхней челюсти (5 больных - 2,9%).
Тактика лечения больных с местно-распространенными опухолями основания черепа зависит от гистологического типа, локализации, а также распространенности опухолевого процесса. Благодаря развитию активных режимов химиолучевого лечения, позволяющих добиться на дооперационном этапе значительной регрессии опухоли, нередко удается перевести процесс в резектабельное состояние у больных, которые раньше считались бесперспективными. В связи с этим 54 (27,6%) пациентам с такими опухолями как плоскоклеточный рак, эстезионейробластома, эмбриональная рабдомиосаркома, на первом этапе было проведено химиолучевое лечение, при этом в 20% случаев удалось добиться полной клинической регрессии. 74 (37,7%) больных в основном с плоскоклеточным/аденокистозным раком верхнечелюстных пазух и различными видами сарком в плане комбинированного лечения на первом этапе получили только лучевую терапию с меньшими показателями непосредственной эффективности лечения – 3,5%.
Оперативные вмешательства выполнены 267 (73%) пациентам. Из них в 170 (63,4%) случаях при доброкачественных процессах, когда объем операции ограничивался в основном удалением опухоли без повреждения соседних структур. Некоторые доброкачественные процессы сопровождаются выраженными костно-деструктивными изменениями, затрудняя правильную диагностику, нередко требуют выполнения обширных комбинированных резекций. Подобные проявления имелись в 26 (15,3%) случаях в основном при ангиофибромах носоглотки и фиброзных дисплазиях костей лицевого скелета.
В большинстве случаев диагноз доброкачественного процесса не представляет сложности на дооперационном этапе, но технические трудности, связанные с удалением обширных опухолей, вынуждают использовать комбинированные доступы для адекватного выполнения оперативного приема. Таким примером могут служить гигантские плеоморфные аденомы, исходящие из глоточного отростка околоушной слюнной железы, которые в наших наблюдениях встречались в 30 (17,6%) случаях. Наружный шейный доступ в большинстве случаев (176 больных) являлся достаточным для удаления опухолей подвисочной ямки. Однако при более распространенных опухолевых процессах, особенно таких злокачественных как саркомы, этот вид доступа приходится комбинировать с различными видами остеотомий, резекцией ветви нижней челюсти и/или скуловой дуги, которые были выполнены у 23 (13,1%) больных.
У больных с распространенными опухолями околоносовых пазух, полости носа и костных структур основания черепа выполнялись расширенно-комбинированные операции (71 случай), состоящие в удалении верхней челюсти с одной либо двух сторон, экзентерации и различных видов резекции стенок орбиты, резекции клеток решетчатого лабиринта, стенок лобных и основной пазух, твердой мозговой оболочки. Основным видом доступа для удаления таких опухолей являлся трансфациальный.
Нередко при распространенных опухолях приходится выполнять резекции непосредственно костных структур основания черепа. При этом дефекты, образующиеся во время таких операций, необходимо одномоментно восстанавливать с целью профилактики различных осложнений, в основном базальной ликвореи. Небольшие дефекты могут быть замещены местным пластическим материалом. Например, при ограниченных по объему орбитофациальных резекциях хорошим пластическим материалом для восстановления дефекта основания черепа в области глазницы может служить височная мышца. Подобного рода операции выполнены 11 (4,1%) больным.
У 35 (9,6%) больных имелось распространение опухоли в полость черепа. При этом основными воротами опухолевой инвазии являются естественные отверстия на основании (сетевидная пластинка, канал зрительного нерва, нижняя глазничная щель, яремное отверстие) либо непосредственное разрушение опухолью костного барьера с распространением на твердую мозговую оболочку и ткани головного мозга. Известно, что больные с поражением твердой мозговой оболочки имеют худший прогноз в связи с высоким риском отдаленного метастазирования; по данным разных авторов 2-летняя выживаемость в таких случаях после проведенного лечения падает с 56% до 40%. Но все же в таких случаях возможно выполнение радикального вмешательства с использованием комбинированного краниофациального доступа. Отход от этого принципа ведет к резкому росту частоты рецидивов.
При выполнении таких обширных по объему резекций встает вопрос использования надежного пластического материала для закрытия дефекта основания черепа. Необходимо отметить, что в данном случае восстановление дефекта твердой мозговой оболочки несет задачу профилактики не только базальной ликвореи, но и такого осложнения как менингоэнцефалит, ограничивая полость черепа от обсемененных патогенной флорой околоносовых пазух. В нашей группе 15 (42,9%) больным с интракраниальным распространением опухоли выполнены одномоментные оперативные вмешательства с пластическим восстановлением дефектов основания черепа. При этом в 5 (33,3%) случаях для восстановления дефектов основания черепа и твердой мозговой оболочки нами использован перикраниальный надкостничный лоскут, в остальных случаях (10 больных - 66,7%) при менее распространенных дефектах - височная мышца.
Осложнения после операций в области основании черепа развились у 27 (9,9%) больных, при этом основными их видами были менингит (2 больных - 0,7%), парез половины гортани вследствие резекции блуждающего нерва (5 больных - 1,9%), различные неврологические расстройства в виде парезов и параличей каудальной группы черепно-мозговых нервов (IX, X, XI, XII), а также синдрома Горнера (15 больных - 5,6%), ликворея (3 больных - 1,1%), острое нарушение мозгового кровообращения (2 больных - 0,7%). Чаще всего неврологическая симптоматика подобного рода возникала при удалении вагальных хемодектом (60%), что связано с близким соседством перечисленных структур с крупными сосудами в области подвисочной ямки наряду с небольшими размерами этой области и недостаточной визуализации проксимальных её отделов.
109 (55,6%) больных злокачественными новообразованиями с поражением основания черепа живы свыше 5 лет после проведенного лечения.
Список литературы:
1. Сдвижков А.М. “Хирургические аспекты лечения распространенных злокачественных опухолей носа, околоносовых пазух и верхней челюсти”, Док. дисс., Москва, 1997.
2. Коновалов А.Н. “Хирургия опухолей основания черепа”, М.: 2004.
3. Jatin Shah “HEAD & NECK, SURGERY & ONCOLOGY”, THIRD EDITION, Mosby, 2003.
4. J.Shah, Narayan S., Joseph G. “Craniofacial Resections for Tumors Involving the Base of the Skull”, The American Journal of Surgery, Vol.154, Oct.1987.
5. Matias C., Carlos C., Julio A., Carlos N., Santiago O. “Repair of large orbito-cutaneous defects by combining two classical flaps”. Journal of Cranio-Maxillofacial Surgery, (2004) 32, p.21-27.
6. Paul J.Donald “Surgery of the Skull Base”, Lippincott-Raven Publishers, Philadelphia, 1998.
Читайте также:
