Синдром Холта-Орама. Гидролетальный синдром
Добавил пользователь Skiper Обновлено: 29.01.2026
Синдром Холта-Орама — редкое генетическое заболевание, характеризующееся аномалией верхней конечности, врожденными пороками сердца и/или нарушениями проводимости. Заболевание обусловлено мутациями гена Tbox5 (локализация 12q24.21), которые наследуются по аутосомно-доминантному типу. Типичными врожденными аномалиями являются дефекты перегородки сердца и изолированная гипоплазия тенара. Представлен клинический случай девочки 7 мес с семейным анамнезом синдрома Холта—Орама: отсутствие I пястной кости левой кисти и множественными пороками развития сердца (дефект межпредсердной перегородки, множественные дефекты межжелудочковой перегородки по типу швейцарского сыра, стенозом аортального клапана). Подробно рассмотрена клиническая диагностика синдрома Холта—Орама, представлен анализ родословной и результаты генетического тестирования ребенка и ближайших родственников.
Ключевые слова
Об авторах
Сойнов Илья Александрович — кандидат медицинских наук, врач сердечно-сосудистый хирург кардиохирургического отделения врожденных пороков сердца, старший научный сотрудник Центра новых хирургических технологий НМИЦ им. акад. Е.Н. Мешалкина.
Дульцева Дарья Анатольевна — врач-ординатор кафедры медицинской генетики и биологии.
630091 Новосибирск, Красный проспект, д. 52
Лейкехман Анастасия Владиславовна — врач-кардиолог кардиохирургического отделения врожденных пороков сердца, старший научный сотрудник Центра новых хирургических технологий НМИЦ им. акад. Е.Н. Мешалкина.
Архипов Алексей Николаевич — кандидат медицинских наук, врач-сердечно-сосудистый хирург, заведующий отделением врожденных пороков сердца, старший научный сотрудник Центра новых хирургических технологий НМИЦ им. акад. Е.Н. Мешалкина.
630055 Новосибирск, ул. Речкуновская, д. 15
Список литературы
2. Van der Linde D, Konings E.E., Slager M.A., Witsenburg M., Helbing W.A. et al. Birth prevalence of congenital heart disease worldwide: a systematic review and meta-analysis. J Am Coll Cardiol 2011; 58: 2241-2247. DOI: 10.1016/j.jacc.2011.08.025
3. Naiche L.A., Harrelson Z., Kelly R.G., Papaioannou V.E. T-box genes in vertebrate development. Annu Rev Genet 2005; 39: 219-239. DOI: 10.1146/annurev.genet.39.073003.105925
4. Barisic I., Boban L., Greenlees R, Garne E., Wellesley D., Calzolari E. et al. Holt Oram syndrome: a registry-based study in Europe. Orphanet J Rare Dis 2014; 9: 156. DOI: 10.1186/s13023-014-0156-y
5. Arkoumanis P.T., Gklavas A., Karageorgou M., Gourzi P., Mantzaris G., Pantou M., Papaconstantinou I. Holt-Oram Syndrome in a Patient with Crohn’s Disease: a Rare Case Report and Literature Review. Med Arch 2018; 72(4): 292-294. DOI: 10.5455/medarh.2018.72.292-294
6. Borozdin W., Bravo Ferrer Acosta A.M., Bamshad M.J., Bot-zenhart E.M., Froster U.G., Lemke J. et al. Expanding the spectrum of TBX5 mutations in Holt-Oram syndrome: detection of two intragenic deletions by quantitative real time PCR, and report of eight novel point mutations. Hum Mutat 2006; 27: 975-976. DOI: 10.1002/humu.9449
7. Heinritz W., Moschik A., Kujat A., Spranger S., Heilbron-ner H., Demuth S. et al. Identification of new mutations in the TBX5 gene in patients with Holt-Oram syndrome. Heart Br Card Soc 2005; 91: 383-384. DOI: 10.1136/hrt.2004.036855
8. Spiridon M.R., Petris A.O., Gorduza E.V., Petras A.S., Popescu R., Caba L. Holt-Oram Syndrome With Multiple Cardiac Abnormalities. Cardiol Res 2018; 9(5): 324-329. DOI: 10.14740/cr767w
9. Newbury-Ecob R.A., Leanage R., Raeburn J.A., Young I.D. Holt-Oram syndrome: a clinical genetic study. J Med Genet 1996; 33: 300-307. DOI: 10.1136/jmg.33.4.300
10. Li Q.Y., Newbury-Ecob R.A., Terrett J.A., Wilson D.I., Curtis A.R., Yi C.H. et al. Holt-Oram syndrome is caused by mutations in TBX5, a member of the Brachyury (T) gene family. Nat Genet 1997; 15: 21-29. DOI: 10.1038/ng0197-21
11. Greulich F., Rudat C., Kispert A. Mechanisms of T-box gene function in the developing heart. Cardiovasc Res 2011; 91: 212-222. DOI: 10.1093/cvr/cvr112
13. Singh G.K. Congenital Aortic Valve Stenosis. Children (Basel) 2019; 6(5). DOI: 10.3390/children6050069
14. Kulyabin Y.Y., Soynov I.A., Zubritskiy A.V., Voitov A.V., Nichay N.R., Gorbatykh Y.N. et al. Does mitral valve repair matter in infants with ventricular septal defect combined with mitral regurgitation? Interact Cardiovasc Thorac Surg 2018; 26(1): 106-111. DOI: 10.1093/icvts/ivx231
15. Voitov A., Omelchenko A., Gorbatykh Y., Zaitsev G., Arkhipov A., Soynov I. et al. Outcomes of perventricular off-pump versus conventional closure of ventricular septal defects: a prospective randomized study. Eur J Cardiothorac Surg 2017; 51(5): 980-986. DOI: 10.1093/ejcts/ezx002
СИНДРОМ ХОЛТА-ОРАМА. ОПИСАНИЕ ДВУХ КЛИНИЧЕСКИХ СЛУЧАЕВ
Цель: демонстрация клинического течения и результатов лечения синдрома Холта-Орама.
Синдром Холта-Орама (предсердно-пальцевая дисплазия, синдром "рука-сердце") впервые описали M.Holt и S.Oram в 1960 г. Частота встречаемости в популяции неизвестна. Соотношение полов при этой патологии составляет 1:1. Тип наследования - аутосомно-доминантный с различной экспрессивностью. Минимальные диагностические признаки: пороки развития верхних конечностей и врожденные дисплазии сердца.
В 85% случаев при данном синдроме выявляются врожденные пороки сердца: дефект межпредсердной перегородки (наиболее часто), дефект межжелудочковой перегородки, открытый артериальный проток, коартация аорты, стеноз легочной артерии. Часто имеется пролапс митрального клапана.
С рождения обнаруживаются нарушения ритма и проводимости сердца. Пороки развития верхних конечностей варьируют от изменений 1 пальца кисти и гипоплазии лучевой кости до фокомелии. К ним относятся поворот лопатки в сторону аксилярной линии грудной клетки, расширение наружного конца головки ключицы, аномальная форма клювовидного отростка лопатки, изменение формы ладьевидной кости, отсутствие, гипертрофия или порочное расположение большого пальца с недостаточным противопоставлением, синдактилия, клинодактилия, воронкообразная грудная клетка.
В редких случаях описывают другие стигмы эмбриогенеза - гипертелоризм, отсутствие большой грудной мышцы, расщелина неба. Биохимические нарушения - задержка азота, повышение уровня мочевины в крови. Нормохромная анемия, спинальная гипоплазия псевдо-Фанкони. Интеллект, как правило, сохранен. Этиопатогенез синдрома - гистодисплазия, нарушение формирования первичного сердца и верхних конечностей на 5-й неделе эмбрионального развития.
Эволюция синдрома заключается в прогрессировании и декомпенсация сердечного порока, развитии нарушений сердечного ритма (СР). Кроме того, отмечается снижение клеточного иммунитета и инфекционные осложнения. Приводим собственные наблюдения клинического течения данного синдрома у двух пациентов.
Один из них, Владислав З., 24 лет, находился на отделении лечения нарушений ритма сердца и электрокардиостимуляции (ЭКС) Клинического центра передовых медицинских технологий с диагнозом: Синдром Холта- -Орама. Врожденная аномалия сердца - синдром бинодальной слабости.
Пациент жаловался на вялость, слабость, головные боли, эпизоды головокружения. Синкопальных состояний не было. Из раннего анамнеза известно, что ребенок от 2-й беременности, сопровождавшейся токсикозом 1-й и 2-й половины и патологической прибавкой массы тела во 2-й половине. Первая беременность в 1965 г. была прервана по причине болезни матери.
На момент беременности матери было 34 года, профессия - химик-технолог, работала на химическом производстве с профессиональной вредностью (имины, фторорганика). За период беременности мать дважды болела ОРВИ, до беременности в течение 12 лет страдала туберкулезным хориоретинитом. Из-за болезни матери ребенок родился в инфекционной больнице путем кесарева сечения с весом 3050 г, длиной тела 50 см. Через месяц после родов был отмечен систолический шум в области сердца, неправильное развитие пальцев левой кисти.
В возрасте 6 месяцев ребенок находился на стационарном лечении в инфекционной больнице с диагнозом: ОРЗ, двусторонняя пневмония, врожденный порок сердца (?), гипотрофия 1-2 степени, рахит 1-2 степени, стафилококковый энтерит, лямблиоз кишечника. Врожденная правосторонняя паховая грыжа. Водянка правого яичка. Врожденная двусторонняя лучевая косорукость.
В 1 год отмечено отставание в весе, психоэмоциональное развитие по возрасту. В 4 года выполнена корригирующая операция по поводу врожденного порока развития кистей - трехфалангового большого пальца, клинодактилии 1 пальца левой кисти (удаление добавочной средней фаланги, устранение клинодактилии). Осталась гипоплазия мышц тенара, резкое нарушение супинации костей без рентгенологически определяемого синостоза, воронкообразная грудная клетка.
В анамнезе ребенка частые ОРВИ, скарлатина, краснуха, эпидпаротит, хронический тонзиллит с частыми обострениями, постоянное отставание в физическом развитии. В 11 лет оперирован по поводу острого аппендицита.
На диспансерном учете у кардиоревматолога состоял с рождения. Первая ЭКГ в возрасте 10 мес. - синусовый ритм, брадикардия 105 уд/мин (Р-Р = 570 мс, P-Q = 160 мc), тенденция к отклонению электрической оси сердца вправо. Неполная блокада правой ножки пучка Гиса.
В возрасте 2,5 лет на ЭКГ регистрировалась синусовая брадиаритмия с частотой сердечных сокращений 77 уд/мин, небольшое замедление атриовентрикулярной проводимости (P-Q = 180 мс). С 3,5 лет - выраженная синусовая брадиаритмия от 83 до 53 в мин. В 7 лет наблюдалась миграция водителя ритма по предсердиям, частота ритма 46 уд/мин.
В 8 лет отмечено появление изоритмической АВ диссоциации, а в 9 лет впервые поставлен диагноз синдрома слабости синусового узла (брадикардия 45 уд/мин, постоянная интерферирующая АВ диссоциация, предсердная экстрасистолия). При дальнейшем наблюдении ЭКГ без существенной динамики.
В возрасте 15 лет после консультации в генетическом центре ребенку был поставлен диагноз: синдром Холта-Орама. При эхокардиографическом исследовании выявлены пролапсы митрального, трикуспидального клапанов и клапана легочной артерии 1 степени.
При рентгенографии грудной клетки в возрасте 9 лет выявлено умеренное усиление легочного рисунка в корневых зонах, расширение сердца в поперечнике за счет всех сегментов (КТИ = 57 при норме до 50). В 16 лет отмечено усиление легочного рисунка за счет гиперволемии, расширение легочного ствола, увеличение правых камер сердца и левого желудочка.
В возрасте 22 лет при Холтеровском суточном мониторировании отмечена выраженная синусовая брадиаритмия, изоритмическая АВ диссоциация с частотой ритма до 28 уд/мин, паузы от 1240 до 3338 мс за счет СА блокады 2 степени 2 типа, 2:1, 3:1 и остановки синусового узла. За время наблюдения зафиксировано 3340 пауз (в среднем 182 в час). Обращало на себя внимание отсутствие выскальзывающих комплексов из центров автоматизма 2 порядка в моменты асистолии. Периодически регистрировалась АВ блокада 1 типа (PQ = 240 мс).
При ЧП ЭФИ максимальное ВВФСУ = 1800 мс (норма до 1540 мс), КВВФСУ = 800 мс (норма до 540 мс), антероградное АВ проведение на нижней границе нормы (точка Венкебаха АВ соединения = 130 имп/мин). Постстимуляционные паузы достигали 2200 мс. После введения атропина максимальная частота ритма составила всего 85 в минуту (при норме не менее 105 в мин). Заключение: Синдром слабости синусового узла (СССУ). Формирование синдрома бинодальной слабости.
Пациенту была предложена операция: имплантация постоянного электрокардиостимулятора (ПЭКС). В отделении ему был имплантирован ПЭКС фирмы Intermedics "Relay" в режиме DDDR. Импортный физиологический электрокардиостимулятор был выделен для пациента по распоряжению Президента РФ.
Улучшение самочувствия пациент отметил уже на второй день после операции. Исчезли слабость, вялость, головокружение. Установлены физиологические параметры стимуляции при удовлетворительных пороговых значениях. При контрольном посещении через три и шесть месяцев после выписки из стационара жалоб у пациента нет, отмечает улучшение аппетита, настроения, повышение толерантности к нагрузкам (по собственному выражению пациента, стал "летать"). В настоящее время закончил аспирантуру и завершает работу над кандидатской диссертацией.
Другая пациентка: Катя Б., 6 лет. Признаками синдрома Холта-Орама являлись врожденная патология обеих кистей, недоразвитие лучевых костей, дефект межпредсердной перегородки, оперированный в возрасте 1,5 лет, нарушения ритма сердца в виде синдрома слабости синусового узла (брадикардия, эпизоды изоритмической АВ-диссоциации и замещающего АВ-ритма, АВ узловая экстрасистолия, отсутствие прироста частоты сердечных сокращений на физическую нагрузку и введение атропина).
По совокупности данных обследования были определены показания для имплантации искусственного водителя ритма. Девочке имплантирован физиологический однокамерный ПЭКС фирмы Pacesetter "Regency SR", в который включен частотно- адаптивный режим VVIR. Параметры электростимуляции удовлетворительные, у девочки улучшился аппетит, уменьшились жалобы. Теперь ей предстоит хирургическая коррекция кистей, для которой сейчас отсутствуют противопоказания со стороны кардиальной патологии.
В заключение следует отметить, что брадиаритмия у пациентов с синдромом Холта-Орама имеет тенденцию к прогрессивному ухудшению с формированием СССУ, а своевременная имплантация физиологической ПЭКС-системы позволяет нормализовать клиническую картину, гемодинамические параметры и значительно улучшить качество жизни.
ЛИТЕРАТУРА
1. Справочник клинических симптомов и синдромов. Под ред. И.Р.Лазовскис. - М., Мед., 1981 г.
2. Козлова С.И., Семанова Е., Демикова Н.С., Блинникова О.Е. Наследственные синдромы и медико-генетическое консультирование. Л.:Медицина, 1987. - с. 227-228.
3. Парщикова Л.С., Рейдерман М.И. Синдром Холта-Орама //Ортопедия, травматология. - 1976. - N 10, с. 69-70.
5. Chang C.H. Holt-Oram Syndrome.//Radiology. - 1967. - v. 88. - p. 479-483.
6. Holt M., Oram S. Familian heart disease with skeletal malformations // Brit. Heart J. - 1960. - N 2. - p. 236.
7. Martin Cl., Badin J., San Juan B., Hehunstere J. Un cas de Syndrome de Holt-Oram // Arch Franc Ped. - 1970. - N 8. - p. 865.
8. Gladstone I.A., Subert V.P. Holt-Oram syndrome: Penetrance of the gene and lack of maternal effect // Clin Genet. - 1982. - V. 21. - p. 99-103.
Российский Научно-Практический
рецензируемый журнал
ISSN 1561-8641
Синдром Холта-Орама, TBX5 м.
Синдром Холта - Орама (синдром «руки-сердца», Holt-Oram Syndrome, OMIM142900) - заболевание, характеризующееся пороками развития верхних конечностей и врождёнными пороками сердца. Пороки развития верхних конечностей варьируют от изменений I пальца кисти (гипоплазия, трехфаланговый палец) и гипоплазии лучевой кости до фокомелии. Левая рука поражается чаще. У 50% больных палец не противопоставлен остальным. Также наблюдаются гипоплазия лопаток и ключиц, сколиоз, воронкообразная деформация грудины, клинодактилия, синдактилия, гипоплазия или аплазия других пальцев кисти и костей запястья. У 85% больных обнаруживают врождённые пороки сердца такие, как наиболее часто встречающийся дефект межпредсердной перегородки, дефект межжелудочковой перегородки, открытый артериальный проток, коарктация аорты, стеноз лёгочной артерии, пролапс митрального клапана. Также описаны гипертелоризм, отсутствие большой грудной мышцы, расщелина нёба. Интеллект, как правило, сохранён.
Пороки развития верхних конечностей варьируют от изменений I пальца кисти (гипоплазия, трехфаланговый палец) и гипоплазии лучевой кости до фокомелии. Левая рука поражается чаще. У 50% больных I палец не противопоставлен остальным.
Также наблюдаются гипоплазия лопаток и ключиц, сколиоз, воронкообразная деформация грудины, клинодактилия, синдактилия, гипоплазия или аплазия других пальцев кисти и костей запястья. В 85% случаев обнаруживают врожденные пороки сердца такие, как наиболее часто встречающийся дефект межпредсердной перегородки, дефект межжелудочковой перегородки, открытый артериальный проток, коарктация аорты, стеноз легочной артерии, пролапс митрального клапана.
Дефект межпредсердной перегородки обусловливает специфическую предсердную аритмию: на ЭКГ удлинение интервала P - Q, синусовая брадикардия с тенденцией к синоатриальному блоку и атриовентрикулярному ритму. В редких случаях наблюдается мерцание предсердий. Также описаны гипертелоризм, отсутствие большой грудной мышцы, расщелина неба. Интеллект, как правило, сохранен. Средняя продолжительность жизни больных - около 40 лет.
Литература
- Козлова С. И., Демикова Н. С. Наследственные синдромы и медико-генетическое консультирование. – М.: КМК, 2007 – 448 с.
- Кеннет Л. Джонс «Наследственные синдромы по Девиду Смиту» Атлас-справочник. Москва, Практика, 2011.
- Basson, C. T., Cowley, G. S., Solomon, S. D., Weissman, B., Poznanski, A. K., Traill, T. A., Seidman, J. G., Seidman, C. E. The clinical and genetic spectrum of the Holt-Oram syndrome (heart-hand syndrome). New Eng. J. Med. 330: 885-891, 1994.
- OMIM.
Специальной подготовки к исследованию не требуется.
Обязательны к заполнению:
*Заполнение «анкеты молекулярно-генетического исследования» необходимо для того, чтобы врач-генетик, на основании полученных результатов, во-первых, имел бы возможность выдать пациенту максимально полное заключение и, во-вторых, сформулировать для него конкретные индивидуальные рекомендации.
ИНВИТРО гарантирует конфиденциальность и неразглашение предоставляемой пациентом информации в соответствии с законодательством Российской Федерации.
Литература
- Козлова С. И., Демикова Н. С. Наследственные синдромы и медико-генетическое консультирование. – М.: КМК, 2007 – 448 с.
- Кеннет Л. Джонс «Наследственные синдромы по Девиду Смиту» Атлас-справочник. Москва, Практика, 2011.
- Basson, C. T., Cowley, G. S., Solomon, S. D., Weissman, B., Poznanski, A. K., Traill, T. A., Seidman, J. G., Seidman, C. E. The clinical and genetic spectrum of the Holt-Oram syndrome (heart-hand syndrome). New Eng. J. Med. 330: 885-891, 1994.
- OMIM.
Типичная клиническая картина.
Литература
- Козлова С. И., Демикова Н. С. Наследственные синдромы и медико-генетическое консультирование. – М.: КМК, 2007 – 448 с.
- Кеннет Л. Джонс «Наследственные синдромы по Девиду Смиту» Атлас-справочник. Москва, Практика, 2011.
- Basson, C. T., Cowley, G. S., Solomon, S. D., Weissman, B., Poznanski, A. K., Traill, T. A., Seidman, J. G., Seidman, C. E. The clinical and genetic spectrum of the Holt-Oram syndrome (heart-hand syndrome). New Eng. J. Med. 330: 885-891, 1994.
- OMIM.
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
дефекты лучевой кости, тромбоцитопения с отсутствием лучевой кости, панцитопении Фанкони, хондроэктодермальная дисплазия, VATER-ассоциация.
Синдром Холта-Орама. Гидролетальный синдром
Синдром Холта-Орама. Гидролетальный синдром
Синдром Холта-Орама (Holt-Oram) включает пороки сердца и аномалии развития верхних конечностей (фокомелия в 4,5%, аплазия лучевой кости, трехфаланговый большой палец кисти, клинодактилия).
Синонимы. Синдром «рука-сердце» (этот синдром генетически отличается от кардиомелических синдромов («сердце-рука») типов II и III).
Распространенность. Встречается нечасто.
Этиология. Аутосомно-доминантный тип наследования со 100% пенетрантностью и отсутствием свидетельств ослабления физического здоровья. Можно ожидать усиления проявлений заболевания в последующих поколениях.
Риск рецидива составляет 50%.
Диагностика. Пороки сердца включают дефекты межпредсердной (30-60%) и межжелудочковой перегородки, открытый артериальный проток, дефект закладки эндокардиальных подушек, гипоплазию левого желудочка и нарушения проводимости, при этом в 17% случаев наблюдаются сочетанные пороки сердца. Состояние кистей при аплазии лучевых костей варьирует от труднодиагностируемого трехфалангового большого пальца до очевидной косорукости. Также может выявляться аплазия большого пальца кисти.
Патогенез. Возможно, дефект кардиомелического поля развития.
Генетические нарушения. Были выявлены мутации двух генов (Т-box) гомеобокса (ТВХ5 и ТВХЗ), локализованных на длинном плече хромосомы 12q24.1, обусловливающие развитие врожденных аномалий при синдроме Холта-Орама (Holt-Oram). Ген ТВХ5 ответственен только за развитие верхних конечностей.
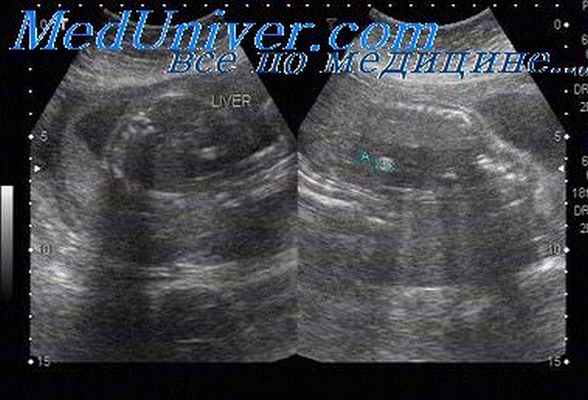
Сочетанные аномалии. Сообщалось также о нескольких непостоянно встречающихся аномалиях, таких как пороки развития почек.
Дифференциальный диагноз. В качестве дифференциального диагноза обычно рассматривается аплазия пальцев лучевого отдела кисти, а также синдром TAR (тромбоцитопении - аплазии лучевой кости), анемия Фанкони (Fanconi), ассоциация VACTERL и синдром атрезии лучевой кости - артезии хоан.
Прогноз. В основном связан с тяжестью проявления сердечных и ортопедических нарушений.
Обычно изменение стандартной тактики пренатального ведения беременности не требуется. Большой прогресс в вопросах ортопедического лечения для обеспечения противотивопоставления большого пальца позволил снизить инвалидизацию у части таких детей.
Гидролетальный синдром
Данный синдром включает полидактилию (постаксиальная форма для кистей и преаксиальная форма для стоп), а также мальформации ЦНС, такие как гидроцефалия. Синонимы. Синдром Салонена-Херва-Норио (Salonen-Herva-Norio).
Распространенность. У родителей часто имеются предки в восточной части Финляндии, где частота нарушений составляет до 0,5 на 10 000 родов. Вне пределов этой подгруппы заболевание встречается очень редко.
Диагностика. Заподозрить данный синдром позволяет выявление признаков выраженной гидроцефалии, микрогнатии, полидактилии (в особенности удвоение большого пальца стопы), косолапости и многоводия. Другие нарушения включают расщелину губы или неба, гипоплазию легких и дефект закладки эндокардиальных подушек.
Дифференциальный диагноз. Синдром Мекеля (Meckel), при котором также отмечаются полидактилия, аномалии ЦНС (цефалоцеле вместо гидроцефалии) и кисты почек.
Прогноз. Как правило, наступает неонатальная гибель, однако в редких случаях дети могут прожить несколько месяцев.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Акрокаллозальный синдром - Acrocallosal syndrome
Акрокаллозальный синдром (также известный как ACLS) является редким аутосомный рецессивный синдром, характеризующийся агенезия мозолистого тела, полидактилия, несколько дисморфические особенности, двигательные и интеллектуальные нарушения и другие симптомы. [1] Синдром был впервые описан Альбертом Шинзелем в 1979 году. [2]
Это связано с GLI3. [3]
Содержание
Признаки и симптомы
Акрокаллозальный синдром (ACLS, ACS, тип Шинцеля, дупликация Hallux) - редкий, гетерогенный [3] аутосомно-рецессивное заболевание, впервые обнаруженное Альбертом Шинзелем (1979) у 3-летнего мальчика. [2] Чтобы унаследовать ACLS, одна копия гена от каждого родителя должна содержать мутацию где-то в гене KIF7 и передаваться ребенку. Характеристики этого синдрома включают отсутствие или слабое развитие области, соединяющей левую и правую части мозга, аномально большую голову, увеличенное расстояние между чертами лица (глазами), плохую моторику, умственную отсталость, лишние пальцы рук и ног, много лицевых деформации, [3] и волчья пасть. Это считается редким заболеванием и занесено в список редких заболеваний Управления редких заболеваний NIH (менее 200 000 случаев). Продолжительность жизни может варьироваться от мертворождения до нормальной продолжительности жизни в зависимости от осложнений беременности и тяжести заболевания. [2] Было показано, что в легких случаях субъекты живут относительно нормальной жизнью, но с задержкой в развитии. [2]
Патология
Акрокаллозальный синдром (ACLS, ACS, тип Шинцеля) - редкое гетерогенное аутосомно-рецессивное заболевание. [3] Гетерогенность этого состояния относится к множеству генов, которые могут действовать, чтобы способствовать различной степени этого синдрома. [3] и часто связано с кровным родством. [2] Характеристики этого синдрома включают агенезию тела, макроцефалию, гипертелоризм, полидактилию, умственную и двигательную отсталость, [2] черепно-лицевой дисморфизм, удвоение большого пальца стопы, [3] и иногда небная расщелина. Также сообщалось, что существует много похожих признаков и симптомов между ACLS, Цефалополисиндактилия Грейга, и гидролетальный синдром (HLS), хотя на данный момент мало доказательств в поддержку общей генетической причинности. [3]
Механизм
Недавние исследования показали, что мутации, ответственные за ACLS, расположены в белке KIF7. KIF7 представляет собой белок из 1343 аминокислот с кинезиновым двигателем, спиральной спиралью и Gli-связывающими доменами. Его функции в значительной степени связаны с моторной функцией ресничек, [3] и является ключевым фактором в путях трансдукции Sonic Hedgehog (Shh), которые имеют решающее значение во время эмбриогенеза. Следовательно, мутации в компонентах передачи сигналов Hedgehog (KIF7) могут приводить к патологиям на основе ресничек и, в конечном итоге, к дефектам в головном мозге и других областях, связанных с ACLS и родственными расстройствами. Более конкретно, мутации, наблюдаемые в гене GLI3, дали характеристики, аналогичные ACLS, но необходимы дополнительные доказательства, поскольку в этих случаях обычно присутствует мозолистое тело. Другие исследования также показали, что KIF7 взаимодействует с факторами транскрипции Gli, поэтому мутации в гене KIF7 могут быть вышестоящими эффекторами GLI3. Дальнейшее понимание функций ACLS и лежащих в их основе механизмов открывает новые возможности для фармакологических манипуляций и других форм молекулярной терапии. [4]
Читайте также:
