Сосудистая опухоль головного мозга (гемангиоперицитома) - патология, морфология
Добавил пользователь Alex Обновлено: 16.01.2026
Гемангиоперицитома - это редкая опухоль, которая развивается из сосудов капиллярного типа, поэтому она может встречаться везде, где есть кровеносные сосуды, но преимущественно на коже го¬ловы и конечностей, в подкожной жировой клетчатке и скелетных мышцах нижних конечностей. В редких случаях гемангиоперицитома может локализоваться в околоносовых пазухах. Обычно она одинаково отмечается как у мужчин, так и у женщин, чаще всего в пожилом возрасте. Гемангиоперицитома редко как проявляется и зачастую выявляется случайно. Для гемангиоперицитом характерно агрессивное течение с тенденцией к рецидивированию и метастазированию. Эта опухоль может также встречаться и в головном мозге, вызывая типичную клиническую картину опухоли мозга. По своему гистологическому типу могут быть доброкачественными, с медленным ростом, и злокачественными, с характерным инфильтрирующим ростом и метастазированием в отдаленные органы (в легкие, костную ткань и т.д.).
Симптоматика гемангиоперицитомы головного мозга
Гемангиоперицитома обычно выявляется в виде мягкотканых образований с бугристой узловатой поверхностью. Кожа над гемангиоперицитомой обычно не изменена, иногда может быть синюшно-красной. Опухоль чаще всего безболезненная. Если гемангиоперицитома локазилизуется в головном мозге, могут возникать такие симптомы, как головная боль, тошнота и рвота, головокружения, нарушения координации движений, нарушение зрения, повышение внутричерепного давления, и другая очаговая неврологическая симптоматика. Обычно проявления интракраниальной локализации гемангиоперицитомы зависит от того, в каком отделе развилась опухоль.
Диагностика гемангиоперицитомы головного мозга
Диагностика гемангиоперицитомы основана на таких методах исследования, как неврологическое обследование и инструментальные методы. Неврологическое исследование включает в себя оценку рефлексов и кожной чувствительности. Врач также оценивает движения в конечностях. При нарущениях зрения проводится консультация офтальмолога. Из других методов диагностики могут применяться электромиография или электронейрография.
При локализации гемангиоперицитомы в головном мозге применяются такие методы, как компьютерная томография и магнитно-резонансная томография, а также рентгенологические методы, как пневмомиелография и вентрикулография. Для их проведения проводится люмбальная пункция, с помощью которой также проводится анализ спинномозговой жидкости на атипичные клетки.
Ключевую роль в диагностике гемангиоперицитомы играют такое методы, как компьютерная томография и магнитно-резонансная томография. Они позволяют получить послойное изображение тканей головного мозга. Это неинвазивные методы, которые основаны на рентгеновском излучении (КТ) и мощном магнитном поле (МРТ). Эти методы диагностики отличаются высокой точностью и позволяют врачу определить точную локализацию опухоли, ее размеры, форму, отношение к соседним тканям и органам.
В некоторых случаях может также применяться УЗИ головного мозга (М-эхо), которое позволяет оценить смещение срединных структур мозга. Помимо указанных методов могут применяться ангиография сосудов головного мозга, электроэнцефалография и сцинтиграфия.
Лечение гемангиоперицитомы
Лечение гемангиоперицитомы включает в себя все методы, которые используются в лечении опухолей головного мозга. Это хирургическое вмешательство и лучевая терапия, а при злокачественных гемангиоперицитомах - химиотерапия.
Стандартным методом лечения гемангиоперицитом головного мозга является хирургическое вмешательство. Выбор того или иного метода оперативного вмешательства зависит от таких факторов, как локализация и размеры опухоли. Хирургическое вмешательство может быть как традиционное открытое, в виде трепанации черепа, так и малоинвазивное, эндоскопическое. Этот метод применяелся при локализации гемангиоперицитомы в области околоносовых пазух. При этом используется эндоназальный доступ через носовые ходы. Преимуществом малоинвазивного метода является его меньшая травматичность, меньший риск осложнений и более быстрое заживление, что означает более короткий послеоперационный период. В некоторых случаях оперативное вмешательство дополняется лучевой терапией, как до операции, так и после нее. Это проводится для уменьшения размеров опухоли, или для полного уничтожения опухолевых клеток, которые могли остаться после операции.
Лучевая терапия может применяться как самостоятельный метод лечения в случае, когда опухоль имеет труднодоступную локализацию, а также когда риск осложнений операции слишком высок. Лучевая терапия проводится в виде курса, который длится несколько недель. Обычно в неделю проводится пять сеансов облучения. Недостатками лучевой обычной терапии может быть риск возникновения лучевого дерматита и выпадение волос на облучаемом участке. Кроме того, традиционная лучевая терапия не приводит к полному уничтожению опухоли, так как для этого пришлось бы применять слишком большие дозы радиации. Однако, сегодня лучевая терапия все чаще уступает место стереотаксической лучевой терапии - так называемой радиохирургии.
Радиохирургия - это инновационная современная неинвазивная технология применения радиации, которая позволяет получить эффект, сравнимый с операцией без всяких разрезов. Суть радиохирургии заключается в том, что с помощью специального аппарата опухоль облучается тонким слабым пучком радиации каждый раз с разных сторон. При этом, через окружающие опухоль мягкие ткани проходит безопасная доза радиации, а на самой опухоли концентрируется максимальная доза облучения. Метод радиохирургии очень точный, и позволяет всегда направлять луч радиации на опухоль. Преимуществами технологии радиохирургии является, прежде всего, ее неинвазивность, что снижает риск осложнений. Кроме того, этот метод совершенно безболезненный, то есть, нет необходимости в проведении анестезии, что также снижает определенную долю риска осложнений.
Радиохирургия применяется обычно в тех случаях, когда оперативное вмешательство невозможно, например, при тяжелом состоянии пациента, высоком риске осложнений, а также при затрудненном доступе к опухоли.
Для радиохирургии не требуется никакой специальной подготовки, а также нет необходимости в восстановительном периоде, и пациент после сеанса облучения может сразу идти домой. По сравнению с традиционной лучевой терапией, лечение кибер-ножом протекает быстрее и после него не требуется никакого периода восстановления. Ограничением к применению радиохирургии является размер гемангиоперицитомы.
(495) 506-61-01 - где лучше оперировать головной мозг
Кибер-нож в лечении опухолей головного мозга
Кибер-нож - современная инновационная технология применения лучевой терапии, позволяющая воздействовать на опухоль мозга и служит альтернативной оперативным методам лечения. Кибер-нож относится к методам так называемой радиохирургии, как и гамма-нож. Подробнее
Гамма-нож в Германии - нейрохирургическая клиника г. Ахен
На базе нейрохирургической клиники Аахенского Университета с 1998 года применяется специальная методика гамма-кобальтового облучения для лечения опухолей и сосудистых новообразований головного мозга. Подробнее
Лечение опухолей мозга в Израиле - Tel Aviv Souraski Medical Center
Национальный Онкоцентр Им. Сураски является интегральной частью крупнейшей муниципальной мед. клиники Сураски и предоставляет передовое лечение опухолей мозга всех видов.Подробнее
Сосудистая опухоль головного мозга (гемангиоперицитома) - патология, морфология
Гемангиоперицитома. Причины и клиника гемангиоперицитом.
Гемангиоперицитома — весьма редкая опухоль, впервые описанная А.Р. Stout и M. R. Murray в 1942 г. К 1998 г. сообщалось о 300 случаях гемангиоперицитомы.
Гемангиоперицитома чаще всего поражает скелетные мышцы нижних конечностей (34,5%), забрюшинное пространство (24,5%) и область головы и шеи (17%). Она является причиной около 1% опухолей центральной нервной системы и около 3% опухолей орбиты. Опухоль поражает забрюшинное пространство, скелетные мышцы нижних конечностей, глазницу и, очень редко, кожу. Младенческая гемангиоперицитома, встречающаяся с рождения или на первом году жизни, проявляется солитарными или множественными дермальными или подкожными узлами.
Этиология гемангиоперицитомы не ясна. Ретровирусоподобные частицы, обнаруженные в гемангиоперицитомоподобных опухолях у мышей, в гемангиоперицитомах человека идентифицированы не были. Причины возникновения опухоли также связывают с механической травмой или наследственной предрасположенностью: описан семейный случай гемангиоперицитомы с аутосомно-рецессивным путем передачи.
В ранних исследованиях, основанных на результатах световой и электронной микроскопии, гемангиоперицитома расценивалась как опухоль, происходящая из перицитов — модифицированных гладкомышечных клеток, находящихся в стенках капилляров и венул. Однако в связи с отрицательным иммуногистохимическим окрашиванием большинства гемангиоперицитом взрослых на актин и другие мышечные маркеры, их происхождение в настоящее время связывают с недифференцированной мезенхимальной клеткой.
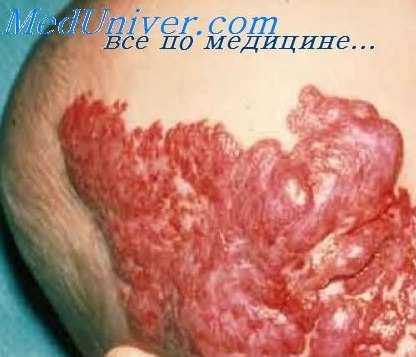
Причины и клиника гемангиоперицитом.
Клинически гемангиоперицитома представляет собой бугристое опухолевидное образование, обычно солитарное, диаметром от 0,5 до 2 см (иногда крупного размера — 35x25 см), различной (мягкой, тестоватой, плотной) консистенции, покрытое неизмененной или синюшно-красной кожей, безболезненное и медленно растущее. Боль (тупая и продолжительная) отмечается при сдавлении опухолью нерва. При определенной локализации опухоли больного могут беспокоить кашель, одышка, тошнота, задержка мочи, гидронефроз, дизурия или запоры; наличием опухоли также могут быть обусловлены телеангиэктазии. одностороннее варикозное расширение вен, геморрой, кровоподтеки, повышение температуры кожи, эндокринные (гипогликемия идр.) и неврологические проявления (при внутричерепных гемангиоперицитомах — головная боль, нарушение походки и равновесия). Опухоль может изъязвляться и давать инфильтрирующий рост, но метастазирует редко.
Макроскопически гемангиоперицитома хорошо отграничена от окружающих тканей или заключена в тонкую капсулу, цвет ее на разрезе варьирует от песочного и серого до розовато-белого, иногда он может быть фиолетовым или красновато-коричневым. Часто встречаются участки некроза, кровоизлияния и явления кистозной дегенерации. При иссечении опухоли нередки профузные кровотечения из окружающего ее большого сплетения крупных сосудов.
Гистологическое строение гемангиоперицитом.
При гистологическом исследовании неопластические перициты выглядят как веретенообразные или овальные клетки со скудной эозинофильной цитоплазмой и плохо очерченными границами. Наибольший диаметр овальных или округлых клеток составляет 7-13 мм. Опухолевые клетки располагаются вне сосудистых каналов, которые очерчены одним слоем эндотелиальных клеток. Опухолевые клетки часто сдавливают сосудистые пространства в виде «оленьих рогов», они отделены от эндотелиальных клеток периваскулярной базальной мембраной — признак, который лучше всего проявляется при окрашивании на ретикулиновые волокна. Ретикулиновые и коллагеновые волокна также обволакивают отдельные опухолевые клетки. Клетки гемангиоперицимтомы всегда располагаются случайным образом, этот признак отличает их от гломусных опухолей, имеющих концентрическое строение, и от синовиальных сарком и фибросарком, в которых опухолевые клетки встречаются в виде узлов и тяжей. Ядра гемангиоперицитомы пузырьковидные и содержат мелкие вакуоли В пределах одной опухоли интенсивность ядерного окрашивания, форма и размеры ядер почти не отличаются, что придает ей монотонный вид. Часты митозы, которые указывают на злокачественное течение. Клеточная анаплазия ассоциируется с большей агрессивностью опухоли.
Сосуды гемангиоперицитом сильно отличаются по калибру. Ткань, окружающая опухоль, содержит расширенные вены. Крупные сосудистые каналы и синусоидные сосуды распространяются радиально внутрь из перикапсулярной ткани, разветвляясь на капилляры или прекапилляры. Эта богатая васкуляризация приводит к выраженной кровоточивости. В опухоли часто видны мелкие очаги кровоизлияний.
И ммуногистохимические характеристики генмангиоперицитомы неспецифичны, но могут помочь в ее отличии от многих гистологически сходных опухолей, а также используются для более точной идентификации происхождения клеток опухоли. Клетки гемангиоперицитомы окрашиваются виментином, маркером мезенхимального происхождения. Наличие положительного окрашивания на фактор XIII во всех исследованных опухолях подтверждает их происхождение из перицитов. В связи с тем, что фактор XIII также экспрессируется злокачественной фиброзной гистиоцитомой, было высказано предположение о тесном родстве этих опухолей. Действительно, эти две опухоли невозможно отличить даже при использовании не только световой и электронной микроскопии, но и иммуногистохимических исследованиях. Иммунореактивность менингиальных, периферических и врожденных вариантов гемангиоперицитом одинакова, что подтверждает общность их происхождения. Хотя ультраструктурные исследования показывают некоторые признаки гладкомышечной дифференцировки, гладкомышечное происхождение гемангиоперицитом не подтверждается их иммунофенотипом. Окрашивание на десмин и актин в этих опухолях положительно лишь иногда. Однако низкий уровень положительного окрашивания на актин не исключает возможности, что перициты проходят дедифференцировку в процессе трансформирования в гемангиоперицитоме.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Диагностика гемангиоперицитомы по КТ, МРТ
а) Терминология:
1. Сокращение:
• Гемангиоперицитома (ГПЦ), менингеальная гемангиоперицитома
2. Синонимы:
• В ранних литературных источниках определяется как «ангиобластическая менингиома», гемангиоперицитарный тип
• В новых публикациях придерживаются терминой солитарная фиброзная опухоль (СФО), гемангиоцитомный тип, клеточная СФО или злокачественная СФО
3. Определения:
• Гиперцеллюлярная мезенхимальная опухоль с богатой васкуляризацией, практически всегда имеющая связь с твердой мозговой оболочкой
• Саркома, развивающаяся вследствие опухолевой трансформации перицитов, сократительных клеток расположенных около капилляров:
о Может возникать в любой области тела, где присутствуют капилляры
б) Визуализация:
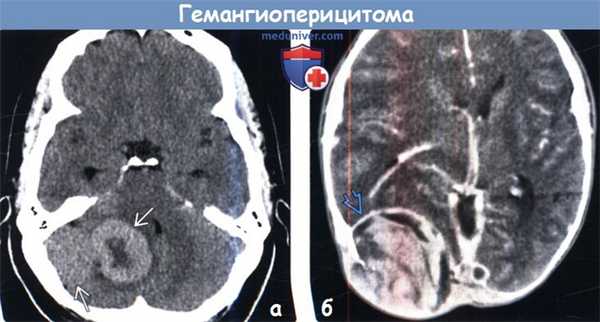
(а) Бесконтрастная КТ, аксиальный срез: в задней черепной ямке определяется гиперденсное объемное образование с локальным масс-эффектом. При резекции была диагностирована анапластическая гемангиоперицитома III степени злокачественности по классификации ВОЗ (grade III).
(б) КТ с контрастированием, аксиальный срез: в затылочной области определяется объемное образование с гетерогенным характером контрастирования и протяженной эрозией кости. Обратите внимание на перифокальный отек и масс-эффект. Локализация и внешние признаки характерны для гемангиоперицитомы. Эти редкие опухоли характеризуются высокой частотой рецидивирования и частым метастатическим поражением за пределами ЦНС.
2. КТ при гемангиоперицитоме (ГПЦ):
• Бесконтрастная КТ:
о Гиперденсное внемозговое объемное образование с перифокальным отеком
- Часто присутствуют участки кистозной и некротической трансформации с низкой КТ-плотностью
о Может наблюдаться эрозия костей свода черепа
о Са++ или гиперостоз отсутствуют
• КТ с контрастированием:
о Интенсивный гетерогенный характер накопления контрастного вещества
3. МРТ при гемангиоперицитоме (ГПЦ):
• Т1-ВИ:
о Объемное образование гетерогенной структуры, изоинтенсивное по отношению к серому веществу
о Могут наблюдаться участки потери сигнала за счет эффекта потока
• Т2-ВИ:
о Гетерогенное изоинтенсивное объемное образование
о Часто наблюдаются выраженные участки потери сигнала за счет эффекта потока
о Характерны перифокальный отек, масс-эффект
о Может наблюдаться гидроцефалия
• Постконтрастное Т1-ВИ:
о Интенсивный, часто гетерогенный характер накопления контраста
о Дуральный «хвост» в 50% случаев о Может наблюдаться область центрального некроза
• МР-венография:
о Может наблюдаться окклюзия синусов твердой мозговой оболочки
4. Ангиография:
• Гиперваскулярное объемное образование с неравномерно выраженными кровоснабжающими опухоль сосудами и пролонгированным контрастированием опухоли по типу «пятна»
• Обширное артериовенозное шунтирование
• Характерно смешанное сосудистое кровоснабжение из твердой и мягкой мозговых оболочек
• Полезна предоперационная эмболизация
5. Радионуклидная диагностика:
• Сцинтиграфия костей:
о Полезна в обнаружении внечерепного метастатического поражения
• ПЭТ:
о Ранее была обнаружена более низкая степень метаболизма ФДГ в ГПЦ по сравнению с серым веществом
6. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о КТ полезна в оценке степени эрозии кости о Мультипланарная МРТ является наиболее чувствительным методом диагностики • Советы по протоколу исследования:
о Мультипланарная МРТ с контрастным усилением ± МР-спектроскопия
о Сцинтиграфия костей полезна для определения тактики дальнейшего ведения пациента, поскольку внечерепные метастазы в кости встречается часто
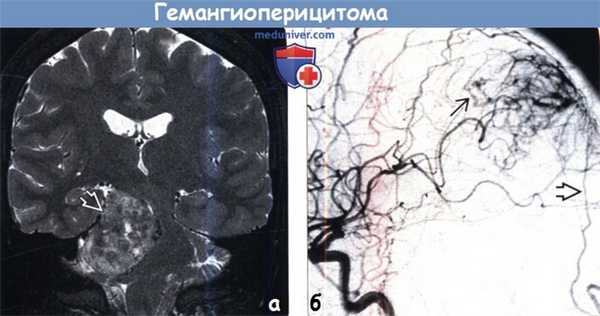
(а) МРТ, Т2-ВИ, режим подавления сигнала от жира, корональный срез: определяется крупное гетерогенное объемное образование, сконцентрированное в правом мостомозжечковом углу и имеющее связь с твердой мозговой оболочкой. При резекции была диагностирована гемангиоперицитома.
(б) ЦСА, контрастирование ВСА, боковая проекция: определяется артериовенозное шунтирование с ранним венозным дренированием. Также наблюдается дополнительный питающий сосуд — ветвь затылочной артерии. Для гемангиоперицитом характерно смешанное кровоснабжение из сосудов твердой и мягкой мозговых оболочек. Часто полезно проведение предоперационной эмболизации.
в) Дифференциальная диагностика гемангиоперицитомы (ГПЦ):
1. Менингиома:
• Может быть неотличима
• Внемозговое накапливающее контраст объемное образование, имеющее связь с твердой мозговой оболочкой широким основанием
• Часто кальцифицируется; симптомом дурального «хвоста»
• Характерен гиперостоз
2. Метастатическое поражение твердой мозговой оболочки:
• Метастатическое поражение твердой мозговой оболочки с инвазией костей свода черепа может быть неотличимо от гемангиоперицитомы (ГПЦ)
• Обычно множественный характер поражения
• Часто известна первичная опухоль:
о Наиболее часто рак груди и простаты
3. Глиоскаркома:
• Редкая глиальная опухоль, часто с поражением твердой мозговой оболочки
• Паренхиматозное объемное образование с гетерогенным характером накопления контраста
4. Лимфома:
• Вовлечение твердой мозговой оболочки при лимфоме может имитировать ГПЦ:
о Объемное образование твердой мозговой оболочки с диффузным характером накопления контраста, часто мультифокальное
о Низкая интенсивность сигнала на Т2-ВИ, обусловленная высокой целлюлярностью
• Вовлечение костей свода черепа наблюдается нечасто
• Участки потери сигнала за счет эффекта потока обычно отсутствуют
5. Нейросаркоидоз:
• Возможны объемные образования, имеющие связь с твердой мозговой оболочкой; часто мультифокальный характер поражения
• Вовлечение костей свода черепа отсутствует
• Характерно контрастирование лептоменинкс
6. Солитарная фиброзная опухоль:
• Хорошо отграниченное от окружающих структур и накапливающее контраст объемное образование, имеющее связь с твердой мозговой оболочкой
• Может наблюдаться сочетание с гиперостозом
• Встречается крайне редко, сообщается о < 20 случаях
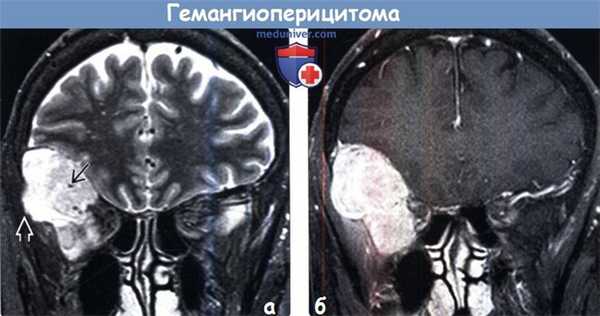
(а) МРТ, Т2-ВИ, режим подавления сигнала от жира, корональный срез: в нижних отделах лобной доли определяются гетерогенное гиперинтенсивное объемное образование с участками потери сигнала за счет эффекта потока в его центральной части, а также эрозия кости, что является характерными признаками гемангиоперицитомы.
(б) МРТ, постконтрастное Т1-ВИ, режим подавления сигнала от жира, корональный срез: у того же пациента определяется диффузный характер контрастирования дольчатого объемного образования. Картина при визуализации имитирует менингиому. КТ может быть полезна для более точного определения эрозии кости. В круг дифференциального диагноза при диагностической визуализации также должны быть включены метастатическое поражение твердой мозговой оболочки и лимфома.
г) Патология:
2. Стадирование и классификация гемангиоперицитомы:
• II степень злокачественности по классификации ВОЗ (grade II)
о IIa: высокая целлюлярность, некротический компонент отсутствует, < 5 митозов/10 полей при микроскопии с высоким разрешением (ПМВУ)
о IIb: высокая целлюлярность, некротический компонент отсутствует, > 5 митозов/10 ПМВУ
• III степень злокачественности по классификации ВОЗ (grade III):
о Высокая целлюлярность, некротический компонент, > 5 митозов/10 ПМУ
3. Макроскопические и хирургические особенности:
• Крайне богатая васкуляризация с тенденцией к кровотечению при оперативном вмешательстве
• Плотное инкапсулированное объемное образование, хорошо отграниченное от окружающих структур и имеющее связь с твердой мозговой оболочкой
• Поверхность среза варьирует от серой до красно-коричневой с видимыми сосудистыми пространствами
4. Микроскопия:
• Гиперцеллюлярная опухоль однообразной структуры со случайно ориентированными округлыми клетками, расположенными в плотной ретикулярной сети
• Характерный сосудистый рисунок по типу «оленьих рогов»:
о Дольки опухолевых клеток окружены широкими ветвящимися капиллярами
• Иммуногистохимия: антитела к фактору XIIIa, Leu-7 и CD34 могут быть полезны при дифференциальном диагнозе с другими опухолями:
о Виментин-позитивность
о Антиген эпителиальной мембраны (АЭМ), S100-негативность
• Выраженная митотическая активность, медиана индекса Ki-67 (MIB-1): 5-10%
д) Клиническая картина:
1. Проявления гемангиоперицитомы:
• Наиболее частые признаки/симптомы:
о Головная боль
• Другие признаки/симптомы:
о Связаны с локализацией опухоли: очаговая неврологическая симптоматика, судороги
2. Демография:
• Возраст:
о Обычно возникает на 4-6 десятке лет, средний возраст - 43 года
о Встречается в любом возрасте, у детей нечасто
• Пол:
о Легкая предрасположенность у мужского пола
• Эпидемиология:
о Составляет < 1 % от первичных опухолей ЦНС (- 0,4%)
о Составляет 2-4% от всех опухолей мозговых оболочек
о Соотношение частоты ГПЦ к менингиомам = 1:50
3. Течение и прогноз:
• Часто возникают локальные рецидивы (50-90%):
о Обычно в пределах 40-70 месяцев
о Вероятность рецидива втечение пяти лет-65%, 12лет-90%
• Часто внечерепное метастатическое поражение (до 30%):
о Обычно печень, легкие, лимфатические узлы, кости
о Медиана показателя выживаемости при метастатическом поражении: два года
• Осложнения:
о Инвазия синусов твердой мозговой оболочки, костей и черепных нервов
о Кровоизлияние (редко)
• Может вызывать онкогенную остеомаляцию:
о Редкий паранеопластический синдром, связанный с мезенхимальными опухолями
• Пятилетняя выживаемость увеличилась (до 93%)
• Тотальная резекция и адъювантная лучевая терапия увеличивают общую выживаемость
е) Диагностическая памятка:
1. Обратите внимание:
• Эрозия кости наиболее часто наблюдается при метастатическом поражении, но может быть признаком гемангиоперицитомы (ГПЦ)
• Симптом дурального «хвоста» неспецифичен и гораздо более часто встречается при менингиоме
2. Советы по интерпретации изображений:
• Предполагайте гемангиоперицитому (ГПЦ) при обнаружении у «менингиомы» атипичных признаков (выраженная эрозия кости, множественные участки потери сигнала за счет эффекта потока)
ФГБУ "НИИ нейрохирургии им. акад. Н.Н. Бурденко" РАМН, Москва
ФГБНУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко», Москва, Россия
ФГУ "НКЦ оториноларингологии" ФМБА России
ФГКУ "Центральный клинический военный госпиталь" ФСБ России, Москва
Редкое наблюдение гигантской гемангиоперицитомы
Приводится пример успешного лечения больного с гигантской интракраниальной гемангиоперицитомой. Гемангиоперицитомы являются агрессивными опухолями с высокой частотой рецидивирования и отдаленного метастазирования. Хотя эти опухоли и относятся к злокачественным новообразованиям, они часто достигают больших размеров при незначительных клинических проявлениях. Хирургический метод лечения до настоящего времени остается основным в лечении данных новообразований.
Менингеальные гемангиоперицитомы (ГП) являются агрессивными опухолями с высокой частотой рецидивирования и отдаленного метастазирования. Хотя эти опухоли и относятся к злокачественным новообразованиям, они часто достигают больших размеров при незначительных клинических проявлениях. Хирургический метод лечения до настоящего времени остается основным в лечении данных новообразований.
ГП является злокачественной опухолью, происходящей из перикапиллярных клеток, или перицитов Циммермана. Эти опухоли обычно возникают в нижних конечностях, тазу и забрюшинном пространстве.
Внутричерепные ГП редки, поскольку они составляют 2-4% всех менингеальных опухолей и менее 1% всех внутричерепных опухолей.
Согласно последней международной классификации опухолей мягких тканей и костей ВОЗ 2013 г. [25, 26], ГП включены в качестве гистологического варианта в единую нозологическую форму - экстраплевральную солитарную фиброзную опухоль под названием «солитарная фиброзная опухоль с преобладанием гемангиоперицитарно подобного сосудистого компонента». Термин «гемангиоперицитома» рассматривается как устаревший синоним.
Несмотря на это, мы, учитывая локализацию процесса и основываясь на ныне действующей классификации опухолей ЦНС ВОЗ от 2007 г., анализируя ретроспективно источники литературы, посвященные опухолям, ранее диагностированным как ГП, оставляем за собой право использования этого термина в настоящей работе.
Больной П., 40 лет, поступил 13.03.09 в ФГКУ «Центральный военный клинический госпиталь» ФСБ России с жалобами на двустороннее снижение зрения, двоение, выраженную постоянную головную боль преимущественно в лобно-теменных областях.
По данным медицинских документов и со слов больного, начало заболевания с декабря 2008 г., когда появилась головная боль. В дальнейшем, в течение 1 мес развились зрительные нарушения - диплопия, концентрическое сужение полей зрения.
В январе 2009 г. при диспансеризации осмотрен офтальмологом, выявлен застой на глазном дне, направлен на стационарное лечение и обследование в лечебное учреждение по месту жительства. При обследовании диагностировано гигантское объемное образование левой гемисферы головного мозга, предположительно менингиома области переднего наклоненного отростка левого крыла основной кости. Для продолжения обследования и лечения госпитализирован в отделение нейрохирургии ЦКВГ ФСБ России, где при дообследовании диагноз подтвержден, начата противоотечная и дегидратационная терапия кортикостероидами.
При обследовании патологии внутренних органов не обнаружено. Больной в сознании, контактен. Критика к своему состоянию и к окружающему снижена. На вопросы отвечает адекватно, но периодически с элементами копролалии. Неврологический статус: не доводит глазные яблоки кнаружи влево, парез взора вверх, аккомодация отсутствует, лицо асимметричное, правый угол рта опущен. Мышечная сила в руках и ногах достаточная - 5 баллов с двух сторон. Сухожильные рефлексы повышены, анизорефлексия с повышением сухожильных рефлексов справа с расширением рефлексогенных зон. Клонусы надколенников и стоп, больше справа. Положительные симптомы Оппенгейма и Пуссепа слева. Симптом Маринеску-Радовичи с обеих сторон. Дистальный гипергидроз. Осмотр окулиста: VIS OS = 0,9, VIS OD = 1,0. Поля зрения: концентрическое сужение полей зрения до 20-30° справа от точки фиксации и до 30-40° слева от точки фиксации, абсолютные парацентральные скотомы обоих глаз. Глазное дно: диски зрительных нервов гиперемированы, отечны, границы смазаны, проминируют в стекловидное тело, перипапиллярно - отек, мелкие кровоизлияния, экссудаты, артерии резко сужены, спазмированы; вены расширены с разрывами, экссудацией. Застойные диски зрительных нервов обоих глаз.
При тотальной селективной каротидной ангиографии (КАГ) выявлено гиперваскуляризированное образование передней и средней черепной ямок слева, размером 7×7 см, питающееся ветвями левых средней мозговой артерии (СМА), наружной сонной артерии (НСА), интракраниального сегмента внутренней сонной артерии (ВСА). Венозные синусы проходимы, без признаков тромбоза (рис. 1).
Рисунок 1. Селективная КАГ(S). Гиперваскуляризированное образование передней и средней черепной ямок слева, размером 7×7 см, питающееся ветвями левых СМА, НСА, интракраниального сегмента ВСА. Венозные синусы проходимы, без признаков тромбоза.
При КТ головного мозга преимущественно в левой лобно-височно-теменной области определяется крупное объемное образование с достаточно четкими бугристыми контурами размером 78×76×64 мм, в базальных отделах прорастающее в правую лобную долю на 10-12 мм. Образование интимно прилежит к сифону левой ВАС, дну передней черепной ямки и к переднему бугорку турецкого седла, кости, образующие дно передней черепной ямки, «изъедены». Образование компримирует передние отделы левого бокового желудочка и, вероятно, распространяется в его просвет. При внутривенном контрастном усилении образование несколько неравномерно накапливает контрастный препарат (до +60 - +85 Ед. Хаунсфильда). К образованию подходит множество артериальных сосудов диаметром до 2-3 мм, преимущественно с медиальной и передней сторон образования. Определяется незначительно выраженный перифокальный отек (максимально до 7 мм у латерального края образования в левой височной области) (рис. 2).
Рисунок 2. КТ с контрастным усилением до операции. а - аксиальная проекция; б - фронтальная проекция. В левой лобно-височно-теменной области определяется крупное объемное образование с достаточно четкими бугристыми контурами размером 78×76×64 мм, в базальных отделах прорастающее в правую лобную долю на 10-12 мм. Образование компримирует передние отделы левого бокового желудочка и, вероятно, распространяется в его просвет, образование неравномерно накапливает контрастный препарат. Определяется незначительно выраженный перифокальный отек.
25.03.09 произведена операция. Осуществлен дугообразный разрез в левой лобно-теменно-височной области. Произведен расширенный птериональный доступ. Экстрадурально осуществлена резекция наружных отделов левого крыла основной кости. Твердая мозговая оболочка (ТМО) резко напряжена, выбухает, пульсация головного мозга не определяется. ТМО вскрыта по наружному краю базальных отделов левой лобной доли. Дальнейший ход операции с использованием операционного микроскопа и микрохирургического инструментария. Отведена от основания черепа лобная доля. Обнаружена ярко-розового цвета отграниченная от вещества головного мозга мелкобугристая опухоль, мягкая, легко кровоточивая - по виду больше похожа на параганглиому, чем на менингиому. Кровотечение интенсивное (алая кровь), гемостаз произведен при помощи придавливания опухоли ватниками с перекисью водорода. Возникло острое набухание и вспучивание мозга с грибовидным выбуханием его в дефект ТМО. Проведены противоотечные мероприятия. После устойчивого уменьшения напряжения и выбухания мозга возобновлены микрохирургические действия. Опухоль довольно легко фрагментировалась и удалялась обычным вакуумным отсосом. Часть опухоли отправлена на срочное гистологическое исследование, предварительный результат - менингиома смешанного строения. В основном опухоль гомогенная, кровоточивая, лишь в медиально-базальных отделах опухоль по строению напоминает бугристую с плотной стромой ячеистую менингиому, где имеет более отчетливо сформированные сосуды в строме и бо`льшую плотность. Кровоснабжение опухоли осуществлялось преимущественно из переходных пиальных сосудов, в связи с чем при удалении опухоли по границе с веществом головного мозга сопровождалось особенно интенсивным кровотечением. Матрикс опухоли обнаружен в медиальных отделах крыла основной кости на границе с передним наклоненным отростком, где стромальная структура опухоли наиболее выражена. ТМО в этой области узурирована, кровоточива, тщательно коагулирована. Опухоль удалена радикально. Визуализирована левая ВСА в супраклиноидном отделе, бифуркация ВСА, начальные сегменты СМА и передней мозговой артерии. Окончательный гемостаз аппликацией кровоостанавливающей ваты Суржицель. Появилась отчетливая пульсация мозга. Мозг расправился, частично запал. Анатомических повреждений мозгового вещества вследствие тракции мозга не произошло. ТМО без натяжения ушита непрерывным швом атравматической нитью. Костный лоскут уложен на место, фиксирован костным швом. Послойное ушивание раны. Интраоперационная кровопотеря около 3500 мл.
Гистологический диагноз: исследование, проведенное в условиях ЦКВГ ФСБ России, - менингиома смешанного строения, отмечается плотное расположение клеток, очаги некрозов и фигуры митозов не определяются.
После иммуногистохимического исследования в лаборатории нейроморфологии НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН: гемангиоперицитома, выраженная экспрессия Vim, CD 34, Factor XIII, ИМ пролиферативного маркера Ki-67 очагово более 5%, Grade III (рис. 3).
Рисунок 3. Микропрепараты опухоли. х400. а - гемангиоперицитома типичного строения с немногочисленными митозами, б - экспрессия CD 34 в клетках гемангиоперицитомы; в - ядерная экспрессия Ki-67 в опухоли. Окраска гематоксилином и эозином.
Послеоперационный период осложнился правосторонней плевропневмонией, формированием эпидуральной гидромы в области операции, сохранялся цефалгический синдром. Получал комплексную терапию: восполнение послеоперационной кровопотери (трансфузия эритроцитной массы - общий объем 1745 мл и свежезамороженной плазмы - 4900 мл), антибактериальную терапию, санационные люмбальные пункции, противоотечную терапию. Посевы ликвора - стерильны, роста нет. Рана зажила первичным натяжением. В ближайшем послеоперационном периоде отмечен регресс общемозговой и очаговой неврологической симптоматики, регресс психических нарушений.
КТ с контрастным усилением в 1-е сутки после операции не выявила участков патологического накопления контраста. Опухоль удалена радикально (рис. 4).
Рисунок 4. КТ с контрастным усилением. 1-е сутки после операции. а - аксиальная проекция; б - фронтальная проекция. Опухоль удалена радикально, геморрагических осложнений в ложе удаленной опухоли нет.
При контрольных КТ и МРТ с контрастным усилением через 5 мес после операции нет признаков рецидива (рис. 5).
Рисунок 5. КТ с контрастным усилением в аксиальной проекции (а) и МРТ с контрастным усилением в аксиальной (б) и фронтальной (в) проекциях. 5 мес после операции (признаков рецидива опухоли нет).
Однако, учитывая гистологию, радиологами НИИ нейрохирургии РАМН рекомендовано проведение по месту жительства лучевой терапии на область удаленной опухоли в суммарной очаговой дозе (СОД) 56 Гр.
Катамнез у больного прослежен в течение 5 лет. Рецидива опухоли нет.
Термин «гемангиоперицитома» впервые применили А. Stout, М. Murray [23] в 1942 г. для описания новообразования, расположенного в забрюшинном пространстве и состоящего преимущественно из пролиферирующих перицитов.
Менингеальные ГП впервые описаны в 1928 г. Р. Bailey и соавт. [2] и считались ангиобластическим вариантом менингиом. Иммуногистохимические, ультраструктурные и генетические исследования впоследствии показали полное отличие ГП от всех других типов менингиом [12, 18]. В последней классификации ВОЗ (2007) опухолей центральной нервной системы ГП отнесены к мезенхимальным неменинготелиальным опухолям и подразделяются на две степени злокачественности: II и III по пролиферативному потенциалу [14]. ГП состоит из мелких овальных клеток с большим количеством тонкостенных сосудов различного калибра, имея характерный сосудистый рисунок в виде «оленьего рога» [18]. Многие авторы указывают на наличие характерных нейрорентгенологических и ангиографических особенностей ГП. В отличие от менингиом большинство ГП имеет многодольчатое строение с нечеткими границами и инфильтрацией окружающей мозговой ткани, без гиперостоза, костных эрозий и кальцификатов. Также отмечается наличие перифокального отека. Кровоснабжение ГП осуществляется преимущественно из ветвей ВСА и задней мозговой артерии в отличие от менингиом, которые питаются в основном из оболочечных артерий НСА. Некоторые авторы [10, 16] отмечают наличие большого количества мелких штопорообразных сосудов в строме и выраженную сосудистую сеть, что является отличительной особенностью ГП.
Предоперационная эмболизация питающих сосудов опухоли, по данным литературы [11], является эффективной в уменьшении кровоснабжения, но, учитывая особенности кровоснабжения ГП, это не всегда возможно.
В настоящее время хирургия расценивается как основной метод лечения менингеальных ГП [10, 13, 15]. Частота «локальных» рецидивов высока даже после радикального удаления ГП, у некоторых авторов [15] данный показатель достигал 50%. Послеоперационная лучевая терапия уменьшает частоту рецидива ГП [19-21, 24]. В случаях труднодоступной локализации опухолей предпочтительна «щадящая» операция в комбинации с послеоперационной лучевой терапией [22]. Наиболее эффективная СОД составляла, по мнению большинства авторов [8, 9, 19, 20], 50-60 Гр.
Химиотерапия была неэффективна в лечении пациентов с менингеальными ГП [8]. По данным Е. Galanis и соавт. [8], только у 1 из 7 больных была положительная динамика при проведении химиотерапии доксорубицином. Однако некоторые авторы [1] сообщают об эффективности использования комбинации ифосфамида и эпирубицина.
Анализ настоящего клинического наблюдения и данных мировой литературы указывает на эффективность хирургического удаления менингеальных ГП как первого и основного метода лечения.
Особенностью данного клинического наблюдения является то, что опухоль достигла гигантских размеров с минимальными клиническими проявлениями. Несмотря на тщательное дообследование, крайне сложно представлялась постановка правильного клинического диагноза до операции.
Учитывая богатую васкуляризацию ГП, основным условием успешного хирургического лечения и исключения послеоперационного геморрагического осложнения является радикальное удаление опухоли. Лучевая терапия является вспомогательным методом лечения после хирургии. В сомнительных случаях установления гистологического диагноза при световой микроскопии необходимым условием для точного диагноза является проведение иммуногистохимического исследования.
Комментарий
Труднодиагностируемые и достаточно редко встречающиеся гемангиоперицитомы (ГП) головного мозга являются злокачественными опухолями, нередко напоминают по своим ocновным характеристикам церебральные менингиомы, но обладают высокой частотой рецидивирования и отдаленного метастазирования.
В данной работе приведено интересное клиническое наблюдение гигантской интракраниальной ГП в нейрохирургическом отделении госпиталя ФСБ: подробно описано клиническое наблюдение, анализированы как жалобы больного, так и динамика развития клинических проявлений, представлены данные объективного неврологического осмотра, причем клинический синдром напоминал таковой, встречающийся при базальных менингиомах с исходным ростом из области наклоненного отростка. Приведены данные объективных нейровизуализованных исследований - КТ с контрастным усилением и тотальной селективной каротидной ангиографии - все хорошо иллюстрировано фотографиями.
Далее подробнейшим образом (и это очень поучительно) представлена по этапам произведенная хирургическая операция по удалению опухоли - выбор адекватного хирургического доступа, его детали и техника выполнения, особенности вскрытия твердой мозговой оболочки (ТМО), визуализационные характеристики обнаруженной опухоли, ее структуры, неоднородной в зависимости от различных отделов опухоли. Детально описаны обнаруживаемые по ходу выполнения операции источники кровоснабжения опухоли и пути успешного гемостаза, который был тем не менее упорным, и кровопотеря составила 3 л, принципиально важно уточнено отношение опухоли к магистральным сосудам, в том числе внутренней сонной артерии (ВСА) в супраклиноидном отделе, бифуркация ВСА, системы средней и передней мозговых артерий. Все убедительно и тщательно описано, но хотелось бы видеть и наглядные интраоперационные снимки этапов проведенной операции - их в работе нет. Послеоперационный период протекал с умеренно выраженными осложнениями, которые удалось своевременно и успешно купировать.
В послеоперационном периоде выполнены контрольные исследования - КТ с контрастным усилением, которые убеждают в успешности произведенной операции. Иммуногистохимическое исследование, проведенное в условиях Института нейрохирургии, уточнило диагноз и степень злокачественности опухоли - Grade III - впоследствии проведена лучевая терапия, катамнез больного прослежен в течение 5 лет, не выявлено рецидивирования опухоли.
В конце работы приведено краткое обсуждение проблемы с анализом данных литературы в историческом аспекте. Подчеркивается, что в отличие от менингиом головного мозга основное кровоснабжение осуществляется из ветвей ВСА и задней мозговой артерии, а не менингеальных артерий. Вследствие выраженной васкуляризации ГП предоперационно по возможности следует выполнять эмболизацию питающих сосудов.
В заключение авторы подчеркивают несомненную значимость хирургического лечения данных опухолей как основы лечебного процесса, и при необходимости выполняется лучевая терапия.
Статья весьма интересная, познавательная, особенно для современных практикующих нейрохирургов. Она отражает актуальные тенденции в поисках оптимальных путей совершенствования техники микрохирургических операций по удалению таких сложных опухолей, как гемангиоперицитомы.
Многопрофильный медицинский центр GMS Clinic, Москва, Россия
Российский онкологический научный центр им. Н.Н. Блохина, Москва
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» РАМН, Москва
НИИ КО ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, Москва, Россия
Редкое наблюдение злокачественной гемангиоперицитомы малого таза
Журнал: Онкология. Журнал им. П.А. Герцена. 2015;4(2): 64‑70
Алиев В.А., Мусаев Э.Р., Татаев И.Ш., Феденко А.А., Овчинникова А.И., Кочура Н.А., Давыдов М.М. Редкое наблюдение злокачественной гемангиоперицитомы малого таза. Онкология. Журнал им. П.А. Герцена. 2015;4(2):64‑70.
Aliev VA, Musaev R, Tataev ISh, Fedenko AA, Ovchinnikova AI, Kochura NA, Davydov MM. Experience in treating a patient with a malignant small pelvic hemangioperocytoma. P.A. Herzen Journal of Oncology. 2015;4(2):64‑70. (In Russ.).
Представлено редкое наблюдение успешного комплексного лечения больного с злокачественной гемангиоперицитомой малого таза. На первом этапе проведена неоадъювантная химиотерапия с последующей радикальной операцией в объеме цилиндрической брюшно-промежностной экстирпации прямой кишки. Продемонстрированы клиническая картина и особенности данного редкого заболевания, а также этапы хирургического вмешательства.
Гемангиоперицитома относится к неэпителиальным опухолям малого таза (синонимы: перицитома, перителеома, лимфангиперицитома, периваскулярная гемангиоэндотелиома). Это редкие злокачественные периваскулярные опухоли, частота которых не превышает 1% от числа сосудистых опухолей [1]. Опухоль состоит из малодифференцированных гладкомышечных клеток, прилегающих к стенкам капилляров и регулирующих их размер. Некоторые авторы рассматривают перициты как источник двух близких опухолей — гемангиоперицитомы и гломанангиомы. Как показывают ультраструктурные исследования, перициты обнаруживаются в стенках капилляров и венул. Они имеют длинные выросты, окружающие сосуд и образующие прерывистый слой между эндотелием и адвентициальной соединительной тканью. Обычно только базальная мембрана отделяет эндотелий от перицитов [2].
Возникает эта опухоль в любом возрасте — от 3 дней жизни до 92 лет, чаще у лиц в возрасте 38—58 лет, с одинаковой частотой у представителей обоих полов. Дифференциальный диагноз следует проводить с саркомой Капоши, ангиолейомиобластомой, фибросаркомой, ангиосаркомой, гломус-ангиомой Баре—Масона, сосудистой лейомиомой, саркомой Юинга [5].
Гемангиоперицитома чаще всего поражает кожу и подкожную жировую клетчатку (34,5%), скелетные мышцы нижних конечностей (24,5%), забрюшинное пространство (24%), область головы и шеи (17%). Опухоль может локализоваться всюду, где имеются капилляры, включая ротовую полость, средостение, забрюшинное пространство [6].
Обычно опухоль имеет овальные и округлые очертания, состоит из отдельных узлов плотноэластической консистенции, серовато-белого или насыщенно-синюшного цвета (в зависимости от степени васкуляризации). С течением времени узлы могут изъязвляться и легко кровоточить. Обычно гемангиоперицитома — солитарная опухоль, реже бывает множественной, сгруппированной на сравнительно небольшом участке тела. Растут опухоли обычно медленно, в редких случаях достигая большого размера, без каких-либо клинических проявлений. Клинические проявления, как правило, связаны со сдавлением опухолью прилежащих органов. В одних случаях возникают явления кишечной непроходимости, в других — дизурические расстройства. Боль возникает в случае сдавливания опухолью нервов.
Возможны эндокринные (гипогликемия) [7], неврологические нарушения, сосудистые изменения (телеангиэктазии, варикозное расширение вен прямой кишки).
Заболевание имеет относительно медленное течение (5—12 лет), но описаны случаи быстрого прогрессирования. Рецидивирование опухоли возможно через много лет после удаления опухоли.
Частота метастазирования при гемангиоперицитоме колеблется от 11,7 до 56,5%. Сроки наблюдения от начала установки диагноза и до обнаружения метастазов составляют от 1 года до 14 лет, в среднем 4,5 года. Наиболее часто опухоль метастазирует в печень, легкие, лимфатические узлы. По данным ряда авторов, летальность в сроки от 3—5 до 15—20 лет колеблется от 23 до 47,8%.
Клиническое наблюдение
Пациент М., 37 лет, обратился с жалобами на боль в малом тазу, иррадиирущую в крестец, тяжесть внизу живота.
Считает себя больным с января 2011 г., когда появились болезненные ощущения в нижних отделах живота и промежности. С марта 2011 г. стал отмечать усиление боли, по поводу чего обратился в одну из городских клиник Москвы, где выявили опухоль малого таза (рис. 1).
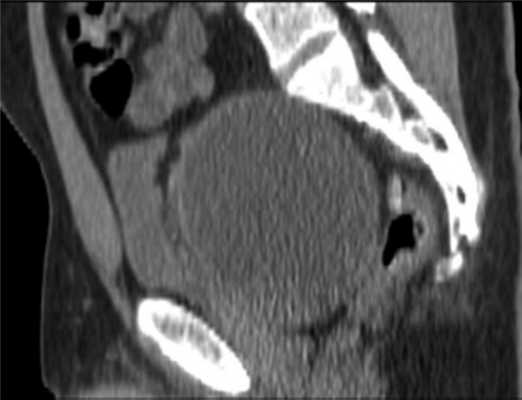
Рис. 1. МР-томограмма малого таза. Опухоль малого таза.
11.04.2011 была выполнена лечебно-диагностическая лапаротомия, удаление опухоли малого таза. При гистологическом исследовании операционного материала выявлена злокачественная шваннома.
В дальнейшем пациент находился под динамическим наблюдением по месту жительства. В январе 2012 г. появились жалобы на боль в промежности.
Больной направлен в ФГБУ «РОНЦ им. Н.Н. Блохина» РАМН, где был диагностирован рецидив опухоли в малом тазу.
Выполнено иммуногистохимическое исследование гистологических препаратов от 11.04.2011: морфоиммуногистохимическая характеристика опухоли соответствует гемангиоперицитоме, на основании чего установлен диагноз: злокачественная гемангиоперицитома малого таза T2bN0M0 G3. Состояние после хирургического лечения от 11.04.2011 — рецидив. В январе 2012 г. прогрессирование. При поступлении состояние относительно удовлетворительное.
При пальцевом исследовании прямой кишки сразу за анусом, внекишечно, пальпируется неподвижное опухолевое образование, занимающее практически весь малый таз, прямая кишка циркулярно сужена с выраженным болевым синдромом, однако слизистая оболочка прямой кишки не изменена.
По данным магнитно-резонансной томографии (МРТ) от 10.02.2012, в полости малого таза пресакрально располагается опухоль размером 9,2×9×7 см. Верхний полюс ее на уровне тела S I позвонка, распространяется в параректальную клетчатку, тесно прилежит к прямой кишке, оттесняя ее влево (граница прослеживается). Нельзя исключить прорастание в кишку, стенки прямой кишки отечны. Опухоль прилежит к семенным пузырькам и предстательной железе (граница прослеживается); мочевой пузырь оттеснен кпереди и кверху; верхний полюс опухоли расположен между грушевидными мышцами, прилежит к передней поверхности крестца и копчика (граница прослеживается), нижний полюс опухоли расположен между волокнами мышцы, поднимающей задний проход; нижние ягодичные сосуды справа оттеснены кпереди, тесно прилежат к опухоли на протяжении 3 см (рис. 2).
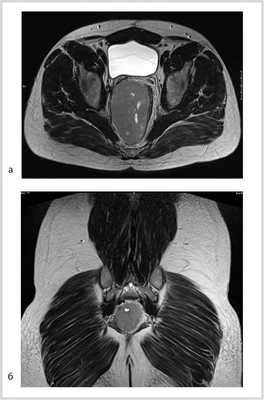
Рис. 2. МР-томограммы малого таза. Пресакрально располагается опухоль размером 9,2×9×7 см. а — сагиттальный срез; б — фронтальный срез.
Учитывая данные иммуногистохимического исследования (G3, количество митозов >30%) и местный рецидив опухоли, больной консультирован химиотерапевтом из группы лечения сарком и радиологом, после чего решено провести неоадъювантную полихимиотерапию.
Проведено 6 курсов полихимиотерапии по схеме HD AI (препараты: ифосфамид 2000 мг/м 2 в/в в 1—5-й день, СД =20 000 мг; месна 2000 мг/м 2 в/в в 1—5-й день, СД =20 000 мг; доксорубицин 60 мг/м 2 в/в в 1-й день, СД =120 мг; нейпомакс по 300 мкг п/к в 6—15-й день).
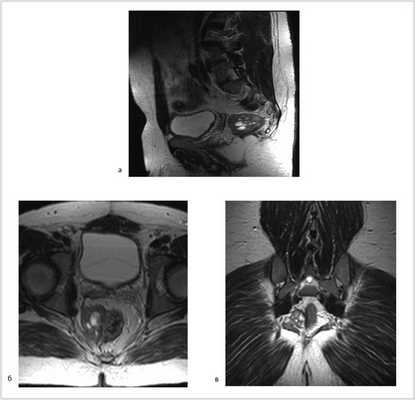
Рис. 3. МР-томограммы малого таза. Опухоль уменьшилась в размере до 5,5×3,5×4 см, однако тесно прилежит к правой стенке прямой кишки. а — аксиальный срез; б — сагиттальный срез; в — фронтальный срез.
По данным ультразвукового исследования компьютерной томографии брюшной полости и рентгенографии органов грудной клетки отдаленных метастазов не выявлено.
В отделении проведен повторный консилиум с участием химиотерапевтов саркомной группы, хирургов сакральной группы, а также сотрудников отделения онкопроктологии. Учитывая нерадикальность предыдущей операции по поводу неэпителиальной опухоли малого таза, положительную динамику на фоне полихимиотерапии в виде уменьшения размера опухоли (более чем в два раза), а также молодой возраст пациента, принято решение вторым этапом выполнить оперативное вмешательство в объеме цилиндрической (экстралеваторной) брюшно-промежностной экстирпации прямой кишки, предложенной австрийским хирургом Т. Holm в 2007 г.
07.11.2012 выполнена цилиндрическая или экстралеваторная экстирпация прямой кишки. Через тазовую брюшину в мезоректальной клетчатке справа пальпируется верхний полюс опухоли, подрастающей к стенке прямой кишки, опухоль фиксирована к правой боковой стенке таза. Отдаленных метастазов нет (рис. 4).
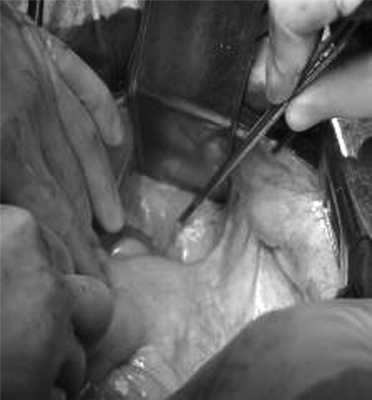
Рис. 4. Этап операции. Ревизия опухоли.
Произведена мобилизация прямой кишки по левой и задней полуокружности, а также пресакрально до мышц тазового дна с соблюдением всех онкологических правил (рис. 5). По левой боковой стенке таза опухолевая капсула интимно прилежит к внутренней подвздошной вене и артерии, острым путем последняя мобилизована от магистральных сосудов.
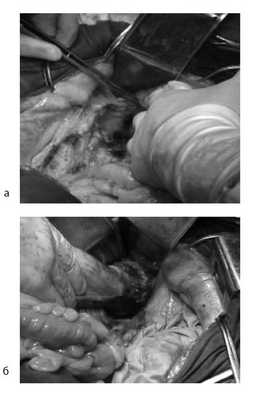
Рис. 5. Этапы операции. а — мобилизация слева; б — мобилизация справа.
Далее сигмовидная кишка пересечена на уровне ее дистальной трети, а прямая кишка погружена в малый таз, при этом тазовая брюшина ушита над заглушенной культей прямой кишки. Затем сигмовидная кишка забрюшинно выведена в левом боковом отделе живота на переднюю брюшную стенку и сформирована плоская колостома, после чего брюшная полость ушита наглухо послойно (рис. 6).
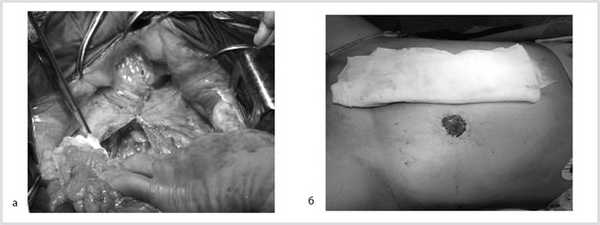
Рис. 6. Этапы операции. а — ушивание тазовой брюшины; б — сигмостома.
Далее больной перевернут на живот в положении по типу «перочинного ножа» (рис. 7).
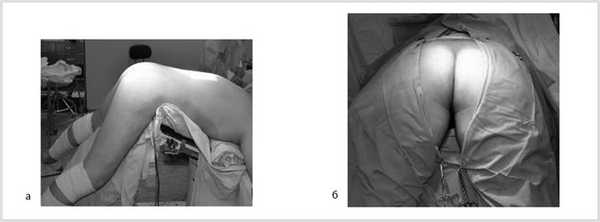
Рис. 7. Положение больного на столе (а). Вид операционного поля промежности (б).
После обработки операционного поля мобилизация прямой кишки продолжена из широкого промежностного доступа. Выполнено ушивание заднего прохода кисетным швом, намечены края резекции. В проекции крестцово-копчикового сочленения кожа и подкожная жировая клетчатка рассечены до задней крестцово-копчиковой связки. Последняя пересечена в поперечном направлении. Выполнена ампутация копчика с последовательным пересечением передней крестцово-копчиковой и крестцово-прямокишечной связок (рис. 8).
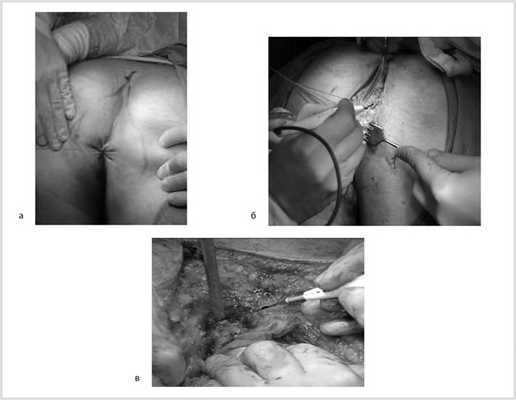
Рис. 8. Этапы операции. а — ушивание ануса; б — рассечение кожи и подкожной жировой клетчатки; в — пересечение крестцово-копчиковых связок.
Далее прямая кишка с опухолью в едином блоке мобилизована острым путем от предстательной железы и правой стенки таза, после чего выполнена цилиндрическая брюшно-промежностная экстирпация прямой кишки. Малый таз дренирован двумя силиконовыми дренажами и ушит наглухо (рис. 9).
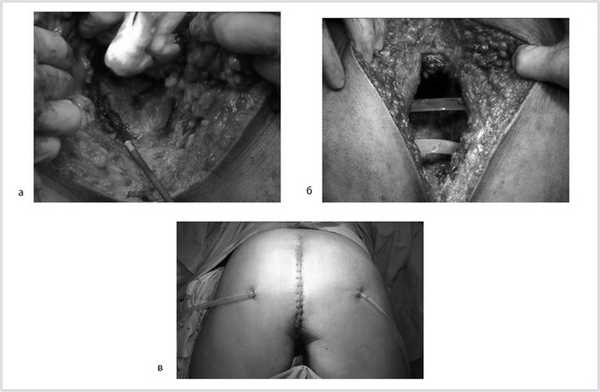
Рис. 9. Этапы операции. а — мобилизация простаты; б — дренирование малого таза; в — конечный вид раны.
Гистологическое заключение: в жировой клетчатке прямой кишки, с учетом иммуногистохимического исследования разрастания злокачественной гемангиоперицитомы с признаками лечебного патоморфоза 1-й степени (жизнеспособной опухолевой ткани более 50% по DWORAK). Опухоль не прорастает в прилежащий мышечный слой кишки. В одном лимфатическом узле прилежащей клетчатки элементов опухолевого роста нет. В краях резекции кишки без элементов опухолевого роста. Под маркировкой «латеральный край опухоли» — кусочек фиброзной ткани с очагами ксантоматоза (рис. 10).
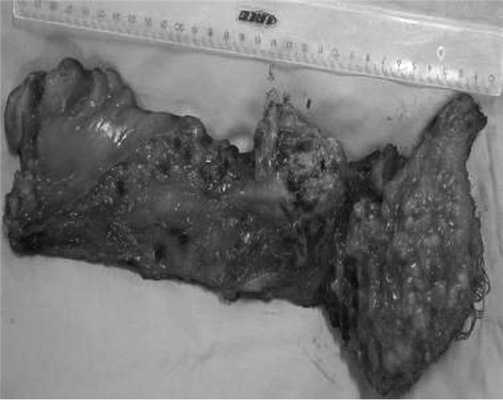
Рис. 10. Макропрепарат.
Продолжительность операции составила 3 ч 30 мин, кровопотеря — 500 мл. Интраоперационных и ранних послеоперационных осложнений не было. Пациент на 12-е сутки выписан из хирургического отделения.
Заключение
Лечение больных с опухолями малого таза представляет собой сложную задачу, ключом к решению которой является мультидисциплинарный подход. В настоящее время нет четких дифференциальных диагностических критериев гемангиоперицитом, сарком и солитарных фиброзных опухолей. Несмотря на то что данные опухоли традиционно считаются радиорезистентными, до недавнего времени при лечении сарком таза часто использовали лучевую или химиолучевую терапию. Сегодня сложно переоценить важность точной диагностики, так как правильный диагноз должен быть установлен лишь на основании иммуногистохимического исследования, которое позволяет прогнозировать ход дальнейшего лечения и прогноз заболевания. В литературе имеются лишь единичные наблюдения хирургического лечения гемангиоперицитом малого таза. На наш взгляд, радикальное хирургическое вмешательство — основной метод лечения больных с гемангиоперицитомой. Однако при местно-распространенной опухоли или в случае рецидива заболевания, при которых имеется тесная связь опухоли с прилежащими анатомическими структурами малого таза, возможность достижения свободного от опухоли латерального края резекции и радикальности операции становится обоснованно сомнительной. При повторном рецидивировании возможно использование рентгенохирургических технологий, таких как «Кибер-нож». В таких случаях коллегиальное обсуждение с участием хирургов, химиотерапевтов и лучевых терапевтов становится залогом успешного лечения больного.
В данном клиническом наблюдении продемонстрировано успешное комплексное лечение больного со столь редкой патологией. На наш взгляд, хотя проведенное предоперационное лечение было эффективным, выполнение экстралеваторной брюшно-промежностной экстирпации, явилось ключевым элементом радикального лечения больного.
Читайте также:
