Специфическая противовирусная защита. Иммуноглобулины.
Добавил пользователь Дмитрий К. Обновлено: 30.01.2026
Кондратенко И.В. * , Заплатников А.Л. ** , Бологов А.А. *
* РДКБ, Москва, Кондратенко Ирина Вадимовна, д.м.н., профессор
* РДКБ, Москва, Бологов Андрей Анатольевич, к.м.н., зам. главного врача по лечебной работе
** РМАПО, кафедра педиатрии, Заплатников Андрей Леонидович, д.м.н., профессор
Недостаточность иммуноглобулинов, и связанные с этим нарушения противоинфекционной резистентности возникают при первичных (генетически детерминированных) иммунодефицитах и вторичных иммунодефицитах, возникающих при воздействии неблагоприятных факторов на организм. Такими неблагоприятными факторами могут быть химио- и радиотерапия злокачественных новообразований, иммуносупрессивная терапия в трансплантологии, потеря белков плазмы и иммунокомпетентных клеток при кровопотерях, операциях, ожоговой болезни; воздействие эндотоксинов при некоторых инфекционных и паразитарных заболеваниях (4,5,6)
Другими областями применения ВВИГ являются лечение и профилактика определенных вирусных инфекций и лечение аутоиммунных заболеваний [7,8,9].
Существует много различных статей и монографий по применению иммуноглобулинов для внутривенного введения в различных областях медицины. Однако постоянно дискутируются три главных вопроса:
- Когда применять иммуноглобулин?
- Какая доза препарата должна вводиться?
- Какой иммуноглобулин следует выбрать? Есть ли разница между ними?
Для того чтобы ответить на эти вопросы, необходимо определиться с классификацией иммуноглобулинов, представленных на Российском рынке. Для практических целей может быть использована классификация ИГВВ, в основу которой положена особенность антительного состава препаратов. Принято выделять следующие группы ИГВВ:
- Стандартные иммуноглобулины для внутривенного введения - (Интратект,Интраглобин, Октагам, Гамунекс, иммуноглобулин человека нормальный для внутривенного введения и др.).
- Обогащенные иммуноглобулины для внутривенного введения –препараты ИГВВ, содержащие антитела класса IgG и обогащенные антителами класса IgМ и IgА (Пентаглобин).
- Специфические или гипериммунные иммуноглобулины для внутривенного введения – препараты ИГВВ, содержащие антитела класса IgG, при этом против определенных возбудителей концентрация антител значительно выше, чем в стандартных иммуноглобулинах (Неоцитотект, Неогепатект и др.).
- Разный способ производства
- Разный состав
- Разное содержание IgA и IgM
- Разный состав подклассов IgG
- Разные способы и количество стадий инактивации и элиминации вирусов
У иммунобиологических препаратов производственный процесс влияет на качество. Поэтому так важно определиться в выборе препарата при рассмотрении клинической ситуации и быть уверенным в его эффективности и безопасности.
Вирусная безопасность препарата ВВИГ обеспечивается вирусной безопасностью плазмы и совершенством технологии производства. Контроль плазмы осуществляется при обследовании доноров в донорских центрах, карантинизацией с обязательным контрольным обследованием доноров в этот период. В процессе производства обязательна вирусная очистка и вирусная инактивация. Вирусная очистка включает:
- фракционирование этанолом по Кону (уменьшает концентрацию вирусного загрязнения, физически удаляя вирусные частицы);
- методы фильтрации и ультрафильтрации (удаляют оболочечные - гепатиты В,С, ВИЧ и безоболочечные - гепатит А, парвовирус В19 вирусы);
Методы, используемые для вирусной инактивации варьируют у разных производителей: сольвент/детергентный метод, инкубация с низким рН , обработка бета-пропиолактоном, адсорбция на аэросиле, обработка октановой (каприловой) кислотой. Должно быть использовано не менее двух методов. Особое внимание необходимо обратить на гарантии элиминации парвовируса В19.
В противоположность здоровым людям, у которых парвовирусная инфекция манифестирует в виде инфекционной эритемы или полиартропатии, у пациентов группы риска парвовирус В19 может вызвать серьезные нарушения кровообразования, в особенности эритропоэза.
У пациентов с врожденной и/или приобретенной гемолитической анемией или другими заболеваниями, сопровождающимися т.н. «эритропоэтическим стрессом», например, при железодефицитах, кровотечениях, после трансплантации почек или стволовых клеток, инфицирование парвовирусом В 19 может вызвать требующий срочной терапии «временный апластический криз». Он характеризуется утяжелением хронической анемии или на фоне компенсированного гемолиза внезапным появлением анемии с ретикулоцитопенией, сильным снижением или отсутствием эритроидных клеток-предшественников наряду с обнаружением проэритробластов в костном мозге, а также возможно сопровождается нейтропенией и тромбоцитопенией.
В группу риска входят также иммунокомпрометированные пациенты, так как вследствие нарушений гуморального иммунитета и недостаточной способности к элиминации вируса может возникнуть персистирующая инфекция с хронически протекающей парциальной красноклеточной аплазией костного мозга. Это касается пациентов с врожденным или приобретенным иммунодефицитом, пациентов с лимфопролиферативными заболеваниями во время/после химиотерапии и пациентов с ятрогенной иммуносупрессией (например, после высокодозовой химиотерапии и трансплантации стволовых клеток, вследствие аутоиммунных заболеваний, после трансплантации органов). Специфической противовирусной терапии не существует. В этом случае приходится прерывать терапию иммунодепрессантами или цитостатиками. В качестве методов лечения следует применять иммуноглобулины, предварительно убедившись, что они сами не контаминированы парвовирусом (так как обычные методы вирусинактивации не являются эффективными) и имеют специфические антитела против парвовируса.
Помимо хронической анемии у пациентов после аллогенной и аутологичной ТКМ было отмечено поражение парвовирусом внутренних органов. Так, у нескольких пациентов с кожной экзантемой при помощи ПЦР вирус был обнаружен не только в крови, но и частично в коже, у пациента с кардимиопатией – в миокарде, у пациента с гепатитом – в печени, а у пациента с гемолитико-уремическим синдромом – в почке. Летальность, ассоциированная с парвовирусной инфекцией, в данной группе пациентов составила 7%. Поэтому у иммунокомпрометированных пациентов с невыясненной причиной органной недостаточности следует исключать паровирусную инфекцию при помощи ПЦР из биопсийного материала.
Исходя из вышеизложенного, в терапии иммуноглобулинами пациентов из группы риска следует использовать только препараты, абсолютно безопасные с точки зрения передачи парвовируса В19.
Эффективность и переносимость ВВИГ обеспечивается:
- 100% сохранностью Fс фрагментa
- Общим содержание IgG (%): >95%
- Содержанием мономеров и димеров (%): > 90%
- Отсутствием фрагментов
- Распределение подклассов IgG должно соответствовать распределению в нормальной плазме: IgG1-66%, IgG2-23%, IgG3-7%, IgG4-4%
Применение стандартных иммуноглобулинов - IgG.
Основные показания к применению стандартных иммуноглобулинов:
1. Профилактика или заместительная терапия.
Механизм действия заместительной терапии заключается в связывании и нейтрализация микробного антигена, блокировании присоединения вирусов и бактерий к клетке-мишени, опсонизации и инициация поглощения и переваривания вирусов и бактерий фагоцитами, наличием нейтрализующих антител против суперантигенов. Стандартными дозами ВВИГ для заместительной терапии являются 400-500 мг/кг массы тела пациента 1 раз в 3-4 недели (период полураспада IgG). Необходимо обратить внимание на то, чтобы претрансфузионный уровень сывороточного IgG был не менее 4-5 г/л. Хорошее состояние и нормальный претрансфузионный уровень IgG не являются показанием для уменьшения дозы вводимого ВВИГ и/или увеличения интервалов между трансфузиями. Для заместительной терапии используют только препараты стандартных иммуноглобулинов (11, 12). Применение Пентаглобина нерационально и может вызвать серьезные побочные реакции в связи активацией комплемента и образованием IgM содержащих иммунных комплексов (13, 14). Кому же применяется заместительная терапия?
- Больным с первичными иммунодефицитами с нарушениями продукции антител (со сниженным или нормальным содержанием общего IgG),
- При СПИДе у детей с повторяющимися инфекциями
- При аллогенной трансплантация костного мозга
- При развитии гипогаммаглобулинемии на фоне иммуносупрессии
2. Терапия аутоиммунных заболеваний.
Эффект высокодозовой терапии (1-2 г/кг массы тела пациента в течение последовательных 2-3 дней) обеспечивается следующими механизмами (15, 16, 17, 18):
- предоставлением нейтрализующих антител к неизвестному до настоящего времени причинному инфекционному агенту
- подавлением формирования аутоантител по принципу антиидиотипического действия
- блокирование Fc рецепторов IgG на фагоцитирующих клетках
- подавление пролиферации Т-клеток и продукции иммуноглобулинов
- взаимодействие с системой комплемента
- блокирование активации и действия цитокинов
- блокирование экспресс молекул адгезии на эндотелиальных клетках
Препаратами первой линии терапии ВВИГ являются при:
- Синдроме Кавасаки
- Идиопатической тромбоцитопенической пурпуре
- Синдроме Гийена-Барре
- Аутоиммунных полинейропатиях
- Энтеровирусных энцефалитах у пациентов с агаммаглобулинемией
Высокодозовая терапия ВВИГ используется также при:
Рассеянном склерозе, миастении гравис, воспалительных миозитах, системных васкулитах, аутоиммунных цитопениях при системной красной волчанке, аутоиммунных дерматитах, в профилактике спонтанных абортов (лечение антифосфолипидного синдрома), аутоиммунных цитопениях (аутоиммунная нейтропения, аутоиммунная гемолитическая анемия, аллоиммунной неонатальной тромбоцитопении и гемолитической анемии) (19, 20).
За 30 лет применения ВВИГ проведено много рандомизированных, контролируемых исследований, которые достоверно доказали снижение частоты и интенсивности инфекционных осложнений при проведении ежемесячной терапии иммуноглобулином IgG в дозе 250-500 мкг/кг массы тела (21, 22, 23).
Вторая группа – поликлональных ВВИГ, обогащенных IgM и IgA, представлена единственным препаратом, не имеющим аналогов, под торговым названием Пентаглобин. Состав препарата: Ig G = 76%, Ig M = 12% и Ig А=12 %.
Все положительные эффекты данного препарата связаны именно с наличием в их структуре иммуноглобулина М и иммуноглобулина А.
Пентаглобин разработан для лечения распространенных тяжелых бактериальных инфекций за счет специфических функций, которыми обладают иммуноглобулины классов А и М.
Основным показанием к клиническому применению Пентаглобина является адъювантная терапия бактериальных инфекций. Преимущество Пентаглобина перед стандартными ВВИГ в терапии сепсиса доказано многочисленными клиническими исследованиями. Вначале проводились оригинальные, рандомизированные клинические исследования, а с 2001 года начали проводиться мета-анализы для получения более достоверных с точки зрения статистики данных, которые объединяют качественные клинические исследования и оценивают эффективность адъювантной терапии иммуноглобулинами. Все они показали преимущества Пентаглобина и подтверждены международными экспертами 28. Один из ведущих специалистов в области интенсивной терапии профессор Werdan K в 2007 году провел мультицентровое исследование SBITS (30) с целью доказательства эффективности применения стандартных иммуноглобулинов (IgG) в лечении сепсиса у взрослых больных. Протокол был опубликован до начала исследования и послужил основой для последующей дискуссии о методологии клинических исследований по сепсису. Результаты работы были опубликованы в одном из самых авторитетных журналов по интенсивной терапии Critical Care Medicine. В группу IgG было включено 321 пациент, в контрольной группе (плацебо альбумин) было 303 больных.
Летальность в группе IgG составила 39,3%, а группе альбумина 37,3%.
Ожидания исследователей не оправдались: у взрослых пациентов с сепсисом не произошло статистически достоверного снижения летальности. Авторы сделали вывод, что стандартные иммуноглобулины IgG не должны использоваться в качестве адъювантной терапии сепсиса.
По мнению международных экспертов, это исследование превосходит все проведенные прежде исследования как по качеству, так и по числу включенных пациентов, и должно рассматриваться как знаковое в этой области.
Таким образом, пентаглобин является первым и единственным препаратом, который воплощает естественные, природные принципы физиологической защиты организма человека:
- Содержит широкий спектр антител против клинически релевантных микроорганизмов комплемент - опосредованного уничтожения микроорганизмов и повышения фагоцитарной активности моноцитов/макрофагов и гранулоцитов.
- Модулирует cиcтемные чрезмерные реакции воспаления и результате ингибирования провоспалительно действующих цитокинов и стимуляции высвобождения их антагонистов
- Модулирует воспалительное действие комплемента за счет нейтрализации факторов комплемента С3b и C4b, и тем самым комплемент - опосредованного разрушения клеток
Терапия Пентаглобином является «золотым стандартом» лечения сепсиса и септического шока.
Третья группа – специфические гипериммунные иммуноглобулины. К ним относятся антицитомегаловирусный ВВИГ - Неоцитотект (цитотект) и иммуноглобулин, обогащенный антителами к HBs – Неогепатект. Оба этих иммуноглобулина готовятся из плазмы специально отобранных доноров, с исходно более высоким, чем общепопуляционный, титром специфических антител.
Распространенность инфицирования ЦМВ в развитых странах составляет 50 – 80% у взрослых и 65% у детей школьного возраста. Риск манифестации симптоматической инфекции возрастает во время беременности, у новорожденных и при иммунной недостаточности (врожденных иммунодефицитах, после транплантации органов и костного мозга. Показания к применению Неоцитотекта - лечение активной цитомегаловирусной инфекции (ЦМВИ) у иммунокомпрометированных пациентов, у беременных женщин с целью снижения риска антенатальной передачи вируса и поражения плода (31), для лечения активной ЦМВИ у новорожденных и детей раннего возраста (12, 32), для профилактики манифестации заболевания у инфицированных больных в трансплантологии.
Режим дозирования: лечение активной инфекции 1 – 2 мл на кг массы тела каждые 48 часов 3 – 5 введений или до исчезновения клинических симптомов; профилактика реактивации – 1 мл/кг массы тела 1 раз в триместр у беременных или 6 раз с интервалом 3-4 недели после трансплантации. Необходимо отметить, что использование иммуноглобулинов совместно с виростатическими препаратами дает лучшие результаты (33).
Применение Неоцитотекта предотвращает развитие вирус-индуцированной лимфопролиферации (34). Результаты ретроспективного анализа более чем 26000 пациентов с трансплантированной почкой выявили стандартизированную частота развития опухоли в 1-й год после операции:
- Пациенты после трансплантации почки без профилактики ЦМВ 26,4
- Пациенты после трансплантации почки с противовирусной терапией 24,2
- Пациенты после трансплантации почки с терапией анти-ЦМВ IgG 0
Неогепатект применятся для профилактики заражения гепатитом В одновременно с вакцинацией у новорожденных, родившихся от матерей вирусоносителей, пациентов, получающих терапию гемодиализом, пациентов, получающих множественные гемотрансфузии; у невакцинированных лиц, при контакте с кровью больного (35, 36, 37, 38, 39, 40). Также Неогепатект вводится лицам, не ответившим на предшествующую вакцинацию при риске заражения. Режим дозирования:
Специфическая противовирусная защита. Иммуноглобулины.
Важным этапом противовирусной защиты является формирование специфических антител (AT). Этот процесс осуществляется В-лимфоцитами, которые после встречи с вирусным агентом дифференцируются либо в зрелую плазматическую клетку, которая секретирует иммуноглобулины только одного класса, представляющие собой специфические антитела, либо в В-клетку памяти. Дифференцировка и пролиферация В-клеток находится под контролем Т-хелперов СД4+. Обычно формируются антитела всех классов. Особый интерес в последние годы вызывают AT класса А, которые, по современным данным, формируют защитный барьер, предохраняющий от адсорбции вирусов всю систему слизистых как респираторного, так и желудочно-кишечного тракта. Доказано, что В-1 клетки, являющиеся источником плазматических клеток, продуцирующих IgA, чаще всего содержатся в плевральной и перитонеальной жидкости и селезенке, но практически отсутствуют в лимфатических узлах и пейеровых бляшках. Наибольшей защитной активностью обладают полимерные варианты IgA. В регуляции синтеза AT класса А активно принимают участие цитокины, переключающие синтез с IgM изотипа на изотип А, а также цитокины, воздействующие на терминальные фазы дифференцировки секреторных IgA+ - В клеток в плазматические клетки, секретирующие IgA. ИЛ-5 и ИЛ-6 усиливают синтез IgA. Помимо способности блокировать прикрепление вируса к клеточной мембране, полимерный IgA даже в низких концентрациях может подавлять внутриклеточную репликацию вируса.
Иммуноглобулин М (IgM) - самый ранний из формирующихся в ответ на вирусную инфекцию иммуноглобулинов, играет главную роль в нейтрализации вируса, которая, по-видимому, является результатом либо связывания вируса со специфическими клеточными рецепторами, либо аггрегации вирусных частиц макроглобулином.
Иммуноглобулин G - доминирует среди иммуноглобулинов во внутренних жидкостях организма, возникает на несколько дней позднее IgM и наряду с ним и IgA участвует в нейтрализации вируса и его токсинов, активирует комплемент.
Иммуноглобулин E - защищает внешние слизистые оболочки организма путем локальной активации факторов плазмы на зффекторных клетках, благодаря индукции воспалительных реакций, ответственен за развитие аллергии.
Иммунный ответ на вирусную инфекцию может также завершаться образованием аутоантител, направленных против нормальных тканей, не зараженных вирусом, что связано с нарушением специфического процесса распознавания "своих" и "чужих" антигенов. К числу физиологических аспектов антителогенеза относят формирование антиидиотипических антител против соединяющейся с антигеном вариабильной части молекулы иммуноглобулина. Полагают, что этот процесс является частью регулирующей системы иммунитета.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Клеточный иммунный ответ. Гуморальный иммунный ответ. Защитные функции иммуноглобулинов ( антител ).
Клеточный иммунный ответ направлен против внутриклеточно паразитирующих микроорганизмов, основная защитная роль в нем принадлежит активированным макрофагам и цитотоксическим лимфоцитам (CD8+ CTL).
Макрофаги, инфицированные микроорганизмами, получают от Thl в качестве сигналов активации цитокины: гамма-интерферон и туморнекротизирующий фактор (ТНФ), которые действуют через свои рецепторы, вызывая усиленную продукцию макрофагами супероксидных и нитроксидных радикалов, убивающих внутриклеточные паразиты.
Цитотоксические CD8+ CTL способны убивать зараженные вирусами клетки при непосредственном контакте с ними. В месте контакта из CTL в мембрану клетки-мишени проникают порообразующие белки — перфорины, формирующие в мембране микроканалы, через которые в клетку-мишень проникают ферменты — фрагментины, вызывающие разрушение ядра клетки и ее гибель.
Гуморальный иммунный ответ
Гуморальный иммунный ответ защищает преимущественно против внекле-точно паразитирующих микроорганизмов, которые доступны действию специфических антител. Продуцентами антител (иммуноглобулинов) являются потомки активированных В-лимфоцитов — плазматические клетки.
В-лимфоцит получает сигнал активации при соединении его антиген-распознающего рецептора с антигеном. Для активной пролиферации и дифференцировки в плазматические клетки потомки В-лимфоцита получают дополнительные сигналы активации — продуцируемые Th2 цитокины: интерлейкины-4, -5, -6, -10, -13. Те же цитокины усиливают продукцию и секрецию специфических для данного антигена антител зрелыми плазматическими клетками.
Таблица 8.5. Защитные функции иммуноглобулинов (антител) разных изотипов
| Изотипы (классы) иммуноглобулинов | Локализация | Защитные функции |
| Иммуноглобулин G | Кровяное русло и ткани | Нейтрализация токсинов и вирусов, активация системы комплемента, усиление фагоцитоза |
| Иммуноглобулин М | Только кровяное русло | Активация системы комплемента |
| Иммуноглобулин А (секреторный) | Секреты на слизистых оболочках, грудное молоко | Препятствие адгезии бактерий и вирусов на слизистых оболочках, их связывание |
Специфические антитела — иммуноглобулины против конкретных антигенов бактерий (стафилококки, стрептококки, возбудители дифтерии, кишечных инфекций, клостридии и др.), связываясь с бактериальными токсинами, вызывают их нейтрализацию, т. е. утрату токсического действия на организм. Сами бактерии, связавшиеся со специфическими антителами, быстрее и легче захватываются и убиваются фагоцитирующими клетками или лизируются активированной системой комплемента.
Иммуноглобулины делятся на пять классов (изотипов): IgG, IgM, IgA, IgE, IgD. В нормальной сыворотке крови 80 % всех иммуноглобулинов составляют IgG, на долю IgM приходится 6 %, на долю IgA— 13 %, а на долю IgE и IgD — сотые или тысячные доли процента. Главными защитными иммуноглобулинами являются IgG. У иммуноглобулинов разных изотипов различаются защитные свойства (табл. 8.5).
Типы гуморального иммунного ответа при вирусной инфекции. Иммуноглобулин A.
Иммунная система организма на вирусные инфекции или иммунизацию вирусными вакцинами отвечает выработкой антител, обладающих специфичностью к различным вирусным компонентам и принадлежащих к разным классам иммуноглобулинов.
Важнейшая биологическая функция иммуноглобулинов - специфическое связывание с антигеном. Антитела против некоторых эпитопов на поверхности вирионов нейтрализуют инфекционность, они могут также действовать как опсонины, облегчая поглощение и разрушение макрофагами. Кроме того, антитела могут прикрепляться к вирусным антигенам на поверхности инфицированных клеток, вызывая их разрушение вследствие активации классического или альтернативного действия комплемента или с помощью активации Fc-рецепторсвязывающих клеток, таких как NK-клетки, полиморфноядерные лейкоциты и макрофаги (антителозависимая цитотоксичность).
Различают четыре основных класса антител: два мономера IgG и IgE и два полимера IgM и IgA. Все иммуноглобулины имеют подобную структуру, но широко варьируют по аминокислотной последовательности антигенсвязывающего сайта, который определяет их специфичность для данной антигенной детерминанты. N-концевая последовательность L- и Н-цепей образует антигенсвязывающий центр, то есть антидетерминанту. Чем больше антидетерминант на поверхности иммуноглобулина, тем выше его активность.
Авидность характеризует прочность связи антитела с соответствующим антигеном. Афинность - прочность связи между отдельными антидетерминантами и детерминантами.
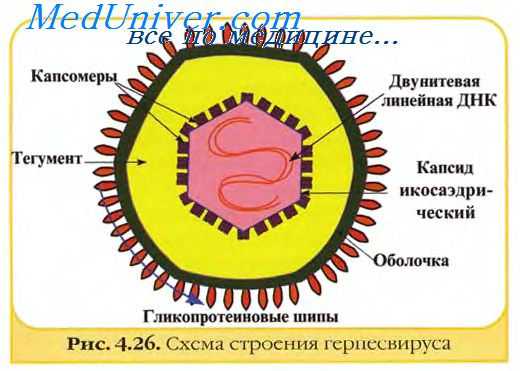
IgG является основным классом антител в крови. Он состоит из двух Н- и L-цепей, каждая из которых содержит постоянные и вариабельные участки. Молекулы IgG содержат два идентичных антигенсвязывающих Fab-фрагмента и Fc-фрагмент, выполняющий эффекторные функции (связывание комплемента, прикрепление к фагоцитам и плацентарному или колостральному трансферу).
В результате системной вирусной инфекции IgG синтезируется в течение длительного периода и является главным фактором защиты от реинфекции. Субклассы IgG отличаются константной областью их V-цепей и, соответственно, биологическими свойствами, такими как фиксация комплемента и прикрепление к фагоцитам.
Первоначально антитела относятся к классу IgM, но соматические рекомбинации (транслокации) затем рождают класс, обусловленный связыванием V-генных сегментов различными постоянными участками Н-цепей. В изменении изотипов (переход изотипов на другой путь) важная роль принадлежит различным цитокинам. Таким образом, через несколько дней IgG , IgA и иногда IgE-антите-ла той же самой специфичности становятся доминантными в иммунном ответе.
Тц-клетки достигают своего пика обычно через неделю после инфекции, а антитела — через 2—3 недели. NK-клетки максимально активируются через два дня, а активность интерферона совпадает с пиком концентрации вируса.
Динамика гуморального иммунного ответа проявляется, в первую очередь, в смене синтеза антител различных классов. В начальной фазе иммунного ответа синтезируется преимущественно IgM с относительно слабым сродством к антигену (авидный класс антител). IgM является пентамером с 10 Fab-фрагментами. Синтез IgM сменяется синтезом IgG, а затем IgA. IgM-антитела находятся в большинстве случаев в плазме крови и лимфе, обладая способностью преципитировать, агглютинировать и лизировать антигены.
Устойчиво высокие титры антител могут отражать также персистенцию вирусной инфекции (например, вирусов герпеса, кори) или повторную стимуляцию вирусным антигеном, однако антитела к некоторым вирусам могут персистировать и без явных признаков заболевания. IgG -антитела содержатся в сыворотке крови в наиболее высокой концентрации (~12г/л), откуда они поступают в тканевую жидкость. В отличие от других иммуноглобулинов, у человека и приматов они способны проникать через плаценту и снабжать плод материнскими антителами. Период полураспада их равен 10-35 дням.
Иммуноглобулин A (IgA) является димером с 4 Fab-фрагментами. Проходя через эпителиальные клетки, IgA приобретает J-фрагмент (секреторный фрагмент), становясь секреторным slgA, который секретируется через эпителий респираторного, кишечного и урогенитального трактов. Секреторный IgA более устойчив к протеазам, чем другие иммуноглобулины, и является основным иммуноглобулином на слизистых поверхностях, в молозиве и молоке многих видов млекопитающих. Поэтому IgA-антитела играют важную роль в защите от инфекции респираторного, кишечного и урогенитального трактов. Иммунизация через слизистые при некоторых инфекциях является более эффективной, чем системное введение вакцины.
Секреторные антитела появляются на 4-7-й день после инфицирования и представлены в основном IgA, IgG и IgM. Они считаются менее специфичными, чем сывороточные. Динамика накопления антител в сыворотке крови и секретах практически одинакова.
В отличие от сывороточного IgA, большая часть которого является мономером, молекула секреторного IgA представляет собой димер. Мономерный IgA синтезируется плазматическими клетками костного мозга, периферических лимфатических узлов, селезенки и других органов. Димерные формы sIgA с соединительной j-цепью синтезируются лимфоидной тканью желудочно-кишечного, респираторного и урогенитального трактов.
Добавочный структурный компонент секреторного IgA, вероятно, функционирует как поверхностный рецептор клеток секреторного эпителия и придает устойчивость sIgA к действию протеаз. Биологическая функция sIgA состоит в основном в местной защите слизистых оболочек от инфекции. Формирование местных секреторных IgA на поверхности слизистых оболочек имеет особое значение для формирования устойчивости организма к вирусам, обычно проникающим через дыхательный, кишечный или урогенитальный эпителий. Для индукции секреторных IgA в кишечнике вирус должен вступить в контакт с лимфоидной тканью кишечника. После формирования местного ответа В-клетки памяти, образующие IgA, мигрируют в другие участки кишечника. Аналогичный механизм индукции IgA функционирует в респираторном тракте.
Система секреторного иммунитета функционирует и регулируется иначе, чем иммунная система в целом. Она может коррелировать с общей иммунной реакцией или быть независимой от нее. Кроме секреторного IgA, существенное значение для иммунитета слизистых оболочек имеют содержащиеся в секретах у человека IgM и IgG. IgM также представляет секреторный иммуноглобулин, однако он не так прочно, как sIgA, связывает секреторный компонент. В пищеварительном тракте IgM играет более важную роль, чем IgG, а в носоглотке - наоборот.
Иммунитет человека
Пожалуй, каждый знает, насколько важным является иммунитет человека. Но далеко не все представляют, что означает это понятие. В основном оно ассоциируется у людей с защитой организма, что не совсем верно. Иммунитет человека – это способность организма сопротивляться различным болезнетворным влияниям, в частности инфекционным агентам и вредным бактериям. Благодаря иммунной системе, постоянно поддерживается состояние невосприимчивости к определенным микроорганизмам, а также к их продуктам жизнедеятельности. Компоненты иммунной системы распознают и разрушают чужеродные структуры (антигены), которые попадают из внешней среды или становятся опасными изнутри. Реакция иммунной системы организма на внедрение вирусов, грибов, паразитов, как правило, незамедлительная. Как только микроб попадает в организм, к нему устремляются иммунные клетки.
Общая сопротивляемость организма
В результате вокруг микроорганизма формируется очаг воспаления, который с одной стороны является барьером, направленным на предотвращение распространения возбудителя, а с другой – предупреждает организм о вторжении чужеродного агента. Далее происходит распознавание опасного агента и выработка факторов защиты против конкретного микроба, а также его частичное разрушение. Кроме того, формируется иммунологическая память о данных процессах, благодаря которой при следующей атаке этого микроба (антигена) запуститься сигнал для распознавания его особыми клетками иммунной системы. После того, как микроб изолирован и распознан, он подвергается полному уничтожению.
Клеточный и гуморальный иммунитет
Все защитные реакции в организме осуществляются за счет разных компонентов иммунитета: клеток и белков. Макрофаги и некоторые лимфоциты формируют клеточное звено. Причем макрофаги захватывают и переваривают чужеродные структуры, а затем передают информацию об этом лимфоцитам. В клеточном звене образуется клон лимфоцитов (разновидность белых клеток крови), который обладает способностью разрушать мембраны, так называемых клеток-мишеней, где имеются чужеродные структуры. Гуморальный иммунитет человека обеспечивается специфическими белками (антителами). Его действие реализуется через В-лимфоциты, которые еще не контактировали с антигенами, но после контакта они начинают активно вырабатываться антитела (иммуноглобулины, Ig), которые действуют на чужеродный агент. Эти белки обладают свойством прилипать к некоторым компонентам микроба, приводя к его разрушению или быстрому выведению из организма. Есть несколько видов антител, и каждый выполняет свою специфическую функцию.
Роль иммуноглобулинов
Антитела делятся на несколько классов: иммуноглобулины А, E, D, G, M. Иммуноглобулины типа А участвуют в первичном поверхностном контакте с микробами, в частности препятствуют проникновению микробов в организм, формируют антитоксический иммунитет. Они способны создавать особые полимерные формы – секреторный иммуноглобулин А. Именно этот иммуноглобулин препятствует прикреплению чужеродного агента к клеткам пограничных тканей (слизистых оболочек). Благодаря иммуноглобулинам типа G и M осуществляется защита организма от уже проникших внутрь инфекционных агентов. Ранними защитными белками являются иммуноглобулины М, а иммуноглобулины класса G являясь основным фактором гуморального звена иммунитета человека, отвечают за выздоровление организма в целом. К тому же, иммуноглобулины этого класса могут на протяжении долгого времени защищать от повторного внедрения различных микроорганизмов. Иммуноглобулины Е несут ответственность за возникновение аллергической реакции.
Функции интерферонов
В ответ на действие различных антигенов (к примеру, вирусов) клетки иммунной системы образуют сложные белковые соединения – интерфероны, которые осуществляют ряд защитный функций. Выделяют несколько типов интерферонов. Стоит отметить интерфероны 1 типа – альфа, которые обладают противовирусным эффектом. Человек, после инфицирования вирусным агентом некоторое время еще не знает о болезни (продромальный период инфекции). Но интерфероны альфа уже проявляют заботу. Они способны создавать невосприимчивость клеток к инфицированию вирусами, а в уже поврежденных клетках – блокируют размножение вирусов.
Механизм действия альфа-интерферонов
Вирусы покрыты оболочкой, защищающей располагающиеся внутриядерные молекулы ДНК или РНК. Когда они проникают в клетку, оболочка разрушается и происходит производство вирусных белков. Формируется вирусное потомство – иногда миллионы новых копий вируса. Воспроизведенные таким образом вирусы ищут новые клетки. А пораженные клетки человека, как правило, погибают. Альфа-интерфероны устремляются к клетке с вирусом, запуская ряд сигнальных реакций и не дают вирусу возможности синтезировать собственные белки для начала размножения. Кроме того, альфа-интерфероны вступают в контакт с соседними клетками, изменяют свойства их мембран таким образом, что они становятся невосприимчивыми к атакам вирусов. К тому же, интерфероны 1 типа корректируют и восстанавливают иммунитет, а также помогают иммунной системе бороться с антигенами. Иммуномодулирующий эффект альфа-интерферонов заключается в том, они регулируют экспрессию белков HLA, участников формирования иммунного ответа, и чувствительность к информационным белковым молекулам (цитокинам), определяющих выживаемость иммунных клеток. Они также повышают активность естественных киллеров, которые устанавливают с пораженной клеткой прямой контакт и уничтожают ее. Помимо этого интерфероны усиливают действие макрофагов, которые захватывают чужеродные частицы и переваривают их. Интерфероны 1 типа увеличивают и стимулируют рост иммунных клеток, усиливая борьбу иммунной системы против возбудителей самых разных заболеваний.
По материалам:
“Иммунология в клинической практике”, К.А. Лебедев, И.Д.Понякина.
“Вторичные иммунодефициты: необходимость корректной диагностики и адекватной интерфероно- и иммунотерапии”, И.В. Нестерова.
Материалы подготовлены сотрудниками компании ООО «Ферон» на основе открытых информационных источников
Читайте также:
