Тиреотропный гормон. Влияние гипоталамуса на гипофиз
Добавил пользователь Евгений Кузнецов Обновлено: 29.01.2026
Основой репродуктивной системы женщины является взаимосвязанная цепочка нейроэндокринных органов – гипоталамус – гипофиз – яичник, правильное функционирование которой обеспечивает созревание полноценной яйцеклетки, изменение структуры эндометрия, необходимое для нормальной имплантации эмбриона, правильное функционирование эпителия маточных труб для продвижения оплодотворенной яйцеклетки в матку, имплантацию и сохранение ранней беременности.
Наивысшим органом регуляции гипоталамо-гипофизарно-яичниковой системы является центральная нервная система, путем целого комплекса прямых и обратных взаимодействий обеспечивающая стабильную работу системы репродукции.
Гипоталамус (структура головного мозга) является центром регуляции менструального цикла. С помощью рилизинг-гормонов гипоталамус управляет работой нижележащей железы – гипофиза. Гипофиз, в свою очередь, регулирует работу всех желез внутренней секреции – вырабатывает фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), тиреотропный гормон (ТТГ). Под влиянием гормонов гипофиза (ФСГ, ЛГ и пролактина) осуществляются циклические изменения в яичниках: созревание яйцеклетки и овуляция. При большинстве гипоталамо-гипофизарных заболеваний у женщин развивается менструальная дисфункция вплоть до прекращения менструации.
Гипоталамо-гипофизарная недостаточность
Гипоталамо-гипофизарная недостаточность характеризуется снижением уровня гормонов гипоталамуса, приводящим к гипоменструальному и гиперменструальному (реже) синдрому – скудные или обильные со сгустками менструации.
У пациенток с гипоталамо-гипофизарной недостаточностью матка уменьшена в размерах, шейка матки имеет коническую форму, трубы удлиненные, тонкие, извитые, атоничные, влагалище узкое. Такое патологическое состояние называют половым инфантилизмом (недоразвитием). Такие анатомические особенности половых органов играют определенную роль в происхождении бесплодия, но приоритетное значение имеет отсутствие овуляции вследствие снижения уровня фолликулостимулирующего гормона и, как итог, низкого показателя эстрогенов крови.
Лечение эндокринного бесплодия проводится в зависимости от характера и локализации пораженного органа. При гипоталамо-гипофизарной дисфункции в сочетании с половым инфантилизмом только своевременное назначение гормонотерапии приводит к положительным репродуктивным прогнозам. Гормональная терапия обязательно должна проводиться под контролем гинеколога-эндокринолога с обязательной оценкой уровня эстрадиола крови.
Гипоталамо-гипофизарная дисфункция
Причинами дисфункции гипоталамо-гипофизарной системы могут быть физический или психо-эмоциональный стресс, инфекционные заболевания (менингит, энцефалит), заболевания носоглотки (тонзиллит, гайморит), черепно-мозговые травмы, нарушение сна, голодание. В результате нарушается количество и цикличность синтеза половых гормонов. Клинические проявления гипоталамо-гипофизарной дисфункции с расстройствами менструального цикла: недостаточность лютеиновой фазы, ановуляторные циклы (отсутствие овуляции) или аменорея (отсутствие менструации). Отмечается повышенная секреция эстрогенов и высокий уровень пролактина и гонадотропина в крови (гормонов, синтезирующихся в гипоталамусе).
Недостаточное количество ФСГ приводит к отсутствию роста фолликулов, ановуляции и, как следствие, к ановуляторному бесплодию. При ановуляторном бесплодии всегда страдает рост и созревание эндометрия, то есть присоединяется маточный фактор бесплодия. К этой же группе можно отнести женщин с повышенным уровнем выработки яичниками андрогенов (гормонов, отвечающих за мужские половые признаки). Постоянно высокий уровень андрогенов приводит к хроническому подавлению овуляции и может вызвать гирсутизм (повышенное оволосение в нетипичных для женщин местах), угревую сыпь (акне), бесплодие, отсутствие менструаций в течение более чем 6 месяцев. У женщин с гипоталамо-гипофизарной дисфункцией лечение зависит от уровня гормонов в крови.
Гормональное обследование является приоритетным и необходимым условием успешного лечения гипоталамо-гипофизарной дисфункции. При наличии высокого уровня пролактина в крови в сочетании с ановуляцией перед назначением гормональной терапии проводится курс лечения, направленного на снижение выработки пролактина. Если после снижения уровня пролактина восстановления самостоятельной овуляции не произошло, решается вопрос о применении стимуляции функции яичников. На фоне гормональной терапии гиперпролактинемии также проводят стимуляцию овуляции определенными препаратами, что зачастую дает возможность зачать ребенка.
Недостаточность лютеиновой фазы менструального цикла
Одной из причин гипоталамо-гипофизарной дисфункции является недостаточность лютеиновой фазы (НЛФ) менструального цикла. Эта патология возникает при выработке желтым телом недостаточного количества прогестерона, что приводит к неполноценному созреванию структуры эндометрия, необходимому для нормальной имплантации эмбриона, нарушению функционирования эпителия маточных труб для продвижения оплодотворенной яйцеклетки в матку, нарушению процессов имплантации из-за тонкой структуры и морфологического несоответствия эндометрия. Это может привести к эндокринному бесплодию, появлению мажущих кровянистых выделений за 4-5 дней до начала очередной менструации или же к самопроизвольной потере на ранних сроках беременности (6-8 недель).
Гормональным проявлением недостаточности лютеиновой фазы является снижение продукции прогестерона желтым телом, сопровождающееся нормальной или повышенной секрецией эстрадиола. На клеточном уровне недостаточность лютеиновой фазы проявляется усилением клеточных делений (эндометрий, молочная железа, миометрий). Клинически недостаточность лютеиновой фазы проявляется предменструальным синдромом, нарушениями менструального цикла, бесплодием, доброкачественными заболеваниями молочных желез (фиброзно-кистозная мастопатия, фиброаденома молочной железы), патологией эндометрия (полип эндометрия, гиперплазия эндометрия), патологией миометрия (миома матки).
Причинами бесплодия при недостаточности лютеиновой фазы являются недостаточная морфологическая зрелость эндометрия, затрудняющая нормальную имплантацию яйцеклетки, и низкий уровень прогестерона, недостаточный для поддержки беременности малого срока. Недостаточность прогестерона встречается в 25-30 % случаев эндокринного бесплодия. Лечение бесплодия у пациенток с недостаточностью лютеиновой фазы проводится путем назначения препаратов прогестерона во вторую фазу менструального цикла.
Диагностика гипоталамо-гипофизарной дисфункции
Для диагностики нарушений в гипоталамо-гипофизарной-яичниковой системе необходим весь спектр клинико-лабораторных, биохимических и гормональных исследований крови, рентгенологический снимок черепа (области турецкого седла, где находится гипофиз, с целью исключения пролактиномы). Информативным является измерение базальной температуры с построением графика. В период овуляции отмечается увеличение ректальной температуры в среднем на 1°С. При недостаточности лютеиновой фазы отмечается укорочение второй фазы цикла, разница температуры в обе фазы цикла составляет менее 0.6°С. Проводится ультразвуковое исследование роста фолликулов и толщины эндометрия в определенные дни менструального цикла. Проводится биопсия эндометрия за 2–3 дня до начала менструации, позволяющая определить морфологическое созревание эндометрия.
Информативным методом исследования гипофиза является компьютерная томография. Компьютерная томография области турецкого седла позволяет выявить изменения плотности гипофиза, дифференцировать микро- и макроаденомы, «пустое» седло и кисты от нормальной ткани гипофиза.
Для диагностики новообразований гипоталамо-гипофизарной области применяется магнитно-резонансная томография. Магнитно-резонансная томография позволяет различить стебель гипофиза, малейшие изменения структуры гипофиза, отдельные кисты, кистозную опухоль, кровоизлияния, кистозное перерождение гипофиза. Преимущество магнитно-резонансной томографии – в отсутствии рентгеновского облучения, что дает возможность многократно проводить обследование пациентки в динамике.
Описание исследования
Тиреотропный гормон (ТТГ) – это гормон гипофиза, осуществляющий регулирование работы щитовидной железы. Исследование его уровня является самым информативным показателем при диагностике ее заболеваний.
Молекулярная масса ТТГ составляет порядка 28 кДа. Его синтез осуществляется передней долей гипофиза. Под действием гормона активируется образование тиреоидных гормонов (т.е. гормонов, продуцируемых щитовидной железой) и их выделение, он инициирует рост и размножение клеток щитовидной железы. На производство и выделение (синтез и секрецию) ТТГ влияет тиротропин-рилизинг-гормон гипоталамуса. Активация процесса начинается в том случае, если концентрация циркулирующих гормонов щитовидной железы уменьшается. Уровни вырабатываемого ТТГ и Т4 находятся в обратнопропорциональной зависимости: чем выше уровень Т4, тем меньше продукция ТТГ и наоборот, чем меньше Т4, тем более интенсивно вырабатывается тиреотропный гормон. Таким образом, происходит компенсация количества гормонов щитовидной железы и поддерживается их нормальное содержание. На количество выделяемого ТТГ оказывают влияние различные процессы нервной системы организма. Уровень гормона изменяется во сне, при изменении температуры, при неспецифическом стрессе (активности нервной системы, возникающей при необходимости отреагировать на новую ситуацию – повышение общего тонуса, обострение восприятия органов чувств (зрения, слуха, обоняния) или, наоборот, их притупление, концентрация внимания, познание окружающего мира и пр.). Кроме того, концентрация ТТГ зависит от времени суток: максимальные показатели отмечаются в 2-4 часа и сохраняются на высоком уровне до 6-8 часов; самое низкое содержание гормона – в 17-18 часов. Приводимые в интерпретации результатов референсные значения выведены на основании обследования пациентов в период с 8 до 18 часов. При ночном бодрствовании происходит сбой ритма выделения гормона.
Явное нарушение работы щитовидной железы, при котором снижается уровень вырабатываемых ею гормонов (выраженный первичный гипотиреоз) вызывает значительное повышение концентрации ТТГ. Первичный гипертиреоз (избыточное продуцирование тиреоидных гормонов), наоборот приводит к значительному понижению концентрации ТТГ, иногда настолько низкому, что его невозможно определить. Посредством исследования количественного содержания тиреотропного гормона можно выявить также заболевание в субклинической стадии – когда выраженных симптомов еще не наблюдается и уровень гормонов поддерживается в диапазоне нормальных значений. Тестирование концентрации ТТГ является единственным способом первичного обследования состояния щитовидной железы. Тест может проводиться в сочетании с исследованием концентрации свободного тироксина (Т4).
Препараты Т4, принятые накануне забора крови, никак не сказываются на результатах тестирования. Заместительное лечение L-тироксином при гипотиреозе (недостаточном продуцировании щитовидной железой гормонов) очень медленно нормализует концентрацию ТТГ – недели, а иногда и месяцы. Это объясняется тем, что хронический выраженный гипотиреоз является причиной избыточного образования клеток передней доли гипофиза (тиреотрофов), которые продуцируют ТТГ. При этом возникает нехарактерное состояние, искусственно спровоцированное применением препарата – одновременное повышение уровня ТТГ и Т4. Мониторинг проводимого лечения предполагает периодические отборы проб, но при изменении количества или вида лекарственного средства забор крови не резонно делать раньше, чем через 6 недель.
Вторичный и третичный гипотиреозы, возникающие по причине нарушения функций гипофиза и гипоталамуса, характеризуются очень низкими концентрациями тиреоидных гормонов (Т3 и Т4). При этом содержание ТТГ нормальное или слегка повышенное, однако биологическая активность его при этом снижена. Вторичный гипертиреоз может возникнуть из-за образования опухолей передней доли гипофиза, которые выделяют ТТГ, но такие случаи наблюдаются редко.
Концентрация ТТГ может изменяться во время тяжелых болезней, не связанных с нарушением функций щитовидной железы. Влиять на уровень гормона могут применяемые при лечении препараты или последствия болезни как таковой. Пониженным уровнем ТТГ характеризуется острая стадия болезни, незначительно повышенным – период выздоровления. Если при этом есть необходимость в обследовании, то границы референсных значений уровня ТТГ расширяются (0,02-10 мЕд/л) и наряду с определением ТТГ исследуется уровень Т4 общего или свободного.
Изменение количественного содержания ТТГ происходит по физиологическим причинам в период беременности. Процесс объясняется тем, что через несколько дней после оплодотворения яйцеклетки внешняя оболочка эмбриона (хорион) начинает вырабатывать большое количество хорионического гонадотропина – гормона, структурно схожего с ТТГ. Благодаря схожести, он способен стимулировать производство гормонов щитовидной железы. Первый триместр характеризуется временным увеличением уровня Т4 и уменьшением содержания ТТГ. В течение двух последующих триместров концентрация тиреотропного гормона нормализуется. Его высокий уровень в начале беременности может являться сигналом о наличии у женщины скрытого гипотиреоза, представляющего потенциальную опасность для развивающегося ребенка.
Подготовка к исследованию
Назначение времени и условий проведения обследования производятся врачом, направляющим пациента.
Важно! Проба крови отбирается только до проведения рентгеноконтрастных исследований.
Важно! Операции на щитовидной железе, радиотерапия или прием лекарственных средств, особенно гормонов щитовидной железы или препаратов, содержащих йод, могут исказить результаты тестирования.
Общие рекомендации для всех видов обследования:
- оптимальное время сдачи анализа с 8 до 11 часов, натощак;
- накануне обследования избегать физических и эмоциональных перегрузок;
- не употреблять алкоголь за сутки и не курить за час до проведения тестирования;
- прием любых лекарственных препаратов, проведение терапии перед обследованием и во время него необходимо согласовывать с лечащим врачом.
Важно! Непосредственно перед отбором пробы пациент должен находиться в состоянии покоя не менее 30 минут.
Показания к исследованию
- с целью диагностирования невыраженных форм первичных гипотиреоза и гипертиреоза;
- для диагностирования причин:
- задержки умственного и полового развития у детей;
- сердечных аритмий;
- миопатии (нервно-мышечного заболевания);
- снижения температуры тела ниже 35°C без видимых к тому предпосылок (идиопатической гипотермии);
- депрессии;
- бесплодия;
- импотенции;
- снижения полового влечения;
- алопеции (патологического выпадения волос);
- аменореи (нарушения цикличности менструации с полугодовыми и более задержками);
- гиперпролактинемии (повышенного содержания гормона пролактина);
- при зобе;
- для определения эффективности заместительной терапии при первичном гипотиреозе;
- при первичном обследовании беременных на малом сроке (до 3-х месяцев) с целью выявления скрытого гипотиреоза;
- для мониторинга состояния больного гипотиреозом (до двух раз в год, пожизненно);
- для контроля состояния пациента с диффузным токсическим зобом (1-3 раза в месяц на протяжении полутора-двух лет).
Интерпретация исследования
Уровень ТТГ измеряется в микромеждународных единицах на миллилитр (мкМЕ/мл).
По мере взросления человека референсные значения изменяются. Нормы интерпретации для разных возрастов отражены в таблице:
Тиреотропный гормон. Влияние гипоталамуса на гипофиз
Тиреотропный гормон. Влияние гипоталамуса на гипофиз
Большие трудности возникают при изучении влияния гипоталамуса на секрецию тиреотропного гормона (ТТГ) аденогипофизом, так как секреция этого гипофизарного гормона отличается рядом характерных черт. Она в значительно меньшей степени зависит от воздействия факторов внешней среды, в ней не наблюдается четкого суточного ритма. Установлено, что из внешних факторов на секрецию ТТГ оказывают влияние только «стрессовые» ситуации (Schreiber, 1963). При «стрессе» секреция ТТГ понижается и активность щитовидной железы уменьшается. Угнетающее влияние на секрецию ТТГ оказывают также глюкокортикоиды. Возможно, что влияние «стрессовых» ситуаций связано с повышенным выделением АКТГ, так как установлено, что этот гормон так же, как и глюкокаротиноиды, выделяющиеся под его воздействием, угнетают выделение ТТГ и понижают функцию щитовидной железы.
Установлено, что «стрессовые» реакции оказывают и непосредственное угнетающее влияние на секрецию ТТГ у животных с удаленными надпочечниками (Schreiber, 1963). По-видимому, существуют обратные взаимоотношения между секрецией двух тропных гормонов — АКТГ и ТТГ. При повышенном выделении АКТГ секреция ТТГ понижается. Секреция ТТГ также находится под контролем гипоталамуса, стимулирующего его выделение путем особого вещества, названного thyreotropin-releasing-factor (TRF), которое доставляется в аденогипофиз через местную портальную систему.
Однако в отношении секреции этого тропного гормона аденогипофиз обладает известной автономностью и не всегда поддается контролю гипоталамуса.
Некоторой автономностью обладает и функция самой щитовидной железы, поэтому при патологии этой системы, например при гипертиреозе, центральный контроль уже не осуществляется.
Большинство авторов считают, что тиреотропной функцией гипофиза ведает передний отдел гипоталамуса. Данные Б. В. Алешина (1960) свидетельствуют о том, что гипоталамус может оказывать свое влияние на щитовидную железу не только через посредство аденогипофиза путем стимуляции секреции ТТГ, но также и непосредственно — парагипофизарно.
Имеются данные о влиянии гипоталамуса на секрецию аденогипофизом других «тропных» гормонов, в частности о стимулирующем его воздействии на гонадотропный гормон (ГТГ). Повреждение гипоталамуса или перерыв его связи с аденогипофнзом угнетают секрецию гонадотропного гормона. Влияние гипоталамуса на секрецию соматотропного гормона (СТГ) пока еще достоверно не доказано.
Некоторые авторы, придерживающиеся старой точки зрения, предполагают, что стимулятором «тропных» гормонов является вазопрессин нейрогипофиза. Однако большинство современных авторов считает, что гипоталамус выделяет специальные вещества, стимулирующие секрецию «тропных» гормонов.
Усиленное выделение «тропных» гормонов вызывает повышенную секрецию соответствующих гормонов соподчиненных желез, одновременно с этим в физиологических условиях провоцируется также и усиленная их инактивация (С. Г. Генес, 1960). Гормоны белковой природы часто провоцируют выработку антител. Grollman (1964) указывает, что выработка таких антигормонов не сопровождается общими аллергическими реакциями и может протекать бессимптомно.
Тиреотропный гормон
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима и приводимая ниже информация носит исключительно справочный характер.
ТТГ (тиреотропный гормон, тиротропин, Thyroid StimulatingHormone, TSH): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Тиреотропный гормон синтезируется в передней доле гипофиза (железа в головном мозге) и стимулируетфункцию щитовидной железы по принципу «обратной связи».
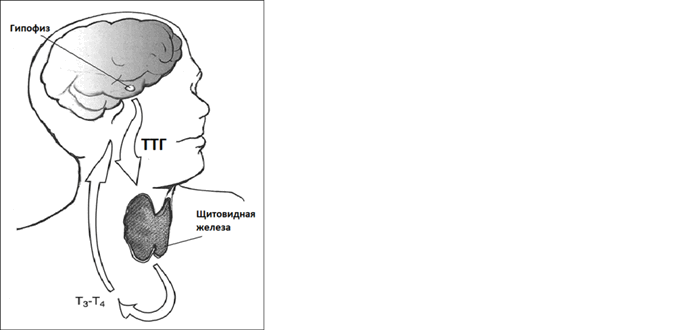
При нехватке гормонов щитовидной железы (тиреоидных гормонов) в крови продукция тиреотропного гормона увеличивается, и наоборот, при повышении уровня гормонов щитовидной железы в крови синтез ТТГ снижается.
В каких случаях необходим анализ ТТГ Определение уровня тиреотропного гормона используют как базовый тест для оценки функции щитовидной железы как при гипотиреозе, так и при гипертиреозе.
Гипотиреоз (уменьшение выработки гормонов щитовидной железы), характеризуется замедлением основных функций организма: пациент, как правило, жалуется на слабость, депрессию, усталость, низкое артериальное давление, выпадение волос и др. Тяжелая форма гипотиреоза называется микседемой и может приводит к сердечной недостаточности, судорожному синдрому и коме.
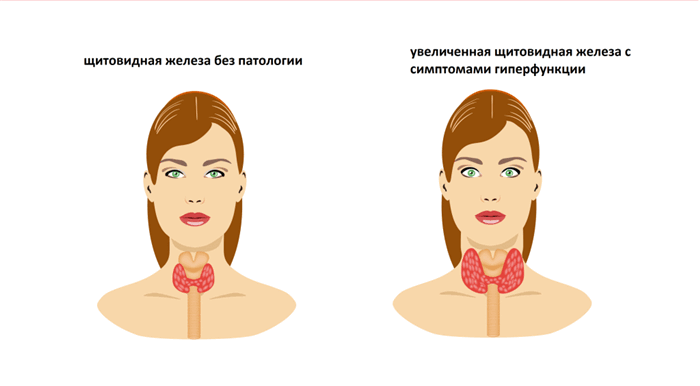
Гипертиреоз (избыточная выработка гормонов щитовидной железы)характеризуется ускорением функций организма: пациенты, наоборот, жалуются на учащенное сердцебиение, беспокойство, тревожность, бессонницу, потерю веса. Наиболее тяжелая форма гипертиреоза – тиреотоксический криз- жизнеугрожающее состояние.
К изменению синтеза ТТГ приводят
- Травмы головного мозга, массивные кровопотерии гипоталамо-гипофизарные заболевания, в первую очередь опухоли в области гипоталамо-гипофизарной зоны.
- Опухоли гипофиза (преимущественно аденомы передней или железистой доли) вызывают увеличение продукциигипофизарных гормонов. Они, в свою очередь, влияют на деятельность других эндокринных желез (щитовидной железы, яичников, надпочечников и т.д.) и способствуют развитию гипотиреоза, сахарного и несахарного диабета,гипоталамо-гипофизарной недостаточности и эндокринного бесплодия.
- Заболевания других эндокринных желез, в частности опухоли или недостаточность надпочечников, также могут подавлять или стимулировать выработку ТТГ.
- Гипоталамо-гипофизарная недостаточность, возникающая припоражении гипофиза и ядер гипоталамусавследствие инфекционного процесса, токсического воздействия, аутоиммунных (при которых иммунная система атакует ткани организма) и сосудистыхзаболеваний, а также удаления гипофиза, сопровождается изменением уровня ТТГ и требует его контроля.
- Кровоизлияние (геморрагический инсульт) в области гипофиза вызывает резкое падение уровня ТТГ, однако при этой патологии на первый план выступают симптомы мозгового кровотечения(нарушение сознания, резкая головная боль диффузного характера, светобоязнь, тошнота, многократная рвота).
- У женщин уровень ТТГ меняется при осложненных родах или абортах, а также во время беременности. Анализ на ТТГ в обязательном порядке назначают при скрининге беременных в I триместре.
Подготовка к процедуре
На уровень ТТГ может влиять изменение суточного ритма: наблюдается снижение ТТГ при нарушении сна илиработе ночью.Наиболее высокий уровень гормона фиксируется с 2 ч ночи до 6–8 ч утра, тогда как вечером он снижается.
За три дня до исследования необходимо отказаться от приема алкоголя, жирной и острой пищи. Взятие биоматериала (кровь) для анализа проводят натощак (допустимо через 4 часа после легкого перекуса), в одно и то же время при динамическом исследовании ТТГ (например, для контроля эффективности лечения).
Срок исполнения
Результат исследования можно получить в течение одного рабочего дня (исключая день взятия материала).
Что может повлиять на результаты анализа ТТГ
- Суточные ритмы
- Стрессы и длительное нервное напряжение
- Беременность
- Возраст (наиболее высокие показатели ТТГ у новорожденных, с возрастом уровень гормона существенно снижается)
- Лекарственные препараты
Сдать анализ крови для определения тиреотропного гормона (ТТГ, тиротропин, Thyroid StimulatingHormone, TSH) вы можете в ближайшем медицинском офисе ИНВИТРО. Список офисов, где принимается биоматериал для лабораторного исследования, представлен в разделе «Адреса».
Для исследования используют сыворотку венозной крови.
Концентрацию ТТГ в сыворотке определяют с помощью иммунохемилюминесцентного анализа на микрочастицах.Анализ заключается в исследовании специфической реакции антигенов (рецепторов ТТГ) и антител к ним и отличается высокой чувствительностью – до 90%.
Тиреотропный гормон: нормальные значения
В норме средние показатели ТТГ в крови различаются в зависимости от возраста, особенно изменяясь в первые месяцы жизни ребенка.
| Возраст | Концентрация ТТГ, мЕд/л |
| 4 дня – 6 месяцев | 0,73–4,77 |
| 6 месяцев – 14 лет | 0,7–4,17 |
| 14–19 лет | 0,47–3,41 |
| > 19 лет | 0,4–4,0 |
Во время беременности уровень ТТГ в крови снижается и референсные значения выглядят так:
| Триместр беременности | Концентрация ТТГ, мЕд/л |
| I триместр | 0,1–2,5 |
| II триместр | 0,2–3,0 |
| III триместр | 0,3–3,0 |
Расшифровка показателей:
Что значат повышенные показатели ТТГ
- Повышение концентрации ТТГ может происходить вследствиепервичного гипотиреоза, даже при бессимптомном течении. Однако, при более детальном опросе пациент может отмечать физическую слабость и утомляемость,неустойчивое настроение с преобладанием апатии,нарушение памяти, выпадение волос, сухость кожи.
- Увеличение концентрацииТТГ может быть следствием подостроготиреоидита– воспалительного заболевания щитовидной железы (тиреоидита де Кервена, гранулематозноготиреоидита). В этих случаях ткань щитовидной железы повреждается вследствие инфекционного заболевания верхних дыхательных путей. При этом отмечается болезненность и увеличение долек щитовидной железы с одной или двух сторон, а также мышечные боли, слабость и утомляемость.
- Рост концентрации ТТГ в кровиотмечается в случае аномального синтеза этого гормона опухолевой тканью при раке легкого или молочной железы, при аденоме гипофиза и раке щитовидной железы.
- Высокий уровень ТТГ обнаруживается при многих тяжелых заболеваниях в фазе выздоровления и при синдроме резистентности к гормонамщитовидной железы.
- Прием некоторых лекарственных препаратов может вызывать повышение уровня ТТГ (бета-адреноблокаторы (атенолол, метопролол, пропранолол), нейролептики (производныефенотиазина, аминоглутетимид),прокинетики (мотилиум, метоклопрамид), противосудорожные(фенитоин, карбамазепин) и йодсодержащие препараты, а также кломифен, фуросемид,соли лития и т.д.)
Что значат пониженные показатели ТТГ
- Заболевания щитовидной железы: первичный гипертиреоз (диффузный токсический зоб, токсический многоузловой зоб, токсическая аденома, автономно функционирующие тиреоидные узлы), субклинический гипертиреоз и др.
- Синдром Иценко–Кушинга, который возникает при повышении выделения корой надпочечников гормона кортизола, также сопровождается снижением уровня ТТГ.
- Обширные травмы головного мозга.
- Инсульт в гипоталамо-гипофизарной области.
Снижение концентрации ТТГ ниже референсных значений не обязательно свидетельствует о заболевании. Уровень ТТГ в крови уменьшается во время беременности, а также на фоне стресса или голода.
Снижение ТТГ в крови может провоцировать прием некоторых лекарственных препаратов. К их числу относятся кортикостероиды, допамин, тироксин, трийодтиронин, амиодарон, цитостатики, бета-адреномиметики (добутамин, допексамин), соматостатин, октреотид, нифедипин, средства для лечения гиперпролактинемии (метерголин, перибедил, бромкриптин), гепарин и препараты ацетилсалициловой кислоты (аспирин).
Дополнительные обследования
Как правило, анализ на ТТГ дополняется исследованием уровня трийодтиронина и тироксина (Т3 и Т4), которые вырабатываются щитовидной железой, и их уровень позволяет более точно выявить причину заболевания.
- трийодтиронин общий (Т3 общий, Total Triiodthyronine, TT3) ;
- трийодтиронин свободный (Т3 свободный, FreeTriiodthyronine, FT3) ;
- тироксин общий (Т4 общий, тетрайодтиронин общий, TotalThyroxine, TT4) ;
- тироксин свободный (Т4 свободный, FreeThyroxine, FT4) ;
- антитела к тиреоглобулину (АТ-ТГ, anti-thyroglobulinautoantibodies) ;
- антитела к тиреоидной пероксидазе (АТ-ТПО, микросомальные антитела, anti-thyroid) ;
- АТ к рТТГ (антитела к рецепторам ТТГ, TSH receptorautoantibodies) .
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Общие сведения о гипофизе
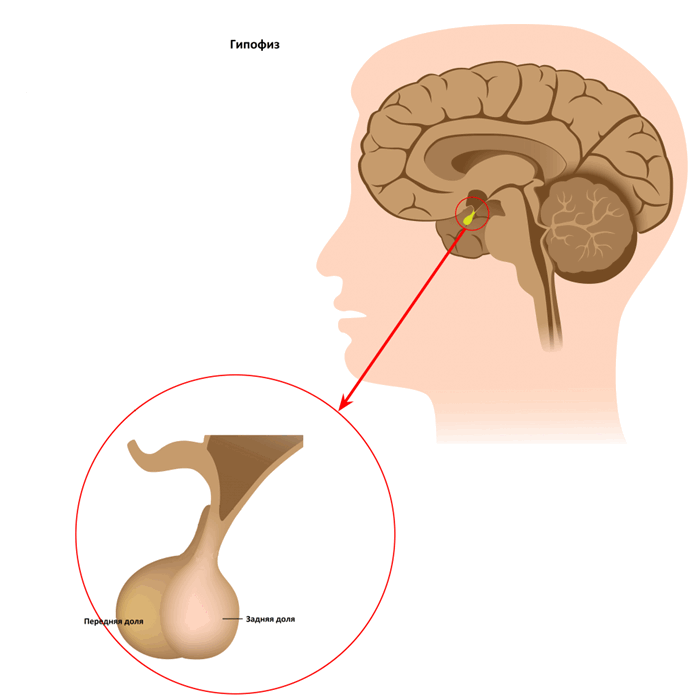
Гипофиз — это железа размером с горошину, расположенная в костной структуре (турецкое седло) в основании головного мозга. Турецкое седло защищает гипофиз, оставляя немного пространства для расширения.
Гипофиз управляет работой большинства эндокринных желез, поэтому иногда его называют главной железой. В свою очередь, гипофиз контролируется гипоталамусом, областью головного мозга, расположенной непосредственно над гипофизом. Определяя уровень гормонов, вырабатываемых железами под контролем гипофиза (железы-мишени), гипоталамус или гипофиз способны определить степень необходимой стимуляции желез-мишеней.
Гипофиз и его органы-мишени
Гипофиз имеет две выраженные части:
Передняя (фронтальная) доля, которая составляет 80 % всей массы гипофиза
Доли соединяются с гипоталамусом посредством ножки, которая содержит кровеносные сосуды и проекции нервных клеток (нервные волокна или аксоны). Гипоталамус контролирует переднюю долю, высвобождая гормоны из соединяющих их кровеносных сосудов. Он контролирует заднюю долю с помощью нервных импульсов.
Гипофиз вырабатывает часть гормонов непостоянно. Большая часть высвобождается эпизодически, раз в 1–3 часа, чередуя периоды активности и неактивности. Такие гормоны, как адренокортикотропный гормон ( АКТГ ), гормон роста и пролактин, следуют суточному ритму: Их уровни предсказуемо повышаются и понижаются в течение дня, обычно достигая максимального значения непосредственно перед пробуждением и снижаясь до минимального значения непосредственно перед сном. Уровни других гормонов изменяются под воздействием и других факторов. Например, у женщин уровень лютеинизирующего гормона и фолликулостимулирующего гормона, контролирующих репродуктивные функции, варьируется в ходе менструального цикла.
Гипофиз: Главная железа
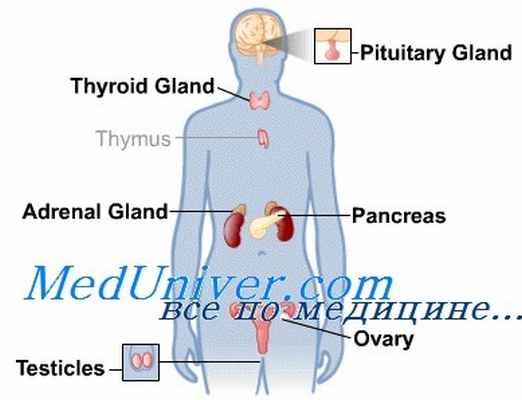
Гипофиз, представляющий собой железу размером с горошину, расположенную в основании головного мозга, вырабатывает несколько видов гормонов. Каждый из этих гормонов воздействует на определенную часть организма (орган-мишень или ткань-мишень). Поскольку гипофиз контролирует функционирование большинства других эндокринных желез, его часто называют главной железой.
Орган-мишень или ткань-мишень
Адренокортикотропный гормон ( АКТГ )
Головной мозг и иммунная система
Яичники или яички
Яичники или яички
Матка и молочные железы
Вазопрессин (антидиуретический гормон)*
* Эти гормоны вырабатываются в гипоталамусе, но хранятся в гипофизе и высвобождаются из него.
Гормоны передней доли
Передняя доля гипофиза вырабатывает и высвобождает (секретирует) шесть основных гормонов:
адренокортикотропный гормон ( АКТГ ), также называемый кортикотропином , который стимулирует надпочечники к выработке кортизола и других гормонов;
фолликулостимулирующий гормон и лютеинизирующий гормон (гонадотропины), которые стимулируют яички к выработке спермы, яичники к выработке яйцеклеток и половые органы к выработке половых гормонов ( тестостерона и эстрогена );
гормон роста, который регулирует рост и физическое развитие, а также оказывает важное влияние на форму тела, стимулируя формирование мышц и уменьшая жировую ткань;
пролактин, который стимулирует молочные железы к выработке молока;
тиреотропный гормон, который стимулирует щитовидную железу к выработке гормонов щитовидной железы.
Передняя доля также вырабатывает некоторые другие гормоны, включая гормон, отвечающий за потемнение кожи (бета-меланоцитостимулирующий гормон), и гормоны, которые подавляют чувство боли (энкефалины и эндорфины) и контролируют иммунную систему (эндорфины).
Гормоны задней доли
Задняя доля гипофиза вырабатывает только два гормона:
Окситоцин вызывает сокращение матки во время родов и непосредственно после них для предотвращения обильного кровотечения. Окситоцин также стимулирует сокращение молочных протоков в молочных железах, которые направляют молоко к соску («молоко прибывает») у кормящих женщин. Окситоцин выполняет еще некоторые другие функции как у мужчин, так и у женщин.
Нарушение функции гипофиза
Нарушение функции гипофиза обычно возникает в результате развития доброкачественной опухоли (аденомы). Опухоль может вырабатывать повышенное количество одного или нескольких гормонов гипофиза, либо воздействовать на нормальные клетки гипофиза, вызывая недостаточную секрецию одного или нескольких гормонов гипофиза.
Опухоль также может вызывать увеличение гипофиза Увеличение гипофиза Увеличение гипофиза обычно возникает из-за наличия опухоли, но причины также могут включать кровотечение в железу или наличие другого заболевания, например, туберкулеза или саркоидоза. В некоторых. Прочитайте дополнительные сведения , с нарушением выработки гормона или без ее нарушения. Иногда опухоль гипофиза становится причиной одновременного повышения секреции одного гормона и недостаточной секреции другого в связи со сдавлением.
Пониженное или повышенное количество гормона гипофиза приводит к различным симптомам.
Повышенная секреция гормонов гипофиза приводит к развитию заболеваний, в том числе следующих:
Болезнь Кушинга Синдром Кушинга При синдроме Кушинга наблюдается избыточный уровень кортикостероидов, как правило, из-за приема кортикостероидных препаратов или гиперсекреции надпочечниками. Синдром Кушинга обычно возникает. Прочитайте дополнительные сведения Бесплодие Общие сведения о бесплодии Бесплодие обычно определяется как неспособность пары зачать ребенка при регулярной половой жизни без использования средств контрацепции в течение 1 года. Регулярная половая жизнь без контрацепции. Прочитайте дополнительные сведенияНедостаточная секреция гормонов гипофиза приводит к развитию заболеваний, в том числе следующих:
Врачи могут определить уровень гормонов гипофиза, используя обычный анализ крови. В зависимости от симптоматики, врачи выбирают гормоны, уровень которых они считают необходимым измерить. Иногда уровень гормонов гипофиза сложно интерпретировать, поскольку они значительно различаются в течение дня и в зависимости от потребностей организма. Оценка произвольного образца крови не предоставит полезной информации в отношении подобных гормонов.
При определении уровня некоторых гормонов врачи дают вещество, которое обычно оказывает воздействие на выработку гормона, а затем измеряют его уровень. Например, если врач введет инсулин , должен повыситься уровень АКТГ , гормона роста и пролактина. Врачи не измеряют непосредственно уровень гормона роста, они часто оценивают уровень другого гормона, инсулиноподобного фактора роста 1 (ИФР-1). Гормон роста вырабатывается эпизодически, его уровень быстро снижается, но уровень ИФР-1 отражает общее суточное выделение гормона роста. Учитывая все эти причины, интерпретация результатов анализа крови на гормоны гипофиза является сложным процессом.
ПРИМЕЧАНИЕ: Это — пользовательская версия ВРАЧИ: Нажмите здесь, чтобы перейти к профессиональной версии
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Читайте также:
