Влияние калия на ЭКГ. ЭКГ при гиперкалиемии и гипокалиемии
Добавил пользователь Евгений Кузнецов Обновлено: 29.01.2026
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гиперкалиемия: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Гиперкалиемией называют одно из нарушений водно-электролитного баланса, при котором уровень сывороточного калия превышает 5,1 ммоль/л у взрослых. Порог нормы у младенцев и детей зависит от возраста. Уровни выше 6,0 ммоль/л могут привести к значительным гемодинамическим и неврологическим последствиям.
С увеличением концентрации калия в крови симптомы нарушений в сердце нарастают вплоть до полной блокады и остановки сердца. Тяжелая гиперкалиемия может также вызвать паралич дыхания и быстро привести к летальному исходу.
Калий – основной внутриклеточный катион (К+) в отличие от натрия – основного внеклеточного катиона (Na+). Калий в организме содержится в большом количестве внутри клеток, очень много его в мышцах, где концентрация этого микроэлемента в 30 раз выше, чем вне клеток. Функционально калий и натрий связаны между собой. Натрий задерживает воду, а калий пытается ее вывести, что позволяет жидкости циркулировать внутри клетки. Вместе с внеклеточным натрием калий поддерживает разность электрических потенциалов клеточной мембраны, участвует в механизмах передачи нервного импульса и сокращения мышц (в том числе и сердечной мышцы).
Калий не синтезируется в организме, а поступает с продуктами питания. На эффективное усвоение калия влияет витамин B6. Концентрации калия в крови зависят от его всасывания, выведения и обмена между клетками и кровью. Органом, играющим наиважнейшую роль в этом процессе, являются почки, которые при необходимости способны выводить большое количество калия. Поэтому у людей с правильно функционирующей выделительной системой гиперкалиемия является редким явлением.
Внутренними факторами, обусловливающими межклеточный транспорт калия, являются:
- альдостерон – гормон, отвечающий за удерживание солей натрия и выделение калия почками. Наиболее важное влияние на уровень альдостерона оказывает ренин-ангиотензиновая система;
- инсулин – стимулирует поступление калия в клетки. При низких концентрациях инсулина калий выходит из клеток, в результате его концентрация в сыворотке крови увеличивается;
- бета-адренергическая активность;
- кислотно-щелочное равновесие. Ацидоз (повышение кислотности), вызванный накоплением минеральных кислот, может повышать уровень калия в сыворотке крови.
Колебания уровня калия даже в пределах нормального интервала при определенных условиях могут повышать риск смерти, например, у пациентов, перенесших инфаркт миокарда.
Гиперкалиемия наблюдается примерно у 10-12% пациентов, госпитализированных в стационары, что может быть объяснено приемом лекарств, влияющих на ренин-ангиотензин-альдостероновую систему.
Разновидности гиперкалиемии
Гиперкалиемию классифицируют в зависимости от степени превышения концентрации калия:
- легкая гиперкалиемия – уровень калия в крови 5,2-5,9 ммоль/л;
- умеренная гиперкалиемия – уровень калия в крови 6,0–6,4 ммоль/л;
- острая гиперкалиемия – уровень калия в крови превышает 6,5 ммоль/л.
Устойчивая гиперкалиемия обычно подразумевает уменьшение экскреции (выведения) калия почками, особенно при олигурии (уменьшении суточного диуреза).
В ряде случаев регистрируют псевдогиперкалиемию (ложную гиперкалиемию):
- избыточное поступление калия в организм, например, при быстром вливании растворов калия;
- выход K+ из клеток во внеклеточную жидкость при массивном гемолизе (разрушении эритроцитов), кровоизлиянии в мягкие ткани или желудочно-кишечный тракт, рабдомиолизе (повреждении скелетных мышц), распаде опухолей, тяжелых ожогах, некрозе мышечной ткани;
- длительное сдавливание плеча жгутом во время забора крови;
- неправильное хранение биологического материала, гемолиз в пробирке (при этом калий из разрушенных клеток попадает в плазму), забор крови после приема препаратов калия, травмирование вены во время забора крови;
- высокий лейкоцитоз или тромбоцитоз (тромбоциты выделяют калий во время свертывания);
- гиперкалиемический семейный периодический паралич (редкое генетическое заболевание). Во время приступов развивается слабость мышц, которая может прогрессировать до паралича.
Гиперкалиемия возникает при повышенном потреблении калия (обычно ятрогенном):
- избыточное употребление продуктов, содержащих калий (суховфруктов, орехов, бобовых);
- пероральный прием препаратов калия;
- переливание крови;
- внутривенное введение растворов с калием;
- парентеральное питание.
- обструкцию мочевыводящих путей, острую или хроническую почечную недостаточность (сниженное выведение K+ почками);
- болезнь Аддисона;
- гипоальдостеронизм (надпочечниковая недостаточность);
- сахарный диабет, голодание (недостаточность инсулина);
- дегидратацию (уменьшение объема внеклеточной жидкости);
- дефицит минералкортикоидов (адренокортикотропного гормона, кортизона и гидрокортизона).
Очень распространенной причиной развития гиперкалиемии являются лекарственные препараты, которые провоцируют ее разными способами.
Лекарственные препараты могут нарушать калиевый гомеостаз за счет активации трансмембранного транспорта калия, уменьшения почечной экскреции. Риск возрастает, когда такие препараты принимают пациенты с патологиями почек. Особенно подвержены развитию гиперкалиемии пожилые пациенты и пациенты с диабетом.
Препараты, которые могут способствовать развитию гиперкалиемии:
- ингибиторы ангиотензин-превращающего фермента (капотен, эналаприл, престариум, каптоприл и др.);
- блокаторы рецептора ангиотензина II (лозартан, лозап);
- нестероидные противовоспалительные препараты (ибупрофен, мовалис, аркоксиа);
- прямые ингибиторы ренина (алискирен);
- ингибиторы неприлизина (сакубитрил);
- калийсберегающие диуретики (амилорид, триамтерен);
- препараты гепарина;
- бета-адреноблокаторы (атенолол, пропанол);
- дигоксин;
- противогрибковые препараты (кетоконазол, флуконазол, интраконазол);
- противомикробные препараты (триметоприм, пентамидин);
- циклоспорины (сандиммун);
- препараты лития (квилониум);
- програф (такролимус);
- гиперосмолярные растворы (маннитол, глюкоза);
- суксаметоний (листенон);
- внутривенное введение положительно заряженных аминокислот (лизин, аргинин).
К каким врачам обращаться при гиперкалиемии
Обычно диагностирует гиперкалиемию врач-терапевт , врач общей практики, врач-нефролог, врач-эндокринолог или врач-кардиолог. Врач-диетолог помогает подобрать питание с необходимым количеством калия и белка для удовлетворения потребностей вашего организма.
Диагностика и обследования при гиперкалиемии
Диагностические мероприятия обычно начинают с обследования почек:
- оценка функции почек, включая уровень калия в сыворотке крови;
Влияние калия на ЭКГ. ЭКГ при гиперкалиемии и гипокалиемии

Анна Симбирцева, ассистент кафедры пропедевтики внутренних болезней педиатрического факультета ФГБАУ РНИМУ им. Н.И. Пирогова Минздрава России, к.м.н.
Принято разделять гиперкалиемию по степеням: при тяжелой гиперкалиемии концентрация калия в крови выше 6,5 ммоль/л, при умеренной – от 5,5 ммоль/л до 6,5 ммоль/л.
Кто же из пациентов, постоянно наблюдающихся у терапевта или врача общей практики, находится в зоне высокого риска развития гиперкалиемии? Существует несколько распространенных фенотипов.
Пациенты с артериальной гипертонией, распространенность которой в России – 43 млн человек. Их можно разделить на 3 группы. Первая – молодые пациенты до 65 лет с целевым уровнем САД ниже чем 130 мм рт.ст., но не ниже чем 120 мм рт. ст., достижение которого обычно производится за счет титрации дозы иАПФ. Вторая группа – пациенты 65–80 лет с целевым уровнем САД ниже чем 140 мм рт.ст., но не ниже чем 130 мм рт.ст. И, наконец, третья – пациенты старше 80 лет с целевым уровнем ДАД 80 мм рт.ст.
Достижение целевых значений САД и ДАД у пожилых пациентов, как правило, требует титрации иАПФ и сартанов. Необходимо помнить, что любой пациент в период титрации дозы, увеличения дозы комбинированных препаратов может быть угрожаем в отношении развития гиперкалиемии.
Пациенты с абдоминальным ожирением, то есть те мужчины, у которых отношение обхвата талии (ОТ) к обхвату бедер (ОБ) более 0,9, и женщины, у которых ОТ/ОБ более 0,85. Большое количество жира в брюшной полости, сальник, который может достигать веса 12–17 кг, – факторы, ведущие к изменению гормонального профиля. Как правило, это пациенты с метаболическим синдромом, и врач будет выбирать иАПФ в составе комплексного лечения.
Пациенты с установленной патологией почек. Снижение почечной функции приводит к снижению выведения калия и риску развития гиперкалиемии.
Пациенты, постоянно получающие такие препараты, как иАПФ, сартаны, калийсберегающие диуретики, нестероидные противовоспалительные средства (НПВС) и сердечные гликозиды. Врачу следует проявить настороженность в отношении пациентов с ХСН и выраженной недостаточностью кровообращения, то есть с фракцией выброса менее 35% или III–IV функциональным классом по Нью‑Йоркской классификации (за 6 минут такие пациенты могут пройти менее 300 и 150 м), а также пожилых пациентов с вероятным снижением СКФ. Пациенты с предиабетом.
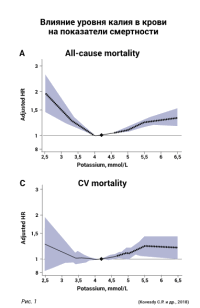
Гиперкалиемия – независимый фактор риска смерти госпитализированных пациентов. Около 10% пациентов в стационарах имеют повышенную концентрацию калия в крови. Даже незначительное повышение или понижение концентрации увеличивает риск смерти от всех причин
При осмотре следует обращать внимание на черный акантоз – бархатистые пигментные пятна на шее, подмышечных впадинах, паховой области (в крупных складках кожи). Основной фактор риска и причина черного акантоза – инсулинорезистентность. В данной группе пациентов в составе медикаментозной поддержки также назначаются иАПФ и сартаны.
Пациенты, получающие оральные антикоагулянты в течение длительного времени. Так, прием варфарина в течение 8 и более лет приводит к кальцинозу мелких сосудов, что непременно сказывается на скорости клубочковой фильтрации, снижая ее.
Диагностика гиперкалиемии
Симптомы гиперкалиемии обычно развиваются при повышении концентрации калия выше 6,5–7 ммоль/л, но более важна скорость увеличения концентрации. Так, пациенты с хронической и тяжелой гиперкалиемией могут не иметь симптомов, а пациенты с быстро развившейся умеренной гиперкалиемией – сообщать о мышечной слабости, «ватных» руках и/или ногах, онемении лица и нарушениях ритма сердца, что подтверждается данными ЭКГ.
Врач должен помнить о том, что довольно распространена и так называемая псевдогиперкалиемия – ложное повышение значений калия из‑за ошибок при сборе образцов крови, обращении с ними или по другим причинам, чаще всего – гемолиз в пробирке (при этом калий из разрушенных клеток попадает в плазму), слишком большое время наложения жгута или даже слишком сильное сжатие кулака пациентом. Также уровень калия может быть ложно повышен у пациентов с лейкоцитозом и/или тромбоцитозом. Так, концентрация калия по данным лаборатории может достигать 9 ммоль/л, но пациент при этом ни на что не жалуется, ЭКГ интактна. Перед началом агрессивного лечения гиперкалиемии следует подтвердить диагноз, особенно в случаях, когда не выявлены причины повышения уровня калия. Гиперкалиемия развивается вследствие почечной недостаточности, массивного разрушения клеток (рабдомиолиз, гемолиз, метаболический ацидоз, диабетический кетоацидоз и др.), избыточного внутривенного введения калия у пациентов без патологии почек, например, препаратов с высоким содержанием калия, или у пациентов на полном парентеральном питании, или после массивного переливания компонентов крови и т. д.
Изменения на ЭКГ при гиперкалиемии включают: уменьшение вольтажа зубца Р вплоть до его исчезновения, удлинение интервала РQ, увеличение вольтажа зубца R, расширение комплекса QRS, высокий симметричный («пикообразный») зубец Т. Типичные изменения ЭКГ, встречающиеся при различных значениях калия, приведены на рис. 2. Однако важно помнить о том, что скорость увеличения концентрации калия в крови имеет важное значение – изменения ЭКГ могут появляться и при меньших значениях, если процесс идет стремительно. Но и при хронической гиперкалиемии ЭКГ может выглядеть относительно нормальной.
Дополнительные тесты для определения причины гиперкалиемии могут включать в себя исследование уровней креатинина и мочевины, расчет скорости клубочковой фильтрации, анализы мочи для выявления патологии почек; общий анализ крови для определения уровня лейкоцитов и тромбоцитов; анализ на уровень глюкозы, газы крови и КЩС при подозрении на метаболический ацидоз или кетоацидоз; ЛДГ, КФК, КФК‑МВ, билирубин при подозрении на гемолиз и рабдомиолиз; также важно знать концентрацию кальция в крови, так как его дефицит может усугубить нарушения ритма сердца.
Влияние калия на ЭКГ. ЭКГ при гиперкалиемии и гипокалиемии
Влияние калия на ЭКГ. ЭКГ при гиперкалиемии и гипокалиемии
Гиперкалиемия ассоциируется с характерной последовательностью изменений на ЭКГ. Самое раннее проявление — сужение и заострение в виде шалаша вершины зубца Т.
Интервал QT на этой стадии укорачивается, соответствуя уменьшению ллительности ПД. Развивающаяся внеклеточная гиперкалиемия уменьшает мембранный потенциал покоя предсердий и желудочков, тем самым инактивируя натриевые каналы, которые снижают Vmax и скорость проведения. Комплекс QRS начинает расширяться, а амплитуда зубца Р снижаться. Может появиться удлинение интервала PR, за которым иногда слелует АВ-блокада II или III степени.
Полное исчезновение зубцов Р может быть связано с узловым замещающим ритмом или с так называемым синовентрикулярным проведением (при синовентрикулярном проведении отсутствует возбудимость миокарда предсердий при интактной проводящей системе.
При этом импульс от синусового узла проводится на желудочки через АВ-соединение с образованием псевдожелудочкового — без зубца Р на ЭКГ — ритма с узкими желудочковыми комплексами.
Это «скрытый синусовый ритм», учащающийся при нагрузке).
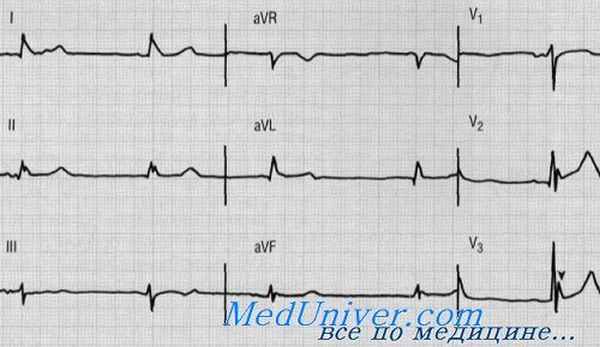
ЭКГ при гиперкалиемии
В более поздний период развития гиперкалиемии синусовый импульс проводится от СА-узла к АВ-узлу, но четкого зубца Р не образуется.
Умеренная и тяжелая гиперкалиемия иногда проявляется в виде элевации ST в правых грудных отведениях (V1 и V2) и симулирует ишемический ток повреждения или конфигурацию, наблюдаемую при синдроме Brugada. Однако даже тяжелая гиперкалиемия может иметь атипичные или недиагностируемые изменения па ЭКГ.
Очень выраженная гиперкалиемия при наличии некоторых дополнительных условий приводит к асистолии, иногда с предшествующим медленным волнообразным (синусоидальным) трепетанием желудочков.
Триада, состоящая из высоких, с заостренными вершинами зубцов Т (в результате гиперкалиемии), удлиненного QT (в результате гипокальциемии) и ГЛЖ (в результате артериальной гипертензии), является высоковероятным признаком хронической почечной недостаточности.
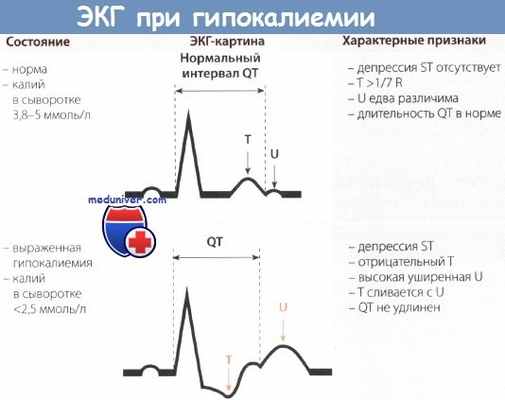
В результате электрофизиологических изменений, связанных с гипокалиемией, наоборот, происходит гиперполяризация мембран КМЦ и увеличивается длительность ПД. Основным ЭКГ-признаком этого отклонения от нормы является депрессия ST с уплощенными зубцами Т и увеличенными зубцами U. Зубцы U могут превышать амплитуду зубцов Т.
Клинически разделение зубца Т и зубца U на поверхностных ЭКГ может быть затруднено или даже невозможно. Видимый зубец U при гипокалиемии и других патологических условиях может быть, действительно, частью зубца Т, форма которого изменяется под влиянием градиента напряжения между М-клетками, или среднемиокардиальными клетками, и соседними миокардиальными слоями.
Удлинение реполяризании при гипокалиемии как часть синдрома приобретенного удлиненного QT(U) предрасполагает к возникновению тахикардии torsades de pointes. Гипокалиемия при приеме дигиталиса также повышает вероятность появления тахиаритмий.
Калий
К является основным катионом внутриклеточной жидкости, где содержится 98% калия всего организма. Kатион обеспечивает осмолярность цитоплазмы и создает условия для протекания в ней биохимических реакций. Поступление К в клетку через плазматическую мембрану определено многими факторами. Калиевые каналы обеспечивают пассивную проницаемость мембраны для катиона, при этом движение К определено величиной электрического потенциала и градиентом концентрации. Калиевые каналы могут находиться в открытом и закрытом состоянии, пассивный поток К в клетку определен именно количеством открытых в данный момент каналов. Высокая проницаемость мембран клеток для К, особенно в состоянии возбуждения, и «относительная непроницаемость» для Na, приводит к возникновению разности потенциалов на плазматической мембране.
Стабильность содержания К в организме является следствием сбалансирования процессов его поступления и выделения. Поступление К с пищей является самым важным в регуляции общего пула катиона. Взрослый человек потребляет ежедневно 80–100 ммоль К. От 85 до 90% К, принятого с пищей, экскретируют почки. При отсутствии К в пище в течение нескольких дней с мочой выделяется 40–60 ммоль/сутки, после чего потеря К с мочой уменьшается до 10–20 ммоль/сутки. 10–15% потребленного с пищей К выводится через ЖКТ. Этот путь выведения катиона может быть усилен в условиях гиперсекреции минералокортикоидов и почечной недостаточности. Через кожу значительное количество К может быть выделено только в случае интенсивного потоотделения.
Клетки нервной и мышечной систем быстро реагируют на снижение уровня К в плазме, что объясняет раннее появление симптоматики – гипотония мышц, слабость и астения, ослабление рефлексов. Некоторые случаи гипокалиемии приводят к явлениям паралича и даже рабдомиолиза. Выраженная гипокалиемия сопровождается возникновением нарушения проводимости и ритма сердечной деятельности, что отражается на ЭКГ (уменьшение амплитуды зубцов, инверсия зубца Т, расширение интервала S-Т и появление зубца U). При хроническом дефиците К увеличиваются размеры сердца, возникают нарушения ритма, при резком снижении уровня К в плазме возможна остановка сердца в систоле.
Симптомы гиперкалиемии зависят от скорости нарастания содержания катиона в плазме и связаны с изменением мембранного потенциала нейронов и мышечных клеток. Нейромышечные симптомы гиперкалиемии выражаются в парестезиях, а в более тяжелых случаях – в восходящем параличе конечностей. Выраженность кардиальных симптомов зависит от степени повышения К в плазме – от минимальных изменений ЭКГ до серьезных нарушений ритма и проводимости (поперечная блокада и фибрилляция желудочков). При концентрации К выше 6 ммоль/л, как правило, обнаруживают изменения ЭКГ (заострение зубца Т, удлинение зубца Р и интервала Р-R, расширение комплекса QRS, элевация или депрессия сегмента ST), которые при прогрессировании гиперкалиемии становятся все более выраженными. При уровне К выше 7 ммоль/л отмечено развитие аритмии сердца с летальным исходом, при концентрации К выше 10 ммоль/л сердце может остановиться в диастоле. В клинике продолжительная гиперкалиемия чаще всего является следствием хронической почечной недостаточности.
Калий в крови
В клинической биохимии обмен К оценивают на основании его содержания в плазме крови (внутрисосудистый пул), хотя в нем содержится не более 2% от общего количества катиона. Подавляющая часть К в организме находится внутри клеток, и его концентрация в плазме, которая лишь приблизительно отражает общее содержание элемента в организме, может колебаться в значительных пределах, особенно при тяжелых патологиях. Она тесно связана с состоянием кровообращения и кислотно-основным равновесием, поэтому определение К в плазме или сыворотке крови — один из важнейших показателей в период реанимации.
Существенное влияние на уровень К в плазме крови оказывает нарушение pH крови. Метаболический ацидоз вызывает перемещение ионов водорода внутрь клетки в обмен на внутриклеточный К, что приводит к снижению содержания калия в тканях. При алкалозе, напротив, наблюдается возрастание содержания К в тканях. На уровень К в плазме влияет содержание в крови аниона НСО3 -, которое отражает активность катаболических процессов.
Снижение концентрации калия в крови возникает при недостаточном поступлении К с пищей, усиленной потере почками (прием диуретиков, диуретическая стадия острой почечной недостаточности, тубулярный ацидоз, повышение секреции АДГ,. избыток минералокортикоидов и др.); увеличении потерь при рвоте или поносе, внутривенном введении больших объемов жидкости, не содержащей К, перераспределении К между вне- и внутриклеточной жидкостью (острый и хронический метаболический ацидоз, острый респираторный алкалоз, введение инсулина или глюкозы). Наиболее частой причиной гипокалиемии является повышенная потеря К почками, недостаточное потребление К редко вызывает гипокалиемию.
Гипокалиемия может иметь место у алкоголиков даже при небольшом повышении в крови содержания Na. Употребление больших количеств пива также приводит к гипокалиемии и гипонатриемии; в пиве содержится очень мало солей.
Гиперкалиемия может развиваться в случаях повышенного поступления К (прием избытка К при терапии диуретиками, парентеральное введение, переливание крови с просроченным сроком хранения), перераспределения К между водными пространствами (повреждение тканей, активация катаболических процессов, системный ацидоз), снижения выведения К+ (острая и хроническая почечная недостаточность, длительный прием калийсберегающих диуретиков, недостаточность минералкортикоидов).
Гиперкалиемия при недостаточности надпочечников сопровождается низким уровнем Na в плазме крови, гипокалиурией, высокой активностью ренина. Гиперкалиемия при селективной недостаточности альдостерона сопровождается низким уровнем ренина и нарушением содержания кортизола в крови. Нарушения метаболизма углеводов при острой и хронической почечной недостаточности провоцируют гиперкалиемию и метаболический алкалоз.
Частой причиной повышенного содержания К в плазме крови является несоблюдение условий взятия крови. Наиболее частая ошибка – гемолиз. При большом количестве тромбоцитов или лейкоцитов, что имеет место в случаях миэлопролиферативных заболеваний, может возникнуть псевдогиперкалиемия из-за повышенного выхода К из клеток.
Показания к исследованию
- Заболевания сердечно-сосудистой системы (аритмии, артериальная гипертензия);
- патология почек;
- недостаточность надпочечников;
- контроль терапии диуретиками, сердечными гликозидами;
- проведение гемодиализа.
Особенности взятия и хранения образца: сыворотка крови без признаков гемолиза. Взятие крови проводить с минимальным пережатием вены без мышечной нагрузки. Образцы стабильны не более 3 часов при комнатной температуре.
Метод исследования: определение концентрации ионов калия в крови в настоящее время проводят преимущественно ионоселективным методом.
Референтный интервал: 3,5 – 5,1 ммоль/л
Повышенные значения
- Гипоальдестеронизм первичный и вторичный;
- острая почечная недостаточность;
- прием ингибиторов АПФ; калийсберегающих диуретиков;
- диабетический кетоацидоз;
- повышенный распад клеток и тканей (внутрисосудистый гемолиз, рабдомиолиз, длительное голодание, судороги, тяжелые травмы, глубокие ожоги, разрушение опухолевых клеток);
- дегидратация.
Пониженные значения
- Гиперальдостеронизм первичный и вторичный;
- гиперкортицизм;
- нарушение функции почек;
- повышенная потеря калия через ЖКТ;
- гипергликемия;
- гипотермия;
- недостаток поступления калия в организм (хроническое голодание, анорексия).
Калий в моче
Ионы К свободно фильтруются через гломулярную мембрану. Содержание К в первичном фильтрате соответствует таковому в плазме крови, при учете различия в содержании белка. Далее 50–70% К реабсорбируется в проксимальном (извитом) сегменте нефрона. Экскреция К является результатом сочетания процессов фильтрации, реабсорбции и секреции. При патологии большое значение имеют экстраренальные пути выделения К. В условиях гиперкалиемии в извитых канальцах подавляется реабсорбция как К, так и воды.
Факторы, которые могут изменить электрохимический потенциал мембраны клеток извитого канальца, оказывают влияние на экскрецию К. К ним относятся: КОР, скорость протекания мочи по дистальному канальцу, действие минералокортикоидов, поступление нереабсорбируемых в дистальном канальце анионов бикарбоната (HCO3–) при почечном канальцевом ацидозе и др.
Альдостерон увеличивает поступление К в клетки и экскрецию его с мочой, контролируя реабсорбцию в дистальных канальцах. Гиперкалиемия, в свою очередь, стимулирует секрецию альдостерона. Введение большой дозы глюкокортикоидов вызывает гиперкалиемию и усиливает калийурез. Экскреция ионов К в почках имеет циркадный ритм, с минимумом в ночное время, она быстро возрастает в ответ на нагрузку катионом.
Увеличение выведения калия с мочой происходит при нарушениях КОР, приеме мочегонных средств. При недостаточности коры надпочечников экскреция К с мочой снижается и может развиться гиперкалиемия. В то же время, при гиперактивности коры надпочечников, гиперальдостеронизме, усиленная реабсорбция Na приведет к повышенному выделению К и угрожающей гипокалиемии (2,4–1,6 ммоль/л).
Показания к исследованию
- Заболевания сердечно-сосудистой системы (аритмии, артериальная гипертензия);
- патология почек;
- недостаточность надпочечников;
- контроль терапии диуретиками, сердечными гликозидами.
Метод исследования: определение концентрации ионов калия в моче проводят ионоселективным методом.
Изменения концентрации калия: гипер и гипокалиемия
Этот способ может применяться в сочетании с перемещением ионов калия внутрь клеток. 10% раствор кальция глюконата вводят внутривенно из расчета 50-100 мг/кг веса тела, что соответствует 0.5-1 мл на кг веса тела. Важно вводить раствор медленно в течение нескольких минут (желательно – не менее 20 минут), разведенный в физ. растворе. Цель применения препаратов кальция – снижение порогового потенциала и повышение разницы потенциалов между потенциалом покоя и пороговым потенциалом клеточной мембраны. Этот эффект виден в течение нескольких минут и длится примерно 20-30 минут. При этом необходим ЭКГ-мониторинг, чтобы выявить и не допустить развитие аритмий, вызываемых ионами кальция.
Усиление экскреции и «разбавление» – инфузионная терапия кристаллоидными растворами
Метод используется как вспомогательный для коррекции и предотвращения рецидива гиперкалиемии. Может применяться в сочетании с перемещением калия внутрь клеток. Ограничениями к использованию метода являются застойная сердечная недостаточность, а также гипоурия и анурия при острой почечной недостаточности. В случае необходимости использования инфузионной терапии при данных патологических состояниях следует тщательно контролировать центральное венозное давление с целью предупреждения объемной перегрузки.
Перитонеальный или гемодиализ
Применяется только при неэффективности предыдущих методов. К этому способу коррекции гиперкалиемии приходится прибегать крайне редко, так как в подавляющем большинстве случаев гиперкалиемию удается купировать с использованием ранее описанных способов.
Немаловажно отметить, что все рассмотренные меры будут малоэффективны в случае отсутствия коррекции основного заболевания. Более того, нередко встречаются болезни, при которых гиперкалиемию можно купировать исключительно посредством коррекции первопричины. Однако всегда следует отталкиваться от данных конкретного пациента, стойкости и степени выраженности гиперкалиемии.
Гипокалиемия
Противоположное гиперкалиемии состояние также может сопровождаться целым спектром нежелательных патологий и осложнений.
Ведущим клиническим признаком гипокалиемии является так называя миопатия, выражающаяся в слабости гладкой и поперечно-полосатой мускулатуры. Проявляться она будет мышечной слабостью, в том числе вентрофлексией, судорогами, угнетением, илеусом, задержкой мочи вследствие нарушения тонуса мочевого пузыря, неспособностью концентрировать мочу. В худшем случае возможны ишемия и последующий некроз мышц.
Всегда следует правильно интерпретировать концентрации ионов калия, способные привести к симптомам гипокалиемии. Биохимическая гипокалиемия не всегда тождественна клинически значимой. Так, концентрация калия в сыворотке крови < 3,5 мг-экв/л соответствует биохимической гипокалиемии кошек и собак. При этом симптомы гипокалиемической миопатии проявятся при концентрации ионов калия в сыворотке крови < 3.0 мг-экв/л у кошек и < 2.5 мг-экв/л у собак.
- Снижение потребления калия или его потери через ЖКТ.
- Повышенное перемещение калия внутрь клетки.
- Повышенная потеря калия с мочой.
- Лекарственные средства, способные вызвать гипокалиемию.
- Наследственная гипокалиемия бурманских кошек, которая проявляется в основном в возрасте от 2 до 12 месяцев.
Рассмотрим перечисленные выше причины подробнее
Снижение потребления калия или его потери через ЖКТ
- Анорексия.
- Рвота.
- Диарея.
- Снижение потребления калия наряду с введением растворов с пониженным содержанием калия.
Повышенное перемещение ионов калия внутрь клетки
Самая часто встречаемая причина гипокалиемии в этой группе носит ятрогенный характер – это инсулинотерапия. Как упоминалось ранее, инсулин способствует транспорту в цитоплазму клетки из сыворотки крови не только молекул глюкозы, но и ионов калия. У пациентов с диабетическим кетоацидозом при начале инсулинотерапии регистрируется наиболее тяжелая степень гипокалиемии. Соответственно, начиная лечение подобных пациентов, мы заведомо можем предполагать и профилактировать данное осложнение.
Кроме инсулина, из эндогенных и экзогенно вводимых гормонов к гипокалиемии способны привести также катехоламины. К выделению катехоламинов приводят тяжелые стрессовые ситуации и различные тяжелые болезни.
Из ятрогенных причин, помимо инсулинотерапии, гипокалиемию способно спровоцировать введение и других лекарственных средств: в повседневной клинической практике нередко гипокалиемию могут вызвать препараты глюкозы и бикарбоната натрия.
Гипокалиемический периодический паралич, редко встречаемый у бурманских кошек, также относится к указанной группе причин. Транспорт ионов калия внутрь цитоплазмы клеток усиливается также при гипотермии и алкалемии, сопровождающей некоторые болезни.
Повышенная потеря ионов калия с мочой
- Хроническая гипокалиемия может привести к развитию метаболического ацидоза.
- Сильная гипокалиемия ( < 1.5 ммоль/л) может привести к слабости дыхательной мускулатуры и неадекватной вентиляции легких или остановке дыхания.
- Влияние на сердце регистрируется не часто, для этой патологии характерны суправентрикулярные и желудочковые аритмии, удлинение интервала Q-T и появление зубцов U.
- Влияние на почки: гипокалиемия приводит к снижению восприимчивости канальцев к АДГ, повышению аммониогенеза.
- Повышение уровня креатинкиназы.
- Эхокардиографические находки: ↓ сократительной способности миокарда, ↓ сердечного выброса.
- ХБП.
- Инсулинотерапия.
- Быстро растущие новообразования.
- Гиперальдостеронизм.
- Алиментарные патологии.
- Гипертиреоз (который также приводит к потенциальному дефициту тиамина).
Анамнез (особое внимание следует уделить используемым ранее препаратам, в том числе средствам для седации)
↓
Клинические признаки, данные физикального исследования
↓
Исследования: биохимическое исследование сыворотки крови, ОКА, Т4 о, ГК, анализ мочи; ультразвуковое исследование брюшной полости; при необходимости – рентгенологическое исследование и другие методы визуальной диагностики.
Помимо гипокалиемии, к мышечной слабости может привести еще целый ряд заболеваний. В связи с этим нельзя отождествлять гипокалиемию и миопатию. В качестве дифференциальных диагнозов при наличии симптомов миопатии следует рассматривать следующие патологические состояния: гипогликемия; болезни сердца; респираторные болезни; полимиозит (включая токсоплазмоз); гипо- или гиперкальциемия; дефицит тиамина (вызывает в том числе вентрофлексию); миастения; анемия.
Терапия гипокалиемии показана только в случае наличия клинически значимой формы течения болезни: для кошек – при концентрации калия в сыворотке крови < 3 ммоль/л, для собак – < 2.5 ммоль/л. Вопрос, который стоит решить первостепенно, – это прекращение введения любых препаратов, применение которых может быть ответственно за развитие гипокалиемии (за исключением тех случаев, когда их использование не является жизненно необходимым). Безусловно, как и в случае с гиперкалиемией, мы не сможем рассчитывать на успех лечения, если своевременно не выявим и не попытаемся устранить причину гипокалиемии.
Профилактика гипокалиемии осуществляется путем внутривенного введения растворов, содержащих 14-20 мЭкв/л калия, что предотвращает развитие гипокалиемии.
- перитоните, вызванном панкреатитом;
- парвовирусном энтерите и панлейкопении;
- диабете (особенно в случае осложнения диабетическим кетоацидозом);
- постобструктивном диурезе;
- сниженном потреблении калия или потерях калия через ЖКТ;
- повышенном перемещении калия внутрь клетки;
- повышенной потере ионов калия с мочой;
- использовании препаратов, способных вызвать гипокалиемию.
В качестве вспомогательных можно использовать следующие данные для пересчета:
1 г калия хлорида = 13,4 мЭкв;
1 ммоль = 1 мЭкв = 39,1 мг элементарного калия;
1 г элементарного калия = 26,5 ммоль.
Расчет необходимого объема растворов с ионами калия проводится исходя из концентрации калия в сыворотке крови (см. таблицу №2):
В крайних ситуациях при неизвестной концентрации калия в сыворотке крови допустимо вводить препараты калия из расчета 40 ммоль калия на 1 л кристаллоидного раствора. В любом случае, какой бы формулой расчета мы ни воспользовались, скорость введения препаратов калия не должна превышать 0.5 мЭкв (ммоль)/кг/ч.
Рассмотрим расчет необходимого для введения объема препарата калия на клиническом примере:
Беспородная кошка в возрасте 9 лет с клинически значимой гипокалиемией на фоне инсулинотерапии при сахарном диабете 3-го типа (стероидиндуцированном), осложненном кетоацидозом (с симптомами рвоты, анорексии).
Данные о пациенте, необходимые для расчетов: вес 5.5 кг, концентрация калия в сыворотке крови – 1.8 ммоль/л.
Допустимая скорость инфузии калия – 0.5 мЭкв/кг/ч: 5.5 кг × 0.5 мЭкв = 2.75 мЭкв/час.
1 мл 10% раствора калия хлорида = 1.33 мЭкв калия хлорида (см. таблицу №1).
2.75 мЭкв калия хлорида = 2 мл 10% раствора калия хлорида (см. таблицу №1).
Таким образом, в течение часа вводим внутривенно капельно 2 мл 10% раствора калия хлорида (80 мг), разведенного физ. раствором. Инфузию продолжаем до достижения нормокалиемии и стабилизации состояния пациента.
В случае тяжелой гипокалиемии, угрожающей жизни пациента, может потребоваться болюсная инфузия. Также можно вводить препараты калия с высокой скоростью у пациентов с сильной гипокалиемией, которые не отвечают на терапию со скоростью 0.5 мЭкв/кг/ч. При введении болюса необходим постоянный контроль ЭКГ. Количество вводимого препарата калия рассчитывается по следующей формуле [1, с. 351]:
Общее количество KCl = (идеальный K+ – определенный K+ пациента) × определенный сосудистый объем пациента (л)
Идеальный K+ = 4.5 ммоль/л
Определенный сосудистый объем пациента (л) = масса тела × 60 мл (кошка) или 80 мл (собака).
Необходимое количество калия разводят в равном или двукратном объеме физ. раствора и вводят в яремную вену через центральный катетер в течение 10-15 минут. Введение в яремную вену позволяет избежать боли. При введении болюса в периферические вены возрастает риск флебита. Применение болюсной инфузии можно рассмотреть на следующем примере:
Беспородный кот в возрасте 10 лет с клинически значимой гипокалиемией и дыхательной недостаточностью в результате слабости дыхательной мускулатуры.
Идеальный K+ = 4.5 ммоль/л.
Определенный K+ пациента = 1.5 ммоль/л.
Определенный сосудистый объем (л) = вес пациента × 60 мл/кг массы тела = 2.8 кг × 60 мл (0.06 л) = 0.168 л.
Общее количество KCl = (4.5 ммоль/л – 1.5 ммоль/л) × 0.168 л = 3.0 ммоль/л × 0.168 л = 0.504 мЭкв.
0.504 мЭкв = 0.38 мл 10% раствора калия хлорида (см. таблицу № 1).
Полученный объем (0.38 мл) ввели с добавлением 1 мл физ. раствора в течение 10 минут в яремную вену.
Контроль концентрации калия в сыворотке крови в первое время лечения должен проводиться регулярно, чтобы определить ответ на проводимое лечение и избежать развития гиперкалиемии. Во время острой фазы лечения – не менее 1 раза в 12-24 часа. Отсутствие возможности мониторинга уровня калия в сыворотке крови является одной из причин неэффективности проводимого лечения.
Пероральное применение солей калия – это, пожалуй, самый безопасный способ коррекции гипокалиемии. К сожалению, этот способ не подходит в ситуации, когда требуется достаточно быстрое восполнение концентрации калия в сыворотке крови или в случае, когда применение пероральных лекарственных средств представляется невозможным (например, при рвоте, диарее, нарушении глотания). При пероральном применении солей калия крайне маловероятны передозировка и осложнение в виде гиперкалиемии, так как калий всасывается по градиенту концентрации. Но этот способ предпочтителен и незаменим в случае необходимости длительной терапии. Также он может быть использован в качестве метода выбора, если есть время на восполнение концентрации калия (то есть гипокалиемия не угрожает жизни) и нет относительных или абсолютных ограничений к использованию пероральных лекарственных средств. В этом случае кошка должна получать 2-6 ммоль в день с подбором дозы, основанной на ежедневном определении концентрации калия в сыворотке крови. Альтернативная доза составляет 0.5 мЭкв/кг массы тела каждые 12 часов до устранения причины и симптомов гипокалиемии. Текущая поддерживающая терапия требуется, если коррекция базового процесса болезни не представляется возможной. В зависимости от причины может быть необходимо длительное пероральное введение препаратов калия.
В качестве дополнительных средств корректировки гипокалиемии рекомендовано использовать также ИАПФ и калийсберегающие диуретики (антагонисты альдостерона). Однако к их применению приходится прибегать нечасто.
Ожидаемый ответ на проводимое лечение – это устранение мышечной слабости. Клиническое улучшение следует ожидать в течение 2-3 часов после начала внутривенного введения препаратов калия или в течение 1-3 дней после начала перорального применения солей калия.
Прогноз и устранение симптомов гипокалиемии зависит от основного заболевания. Неспособность устранить основное заболевание – самая главная причина неэффективности проводимого лечения. У бурманских кошек с гипокалемической полимиопатией болезнь может спонтанно пройти в возрасте 1-2 лет.
1. Макинтайр Д., Дробац К., Хаскингз С., Саксон У. Скорая помощь и интенсивная терапия мелких домашних животных. – М.: Аквариум, 2013. – 560 с.
2. Нельсон Р., Фельдман Э. Эндокринология и репродукция собак и кошек. – «Софион», 2008. – 1256 с.
3. Современный курс ветеринарной медицины Кирка /под ред. Дж. Д. Бонагура; пер. с англ. - М.: Аквариум-Принт, 2005. – 1376 с.
4. Торранс Э. Д., Муни К. Т. Эндокринология мелких домашних животных. – М.: Аквариум, 2006. – 311 с.
5. Kenneth J. Drobatz, Merilee F. Costello. Feline Emergency and Critical Care Medicine, 2010. – 672 p.
6. Mooney C. T., Peterson M. E. Canine and Feline Endocrinology. – BSAVA, 2004. – 248 p.
7. Silverstein D. C., Hopper K. Small Animal Critical Care Medicine, 2nd Edition. Saunders. – 2009. – 1152 p.
8. Stephen P. DiBartola. Fluid, Electrolyte and Acid-Base Disorders in Small Animal Practice. StLouis, ed. 3, – 2006 p.
9. Textbook of Small Animal Medicine. Editor, John K. Dunn. – W. B. Saunders, 1999. – 1065 p.
Читайте также:
