Воспаление тонкокишечного резервуара - резервуарит
Добавил пользователь Владимир З. Обновлено: 27.01.2026
Медикаментозное лечение болезни Крона и язвенного колита (являющихся частью группы воспалительных заболеваний кишечника – ВЗК) преследует две основные цели:
- Достижение ремиссии (отстутствие симптомов и воспаления в пораженной части желудочно-кишечного тракта)
- Поддержание ремиссии (предупреждение обострений).
Эти цели необходимо достичь с минимальным количеством побочных эффектов и с наименьшим возможным риском. Для этого задачей лечения является контроль воспаления в кишечнике – причины симптомов ВЗК.
Для лечения обострений ВЗК часто применяются антибиотики, хотя не было обнаружено инфекционных агентов, являющихся причиной этих заболеваний. По мнению многих исследователей, антибиотики помогают контролировать симптомы ВЗК, ослабляя кишечные бактерии и непосредственно подавляя иммунную систему кишечника. Также антибиотики могут быть эффективны при долгосрочном лечении пациентов(ок) с ВЗК (причем, это относится в большей степени к пациентам с болезнью Крона, нежели чем к больным язвенным колитом), особенно, если у них образовались свищи (каналы, соединяющие прилежащие петли кишку или кишку с другим органом, например, с кожей) или рецидивирующие асбцессы (скопления гноя).
Симптомы инфекций могут быть очень похожи на симптомы обострения, поэтому необходимо сделать анализ кала паразитов, в частности, на наличие кишечной лямблии, и на дисбактериоз, в особенности на наличие бактерии Clostridium difficile (с.diff), которая чаще возникает у больных ВЗК. Такие инфекции быстро лечатся с помощью антибиотиков, в состав которых входит метронидазол или ванкомицин. Новым антибиотиком для лечения c.diff является фидаксомицин.
Хотя многие антибиотики являются эффективными при борьбе с ВЗК, чаще всего выписывают:
- Метронидазол (Флагил®)
- Ципрофлоксацин (Ципро®)
- Рифаксимин (Ксифаксан®)
И метронидазол, и ципрофлоксацин являются антибиотиками широкого спектра действия, направленные на большой диапазон бактерий как внутри, так и снаружи кишок. Рифаксимин же не всасывается и поэтому оказывает непосредственное влияние только на бактерии желудочно-кишечного тракта. Метронидазол является самым активно изучаемым антибиотиком при лечении ВЗК. Являясь основным медикаментом при лечении обострений болезни Крона, действие этого препарата сильнее действия плацебо (пустышек) и соответствует сульфасалазину – особенно, когда болезнь поражает толстую кишку.
Метронидазол также снижает риск рецидива в течение первых трех месяцев после резекции подвздошной кишки. Метронидазол эффективен при лечении болезни Крона с поражением области промежности, как было выявлено у 50% пациентов.
И метронидазол, и ципрофлоксацин могут при необходимости вводиться внутривенно, и продаются в ампулах. Рифаксимин применяется только перорально.
Метронидазол: распространенными побочными эффектами являются тошнота, рвота, потеря аппетита, появление «металлического» привкуса во рту, диарея, головокружение, головные боли, окрашивание мочи (в темно-коричневый или красно-коричневый цвет). Другим побочным эффектом, возникающим вследствие долгосрочного приема медикамента, является дрожь в руках и ногах, которая может продолжаться даже после отмены препарата.
Ципрофлоксацин: побочные действия включают головные боли, тошноту, рвоту, диарею, боль в животе, сыпь, беспокойство – и являются редкими. Также наблюдались случаи тендинита (боли и воспаления сухожилий), в частности, поражающего ахиллово сухожилие (соединяющее икроножную мышцу с пяточной костью) и разрыва сухожилий.
Рифаксимин: побочные эффекты проявляются редко, но могут включать тошноту, боль в животе, головокружения, усталость, головные боли, напряженность мышц и боль в суставах.
Пациентам, принимающим одновременно несколько препаратов (по рецепту или безрецептурных) нужно внимательно изучить взаимодействие медикаментов между собой. Такое взаимодействие может уменьшить эффективность лекарственных средств, усилить действие препарата или спровоцировать необычные побочные эффекты. Перед приемом любых препаратов, необходимо тщательно ознакомиться с инструкцией. Необходимо поставиьт врача в известность обо всех принимаемых средствах (включая безрецептурные препараты, добавки и альтернативные лекарственные средства), а также обо всех имеющихся у пациента(ки) заболеваниях.
Метронидазол ослабляет распад спирта в организме, и это может привести к тошноте и рвоте. Поэтому необходимо избегать алкоголь в любой форме во время курса лечения этим препаратом, а также как минимум в течение как минимум двух дней после принятия последней дозы.
Ципрофлоксацин может взаимодействовать с антацидами (например, Ролаид, Тамс), что снижает его эффективность. Скорее всего, врач порекомендует не принимать эти два медикамента одновременно. Аналогичное взаимодействие наблюдается с витаминными и минеральными добавками, содержащими кальций, железо или цинк.
Если вы беременны, сообщите об этом врачу перед тем, как принимать метронидазол или ципрофлоксацин. Их часто прописывают беременным пациенткам, но все же рекомендуется сначала проконсультироваться с врачом. Несмотря на то, что рифаксимин плохо всасывается, его обычно не выписывают беременным.
Во время лечения ципрофлоксацином избегайте нахождения на солнце. Пользуйтесь солнцезащитным кремом днем и воздержитесь от посещения солярия.
Антибиотики плохо взаимодействуют с антикоагулянтами, такими как варфарин (Кумадин®), чрезмерно уменьшая свертываемость крови и увеличивая риск возникновения кровотечения. Может потребоваться изменение дозы варфарина. О том, что вы принимаете варфарин, необходимо сообщить врачу, который прописывает вам антибиотики.
Узнавайте как можно больше информации от врачей. Также можно воспользоваться достоверными интернет-ресурсами, веб-сайтами фармацевтических компаний.
5.6 Резервуарит и другие осложнения хирургического лечения с формированием тонкокишечного резервуара
Резервуарит представляет собой неспецифическое воспаление тонкокишечного резервуара и наиболее частое осложнение ИАРА. Частота его возникновения колеблется в широком диапазоне от 15 до 50% в течение 10 лет после формирования ИАРА в крупных специализированных центрах 116 , 117 , 118 . Такие различия могут быть обусловлены существенно большим риском резервуарита при ЯК, превышающим частоту этого осложнения при формировании ИАРА по поводу других заболеваний (в частности, семейного аденоматоза толстой кишки 119 , 120 ).
5.6.1. Диагностика резервуарита
Диагноз устанавливается на основании клинических симптомов, а также характерных эндоскопических и гистологических изменений (УД3а, СР B). Риск резервуарита по-видимому выше у некурящих и принимающих НПВС лиц, а также у пациентов с протяженным ЯК и внекишечными проявлениями (ПСХ) (УД3b, СРD).
К симптомам резервуарита относятся учащение дефекаций, в том числе и жидкими каловыми массами, спастические боли в животе, недержание стула (может быть и самостоятельным сипмтомом) и тенезмы. В редких случаях возможно появление лихорадки и внекишечных проявлений. Выделение крови не является характерным и, как правило, возникает при воспалении сохраненной слизистой оболочки прямой кишки (УД1с, СР В).
У пациентов с симптомами, соответствующими резервуариту, для подтверждения диагноза необходимо провести резервуароскопию с биопсией слизистой оболочки резервуара. У больных с илеоанальным резервуаром нередко имеется стриктура резервуаро-анального анастомоза, поэтому для резервуароскопии предпочтительнее использовать фистулоскоп, а не колоноскоп. Всегда следует предпринять попытку провести аппарат в приводящую петлю подвздошной кишки. Следует отметить, что при достижении клинической ремиссии рутинная резервуароскопия не требуется (УД5, СР D). Эндоскопические признаки, соответствующие резервуариту, включают диффузную эритему, которая может быть очаговой, в отличие от таковой при ЯК. Характерными эндоскопическими проявлениями также являются отек и зернистость слизистой оболочки, спонтанная и контактная кровоточивость, эрозии и изъязвления. Эрозии и/или язвы по линии скобок не обязательно свидетельствуют о резервуарите. Биоптаты следует брать из слизистой оболочки резервуара и приводящей петли над резервуаром, но не из линии скобок.
Гистологические проявления резервуарита также неспецифичны и включают признаки острого воспаления с полиморфоядерной лейкоцитарной инфильтрацией, крипт-абсцессами и изъязвлениями на фоне хронической воспалительной инфильтрации.
Осложнения резервуарита включают абсцессы, свищи, стеноз резервуаро-анального анастомоза и аденокарциному резервуара. Последнее осложнение встречается исключительно редко и почти всегда – при выявленной дисплазии или раке в операционном препарате, полученном при выполнении колэктомии.
Дифференциальный диагноз при подозрении на резервуарит проводится с синдромом раздраженного резервуара (СРР), ишемическими поражениями, болезнью Крона (БК) и другими редкими причинами дисфункции резервуара, такими как коллагенозный, цитомегаловирусный и Clostridium difficile-ассоциированный резервуарит. Следует учитывать возможность развития неспецифического илеита, вызываемого приемом НПВС и синдрома избыточного бактериального роста.
РЕЗЕРВУАРИТ ПОСЛЕ ФОРМИРОВАНИЯ ТОНКОКИШЕЧНЫХ РЕЗЕРВУАРОВ У БОЛЬНЫХ ЯЗВЕННЫМ КОЛИТОМ
Резервуарит является наиболее распространенным осложнением среди пациентов с тазовым тонкокишечным резервуаром (ТТР) и встречается почти у 50% больных хотя бы однажды в течение жизни. Тем не менее, можно констатировать, что острый резервуарит у большинства пациентов достаточно быстро и эффективно поддается лечению. Проблема подбора адекватной терапии для лечения хронических форм воспаления резервуара, составляющих почти 20% от всех резервуаритов, учитывая антибиотико-зависимость и антибиотико-резистентность, как факторов неблагоприятного прогноза в этой группе, является довольно актуальной. У многих больных лечение должно включать не только «индукционную» терапию, направленную на достижение ремиссии, но также и поддерживающую терапию. При неэффективности консервативного лечения и определении медикаментозной резистентности, следует исключить вторичные причины воспаления резервуара. По мере накопления опыта, анализа, понимания причин возникновения резервуарита с целью исключения неблагоприятных провоцирующих факторов, в дальнейшем можно ожидать снижение частоты резервуаритов у носителей ТТР. В то же время данная проблема далека от разрешения. Поэтому сохраняется необходимость в продолжении исследований в данном направлении.
Ключевые слова
Об авторах
Список литературы
1. Кашников, В.Н. Осложнения тонкокишечных резервуаров и их влияние на функциональные результаты и качество жизни больных, оперированных по поводу язвенного колита (обзор литературы). / В.Н.Кашников, С.И.Ачкасов, О.И.Сушков и соавт. // Колопроктология. - 2015. - №3 (53). -с. 84-91.
2. Сафин, А.Л. Факторы риска развития диареи, ассоциированной с Clostridium difficile, у колопроктологических больных (обзор литературы). / A.Л.Сафин, С.И.Ачкасов, М.А.Сухина и соавт. // Колопроктология. - 2017. - №1 (59). - с. 59-67.
3. Шелыгин, Ю.А. Единый лапароскопический доступ при многоэтапном хирургическом лечении пациента с язвенным колитом. / Ю.А.Шелыгин, С.И.Ачкасов, B.Н.Кашников и соавт.// Колопроктология. - 2013. -№3 (45) c. 30-34.
4. Abdelrazeq, A.S. Rifaximin-ciprofloxacin combination therapy is effective in chronic active refractory pouchitis. / A.S.Abdelrazeq et al. // Colorectal disease: the official journal of the Association of Coloproctology of Great Britain and Ireland. - 2005. - №2 (7). - р. 182-6.
5. Andersson, P. Surgery in ulcerative colitis: indication and timing. / P.Andersson, J.D.Söderholm // Digestive diseases (Basel, Switzerland). - 2009. - №3 (27). -р. 335-40.
6. Angriman, I. Relationship between pouch microbiota and pouchitis following restorative proctocolectomy for ulcerative colitis / I.Angriman, M.Scarpa, I.Castagliuolo // World Journal of Gastroenterology. - 2014. - №29 (20). - р. 9665.
7. Asha, N.J. Comparative Analysis of Prevalence, Risk Factors, and Molecular Epidemiology of Antibiotic-Associated Diarrhea Due to Clostridium difficile, Clostridium perfringens, and Staphylococcus aureus / N.J.Asha, D.Tompkins, M.H.Wilcox // Journal of Clinical Microbiology. - 2006. - №8 (44). - р. 2785-2791.
8. Bartlett, J.G. Antibiotic-Associated Pseudomembranous Colitis Due to Toxin-Producing Clostridia / J.G.Bartlett et al. // New England Journal of Medicine. - 1978. - №10 (298). - р. 531-534.
10. Casadesus, D. Possible role of human cytomegalovirus in pouchitis after proctocolectomy ней самих пациентов, врачей, участвующих в лечении этих больных, также может помочь в решении этой актуальной проблемы. with ileal pouch-anal anastomosis in patients with ulcerative colitis. / D.Casadesus et al. // World journal of gastroenterology. - 2007. - №7 (13). - р. 1085-9.
11. Coffey, J.C. Pathogenesis of and unifying hypothesis for idiopathic pouchitis. / J.C.Coffey et al. // The American journal of gastroenterology. - 2009. -№4 (104). - р. 1013-23.
12. Dalal, R.L. Management of Pouchitis and Other Common Complications of the Pouch / R.L.Dalal, B.Shen, D.A.Schwartz // Inflammatory Bowel Diseases. - 2018. - №5 (24). - р. 989-996.
13. Das, P. Assessment of the mucosa of the indefinitely diverted ileo-anal pouch / P.Das et al. // Colorectal Disease. - 2008. - №5 (10). - р. 512-517.
14. Eckburg, P.B. Diversity of the Human Intestinal Microbial Flora / P.B.Eckburg et al. // Science. -2005. - №5728 (308). - р. 1635-1638.
15. Fazio, V.W. Ileal pouch anal anastomosis: analysis of outcome and quality oflife in 3707 patients. / V.W.Fazio et al. // Annals of surgery. - 2013. - №4 (257). -р. 679-85.
16. Febo, G.Di. Endoscopic assessment of acute inflammation of the ileal reservoir after restorative ileoanal anastomosis. / G. Di.Febo et al. // Gastrointestinal endoscopy. - №1 (36). - р. 6-9.
18. Gionchetti, P. High-dose probiotics for the treatment of active pouchitis. / P.Gionchetti et al. // Diseases of the colon and rectum. - 2007. - №12 (50). -р. 2075-82; discussion 2082-4.
19. Gionchetti, P. Oral beclomethasone dipropionate in chronic refractory pouchitis. / P.Gionchetti et al. // Journal of Crohn's & colitis. - 2014. - №7 (8). -р. 649-53.
20. Gionchetti, P. Oral budesonide in the treatment of chronic refractory pouchitis / P.Gionchetti et al. // Alimentary Pharmacology & Therapeutics. - 2007. -№10 (25). - р. 1231-1236.
21. Herfarth, H.H. Use of Biologics in Pouchitis: A Systematic Review. / H.H.Herfarth, M.D.Long, K.L.Isaacs // Journal of clinical gastroenterology. -2015. - №8 (49). - р. 647 - 54.
22. Kazakova, S.V. A Hospital Outbreak of Diarrhea Due to an Emerging Epidemic Strain of Clostridium difficile / S.V.Kazakova et al. // Archives of Internal Medicine. - 2006. - №22 (166). - р. 2518.
23. Kienle, P. Association of decreased perfusion of the ileoanal pouch mucosa with early postoperative pouchitis and local septic complications. / P.Kienle et al. // Archives of surgery (Chicago, Ill.: 1960). 2001. - №10 (136). - p. 1124-30.
24. Kohyama, A. Bacterial population moves toward a colon-like community in the pouch after total proctocolectomy / A.Kohyama et al. // Surgery. -2009. - №4 (145). - p. 435-447.
26. Madden, M.V. Inflammation in ileal reservoirs: «pouchitis». / M.V.Madden, M.J.Farthing, R.J.Nicholls // Gut. - 1990. - №3 (31). - p. 247 - 9.
27. Madden, M.V. Double-blind crossover trial of metronidazole versus placebo in chronic unremitting pouchitis. / M.V.Madden, A.S.McIntyre, R.J.Nicholls // Digestive diseases and sciences. - 1994. - №6 (39). -p. 1193-6.
28. Mahadevan, U. Diagnosis and management of pouchitis. / U.Mahadevan, W.J.Sandborn // Gastroenterology. - 2003. - №6 (124). - p. 1636-50.
29. Mann, S.D. Clostridium difficile infection--an unusual cause of refractory pouchitis: report of a case. / S.D.Mann et al. // Diseases of the colon and rectum. - 2003. - №2 (46). - p. 267-70.
30. Mimura, T. Four-week open-label trial of metronidazole and ciprofloxacin for the treatment of recurrent or refractory pouchitis. / T.Mimura et al. // Alimentary pharmacology & therapeutics. - 2002. -№5 (16). - p. 909-17.
32. Moskowitz, R.L. An assessment of inflammation in the reservoir after restorative proctocolectomy with ileoanal ileal reservoir. / R.L.Moskowitz, N.A.Shepherd, R.J.Nicholls // International journal of colorectal disease. - 1986. - №3 (1). - p. 167-74.
33. Munoz-Juarez, M. Misdiagnosis of specific cytomegalovirus infection of the ileoanal pouch as refractory idiopathic chronic pouchitis: report of two cases. / M.Munoz-Juarez et al. // Diseases of the colon and rectum. - 1999. - №1 (42). - p. 117-20.
34. Navaneethan, U. Impact of budesonide on liver function tests and gut inflammation in patients with primary sclerosing cholangitis and ileal pouch anal anastomosis. / U.Navaneethan et al. // Journal of Crohn's & colitis. - 2012. - №5 (6). - p. 536-42.
35. Navaneethan, U. Secondary Pouchitis: Those With Identifiable Etiopathogenetic or Triggering Factors / U.Navaneethan, B.Shen // The American Journal of Gastroenterology. - 2010. - №1 (105). - p. 51-64.
36. Ohge, H. et al. Association Between Fecal Hydrogen Sulfide Production and Pouchitis / H.Ohge et al. // Diseases of the Colon & Rectum. - 2005. - №3 (48). -p. 46 9 -475.
37. Onaitis, M.W. Ileal pouch-anal anastomosis for ulcerative colitis and familial adenomatous polyposis: historical development and current status. / M.W.Onaitis, C.Mantyh // Annals of surgery. - 2003. -№6 Suppl (238). - p. S42-8.
38. Pardi, D.S. Clinical guidelines for the management of pouchitis / D.S.Pardi et al. // Inflammatory Bowel Diseases. - 2009. - №9 (15). - p. 1424-1431.
39. Parsi, M.A. Fecal lactoferrin for diagnosis of symptomatic patients with ileal pouch-anal anastomosis / M.A.Parsi et al. // Gastroenterology. -2004. - №5 (126). - p. 1280-1286.
40. Sambuelli, A. Budesonide enema in pouchitis--a double-blind, double-dummy, controlled trial. / A.Sambuelli et al. // Alimentary pharmacology & therapeutics. - 2002. - №1 (16). - p. 27-34.
41. Sandborn, W.J. Pouchitis after ileal pouch-anal anastomosis: a Pouchitis Disease Activity Index. / W.J.Sandborn et al. // Mayo Clinic proceedings. -1994. - №(69). - p. 409-15.
42. Sandborn, W.J. Pouchitis following ileal pouchanal anastomosis: definition, pathogenesis, and treatment. / W.J.Sandborn // Gastroenterology. -1994. - №6 (107). - p. 1856-60.
43. Sandborn, W.J. Clinical management of pouchitis. / W.J.Sandborn, D.S.Pardi // Gastroenterology. - 2004. -№6 (127). - p. 1809-14.
44. Sartor, R.B. Microbial Influences in Inflammatory Bowel Diseases / R.B.Sartor // Gastroenterology. -2008. - №2 (134). - p. 577-594.
45. Scarpa, M. et al. Relationship between mucosa-associated microbiota and inflammatory parameters in the ileal pouch after restorative proctocolectomy for ulcerative colitis / M.Scarpa et al. // Surgery. - 2011. -№1 (150). - p. 56-67.
46. Scarpa, M. TLR2 and TLR4 Up-regulation and Colonization of the Ileal Mucosa by Clostridiaceae spp. in Chronic/Relapsing Pouchitis / M.Scarpa et al. // Journal of Surgical Research. - 2011. - №2 (169). -p. e145-e154.
47. Sekirov, I. Gut Microbiota in Health and Disease / I.Sekirov et al.// Physiological Reviews. - 2010. -№3 (90). - p. 859-904.
48. Shen, B. Endoscopic and histologic evaluation together with symptom assessment are required to diagnose pouchitis. / B.Shen et al. // Gastroenterology. - 2001. - №2 (121). - p. 261-7.
49. Shen, B. A randomized clinical trial of ciprofloxacin and metronidazole to treat acute pouchitis. / B.Shen et al. // Inflammatory bowel diseases. - 2001. -№4 (7). - р. 301-5.
50. Shen, B. Irritable pouch syndrome: a new category of diagnosis for symptomatic patients with ileal pouchanal anastomosis. / B.Shen et al. // The American journal of gastroenterology. - 2002. - №4 (97). - p. 972-7.
51. Shen, B. Collagenous pouchitis / B.Shen et al. // Digestive and Liver Disease. - 2006. - №9 (38). -р. 704-709.
52. Shen, B. Clostridium Difficile-Associated Pouchitis / B.Shen et al.// Digestive Diseases and Sciences. - 2006. - №12 (51). - p. 2361-2364.
54. Shen, B. Effect of Withdrawal of Nonsteroidal Anti-Inflammatory Drug Use on Ileal Pouch Disorders / B.Shen et al. // Digestive Diseases and Sciences. - 2007. - №12 (52). - p. 3321-3328.
55. Shen, B. A Proposed Classification of Ileal Pouch Disorders and Associated Complications After Restorative Proctocolectomy / B.Shen et al. // Clinical Gastroenterology and Hepatology. - 2008. - №2 (6). -p. 145-158.
56. Shen, B. Rifaximin for maintenance therapy in antibiotic-dependent pouchitis / B.Shen et al. // BMC Gastroenterology. - 2008. - №1 (8). - p. 26.
57. Shen, B. Clostridium difficile Infection in Patients With Ileal Pouch-Anal Anastomosis / B.Shen et al. // Clinical Gastroenterology and Hepatology. - 2008. -№7 (6). - p. 72-788.
58. Shepherd, N.A. Restorative proctocolectomy with ileal reservoir: pathological and histochemical study of mucosal biopsy specimens. / N.A.Shepherd et al. // Journal of clinical pathology. - 1987. - №6 (40). p. 601-7.
59. Shepherd, N.A. Distribution of mucosal pathology and an assessment of colonic phenotypic change in the pelvic ileal reservoir. / N.A.Shepherd et al. // Gut. -1993. - №1 (34). - p. 101-5.
60. Stahlberg, D. Pouchitis following pelvic pouch operation for ulcerative colitis. Incidence, cumulative risk, and risk factors. / D.Stahlberg et al. // Diseases of the colon and rectum. - 1996. - №9 (39). - p. 1012-8.
61. Stallmach, A. Fecal Microbiota Transfer in Patients With Chronic Antibiotic-Refractory Pouchitis. / A.Stallmach et al. // The American journal of gastroenterology. - 2016. - №3 (111). - p. 441-3.
63. Swidsinski, A. Spatial organization of bacterial flora in normal and inflamed intestine: a fluorescence in situ hybridization study in mice. / A.Swidsinski et al. // World journal of gastroenterology. - 2005. -№8 (11). - p. 1131-40.
64. Tamboli, C.P. Dysbiosis as a prerequisite for IBD. / C.P.Tamboli et al. // Gut. - 2004. - №7 (53). - p. 1057.
65. Thapa, D. Clotrimazole Ameliorates Intestinal Inflammation and Abnormal Angiogenesis by Inhibiting Interleukin-8 Expression through a Nuclear Factor -B-Dependent Manner / D.Thapa et al. // Journal of Pharmacology and Experimental Therapeutics. -2008. - №2 (327). - p. 353-364.
66. Zwolinska-Wcislo, M. Effect of Candida colonization on human ulcerative colitis and the healing of inflammatory changes of the colon in the experimental model of colitis ulcerosa. / M.Zwolinska-Wcislo et al. // Journal of physiology and pharmacology: an official journal of the Polish Physiological Society. - 2009. -№1 (60). - p. 107-18.
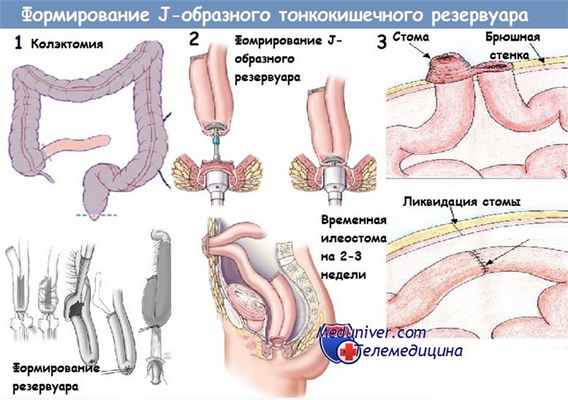
Воспаление тонкокишечного резервуара - резервуарит
Воспаление тонкокишечного резервуара - резервуарит
Проктоколэктомия с реконструкцией - метод выбора при хирургическом лечении больных с рефрактерным к терапии язвенным колитом или признаками его злокачественной трансформации, а также при САТК. Превосходный общий результат и удовлетворенность больных с ожидаемой частотой дефекаций от 4 до 8 раз в день, хорошей функцией держания, способностью задерживать дефекацию до достижения социально приемлемых условий (туалета), возможностью работать и улучшением качества жизни.
Илеоанальная дисфункция расценивается как неудача лечения, направленного на достижение вышеперечисленных целей, и бывает острой, рецидивирующей или хронической. Резервуарит - наиболее частое осложнение в отдаленном периоде после проктоколэктомии с реконструкцией или континентных илеостом, сформированных по поводу язвенного колита, а также наиболее частая причина илеоанальной дисфункции при интактном резервуаре. Патогенез неясен (избыточное размножение бактерий или дисбаланс флоры, повышенная концентрация сульфидов, аутоиммунные процессы при ВЗК, нутритивные причины и т.д.).
Слабая корреляция между морфологическими (эндоскопическими) и функциональными параметрами => для постановки диагноза резервуарита руководствуются клиническими критериями:
• Интактный резервуар, включенный в пассаж кишечного содержимого.
• Внезапное изменение клинического течения (начало диареи, лихорадка, недомогание, императивные позывы, инконтиненция).
• Отсутствие признаков стриктуры в резервуаре или тазовых симптомов болезни Крона, абсцессов в полости таза, свища резервуара.
• Отрицательные бактериологические исследования.
• Быстрый ответ на антибиотики (метронидазол, ципрофлоксоцин, рифаксимин). Индекс активности резервуарита: шкала, основанная на клинических, эндоскопических и гистологических параметрах.
а) Эпидемиология. Язвенный колит: у 40-50% больных возникает, по крайней мере, один эпизод резервуарита; у 60% больных, перенесших одну атаку резервуарита, в дальнейшем возникают рецидивные эпизоды; у 5-10% больных в течение десяти лет развивается устойчивая к терапии дисфункция => риск потери резервуара. При САТК риск резервуарита ниже (10-15%).
б) Симптомы резервуарита:
• Первичные симптомы: диарея, усиливающаяся/непереносимая частота стула или императивных позывов, превышающая «нормальную» частоту дефекаций (4-8 раз в день), инконтиненция или подтекание кишечного содержимого, газообразование, отхождение слизи и крови.
• Вторичные симптомы: перианальный дерматит с/без экскориаций —> перианальная/периректальная боль, зуд/жжение.
• Системные симптомы: лихорадка, возможна гриппоподобная симптоматика, в частности при остром начале заболевания; вспышка внекишечных проявлений.
в) Дифференциальный диагноз резервуарита:
• Резервуарит: неспецифическое воспаление в тонкокишечном резервуаре неизвестной этиологии и наиболее частое нежелательное явление после технически успешно выполненной проктоколэктомии с реконструкцией. Выявляется по:
1) клиническим критериям, таким как учащение стула, диарея, газообразование, гриппоподобные симптомы;
2) морфологическим критериям, таким как воспаление слизистой, изъязвления.
• Синдром раздраженного резервуара: такие же симптомы, как и при резервуарите, но полное отсутствие воспалительных изменений.
• Воспаление анальной переходной зоны (АПЗ) в культе прямой кишки: морфологически нормальное состояние резервуара («резервуарография», «резервуароскопия») при значительном остром и хроническом воспалении АПЗ в культе прямой кишки с/без изъязвления => свечи с месалазином или стероидами местно, мукозэктомия с низведением резервуара в анальный канал при рефрактерном воспалении.
• Специфическая инфекция в резервуаре: С. difficile, кандидоз, цитомегаловирус => специфическое лечение.
• Недостаточный объем резервуара: техническая проблема (слишком короткие колена, неполное рассечение перегородки между ними) или следствие наружного или внутреннего сдавления (абсцесс, десмоид, опухоль в резервуаре и т.д.) => аугментация (операция, направленная на увеличение объема) резервуара или формирование резервуара заново, полное разделение перегородки (трансанально с помощью эндоскопического линейного степлера), удаление резервуара из полости таза без повторного низведения в зависимости от этиологических факторов.
• Пролапс резервуара (при ИРА с тонкокишечным резервуаром или при континентной илеостоме) => резервуаропексия, резекция выпавшего участка, формирование резервуара заново.
• Стриктура: результат длительно существующей несостоятельности анастомоза, ишемии сегмента, постлучевых изменений, образования десмоида => лечение с помощью повторных бужирований, стриктуропластики, формирование резервуара заново.
• Свищ: результат несостоятельности анастомоза, болезни Крона, криптогландулярное происхождение => повторное отключение от пассажа, дренирование, реанастомозирование резервуара с поворотом вокруг собственной оси, коллагеновая пломба, низведение лоскута, интерпозиция мышцы.
• Патологическая полость (синус): результат отграниченной несостоятельности анастомоза => марсупиализация или объединение с резервуаром, или формирование резервуара заново.
• Полип резервуара => рак в резервуаре. Профилактика: адекватное наблюдение за состоянием резервуара, если возник рак => онкологическая резекция и дальнейшее клиническое сопровождение.
• Обструкция отводящего сегмента резервуара: резервуар низкого давления сформирован проксимальнее области высокого давления, например S-образный резервуар с длинным отводящим коленом, J-резервуар, анастомозированный с длинной культей прямой кишки => функциональная обструкция или органическая стриктура => хирургическое вмешательство или поддерживающие меры (введение трубок, регуляция стула).
• Болезнь Крона: частота 2-7% случаев. Диагностика трудна: воспаление слизистой/изъязвление тонкой кишки проксимальнее сформированного резервуара, свищ резервуара или другие перианальные осложнения спустя 3 месяца после закрытия временной илеостомы.
г) Патоморфология
Макроскопическое исследование:
• Диффузная или очаговая эритема и токсическая зернистость, «смазанность» сосудистого рисунка, ранимость слизистой с тенденцией к кровотечению, экссудат, очаговые изъязвления, афтоидные изменения; хотя изменения обычно диффузные, задние отделы резервуара более подвержены стазу кишечного содержимого и воспалительные изменения в них могут быть более выраженными; приводящая петля тонкой кишки интактна, в противном случае следует подозревать болезнь Крона.
Микроскопическое исследование:
• Зависит от течения и активности резервуарита: воспалительные инфильтраты различной степени выраженности (хронические: лимфо-/плазмоцитарные; острые/ подострые: нейтрофильные и эозинофильные), поверхностные острые (нейтрофилы) и хронические (лимфоциты) очаговые изъязвления слизистой с фибриноидным экссудатом.
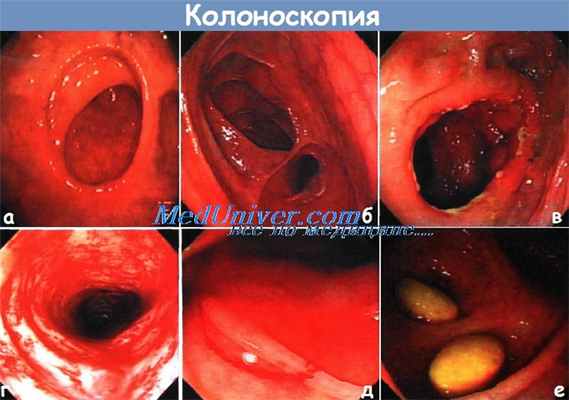
а - Нормальная эндоскопическая картина анастомоза толстой кишки типа «конец в конец».
б - Нормальная конфигурация мешковидного расширения при колоанальной пластике.
в - Образование язвы в области анастомоза после резекции вследствие рака.
Язва доброкачественного характера вызвана шовным материалом, рецидива рака нет.
г - Ложный колит — неспецифическое воспаление дистальнее нефункционирующей стомы, у больного без заболеваний прямой кишки в анамнезе.
д - Обычная травма с кровотечением сразу после неприцельной биопсии слизистой оболочки для исключения микроскопического колита у больного с поносом.
е - При колоноскопии видны нераспавшиеся и невсосавшиеся таблетки.
д) Обследование при резервуарите
Необходимый минимальный стандарт:
• Клиническое обследование (осмотр): раздражение перианальной кожи с/без экскориаций. Пальцевое обследование прямой кишки: стриктура, признаки свища и т.д.
• Резервуароскопия (ригидная или гибким эндоскопом): оценка состояния слизистой АПЗ в культе прямой кишки и резервуаре (подозрение на болезнь Крона, только если есть изъязвления в приводящей петле тонкой кишки).
• Рентгеноконтрастные исследования => форма резервуара, несостоятельность, патологические полости, свищ, стриктура, конфигурация, объем и размер резервуара, расстояние до крестцового изгиба.
Дополнительные исследования (необязательные):
• Дефекография, проктография/резервуарография: конфигурация, пролапс.
• КТ/МРТ, возможно, с 3D реконструкцией: наружные проблемы (сдавление, абсцесс и т.д.).
• Посевы из резервуара (при рефрактерных к лечению или рецидивных эпизодах): токсин С. difficile, кандида, цитомегаловирус, посевы кала (Salmonella, Shigella, Е. coli, Campylobacter и т.д.).
е) Классификация:
• Идиопатический резервуарит: острый, рецидивный, хронический.
• Специфический резервуарит: идентифицируемая/подлежащая лечению микробная инфекция.
• Органическая илеоанальная дисфункция.
ж) Лечение без операции резервуарита
Общие меры:
• Улучшение ухода за перианальной кожей: барьерные кремы, избегать увлажнения, кремы на вазелиновой основе обычно уменьшают секрецию. Тяжелые кожные экскориации/изъязвления => аппликации смеси Маалокса с порошком нистатина до наступления улучшения.
• Увеличение дозы или смена антидиарейных препаратов, добавление клетчатки.
• Оптимизация диеты и режима питания.
Специфические меры:
1. Резервуарит
а. Начальное эмпирическое лечение при подозрении на резервуарит:
1) Антибиотикотерапия (например, метронидазол, ципрофлоксоцин, рифаксимин) в течение 10-14 дней.
2) Оптимизация диеты, антидиарейных препаратов (дифеноксилат/атропин, лоперамид, гликопирролат (робинул)), защита перианальной кожи.
б. Варианты лечения при рецидиве резервуарита:
1) Пролонгированная поддерживающая антибиотикотерапия как описано выше, но со сниженной дозой (внимание: полинейропатия, обусловленная приемом метронидазола), альтернативные схемы антибиотикотерапии.
2) Специфический резервуарит => коррекция схемы антибиотикотерапии в зависимости от результатов посева.
3) Назначение пероральных препаратов висмута.
4) Антибиотик.
5) Клизмы с месаламином.
2. Стриктура: бужирование => пальцевое или бужами (например, расширителем Гегара), катетером Фолея (амбулаторно), или самостоятельное бужирование с помощью дилататоров (дорого) или свечей (дешевый метод).
3. Воспаление культи прямой кишки: свечи с месаламином.
4. Обструкция функционирующего колена: введение трубки для эвакуации, возможна комбинация с клизмами.
з) Операция при резервуарите.
Показания:
• Неэффективность неоперативного лечения с неприемлемым качеством жизни.
• Органическая илеоанальная дисфункция.
Хирургический подход:
1. Трансанальный доступ:
• Исследование под анестезией.
• Бужирование стриктуры.
• Мукозэктомия АПЗ.
• Местные операции по поводу свища.
• Рассечение перегородки степлером.
• Марсупиализация патологической полости.
2. Абдоминальный доступ:
• Ревизия резервуара, формирование резервуара заново.
• Резервуаропексия.
• Удаление резервуара => концевая илеостома или континентная илеостома.
и) Результаты лечения резервуарита. В зависимости от причины илеоанальной дисфункции: 5-10% резервуаров удаляются в течение каждого десятилетия. Риск периферической нейропатии при длительном применении метронидазола.
к) Наблюдение:
• Тщательное ведение больных после проведенного лечения.
• Обследование резервуара один или два раза в год.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Язвенный колит
Язвенный колит – хроническое воспалительно-язвенное заболевание слизистой оболочки толстой кишки, чаще всего проявляющееся кровянистой диареей. Есть вероятность внекишечных проявлений, в особенности артритов. Отдаленный прогноз характеризуется повышенным риском развития рака толстой кишки, по сравнению с неподверженными данному заболеванию лицами. Диагноз основывается на данных колоноскопии. Лечение подразумевает назначение 5-аминосалициловой кислоты, кортикостероидов, иммуномодуляторов, биологических препаратов, антибиотиков, в части случаев – хирургическое вмешательство.
Патофизиология язвенного колита
Язвенный колит, как правило, начинается с поражения прямой кишки. Процесс может оставаться локализованным на этом уровне (язвенный проктит) или распространяться в проксимальном направлении, в ряде случаев поражается вся толстая кишка. В редких случаях колит с самого начала охватывает большую часть толстой кишки.
Воспаление в рамках язвенного колита затрагивает слизистую оболочку и подслизистый слой, характерно наличие четкой границы между здоровой и пораженной тканью. Мышечный слой поражается только при тяжелом течении. На ранних стадиях болезни слизистая оболочка эритематозна, поверхность покрыта мелкими гранулами, легко ранима, нормальный сосудистый рисунок исчезает, часто определяются рассеянные геморрагические элементы. Для тяжелых форм характерны крупные изъязвления слизистой с обильным гнойным отделяемым. Островки относительно сохранной или воспаленной гиперплазированной слизистой (псевдополипы) выступают над изъязвленной поверхностью. Формирования свищей и абсцессов не наблюдается.
Токсическый колит
Токсический, или фульминантный, колит наблюдается при трансмуральном распространении язвенного процесса, при котором развивается локальный илеус и перитонит. В течение от нескольких часов до нескольких дней, толстая кишка теряет мышечный тонус и начинает расширяться.
Термины токсический мегаколон и токсическое расширение толстой кишки не рекомендуются, т. к. состояние токсического воспаления и его осложнения могут протекать без развития явного мегаколона (признаком последнего служит увеличение диаметра поперечной ободовой кишки > 6 см во время обострения).
Токсический колит – неотложное состояние, развивающееся, как правило, спонтанно при очень тяжелом течении колита, но может быть спровоцировано приемом опиоидов или антидиарейных препаратов антихолинергического действия. Такое состояние несет риск перфорации толстой кишки, существенно повышающий вероятность летального исхода.
Симптомы и признаки язвенного колита
У пациентов обычно наблюдаются
Приступы геморрагической диареи различной выраженности и продолжительности сменяются периодами отсутствия симптомов.
Как правило, атака начинается неожиданно, с появления неотложных позывов на дефекацию, неинтенсивной схваткообразной боли внизу живота, примеси крови и слизи в стуле. В части случаев симптомы обострения развиваются на почве инфекции (амебиаза, шигеллеза).
При язвенном поражении ректосигмоидного отдела стул может быть нормальным либо плотным и сухим, однако при дефекации или между эпизодами опорожнения кишечника отмечаются выделения слизи с кровью и лейкоцитами. Системные проявления отсутствую или слабовыражены.
При более проксимальном распространении язвенного процесса стул становится неоформленным, с частотой > 10 в день, нередко – с выраженной схваткообразной болью и мучительными тенезмами, продолжающимися и в ночное время. Испражнения могут быть водянистыми, содержать слизь или полностью состоять из крови и гноя.
Токсический, или фульминантный, колит манифестирует внезапным появлением тяжелой диареи, повышением температуры до 40 ° С, боли в животе, признаков перитонита (в частности, феномена «рикошетной болезненности»), выраженной интоксикации.
Диагностика язвенного колита
Микробиологическое исследование и микроскопия кала (с целью исключения инфекционной патологии)
Сигмоскопия с биопсией
Начало болезни
Заподозрить язвенный колит позволяют типичные симптомы, в особенности в сочетании с внекишечными проявлениями и при указании на предшествующие сходные атаки. Язвенный колит следует дифференцировать от болезни Крона Болезнь Крона Болезнь Крона – хроническое воспалительное заболевание кишечкика с трансмуральным характером поражения, преимущественно поражающее дистальную часть подвздошной и толстой кишки, при котором также. Прочитайте дополнительные сведенияВ каждом случае показано культуральное исследование кала на патогенную кишечную микрофлору Этиология Гастроэнтерит представляет собой воспаление слизистой оболочки желудка, тонкой и толстой кишок. В большинстве случаев оно связано с инфекцией, но может развиваться вследствие воздействия лекарств. Прочитайте дополнительные сведения , также необходимо исключать наличие Entamoeba histolytica в свежих образцах кала. Если данные анамнеза (эпидемиологическая обстановка, поездки) дают основания подозревать амебиаз Амебиаз Амебиаз – инфекция, вызываемая Entamoeba histolytica. Он приобретается путем фекально-оральной передачи. Инфекция обычно бессимптомна, но могут проявляться симптомы и в пределах от умеренной. Прочитайте дополнительные сведения , необходимо проводить гистологическое и серологическое исследования. Указания на предшествующее применение антибиотиков или пребывание в стационаре делают необходимым оценку кала на наличие токсинов Clostridioides difficile (ранее Clostridium difficile). Пациентов из групп риска необходимо исследовать на ВИЧ-инфекцию, гонорею, инфекцию вирусом герпеса, хламидиоз и амебиаз. В условиях иммуносупрессии следует исключить оппортунистические инфекции (в частности, цитомегаловирусную, Mycobacterium avium-intracellulare) и саркому Капоши. У женщин возможно развитие колита, индуцированного оральными контрацептивами; как правило, он разрешается самопроизвольно после прекращения приема препаратов. Исследование стула на лактоферрин и фекальный кальпротектин может быть полезным для дифференциации ВЗК от функциональной диареи.
Необходимо проводить сигмоскопию, т.к. данное исследование позволяет подтвердить наличие колита, взять слизь и кал для культурального и микроскопического исследования, а также материал для гистологического исследования из пораженных участков. Хотя эндоскопия и биопсия могут не дать диагностической информации (различные типы колита имеют сходные черты), все же острый саморазрешающийся инфекционный колит, как правило, имеет гистологические отличия от хронического идиопатического язвенного колита и болезни Крона. Тяжелое перианальное поражение, щадящее поражение прямой кишки, выделения крови и несимметричный или сегментарный характер поражения толстой кишки в большей степени свидетельствуют в пользу наличия болезни Крона, чем в пользу язвенного колита. Необходимость проведения колоноскопии возникает в отдельных случаях, когда воспаление распространяется проксимальнее уровня достижения сигмоскопа.
Лабораторные исследования проводят с целью выявления анемии, гипоальбуминемии, электролитного дисбаланса. Необходимо оценить печеночные тесты; повышение активности щелочной фосфатазы и гамма-глутамилтранспептидазы могут указывать на наличие первичного склерозирующего холангита. Анализ на перинуклеарные антитела к цитоплазме нейтрофилов относительно специфичен для язвенного колита (60–70%). Антитела к Saccharomyces cerevisiae относительно специфичны для болезни Крона. Однако эти исследования не позволяют надежно различить ЯК и БК и не рекомендованы для применения в ежедневной практике. Также возможно наличие лейкоцитоза, тромбоцитоза и повышения острофазовых показателей (например, скорости оседания эритроцитов, С-реактивного белка).
При рентгеновском исследовании можно выявить патологические изменения, но сложно поставить точный диагноз. При рентгенографии брюшной полости определяется отек слизистой, сглаженность гаустраций и отсутствие оформленных каловых масс в пораженной толстой кишке. При ирригоскопии изменения выявляются более отчетливо, также могут обнаруживаться изъязвления, однако исследование нельзя проводить в острую фазу болезни. По истечении нескольких лет болезни может определяться укороченная, ригидная ободочная кишка с атрофией слизистой или наличием псевдополипов. Рентгенологические признаки «отпечатка большого пальца» и сегментарный характер поражения в большей степени характерны для ишемического колита или возможно болезни Крона, чем для язвенного колита.
Рецидивирующие проявления
При уже установленном диагнозе и развитии типичных симптомов следует провести осмотр пациента, расширенное обследование требуется не всегда. В зависимости от продолжительности и выраженности обострения проводят сигмоскопию или колоноскопию и общий анализ крови. Анализ кала на яйца глист и паразитов, токсин C. difficile необходимо проводить в случае атипичной симптоматики, обострении после периода длительной ремиссии, при вспышках инфекций, после применения антибиотиков или при подозрении на наличие этой причины кишечных симптомов.
Острые тяжелые приступы
При внезапном тяжелом обострении пациенты нуждаются в срочной госпитализации. Проводится рентгенография брюшной полости в горизонтальном и вертикальном положении; на снимках могут определяться признаки мегаколона – скопление газа в просвете протяженного сегмента кишечника, находящегося в паралитическом состоянии в результате потери способности гладкомышечных клеток к поддержанию тонуса. Проведения колоноскопии и ирригоскопии следует избегать из-за опасности перфорации, но тщательная сигмоидоскопия рекомендуется для оценки тяжести и исключения инфицирования. Следует проводить исследование общего анализа крови, определение уровней тромбоцитов, скорости оседания эритроцитов, С-реактивного белка, электролитов и альбумина. В случаях тяжелого кровотечения также показано исследование протромбинового времени, частичного тромбопластинового времеени, групы крови и резус-фактора.
Состояние пациента необходимо внимательно контролировать для выявления признаков развивающегося перитонита или перфорации. Оценка печеночной тупости методом перкуссии позволяет выявить первый клинический признак свободной перфорации – исчезновение тупости, особенно у пациентов, получающих лечение кортикостероидами в высоких дозах, что «стирает» симптомы раздражения брюшины. Каждые 1–2 дня проводят рентгенографию брюшной полости для контроля состояния расширенного участка кишечника и выявления свободного или внутристеночного газа; КТ более чуствительная в определении внепросветного газа или околоободочного абсцесса.
Читайте также:
