Что значит дс ифа вич агат

Иммуноферментный анализ (ИФА) — метод лабораторной диагностики, позволяющий обнаруживать специфические антитела и антигены при самых разных патологиях.
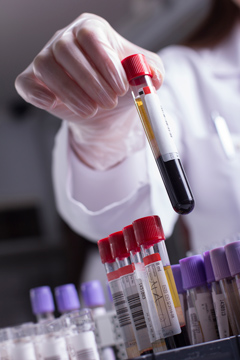
ИФА — один из самых распространенных и точных методов для выявления инфекций, передающихся половым путем, в частности ВИЧ, ВПЧ, гепатита В.

Для того чтобы результаты анализов были максимально достоверными, необходимо правильно подготовиться к их сдаче.

Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
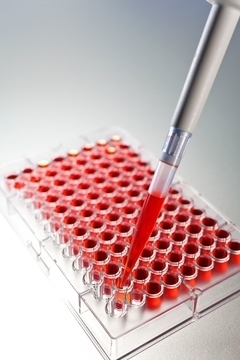
Контроль качества лабораторных исследований, осуществляемый по международным стандартам, — дополнительная гарантия точности результатов анализов.
Современная диагностика в медицине немыслима без высокочувствительных лабораторных анализов. Прежде для установления причин тех или иных симптомов врачи были вынуждены ориентироваться на косвенные признаки болезни, а также проводить многоступенчатые микроскопические исследования в попытке обнаружить возбудителя инфекции. Сегодня достаточно одного-единственного теста — такого как иммуноферментный анализ — чтобы подтвердить или опровергнуть первоначальный диагноз.
Основные понятия и принцип метода иммуноферментного анализа
Существует несколько разновидностей антител, каждая из которых вступает в действие на определенном этапе иммунного ответа. Так, первыми в ответ на проникновение антигена в организм синтезируются иммуноглобулины класса М (IgM). Содержание этих антител наиболее высоко в первые дни инфекционного процесса.
Следом за ними иммунная система выбрасывает в кровь иммуноглобулины класса G (IgG), которые помогают уничтожать антигены до полной победы над инфекцией, а также продолжают циркулировать по сосудам в дальнейшем, обеспечивая иммунитет к повторному заражению. На этом явлении основана вакцинация: благодаря прививкам, содержащим ослабленные антигены микробов и вирусов, в нашей крови появляется большое количество IgG, которые при контакте с реальной угрозой быстро подавляют инфекцию — до того, как она нанесет вред здоровью.
Как узнать, какие именно антигены или антитела присутствуют в организме человека? Когда врач предполагает, что причиной заболевания является определенная инфекция, или желает измерить концентрацию определенного гормона, он назначает пациенту иммуноферментный анализ.
ИФА бывает качественным и количественным. В первом случае подразумевается однозначный ответ: искомое вещество или найдено, или не найдено в образце. В случае с количественным анализом более сложная цепь реакций дает возможность оценить концентрацию антител в крови человека, что в сравнении с результатами предыдущих тестов даст ответ на вопрос о том, как развивается инфекционный процесс.
Бесспорные преимущества ИФА — высокая чувствительность и специфичность метода. Чувствительность — это возможность распознать искомое вещество, даже если его концентрация в образце невысока. Специфичность же подразумевает безошибочность диагностики: если результат положительный, значит, найдены именно те антитело или антиген, которые предполагались, а не какие-то другие.
Высокая степень технологичности проведения иммуноферментного анализа минимизирует влияние человеческого фактора, что снижает вероятность ошибки. Большинство используемых в современных лабораториях тест-систем и реактивов для ИФА выпускаются в промышленных условиях, что гарантирует точный результат.
В случае диагностики инфекционных заболеваний иммуноферментный анализ не может найти возбудителя и определить его специфичные свойства: он лишь указывает на наличие антител в крови у больного, косвенно свидетельствующих о присутствии чужеродного микроорганизма в теле человека.
ИФА — крайне точный, но не дешевый метод, поэтому обращаться к нему нужно с умом, а интерпретацией результатов должен заниматься квалифицированный врач.
Невозможно охватить полный список показаний к проведению ИФА. Вот наиболее распространенные цели анализа:
- Диагностика острых и хронических инфекционных заболеваний:
- IgM и IgG к вирусным гепатитам А, B, C, E, а также антигенов гепатитов В и С;
- IgG к ВИЧ;
- Ig M и IgG к цитомегаловирусной инфекции;
- Ig M и IgG к вирусу Эпштейна-Барр;
- Ig M и IgG к герпетическим инфекциям;
- Ig M и IgG к токсоплазмозу;
- Ig M и IgG к кори, краснухе, сальмонеллезу, дизентерии, клещевому энцефалиту и другим заболеваниям;
- IgG к паразитарным заболеваниям;
- Ig M и IgG к инфекциям, передающимся половым путем;
- IgG к хеликобактерной инфекции.
- Общая оценка показателей иммунитета человека и маркёров некоторых аутоиммунных заболеваний.
- Выявление онкологических маркёров (фактора некроза опухоли, простатспецифического антигена, раково-эмбрионального антигена и других).
- Определение содержания гормонов в сыворотке крови (прогестерона, пролактина, тестостерона, тиреотропного гормона и других).
Основной биоматериал для проведения ИФА — это сыворотка крови: в лаборатории у пациента берут образец крови из вены, из которого в дальнейшем удаляют форменные элементы, затрудняющие проведение анализа. В некоторых других случаях для анализа используется спинномозговая жидкость, околоплодные воды, мазки слизистых оболочек и т.д.
Для того чтобы избежать искажений в результатах, рекомендуется сдавать кровь натощак, а за две недели до исследования (если целью является диагностика хронических, скрыто протекающих инфекционных заболеваний) необходимо отказаться от приема антибиотиков и противовирусных препаратов.
При наличии необходимых реактивов и хорошей организации работы лаборатории результат анализа вы получите в течение 1–2 суток после забора крови. В некоторых случаях, при необходимости получения экстренного ответа, этот срок может быть сокращен до 2–3 часов.
- IgM — наличие этого класса иммуноглобулинов говорит об остром инфекционном процессе в организме. Отсутствие IgM может говорить как об отсутствии конкретного возбудителя в организме, так и о переходе инфекции в хроническую стадию.
- IgA при отрицательном результате теста на IgM чаще всего свидетельствует о хронической или скрыто протекающей инфекции.
- IgM и IgA (совместное присутствие) — два положительных результата говорят о разгаре острой фазы заболевания.
- IgG говорит либо о хронизации заболевания либо о выздоровлении и выработке иммунитета к инфекционному агенту.
В зависимости от содержания анализа в бланке могут быть представлены данные в виде таблицы с перечислением всех антител или антигенов с пометками об отрицательной или положительной реакции, либо будет указано количественное значение результата (отрицательный, слабоположительный, положительный или резко положительный). Последний вариант определяет, сколько антител содержится в анализируемом образце.
Еще один количественный показатель — индекс авидности антител, выраженный в процентах. Он указывает, сколько времени прошло от начала инфекционного процесса (чем выше индекс — тем больше).
Сегодня выпускаются тысячи видов тест-систем ИФА, позволяющих обнаруживать специфические антитела и антигены при самых разных патологиях. Поэтому этот анализ используется практически во всех медицинских отраслях. Диагноз, поставленный с помощью ИФА, — это гарантия назначения адекватной терапии и эффективного лечения заболевания.
Информативность ИФА делает этот анализ важным инструментом в работе многих медицинских центров. Но можно ли доверять такую диагностику государственным лабораториям или лучше самим выбрать, где провести такое исследование?
НАИМЕНОВАНИЕ ТЕСТ-СИСТЕМ
КРАТКОЕ ОПИСАНИЕ
Тест-система иммуноферментная для выявления антител к вирусам иммунодефицита человека l и ll типов в сыворотке и плазме крови человека.
Суммарное время инкубаций – 2 ч.
Срок годности – 12 мес.
Подходит для ручной постановки и постановки на автоматических анализаторах.
Тест-система иммуноферментная для выявления (подтверждения) антигена ВИЧ-1 (р 24) в сыворотке и плазме крови человека. Чувствительность – 0,5 пг/мл.
Суммарное время инкубаций – 1 ч 55 мин. (шейкер).
Срок годности – 12 мес.
Подходит для ручной постановки и постановки на автоматических анализаторах.
Тест-система иммуноферментная для одновременного выявления антител к ВИЧ-1 и ВИЧ-2, ВИЧ-1 группы О и антигена ВИЧ-1 (р24) в сыворотке и плазме крови человека.
Чувствительность по р24 – 10 пг/мл.
Суммарное время инкубаций – 1 ч 25 мин. (шейкер),1 ч 50 мин. (термостат).
Срок годности – 12 мес.
Подходит для ручной постановки и постановки на автоматических анализаторах.
Тест-система иммуноферментная для идентификации суммарных антител к отдельным белкам ВИЧ-1 – gp 41 env , gp 120 env , p 31 pol , ВИЧ-1 группы О gp 41 env , ВИЧ-2 gp 36 env и выявления антигена ВИЧ-1 (р24) в сыворотке и плазме крови человека. Чувствительность по р24 – 5 пг/мл. Одностадийный вариант.
Суммарное время инкубаций – 1 ч 25 мин. (шейкер), 2 ч 20 мин. (термостат).
Срок годности – 18 мес.
Тест-система иммуноферментная для одновременного выявления антител к вирусу иммунодефицита человека 1 и 2 типов (ВИЧ-1 и ВИЧ-2), ВИЧ-1 группы О и антигена ВИЧ-1 (р-24) в сыворотке (плазме) крови человека.
Чувствительность по p 24 – 5 пг/мл.
Суммарное время инкубаций – 1 ч 35 мин.
Срок годности – 18 мес.
Подходит для ручной постановки и постановки на автоматических анализаторах.
НАИМЕНОВАНИЕ ТЕСТ-СИСТЕМ
КРАТКОЕ ОПИСАНИЕ
Тест-система иммуноферментная для выявления антител к вирусам иммунодефицита человека l и ll типов в сыворотке и плазме крови человека.
Суммарное время инкубаций – 2 ч.
Срок годности – 12 мес.
Подходит для ручной постановки и постановки на автоматических анализаторах.
Тест-система иммуноферментная для выявления (подтверждения) антигена ВИЧ-1 (р 24) в сыворотке и плазме крови человека. Чувствительность – 0,5 пг/мл.
Суммарное время инкубаций – 1 ч 55 мин. (шейкер).
Срок годности – 12 мес.
Подходит для ручной постановки и постановки на автоматических анализаторах.
Тест-система иммуноферментная для одновременного выявления антител к ВИЧ-1 и ВИЧ-2, ВИЧ-1 группы О и антигена ВИЧ-1 (р24) в сыворотке и плазме крови человека.
Чувствительность по р24 – 10 пг/мл.
Суммарное время инкубаций – 1 ч 25 мин. (шейкер),1 ч 50 мин. (термостат).
Срок годности – 12 мес.
Подходит для ручной постановки и постановки на автоматических анализаторах.
Тест-система иммуноферментная для идентификации суммарных антител к отдельным белкам ВИЧ-1 – gp 41 env , gp 120 env , p 31 pol , ВИЧ-1 группы О gp 41 env , ВИЧ-2 gp 36 env и выявления антигена ВИЧ-1 (р24) в сыворотке и плазме крови человека. Чувствительность по р24 – 5 пг/мл. Одностадийный вариант.
Суммарное время инкубаций – 1 ч 25 мин. (шейкер), 2 ч 20 мин. (термостат).
Е. Н. БАРАНОВА, И. Н. ШАРИПОВА, Е. Н. КУДРЯВЦЕВА, О. А. ЛОБАНОВА, В. Ф. ПУЗЫРЕВ,
С. А. РЯБИНИНА, А. Н. БУРКОВ, А. П. ОБРЯДИНА, Т. И. УЛАНОВА
Московский областной научно-исследовательский клинический институт
Серологическая диагностика ВИЧ инфекции в России строится на выявлении суммарного спектра антител против антигенов ВИЧ c помощью иммуноферментных тест-систем
3 поколения, либо на одновременном выявлении антител и вирусного антигена р24 тест-системами 4 поколения. Для верификации результатов ИФА в России используют метод иммунного блоттинга (ИБ), который позволяет выявлять антитела к отдельным белкам ВИЧ.
Одной из основных проблем лабораторной диагностики ВИЧ инфекции является
-
Ранняя и поздняя стадии ВИЧ инфекции, когда уровень антител низкий, в ИБ выявляются антитела только IgG класса, а подтверждение наличия антигена р24 не предусмотрено; Кросс-реактивность между ВИЧ-1 и ВИЧ-2; Кросс-реактивность c другими антигенами, не связанными с ВИЧ
для раздельного выявления антител к отдельным белкам ВИЧ 1 и 2 типов и антигена
р24 в анализируемом образце.
Результаты и обсуждение. Действующим началом разработанной тест-системы являются: рекомбинантные антигены, аналогичные структурным белкам ВИЧ-1 – gp120 (env), p24 (gag), p31 (pol), gp41 (env) ВИЧ-1 и ВИЧ-1 группы О, ВИЧ-2 – gp36 (env); моноклональные антитела мыши к антигену ВИЧ-1 р24 gag, сорбированные раздельно на стрипах
полистиролового разборного планшета; конъюгаты – рекомбинантные антигены и
моноклональные антитела, меченые биотином и стрептавидин, меченый пероксидазой.
поэтапным внесением конъюгатов, что позволило значительно увеличить чувствительность анализа за счет процесса амплификации сигнала при взаимодействии биотина со стрептавидин-пероксидазой. Разработана система визуальной оценки внесения всех компонентов и образцов. Отсутствие этапа промывания планшета между двумя стадиями позволило сделать постановку анализа более удобной и сократить общее время анализа до 1 ч 25 мин.
(2 образца) при первичном тестировании в ИБ. При исследовании в динамике эти образцы продемонстрировали в ИБ позитивный результат.
Труды конференции «Эпидемиология, диагностика и профилактика вирусных гепатитов. Современное состояние, С.-Петербург, 5-6 октября 2006.- С.
Аннотация научной статьи по наукам о здоровье, автор научной работы — Шарипова Ирина Николаевна, Ходак Н. М., Пузырев В. Ф., Бурков А. Н., Уланова Т. И.
Похожие темы научных работ по наукам о здоровье , автор научной работы — Шарипова Ирина Николаевна, Ходак Н. М., Пузырев В. Ф., Бурков А. Н., Уланова Т. И.
The comparative study of specificity of test-systems in diagnostic of HIV-ifnection on categories of samples of blood serum of pregnant women
Шарипова И.Н., Ходак Н.М., Пузырев В.Ф., Бурков А.Н., Уланова Т.И.
сравнительное исследование специфичности тест-систем для диагностики вич-инфекции на категории образцов сывороток Крови беременных женщин
Ключевые слова: ВИЧ-инфекция; специфичность; образцы сывороток крови беременных женщин. Sharipova I.N., KhodakN.M., Puzirev V.F., Burkov A.N., Ulanova T.I.
THE COMPARATIVE STUDY OF SPECIFICITY OF TEST-SYSTEMS IN DIAGNOSTIC OF HIV-INFECTION ON CATEGORIES OF SAMPLES OF BLOOD SERUM OF PREGNANT WOMEN
The R&D production complex «Diagnostic systems’, Nizhnii Novgorod, Russia
Keywords: HIV-infection; specificity; sample; blood serum’ pregnant woman.
В нормативных документах ВОЗ [1] и Евросоюза [2] указаны пределы минимально допустимого уровня специфичности для скрининговых тестов на основе иммуноферментного анализа (ИФА): > 98 и 99,5% соответственно. В настоящее время использование ИФА-тест-систем для одновременного выявления специфических антител (АТ) к ВИЧ-1 и ВИЧ-2, а также антигена р24 ВИЧ-1 является стандартным методом лабораторной диагностики ВИЧ-инфекции. Достаточно хорошо известен перечень факторов, которые не связаны с ВИЧ-инфекцией, но могут способствовать возникновению ложноположительных реакций (ЛПР) при ИФА-диагностике [3]. Наиболее значимые причины ЛПР в ИФА-диагностике ВИЧ-инфекции приведены в табл. 1.
Однако это не означает, что все вышеперечисленные факторы непременно приводят к ЛПР. Многое зависит от конструктивных особенностей используемого теста, времени воздействия инородных антигенов, в том числе возбудителей
Шарипова Ирина Николаевна, нач. участка отработки технологии диагностикумов
Адрес: 603093, Нижний Новгород, ул. Яблоневая, 22, а/я 69 E-mail: sharipovain@npods.ru
инфекционных заболеваний, на человека. Чем шире набор АТ в организме человека, тем выше вероятность наличия нескольких перекрестно реагирующих АТ. Особенно часто это наблюдают у потребителей инъекционных наркотиков. Их организм просто перегружен антигенами.
Согласно приказу Минздрава РФ от 19.12.03 № 606 [4] и приказу Минздравсоцразвития РФ от 30.05.05 № 375 [5], тестирование на ВИЧ включено в перечень рутинных лабораторных анализов, рекомендованных для обследования беременных женщин. Сыворотки крови беременных в лабораториях традиционно считают сложными, при их исследовании на ВИЧ высока вероятность получения ЛПР. Это связывают с тем, что во время гестации в крови женщин изменяются микроэлементный состав, концентрация цитокинов и гормонов, а кроме того, формируются специфические белки беременности 6. Нередко ложноположительные результаты на ВИЧ при беременности отмечают у женщин с наличием в анамнезе инфекционных, аутоиммунных и хронических соматических заболеваний. Для того чтобы выяснить, является ли проблема получения ЛПР проблемой только для какой-то конкретной тест-системы или она присуща всем тестам на ВИЧ, провели исследование образцов сывороток крови беременных с использованием трех тест-систем четвертого поколения для диагностики ВИЧ-инфекции.
ИММУНОЛОГИЯ Таблица 1
Перечень факторов, являющихся причинами лПр ИФА-тестов для диагностики ВИЧ-инфекции
1. Факторы, ассоциированные с другими инфекциями
Респираторные инфекции верхних дыхательных путей Острые вирусные инфекции, в том числе вызванные ДНК-содержащими
Лепра IgM к вирусу гепатита А
Туберкулез IgM к ядерному антигену вируса гепатита В
Инфекция, вызванная Mycobacterium avium Ку-лихорадка (с сопутствующим гепатитом)
Инфекция, вызванная вирусом простого герпеса 1-го и 2-го Инфекции, вызванные другими ретровирусами типов (ВПГ-1, ВПГ-2)
Грипп Инфекция, вызванная вирусом Эпштейна-Барр
Малярия Висцеральный лейшманиоз
Недавно перенесенная вирусная инфекция
2. Факторы, связанные с иммунизацией
Вакцинация против гриппа Пассивная иммунизация: введение иммуноглобулинов
Вакцинация против гепатита В Использование препаратов иммуноглобулинов, изготовленных до 1985 г.
Вакцинация против столбняка
3. Факторы, связанные с системными аутоиммунными заболеваниями и реакциями
Аутоиммунные заболевания: системная красная волчанка, Высокий уровень циркулирующих иммунных комплексов системная склеродермия, дерматополиомиозит
4. Факторы, связанные с присутствием АТ в крови Антикарбогидратные АТ АТ к гладкой мышечной ткани
Нормальные (естественные) АТ АТ к париетальным клеткам желудка
Гипергаммаглобулинемия Нормальные рибонуклеопротеины человека
Антилимфоцитарные АТ АТ HLA (к антигенам лейкоцитов классов I и II)
Антимитохондриальные АТ АТ к антигенам Т-клеточных лейкоцитов
Антинуклеарные АТ АТ с высокой способностью связываться с полистиролом (используют в
Антимикросомальные АТ АТ к коллагену (определяют у мужчин, практикующих секс с мужчинами,
у больных гемофилией и у больных лепрой)
5. Факторы, связанные с потенциально кросс-реактивными реакциями Беременность (особенно у неоднократно рожавших женщин) ЛПР в других тестах, включая RPR-тест на сифилис Гемолизированные образцы сыворотки крови Кросс-реактивность неясного генеза у здоровых людей Образцы сыворотки крови с гиперлипемией Загрязнение фильтровальной бумаги веществами белковой природы Образцы сыворотки крови, подвергшиеся тепловой обработке Анальный секс
6. Факторы, связанные с гемотрансфузией и трансплантацией органов
Гемотрансфузии, особенно множественные Терапия препаратами а-интерферона пациентов, находящихся на гемодиализе
Трансплантация органов (в том числе почек) Гемодиализ/почечная недостаточность
7. Факторы, связанные с неинфекционными болезнями и новообразованиями Первичный склерозирующий холангит Гемофилия
Первичный билиарный цирроз Злокачественные новообразования лимфоидной, кроветворной и род-
ственных им тканей/лимфома
Алкогольный гепатит/алкогольное поражение печени Злокачественные новообразования (рак)
Гипербилирубинемия Миеломная болезнь
Синдром Стивенса-Джонсона Рассеянный склероз
Цель настоящей работы — сравнительная оценка специфичности ИФА-тест-систем для диагностики ВИЧ-инфекции при исследовании образцов сывороток крови беременных женщин.
Материалы и методы. Исследование образцов сывороток крови беременных женщин проводили с использованием
Характеристика ИФА-тест-систем, используемых в исследовании
Тест Формат теста Набор АТ и антигенов Чувствительность при выявлении антигена р24 ВИЧ-1 Время проведения анализа
результаты исследования образцов сывороток крови беременных
различных лечебно-профилактических учреждений Нижнего Новгорода.
Результаты и обсуждение. При первичном исследовании 440 образцов сывороток крови беременных во всех трех тест-системах выявили первично позитивные образцы: 15 образцов
коэффициент позитивности (КП)
16 1,3 0,8 0,92 — Отрицательный
44 21,6 25,4 11,0 Полный блот Положительный
52 6,3 0,4 0,27 — Отрицательный
98 20,7 24,8 11,4 Полный блот Положительный
99 0,05 0,22 5,3 р34/31 Неопределенный
101 9,4 0,18 0,4 — Отрицательный
115 0,08 0,14 1,02 — «
130 19,6 24,8 11,4 Полный блот Положительный
131 0,13 2,8 3,8 р55 Неопределенный
136 0,1 1,1 2,5 — Отрицательный
181 14,3 26,3 11,4 Полный блот Положительный
244 1,56 0,29 0,32 — Отрицательный
320 15,6 21,6 12,2 Полный блот Положительный
370 6,0 0,32 0,28 — Отрицательный
412 15,0 22,7 11,0 Полный блот Положительный
416 0,13 1,2 1,12 — Отрицательный
Выводы. 1. При исследовании образцов сывороток крови беременных в тест-системах, выявляющих маркеры ВИЧ-инфекции, специфичность тестов разных производителей совпадает и составляет 98,64% (95% доверительный интервал 97,06-99,37).
2. Результаты, полученные при исследовании трех тестов на ВИЧ, показали, что ЛПР присущи всем тест-системам, при этом спектр ЛП-образцов может различаться. Следует отметить, что не существует ИФА со 100% специфичностью.
3. Предложен альтернативный подход к решению вопроса ЛПР на ВИЧ при скрининговом исследовании образцов сывороток крови беременных женщин — последовательное использование двух тест-систем четвертого поколения с различным форматом постановки реакции.
1. World Health Organization. HIV assays operational characteristics: HIV rapid diagnostic tests (detection of HIV-1/2 antibodies): report 17; 2013.
2. Commission decision of 3 February 2009 amending Decision 2002/364/ EC on common technical specifications for in vitro-diagnostic medical devices. Off Jof theEuropean Union. 2009; 39: 34-49.
3. Johnson C. Whose antibodies are they anyway? Continuum. 1996; Sept./Oct.
6. Никулина Д.М. Минорный белок сыворотки крови — связанный с беременностью альфа2-гликопротеин: теоретические и практические аспекты: Дис. Москва; 2008.
7. Спиридонова Н.В., Балтер Р.Б. Прогнозирование развития гесто-за с помощью многомерного математического анализа. Вестник СамГУ- Естественнонаучная серия. 2007; 2 (52): 264-76.
8. Чистякова Г.Н., Газиева И.А., Ремизова И.И., Черданцева Г.А., Черешнев В.А. Оценка цитокинового профиля при физиологической и нормально протекающей беременности. Цитокины и воспаление. 2007; 6 (1): 3-8.
9. Chao T.T., Sheffield J.S., Wendel G.D. Jr., Ansari M.Q., McIntire D.D., Roberts S. W. Risk factors associated with false positive HIV test results in a low-risk urban obstetric population. J. Pregnancy. 2012; 2012: 841979.
10. Doran T.I., Parra E. False-positive and indeterminate human immunodeficiency virus test results in pregnant women. Arch. Fam. Med. 2000; 9(9): 924-9.
11. Wesolowski L.G., Delaney K.P., Lampe M.A., Nesheim S.R. False-positive human immunodeficiency virus enzyme immunoassay results in pregnant women. PLoS One. 2011; Jan 27; 6(1): e16538.
12. Евстигнеев И.В. Лабораторные методы диагностики острой, ранней и текущей ВИЧ-инфекции. Клиническая иммунология. Аллергология. Инфектология. 2012; 4: 34-40.
1. World Health Organization. HIV assays operational characteristics: HIV rapid diagnostic tests (detection of HIV-1/2 antibodies): report 17; 2013.
2. Commission decision of 3 February 2009 amending Decision 2002/364/EC on common technical specifications for in vitro-diagnostic medical devices. Off J of the European Union. 2009; 39: 34-49.
3. Johnson C. Whose antibodies are they anyway? Continuum. 1996; Sept./Oct.
Полный текст:
Целью работы являлось сравнение пяти наиболее широко используемых на территории Российской Федерации тест-систем ИФА для обнаружения антител к вирусу иммунодефицита человека.
4. Hemelaar J. Implications of HIV diversity for the HIV-1 pandemic. J. Infect., 2013 May, Vol. 66, No. 5, pp. 391–400. URL: DOI: 10.1016/j.jinf.2012.10.026.
5. Gaudy C., Moreau A., Brunet S., Descamps J.M., Deleplanque P., Brand D., Barin F. Subtype B human immunodeficiency virus (HIV) type 1 mutant that escapes detection in a fourth generation immunoassay for HIV infection. J. Clin. Microbiol., 2004, Vol. 42, pp. 2847–2849. 6. Ly T.D., Plantier J.C., Leballais L., Gonzalo S., Lemée V., Laperche S. The variable sensitivity of HIV Ag/Ab combination assays in the detection of p24 Ag according to genotype could compromise the diagnosis of early HIV infection. J. Clin. Virol., 2012, Vol. 55, pp. 121–127. URL: DOI: 10.1016/j.jcv.2012.06.012.
6. Qiu X., Sokoll L., Yip P., Elliott D.J., Dua R., Mohr P., Wang X.Y., Spencer M., Swanson P., Dawson G.J., Hackett J. Jr. Comparative evaluation of three FDA-approved HIV Ag/Ab combination tests using a genetically diverse HIV panel and diagnostic specimens.J. Clin. Virol., 2017 Jul., Vol. 92, pp. 62–68. URL: DOI: 10.1016/j.jcv.2017.05.005.
7. Баранова Е.Н., Шарипова И.Н., Денисова Н.М., Сусекина М.Е., Пузырев В.Ф., Саркисян К.А., Воробьева М.С., Бурков А.Н., Уланова Т.И. Возможности современных тест-систем при подтверждении ранней ВИЧ-инфекции // Вопросы вирусологии. 2009. Т. 54, № 5. С. 37–40. [Baranova E.N., Sharipova I.N., Denisova N.M. Susekina M.E., Puzyrev V.F., Sarkisyan K.A., Vorobyeva M.S., Burkov A.N., Ulanova T.I. The possibilities of modern test systems for the early confirmation of HIV infection. Questions of Virology, 2009, Vol. 54, No. 5, pp. 37–40 (In Russ.)].
8. Иванова Н.И., Пекшева О.Ю. Опыт выявления маркеров ВИЧ-инфекции с использованием нового ИФА-диагностикума ДС-ИФА-ВИЧ-АТ/АГ-СПЕКТР в лабораториях центров по профилактике и борьбе со СПИДом Приволжского Федерального округа // Клиническая лабораторная диагностика. 2009. № 3. С. 46–48. [Ivanova N.I., Peksheva O.Yu. Experience identifying markers of HIV with the new ELISA antigen of DS-ELISA-HIV-at/AG-SPECTRUM in the laboratories of the centers for the prevention and control of AIDS of the Volga Federal district. Clinical Laboratory Diagnostics, 2009, No. 3, pp. 46–48 (In Russ.)].
9. Распопина И.В., Панкова Л.В., Кожевникова И.В. Опыт выявления маркёров ВИЧ-инфекции с использованием нового ИФА-диагностикума Инвитролоджик ВИЧ 1,2-АГ/АТ // Вестник Челябинской областной клинической больницы. 2013. № 1 (20). С. 84. [Raspopina I.V., Pankova L.V., Kozhevnikov I.V. Experience of identifying markers of HIV with the new ELISA antigen of Envitrologic HIV-1,2-AG/AT. Bulletin of the Chelyabinsk Regional Clinical Hospital, 2013, No. 1 (20), pp. 84 (In Russ.)].
10. Шарипова И.Н., Ходак Н.М., Пузырев В.Ф., Бурков А.Н., Уланова Т.И. Сравнительное исследование специфичности тест-систем для диагностики ВИЧ-инфекции на категории образцов сывороток крови беременных женщин // Клиническая лабораторная диагностика. 2015. Т. 60, № 3. С. 38–41. [Sharipova I.N., Khodak N.M. Puzyrev V.F., Burkov A.N., Ulanova T.I. Comparative study of the specificity of test systems for the diagnosis of HIV infection in the category of blood serum samples of pregnant women. Clinical Laboratory Diagnostics, 2015, Vol. 60, No. 3, pp. 38–41 (In Russ.)].
11. Лисицина З.Н., Дмитриевская К.А., Коробан Н.В., Кондрашова Т.В. Иммунные тесты и диагностика острой стадии ВИЧ-инфекции // ВИЧ-инфекция и иммуносупрессии. 2017. Т. 9, № 2. С. 36–41. [Lisitsina Z.N., Dmitrievskaya K.A., Koroban N.V., Kondrashova T.V. Immune tests and diagnosis of the acute stage of HIV infection. HIV Infection and Immunosuppressive Disorders, 2017, Vol. 9, No. 2, pp. 36–41 (In Russ.)].
12. HIV assays: laboratory performance and other operational characteristics: rapid diagnostic tests (combined detection of HIV-1/2 antibodies and discriminatory detection of HIV-1 and HIV-2 antibodies): report 18. Geneva: World Health Organization, 2015.
13. Chaves P., Wesolowski L., Patel P., Delaney K., Owen S.M. Evaluation of the performance of the Abbott ARCHITECT HIV Ag/Ab Combo Assay. J. Clin. Virol., 2011 Dec., Vol. 52, Suppl. 1, pp. S51–S55. URL: DOI: 10.1016/j.jcv.2011.09.010.
14. Mitchell E.O., Stewart G., Bajzik O., Ferret M., Bentsen C., Shriver M.K. Performance comparison of the 4-th generation Bio-Rad Laboratories GS HIV Combo Ag/Ab EIA on the EVOLIS™ automated system versus Abbott ARCHITECT HIV Ag/Ab Combo, Ortho Anti-HIV 1+2 EIA on Vitros ECi and Siemens HIV-1/O/2 enhanced on Advia Centaur.J. Clin. Virol., 2013 Dec., Vol. 58, Suppl. 1, pp. e79–e84. URL: DOI: 10.1016/j.jcv.2013.08.009. 16. Product Package Insert. ARCHITECT HIV Ag/Ab Combo Reagent Kit. USA: Abbott Laboratories.
17. Лаповок И.А., Лопатухин А.Э., Киреев Д.Е. и др. Молекулярно-эпидемиологический анализ вариантов ВИЧ-1, циркулировавших в России в 1987–2015 гг. // Терапевтический архив. 2017. Т. 89, № 11. С. 44–49. [Lapovok I.A., Lopatukhin A.E., Kireev D.A. et al. Molecular epidemiological analysis of HIV-1 circulating in Russia in the years 1987–2015. Therapeutic Archive, 2017, Vol. 89, No. 11, pp. 44–49 (In Russ.)].

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Читайте также:


