Классификация вич у детей по возрасту
ВИЧ у детей, как и у взрослых, проходит три стадии развития:
- Асимптоматическое носительство ВИЧ;
- СПИД — родственный комплекс;
- Собственно СПИД.

Фото: Википедия
Особенность симптомов ВИЧ у детей
Особенность заключается в том, что симптомы СПИД у детей более злокачественна и труднее поддается лечению. Характерен высокий уровень вирусной нагрузки, который сохраняется в организме ребенка в течение длительного времени.
Первые симптомы вич у детей
Гепатоспленомегалия и генерализованная лимфаденопатия (ГЛАП) у больных ВИЧ-инфекцией детей зачастую бывает первым признаком процесса на ранних стадиях. Латентный период у детей короче, и, по данным Rogers М. et al., 1999, 10-20% инфицированных детей имеют быструю прогрессию болезни с развитием СПИДа в пределах первых 4-х лет от инфицирования. Более благоприятно протекает приобретенная ВИЧ-инфекция у детей, инфицированных в возрасте старше 1 года.

Генерализованная лимфаденопатия у ребенка с ВИЧ, 6 лет. Фото: Arthur Ammann, MD, Global Strategies for HIV Prevention
Развивающийся у детей иммунодефицит проявляется повышенной восприимчивостью к различным инфекциям и отражается на их течении. Спектр СПИД-ассоциированных заболеваний у детей отличается от спектра у взрослых.
Наиболее ранние проявления иммунодефицита — рецидивирующие бактериальные инфекции, вызванные Haemophilus influenzae, Streptococcus pneumonie, Salmonella. Клинически диагностируют рецидивирующие гнойные отиты, менингит, гнойные поражения кожи на фоне экземы, типичны массивные бактериальные пневмонии с абсцедированием и выпотом в плевральную полость, неоднократные эпизоды бактериального сепсиса, бактериальная инфекция костей, суставов. Оппортунистические бактериальные инфекции протекают злокачественно, труднее подаются лечению и являются основными причинами смертности. На этом основании центр по контролю за болезнями США (CDC) включил их в список “индикаторных” болезней, при которых диагноз ВИЧ- инфекции у детей предполагается без исследования сероконверсии. Для больных ВИЧ/СПИД характерны инфекции, вызванные цитомегаловирусом, герпесвирусом, вирусом Эпштейна-Барр. Пневмоцистную пневмонию заменяет лимфоидная интерстициальная пневмония (ЛИП), протекающая значительно доброкачественнее. У детей реже встречаются микобактериоз, криптоспоридиоз и криптококкоз, зато чаще развиваются кандидозные поражения кожи и слизистых оболочек.
К классическим СПИД — ассоциируемым заболеваниям у ВИЧ — инфицированных детей относят волосатую лейкоплакию языка. Она появляется у детей на стадии АЗ, на стадии ВЗ уже у каждого четвертого ребенка, на терминальной стадии — у всех детей.
Поражение ЦНС относится к постоянным синдромам в клинике ВИЧ- инфекции детей, поражаются преимущественно клетки микроглии, развивается неврологическая симптоматика в виде энцефалопатии, судорог и их эквивалентов. Задержка психомоторного развития связана с атрофией мозговых структур. Первые симптомы в виде астено-невротического и церебро-астенического синдромов диагностируются в самом раннем возрасте. На стадии СПИДа поражение ЦНС вирусом ВИЧ диагностируется почти у половины больных.
Саркома Калоши у детей встречается редко, лишь в 4 % случаев. Специфическим проявлением ВИЧ-инфекции у детей является поражение околоушных желез.
Классификация ВИЧ у детей
В 1994 году CDC была предложена новая, основанная на уровне CD4+ клеток и клинических симптомах, классификация ВИЧ-инфекции для детей. Симптомы при перинатальной трансмиссии зависит от стадии онтогенеза, на которой происходит проникновение ВИЧ (внутриутробно или постнатально), а в случае постнатального заражения — от возраста ребенка.
Симптомы ВИЧ у детей при внутриутробном инфицировании
При внутриутробном инфицировании ВИЧ может поражать плаценту гематогенным путем на всех стадиях беременности. Ранняя диагностика острых воспалительных изменений плаценты позволяет начать лечебные мероприятия и снизить риск трансмиссии ВИЧ. Вероятность заражения ребенка зависит от многих факторов: стадии ВИЧ-инфекции матери, вирусной нагрузки у нее, течения беременности, родов, кормления грудью. Возможность передачи вируса ребенку возрастает, если у женщины низкое содержание СД4+ клеток. Внутриутробный путь инфицирования считается доказанным при выделении культуры ВИЧ или подтверждения наличия вируса методом ПЦР в течение первых 48 часов жизни, что удается примерно в 40% случаев. При внутриутробном инфицировании риск умереть в раннем возрасте в два раза выше, по сравнению с инфицированием в родах. Внутриутробно инфицированные дети, родившиеся у матерей с клиническими проявлениями ВИЧ-инфекции, болеют чаще и тяжелее, чем дети, родившиеся у матерей с бессимптомной инфекцией. Полагают, что причина кроется в интенсивности вирусной нагрузки на плазму, в характеристике самого вируса, его репликационной способности и способности к образованию синцития. Именно эти факторы определяют степень выраженности клиники.
Дети, инфицированные внутриутробно, зачастую рождаются недоношенными и с различными неврологическими нарушениям. Уже при рождении у них отмечаются признаки черепно-лицевого дисморфизма и микроцефалия. После рождения они плохо развиваются, склонны к повторным инфекциям, у них постоянно увеличены лимфоузлы, печень и селезенка. Считают, что при появлении клинических признаков болезни на первом году жизни ребенок обычно не переживает первый год.
Симптомы ВИЧ у детей, инфицированные в процессе родоразрешения
Инфицирование в процессе родоразрешения связано с прямым контактом плода с зараженной материнской кровью и секретом гениталий, во время прохождения через родовые пути или с восходящей инфекцией из влагалища, шейки матки. Многие специалисты полагают, что риск передачи ВИЧ-инфекции от матери ребенку во время родоразрешения более велик, чем во время беременности. Считают, что в 62-85% случаев перинатальная трансмиссия происходит в родах или в раннем неонатальном периоде. Чем длиннее период родоразрешения, тем больше вероятность ВИЧ-инфицирования ребенка этим путем. Инфицирование после родов может быть связано и с кормлением грудью ВИЧ-инфицированной матерью, при этом вероятность инфицирования повышается по мере увеличения длительности вскармливания. Это связано с повреждением слизистых оболочек ротовой полости, вызванных стоматитом, оральным кандидозом, прорезыванием зубов у ребенка, маститом у матери.
Симптомы ВИЧ у детей, инфицированных в позднем постнатальном периоде
Приобретенная в позднем постнатальном периоде ВИЧ-инфекция у детей связана с гематогенным инфицированием и, для подростков, с внутривенным потреблением психоактивных средств.
Наиболее частыми признаками приобретенной ВИЧ-инфекции у детей, так же, как врожденной, являются персистирующая генерализованная лимфаденопатия (ПГЛ), гепатоспленомегалия, кандидоз кожи и слизистых оболочек, снижение массы тела, лихорадка, диарея, отставание в психомоторном развитии, тромбоцитопения с геморрагическими проявлениями, анемия.
Пути передачи ВИЧ-инфекции — половой, парентеральный, вертикальный.
Классификация СDС (Центр по контролю и профилактики болезней в США):
А — острое бессимптомное ПГЛА
В — ни А, ни С (соответсвует преСПИДу)
С — СПИД (имеются СПИД маркерные заболевания).
Если человек находится в стадии В3 и получает лечение, то он может достигнуть В2 или В1, но буква уже никогда не изменится.
Показания к назначению антиретровирусной терапии — С1, С2, С3, А3, В3.
Классификация ВОЗ — позволяет назначать лечение, не делая анализ CD4+.
Стадия В разбита на две подстадии.
1 стадия — острое бессимптомное ПГЛА
2 стадия — мягкий преСПИД (снижение веса меньше 10%, хейлит, стоматит, кандидоз и др.)
3 стадия — жёсткий преСПИД
Классификация Покровского (принята в странах СНГ):
1). Стадия инкубации. Продолжается от нескольких недель до нескольких лет. Антитела к ВИЧ не определяются. Вирус можно выявить лишь с помощью ПЦР. Диагноз на этой стадии обычно ставится на эпидемиологических данных (половой контакт с больным СПИДом, использование нестерильных шприцёв).
2). Стадия первичных проявлений.
А. Острая лихорадочная фаза. Характеризуется появлением температуры, интоксикации, мононуклеозоподным синлромом, возможно появление сыпи, увеличение 2-3 групп л/у. Продолжительность этой фазы от нескольких дней до 1-2 месяцев, после чего лимфаденопатия может исчезнуть и болезнь переходит в бессимптомную фазу. Антитела к ВИЧ определяются к концу второй недели.
Б. Бессимптомная фаза. Продолжительность — около 6 мес.
В. Персистирующая генерализованная лимфоаденопатия. Характеризуется увеличением почти всех л/у, продолжающееся месяцы и даже годы. Количество СД4+ больше 500 в 1 мкл.
3). Стадия вторичных заболеваний. Количество СД4+ становится ниже 500 в 1 мкл.
А. Потеря массы тела менее 10%, поверхностные грибковые, бактериальные, вирусные поражения кожи и слизистых оболочек, опоясывающий герпес, повторные фарингиты, синуситы.
Б. Прогрессирующая потеря массы тела более 10%, необъяснимая диарея или лихорака более 1 мес, повторные или стойкие бактериальные, грибковые, протозойные поражения внутренних органов (без диссеминации) или глубокие поражения кожи и слизистых оболочек, повторный или диссименированный опоясывающий лишай, ликализованная саркома Капоши.
В. Генерализованные бактериальные, грибковые, вирусные, протозойные, паразитарные заболевания, пневмоцистная пневмония, кандидоз пищевода, атипичный микобактериоз, внелегочной туберкулёз, кахексия, диссименированная саркома Капоши, поражение ЦНС различной этиологии.
4). Терминальная стадия.
В зависимости от преимущественной локализации инфекционного процесса выделяют ряд клинических форм:
а) с преимущественным поражением лёгких (60%)
б) с поражением ЖКТ
г) с поражением кожи и слизистых оболочек
д) генерализованные и/или септические формы
е) недифференцированные формы (в основном с астеновегетативным синдромом, длительной лихорадкой и потерей массы тела)
Антивертровирусная терапия назначается в 4 стадию, 3 стадию и 2 стадию, если количество лимфоцитов меньше 1200.
Оппортунистическая инфекция активируется при CD4+
Период от момента инфицирования до смерти при отсутствии эффективной ретровирусной терапии составляет в среднем 10-12 лет.
Острый ретровирусный синдром (первичная инфекция, острая инфекция) — это начальная супрессия Т-клеток. Эта стадия развивается у большинства больных и у 90 % имеет клиническую картину инфекционного мононуклеоза или симптомы, схожие с тяжёлым гриппом. Чаще всего симптомы появляются через 1-3 недели после инфицирования (в ряде случаев этот период может удлиняться до 10 мес) и продолжается в среднем 2-3 недели. Обычно проявлением острого ретровирусного синдрома являются лихорадка, боли в горле, головная боль, миалгии и артралгии, тошнота, рвота, фарингиты, длительная диарея, лимфаденопатия. Часто бывает эритематозная или макулопапулёзная сыпь. ОАК — лейкопения, лимфопения, но относительный лимфоцитоз, тромбоцитопения, атипичные мононуклеары.
Антитела к ВИЧ начинают выявляться через 1-3 недели после острой стадии или через 6-8 недель от заражения. Титры IgM достигают пика на 2-5 неделе после исчезновения симптомов и сохраняются до 3 месяцев. IgG появляются вскоре после IgM.
Оппортунистические инфекции, ассоциируемые со СПИДом — простейшие: Toxoplasma gondii, Isospora belli, Cryptosporidium spp., грибы: Pneumocystis carinii, Candida albicans, Cryptococcus neoformas, Histoplasma capsulatum, Coccidioides immitis, бактерии: Salmonella spp., Mycobacterium avium complex, Mycobacterium tuberculosis, вирусы: Herpes simplex, Cytomegalovirus hominis.
Первая группа (заболевания, присущие только тяжёлому иммунодефициту, когда количество клеток меньше 200):
- Кандидоз пищевода, трахеи, бронхов.
- Внелегочной криптококкоз.
- Криптоспоридиоз с диареей больше 1 мес.
- Цитомегаловирусная инфекция с поражением различных органов, помимо печени, селезёнки и лимфоузлов.
- Инфекции, обусловленные вирусом простого герпеса, проявляющиеся язвами на коже и слизистых оболочках.
- Саркома Капоши у лиц моложе 60 лет.
- Первичная лимфома мозга у лиц моложе 60 лет.
- Лимфоцитарная интерстициальная пневмония и/или легочная лимфоидная гиперплазия у детей в возрасте до 12 лет.
- Диссиминированная инфекция, вызванная атипичными микобактериями с внелегочной локализацией.
- Пневмоцистная пневмония.
- Прогрессирующая многоочаговая лейкоэнцефалопатия.
- Токсоплазмоз, с поражением головного мозга, лёгких, глаз у больного старше 1 месяца.
Вторая группа (могут развиваться и без тяжёлого иммунодефицита):
- Бактериальные инфекции, сочетанные или рецидивирующие у детей до 13 лет (более двух случаев за два года наблюдения): септицемия, пневмония, менингит, поражение костей или суставов, абсцессы, обусловленные гемофильной палочкой, стрептококками.
- Кокцидиомикоз диссеминированный (внелегочная локализация).
- ВИЧ-энцефалопатия.
- Гистоплазмоз, диссеминированный с внелегочной локализацией.
- Изоспороз с диареей, персистирующей более 1 мес.
- Саркома Капоши у детей любого возраста.
- В-клеточные лимфомы (за исключением болезни Ходжкина) или лимфомы неизвестного иммунофенотипа.
- Туберкулёз внелегочной.
- Сальмонеллёзная септицемия рецидивирующая.
- ВИЧ-дистрофия.
При СПИДе развивается деменция. У 3-7 % инфицированных СПИД-деменция — первое проявление ВИЧ-инфекции и в настоящее время данный синдром является диагностическим критерием для СПИДа.
ЗАБОЛЕВАНИЯ ОРГАНОВ ДЫХАНИЯ ПРИ ВИЧ-ИНФЕКЦИИ
Легкие и дыхательные пути ВИЧ-инфицированных больных примерно в 70% случаев поражаются условно-патогенными микроорганизмами и опухолями. Основные инфекционные и неинфекционные заболевания представлены ниже.
инфекции верхних дыхательных путей
острый бронхит
острый синусит
бактериальная пневмония
пневмоцистная пневмония
Mycobacterium tuberculosis
Mycobacterium avium intracellulare
грибковая пневмония
саркома Капоши
лимфома
неспецифический интерстициальный пневмонит
лимфоидный интерстициальный пневмонит
Инфекции верхних дыхательных путей, острый бронхит и острый синусит
Клинические проявления этих заболеваний у больных СПИДом такие же, как и у ВИЧ-отрицательных пациентов, но их встречаемость гораздо выше. Так, из 1116 ВИЧ-инфицированных больных за 18-месячный период наблюдения 33% перенесли инфекции верхних дыхательных путей, 16% — острый бронхит, 5% — острый синусит и 16% — обострения хронического синусита. Наиболее часто встречающимися возбудителями оказались Streptococcus pneumoniae, Haemophilus influenzae и Pseudomonas aeruginosa.
Наиболее часто бактериальная пневмония встречается у ВИЧ-инфицированных наркоманов. Спектр возбудителей аналогичен группе микроорганизмов, вызывающих пневмонию среди неинфицированных пациентов: S. pneumoniae, H. influenzae, Staphylococcus aureus и грам-отрицательные бактерии. У больных СПИДом отмечаются высокая частота осложнений, таких как формирование легочных абсцессов и полостей, эмпиема плевры, а также частые рецидивы болезни после адекватной антибактериальной терапии.
Несмотря на широкое применение первичной и вторичной профилактики, Pneumocystis carinii остается распространенным возбудителем среди больных СПИДом и выявляется примерно в половине случаев заболеваний дыхательных путей. Предполагается, что пневмоцистная пневмония у иммунокомпрометированных лиц возникает в результате реактивации приобретенной прежде и протекавшей латентно инфекции.
Рентгенологические признаки примерно у 20% больных являются атипичными (уплотнение доли легкого, инфильтраты в верхних долях, имитирующие туберкулез, медиастинальная лимфаденопатия и т. д.).
Первичная профилактика пневмоцистной пневмонии проводится у больных с низким содержанием Т-хелперов (соотношение T-хелперы/лимфоциты менее 1:5) и с другими ВИЧ-ассоциированными заболеваниями. Вторичная профилактика проводится с целью предотвращения рецидивов. Препаратом первого выбора для лечения и профилактики является котримоксазол, второго — пентамидин. Используются также клиндамицин, примаквин, триметрексат и глюкокортикоиды.
Клинические проявления туберкулеза легких варьируют в зависимости от стадии ВИЧ-инфекции. Так, на ранних стадиях туберкулез имеет сходство с первичным туберкулезом взрослых (характерно уплотнение верхних долей и образование полостей; туберкулиновые пробы положительные). На более поздних стадиях туберкулез трудно диагностировать из-за наличия неспецифических признаков (лихорадка, уменьшение массы тела, повышенная утомляемость), которые можно расценить как прогрессирование ВИЧ-инфекции. Для лечения и с целью профилактики применяются традиционные схемы. Однако у данной категории больных отмечается высокая частота побочных реакций на противотуберкулезные препараты.
Инфекция, вызванная Mycobacterium avium intracellulare
Это диссеминированная инфекция, характеризующаяся высокой летальностью и неспецифическими признаками (лихорадкой, потливостью, снижением массы тела, анорексией, общим недомоганием, анемией, гепатомегалией и болями в животе). Развивается примерно у 50% больных СПИДом с очень низким содержанием Т-хелперов. Обычная антибактериальная терапия малоэффективна. Применяются сочетания различных препаратов (рифампицин с этамбутолом и кларитромицином и др.).
Грибковые пневмонии, вызываемые Cryptococcus neoformans, Aspergillus fumagatus и Histoplasma capsulatum, являются легочными проявлениями диссеминированной инфекции. Клинические и рентгенологические признаки неспецифичны. Лечение проводится амфотерицином или флуконазолом.
Саркома Капоши — наиболее частое злокачественное новообразование у больных СПИДом. Легочные поражения обычно сочетаются с другими проявлениями саркомы Капоши (лимфаденопатией, поражениями кожи и слизистых). Основные жалобы — кашель и прогрессирующая одышка. Рентгенологические признаки неспецифичны: интерстициальные инфильтраты, фокальные затемнения, плевральный выпот и медиастинальная лимфаденопатия. Диагноз подтверждается при бронхоскопии. Основной метод лечения — химиотерапия (винкристин, блеомицин).
Лимфомы у ВИЧ-инфицированных появляются обычно на поздних стадиях заболевания. Внутригрудная лимфома — одно из проявлений поражения всего организма, характеризуется неспецифическими клиническими признаками. Средняя выживаемость составляет менее 1 года.
Неспецифический интерстициальный пневмонит
Клинически данное заболевание напоминает пневмоцистную пневмонию, но может возникать при нормальном содержании Т-хелперов. Диагноз подтверждается при биопсии. Лечения не требуется, но при выраженных симптомах показано применение преднизолона.
Лимфоидный интерстициальный пневмонит
Данная патология отмечается в основном у ВИЧ-инфицированных детей. Легочные проявления могут сопровождаться увеличением околоушных желез и лимфоидной инфильтрацией печени и спинного мозга. Основные жалобы — прогрессирующая одышка и кашель. Отмечен положительный эффект при лечении преднизолоном и зидовудином.
Лечение оппортунистических инфекций:
Пневмоцистная пневмония (микоз) — бисептол 4 раза в день по 4 таблетки 3 недели (в 8 раз превышает терапевтические дозы).
Туберкулёз — не меньше 3 препаратов (рифампицин лучше не назначать, так как он чнижаетяс концентрацию некотрых антиретровирусных препаратов).
Криптококкоз, аспергилёз — амфотерицин В.
Кандидоз — кетоназол, флуконазол.
Герпес — ацикловир, лоскарнет.
- лечение должно начинаться до развития тяжёлого иммунодефицита
- начальное лечение должно включать по меньшей мере 2 перпарата
- модификация терапии должна заклчаться в замене или подключении не менее дву хновых препаратов
- крайне важно измерять уровень СД4+ клеток и вирусную нагрузку
- снижение вирусной нагрузки до уровня, лежащего ниже предела определения чувсвительных методик, отражает оптимальный эффект лечения.
Современные антиретровирусные препараты можно разделить на три группы:
1) Нуклеозидные ингибиторы обратной транскриптазы — зидовудин, диданозин, зальцитабир, ставудин, ламивудин, абакавир, адефовир, комбивир (зидовудин + абакавир), тризивир (зидовудин + ламивудин + абакавир).
2). Ненуклеозидные ингибиторы обратной транскриптазы — делавердин (рескриптор), невирапин (вирамун), лоривид, ифавиренц.
3). Ингибиторы протеаз — санквинавир, ритонавир, индинавир, нельфинавир, ампренавир, лопинавир.
Профилактика вертикальной передачи инфекции. Беременным ВИЧ-инфицированным женщинам, начиная с 14 недель беременности назначается азидотимидин (ретровир, тимазид) орально в суточной дозе 100 мг 5 раз в сутки. Непосредственно в родах назначается в/в капельно азидотимидин в дозе 2 мг/кг в течение двух часов. Новорождённым назначают сироп азидотимидина в течении первых 6 недель жизни.
При травме кожи или слизистых при работе с ВИЧ-материалом — 4 недели пить ретровир по 150 мг 3 раза в день либо индинавир по 800 мг 3 раза в день. Сдать кровь на исследование через 6 недель, 12 недель и 6 месяцев.
Лекция по детским инфекционным болезням
Тема: ОСОБЕННОСТИ ВИЧ-ИНФЕКЦИИ
Учебные и воспитательные цели:
1. Факторы риска и частота перинатальной трансмиссии ВИЧ
2. Патогенез врожденной ВИЧ-инфекции
3. Клинические классификации ВИЧ-инфекции у детей
4. Естественное течение ВИЧ-инфекции у детей
5. Лечение ВИЧ-инфекции у детей: понятие ВААРТ, группы препаратов, критерии назначения препаратов, мониторинг терапии
РАСЧЕТ УЧЕБНОГО ВРЕМЕНИ
Перечень учебных вопросов
К-во выделяемого времени в минутах
Факторы риска и частота перинатальной трансмиссии ВИЧ
Патогенез и естественное течение ВИЧ-инфекции у детей
Диагностика ВИЧ-инфекции у детей
Классификации ВИЧ-инфекции у детей
Терапия ВИЧ-инфекции у детей
Лекцию подготовила доцент, к.м.н. Матиевская Н.В.
В настоящее время пандемия ВИЧ-инфекции достигла территории Республики Беларусь и постепенно становится все более и более актуальной проблемой здравоохранения РБ. Так, количество зарегистрированных случаев ВИЧ-инфекции на начало 2010 года составило около 11 тысяч, среди них умерло около 2-х тысяч больных. Подавляющее большинство больных это люди молодого работоспособного возраста – до 35 лет. Начиная с 2001-2002 г.г. во всех регионах республики начинает доминировать половой путь инфекции, так как в эпидпроцесс по ВИЧ вовлечены лица репродуктивного возраста. Все большее число случаев ВИЧ-инфекции регистрируется среди молодых женщин при постановке на учет по беременности. Соответственно, вероятность рождения ВИЧ-инфицированных детей возрастает. Течение врожденной ВИЧ-инфекции у детей имеет особенности, связанные с характером иммунного ответа у детей в разные возрастные периоды жизни, знание которых необходимо для осуществления рационального мониторинга ВИЧ-инфекции у детей.
Факторы риска и частота перинатальной трансмиссии ВИЧ
Наиболее значимая причина ВИЧ-инфекции у детей до 15 лет - это вертикальная передача ВИЧ от матери к ребенку во время беременности. Приблизительно 1800 детей во всем мире инфицируются данным путем ежедневно, большинство из них в развивающихся странах. Частота перинатальной трансмиссии (ПТ) ВИЧ в развитых странах составляет около 15-25% в год, в развивающихся – 25-45%.
Использование различных режимов профилактики ПТ ВИЧ позволяет снизить риск вертикальной трансмиссии до 2%.
При отсутствии профилактики риск ПТ составляет 19-36%. Частота зависит от пренатальных, интранатальных и постнатальных факторов, которые необходимо учитывать при проведении профилактики ПТ.
В зависимости от периода частота ПТ распределяется следующим образом:
Пренатальный период, преимущественно на последних стадиях беременности - 25-35%
Интранатальный период (роды) – 70-75%
Постнатальный период (грудное вскармливание) – 10-16%.
При грудном вскармливании (ГВ) наиболее высок риск ПТ в первые 3-4 месяца жизни ребенка
Считается, что если ребенок является позитивным на ВИЧ методом ПЦР в первые 48 часов жизни – он был инфицирован пренатально, если он становиться ПЦР-позитивным после 48 часов – инфицирование произошло во время родов.
Риск постнатального инфицирования, связанного с грудным вскармливанием возрастает в течение времени вскармливания. Отмечается прямая зависимость между риском ПТ и продолжительностью ГВ, уровнем ВН у матери. Высокий уровень антител к ВИЧ в грудном молоке (ГМ) снижает риск передачи. Имеет значение наличие докорма смесями (снижение риска), а также наличие у матери мастита, трещин сосков, абсцессов, инфекционной патологии у ребенка. В развитых странах грудное вскармливание для ВИЧ-позитивных матерей запрещено, в развивающихся странах – вопрос решается с учетом наличия возможности искусственного вскармливания и риска инфицирования для ребенка при переводе на искусственное вскармиливание. Матери, получающие ВААРТ, имеют низкий риск трансмиссии ВИЧ при ГВ.
Факторы, влияющие на ПТ условно могут быть разделены на 5 групп (табл. 1):
1. материнские факторы
2. вирусные факторы
3. акушерские факторы
4. факторы плода
5. факторы ребенка
Табл.1 – Факторы, влияющие на ПТ ВИЧ
Тип влияния фактора
Уровень виремии ВИЧ
Иммунный статус матери
Низкий уровень CD4+или терминальная стадия ВИЧ – увеличение риска ПТ
Инфекции урогенитального тракта
Наличие инфекций, особенно с изъязвлением слизистых УГТ – увеличение риска ПТ
При ВН матери >1000 кп/мл снижает риск ПТ на 50-70%, при ВН 299 000 кп/мл) четко ассоциируется с прогрессированием заболевания и развитием смерти, однако такие показатели ВН у детей встречаются редко.
Иммунологические особенности. Абсолютное значение показателя CD4+лимфоцитов зависит от возраста ребенка и у неинфицированных детей существенно выше, чем у взрослых. Показатели приближаются к уровню взрослого лишь к 4-6 году жизни (табл.2).
Табл.2 - Иммунологические категории при ВИЧ-инфекции у детей (1994)
Отсутствие значимой ИС
0,5см в диаметре
двух и более анатомических групп);
• хронический ВИЧ-паротит 1;
• рецидивирующие или постоянно персистирующие инфекции верхних дыхательных путей, синуситы и средние отиты.
· категория В (умеренная симптоматика): наличие связанной с ВИЧ-инфекцией клинической симптоматики, не входящей в категории А и С; ниже приведен примерный (но не исчерпывающий) список примеров такой симптоматики:
• анемия ( 9 /л), персистирующие более З0 дней;
• бактериальный менингит, пневмония или сепсис (хотя бы 1 эпизод);
• кандидоз орофарингеальный длительностью более 2 месяцев (у ребенка старше 6 месяцев);
• ЦМВ-инфекция (у ребенка старше 1 месяцев);
• диарея рецидивирующая или хроническая;
• герпетический (ВПГ 1 или 2) стоматит рецидивирующий (более 2-х эпизодов в год);
• герпетические (ВПГ 1 или 2) бронхиты, пневмонии, эзофагиты у детей старше 1 месяца;
• опоясывающий лишай (ВПГ 3) более 2-х раз в год или захватывающая дерматома, диссеминированная или осложненная ветряная оспа;
• лимфоидная интерстициальная пневмония (ЛИП) или гиперплазия прикорневых лимфоузлов;
• токсоплазмоз у ребенка старше 1 месяца, диссеминированный или осложненный;
• лихорадка персистирующая более 1 месяца;
• категория С (тяжелая симптоматика): наличие СПИД-ассоциируемых заболеваний (исключая ЛИП):
• серьезные бактериальные инфекции, множественные или рецидивирующие, как минимум 2 раза за двухлетний период, подтвержденные выделением возбудителя из гемокультуры, в виде сепсиса, пневмонии, менингита, остеомиелита, абсцессов различных органов и полостей, исключая отит, поверхностные кожно-слизистые абсцессы и катетер-ассоциированные инфекции;
• кандидоз глубокий (пищевода, бронхов, трахеи, легких);
• криптококкоз внелегочный (как правило, менингит);
• криптоспоридиоз или изоспороз с диареей более 1 месяца;
• ЦМВ-инфекция у ребенка старше 1 месяца (исключая изолированные поражения печени, легких и лимфоузлов);
• энцефалопатии: наличие прогрессирующих симптомов более 2 месяца при отсутствии других заболеваний кроме ВИЧ-инфекции:
а) задержка развития мозга, нарушение интеллекта, подтвержденное нейрофизиологическим тестами, или приобретенная микроцефалия, атрофия мозга, подтвержденная КТ или МРТ, у ребенка старше 2 лет;
б) приобретенные моторные нарушения (2 и более): парез, патологические рефлексы, атаксия или нарушение походки;
• герпетические (ВПГ 1 или 2) инфекции: кожно-слизистые язвы персистирующие более 1мес, или бронхиты, пневмонии, эзофагиты (у детей старше 1мес);
• туберкулез или атипичный микобактериоз диссеминированный или висцеральный;
• сальмонеллезная бактериемия (исключая S. typhi) рецидивирующая;
• токсоплазмозный энцефалит у ребенка старше 1 месяца;
• wasting-синдром (стойкая потеря массы >10% вследствие хронической диареи (стул не менее 3 раз в сутки длительностью не менее 1 месяца у детей старше 5 лет) и документированной лихорадки более 1 месяца постоянной или интермиттирующей) при отсутствии заболеваний, сходных с ВИЧ-инфекцией и объясняющих перечисленные симптомы;
• опухоли ВИЧ-ассоциируемые (саркома Капоши, злокачественные лимфомы: в первую очередь первичная лимфома головного мозга, а также В-клеточная лимфома и лимфома Беркитта);
• прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ).
Особенностью данной классификации является то, что пациент, единожды отнесенный к категории В, не может в последующем перейти в категорию А после излечения соответствующего заболевания. То же относится и к категории С. Все пациенты в группах A3, ВЗ, С1-3 расцениваются как пациенты, потенциально нуждающиеся в антиретровирусной терапии.
При невозможности определнения показателя CD4+ используется клиническая классификация ВИЧ-инфекции, где стадия ВИЧ-инфекции определяется с учетом клинических проявлений заболевания, параметров физического и нейропсихологического развития ребенка.
Пересмотренная клиническая классификация ВИЧ-инфекции у детей
(протоколы ВОЗ, 2006 г.)
Версия для Европейского региона, для детей 18 месяцев, выявление ДНК, РНК или антигена р24 у детей 12 месяцев
В зависимости от содержания CD4 лимфоцитов
В зависимости от содержания CD4 лимфоцитов
Примечание: * В некоторых случаях возможен индивидуальный подход к старту терапии при условии хорошего диспансерного наблюдения за больным.
Как видно из табл. 6, ВААРТ показана при манифестных стадиях ВИЧ-инфекции (3 и 4 стадия) независимо от уровня CD4+лимфоцитов. При 1 и 2 клинической стадии ВИЧ-инфекции вопрос о назначении терапии у детей старше 1 года основывается на данных иммунологического исследований. В то же время у детей с верифицированной врожденной ВИЧ-инфекцией терапия показана практически во всех случаях. Такая позиция связана с постоянно высокой ВН на 1 году жизни и риском развития осложнений, приводящих к смерти.
В то же время иммунологические критерии начала ВААРТ позволяют детям 1-го года жизни с отсутствием иммуносупрессии отложить терапию (табл. 7).
Таблица 7. Иммунологические критерии начала APT у детей (ВОЗ, 2006)
Пороговые значения CD4-лимфоцитов в зависимости от возраста, при которых показано назначение APT
Доля СD4-лимфоцитов плазмы (%)
25% у детей моложе 11 месяцев терапия может быть отложена, при условии тщательного мониторинга состояния здоровья ребенка.
Вирусологические показатели (вирусная нагрузка, ВН) не констатируют стадию ВИЧ-инфекции (как иммунологические и клинические данные), поскольку не отражают состояние организма (сохранность его иммунитета), а говорят только об активности репликации вируса. И если у подростков и взрослых значения ВН могут быть использованы для прогнозирования риска развития иммунодефицита в будущем, то у детей, особенно первого года жизни, это делать трудно из-за постоянно очень высокой ВН.
Тем не менее, ВН следует определять до начала APT, поскольку это объективный и ранний показатель ответа на лечение. Ведь целью APT является снижение ВН до неопределяемого уровня, при котором репликация вируса прекращается и снижается вероятность развития устойчивости к применяемой схеме APT.
АРП классифицируются в зависимости от механизма действия и точек приложения препарата, которые связаны с определенными этапами цикла репликации ВИЧ в клетках инфицированного пациента (рис. 3).
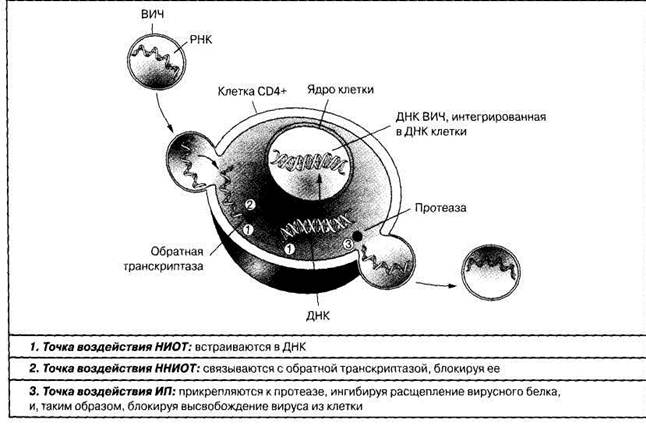
Рис. 3 – Целевые точки приложения АРП
К октябрю 2005 года к применению у взрослых и подростков был сертифицирован 21 антиретровирусный препарат в настоящее время к применению у детей доступны 4 группы АРП:
• Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ и НтИОТ)
• Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ)
• Ингибиторы протеазы (ИП)
• Ингибиторы слияния (ИС)
1 группа. Нуклеозидные ингибиторы обратной транскриптазы (НИОТ)
Существуют в виде монопрепаратов и комбинированных форм.
К монопрепаратам относят:
1. Ретровир (Retrovir, zidovudin, тимазид, азидотимидин, AZT, ZDV, 1987)
2. Ставир (Ставудин, Зерит, d4T, 1994)
3. Дивир (Диданозин, Видекс, ddl, 1991)
4. Зальцитобин (Хивид, Замицид, 1992)
5. Зиаген (Ziagen, Абакавир, АВС, 1998)
6. Эпивир (Epivir, Ламивудин, 3TC, LMV, 1995)
7. Тенофавир (Tenofavir, PMPA, Viread, 2001)
8. Эмтрицитабин (Эмтрива, 2003)
Комбинированные формы НИОТ представлены 6 препаратами:
1. Комбивир – ламивудин + зидовудин
2. Эпзиком – абакавир + ламивудин
3. Тризивир - абакавир + ламивудин+ зидовудин
4. Тенофавир+абакавир+ ламивудин
5. Тенофавир+диданозин + ламивудин
6. Трувада – эмтрицитабин + тенофовир
Комбинированные формы удобны в применении т.к. уменьшают количество таблеток, принимаемых больным.
2 группа. Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) представлены 3 препаратами. В РБ используются 2 препарата:
· Невирапин (Невимун, Viramune, NVP)
· Эфавир (Эфавиренз, Ифавиренц, Сустива, Стокрин, EFZ)
3 группа препаратов. Ингибиторы протеазы (ИП).
· Инвираза (Саквинавир твердые капсулы, SQV-HGC);
· Нелфинавир (Вирасепт, Nelvir, NFP);
· Норвир (Ритонавир, RTV);
· Калерта (Лопиновир/ритоновир, LPV/r);
4 группа. Ингибиторы фузии.
Единственный одобренный на сегодня препарат этой группы энфувиртид (T-20) вводится подкожно.
Принципы комбинации АРВ препаратов:
· Комбинации, основанные на ННИОТ (2 НИОТ и 1 ННИОТ)
· Комбинации, основанные на НИОТ (3 препарата из группы НИОТ)
· Комбинации, основанные на ИП (ИП и 2 НИОТ)
· Не рекомендуется комбинировать 1 НИОТ и 2 ННИОТ
· При неэффективности предложенных схем – ИП и НИОТ и ННИОТ
Особенности применения АРТ у детей.
Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ).
Невирапин. Схемы ВААРТ, включающие Невирапин + 2 НИОТ рекомендуются для широкого применения у детей младше 3 лет и тех, кому требуется жидкая форма препарата , одобрен к применению у детей с 2 месяцев. Препарат хорошо переносится детьми, дозировка препарата хорошо разработана в разных возрастных категориях. К неблагоприятным эффектам относится – возможность гепатотоксичности, возникновение аллергической сыпи, резистентность к препарату, если матери для профилактики ПТ назначался невирапин.
Эфавиренз препарат в капсулах, его жидкая форма проходит клинические испытания. В качестве схемы ВААРТ Эфавиренз+ 2 НИОТ разрешен к назначению в виде стартовой схемы детям старше 3 лет. Позитивными сторонами препарата является возможность назначения в виде однократной суточной дозы, а также способность его потенцировать антивирусный эффект других препаратов в схеме. В то же время доза для детей младше 3 лет не установлена. Препарат способен вызывать неиропсихические нарушения (бред, галлюцинации, возбуждение ит.д.) . Необходимо помнить о тератогенных эффектах препарата при назначении девочкам подросткового возраста.
Делавирдин выпускается только в таблетках и к применению у детей не одобрен, поскольку пока не изучен на детях.
Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ и НтИОТ).
- настоятельно рекомендуемые комбинации для первой схемы антиретровирусной терапии: зидовудин + ламивудин, зидовудин + диданозин и ставудин +ламивудин.
- рекомендуемыекомбинации для первой схемы антиретровирусной терапии: зидовудин + абакавир, ламивудин +абакавир и диданозин + ламивудин.
- не рекомендуются комбинации: зидовудин + ставудин (эти препараты снижают антиретровирусную активность друг друга), а также комбинации зальцитабина с диданозином, ставудином и ламивудином (эти комбинации плохо изучены у детей и все эти препараты нейротоксичны)
Тройные комбинации НИОТ в педиатрической практике.
По результатам нескольких педиатрических исследований тройная комбиниция НИОТ: ABC+ 3TC+ ZDV (Тривир) может рекомендоваться в качестве стартовой терапии у детей, но лишь в тех случаях, когда нет возможности использовать схемы с ННИОТ или ИП. 2 другие тройные комбинированные формы НИОТ (TNF+ ABC+ 3TC и TNF+ddI+3TC) не рекомендуются к применению в педиатрической практике.
Ингибиторы протеазы (ИП).
Наиболее часто используемая стартовая схема с ИП у детей в настоящее время это лопиновир/ритоновир (LPV/r, Калетра) +2 НИОТ. LPV/r имеет высокую антивирусную активность, высокий генетический барьер, хорошо изученную возрастную дозировку (даже у новорожденных), низкую токсичность.
Альтернативная схема: фосампренавир + RTN +2 НИОТ (для детей старше 6 лет). Жидкая форма фосампренавир появилась с 2007 г., рекомендуется у детей старше 2 лет.
Новые группы АРП в педиатрической практике. Ингибитор фузии – Т-20 был изучен на небольшой группе детей старше 6 лет, рекомендуется в режимах альтернативной терапии. Ингибитр интегразы (Ралтегравир) и ингибиторы входа (Маравирок) – не изучались на детях.
Диспансеризация детей получающих пожизненную ВААРТ.
Наблюдение детей, получающих длительные курсы ВААРТ имеет свои особенности. Несмотря на достижение успеха в первые годы терапии, очень часто на более поздних этапах констатируется отсутствие эффекта лечения. В такой ситуации требуется пересмотр терапии и смена стартовых режимов ВААРТ. Причины возникновения неэффективности терапии связаны со многими факторами: несоблюдение режима терапии, плохая переносимость препаратов, лекарственные взаимодействия, неадекватный уровень препарата, низкая противовирусная активность используемой схемы и т.д. Все данные факторы должны быть учтены и проанализированы прежде, чем менять схему терапии.
Необходимо помнить, что спектр выбора АРП у детей меньше, чем у взрослых. Поэтому прежде, чем принять решение о смене схемы лечения необходимо тщательно взвесить все факторы, максимально обследовать ребенка, используя генетические методы и т.д., а также проанализировать приверженность пациента к терапии. Необходимо понимать, что наблюдение ВИЧ-инфицированного ребенка должно проводиться с учетом всех обстоятельств жизни ребенка: социальных, экономических, психологических, культурных, семейных и т.д. Клиницисты должны понимать, что имеют дело с ребенком, страдающим сложным, многокомпонентным хроническим заболеванием, имеющем место в постоянно развивающемся и изменяющемся организме ребенка.
Читайте также:


