Лекарство от вич zolinza
Показания к применению
- лечение кожной Т-клеточной лимфомы, которая прогрессирует, персистирует или рецидивирует, несмотря на проведенную системную терапию.
Возможные аналоги (заменители)
Действующее вещество, группа
Лекарственная форма

Противопоказания
- повышенная чувствительность к компонентам препарата;
- тяжелая степень печеночной недостаточности;
- детский и подростковый возраст до 18 лет;
- период лактации (грудного вскармливания).
С осторожностью назначают препарат при следующих заболеваниях и состояниях: умеренная степень печеночной недостаточности; тромбоэмболии в анамнезе; исходные тошнота, рвота и диарея (должны быть устранены до начала лечения); сахарный диабет и риск развития сахарного диабета.
Как применять: дозировка и курс лечения
Капсулы следует принимать внутрь во время еды, не вскрывать, проглатывать целиком.
Рекомендуемая доза препарата составляет 400 мг один раз в сутки. В случае возникновения непереносимости дозу можно снизить до 300 мг один раз в сутки в течение 5 последовательных дней в неделю.
Лечение проводят до достижения полного контроля заболевания (отсутствие признаков дальнейшего прогрессирования) или до появления признаков неприемлемой токсичности.
Возрастную коррекцию дозы у пожилых людей проводить не требуется.
Переносимая суточная доза вориностата для пациентов с легкой и средней степенью печеночной недостаточности составляет 300 мг и 200 мг соответственно.
Фармакологическое действие
Противоопухолевый препарат, ингибитор гистон-деацетилазы. По данным исследований на клеточных культурах вориностат индуцирует апоптоз у большого числа видоизмененных (опухолевых) клеток. На культурах опухолевых клеток вориностат продемонстрировал дополнительную или синергичную активность при совместном использовании с другими видами противоопухолевой терапии, включая лучевую терапию и химиотерапию ингибиторами киназ, цитотоксическими препаратами и индукторами дифференцировки клеток. In vivo вориностат продемонстрировал противоопухолевую активность на широком диапазоне моделей рака у грызунов, включая модели ксенотрансплантатов злокачественных опухолей простаты, молочной железы и толстой кишки человека.
Побочные действия
Безопасность препарата оценивалась у 111 пациентов с кожной Т-клеточной лимфомой в двух клинических исследованиях. 86 пациентов принимали препарат в дозе 400 мг один раз в сутки. Характерные нежелательные реакции, связанные с приемом препарата в режиме 400 мг один раз в сутки могут быть объединены в 4 группы симптомокомплексов: симптомы со стороны органов желудочно-кишечного тракта (диарея, тошнота, анорексия, снижение массы тела, рвота, запор, снижение аппетита), общие симптомы (повышенная утомляемость, озноб), гематологические нарушения (тромбоцитопения, анемия) и расстройство вкусовых ощущений (дисгевзия, сухость во рту).
Наблюдаемые очень часто (> 1/10) нежелательные реакции (клинические и лабораторные), связанные с лечением препаратом, у пациентов с кожной Т-клеточной лимфомой, принимавших препарат в дозе 400 мг один раз в сутки:
Нарушения со стороны крови и лимфатической системы: тромбоцитопения, анемия.
Нарушения со стороны обмена веществ и питания: анорексия, снижение аппетита.
Нарушения со стороны желудочно-кишечного тракта: диарея, тошнота, сухость во рту, рвота, запор.
Нарушения со стороны кожи и подкожных тканей: алопеция, кожный зуд.
Нарушения со стороны скелетно-мышечной и соединительной ткани: мышечные спазмы.
Нарушения со стороны нервной системы: дисгевзия, головокружение, головная боль.
Общие расстройства и нарушения в месте введения: повышенная утомляемость, озноб; часто: повышение температуры тела.
Нарушения со стороны сосудов: периферические отеки.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: частые: кашель, инфекции верхних дыхательных путей.
Лабораторные и инструментальные данные: снижение массы тела, увеличение плазменной концентрации креатинина.
Нежелательные реакции 3-5 степени тяжести наблюдались для следующих из перечисленных выше реакций:
тромбоцитопения (5,8%), анемия (2,3%), анорексия (2,3%), снижение аппетита (1,2%), тошнота (3,5%), мышечные спазмы (2,3%), повышенная утомляемость (2,3%), озноб (1,2%) и снижение массы тела (1,2%). Ни одна из нежелательных реакций не имела 5 степени тяжести. Профиль нежелательных реакций у пациентов, получавших другие дозы препарата, был аналогичным. Частота выраженных тромбоцитопении, анемии и чувства усталости была повышенной при лечении дозами препарата свыше 400 мг в режиме один раз в сутки.
В клинических исследованиях у пациентов с кожной Т-клеточной лимфомой наблюдали следующие связанные с лечением серьезные нежелательные реакции (вне зависимости от принимаемой дозы препарата): Частые (>1/100 и 1/1000 и *
Международное наименование: Zolinza
Состав и форма выпуска
Капсулы твердые желатиновые, размер №3, непрозрачные, белого цвета, с черной надписью "568" и белой надписью на черном фоне "100 mg", содержимое капсул - порошок от белого до светло-оранжевого цвета. В 1 капсуле содержится 100 мг вориностата. К вспомогательным веществам относятся целлюлоза микрокристаллическая - 44,33 мг, кроскармеллоза натрия - 4,5 мг, магния стеарат - 1,17 мг.
Состав оболочки капсулы: титана диоксид (Е171) - 2,9079%, желатин - до 100%.
Состав чернил: опакод черный (Opacode Black) S-1-17822 (раствор глазури шеллака 45% в этаноле - 44,5%, краситель железа оксид черный - 23,4%, бутанол - 16,6%, изопропанол - 12,5%, пропиленгликоль - 2%, аммония гидроксид 28% - 1%) или опакод черный (Opacode Black) S-1-17823 (раствор глазури шеллака 45% в этаноле - 44,5%, краситель железа оксид черный - 23,4%, бутанол - 2,2%, изопропанол - 26,9%, пропиленгликоль - 2%, аммония гидроксид 28% - 1%).
Во флаконе 120 капсул. Упакован в картонную пачку.
Клинико-фармакологическая группа
Фармако-терапевтическая группа
Фармакологическое действие
Противоопухолевый препарат, ингибитор гистон-деацетилазы. Вориностат является мощным ингибитором гистон-деацетилаз (HDAC) - HDAC1, HDAC2 и HDAC3 (класс I), а также HDAC6 (класс II) (ПК 50 max и медианы (диапазона) T max составили 5,5±1,8 мкмоль/л×ч, 1,2±0,62 мкмоль/л и 4 (2-10) ч соответственно. После однократного приема внутрь препарата в дозе 400 мг натощак средние значения AUC, C max и медианы Т mах составили 4,2±1,9 мкмоль/л×ч, 1,2±0,35 мкмоль/л и 1,5(0,5-10) ч соответственно. Таким образом, одновременный прием вориностата с жирной пищей сопровождается увеличением (на 33%) величины всасывания и незначительным снижением скорости всасывания (увеличение Т mах на 2,5 ч) по сравнению с приемом препарата натощак. В целом, предполагается, что эти незначительные отклонения фармакокинетических параметров не имеют клинического значения.
При многократном приеме внутрь вориностата в дозе 400 мг одновременно с пищей значения AUC, C max и медианы Т mах в равновесном состоянии составили 6.0±2.0 мкмоль/л×ч, 1,2±0,53 мкмоль/л и 4 (0,5-14) ч соответственно.
В диапазоне плазменных концентраций от 0,5 до 50 мкг/мл связывание вориностата с белками плазмы составляет примерно 71%. Вориностат быстро проникает через плацентарный барьер у крыс и кроликов при введении в суточных дозах 15 мг/кг и 150 мг/кг соответственно (что соответствует меньшему значению экспозиции, нежели у человека по данным AUC 0-24 ), с достижением трансплацентарного равновесия примерно через 30 мин после введения.
Основными путями метаболизма вориностата являются реакции глюкуронизации и гидролиза с последующим β-окислением. Были измерены плазменные концентрации двух метаболитов - О-глюкуронида вориностата и 4-анилино-4-оксобутановой кислоты. Оба метаболита фармакологически неактивны. По сравнению с вориностатом, в равновесном состоянии экспозиция О-глюкуронида вориностата и 4-анилино-4-оксобутановой кислоты превышает экспозицию вориностата примерно в 4 и 13 раз соответственно.
Проведенные исследования in vitro на микросомах печени человека указывают на незначительную биотрансформацию препарата ферментами системы цитохрома Р450.
Вориностат преимущественно метаболизируется в печени, в неизмененном виде почками выводится менее 1% введенной дозы, следовательно, почечная экскреция практически не играет роли в выведении препарата из организма. По достижении равновесного состояния в моче обнаруживали два фармакологически неактивных метаболита вориностата - О-глюкуронид вориностата в количестве 16±5.8% от введенной дозы вориностата и 4-анилино-4-оксобутановую кислоту в количестве 36 ± 8,6 % от введенной дозы вориностата. Таким образом, количество обнаруживаемых в моче неизмененного вориностата и двух указанных метаболитов составило в среднем 52±13,3% от введенной дозы вориностата. T 1/2 вориностата и его О-глюкуронид метаболита составил около 2 ч, а T 1/2 4-анилино-4-оксобутановой кислоты составил примерно 11 ч.
Фармакокинетика у особых групп пациентов
По данным анализа ограниченного объема данных пол, раса и возраст пациентов не оказывали клинически значимого влияния на фармакокинетические параметры вориностата.
Фармакокинетические параметры вориностата у детей и подростков до 18 лет не изучены.
Вориностат противопоказан к применению у пациентов с печеночной недостаточностью тяжелой степени и не рекомендован к применению у пациентов с печеночной недостаточностью умеренной степени. Данные рекомендации основаны на первичных результатах проходящих фармакокинетических исследований у пациентов с легкой, умеренной (общий билирубин в 1,5-3 выше ВГН) и тяжелой (общий билирубин более чем в 3 раза выше ВГН) степени печеночной недостаточности. Эти исследования предполагают, что у пациентов с тяжелой степенью печеночной недостаточности после приема вориностата риск дозозависимой токсичности выше, чем у пациентов без нарушений функции печени.
В целом, из исследования вориностата исключают пациентов с тяжелой степенью печеночной недостаточности. Однако есть ограниченное число пациентов с печеночной недостаточностью умеренной степени, которые были включены в клинические исследования. Не обнаружено клинически значимого различия в развитии побочных эффектов, связанных с функцией печени, у пациентов с печеночными нарушениями в анамнезе по сравнению с пациентами без таковых.
Фармакокинетические параметры препарата у пациентов с почечной недостаточностью не изучены. Следует отметить, что почечная экскреция не задействована в выведении вориностата из организма.
Лечение кожных проявлений у пациентов с Т-клеточной лимфомой, которая имеет прогрессирующий, стойкий или рецидивирующий характер во время или после двух курсов системной терапии.
Противопоказания к применению препарата Золинза
Повышенная чувствительность к компонентам препарата; тяжелая степень печеночной недостаточности; детский и подростковый возраст до 18 лет; беременность; период лактации (грудного вскармливания).
С осторожностью: умеренная степень печеночной недостаточности; тромбоэмболии в анамнезе; исходные тошнота, рвота и диарея (должны быть устранены до начала лечения); сахарный диабет и риск развития сахарного диабета.
Режим дозирования и способ применения препарата Золинза
Рекомендуемая доза – 400 мг внутрь 1 раз/сут во время еды.
При непереносимости терапии дозу можно уменьшить до 300 мг 1 раз/сут во время еды.
При необходимости в дальнейшем доза может быть уменьшена до приема в дозе 300 мг ежедневно 1 раз/сут после еды в течение 5 последовательных дней еженедельно.
У пациентов с легкими или умеренными нарушениями функции печени возможно применение в дозе 200 мг/сут и 300 мг/сут соответственно.
Длительность лечения определяется возникновением симптомов прогрессирования заболевания и развития неприемлемой токсичности.
Побочные эффекты
Со стороны пищеварительной системы: диарея, тошнота, снижение аппетита, анорексия, уменьшение массы тела, рвота, запор, дисгевзия, сухость во рту, холецистит, кровотечение из ЖКТ.
Со стороны системы кроветворения: тромбоцитопения, анемия.
Со стороны дыхательной системы: кашель, инфекции верхних дыхательных путей, легочная эмболия, долевая пневмония.
Со стороны сердечно-сосудистой системы: тромбоз глубоких вен, инфаркт миокарда, ишемический инсульт.
Со стороны костно-мышечной системы: мышечные спазмы, повреждение позвоночника.
Дерматологические реакции: алопеция, зуд, эксфолиативный дерматит.
Со стороны мочевыделительной системы: повышение содержания сывороточного креатинина, протеинурия, обструкция мочевыводящих путей.
Со стороны нервной системы: головокружение, головная боль, синкопе.
Инфекции: энтерококковая инфекция, сепсис, стрептококковая бактериемия.
Общие реакции: утомляемость, озноб, пирексия, дегидратация.
Прочие: периферические отеки, сквамозно-клеточная карцинома.
Частота развития тромбоцитопении, анемии, утомляемости повышалась при дозах более 400 мг/сут.
Применение при беременности и кормлении грудью
Адекватных и строго контролируемых исследований применения вориностата при беременности не проводилось.
Если беременность наступила во время применения вориностата, пациентку следует поставить в известность о существующей опасности для плода.
Неизвестно, выделяется ли вориностат с грудным молоком у человека. При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания
В экспериментальных исследованиях на животных показано, что вориностат проникает через плацентарный барьер и его концентрация в плазме плода составляет 50% от концентрации в плазме матери. Показано, что вориностат оказывает тератогенное действие и способен вызывать нарушения развития плода.
Особые указания при приеме препарата Золинза
С осторожностью применять у пациентов при подозрении на легочную эмболию и тромбоз глубоких вен, особенно у при указании в анамнезе на тромбоэмболию.
С осторожностью применять у пациентов с легкими и умеренными нарушениями функции печени.
Данные о применении у пациентов с нарушениями функции почек отсутствуют.
Не следует применять вориностат в периоперационном периоде у пациентов, которым показано хирургическое вмешательство на кишечнике.
При уменьшении количества тромбоцитов и/или гемоглобина следует корректировать дозу вориностата или при необходимости отменить терапию.
Во время лечения может потребоваться применение противорвотных и противодиарейных препаратов.
Перед началом терапии вориностатом необходимо провести адекватную терапии тошноты, рвоты и диареи.
Для предотвращения дегидратации следует скорректировать потерю жидкости и электролитов.
В период лечения следует контролировать содержание глюкозы в крови, особенно у пациентов с сахарным диабетом или при подозрении на него. При необходимости может потребоваться соответствующая диета и/или гипогликемическая терапия.
Следует тщательно контролировать клеточный состав крови, проводить биохимическое исследование крови, содержание электролитов (в т.ч. калия, магния, кальция), глюкозы в крови, сывороточного креатинина каждые 2 недели в течение первых 2 месяцев терапии и в последующем ежемесячно.
Гипокалиемия или гипомагниемия должны быть скорректированы до начала применения вориностата. Особенно тщательный контроль содержания калия и магния следует проводить у пациентов с клиническими симптомами (тошнота, рвота, диарея, нарушение баланса жидкости и симптомы со стороны сердца).
Безопасность применения вориностата у детей не установлена.
Взаимодействия с другими лекарственными препаратами
При одновременном применении вориностата и антикоагулянтов производных кумарина наблюдалось увеличение протромбинового времени и МНО (при данной комбинации следует тщательно контролировать протромбиновое время и МНО).
При одновременном применении вориностата с другими ингибиторами гистон-деацетилазы (например, с вальпроевой кислотой) отмечались тромбоцитопения и кровотечения из ЖКТ (при таких комбинациях следует контролировать содержание тромбоцитов каждые 2 недели в течение первых 2 месяцев терапии).
Применение препарата Золинза только по назначению врача, описание дано для справки!
Почему борода и усы увеличивают риск заразиться коронавирусом?
Содержание инструкции
Названия
Русское название: Золинза.
Английское название: Zolinza.
ATX код
Фарм Группа
•Другие противоопухолевые средства.
(Данные взяты из действующего вещества Vorinostat).
• C84 Периферические и кожные T-клеточные лимфомы.
Противопоказания компонентов
Гиперчувствительность; тяжелая степень печеночной недостаточности; возраст до 18 лет (безопасность и эффективность не изучены); беременность и кормление грудью.
Категория действия на плод по FDA. D.
Не проводилось адекватно-контролируемых исследований вориностата у беременных. Женщинам детородного возраста следует избегать беременности во время лечения вориностатом. Если необходимость в лечении возникает в период беременности или беременность наступает во время лечения, пациентка должна быть осведомлена о потенциальном вреде лечения для плода.
Отсутствуют данные о секреции вориностата в грудное молоко. Учитывая, что в грудное молоко секретируется большинство ЛС и вориностат может вызвать побочные эффекты у младенца, грудное вскармливание во время лечения вориностатом не рекомендуется.
Побочные эффекты компонентов
Безопасность вориностата оценивалась у 111 пациентов с кожной Т-клеточной лимфомой в двух клинических исследованиях. 86 пациентов принимали вориностат в дозе 400 мг 1 раз в сутки. Характерные нежелательные реакции. Связанные с приемом вориностата в режиме 400 мг 1 раз в сутки. Могут быть объединены в 4 группы симптомо-комплексов: со стороны органов ЖКТ (диарея. Тошнота. Анорексия. Снижение массы тела. Рвота. Запор. Снижение аппетита). Общие симптомы (повышенная утомляемость. Озноб). Гематологические нарушения (тромбоцитопения. Анемия) и расстройство вкусовых ощущений (дисгевзия. Сухость во рту).
Наблюдаемые очень часто (≥1/10) нежелательные реакции (клинические и лабораторные), связанные с лечением вориностатом, у пациентов с кожной Т-клеточной лимфомой, принимавших это средство в дозе 400 мг 1 раз в сутки, указаны ниже.
Со стороны крови и лимфатической системы. Очень часто — тромбоцитопения, анемия.
Со стороны обмена веществ и нарушение питания. Очень часто — анорексия, снижение аппетита.
Со стороны ЖКТ. Очень часто — диарея, тошнота, сухость во рту, рвота, запор.
Со стороны кожи и подкожных тканей. Очень часто — алопеция, кожный зуд.
Со стороны скелетно. Мышечной системы и соединительной ткани — очень часто — мышечные спазмы.
Со стороны нервной системы. Очень часто — дисгевзия, головокружение, головная боль.
Общие расстройства и нарушения в месте введения. Очень часто — повышенная утомляемость, озноб; часто — повышение температуры тела.
Со стороны сосудов. Очень часто — периферические отеки.
Со стороны дыхательной системы, органов грудной клетки и средостения. Часто — кашель, инфекции верхних дыхательных путей.
Лабораторные и инструментальные данные. Очень часто — снижение массы тела, увеличение плазменной концентрации креатинина.
Нежелательные реакции 3–5-й степени тяжести наблюдались для следующих из перечисленных выше реакций: тромбоцитопения (5. 8%). Анемия (2. 3%). Анорексия (2. 3%). Снижение аппетита (1. 2%). Тошнота (3. 5%). Мышечные спазмы (2. 3%). Повышенная утомляемость (2. 3%). Озноб (1. 2%) и снижение массы тела (1. 2%). Ни одна из нежелательных реакций не имела 5-ю степень тяжести.
Профиль нежелательных реакций у пациентов, получавших другие дозы вориностата, был аналогичным. Частота выраженной тромбоцитопении, анемии и чувства усталости была повышенной при лечении дозами свыше 400 мг в режиме 1 раз в сутки.
Серьезные нежелательные реакции.
В клинических исследованиях у пациентов с кожной Т-клеточной лимфомой наблюдали следующие связанные с лечением серьезные нежелательные реакции (вне зависимости от принимаемой дозы).
Часто (≥1/100 и.
Инфекционные и паразитарные заболевания. Нечасто — стрептококковая бактериемия.
Со стороны крови и лимфатической системы. Часто — тромбоцитопения, анемия.
Со стороны обмена веществ и нарушение питания. Часто — дегидратация.
Со стороны сосудов. Нечасто — тромбоз глубоких вен, снижение АД.
Со стороны дыхательной системы, органов грудной клетки и средостения. Часто — эмболия ветвей легочной артерии.
Со стороны ЖКТ. Нечасто — диарея, желудочно — кишечные кровотечения, тошнота, рвота.
Со стороны печени и желчевыводящих путей. Нечасто — ишемия печени.
Со стороны нервной системы. Нечасто — ишемический инсульт, обморок.
Общие расстройства и нарушения в месте введения. Нечасто — боль в груди, смерть (неизвестной этиологии), пирексия.
Прекращение лечения.
Из подгруппы пациентов с кожной Т-клеточной лимфомой. Принимавших вориностат в режиме 400 мг 1 раз в сутки. 10. 5% пациентов прекратили лечение в связи со связанными с лечением нежелательными реакциями. В частности анемией. Ангионевротическим отеком. Астенией. Болью в груди. Тромбозом глубоких вен. Ишемическим инсультом. Летаргией. Эмболией ветвей легочной артерии. Поражением кожи и летальным исходом.
Изменение дозы.
В подгруппе пациентов с кожной Т-клеточной лимфомой. Принимавших вориностат в режиме 400 мг 1 раз в сутки. У 10. 5% пациентов потребовалось снизить дозу в связи с нежелательными реакциями. В частности увеличением плазменной концентрации креатинина. Снижением аппетита. Гипокалиемией. Лейкопенией. Нейтропенией. Тромбоцитопенией и рвотой. Среднее время до появления первого побочного эффекта, повлекшего за собой снижение дозы, составило 42 дня (от 17 до 263 дней).
Лабораторные и инструментальные данные.
Отклонения лабораторных параметров наблюдали у 86 пациентов, принимавших вориностат в суточной дозе 400 мг, и у 1 пациента, принимавшего его в суточной дозе 350 мг.
Увеличение плазменной концентрации глюкозы наблюдали у 69% пациентов с кожной Т-клеточной лимфомой, при этом выраженные изменения (3-й степени тяжести) наблюдались только у 5 пациентов. Связь гипергликемии с проводимым лечением установлена у 4,7% пациентов с кожной Т-клеточной лимфомой, принимавших вориностат в суточной дозе 400 мг. Транзиторное невыраженное увеличение плазменной концентрации креатинина наблюдалось у 47,1% пациентов с кожной Т-клеточной лимфомой.
Протеинурия наблюдалась у 51,4% (у 38 пациентов из 74) обследованных пациентов. Клиническая значимость протеинурии не установлена.
Дегидратация.
Исходя из имевших место в клинических исследованиях случаев дегидратации, рассматриваемых как серьезную, связанную с лечением нежелательную реакцию, пациентам рекомендовали соблюдать питьевой режим — не менее 2 л жидкости в день для обеспечения адекватной гидратации. После введения рекомендации в действие частота эпизодов дегидратации снизилась.
Побочные действия у пациентов с другими онкологическими (некожная Т. Клеточная лимфома) заболеваниями.
В клинических исследованиях участвовали пациенты с сóлидными опухолями или другими онкогематологическими заболеваниями (некожная Т-клеточная лимфома), принимавшие вориностат в качестве монотерапии или в комбинации с другими противоопухолевыми средствами. Связанные с лечением нежелательные реакции в этой группе пациентов были в целом сравнимы с профилем нежелательных реакций, наблюдаемых у пациентов с кожной Т-клеточной лимфомой. Частота отдельных нежелательных реакций в группе пациентов с некожной Т-клеточной лимфомой была выше. Наблюдаемые только в группе пациентов с сóлидными опухолями и другими онкогематологическими заболеваниями нежелательные реакции включали единичные эпизоды: нечеткость зрения и слуха. Дисфагию. Астению. Боль в животе. Дивертикулит. Гипонатриемию. Немелкоклеточный рак легкого. Кровотечение из опухоли. Синдром Гийена-Барре. Почечную недостаточность. Задержку мочи. Кашель. Кровохарканье. Эпизоды повышения АД и васкулиты.
У некоторых пациентов в восстановительный период после операций на кишечнике наблюдалось нарушение процесса заживления анастомоза. В связи с этим следует соблюдать осторожность при применении вориностата в периоперационный период, если пациенту требуется операция на кишечнике.
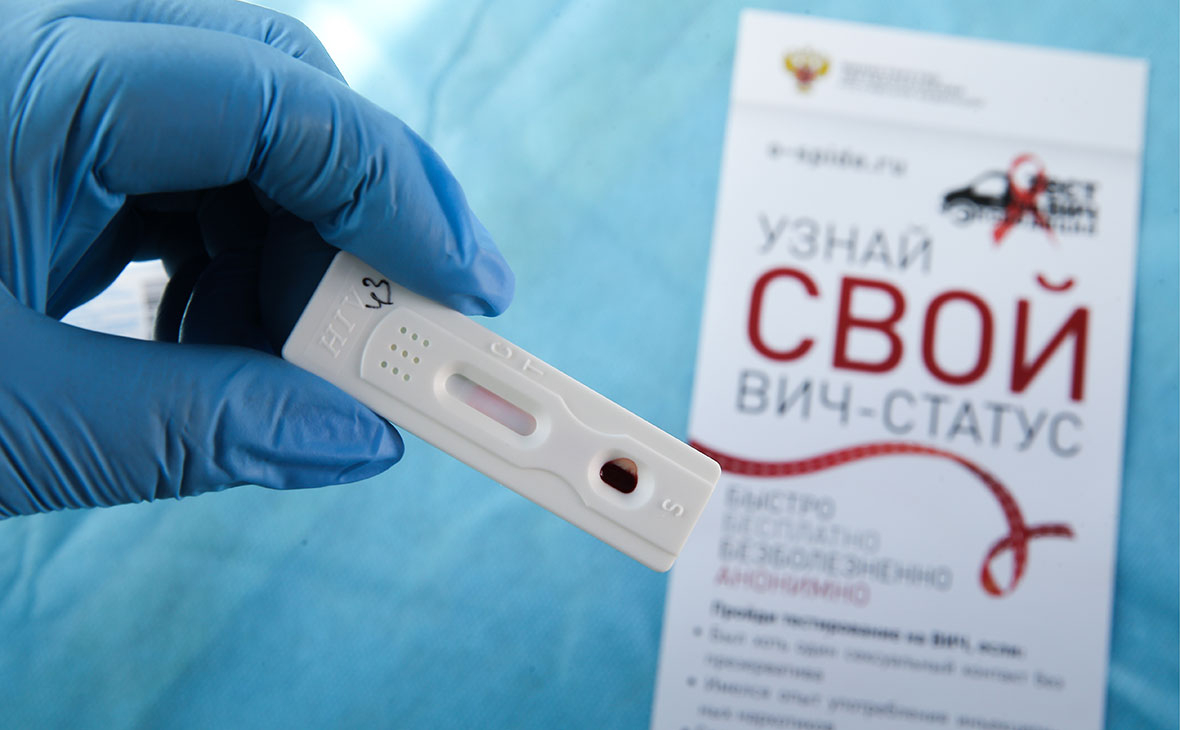
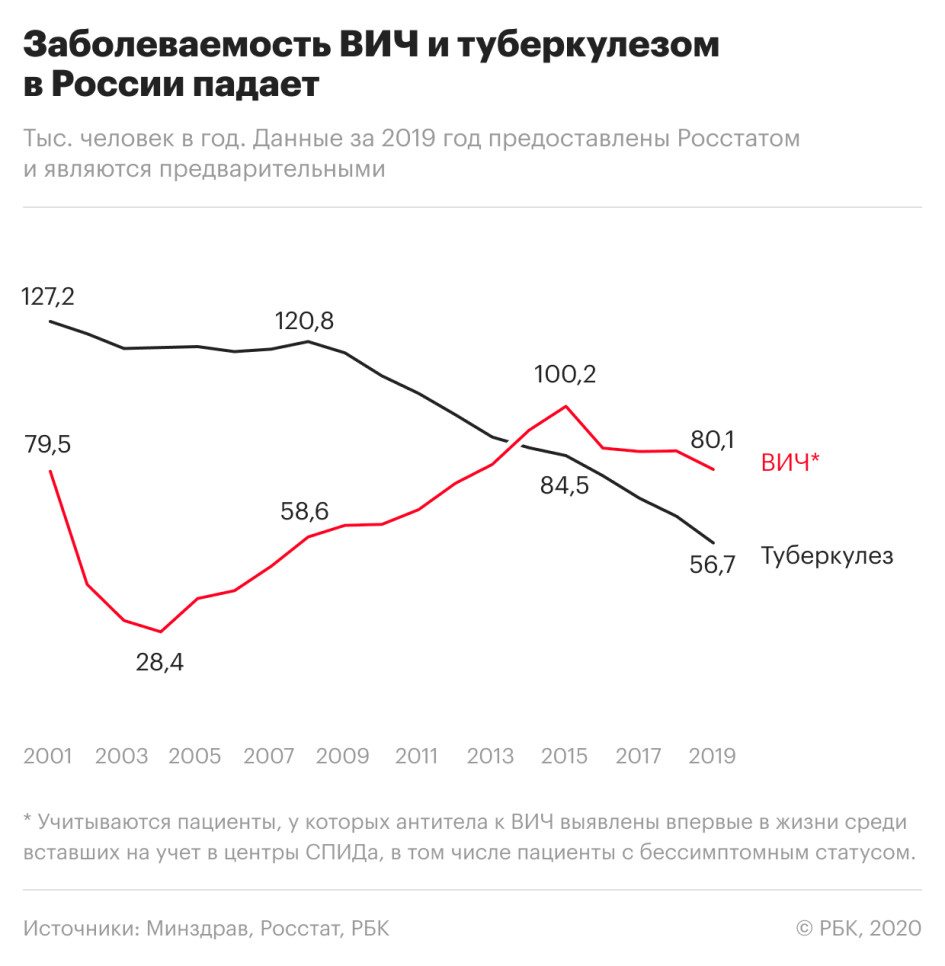
Число заболевших ВИЧ-инфекцией снизилось на 7% по сравнению с 2018 годом — такое значительное снижение наблюдается впервые с 2015 года.
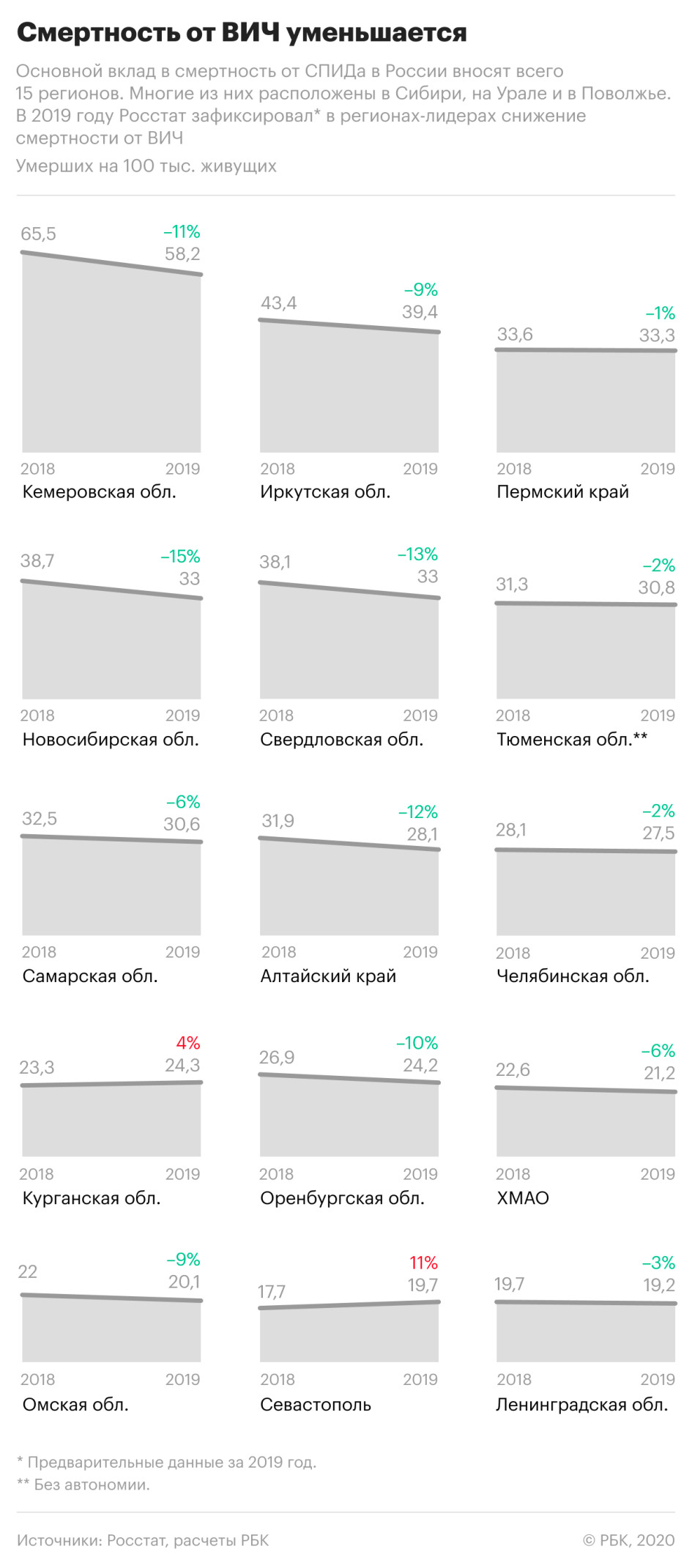
Смертность, связанная с ВИЧ, также уменьшилась — на 8% по сравнению с 2018 годом. В частности, от СПИДа, который развивается на фоне ВИЧ-инфекции, в прошлом году умерли 18,9 тыс. россиян.
При этом смертность от вызванных ВИЧ-инфекцией заболеваний значительно снизилась в регионах, которые являлись лидерами по этому показателю в предыдущие годы. Так, в Кемеровской области смертность по причинам, связанным с ВИЧ-инфекцией, снизилась на 11%, в Иркутской области — на 9%, в Свердловской области — на 13%, в Новосибирской — почти на 15%.
Одновременно показатель существенно вырос в Севастополе — +11%, рост на 4% зафиксирован в Курганской области. РБК направил запросы властям этих регионов.
Кемеровская область, несмотря на снижение смертности, осталась в России лидером по смертям, вызванным ВИЧ-инфекцией. В 2019 году там умерли около 38 тыс. человек, из них 1552 — от вызванных ВИЧ заболеваний, это каждый 25-й из умерших. В Кузбассе, как и в некоторых других регионах Сибири, от иммунодефицита по-прежнему умирают чаще, чем в результате самоубийств, убийств, ДТП и отравлений алкоголем вместе взятых.
По данным министерства здравоохранения региона, в Кемеровской области живут более 31,5 тыс. носителей ВИЧ — это более 2% трудоспособного населения. Антиретровирусную терапию (АРВТ) получают 73% больных — в министерстве уточнили, что это все, у кого есть показания для назначения лечения. Министр здравоохранения области Михаил Малин рассказал РБК, что в 2019 году регион потратил 288,7 млн руб. на противодействие ВИЧ, в 2020 году эта сумма вырастет в 1,4 раза, причем большую часть ее составляют средства регионального бюджета.
В Новосибирской области охват АРВТ составляет 75%, рассказал РБК министр здравоохранения региона Константин Хальзов. Это позволяет увеличить продолжительность жизни зараженных, уточнил он. Всего в регионе живут 31,3 тыс. носителей ВИЧ — это 2% жителей Новосибирской области трудоспособного возраста. Терапию из них получают 61%. Для борьбы с распространением инфекции в регионе действует программа равного консультирования, которая, по мнению министра, помогает социализации людей, живущих с ВИЧ, и формирует у них желание лечиться. Равные консультанты — это люди, живущие с вирусом и обученные консультировать новых пациентов.
В Иркутской области живут 30,1 тыс. больных ВИЧ, сообщила РБК замминистра здравоохранения Иркутской области Елена Голенецкая. АРВТ получают 58% из них. По словам Голенецкой, это все пациенты, которые нуждаются в терапии. Улучшение ситуации с смертностью от ВИЧ в регионе связывают с ростом числа пациентов, проходящих диспансеризацию.
Наркотрафик и другие причины эпидемии
Регионы, в которых больше всего жителей заразилось ВИЧ-инфекцией и умерло от СПИДа, во многом пересекаются с регионами, в которых популярны наркотики опийной группы. Именно в этих регионах, как показывает статистика МВД, в 2019 году правоохранительные органы изъяли большую часть опиатов.
Осторожный оптимизм и фильм Дудя
В 2019 году каждый четвертый россиянин прошел тестирование на ВИЧ, сообщили РБК в пресс-службе Минздрава. Антиретровирусную терапию получают 68,9% заболевших. Эти показатели выше плановых, указанных в Государственной стратегии по противодействию распространения ВИЧ-инфекции.


Кроме того, по словам Вадима Покровского, в некоторых регионах еще остается практика, когда вместо диагноза СПИД ставят непосредственную причину смерти пациента для улучшения отчетности.
Агрессивный новичок
- Вадим Альбертович, ВИЧ был обнаружен еще в конце прошлого века. Почему лекарство так сложно было создать? Чем этот вирус отличался от других?
- С точки зрения биологии этот вирус очень похож на многие другие. Единственное, его фатальное отличие от других вирусов – это поражение иммунной системы человека, именно поэтому организм не может с ним бороться самостоятельно.
- Это своего рода агрессивный новичок?
Мыши на вес золота
- Вы уже дошли до клинических испытаний?
- До клинических - нет, но лабораторных мышей мы уже успешно лечим.
- Зачем в этом проекте мы и американцы нужны друг другу?
- Во-первых, потому что работа с вирусом ВИЧ требует астрономических денежных ресурсов. Ни одна сторона не хотела брать на себя всю тяжесть потенциальных финансовых потерь, поскольку велик риск, что мы будем много работать, но в итоге не сможем создать препарат принципиально нового поколения. Во-вторых, это крайне сложная работа, ее невозможно было сделать только в России, у нас нет ни адекватных моделей на животных, ни биологических технологий для проведения тестов. Например, для экспериментов на животных надо использовать безумно дорогих мышей, которые есть только в США. В то же время, российская химическая школа является ведущей мировой школой в области тонкого химического синтеза. Мы были лидерами 100 лет назад, и надеюсь, останемся ими в будущем. Именно поэтому наших ученых и привлекли для участия в совместном проекте.
- Почему нужны безумно дорогие мыши? Нельзя было найти подешевле?
- А это особые мыши - гуманизированные. У них с помощью современных технологий создали иммунную систему, которая идентична человеческой, можно сказать, что это просто человеческая иммунная система. Такие мыши - очень удобный лабораторный объект, можно испытать препарат и понять, как он будет воздействовать на человека.
- Как с американцами делили зоны ответственности?
- Как я уже сказал, российская сторона отвечает за химическую составляющую, дизайн и синтез соединений. Американские коллеги занимаются биологической частью и компьютерным моделированием. Выглядело это так: сначала мы с американскими партнерами обсуждали идеи, затем их специалисты на суперкомпьютерах проверяли насколько наши предположения реалистичны. Так формировался некий список перспективных соединений. Синтез этих соединений осуществляется здесь в Москве , в ФИЦ Биотехнологии РАН. И в конечном итоге готовые соединение тестируются в США.
От лаборатории до аптеки дистанция 10 лет
- Когда готовое лекарство может появиться в аптеках?
- От лаборатории до аптеки очень длинная дистанция. При благоприятном раскладе понадобится минимум 10 лет. Быстрее невозможно. Это связано с определенной последовательностью экспериментов и необходимым количеством данных, которые надо накопить. А отчасти с тем, что человечество само себе создало огромное количество преград на пути появления новых лекарств. Пройти согласование во всех регулирующих инстанциях очень тяжело и очень дорого. И это не только у нас, это практика всех стран мира. Кроме того, через год наш совместный проект заканчивается и надо будет искать финансирование под практические работы. Многие фармкомпании и фонды не стремятся вступать в такие долгие и дорогостоящие проекты, именно поэтому и сегодня наши исследования финансируются государственными фондами как со стороны России, так и со стороны США. Разработка лекарства для борьбы с ВИЧ это скорее задача государства.
- Я с большой осторожностью отношусь к заявлениям, что кто-то от чего-то вылечился на единичном примере. Мы не знаем достоверно, вылечился он или нет, это не клинические испытания, которые делаются в соответствии с очень строгим протоколом и которым можно доверять. Вирус может затаиться в нейронах и проснуться, когда пройдет много времени. Мы в своей работе придерживаемся позиций доказательной медицины, когда есть слепые клинические испытания на большой выборке. Что касается стволовых клеток, то это вопрос неоднозначный. Безусловно, есть примеры, когда стволовые клетки работают успешно, но это не касается вируса ВИЧ. Поэтому мы исходим из традиционных подходов: с одной стороны, есть вирус, с другой стороны - надо найти вещество, которым этот вирус можно уничтожить.
- А откуда все-таки появился ВИЧ? Существуют самые разные теории, по одной из версий вирус - это побочный эффект разработок биологического оружия…
- Происхождение вируса не является областью моей компетенции, моя ответственность - это разработка вещества, способного убить вирус. На самом деле есть только одна серьезная научная версия происхождения ВИЧ. Вирус появился в процессе мутации в Африке . Сначала он возник у человекообразных приматов, потом был перенесен на человека. Все остальные версии: космические, Божественные, конспирологические, не имеют отношения к здравому смыслу и научным сообществом не рассматриваются. И это не последний случай появления неизвестных ранее смертельных инфекций. Мы считаем, что новые вирусы будут появляться по мере развития человека, а мы будем придумывать вещества для их уничтожения. Это бесконечный непрерывный процесс.
ЧИТАЙТЕ ТАКЖЕ
В Лондоне выздоровел пациент с ВИЧ: случайный успех или победа человечества над СПИДом?
Пациенту, у которого болезнь перешла в смертельно тяжелую стадию, пересадили костный мозг, и ВИЧ пропал из организма (подробности)
Читайте также:


