Обзор литературы вич инфекция
Пожалуй, самой серьезной медицинской проблемой современности следует назвать вирус приобретенного иммунодефицита (ВИЧ) - инфекцию, распространяющуюся по миру со скоростью если не взрывной, то огненной волны.
Пандемия инфекции, вызываемой вирусом иммунодефицита человека (ВИЧ), является в истории человечества крупнейшим событием конца XX века, которое можно поставить в один ряд с двумя мировыми войнами как по числу жертв, так и по тому ущербу, который она наносит обществу. ВИЧ, как война, неожиданно обрушился на человечество и продолжает наступать, поражая новые страны и континенты. В отличие от военных действий ВИЧ-инфекция в большинстве стран распространилась незаметно, и человечеству открылись уже последствия этого тайного распространения - болезнь и смерть миллионов людей.
Еще в 1984 г., когда количество зарегистрированных случаев заболевания исчислялось сотнями, многие исследователи сомневались в том, что люди имеют дело с этиологически самостоятельным и ранее неизвестным заболеванием. Однако спустя десятилетие, к середине 1994 г., стало известно, что 2 млн. жителей земли уже умерли от СПИД. По прогнозу Всемирной организации здравоохранения (ВОЗ), к 2000-му году число зараженных ВИЧ, т.е. людей, почти наверное обреченных умереть от СПИД достигнет 8 млн. человек. Только в США за первые 6 недель 1996 г. от СПИД умерло 4357 человек. Прогноз группы независимых экспертов значительно хуже: минимальное число зараженных ВИЧ в 2000-м году составит 38 млн., а вероятнее всего - 110 млн.
Эти прямые последствия заражения ВИЧ - болезнь и смерть - играют решающую роль в судьбе отдельных личностей, однако, этим не исчерпываются мрачные последствия развития эпидемии. Страдает вся семья инфицированного ВИЧ, что может проявиться в психической травме, потере доходов от труда зараженного члена семьи, увеличение затрат на его содержание и лечение.
Для нации в целом распространение ВИЧ-инфекции означает потерю части населения, а также увеличение уровня тревоги. Недаром во многих странах население относит ВИЧ к одной из самых серьезных опасностей, угрожающих человечеству.
Сама болезнь и ее прямые и косвенные последствия являются катастрофическими для человечества. К 1995-му году на Земле осталось практически не более десятка стран, о появлении в которых случаев ВИЧ-инфекции не было бы официально объявлено. Следовательно, борьба с последствиями пандемии стала общей задачей мирового сообщества.
Разумеется, в истории человечества были времена, когда некоторые инфекции вызывали и более значительные последствия, однако с ними научились бороться или, по крайней мере, подавлять их с помощью карантинных мероприятий, вакцин и антибиотиков.
Хотя грипп продолжал собирать ежегодную дань, малярия стойко держалась в тропических районах, а холера даже устраивала отдельные вылазки, оставалась твердая уверенность в том, что совершенствование средств профилактики и лечения позволит покончить и с этими врагами в ближайшее время. Считалось, что вследствие общих изменений условий жизни на Земле, благодаря победам так называемой цивилизации исчезли многие факторы, необходимые для повторения пандемий.
В случае же ВИЧ-инфекции человечество ощутило себя совершенно беззащитным перед лицом незнакомого и поразительно коварного врага. По этой причине на Земле распространилась еще одна эпидемия - эпидемия страха перед ВИЧ.
Мир был поражен и тем, что среди первых и наиболее пораженных ВИЧ стран оказались США - государство, претендующее на роль мирового лидера во всех областях жизни. Болезнь поставила под сомнение многие ценности современной западной цивилизации: сексуальную свободу и свободу перемещения. ВИЧ бросил вызов всему современному образу жизни, и трудно назвать область общественных отношений, на которую он прямо или косвенно не влияет.
Даже сейчас, когда прошло уже более 10 лет со времени открытия возбудителя болезни - вируса иммунодефицита человека, в мире все еще не существует единой концепции противодействия эпидемии, что связано с различиями в общественном устройстве, а также в реальных условиях жизни и мировоззрении людей в разных странах.
Несмотря на то, что на изучение ВИЧ-инфекции уже истрачено больше средств, чем в прошлом на изучение всех других инфекций, многие загадки ВИЧ-инфекции остаются нерешенными. До сих пор не исчезли сомнения относительно путей распространения ВИЧ, неизвестны в деталях клиническое течение заболевания и его возможные исходы, нет единого представления о патогенезе. Не решен и основной вопрос: как остановить пандемию.

Дата публикации: 26.07.2019 2019-07-26
Статья просмотрена: 67 раз
Ключевые слова: ВИЧ-инфекция, антиретровирусная терапия, лимфоциты CD4.
ВИЧ-инфекция — медленно прогрессирующее заболевание, вызываемое вирусом иммунодефицита человека (ВИЧ). Вирус поражает клетки иммунной системы, имеющие на своей поверхности рецепторы CD4: Т-хелперы, моноциты, макрофаги, клетки Лангерганса, дендритные клетки, клетки микроглии.
Основные пути передачи ВИЧ:
- незащищенный половой контакт с ВИЧ-инфицированным;
- совместное использование с ВИЧ-инфицированным принадлежностей для инъекций;
- вертикальный путь передачи ВИЧ от ВИЧ-инфицированной матери ребенку (во время беременности, родов или после родов, через грудное молоко). [2]
Эпидемиология. Первые случаи СПИДа были описаны в США в 1981 г. Открытие ВИЧ как причины развития СПИДа произошло в 1983 г. Ежегодно ВИЧ заражаются 2,6 млн жителей планеты. Первыми инфицируются, как правило, лица из так называемых групп риска (потребители инъекционных наркотиков, работники коммерческого секса, гомосексуалисты); впоследствии инфекция распространяется половым путем на другие группы населения (при незащищенных половых контактах). [2]
Патогенез. Репликация ВИЧ происходит постоянно, период полужизни вируса составляет около 30 минут. За сутки образуется около 10 10 новых вирионов. На ранней стадии инфекции в ответ на виремию происходит увеличение скорости пролиферации и созревания новых лимфоцитов.
Наружный оболочечный гликопротеин gp120 присоединяется к CD4-рецептору клетки-мишени, вследствие чего gp41 встраивается в мембрану клетки CD4, далее происходит слияние оболочки вируса и клеточной мембраны, в результате чего сердцевина вируса переносится в цитоплазму клетки. Далее с помощью обратной транскриптазы синтезируется ДНК-копия РНК-генома вируса, которая переносится в ядро клетки, встраивается в ДНК инфицированной клетки при помощи вирусной интегразы. Затем происходит процессинг транслированных вирусных белков вирусными интегразами, сборка новых вирионов, которые высвобождаются из клетки и инфицируют новые клетки-мишени.
Клиническое стадии ВИЧ-инфекции по классификации ВОЗ:
– стадия I: бессимптомное течение;
– стадия II: потеря веса 10 % от исходного, продолжающаяся более месяца диарея неясного генеза и/или лихорадка неясного генеза, кандидозный стоматит, волосатая лейкоплакия слизистой полости рта, туберкулез легких, развившийся в течение года;
– стадия IV: СПИД согласно диагностическим критериям.
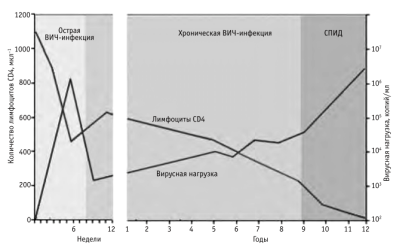
Рис. 1. Естественное течение ВИЧ-инфекции
Лабораторная диагностика. ВИЧ устанавливается при обнаружении антител (АТ) к вирусу, вирусных антигенов (АГ), вирусной РНК или ДНК. Стандарт диагностики — анализ крови на АТ к ВИЧ.
- Положительный результат скринингового теста (ИФА), подтвержденный результатами вестерн блота, непрямого иммунофлюоресцентного анализа или дополнительного анализа на АТ к ВИЧ.
- Выявление маркеров ВИЧ-инфекции в количестве, превышающем установленные уровни определения ДНК или РНК ВИЧ, антигена р24 или выделение культуры ВИЧ.
Важно выявить ВИЧ-инфекцию на ранней стадии, поскольку она характеризуется высоким риском передачи ВИЧ; в это время стандартные серологические анализы на АТ к ВИЧ дают ложноотрицательные результаты и выявление ВИЧ-инфекции может объяснить появление непонятных клинических симптомов. [1]
Согласно рекомендациям: тестирование на ВИЧ должно проводиться всем пациентам в возрасте 13–64 лет и проводиться во всех медицинских учреждениях; пациентов следует предупреждать о том, что обследование будет включать тестирование на ВИЧ; пациентов с положительным результатом следует направлять в медицинское учреждение, специализирующееся на лечении ВИЧ.
Лечение. Цели антиретровирусной терапии:
– клинические: снизить заболеваемость и смертность, связанные с ВИЧ-инфекцией и ее лечением. Увеличить продолжительность и качество жизни ВИЧ-инфицированных;
– вирусологические: снизить вирусную нагрузку до минимального уровня ( -1 ;
– количество лимфоцитов CD4 >500 мкл -1 , при готовности пациента начать терапию;
– независимо от количества лимфоцитов CD4: ВИЧ-ассоциированная нефропатия; беременность, чтобы предупредить перинатальную передачу ВИЧ; сопутствующий гепатит В, при наличии показаний к его лечению, высокая вирусная нагрузка >100 000 копий/мл; возраст инфицированного.
Для лечения ВИЧ-инфекции разрешены к применению 30 отдельных и комбинированных препаратов. Эти препараты принадлежат к пяти фармакологическим группам:
- Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ) (Видекс, Вирид, Зерит, Ретровир, Эмпивир).
- Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) (Вирамун, Интеленс, Рескриптор, Эдурант).
- Ингибиторы протеазы (ИП) (Аптивус, Вирасепт, Инвираза, Калетра, Норвир, Телзир).
- Ингибиторы проникновения (блокаторы корецепторов и ингибиторы слияния) (Селзентри, Фузеон).
- Ингибиторы интегразы (Исентресс). [2]
После начала АРТ наблюдается быстрое снижение уровня РНК ВИЧ в течение 2–4 недель. Максимальный противовирусный эффект ожидается через 4–6 месяцев. Вирусная нагрузка — самый важный критерий эффективности терапии, хотя лучшим прогностическим показателем клинического прогрессирования ВИЧ служит количество лимфоцитов CD4. При низком уровне вирусной нагрузки ( ВИЧ-инфекция, антиретровирусная терапия, лимфоциты CD4
Похожие статьи
[7]. Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ) активны в инфицированных ВИЧ Т-клетках и
Можно выделить три основных направления в генной терапии ВИЧ. Первое — введение генетических последовательностей, которые кодируют.
На модели вирусной ко-инфекции клеток изучено действие антигерпетического препарата ганцикловир и аномального нуклеозида G8.
Моделирование смешанной адено-герпетической инфекции клеток MDBK, ее характеристика и особенности антивирусного действия веществ.
В данной статье представлены методы диагностики, лечения и профилактики вирусного поражения шейки матки. В связи с тем, что происходит омоложение патологии шейки матки, необходимы наиболее ранняя диагностика, своевременное лечение с использованием.
Нуклеозидные (НИОТ) и Нуклеотидные (НтИОТ) ингибиторы обратной транскриптазы блокируют один из ферментов ВИЧ, называемый обратная транскриптаза. Эти препараты часто объединяются в одну группу, называемую НИОТ. Препараты НИОТ подменяют нуклеотиды и.
Вирусное поражение шейки матки (ВПШМ) занимает второе место среди гинекологических заболеваний в мире, в
Если ранее опухолевый процесс на поздних стадиях выявлялся у женщин в возрасте 60 лет и старше, то все чаще вирусное поражение встречается у женщин.
Вопрос информативности анти-Hsp60 антител у больных различными инфекциями в последнее время является актуальным в связи с тем, что выработка этих антител является неспецифической защитной реакцией против патогенов.
На сегодняшний день издано целый ряд научных работ, которые посвящены взаимосвязи герпесвирусной инфекции и бактериальной инфекции при заболеваниях полости рта [7,16,17]. Открыто 80 представителей семейства Herpesviriolae.
В данной статье рассмотрены проблемы герпес-вирусной инфекции. Основное содержание исследования составляет выявление особенностей клинического течения у пациентов разного пола с герпес-вирусной инфекцией.
Данная статья посвящена проблемам диагностики и лечения вирусного иммунодефицита кошек в условиях ветеринарных клиник г. Краснодара. Представлены пошаговый план развития ветеринарных клиник по улучшению диагностики, а также мероприятия, способствующие.
Полный текст:
1. Аглиуллина С.Т., Хасанова Г.Р., Мухарямова Л.М., Хасанова Р.Н. Отношение студентов медицинских факультетов к проблеме ВИЧ-инфекции // Профилактическая и клиническая медицина. -2017. - № 2 (63). - С. 72-77
2. Афонина Л.Ю., Воронин Е.Е. Демографические и клинические особенности ВИЧ-инфицированных женщин в Российской Федерации // Актуальные вопросы профилактики передачи ВИЧ-инфекции от матери ребенку: Материалы межд. науч.-практ. конф. -СПб.: Человек и его здоровье, 2015. - С. 168-170
4. Вехова Е.В., Комарова М.В., Садыкова Г.Б., Струкова Е.А. Оценка информированности молодого поколения о факторах риска инфицирования ВИЧ как один из методов популяционной профилактики в регионе с высоким уровнем пораженности населения // ВИЧ-инфекция и иммуносупрессии. - 2013. - Т. 5, № 2. - С. 117-121
5. Всемирная организация здравоохранения. Расширение тестирования и консультирования на ВИЧ как обязательный компонент мероприятий по обеспечению всеобщего доступа к профилактике, лечению, уходу и поддержке при ВИЧ-инфекции в Европейском регионе ВОЗ. - Копенгаген, 2010. - 28 с
9. Денисов Б.П., Сакевич В.И. Аборты в постсоветской России: есть ли основания для оптимизма? // Демографическое обозрение. - 2014. - Т. 1, № 1. -С. 144-169
10. Кольцова О.В., Яковлева Н.Л., Рассохин В.В., Швед А.Г. Социальные и поведенческие особенности людей, заразившихся ВИЧ-инфекцией // ВИЧ-инфекция и иммуносупрессии. - 2011. - Т. 3, № 4. -C. 75-80
13. Мухарямова Л.М., Хасанова Г.Р., Назарова О.А., Анохин В.А., Созинов А.С. ВИЧ-инфицированные беременные женщины как объект медико-социального анализа: возможности применения качественных социологических методов // Социология медицины. -2007. - № 1. - С. 24-33
15. Плавинский С.Л., Бобрик А.В., Баринова А.Н., Ерошина К.М., Новожилов А.В. Эффективность программ снижения вреда для предотвращения распространения ВИЧ-инфекции в Российской Федерации // Российский семейный врач. - 2009. - Т. 13, № 2. -С. 20-24
16. Проект ГЛОБУС, 2004-2009. ГРАНТ Глобального фонда для борьбы со СПИДом, туберкулезом и малярией RUS-304-G01-H. - М., 2009. - 104 с
17. Самойлова О.С., Артеменко Е.Г., Алексеева Е.Г., Поликарпов Р.В. Обучение врачей акушеров-гинекологов навыкам консультирования женщин по вопросам ВИЧ-инфекции // Актуальные вопросы ВИЧ-инфекции: Материалы межд. науч.-практ. конф. - СПб.: Человек и его здоровье, 2016. - С. 304
18. Сизова Н.В., Губа З.В., Дементьева Н.Е. Развитие резистентности к ВИЧ-препаратам // Экономические и клинические вопросы ВИЧ-инфекции. -2014. - № 6. - С. 187-197
19. Смольская Т.Т. Профилактика ВИЧ-инфекции и ее роль в контексте будущего эпидемии в Российской Федерации // Экология человека. - 2012. - № 2. -С. 47-54
20. СПИДвцифрах. Женева: Объединённая программа Организации объединённых наций по ВИЧ/ СПИДу (ЮНЭЙДС). - 2015. - 12 с
21. Султанбекова Л.Н., Ниаури Д.А., Петрова Н.Н. Социальные аспекты и репродуктивное поведение у ВИЧ-инфицированных женщин // Актуальные вопросы профилактики передачи ВИЧ-инфекции от матери ребенку: Материалы межд. науч.-практ. конф. - СПб.: Человек и его здоровье, 2015. - С. 116-122
22. Таенкова И.О., Троценко О.Е., Балахонцева Л.А., Таенкова А.А. Методы оценки уровня информированности учащейся молодежи Хабаровского края о факторах риска заражения ВИЧ-инфекцией // Анализ риска здоровью. - 2016. - № 4. - С. 119-127. doi: 10.21668/health.risk/2016.4.13
23. Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека. О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2015 году. Государственный доклад. - М., 2016. - С. 106-108
24. Шпаковская Л. Гражданский брак в России: свобода и отношения // Практики и идентичности: гендерное устройство. Сборник статей. - СПб.: Издательство Европейского университета в Санкт-Петербурге, 2010. - C. 27-68
27. Abdool Karim Q., Abdool Karim S.S., Frohlich J.A., Grobler A.C., Baxter C., Mansoor L.E., Kharsany AB, Sibeko S, Mlisana KP, Omar Z, Gengiah TN, Maarschalk S, Arulappan N, Mlotshwa M, Morris L, Taylor D., CAPRISA 004 Trial Group. (2010). Effectiveness and safety of Tenofovir gel, an antiretroviral microbicide, for the prevention of HIV infection in women. Science, 329 (5996), 1168-1174. doi: 10.1126/science.1193748.
28. Anglemyer A., Rutherford G.W., Horvath T., Baggaley R.C., Egger M., Siegfried N. (2013). Antiretroviral therapy for prevention of HIV transmission in HIV-discordant couples. Cochrane Database Syst Rev, 4, CD009153. doi:10.1002/14651858.CD009153.pub3.
30. Baeten J.M., Palanee-Phillips T., Brown E.R., Schwartz K., Soto-Torres L.E., Govender V., Mgodi N.M., Matovu Kiweewa F., Nair G., Mhlanga F., Siva S., Bekker L.G., Jeenarain N., Gaffoor Z., Martinson F., Makanani B., Pather A., Naidoo L., Husnik M., Richardson B.A., Parikh U.M., Mellors J.W., Marzinke M.A., Hendrix C.W., van der Straten A., Ramjee G., Chirenje Z.M., Nakabiito C., Taha T.E., Jones J., Mayo A., Scheckter R., Berthiaume J., Livant E., Jacobson C., Ndase P., White R., Patterson K., Germuga D., Galaska B., Bunge K., Singh D., Szydlo D.W., Montgomery E.T., Mensch B.S., Torjesen K., Grossman C.I., Chakhtoura N., Nel A., Rosenberg Z., McGowan I., Hillier S., MTN-020-ASPIRE Study Team. (2016). Use of a vaginal ring containing Dapivirine for HIV-1 prevention in women. N Engl J Med, 375 (22), 2121-2132. doi: 10.1056/NEJMoa1506110.
32. Bokazhanova A., Rutherford G.W. (2006). The Epidemiology of HIV and AIDS in the world. Coll Antropol, (30), Suppl 2, 3-10.
33. Charania M.R., Crepaz N., Guenther-Gray C., Henny K., Liau A., Willis L.A., Lyles C.M. (2011). Efficacy of structural-level condom distribution interventions: a meta-analysis of U.S. and international studies, 1998-2007. AIDS and Behavior, 15 (7), 1283-1297. doi: 10.1007/s10461-010-9812-y.
34. Cohen M.S., Chen Y.Q., McCauley M., Gamble T., Hosseinipour M.C., Kumarasamy N., Hakim J.G., Kumwenda J., Grinsztejn B., Pilotto J.H., Godbole S.V., Mehendale S., Chariyalertsak S., Santos B.R., Mayer K.H., Hoffman I.F., Eshleman S.H., Piwowar-Manning E., Wang L., Makhema J., Mills L.A., de Bruyn G., Sanne I., Eron J., Gallant J., Havlir D., Swindells S., Ribaudo H., Elharrar V., Burns D., Taha T.E., Nielsen-Saines K., Celentano D., Essex M., Fleming T.R. (2011). Prevention of HIV-1 infection with early antiretroviral therapy. N Engl J Med, (365), 493-505. doi: 10.1056/NEJMoa1105243.
35. Donnell D., Baeten J.M., Kiarie J., Thomas K.K., Stevens W., Cohen C.R., McIntyre J., Lingappa J.R., Celum C. (2010). Heterosexual HIV-1 transmission after initiation of antiretroviral therapy: a prospective cohort analysis. Lancet, 375 (9731), 2092-2098. doi: 10.1016/S0140-6736(10)60705-2.
36. Dunkle K.L., Stephenson R., Karita E., Chomba E., Kayitenkore K., Vwalika C., Greenberg L., Allen S. (2008). New heterosexually transmitted HIV infections in married or cohabiting couples in urban Zambia and Rwanda: an analysis of survey and clinical data. Lancet, 371 (9631), 2183-2191. doi: 10.1016/S0140-6736(08)60953-8.
39. LaCroix J.M., Snyder L.B., Huedo-Medina T.B., Johnson B.T. (2014). Effectiveness of mass media interventions for HIV prevention, 1986-2013: a meta-analysis. J Acquir Immune Defic Syndr, (66), 329-340. doi: 10.1097/QAI.0000000000000230.
43. Marrazzo J.M., Ramjee G., Richardson B.A., Gomez K., Mgodi N., Nair G., Palanee Th., Nakabiito C., van der Straten A., Noguchi L., Hendrix C.W., Dai J.Y., Ganesh Sh., Mkhize B., Taljaard M., Parikh U.M., Piper J., Mâsse B., Grossman C., Rooney J., Schwartz J.L., Watts H., Marzinke M.A., Hillier S.L., McGowan I.M., Chirenje Z.M. (2015). Tenofovir-based preexposure prophylaxis for HIV infection among African women. N Engl J Med, 372 (6), 509-518. doi: 10.1056/NEJMoa1402269.
44. Noar S.M. (2008). Behavioral interventions to reduce HIV-related sexual risk behavior: Review and synthesis of meta-analytic evidence. AIDS Behav, 12 (3), 335-353.
45. Onsomu E.O., Moore D., Abuya B.A., Valentine P., Duren-Winfield V. (2013). Importance of the media in scaling-up HIV testing in Kenya. SAGE Open, 1-12. doi: 10.1177/215824401349
47. Roan N.R., Münch J. (2015). Trends improving preclinical models of HIV microbicide efficacy. Microbiol, 23 (8), 445-447. doi:10.1016/j.tim.2015.05.001.
52. Weller SC, Davis-Beaty K. (2007). Condom effectiveness in reducing heterosexual HIV transmission. Cochrane Database Syst Rev, 4, CD003255. doi: 10.1002/14651858.CD003255.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Пожалуй, самой серьезной медицинской проблемой современности следует назвать вирус приобретенного иммунодефицита (ВИЧ) – инфекцию, распространяющуюся по миру со скоростью если не взрывной, то огненной волны.
Пандемия инфекции, вызываемой вирусом иммунодефицита человека (ВИЧ), является в истории человечества крупнейшим событием конца XX века, которое можно поставить в один ряд с двумя мировыми войнами как по числу жертв, так и по тому ущербу, который она наносит обществу. ВИЧ, как война, неожиданно обрушился на человечество и продолжает наступать, поражая новые страны и континенты. В отличие от военных действий ВИЧ-инфекция в большинстве стран распространилась незаметно, и человечеству открылись уже последствия этого тайного распространения – болезнь и смерть миллионов людей.
Еще в 1984 г., когда количество зарегистрированных случаев заболевания исчислялось сотнями, многие исследователи сомневались в том, что люди имеют дело с этиологически самостоятельным и ранее неизвестным заболеванием. Однако спустя десятилетие, к середине 1994 г., стало известно, что 2 млн. жителей земли уже умерли от СПИД. По прогнозу Всемирной организации здравоохранения (ВОЗ), к 2000-му году число зараженных ВИЧ, т.е. людей, почти наверное обреченных умереть от СПИД достигнет 8 млн. человек. Только в США за первые 6 недель 1996 г. от СПИД умерло 4357 человек. Прогноз группы независимых экспертов значительно хуже: минимальное число зараженных ВИЧ в 2000-м году составит 38 млн., а вероятнее всего – 110 млн.
Эти прямые последствия заражения ВИЧ – болезнь и смерть – играют решающую роль в судьбе отдельных личностей, однако, этим не исчерпываются мрачные последствия развития эпидемии. Страдает вся семья инфицированного ВИЧ, что может проявиться в психической травме, потере доходов от труда зараженного члена семьи, увеличение затрат на его содержание и лечение.
Для нации в целом распространение ВИЧ-инфекции означает потерю части населения, а также увеличение уровня тревоги. Недаром во многих странах население относит ВИЧ к одной из самых серьезных опасностей, угрожающих человечеству.
Сама болезнь и ее прямые и косвенные последствия являются катастрофическими для человечества. К 1995-му году на Земле осталось практически не более десятка стран, о появлении в которых случаев ВИЧ-инфекции не было бы официально объявлено. Следовательно, борьба с последствиями пандемии стала общей задачей мирового сообщества.
Разумеется, в истории человечества были времена, когда некоторые инфекции вызывали и более значительные последствия, однако с ними научились бороться или, по крайней мере, подавлять их с помощью карантинных мероприятий, вакцин и антибиотиков.
Хотя грипп продолжал собирать ежегодную дань, малярия стойко держалась в тропических районах, а холера даже устраивала отдельные вылазки, оставалась твердая уверенность в том, что совершенствование средств профилактики и лечения позволит покончить и с этими врагами в ближайшее время. Считалось, что вследствие общих изменений условий жизни на Земле, благодаря победам так называемой цивилизации исчезли многие факторы, необходимые для повторения пандемий.
В случае же ВИЧ-инфекции человечество ощутило себя совершенно беззащитным перед лицом незнакомого и поразительно коварного врага. По этой причине на Земле распространилась еще одна эпидемия – эпидемия страха перед ВИЧ.
Мир был поражен и тем, что среди первых и наиболее пораженных ВИЧ стран оказались США – государство, претендующее на роль мирового лидера во всех областях жизни. Болезнь поставила под сомнение многие ценности современной западной цивилизации: сексуальную свободу и свободу перемещения. ВИЧ бросил вызов всему современному образу жизни, и трудно назвать область общественных отношений, на которую он прямо или косвенно не влияет.
Даже сейчас, когда прошло уже более 10 лет со времени открытия возбудителя болезни – вируса иммунодефицита человека, в мире все еще не существует единой концепции противодействия эпидемии, что связано с различиями в общественном устройстве, а также в реальных условиях жизни и мировоззрении людей в разных странах.
Несмотря на то, что на изучение ВИЧ-инфекции уже истрачено больше средств, чем в прошлом на изучение всех других инфекций, многие загадки ВИЧ-инфекции остаются нерешенными. До сих пор не исчезли сомнения относительно путей распространения ВИЧ, неизвестны в деталях клиническое течение заболевания и его возможные исходы, нет единого представления о патогенезе. Не решен и основной вопрос: как остановить пандемию.
Полный текст:
Представлен обзор научной литературы по современным подходам к проведению антиретровирусной терапии пациентам, инфицированным вирусом иммунодефицита человека, контролю резистентности вируса к антиретровирусным препаратам, вирусологическому обоснованию, клиническим показаниям и результатам исследований по оценке эффективности упрощенных схем антиретровирусной терапии в виде монотерапии или комбинации двух антиретровирусных препаратов. Вирусологическая супрессия вируса иммунодефицита человека (вирусная нагрузка менее 50 копий/мл) является наиболее важным критерием эффективности антиретровирусной терапии, позволяет предотвратить формирование резистентности вируса к антиретровирусным препаратам. Перевод пациентов на упрощенные схемы антиретровирусной терапии позволяет уменьшить частоту нежелательных явлений и взаимодействий антиретровирусных препаратов, повысить приверженность к терапии, снизить стоимость лечения. Внедрение упрощенных схем терапии в клиническую практику возможно при использовании препаратов с высоким генетическим барьером к резистентности у тщательно отобранных пациентов, достигших вирусологической супрессии вируса иммунодефицита человека на стандартных трехкомпонентных схемах, не имевших в прошлом тяжелой иммуносупрессии (CD4+ T-лимфоциты
230009, Гродно, ул. Горького, 80.
3. Samji H., Cescon A., Hogg R.S., Modur S.P., Althoff K.N., Buchacz K., Burchell A.N., Cohen M., Gebo K.A., Gill M.J., Justice A., Kirk G., Klein M.B., Korthuis P.T., Martin J., Napravnik S., Rourke S.B., Sterling T.R., Silverberg M.J., Deeks S., Jacobson L., Bosch R.J., Kitahata M.M., Goedert J.J., Moore R., Gange S.J. North American AIDS Cohort Collaboration on Research and Design (NA-ACCORD) of IeDEA. Closing the Gap: Increases in Life Expectancy among Treated HIV-Positive Individuals in the United States and Canada. PLoS One, 2013, Vol. 18 (8), рр. 81355. DOI: 10.1371/journal.pone.0081355. eCollection 2013.
4. 90–90–90 An ambitious treatment target to help end the AIDS epidemic. URL: unaids.orghttp://www.unaids.org/sites/default/ files/media_asset/90–90–90_en.pdf.
6. Матиевская Н.В. Ко-инфекция ВИЧ/ВГС: этиология, эпидемиология, патогенез, клиника, диагностика, лечение. Гродно: ГрГМУ, 2013, 352 с. [Matevskaya N.V. Co-infection HIV/HCV: etiology, epidemiology, pathogenesis, clinic, diagnostics, treatment. Grodno: Grodno Medical University, Belarus, 2013, 352 p. (In Russ.)].
7. Girard P.M., Antinori A., Arribas J.R., Ripamonti D., Bicer C., Netzle-Sveine B., Hadacek B., Moecklinghoff C. Week 96 efficacy and safety of darunavir/ritonavir monotherapy vs. darunavir/ritonavir with two nucleoside reverse transcriptase inhibitors in the PROTEA trial. HIV Medicine, 2017, Vol. 18, рр. 5–12.
8. Bierman W.F., van Aftmael M.A., Nijhuis M., Danner S.A., Boucher C.A. HIV monotherapy with ritonavir-boosted protease inhibitors: a syste- matic review. AIDS, 2009, Vol. 23, рр. 279–291.
9. Mathis S., Khanlari B., Pulido F., Schechter M., Negredo E., Nelson M., Vernazza P., Cahn P., Meynard J.-L., Arribas J., Bucher H.C. Effectiveness of protease inhibitor monotherapy versus combination antiretroviral maintenance therapy: a meta-analysis. PLoS One, 2011, Vol. 6 (7), рр. 22003. DOI: 10.1371/journal.pone.0022003.
10. Taylor B.S., Olender S.A., Tieu H.-V., Wilkin T. J. CROI 2016: Advances in Antiretroviral Therapy. Top. Antivir. Med., 2016, Vol. 24 (1), рр. 59–81.
13. Scherrer A.U., von Wyl V., Yang W.L., Kouyos R.D., Böni J., Yerly S., Klimkait T., Aubert V., Cavassini M., Battegay M., Furrer H., Calmy A., Vernazza P., Bernasconi E., Günthard H.F. Swiss HIV Cohort Study Emergence of Acquired HIV-1 Drug Resistance Almost Stopped in Switzerland: A 15-Year Prospective Cohort Analysis. Clin. Infect. Dis., 2016, Vol. 62 (10), рр. 1310–1317. DOI: 10.1093/cid/ciw128.
16. Fabeni L., Alteri C., Orchi N., Gori C., Bertoli A., Forbici F., Montella F., Pennica A., De Carli G., Giuliani M., Continenza F., Pinnetti C., Nicastri E., Ceccherini-Silberstein F., Mastroianni C.M., Girardi E., Andreoni M., Antinori A., Santoro M.M., Perno C.F. Recent Transmission Clustering of HIV-1 C and CRF17_BF Strains Characterized by NNRTI-Related Mutations among Newly Diagnosed Men in Central Italy. PLoS One, 2015, Vol. 13 (10), pp. e0135325. DOI: 10.1371/journal.pone.0135325.
17. Armenia D., Di Carlo D., Calcagno A., Vendemiati G., Forbici F., Bertoli A., Berno G., Carta S., Continenza F., Fedele V., Bellagamba R., Cicalini S., Ammassari A., Libertone R., Zaccarelli M., Ghisetti V., Andreoni M., Ceccherini-Silberstein F., Bonora S., Di Perri G., Antinori A., Perno CF., Santoro M.M. Pre-existent NRTI and NNRTI resistance impacts on maintenance of virological suppression in HIV-1-infected patients who switch to a enofovir/emtricitabine/rilpivirine single-tablet regimen. J. Antimicrob. Chemother., 2017, Vol. 72 (3), рр. 855–865. DOI: 10.1093/jac/dkw512.
18. Swenson L.C., Min J.E., Woods C.K., Cai E., Li J.Z., Montaner J.S., Harrigan P.R., Gonzalez-Serna A. HIV drug resistance detected during low-level viraemia is associated with subsequent virologic failure. AIDS, 2014, Vol. 15 (28), рр. 1125–1234. DOI: 10.1097/QAD.0000000000000203.
19. Nozza S., Svicher V., Saracino A., d’Ettorre G., De Luca A., Maggiolo F., Bonora S., di Biagio A., Rusconi S., Mussini C. State of the Art of Dual Therapy in 2015. AIDS Rev., 2015, Vol. 17 (3), рр. 127–134.
21. Tyrer M., Swaden L., Marshall N.J., Johnson M. Switching to dual therapy with darunavir/ritonavir and etravirine: a simplification strategy. J. Int. AIDS Soc., 2010, Vol. 13 (4), рр. 51. DOI: 10.1186/1758-2652-13-S4-P51.
22. Stellbrink H.J., Le Fevre E., Carr A., Saag M.S., Mukwaya G., Nozza S., Valluri S.R., Vourvahis M., Rinehart A.R., McFadyen L., Fichtenbaum C., Clark A., Craig C., Fang A.F., Heera J. Once-daily maraviroc versus tenofovir/emtricitabine each combined with darunavir/rito- navir for initial HIV-1 treatment. AIDS, 2016, Vol. 30 (8), рр. 1229–1238. DOI: 10.1097/QAD.0000000000001058.
23. Ofotokun I., Sheth A.N., Sanford S.E., Easley K.A., Shenvi N., White K., Eaton M.E., Del Rio C., Lennox J.L. A Switch in Therapy to a Reverse Transcriptase Inhibitor Sparing Combination of Lopinavir/Ritonavir and Raltegravir in Virologically Suppressed HIV-Infected Patients: A Pilot Randomized Trial to Assess Efficacy and Safety Profile: The KITE Study. AIDS Res. Hum. Retroviruses, 2012, Vol. 28 (10), рр. 1196–1206. DOI: 10.1089/AID.2011.0336.
24. Merino D., Muñoz L., Pasquau J., Ojeda G., Bancalero P., Chueca N., Pineda J.A., Macías J., Recio E., Márquez M., García C., Jiménez P. Efficacy and safety of once-daily maraviroc plus ritonavir-boosted darunavir in pretreated HIV-infected patients in a real-life setting. HIV Med., 2014, Vol. 15 (7), рр. 417–424. DOI: 10.1111/hiv.12129.
25. Monteiro P., Perez I., Laguno M., Martínez-Rebollar M., González-Cordon A., Lonca M., Mallolas J., Blanco J.L., Gatell J.M., Martínez E. Dual therapy with etravirine plus raltegravir for virologically suppressed HIV-infected patients: a pilot study. J. Antimicrob. Chemother., 2014, Vol. 69 (3), рр. 742–748. DOI: 10.1093/jac/dkt406.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Читайте также:


