Адгезия и миграция нейтрофилов при воспалении в легких.
Добавил пользователь Владимир З. Обновлено: 28.01.2026
Выпускник медицинского факультета УЛГУ. Интересы: современные медицинские технологии, открытия в области медицины, перспективы развития медицины в России и за рубежом.
- Запись опубликована: 24.11.2020
- Reading time: 3 минут чтения
Небольшое перемещение лейкоцитов из кровеносных сосудов в ткани - диапедез или так называемая эмиграция лейкоцитов - нормальное явление. Однако при воспалительных условиях этот процесс идет интенсивно и активно - лейкоциты используют в процессе эмиграции АТФ. И этот процесс уже выходит за пределы нормы.
Почему происходит эмиграция лейкоцитов
Основной фактор, вызывающий эмиграцию лейкоцитов, - положительная гемотаксия в очаге воспаления. Эмиграции способствует повышенная проницаемость сосудистой стенки, замедление кровообращения и экссудации.
Эмиграция лейкоцитов следует за экссудацией, она начинается при артериальной гиперемии, но достигает пика при венозной гиперемии и застое . Экссудация происходит в основном из капилляров и вен, тогда как эмиграция лейкоцитов происходит из капилляров, вен и мелких вен.
Венозный застой
Эндотелиальные клетки сосудов прикрепляются к непрерывной базальной мембране, состоящей из коллагеновых волокон и гомогенного вещества, богатого комплексами белковых полисахаридов. В нормальных условиях эндотелиальная поверхность покрыта тонким слоем фибринового вещества, примыкающего к фиксированному слою плазмы крови, который, в свою очередь, граничит с движущейся частью плазмы.
Как протекает эмиграция лейкоцитов в очаг воспаления
Эмиграцию лейкоцитов в очаг воспаления можно разделить на три периода:
- Адгезия лейкоцитов. Так называемое крайнее положение. Которая длится от нескольких минут до одного часа,
- Прохождение лейкоцитов через эндотелий сосудов - длится несколько минут.
- Лейкоциты перемещаются к очагу воспаления и в тканях очага воспаления - длится много часов и даже дней.
С адгезией лейкоцитов меняется расположение этих элементов на поверхности венозного эндотелия. В нормальных условиях лейкоциты не касаются слоя фибрина, но в случае воспаления структура фибринового цемента изменяется, и внутренняя поверхность сосуда выстлана чешуйчатым материалом, содержащим кислые мукополисахариды, мукопротеины и соляную кислоту. Нити фибрилл могут пересекать просвет даже мелких кровеносных сосудов.
Когда скорость кровообращения снижается, эти нити захватывают белые кровяные тельца, и они контактируют с измененным слоем фибринового цемента. Прежде чем прикрепиться к эндотелию сосудов, лейкоциты часто совершают очень сложные траектории движения - даже против кровотока.
Считается, что адгезия лейкоцитов к эндотелию определяется электрохимическими силами - потерей отрицательного заряда лейкоцитов и специфических химических связей между мембранами контактирующих клеток.
После адгезии к эндотелию сосудов нейтрофил развивает цитоплазматическое расширение, которое проникает между эндотелиальными клетками и образует отверстие в базальной мембране. Важную роль в изменении молекулярной структуры базальной мембраны и повышении ее проницаемости играют ферменты лейкоцитарных гранул (эластаза, коллагеназа).
Гранулы лейкоцитов также содержат катионные белки, которые также действуют на стенку кровеносных сосудов и способствуют эмиграции.
Первоначально в изгнании эмигрирующей клетки органелл нет. Затем за удлинением следует остальная масса гранулоцитов с ядром и гранулами. Эти клетки перемещаются к месту воспаления со скоростью от 6 до 12 микрон в минуту.
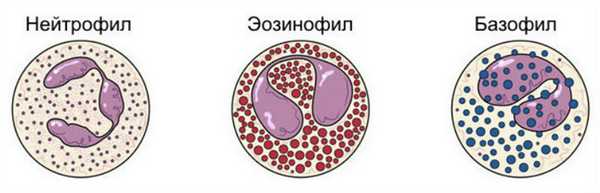
Разновидности гранулоцитов
На эмиграцию гранулоцитов влияет тип воспаления. Например, в случае бактериального воспаления эмигрируют в основном нейтрофилы, но в экссудате аллергического воспаления много лимфоцитов и эозинофилов. Гранулы этих лейкоцитов содержат вещества, инактивирующие гистамин, серотонин и, возможно, хинины, которых много в тканях в условиях гиперчувствительности.
Эмиграция моноцитов и лимфоцитов немного отличается от эмиграции нейтрофилов. Нейтрофилы мигрируют через эндотелиальную щель, а моноциты и лимфоциты мигрируют через эндотелий. После попадания в эндотелиальную клетку вокруг них образуется большая вакуоль. Попадая в него, моноцит и гимфоцит проходят через эндотелиальную клетку.
Эмиграция лимфоцитов и моноцитов - более медленный процесс, эти клетки позже появляются в воспаленных тканях и образуют второй слой или лейкоциты.
Хемотаксис
Хемотаксис - это активное движение лейкоцитов либо в направлении определенных химических раздражителей, либо от них.
В первом случае речь идет о положительной хемотаксии, а во втором - об отрицательной. Положительный хемотаксис играет роль на всех стадиях эмиграции лейкоцитов, особенно когда эти клетки уже покинули кровеносный сосуд и мигрируют во внесосудистое пространство.
И. Мечников первым наблюдал активное движение лейкоцитов к очагу воспаления и описал так называемый закон эмиграции лейкоцитов. Согласно ему, гранулоциты очень чувствительны к раздражителям хемотаксиса - так называемым гемоаттрактантам, поэтому они первыми эмигрируют к очагу воспаления. Хемотаксис моноцитов и лимфоцитов против этих раздражителей ниже. За гранулоцитами следуют моноциты и, наконец, лимфоциты.
Химические раздражители, вызывающие положительный гемотаксис, изучены достаточно подробно. Они делятся на две группы - хемотаксины и хемотаксигены.
- Хемотаксины - это вещества, которые могут привлекать лейкоциты.
- Хемотаксигены сами по себе не вызывают хемотаксии, но способствуют образованию хемотаксинов.
Примерами нейтрофильных хемотаксинов являются денатурированные белки, калихреин, компоненты комплемента (C3, C5), бактериальные токсины и гемотаксигены - трипсин, плазмин, коллагеназа, крахмал, гликоген, комплексы антиген-антитело. Хемотаксис подавляется гидрокортизоном. простагландины Ei и E2, цАМФ, колхицин.
Хемотаксины макрофагов представляют собой бактериальные культуры (Streptococcus pneumoniae, Corynebacteria) фильтрат белковых фракций, компонента С5а комплемента и др., кроме хемотаксигенов - липополисахаридов кишечных микробов, микобактерий, фракций лизосом лейкоцитов, протеиназ макрофагов.
Лейкоциты эозинофилов являются факторами хемотаксиса эозинофилов (высвобождаемых аллергеном и IgE из легких и гладких мышц), лимфокинов и других, но хемотаксигены представляют собой различные иммунные комплексы, а также продукты агрегации IgG и IgM.
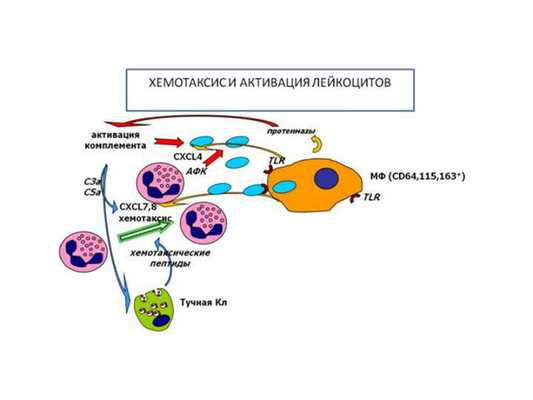
Хемотаксис и активация лейкоцитов
В настоящее время считается, что реципиенты различных хемоаттрактантов присутствуют на поверхности эмигрирующих клеток (макрофагов). Например, были изучены рецепторы на поверхности макрофагов на Fc-фрагменте иммуноглобулинов, компоненте C3 комплемента и лимфокинах. Контакт клеточной мембраны с хемоаттрактантом изменяет мембранный потенциал, увеличивает проницаемость мембраны, увеличивает транспорт ионов Ca и Mg в клетке. Эти ионы контролируют функцию сокращения актомиозина. Активация микрофибрилл и внутриклеточной канальцевой системы способствует гематокриту и эмиграции лейкоцитов.
Отток экссудата способствует прохождению лейкоцитов через эндотелиальную щель. Кроме того, движение лейкоцитов также связано с некоторыми физико-химическими факторами. Воспалительные сурфактанты (аминокислоты, полипептиды) уменьшают поверхностное натяжение поверхности лейкоцитов и образование цитоплазматического объема на их поверхности, но положительно заряженные тканевые макромолекулы снижают отрицательный заряд лейкоцитов, нарушая электростатическую стабильность лейкоцитарной мембраны. Однако основную роль играют активные движения лейкоцитов, использующие энергию мацергических соединений.
Эмигрантские лейкоциты играют важную роль в дальнейшем развитии воспаления. Эти клетки являются источником биологически активных веществ. Однако главная из них - фагоцитарная функция лейкоцитов.
Воспаление. Фагоцитоз. Асептическое и острое воспаление. Часть 7
- Запись опубликована: 25.11.2020
- Reading time: 4 минут чтения
Фагоцитоз - это способность определенных клеток (фагоцитов) удерживать и переваривать плотные частицы. Это явление было открыто И. Мечниковым.
Фагоцитоз осуществляется микрофагами (нейтрофилами) и системой мононуклеарных макрофагов.
Мононуклеарные макрофаги
Система (MMS) включает следующие элементы:
- промоноциты (костный мозг);
- моноциты (кровь);
- тканевые макрофаги;
- гистиоциты соединительной ткани;
- печеночные клетки Куппера;
- легочные альвеолярные макрофаги;
- свободные и фиксированные макрофаги лимфатической ткани;
- плевру и перитонеальные макрофаги.
Клетки мононуклеарной системы объединяет общее происхождение гемопоэтических клеток и саморегуляция.
Моноцитопоэз
Моноцитопоэз - это стимулирующий фактор колонии фибробластов и фактор роста макрофагов, но он же подавляет (отрицательная саморегуляция) интерферон фибробластов и лейкоцитов и т. д.
Процесс фагоцитоза делится на четыре стадии:
- Приближение.
- Адгезия.
- Оседание;
- Стадия пищеварения.
Фаза приближения
Фагоцит приближается к объекту - бактериям, мервому клеточному элементу, инородному объекту. При движении под действием хемотаксиса цитоплазма фагоцита образует удлинения (псевдоподии).
Адгезия
Способствует образованию аминополисахаридов на поверхности фагоцитов и перекрытию фагоцитарного объекта белками сыворотки, особенно иммуноглобулинами. Последний механизм по сути является опсонизацией - бактерии и поврежденные клетки перекрываются с IgM, IgG и компонентами комплемента (C3, C5 и др.), что облегчает адгезию к фагоциту.
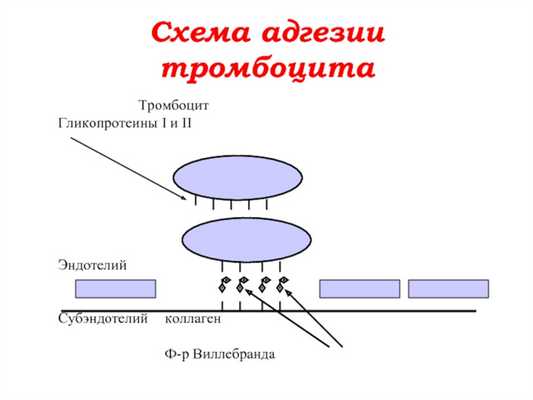
Адгезия
Поверхность фагоцита заряжена отрицательно, поэтому адгезия лучше, если объект, подлежащий фагоцитозу, заряжен положительно. Менее фагоцитарны отрицательно заряженные объекты, такие как опухолевые клетки.
Оседание
Этап фагоцитации объекта - путь инвагинации. Сначала фагоцит образует углубление, а затем фагосому - вакуоль, содержащую объект, подлежащий фагоцитозу. НАДН-зависимая оксидаза в мембране фагоцитов активируется до образования фагосом; в результате O2 превращается в O 2 ~ (супероксид-анион) и образуется H 2 O 2.
Эти продукты обладают бактерицидным действием, а также вызывают образование свободных радикалов. Под действием пероксидаз и каталаз H 2 O 2 расщепляется и высвобождается молекулярный O 2. Свободные радикалы и активный молекулярный O 2 действуют на мембрану фагоцита и объект, подлежащий фагоцитозу, активируя перекисное окисление липидов.
Липопероксиды и свободные радикалы неустойчивы к лизосомным мембранам и способствуют высвобождению лизосомальных ферментов.
Стадия пищеварения
Лизосомы присоединяются к фагосоме, содержащей фагоцитарный объект. Эти органеллы содержат все ферменты, необходимые для расщепления углеводов, белков, жиров и нуклеиновых кислот. В еще неактивной форме они попадают в вакуоль фагоцитов.
Пищеварительная вакуоль образуется при pH около 5,0, близком к оптимальному для лизосомальных ферментов. Активируются лизосомальные ферменты, и фагоцитарный объект постепенно переваривается. Во время стадии пищеварения проницаемость мембраны фагосомы увеличивается, содержимое фагосомы ускользает в цитоплазму, и микрофаг умирает (этому процессу способствует ацидоз). В этом случае фагоцитарный микроорганизм также может сохранять жизнеспособность.
Роль макрофагов в воспалительном процессе
Макрофаги начинают участвовать в фагоцитозе позже микрофагов. Макрофаги также более устойчивы к гипоксии и ацидозу, например, моноциты жизнеспособны даже при pH 5,5.
В очаге воспаления макрофаги выполняют несколько функций:
- Фагоцитируют бактериальные остатки, оставшиеся после эвакуации гноя и продуктов распада тканей - очищающая функция;
- Высвобождают лизосомальные ферменты - гиалуронидазу, аминопептидазу и др;
- Синтезируют компоненты системы комплемента и простагландины.
В то же время воспаленная тканевая среда также стимулирует образование фибробластов и фиброцитов. Постепенно появляется новая, богатая сосудами грануляционная ткань.
Фагоцитоз стимулируется продуктами повреждения тканей - внутриклеточные белки, ферменты, полипептиды, аминокислоты, электролиты и т. д., биологически активными веществами, половыми гормонами, тироксином, адреналином, лихорадкой. Но подавляется недостатком стимулирующих факторов, глюкокортикоидов, гликолортикоидов, ацетилхолина, ацетилхолина.
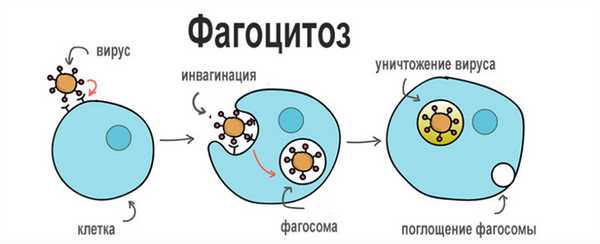
Фагоцитоз
Считается, что клетки плаценты и злокачественные опухоли способны секретировать вещество, которое подавляет функцию макрофагов, иммунологические реакции лимфоцитов и эмиграцию лейкоцитов, что приводит к значительному ослаблению или даже прекращению воспаления.
Объекты, которые фагоциты не могут переваривать, остаются в этих клетках в течение длительного времени и покрываются тонкой пленкой аминополисахаридов. После гибели фагоцитов они повторно фагоцитируются или выводятся из организма. Процесс, при котором фагоцит после переваривания высвобождает часть продуктов своего фагоцитоза в окружающую среду, называется экструзией.
Фагоцитоз - не единственный в организме механизм борьбы с воспалением. Большинство микроорганизмов погибают в условиях ацидоза, а также от ферментов, высвобождаемых во время гибели клеток и функционирования иммунокомпетентной системы.
Нейтрофилы во внеклеточном пространстве секретируют катионные белки, которые могут убивать ферменты без ферментов и фагоцитоза. Таким образом, воспалительные очаги постепенно избавляются от микроорганизмов и мертвых клеток.
Асептическое и острое воспаление
Дальнейшее течение воспаления зависит от того, является ли воспаление асептическим или бактериальным.
В асептических воспалительных условиях, например, вокруг хирургического шва, инородного тела, стенка микрофагов (нейтрофилов) начинает формироваться в течение нескольких часов, достигая максимума в течение дня.
Позже появляется следующий вал макрофагов, который достигает максимума через 2-3 раза. в день. Эмигрировавшие лейкоциты постепенно становятся неподвижными, больше не могут делиться и погибают в течение 3-5 дней. 2-3. на 5 сутки начинает формироваться стенка фибробластов, а на 5 сутки - соединительнотканная капсула.
Таким образом, в случае острого воспаления патогенный агент в организме преобразует белки, которые участвуют в реакции антиген-антитело, медиаторы и модуляторы воспаления, систему фагоцитов и миграцию клеток. В результате заканчивается острое воспаление. Однако, если инфекционные агенты попадают в участок асептического воспаления, например, в результате травмы, это воспаление становится септическим (бактериальным) воспалением.
Бактериальные воспалительные состояния бактерий и токсинов, не вызывающие гиперемии, экссудации и эмиграции лейкоцитов. Между клетками воспаленных тканей и особенно вокруг кровеносных сосудов накапливается все больше и больше микрофагов. Лизосомы микрофагов содержат множество активных ферментов, и эти клетки также начинают процесс фагоцитоза. При пальпации воспаленная ткань в это время кажется плотной, поэтому это называется стадией воспалительной инфильтрации.
По мере прогрессирования воспаления лейкоциты и те тканевые клетки, которые претерпели необратимые изменения во время воспаления, погибают. В этих клетках высвобождаются лизосомальные ферменты, которые расщепляют тканевые белки, белковые и липидные комплексы и другие структуры. Это стадия гнойного размягчения воспаления.
Эти стадии наблюдаются, например, у пациентов с гнойным воспалением перикарда (фурункул), гнойным воспалением апокринных потовых желез (гидраденит) и гнойным воспалением соединительной ткани (флегмона). При вдыхании воспаленная ткань выглядит мягкой, с характерным раскачиванием - флюктуацией. Образуется замкнутое скопление гноя - абсцесс.
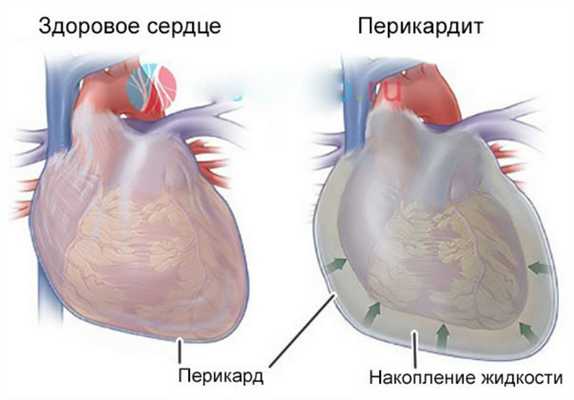
Гнойное воспаление перикарда
Гной разрывается в направлении наименьшего сопротивления (либо наружу, либо внутри тела). Если гной попадает в кровоток (пемия), в организме может развиться множество очагов гноя, но под действием микроорганизмов и токсических веществ - угрожающее общее заболевание (сепсис, септикопиемия). Поэтому важно диагностировать накопление гноя и обеспечить хирургический дренаж гноя наружу.
Воспаление и его атрибуты
Острое воспаление является жизненно важным ответом на травму и инфекцию, который защищает организм от вторжения патогенов и восстанавливает ткани, поврежденные в результате травмы. Острое воспаление является самоограничивающимся с фазой разрешения, которая прекращает воспалительную реакцию и инициирует репаративный процесс.
Хроническое воспаление возникает, если инициирующий раздражитель не устраняется или нарушается программа разрешения, что приводит к состоянию слабовыраженного воспаления. Хроническое воспаление типично для ряда заболеваний , включая атеросклероз, сахарный диабет, неалкогольную жировую болезнь печени и аутоиммунные заболевания. Системное хроническое воспаление увеличивается с возрастом , носит нерезко выраженный, но стойкий характер, а причины включают хронические инфекции, образ жизни и факторы окружающей среды, отсутствие физической активности, дисбактериоз микробиома, диету, психологический стресс и токсины.
Функция нейтрофилов при воспалении
Нейтрофилы, которые являются наиболее распространенными лейкоцитами у человека, хорошо зарекомендовали себя как первые клетки , реагирующие на острое воспаление. В нормальных условиях нейтрофилы способствуют рассасыванию и репарации тканей, фагоцитируя некротические клетки, чтобы они не привлекали больше иммунных клеток, высвобождая медиаторы для стимулирования роста и ангиогенеза, а также вырабатывая резолвины и протектины. В последние десятилетия также было показано, что нейтрофилы играют значительную роль в хроническом воспалении. Нейтрофилы постоянно рекрутируются в очаг хронического воспаления и способствуют развитию процесса за счет высвобождения сериновых протеаз и образования нейтрофильных внеклеточных ловушек (NET), а также активации других иммунных клеток
Взаимодействие нейтрофилов и тромбоцитов в процессе воспаления
Хроническое воспаление характеризуется протромботическим состоянием, обусловленным взаимной активацией нейтрофилов и тромбоцитов . Комплексы нейтрофилов и тромбоцитов обнаруживаются у людей с хроническими воспалительными заболеваниями, такими как воспалительное заболевание кишечника (IBD) , псориаз, язвенный колит (UC) и атеросклероз. Взаимодействие с тромбоцитами запускает несколько ключевых нейтрофильных процессов, включая адгезию к эндотелию и образование NET. Кроме того, количество тромбоцитов увеличивается у пациентов с сахарным диабетом 2 типа (DM2) за счет секреции нейтрофилов S100A8/A9. Связывание S100A8/A9 с рецептором конечных продуктов гликирования (RAGE), экспрессируемым на резидентных в печени клетках Купфера, увеличивает выработку тромбопоэтина, что, в свою очередь, запускает пролиферацию мегакариоцитов и выработку тромбоцитов.
После активации эндотелия стимулами, такими как травмы или распознавание патогенов, тромбоцитарно-нейтрофильные комплексы образуются путем связывания P-селектина тромбоцитов с лигандом P-селектина гранулоцитов (PSGL)-1 на нейтрофилах. Это взаимодействие способствует дальнейшему взаимодействию между молекулой межклеточной адгезии (ICAM)-2 и лигандом CD40 (CD40L) на тромбоцитах и интегрином α L β 2 и CD40 на нейтрофилах, что обеспечивает прочное образование тромбоцитарно-нейтрофильных комплексов. У пациентов с атеросклерозом комплексы нейтрофилов и тромбоцитов стимулируют секрецию S100A8 из нейтрофилов, который связывается с Toll-подобным рецептором (TLR)4 и способствует воспалительной реакции, что приводит к повышению уровня фактора некроза опухоли (TNF)α и интерлейкина (IL). 1β и миграции и адгезии нейтрофилов.
В дополнение к усилению адгезии нейтрофилов к эндотелию перекрестные помехи между тромбоцитами и нейтрофилами приводят к образованию NET. Хемокиновый лиганд с мотивом CXC (CXCL)4, высвобождаемый тромбоцитами пациентов с васкулитом, ассоциированным с антинейтрофильными цитоплазматическими антителами (ANCA), способствует образованию NET. Тромбоциты могут связывать бактерии на поверхности, образуя пучок тромбоцитов-бактерий. Было показано, что эта структура служит платформой для адгезии нейтрофилов и высвобождения NET в мышиной модели сепсиса. Кателицидин (LL-37/CRAMP), который высвобождается из нейтрофилов, способствует агрегации тромбоцитов и лейкоцитов и рекрутированию нейтрофилов путем индукции активации тромбоцитов в тромбах у мышей. Ингибирование агрегации тромбоцитов антитромбоцитарной терапией снижает высвобождение нейтрофил-активирующих веществ из α-гранул при атеротромбозе. Внеклеточные везикулы тромбоцитов (PEV) содержат CXCL5, который может переноситься в эндотелий и тем самым способствовать адгезии нейтрофилов, а поверхность PEV состоит из различных адгезивных гликопротеинов, таких как β1-интегрин и P-селектин. PEV, выделенные от пациентов с системным склерозом, высвобождают более высокие уровни высокоподвижного группового бокса (HMGB) и способствуют активации нейтрофилов и образованию NET in vitro. Роль NET в прокоагулянтном фенотипе была установлена при IBD, и NET человека, происходящие из IBD, повышают риск тромбоза за счет усиления высвобождения микрочастиц тромбоцитов через TLR2 и TLR4 in vitro.
Взаимодействия тромбоцитов с эндотелиальными клетками (EC) имеют решающее значение для рекрутирования миелоидных клеток. Более того, взаимодействие между тромбоцитами и нейтрофилами способствует активации и трансмиграции нейтрофилов к местам повреждения, а также образованию NET. И наоборот, тромбоцитарно-нейтрофильные комплексы усиливают активацию тромбоцитов и образование тромбов.
Взаимодействия нейтрофилов с иммунными клетками
Нейтрофилы взаимодействуют с В-клетками с помощью независимых от контакта сигналов, таких как секреция фактора активации В-клеток (BAFF). BAFF участвует в выживании, созревании и дифференцировке В-клеток, экспрессируется на поверхности нейтрофилов и во внутриклеточных хранилищах и активируется при хронических заболеваниях. Сигаретный дым (CS) является основной причиной хронической обструктивной болезни легких (COPD) , а инфильтрация нейтрофилами в легких мышей дикого типа (WT), подвергшихся воздействию CS, положительно коррелирует с экспрессией BAFF. In vitro секреция BAFF повышалась в нейтрофилах, обработанных экстрактом сигаретного дыма. Соответственно, истощение нейтрофилов снижает экспрессию BAFF в легких, а у мышей с дефицитом BAFF снижается инфильтрация нейтрофилов в легких.
Адгезия и миграция нейтрофилов при воспалении в легких.
1. Ляпина С.А., Федотова Г.Г. Структурно-функциональная организация мембран нейтрофилов при бронхолегочных заболеваниях и коррекция их антиоксидантными препаратами // Современные проблемы науки и образования. 2017. № 6.
2. Ляпина С.А. Активность Na-K и Ca-АТФ-аз нейтрофильных гранулоцитов крови при воздействии in vitro низкоинтенсивным гелий-неоновым лазером. автореф. дис. … канд. биол. наук. Саранск, 1998. 21 с.
3. Негруца К.В. Нарушение функций нейтрофилов как один из механизмов формирования воспаления у больных бронхиальной астмой, хронической обструктивной болезнью легких и внебольничной пневмонией. автореф. дис. … канд. мед. наук. Санкт-Петербург, 2017. 21 с.
4. Jenne C.N., Wong C.H., Zemp F.J., McDonald B., Rahman M.M., Forsyth P.A., McFadden G., Kubes P. Neutrophils recruited to sites of infection protect from virus challenge by releasing neutrophil extracellular traps. Cell host microbe. 2013. vol. 13. no. 2. P. 169-180.
5. Чеснокова Н.П., Понукалина Е.В., Невважай Т.А., Полутова Н.В., Бизенкова М.Н. Морфофункциональные и метаболические особенности гранулоцитов периферической крови // Международный журнал прикладных и фундаментальных исследований. 2015. № 4-2. С. 285-289.
6. Галкин А.А., Демидова В.С. Центральная роль нейтрофилов в патогенезе синдрома острого повреждения легких (острый респираторный дистресс-синдром) // Успехи современной биологии. 2014. Том 134. № 4. С.377-394.
Общепризнанно, что нейтрофил как полноценная функциональная единица принадлежит к наиболее реактивным клеткам. В этом смысле реактивность нейтрофила отражает многообразие функциональных контактов этих клеток с медиаторными системами плазмы и другими клеточными элементами крови и соединительной ткани. Рассматривая нейтрофил как клетку, участвующую в регуляции гомеостаза, внимание обращено на важнейшие проявления реактивности этих клеток: мобилизационные и эффекторные реакции. Роль нейтрофилов традиционно рассматривается главным образом в связи с их участием в противоинфекционном иммунитете. Характерными признаками реактивности активированных нейтрофилов считаются: перестройка процессов метаболизма, миграция, адгезия, «кислородный взрыв», поглощение объекта фагоцитоза, образование пищеварительной вакуоли и регуляторная (секреторная) функция нейтрофилов [1].
Клетки-фагоциты нейтрофилы отличаются характерной структурой и сложным внутриклеточным метаболизмом. Клеточный метаболизм чрезвычайно чувствителен к изменению содержания Nа-К и Са-АТФ-азы в цитозоле клетки. Эти же ионы определяют электрическую активность возбудимых клеток и необходимы для инициации фагоцитоза [2].
В механизме развития бронхолегочной патологии значение имеет степень изменения процесса фагоцитоза [3; 4].
Свои главные эффекторные функции нейтрофилы реализуют через воспалительный процесс: а именно, разрушают и удаляют вызвавшие воспаление агенты и регулируют поведение клеток, участвующих в воспалении [5; 6].
Целью исследования явилось изучение реактивности нейтрофилов при бронхолегочных заболеваниях.
Материалы и методы исследования
Принцип оценки фагоцитарной активности основан на определении поглотительной и переваривающей способности клеток. Определение фагоцитарной активности нейтрофилов осуществляли в иммерсионной системе под микроскопом специальным методом, основанным на определении резервных возможностей нейтрофилов к выполнению их основной функции - поглощению и переработке чужеродных агентов. Определяли показатели фагоцитоза: фагоцитарный индекс (ФИ), фагоцитарное число (ФЧ), индекс бактерицидности нейтрофилов (ИБН).
Кислородзависимые механизмы бактерицидности оценивали по тесту восстановления нитросинего тетразолия (НСТ-тест) - образование в цитоплазме клеток крови гранул формазана.
Цитохимическими методами исследовали активности следующих ферментов: щелочной фосфатазы (ЩФ), кислой фосфатазы (КФ), миелопероксидазы (МПО), Na-K-АТФ-азы, Са-АТФ-азы. Количественный анализ ферментативной активности проводили на микрофотометре. Показатели выражены в относительных единицах плотности.
Электронно-микроскопическое исследование нейтрофилов и процесс фагоцитоза осуществляли в лаборатории электронной микроскопии Медицинского института МГУ имени Н.П. Огарева (Саранск). Приготовление электронограмм проводилось по традиционной методике.
Пациенты с бронхолегочными заболеваниями были представлены тремя группами по 10 человек в каждой:
- I группа - пациенты с бронхитом (острая форма);
- II группа - пациенты с пневмонией (период обострения);
- III группа - пациенты с бронхиальной астмой (хроническая форма).
Результаты исследования и их обсуждение
В развитии легочного воспаления в зависимости от фазы заболевания (обострение или ремиссия) особая роль принадлежит системе фагоцитирующих клеток. При обследовании пациентов с бронхолегочными заболеваниями различного происхождения, показатели фагоцитарной реакции отражают изменения реактивности организма, которая зависит от степени тяжести заболевания.
Нами показано, что в стадии обострения заболевания поглотительная и внутриклеточная переваривающая способность нейтрофилов по показателям ФИ и ФЧ снижена по сравнению с нормой.
Показатели фагоцитоза (ФИ, ФЧ, ИБН), активность внутриклеточно расположенных ферментов (МПО, ЩФ, КФ, Na-K-АТФ-аза, Са-АТФ-аза), кислородзависимые механизмы бактерицидности (НСТ-тест) изучали в зависимости от фазы заболевания (обострение или ремиссия), в результате чего нами были выявлены некоторые особенности.
У пациентов I группы в фазу обострения заметно снижение показателей фагоцитоза по сравнению с группой здоровых доноров: ФИ - на 18,5% и ФЧ - на 42,0%. По нашему мнению, это связано с угнетением поглотительной активности нейтрофилов. Подавление фагоцитарной активности нейтрофилов мы рассматриваем как следствие подавляющего (супрессивного) действия вирусов на фагоцитирующие клетки. В фазе обострения воспалительного процесса происходит увеличение НСТ-позитивных нейтрофилов на 92,7%. ИБН повышается в 2,0 раза.
В крови пациентов II группы наблюдается снижение ФИ и ФЧ на 15,1% и 36,5% соответственно. В фазе обострения отмечается повышение НСТ-теста в 2,5 раза. ИБН увеличивается в 2,3 раза.
В крови пациентов III группы отмечается снижение ФИ на 16,2%, ФЧ - на 40,2%. НСТ-тест увеличивается на 99,3%, ИБН - в 2,2 раза. При бронхиальной астме больного нейтрофилы могут контактировать с комплексом аллерген-антитело путем поглощения и переваривания. При этом функциональная активность нейтрофилов выражена сильнее, чем аллергический процесс. В фазу ремиссии показатели ФИ и ФЧ у пациентов I, II, III группы увеличиваются.
Показатели НСТ-теста и ИБН снижаются у пациентов всех трех групп по сравнению с фазой обострения, что, по всей видимости, связано с процессами перенапряжения функциональной деятельности нейтрофилов и может расцениваться как недостаточность кислородзависимых механизмов бактерицидности нейтрофилов.
Течение бронхолегочных заболеваний сопровождается развитием синдрома эндогенной интоксикации, степень выраженности которой пропорциональна тяжести клинического течения болезни.
Заслуживает особого внимания тот факт, что нейтрофилы являются мощным эффектором и начинающимся механизмом реакций, обеспечивающих развитие воспаления. Реактивность нейтрофила обеспечивается обособленными механизмами, проявляющимися независимо друг от друга.
Полученные в модельных исследованиях результаты определенно указывают на динамику ферментативной активности и фагоцитарной способности нейтрофилов у больных бронхолегочными заболеваниями, при обострении которых содержание ЩФ в клетках-фагоцитах повышалось. Уровень ЩФ нейтрофилов в фазу ремиссии не изменялся. Мы обратили внимание, что наблюдается прямая связь между тяжестью воспалительного процесса и активностью щелочной фосфатазы. В период обострения активность КФ в крови пациентов I группы увеличивалась на 30,0%, II группы - на 38,1% и III группы - на 33,5%.
Нейтрофилы секретируют низкомолекулярные продукты, обладающие супрессорным действием на фоне альтерирующих факторов. После стимуляции нейтрофилов в течение первых нескольких секунд происходит респираторный взрыв, связанный с активностью МПО. Респираторный взрыв, вызванный накоплением в нейтрофилах МПО, составляет у пациентов I группы - 17,0%, II группы - 29,0%, III группы - 24,7%. В фазе обострения активность МПО в нейтрофилах достоверно снижалась по сравнению с фазой ремиссии, что может свидетельствовать о нарушении образования активных кислородных метаболитов.
Общебиологические свойства ионтранспортирующих систем, связанных с функционированием мембранного аппарата клеток, отражают степень активности АТФ-аз, которая выявляется в виде черных цитоплазматических отложений. Нами показано, что при действии повреждающего агента активность Na-K-АТФ-азы и Са-АТФ-азы изменяется. В стадии хемотаксиса и адгезии, когда нейтрофилы движутся в поврежденную ткань и прилипают к поверхности, их активность возрастает; в стадии киллинга и деградации микроорганизмов (кислородзависимый респираторный взрыв) - снижается, наблюдается снижение количества жизнеспособных клеток в конце фагоцитоза.
Противомикробной резистентности, эффекторами которой являются нейтрофилы, как и естественные киллеры и неспецифические гуморальные факторы, отводится существенная роль в защите организма.
Нейтрофилы содержат в своих гранулах и синтезируют в процессе активации высокотоксичные продукты, повреждающие клетки. Это свойство во многом определяет их участие в антимикробной защите, остром бронхолегочном воспалении.
Морфологическая ультраструктура нейтрофилов при бронхолегочной патологии имеет свои особенности. Высвобождение преформированных биологически активных веществ составляет важный этап реализации эффекторного потенциала нейтрофила.
Заключение
Изложенный материал указывает на многогранность реактивных свойств нейтрофилов. Нами выбраны наиболее убедительные и информативные факторы, которые изучались нами в течение долгих лет на большом клиническом материале, с позиции воспалительного процесса. Методы изучения реактивности нейтрофилов, в частности их секреторной функции, позволяющие оценивать биологическую активность продуктов, выделяемых этими клетками в процессе активации, могут быть использованы для тестирования их дефектов у больных. Клиническое и экспериментальное использование таких методов может дать дополнительную информацию не только для диагностики иммунодефицитных состояний и прогноза течения патологических процессов, но и для понимания роли нейтрофилов в регуляции различных звеньев гомеостаза.
Снижение фагоцитарной активности нейтрофилов по показателям ФИ и ФЧ в фазу обострения при всех формах бронхолегочных заболеваний следует рассматривать как следствие супрессорного воздействия бактерий на фагоцитирующие клетки. Уровень щелочной и кислой фосфатаз в цитоплазме нейтрофильных лейкоцитов периферической крови служит показателем, характеризующим защитную функцию этих клеток, и является морфологическим тестом сенсибилизации организма.
Нейтрофил включается в сложную систему регуляции процессов метаболизма и различных функций организма. Можно полагать об изменении в кислородзависимых механизмах бактерицидности нейтрофилов.
Максимальные показатели НСТ-теста и ИБН в стадии обострения заболевания отражают завершенность фагоцитоза. В фазу ремиссии показатели НСТ-теста и ИБН снижаются. НСТ-тест является признанным показателем бактерицидной функции фагоцитов, и его логично рассматривать как функциональный критерий готовности нейтрофилов к завершенному фагоцитозу. Данное обстоятельство, по всей видимости, является важным фактором усиления фагоцитарной функции нейтрофилов.
Возникновение, период разгара и период завершения болезни зависят от реактивности организма, которая, в свою очередь, определяется функциональным состоянием иммунной системы. В общебиологическом отношении активность изучаемых показателей при последовательности реакций патологического процесса указывает на повышение реактивности нейтрофилов, что рассматривается как проявление защитной и приспособительной реакции от нарушения нормального течения жизненных процессов - способа сохранения организма.
Дефекты адгезии лейкоцитов
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Адгезия между лейкоцитами и эндотелием, другими лейкоцитами и бактериями необходима для выполнения основных фагоцитарных функций - перемещения в очаг инфекции, коммуникации между клетками, формирования реакции воспаления. К основным молекулам адгезии относятся селектины и интегрины. Дефекты самих молекул адгезии или белков, участвующих в передаче сигнала от молекул адгезии ведут к выраженным дефектам протиинфекционного ответа фагоцитов. За последние годы было описано несколько подобных дефектов, однако первым среди описанных в этой группе и наиболее типичным по своим клиническим проявлениям является дефект адгезии лейкоцитов I.
Патогенез дефектов адгезии лейкоцитов
LAD I является аутосомно-рецессивным заболеванием, вызванным мутацией гена общей цепи семейства beta-2-интегринов - CD18. Ген носит название ITGB2 и расположен на длинном плече 21 хромосомы, Интегрины являются трансмембранными белками, присутствующими на поверхности всех лейкоцитов. Они необходимы для плотной адгезии лейкоцитов
Симптомы дефектов адгезии лейкоцитов
К настоящему времени описано более 600 случаев заболевания. Инфекции в основном поражают кожу и слизистые. У больных отмечаются параректальные абсцессы, пиодермии, отиты, язвенные стоматиты, гингивиты, парадонтиты, ведущие к выпадению зубов. Также больные страдают инфекциями дыхательных путей, асептическим менингитом, сепсисом. Первым проявлением заболевания часто является позднее отпадение пуповинного остатка (более 21 дня) и омфалит. Поверхностные инфекции часто ведут к некрозу, при этом характерным признаком заболевания является отсутствие формирования гноя при выраженном нейтрофилезе в периферической крови. Нередко формируются хронические, длительно не заживающие язвенные очаги. Основными возбудителями являются S. aureus и грамотрицательные бактерии. У некоторых больных отмечаются тяжелые грибковые поражения. Частота вирусных инфекций не увеличена.
Выраженность клинических проявлений значительно меньше у больных с некоторыми миссенc-мутациями, при которых отмечается небольшая экспрессия CD18 (2,5-10%). Эти больные, как правило, бывают диагностированы позже и могут не страдать жизнеугрожающими инфекциями. Тем не менее, даже в легких случаях отмечается лейкоцитоз, плохое заживление ран и тяжелый парадонтоз.
У носителей мутации отмечается 50% экспрессия CD18, которая не проявляется клинически.
Диагностика дефектов адгезии лейкоцитов
Патогномоничным признаком заболевания является лейкоцитоз (15 - 160 х 10 9 /л) при 50-90% нейтрофилов. При проведении функциональных тестов выявляются нарушения миграции нейтрофилов (кожное окно>, адгезии гранулоцитов к пластику, стеклу, нейлону и др., а также значите тельное снижение комплемент-зависимого фагоцитоза. Другие тесты функций нейтрофилов, как правило, в норме.
Флоуцитометрическое исследование нейтрофилов позволяет выявить отсутствие или значительное снижение экспрессии CD18 и ассоциированных с ним молекул CD11a, CD11b и CD11c на нейтрофилах и других лейкоцитах. Однако описано несколько случаев нормальной экспрессии CD18 при его полной дисфункции.
Лечение дефектов адгезии лейкоцитов
ТГСК является терапией выбора. Более того, пациенты с LAD синдромом, по крайней мере, I типа, в известной мере, являются идеальными кандидатами на трансплантацию, поскольку молекулы адгезии играют ключевую роль в отторжении трансплантата. Соответственно, дефект этих молекул затрудняет отторжение трансплантата и обеспечивает его приживление. Понимание сути LAD I привело в начале 90-х годов к развитию фармакологической профилактики отторжения с помощью моноклональных антител (МАТ) к LFA1 - метода, показавшего свою эффективность у пациентов с различными показаниями к ТГСК. Таким образом, введение анти-LFAl МАТ приводит к искусственному дефекту адгезии, то есть, по сути дела, «эмулирует» у пациента LAD синдром, снижая вероятность отторжения. Особенно успешно этот метод применяется в группе пациентов с a priori высоким потенциалом отторжения, например, при гемофагоцитарных лимфогистиоциозах. Помимо ТГСК, одним из подходов к лечению пациентов с LAD является борьба с инфекциями, которые требуют ранней и массивной антибактериальной терапии. Назначение упреждающей антибактериальной терапии не приводит к значительному снижению частоты инфекций.
Проведение генной терапии у двух больных не увенчалось успехом.
В отсутствие ТГСК, 75% детей с тяжелой формой LAD I не доживают до пятилетнего возраста.
Читайте также:
