Агонисты гонадтропин рилизинг гормона (ГнРГ) для лечения болей при эндометриозе. Эффективность
Добавил пользователь Владимир З. Обновлено: 21.01.2026
Эндометриоз— это эстрогензависимое доброкачественное заболевание, при котором эндометриальная строма ижелезы, часто сфиброзным компонентом, расположены запределами матки. Существуют 3 основные формы эндометриоза: поверхностный перитонеальный эндометриоз, глубокий инфильтративный эндометриоз, при котором глубина инвазии превышает 5мм, иэндометриоидные кисты (эндометриомы). Эндометриоз— заболевание, которое негативно влияет накачество жизни женщин репродуктивного возраста засчет болевого синдрома ибесплодия, встречающегося в50% случаев [1]. Частота встречаемости точно неустановлена, восновном отсутствия специфических симптомов, атакже вследствие того, что только лапароскопия сгистологической верификацией является самым надежным диагностическим тестом. Популяционные исследования приводят цифру около 1,5% встречаемости и6-15% пациентов вгинекологических стационарах [2].
Несмотря на то, что эндометриоз был описан еще в XIX в., полностью причины его появления и распространения не изучены. Также многие вопросы относительно методов лечения остаются далекими от решения. В связи с хроническим и часто рецидивирующим характером течения заболевания Комитет врачебной практики Американского общества репродуктивной медицины (ASRM) заключил следующее: «эндометриоз должен рассматриваться как хроническое заболевание, требующее пожизненного плана ведения, приоритетом которого является медикаментозное лечение и профилактика повторных хирургических процедур» [3].
План лечения должен быть индивидуальным в зависимости от симптомов эндометриоза, распространенности патологического процесса, желания иметь детей, возраста, опыта хирурга, побочных эффектов препаратов и хирургического лечения Возможные методы лечения следующие:
- симптоматическое лечение нестероидными противовоспалительными препаратами (НПВП);
- гормональное лечение (комбинированные оральные контрацептивы (КОК) в циклическом или пролонгированном режиме, агонисты (ГнРГ), даназол, ингибиторы ароматазы);
- хирургическое лечение, которое разделяют на консервативное (органосохраняющее), с сохранением матки и ткани яичников, и радикальное: с удалением матки и, возможно, яичников;
- комплексное лечение: сочетание медикаментозного лечения до и/или после хирургии.
Лапароскопия, бесспорно, является «золотым стандартом» в диагностике и лечении эндометриоза, позволяет коагулировать или иссекать гетеротопии и спайки, и таким образом если не предотвратить, то, как минимум, значительно отсрочить рецидив болезни. Также полное удаление очагов позволяет снизить расходы и побочные реакции медикаментозной терапии. В то же время нередки интраоперационные осложнения, связанные с повреждением нижних отделов кишечника и мочеполового тракта, инфекционные осложнения и формирование послеоперационных спаек, иногда более выраженных, чем до операции. Преимущества и недостатки медикаментозной терапии приведены в таблице 1.
НПВП часто применяются женщинами для купирования болевого синдрома, однако клинические исследования крайне скудны. Главным сдерживающим фактором длительного использования НПВП являются побочные эффекты, такие как язва желудка и ановуляторный эффект при применении в середине менструального цикла [4, 5].
Наиболее часто в клинической практике для лечения эндометриоза используются агонисты ГнРГ, даназол и некоторые прогестины. Эти препараты и КОК имеют общее воздействие на эндометриоз. По сравнению с эутопическим эндометрием эндометрий в имплантатах синтезирует больше простагландинов, эстрогенов и провоспалительных цитокинов, это приводит к пролиферации и инфильтративному росту, обусловливая боль. Более того, повышенная активность ароматазы потенцирует синтез циклооксигеназы типа и выработки простагландина Е2, который усиливает синтез эстрогенов. Таким образом, любой препарат, снижающий синтез эстрогенов в яичниках, негативно влияет на этот патогенетический механизм и снижает боль.
Возможно применение непероральных эстрогенпрогестероновых контрацептивов, однако этот вопрос изучен недостаточно.
Даназол — это андрогенный стероидный препарат, достаточно эффективный при лечении эндометриоза. По данным исследований, более 80% пациенток отмечают исчезновение или значительное ослабление боли 8, но его применение ограничено частыми побочными эффектами: влиянием на липидный профиль, прибавкой массы тела, отечностью, усилением секреции сальных желез и акне, сухостью во влагалище, приливами, гирсутизмом, гепатотоксичностью и атрофией молочных желез.
Пероральные, парентеральные, внутриматочные контрацептивы или прогестины в виде имплантатов используются в течение десятилетий с различной доказательной базой. Однако для достижения терапевтического эффекта зачастую необходимо переходить на более высокие дозировки по сравнению с другими показаниями для их применения, что, конечно, увеличивает частоту побочных реакций (прибавка массы тела, андрогенные эффекты и осложнения) [7,10].
Отдельного внимания заслуживает препарат диеногест (Визанна, Bayer, Германия), который рекомендован в качестве монотерапии эндометриоза в Европе, Японии и др. Он представляет собой синтетический пероральный прогестин с выраженным прогестагенным и умеренным антигонадотропным эффектами, но без андрогенной, глюкокортикоидной и минералокортикоидной активности. Механизм действия на эндометриоидные гетеротопии многофакторный. Диеногест снижает секрецию гонадотропинов, что приводит к значительному снижению синтеза эстрадиола. При продолжительном применении вызывает гипоэстрогению, повышение уровня прогестерона, что приводит к децидуализации, а затем атрофии эндометриальной ткани [11]. В эксперименте на животных также показано, что диеногест вызывает апоптоз гранулезных клеток яичников [12]. В исследованиях на животных показано следующее влияние диеногеста: подавление пролиферации, ангиогенеза и противовоспалительный эффект диеногеста [13, 14].
Рандомизированное клиническое исследование показало, что перорально принимаемый диеногест более эффективен по сравнению с плацебо, уменьшая боль при подтвержденном эндометриозе [15]. В исследованиях, сравнивающих прием диеногеста длительностью 16 и 24 нед. вместе с агонистами ГнРГ у пациентов с эндометриозом, и прием агонистов ГнРГ, получены сопоставимые результаты по уменьшению боли по баллам и по классификации эндометриоза rAFS при повторной лапароскопии [16]. Другое рандомизированное исследование, сравнивающее агонисты ГнРГ и диеногест, предлагают последний как сопоставимый по эффективности, но более безопасный и лучше переносимый, что связано с меньшей гипоэстрогенией, меньшими изменениями минеральной плотности костной ткани и маркеров костной резорбции [17].
Общеизвестно, что самые эффективные методы снижения продукции эстрогенов — это двухсторонняя овариоэктомия и применение агонистов ГнРГ. По понятным причинам удаление яичников в репродуктивном возрасте выполняется крайне редко. Однако частое и длительное применение агонистов ГнРГ ограничено в связи с высокой ценой и побочными эффектами, обусловленными гипоэстрогенией (аменорея, вазомоторные симптомы (80%), нарушение сна, приливы, урогенитальная атрофия (30%), головные боли (30%) и снижение минеральной плотности костной ткани (МПКТ); доказано, что применение ГнРГ увеличивает риск переломов спустя годы после приема препаратов. В рандомизированном исследовании показано, что при лечении агонистами ГнРГ в длительном режиме в сочетании с другими препаратами () качество жизни и эффективность сопоставимы с таковыми при применении КОК в непрерывном режиме [18].
Для выяснения оптимального длительного режима проведено одно большое рандомизированное исследование. Пациентки с болью распределены на 4 группы:
- Агонисты ГнРГ в дозе 3,75 мг каждые 4 нед.
- Агонисты ГнРГ и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
- Агонисты ГнРГ и малые дозы конъюгированного эстрогена 0,625 мг и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
- Агонисты ГнРГ и конъюгированный эстроген в высокой дозе (1,25 мг 1 р./сут) и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
Всем пациенткам назначался кальций 1000 мг/сут на весь срок лечения [19]. В результате данного исследования выяснилось, что женщины без или с прогестином с добавлением 0,625 мг эстрогена или без него имели одинаковые показатели снижения тазовой боли. Добавление низких доз эстрогенов было более эффективно, чем высоких (1,25 мг). В группе с высокой дозой эстрогенов пациентки чаще прекращали лечение боли, вероятно, в связи с тем, что это достаточная доза для поддержания роста и функционирования гетеротопий, что подтверждается и другими исследованиями [20]. МПКТ значимо снижается только в группе без , в остальных группах различий в минеральной плотности костной ткани до и после лечения выявлено не было. Вазомоторные симптомы были значительно снижены во всех группах с . При отслеживании этих пациентов через 12 и 24 мес. после окончания лечения во всех группах симптомы были менее выраженные, чем через 8 мес. после начала активной терапии [21]. В случае, когда невозможно проводить стероидными препаратами, разработаны схемы снижения доз агонистов ГнРГ или увеличения интервала приема.
Конечно, оптимальный режим еще предстоит выяснить, более того, нет сравнительных исследований препарата диеногест с агонистами ГнРГ в сочетании с поддерживающей терапией. Однако, возможно, в будущем в схемах лечения эндометриоза будет сочетание диеногеста и агонистов ГнРГ или их последовательное применение. В пользу этого говорит одно нерандомизированное исследование из Японии, сравнивающее применение диеногеста в дозе 2 мг/сут 12 мес. с последовательным лечением агонистами ГнРГ 4-6 мес., после чего назначался диеногест 1 мг/сут [22]. Были получены обнадеживающие результаты; авторы заключают, что длительное применение диеногеста у женщин после лечения агонистами ГнРГ является обоснованным.
Необходимо признать, что в выборе терапии немаловажным фактором является стоимость, все расходы фактически ложатся на плечи женщины. Любая длительная схема, включающая в себя агонисты ГнРГ, очень затратна и должна быть обоснована с позиции эффективности и безопасности. В этом плане выгодно отличается диеногест, побочные эффекты которого предсказуемы. Однако выраженный клинический эффект не позволяет пациенткам отказываться от лечения в подавляющем большинстве случаев. Тем не менее необходимы более масштабные исследования, направленные на оценку экономической целесообразности применения диеногеста.
Применение ингибиторов ароматазы — это новый многообещающий метод лечения эндометриоза. Эти препараты снижают локальный синтез эстрогенов в эндометриоидных гетеротопиях, к тому же ингибируют образование эстрогенов в яичниках, головном мозге и жировой ткани [23]. В эндометриоидных очагах простагландин E2 стимулирует гиперпродукцию ароматазы, что приводит к локальному синтезу эстрогенов из андрогенов. Эстрогены в свою очередь увеличивают синтез простагландина E2, обеспечивая положительную обратную связь. В нескольких описательных работах и одном рандомизированном исследовании ингибиторы ароматазы использовались для лечения тяжелых форм эндометриоза 31. При систематическом обзоре этих исследований выяснилось, что ингибиторы ароматазы статистически значимо более выраженно снижают боль в сравнении с агонистами ГнРГ [32]. Важно знать, что ингибиторы ароматазы вызывают значительную потерю костной плотности при длительном применении и не могут назначаться в виде монотерапии у пременопаузальных женщин, вызывают мультифолликулярные изменения в яичниках за счет стимуляции ФСГ. В этом случае целесообразно сочетание с агонистами ГнРГ или контрацептивами [28].
Еще одним перспективным направлением в лечении эндометриоза является попытка минимизировать воспалительный компонент в гетеротопиях. Важная роль в генезе симптомов эндометриоза отводится провоспалительным цитокинам и активации оксидативного стресса, при этом происходит активация внутриядерного воспалительного медиатора (ядерный фактор легких цепей активированных ), который может поддерживать воспалительный ответ и стимулировать ангиогенез. Однако систематические обзоры не доказали целесообразность применения антагонистов TNF-α [33] или пентоксифиллина [34] для лечения симптомного эндометриоза.
В качестве заключения хочется отметить общую мысль, проходящую через многие обзорные статьи. В частности, в статье P. Vercellini из Миланского университета с символическим названием «В ожидании Годо» [35] авторы достаточно скептически и пессимистично относятся к современным фармакологическим методам лечения эндометриоза. Делается вывод о том, что многие женщины за свою жизнь, несмотря на применение современных и дорогостоящих препаратов, не избегут повторных операций, таким образом, «должны ли мы все еще ждать Годо»?
Агонисты гонадтропин рилизинг гормона (ГнРГ) для лечения болей при эндометриозе. Эффективность
Эндометриоз — патологический процесс, который формируется на фоне нарушений в гормональном и иммунном гомеостазе и характеризуется доброкачественным разрастанием ткани, сходной по структуре и функции с эндометрием, за пределами нормальной слизистой оболочки матки. В структуре гинекологических заболеваний генитальный эндометриоз занимает третье место, а его частота имеет тенденцию к увеличению [1]. Эндометриоз наблюдается у 7—10% женщин репродуктивного возраста, имеет склонность к омоложению и доминирует в качестве причины хронических тазовых болей у женщин (80%) [2, 3].
Различные клинические проявления, сложности в диагностике, значительные изменения в репродуктивной системе, снижение качества жизни характеризуют его как большую медико-социальную проблему, имеющую колоссальное демографическое значение.
Эндометриоз имеет хроническое, прогрессирующее и рецидивирующее течение и является одной из самых частых причин болевого синдрома и бесплодия.
Несмотря на достигнутые успехи в диагностике и лечении эндометриоза, данное заболевание до сих пор остается предметом глубочайшего интереса ученых и клиницистов. Совершенствуется техника оперативного лечения эндометриоза, внедряются в практику новые методы медикаментозной терапии, однако число тяжелых форм заболевания, в том числе экстрагенитальной локализации, рецидивов заболевания не снижается.
Общепризнано, что эндометриоз — гормонально-зависимое заболевание, характеризующееся наличием эктопических участков эндометрия за пределами матки, однако патофизиология данного заболевания остается невыясненной.
Много дискуссий существует и вокруг подходов к лечению больных с различными формами эндометриоза. Хирургические методики продолжают непрерывно совершенствоваться, однако важнейшее место стремительно занимают медикаментозные способы терапии, препараты для которой должны быть не только максимально эффективными, но и максимально безопасными.
Основными клиническими проявлениями эндометриоза являются следующие: боль, бесплодие, нарушение менструального цикла, кровотечения. Специфичным и наиболее распространенным симптомом эндометриоза является болевой синдром [4, 5]. Боль может носить различный характер: циклический (дисменорея) и постоянный; может проявляться диспареунией, иррадиировать в поясничную область, промежность, задний проход, крестец, копчик. Боль при эндометриозе разнообразна, зависит в большей мере от локализации процесса, чем от степени его распространения.
Оценка интенсивности болевого симптома имеет широкое применение в процессе терапии больных с эндометриозом. При этом используются визуально-аналоговые шкалы боли (ВАШ) и специфические анкеты [6].
Установление правильного диагноза эндометриоза часто проблематично, поскольку симптомы могут быть неспецифическими и связаны с множеством различных условий [7]. Чаще всего его устанавливают или при ультразвуковом исследовании, или при диагностической лапароскопии. В настоящее время неинвазивным тестом для диагностики и оценки эффективности терапии больных с эндометриозом является определение в крови уровней сосудистого эндотелиального фактора роста (СЭФР-А), аннексина V, CA-125, гликоделина А, растворимых молекул межклеточной адгезии 1 (slCAM-1) [8, 9].
При выборе метода лечения пациенток с эндометриозом врач сталкивается с трудностями, которые определяются многими факторами: неизученными до конца этиологией и механизмами формирования боли; отсутствием неинвазивных диагностических маркеров эндометриоза; негативным влиянием на качество жизни; вовлечением в патологический процесс окружающих тканей и органов; высокой частотой рецидивирования эндометриоза.
В связи с развитием хронического болевого синдрома, порой крайне выраженного, в том числе диспареунии, эндометриоз существенно снижает качество жизни больных, что может привести к развитию тяжелой депрессии и астенизации пациенток.
Выбор метода терапии больных с эндометриозом зависит от цели лечения в каждой конкретной клинической ситуации и репродуктивных планов пациентки. Одной из важнейших проблем лечения при эндометриозе является снижение овариального резерва после хирургического удаления эндометриоидных поражений, что в большинстве случаев оказывает негативное влияние на репродуктивную функцию. Поэтому цель системного лечения больных с эндометриозом в течение всей жизни — максимально эффективное использование медикаментозной терапии, чтобы избежать хирургических вмешательств, особенно повторных. Одобренными препаратами для лечения пациенток с эндометриозом остаются агонисты ГнРГ и гестагены (диеногест).
Агонисты ГнРГ имеют высокую эффективность в отношении облегчения боли, поэтому считаются «золотым стандартом» лечения эндометриоза, но их использование может сопровождаться симптомами дефицита эстрогенов: снижением либидо, приливами жара, потливостью, сухостью во влагалище [10].
При этом существует гестаген диеногест, разработанный специально для лечения эндометриоза. Диеногест имеет выраженное антиэстрогенное воздействие на эндометрий, а его способность вызывать секреторную трансформацию эндометрия достоверно выше, чем у множества других прогестагенов. Суточная доза диеногеста 2 мг умеренно снижает уровень эстрадиола и сохраняет его в пределах предложенного «терапевтического окна» (30—40 пг/мл) [11, 12].
В настоящее время не существует универсального и стандартного подхода к лечению эндометриоза, который был бы идеален для всех пациенток. Необходимо проводить лечение эндометриоза с учетом планов и предпочтений каждой пациентки.
В связи с вышеизложенным цель нашего исследования — оценить эффективность и безопасность медикаментозной терапии больных с эндометриозом.
Материал и методы
В поликлиническом отделении ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии» выполнено проспективное клиническое исследование, в которое были включены 60 пациенток в возрасте 31,1±4,78 года. Основную группу составили 40 больных в возрасте 31,2±5,15 года с аденомиозом и наружным генитальным эндометриозом различной степени распространения, в контрольную группу вошли 20 пациенток в возрасте 31,2±4,08 года без признаков эндометриоза.
Отсутствие эндометриоза у пациенток в контрольной группе подтверждено при оперативном лечении — лапароскопии по поводу неэндометриоз-ассоциированной патологии.
Для оценки эффективности и безопасности медикаментозной терапии в зависимости от формы заболевания все пациентки с аденомиозом и наружным генитальным эндометриозом были разделены на 2 группы: 1-ю группу составила 21 пациентка с диффузной формой аденомиоза; во 2-ю группу вошли 19 пациенток с наружно-внутренним генитальным эндометриозом (пациентки с аденомиозом и эндометриоидными кистами). Каждая группа пациенток в зависимости от проводимого лечения с помощью случайного выбора была разделена на 2 подгруппы, одна из которых в качестве лечения получала диеногест в течение 12 мес, а другая получала терапию агонистами ГнРГ в течение 6 мес с последующим назначением диеногеста до 12 мес.
Критерии включения в 1-ю и 2-ю группы пациенток:
1. Женщины в возрасте 18—45 лет с различной степенью распространения аденомиоза и наружного генитального эндометриоза.
2. Размер эндометриоидных кист не более 30 мм.
3. Диффузная форма аденомиоза (размеры: до величины матки, соответствующей таковой при 6—7 нед беременности).
Критерии исключения для всех групп:
1. Размеры эндометриоидных кист более 30 мм.
2. Диффузно-узловая и узловая форма аденомиоза.
3. Женщины, принимавшие гормональные препараты (КОК, а-ГнРГ, прогестины) менее чем за 6 мес до начала исследования.
4. Пациентки, оперированные по поводу эндометриоза в течение 6 мес до момента исследования.
5. Пациентки с тяжелыми соматическими заболеваниями (системная красная волчанка, сахарный диабет 1-го и 2-го типа, аллергический дерматит, гломерулонефрит, хроническая болезнь почек, ишемическая болезнь сердца, онкологические заболевания).
Для выполнения поставленной цели помимо клинико-анамнестических данных в работе при обследовании женщин были использованы следующие лабораторно-инструментальные методы:
1. Визуально-аналоговая шкала (ВАШ) для оценки интенсивности боли.
2. Ультразвуковое исследование (перед назначением гормональных препаратов, а также на фоне лечения, через 6 мес терапии).
3. Иммуноферментный метод: определение неинвазивных биомаркеров эндометриоза (гликоделина А, СЭФР-А, аннексина V, СА-125, молекул межклеточной адгезии 1 (slCAM-1)), антимюллерова гормона (АМГ) и эстрадиола в сыворотке крови проводилось до лечения и через 6 мес от начала приема диеногеста и агонистов ГнРГ.
4. При статистической обработке использовался критерий Стьюдента в различных вариантах.
Результаты и обсуждение
В результате исследования выявлены различия индекса массы тела у пациенток контрольной и основной групп.
Анализ жалоб пациенток с различными формами эндометриоза (табл. 1) показал следующее: дисменорея была чаще выражена у пациенток с аденомиозом — у 19 женщин, что составило 90,48%, однако достоверных различий у пациенток 1-й и 2-й групп выявлено не было, диспареуния чаще проявлялась у пациенток 2-й группы — у 7 (36,84%) пациенток.
Таблица 1. Оценка жалоб больных с различными формами эндометриоза
кафедра акушерства и гинекологии №2 Кемеровской государственной медицинской академии
ГАУЗ Кемеровский областной перинатальный центр им Л.А. Решетовой, Кемерово, Россия
Кемеровский государственный медицинский университет, Кемерово, Россия, 650056
Кемеровский областной клинический перинатальный центр им. Л.А. Решетовой, Кемерово, Россия, 650066
Комбинированное лечение пациенток с эндометриозом и бесплодием с применением агонистов гонадотропин-рилизинг-гормона и диеногеста
Журнал: Проблемы репродукции. 2016;22(5): 93‑97
Цель исследования — провести сравнительную оценку эффективности и комплаентности комбинированного лечения бесплодия у женщин с наружным генитальным эндометриозом (НГЭ) с применением гестагена (диеногеста) и агониста гонадотропин-рилизинг гормона (аГнРГ). Материал и методы. Дизайн — проспективное рандомизированное исследование. Рандомизацию проводили при помощи метода «конвертов». В исследование включены 62 пациентки с гистологически подтвержденным НГЭ и бесплодием: 42 пациенткам после проведения хирургического лечения назначен аГнРГ бусерелин 3,75 мг или диферелин 3,75 мг один раз в 28 дней в течение 3 мес внутримышечно; 20 женщинам — диеногест в дозе 2 мг в сутки в течение 6 мес. Критерии исключения из исследования: возраст моложе 18 и старше 45 лет, мужской фактор бесплодия, хроническая ановуляция, непроходимость маточных труб, тяжелые экстрагенитальные заболевания. Результаты. Показано, что комбинированное лечение бесплодия у пациенток с эндометриозом с применением хирургического метода (коагуляция и иссечение очагов эндометриоза) с последующим назначением аГнРГ или диеногеста является эффективным у 1/3 пациенток и по эффективности не имеет различий в зависимости от варианта медикаментозной терапии. Однако пациентки, получившие аГнРГ, в 2 раза чаще имели неразвивающуюся беременность. Эффективность обоих подходов в отношении симптомов эндометриоза была высокая в обеих группах, однако частота и тяжесть побочных эффектов были более значимыми у пациенток, получивших аГнРГ. Выводы. Эффективность применения аГнРГ и диеногеста у бесплодных пациенток с эндометриозом в лечении инфертильности и купировании болевого синдрома сходная. Частота побочных эффектов и неразвивающейся беременности выше у пациенток, получивших аГнРГ.
В настоящее время эндометриоз является распространенным гинекологическим заболеванием, связанным с бесплодием и, возможно, неблагоприятными исходами беременности [1]. Эндометриоз — хроническое, прогрессирующее рецидивирующее заболевание, поражающее 12—60% женщин репродуктивного возраста, характеризующееся эктопическим разрастанием эндометрия. Эндометриоз — одна из самых распространенных причин болевого синдрома, проявляется дисменореей, диспареунией и приводит к бесплодию. Частота бесплодия при всех локализациях генитального эндометриоза примерно в 3—4 раза превышает частоту бесплодия в популяции, а частота самопроизвольного прерывания беременности (чаще в I триместре) колеблется от 10 до 50% [2, 3].
До настоящего времени вопросы эффективного лечения наружного генитального эндометриоза (НГЭ) остаются спорными. Однако большинство клиницистов едины в одном: хирургическое лечение повышает частоту наступления беременности [3]. Ранее многими исследованиями [4, 5] было показано, что медикаментозное лечение при эндометриозе не улучшает фертильность. В настоящее время существует мнение, что при малых формах эндометриоза (I/II) в связи с риском оперативного лечения должно предлагаться экстракорпоральное оплодотворение [6, 7]. Однако в последние годы сформировалось представление о том, что медикаментозное лечение эндометриоза может быть достойной альтернативой хирургического лечения или дополнять его [8]. Первым этапом лечения должно являться хирургическое удаление очагов эндометриоза [3]. В лечении бесплодия при эндометриозе большинство практикующих врачей отдают предпочтение комбинированной терапии: первый этап — лапароскопия с целью хирургического удаления очагов эндометриоза; второй этап — гормональная терапия, направленная на подавление овариальной и менструальной функции [9]. Хирургический и медикаментозные методы лечения не должны противопоставляться. Преимущества и недостатки каждого метода должны быть тщательно взвешены до начала лечения с учетом индивидуальных особенностей случая. Это позволит свести до минимума отрицательные результаты и, напротив, максимально достичь положительных. До сих пор остается дискуссионным вопрос о критериях выбора самого эффективного препарата для применения в комбинированном лечении генитального эндометриоза, который был бы в то же время наиболее безопасным в каждом индивидуальном случае [10].
В настоящее время на основании многоцентрового открытого рандомизированного исследования с проведением лапароскопии second-look диеногест в дозе 2 мг один раз в день рекомендуется в качестве оптимальной дозы для терапии эндометриоза [11]. Большое количество исследований показало эффективность диеногеста для лечения эндометриоз-ассоциированной боли [12—16]. K. Sugimoto [17] доказана эффективность и безопасность применения препарата у больных с эндометриозом более 53 нед.
Опыт применения диеногеста 2 мг в сравнении с лейпрорелином 3,75 мг в комплексном лечении болевого синдрома, ассоциированного с эндометриозом, в течение 12 мес наблюдения показал сходную эффективность в лечении болевого синдрома и лучшую переносимость диеногеста [18].
В проспективном когортном рандомизированном исследовании Y. Takaesu [19] показано, что послеоперационное назначение гозерилина и диеногеста не имеет существенных различий в частоте рецидива заболевания, однако побочные эффекты наблюдались существенно чаще у пациенток, получавших гозерелин. Однако сравнительные исследования эффективости и безопасности применения гестагенов и агонистов у инфертильных пациенток с НГЭ до настоящего времени не проводились.
Цель — провести сравнительную оценку эффективности и комплаентности комбинированного лечения бесплодия у женщин с НГЭ с применением гестагена (диеногеста) и аГнРГ.
Дизайн исследования: проспективное рандомизированное. Исследование утверждено решением этического комитета ГБОУ ВПО «Кемеровская государственная медицинская академия» Минздрава России. Исследование не имеет конфликта интересов и проведено без финансовой поддержки фармацевтических компаний.
Обследованы 62 пациентки с гистологически подтвержденным НГЭ и бесплодием. Критерии включения в исследование: бесплодие, гистологически подтвержденный НГЭ, желание пациентки участвовать в исследовании и соблюдать протокол лечения.
Критерии исключения из исследования: возраст моложе 18 и старше 45 лет, мужской фактор бесплодия, хроническая ановуляция, непроходимость маточных труб, тяжелые экстрагенитальные заболевания. Рандомизация проводилась методом «конвертов».
Выделены две группы: 1-я группа — 42 пациентки, которым после хирургического лечения назначен аГнРГ бусерелин 3,75 мг или диферелин 3,75 мг один раз в 28 дней — 3 мес внутримышечно; 2-я группа — 20 женщин, которым назначали гестаген (диеногест) в дозе 2 мг в сутки в течение 6 мес.
Средний возраст пациенток в 1-й группе — 31,1±4,5 года, во 2-й —32,3±4,9 года (р=0,97). Средняя продолжительность бесплодия соответственно 3,2±2,8 и 3,2±1,9 года (р=0,29). Согласно пересмотренной классификации Американского общества фертильности (R-AFS), в 1-й группе I степень распространенности заболевания отмечена у 19 (45,2%) пациенток, II степень — у 3 (7,1%), III степень — у 13 (30,9%), IV степень — у 7 (16,7%), во 2-й группе соответственно — у 13 (65%), 1 (5%), 5 (25%), 1 (5%) пациентки (χ 2 =1,86; р=0,82). В обеих группах все пациентки предъявляли специфические для НГЭ жалобы.
В 1-й группе жалобы на наличие бесплодия отмечены у 42 пациенток, абдоминального болевого синдрома — 23 (54,7%) женщины, диспареунии — 14 (33,3%), дисменореи — 14 (33,3%); во 2-й группе — соответственно у 20 (100%), 7 (35%), 7 (35%), 6 (30%) женщин.
Обследование пациенток включало: общеклиническое исследование, специальное гинекологическое обследование, ультрасонографию органов малого таза аппаратом AlokaSSD 3500 (Япония), лапароскопию и гистероскопию с помощью эндоскопической техники фирмы «KARL STORZ» (Германия). Всем пациенткам перед включением в исследование проведены лапароскопия, коагуляция и иссечение очагов эндометриоза с гистологическим подтверждением диагноза. Оценка первичного исхода: частота наступления беременности проведена через год после оперативного лечения в обеих группах. Вторичные исходы: частота болевого синдрома, диспареунии, дисменореи, а также частота побочных эффектов лечения оценивались ежемесячно в течение 6 мес после оперативного лечения.
Оценка степени тяжести болевого синдрома проводилась согласно визуальной аналоговой шкале боли (E. Huskisson, 1974), оценка степени выраженности побочных эффектов — согласно числовой ранговой шкале, состоящей из последовательного ряда чисел от 0 до 10. Пациентам предлагалось оценить свои ощущения цифрами от 0 (нет ощущений) до 10 (максимально возможные ощущения). Статистическую обработку полученных результатов проводили с помощью пакета прикладных программ Statistica v.6.0 с использованием t-теста Стьюдента для групп, представленных параметрическими величинами; оценки корреляционной зависимости для непараметрических, ранговых величин по методу Спирмена (R).
Однако следует отметить высокую частоту неразвивающейся беременности: в 1-й группе у 5 (11,9%) пациенток, во 2-й группе — у 1 (5%).
Частота первичных и вторичных исходов лечения представлена в табл. 1.
Таблица 1. Частота (в %) первичных и вторичных исходов лечения у пациенток с НГЭ на фоне лечения аГнРГ и диеногестом
Оценка вторичных исходов проводилась через 6 мес после лечения.
Только 2 пациентки в обеих группах отмечали незначительные (2—4 балла) периодические боли внизу живота. При этом все пациентки отмечали существенное снижение интенсивности абдоминального болевого синдрома (до лечения — 7—9 баллов). Жалоб на диспареунию и дисменорею через 6 мес лечения аГнРГ и диеногестом пациентки не предъявляли.
Частота побочных эффектов на фоне лечения аГнРГ и диеногестом представлена в табл. 2.
Таблица 2. Частота (в %) первичных и вторичных исходов лечения у пациенток с НГЭ на фоне лечения аГнРГ и диеногестом
Во 2-й группе жалобы наблюдались у 3 (15%) женщин: у 1 — на приливы и раздражительность, у 2 — на ухудшение настроения. Все побочные эффекты в 1-й группе регистрировались значительно чаще, чем во 2-й (p<0,001).
Стремительное нарастание всех симптомов наблюдалось ко 2-му месяцу медикаментозного лечения аГнРГ (см. рисунок).
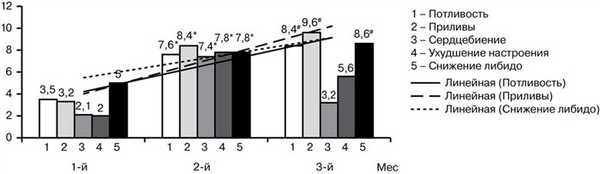
Динамика степени тяжести побочных реакций при лечении аГнРГ. * — p
Наибольшая выраженность ощущения сердцебиения и ухудшение настроения (раздражительность, плаксивость, депрессия) наблюдались через 2 мес терапии. Через 3 мес терапии интенсивность данных симптомов уменьшалась. Жалобы на приливы, повышенное потоотделение, снижение либидо прогрессивно нарастали к 3-му месяцу лечения, достигая максимального значения в среднем 9,6±2,4, 8,4±1,8 и 8,6±1,6 балла соответственно. Через 3 мес лечения аГнРГ 47% женщин оценили жалобы максимальной оценкой — 10 баллов. Жалобы на приливы, потливость сохранялись у ряда пациенток в течение 3—4 мес после прекращения лечения, на снижение либидо — до года после прекращения лечения.
Результаты проведенного обследования показали, что первичный исход комбинированного лечения НГЭ у инфертильных женщин с применением хирургического метода лечения (иссечение и коагуляция очагов эндометриоза) и медикаментозной терапии (аГнРГ или диеногеста) — наступление беременности через год, имел место у 1/3 пациенток в обеих группах. При этом частота неразвивающейся беременности у пациенток, получавших аГнРГ, была в 2 раза выше, чем у пациенток, получавших после оперативного лечения диеногест, что, возможно, обусловлено гипоплазией эндометрия на фоне выраженной гипоэстрогении, обусловленной аГнРГ.
Частота вторичных исходов: абдоминального болевого синдрома, диспареунии, дисменореи — значимо снижалась в обеих группах. Сходные результаты были представлены ранее другими авторами [17, 18].
Отмечены высокая частота (90,5%) и выраженность побочных реакций на фоне аГнРГ, что значительно нарушало качество жизни у этих пациенток. При применении диеногеста только у 15% женщин наблюдались побочные эффекты, которые значимо не влияли на качество жизни и не требовали назначения терапии. В исследовании М.И. Ярмолинской [20] показана также невысокая частота побочных эффектов при применении диеногеста у пациенток с эндометриозом: наиболее часто регистрировались изменения настроения — у 9,1%, мастодиния — у 5,1%, аcne vulgaris — у 4%.
Таким образом, комбинированное лечение бесплодия у пациенток с эндометриозом с применением хирургического метода (коагуляция и иссечение очагов эндометриоза) с последующим назначением аГнРГ или диеногеста является эффективным у 1/3 пациенток и не имеет различий в зависимости от варианта медикаментозной терапии. Однако пациентки, получившие аГнРГ, в 2 раза чаще имели неразвивающуюся беременность. Эффективность обоих подходов в отношении симптомов эндометриоза (межменструальные боли, дисменорея, диспареуния) была высокая в обеих группах, однако частота и тяжесть побочных эффектов были более значимыми у пациенток, получивших аГнРГ.
Таким образом, для инфертильных пациенток, страдающих эндометриозом, более безопасным подходом является применение комбинированного метода лечения с использованием 2 мг диеногеста.
Глубокий инфильтративный эндометриоз — форма эндометриоза, при которой патологическая ткань может проникать до 5 мм под поверхность пораженной структуры. Проблема терапии эндометриоза остается не решенной по настоящее время. Признание заболевания хроническим требует разработки длительных схем лечения пациенток, чаще до менопаузы, что может занимать годы и десятилетия. Принцип «не более одной операции у пациентки с эндометриозом» или попытка вовсе избежать оперативного лечения заставляют выбирать не только высокоэффективные, но и безопасные лечебные препараты. Препаратами первой линии для лечения эндометриоза являются прогестины, в частности диеногест. В статье представлен анализ применения диеногеста, по данным литературы, у пациенток с глубоким инфильтративным эндометриозом, рассмотрен механизм действия препарата. Показаны преимущества диеногеста по сравнению с другими прогестинами. Особое внимание уделено влиянию на болевой синдром и диспареунию. Приводятся возможные осложнения и меры их профилактики. Обоснована необходимость длительного применения. Имеющиеся в настоящее время данные литературы свидетельствуют, что назначение диеногеста (Визанны) в дозе 2 мг/сут после хирургического лечения глубокого инфильтративного эндометриоза является эффективным и безопасным.
Ключевые слова: генитальный эндометриоз, болевой синдром, диспареуния, прогестин, диеногест, Визанна.
Efficacy and safety of long-term administration of dienogest for deep infiltrative endometriosis
V.G. Volkov 1 , N.E. Malykh 2
1 Tula State University, Tula, Russian Federation
2 Tula Multidisciplinary Medical Center «Consultant Farm», Tula, Russian Federation
Deep infiltrative endometriosis is a type of endometriosis characterized by 5-mm penetration of pathological tissue in the affected structure. Treatment approaches to endometriosis still remain elusive. Chronic nature of this disease requires long-term therapeutic strategies up to menopause thus taking years and even decades. To follow the principle of “no more than one surgical procedure in a woman with endometriosis” or to avoid the surgery, one should select highly effective but also safe medications. Progestins, in particular, dienogest, are first-line choice for endometriosis. The paper reviews published data on dienogest use in women with deep infiltrative endometriosis and analyses its mechanism of action. Advantages of dienogest as compared with other progestins are discussed. Special attention is paid to its effects on pain and dyspareunia. Potential treatment complications and their prevention are addressed. Need for long-term administration is ju stified. Current data demonstrate that 2 mg daily of dienogest (Visanne) prescribed postoperatively after the surgery for deep infiltrative endometriosis are effective and safe.
Keywords: genital endometriosis, pain, dyspareunia, progestin, dienogest, Visanne.
For citation: Volkov V.G., Malykh N.E. Efficacy and safety of long-term administration of dienogest for deep infiltrative endometriosis. Russian Journal of Woman and Child Health. 2019;2(3):226-230.
В статье представлен анализ применения диеногеста, по данным литературы, у пациенток с глубоким инфильтративным эндометриозом, рассмотрен механизм действия препарата.
Актуальность
Эндометриоз — патологический процесс, при котором за пределами полости матки происходит доброкачественное разрастание ткани, по морфологическим и функциональным свойствам подобной эндометрию [1]. Несмотря на наличие многих противоречий относительно механизмов, ответственных за его патогенез и прогрессирование, широко известно, что эндометриоз является эстрогензависимым хроническим воспалительным заболеванием [2], рассматриваются также генетические и эпигенетические механизмы [3].
Проблема терапии эндометриоза (как внутреннего, так и наружного) остается не решенной по настоящее время. Основные цели лечения данного заболевания: удаление очага эндометриоза; уменьшение интенсивности болей; лечение бесплодия; предотвращение прогрессирования; профилактика рецидивов, что уменьшает необходимость радикального оперативного вмешательства и позволяет сохранить репродуктивную функцию женщины [1].
Агонисты гонадотропин-рилизинг-гормона (ГнРГ) не могут рассматриваться в качестве препаратов выбора для долгосрочной терапии вследствие побочных вазомоторных эффектов и снижения минеральной плотности костной ткани, связанных с эстрогенным дефицитом [16].
Диеногест в терапии эндометриоза
Диеногест (например, препарат Визанна) является прогестагеном 4-го поколения и объединяет фармакологические свойства группы прогестерона и прогестероноподобных соединений, а также производных 19-нортестостерона [21]. Диеногест — первый гестаген, который дает клинически значимый антиандрогенный эффект, при этом не проявляя эстрогенной и андрогенной активности [23].
Исследования показали, что диеногест оказывает ановуляторное и антипролиферативное влияние за счет подавления секреции цитокинов в строме эндометриальных клеток. Прогестины ингибируют рост эндометриотической ткани, вызывая децидуализацию с последующей атрофией эндометриотических имплантатов [4].
Дополнительные механизмы действия включают подавление опосредованного матриксными металлопротеиназами роста и имплантации эктопического эндометрия [24] и ингибирование ангиогенеза [25]. С другой стороны, диеногест способен улучшить чувствительность к прогестерону в эндометриоидной ткани путем увеличения соотношения изоформ B/A рецептора прогестерона [26]. Точные механизмы ослабления прогестеронового ответа у пациентов с эндометриозом остаются неясными. Возможно, нарушение действия прогестерона в эндометрии пациенток с эндометриозом может быть связано с врожденной устойчивостью самого эндометрия к прогестерону, а не с нарушением секреции прогестерона. Фармакологические механизмы действия диеногеста могут включать антиовуляторную активность, приводящую к снижению сывороточных уровней эстрадиола, и прямое антипролиферативное и противовоспалительное действие на клетки эндометрия. Диеногест значительно снижает уровень эстрогенов в эндометриотической ткани за счет ингибирования ароматазы и 17β-гидроксистероиддегидрогеназы типа 1 в стромальных клетках эндометриом яичников, увеличивает апоптоз эндометриотических клеток и снижает продукцию провоспалительных цитокинов эндометриотическими стромальными клетками [27]. Кроме того, он снижает продукцию и высвобождение индуцированных эстрадиолом ангиогенных факторов, таких как сосудистый эндотелиальный фактор роста, что подтверждает выявленное подавление ангиогенеза, ранее показанное на модели мыши [28]. Кроме того, диеногест способен стимулировать апоптоз в эндометриоидных клетках [29].
Анализ длительного применения диеногеста
Сказанное выше требует проанализировать длительное применение диеногеста для лечения эндометриоза. Двойное слепое плацебо-контролируемое исследование показало, что лечение диеногестом в течение 12 нед. было более эффективным, чем лечение плацебо, в уменьшении боли, связанной с эндометриозом. Примерно аналогичные результаты получены при анализе применения диеногеста в дозе 2 мг/сут на протяжении 24 нед. [30]. Последующее наблюдение за пациентками до 53 нед. также показало устойчивое уменьшение тазовой боли с минимальными побочными эффектами [31]. Согласно инструкции по медицинскому применению препарата Визанна, к наиболее частым побочным эффектам относятся: кровотечения из влагалища, головная боль, дискомфорт в молочных железах, снижение настроения и акне [32]. Объединенный анализ четырех рандомизированных европейских исследований со сроками лечения диеногестом в дозе 2 мг/сут до 65 нед. показал, что побочные эффекты, связанные с приемом диеногеста 2 мг, встречались относительно редко и хорошо переносились пациентками [33]. Есть мнение о том, что частота возникновения кровотечения зависит от исходного уровня эстрогенов, который, в свою очередь, зависит от массы тела. Так, исследование T. Strowitzki et al. показало, что средний уровень эстрадиола в сыворотке крови у европейских женщин, принимающих диеногест, составил приблизительно 66,7 пг/мл при средней массе тела 62,4 кг [34], тогда как в Японии — 38 пг/мл при средней массе тела 52,1 кг [35].
Текущий объединенный анализ показывает, что среднее изменение массы тела при продолжении лечения диеногестом до 62 нед. невелико и существенно не отличается от наблюдаемого в группе плацебо [33].
Важным преимуществом диеногеста считается то, что он не снижает минеральную плотность костной ткани и не вызывает побочных эффектов, связанных с гипоэстрогенией, и поэтому может назначаться в течение более длительного периода [30]. Уровень эстрадиола при лечении диеногестом в дозе 2 мг/сут прогрессивно снижался и составил 36±13 пг/мл через 36 мес. и 28±12 пг/мл через 60 мес. лечения [34]. Таким образом, уровни эстрадиола сохраняются в пределах «терапевтического окна», предложенного в теории порога Барбьери — 30-50 пг/мл [36], при котором подавление уровня эстрогенов является достаточным для ингибирования роста эндометриотических поражений, но достаточно умеренным для предотвращения гипоэстрогенных побочных эффектов [37]. Это имеет особо важное значение для лечения девушек-подростков и молодых женщин, поскольку они еще не достигли максимальной плотности костной ткани.
Например, при использовании агонистов ГнРГ для лечения эндометриоза на сегодняшний день единственным вариантом восстановления уровня эстрадиола, достаточного, чтобы избежать симптомов менопаузы и потери минеральной плотности костной ткани, является совместное применение агониста ГнРГ и эстрогенов/прогестинов (add-back терапия). Однако дополнительное введение эстрогенов может привести к прогрессированию заболевания и увеличить стоимость лечения.
Продолжительная терапия диеногестом в дозе 2 мг/сут также показала достоверное уменьшение болевого синдрома через 24-52 нед. с допустимыми побочными эффектами [21]. По сравнению с прогестинами с андрогенной активностью, такими как медроксипрогестерона ацетат и норэтиндрона ацетат, диеногест имеет более благоприятный профиль безопасности с низкими падениями андрогенных влияний. Показано, что диеногест в дозе 2 мг/сут является более эффективным, чем дидрогестерон в дозе 10 мг 2 р./сут для облегчения эндометриоз-ассоциированного болевого синдрома, с соответствующим профилем безопасности. Этот вывод имеет большое значение, т. к. тазовая боль является одним из самых важных симптомов эндометриоза [38]. Ранние исследования показали, что нет убедительных доказательств в пользу терапевтического применения дидрогестерона при эндометриозе [39]. Кроме того, национальные клинические рекомендации по терапии эндометриоза заявляют, что применение прогестагенов в циклическом режиме (дидрогестерон 40-60 мг в течение 6-18 мес.) неэффективно в сравнении с плацебо [40].
Заключение
Прогестины, в т. ч. диеногест, подобно всем другим лекарствам для терапии эндометриоза, подавляют, но не лечат эктопические очаги. Следовательно, их действие сохраняется до тех пор, пока они используются, и симптомы обычно рецидивируют после прекращения лечения. Это не должно рассматриваться как неэффективность лечения. Известно, что подавляющее большинство хронических заболеваний (сахарный диабет, артериальная гипертензия, аутоиммунные заболевания и др.) требуют медикаментозной терапии на протяжении длительного периода, а иногда и пожизненно, но не излечиваются. Поэтому и лечение эндометриоза как хронического заболевания следует планировать на длительный период, вплоть до наступления менопаузы [47, 48]. Терапевтическая стратегия, основанная на долгосрочном приеме прогестинов, позволяет минимизировать количество различных исследований и посещений гинеколога, снизить затраты и риск хирургического вмешательства. Практическая проблема здесь заключается в определении того, когда медикаментозная терапия является более выгодной по сравнению с операцией, принимая во внимание, что, если выбрано гормональное лечение, оно должно продолжаться до желаемой беременности или физиологической менопаузы. Прием прогестинов может предопределить долгосрочное лечение в обход оперативного вмешательства, и на этот важный аспект необходимо обратить внимание пациентки, как и на то, что хирургическая операция как изолированная мера не гарантирует окончательного облегчения симптомов [49].
Признание генитального эндометриоза хроническим заболеванием в конце ХХ в. явилось одним из важнейших научных достижений в исследовании и лечении этого «загадочного» многосимптомного и полиорганного заболевания. Хронический характер болезни нацеливает врача и пациентку на длительную комплексную индивидуальную терапию. Имеющиеся в настоящее время в литературе данные свидетельствуют, что назначение диеногеста (например, Визанны) в дозе 2 мг/сут после хирургического лечения является эффективным методом терапии эндометриоза, обладающим высоким профилем безопасности и переносимости [50].
Сведения об авторах:
1 Волков Валерий Георгиевич — д.м.н., профессор, заведующий кафедрой акушерства и гинекологии, ORCID iD 0000-0002-7274-3837;
2 Малых Наталья Евгеньевна — к.м.н., врач высшей категории, ORCID iD 0000-0002-5137-1202.
1 ФГБОУ ВО «ТулГУ». 300012, Россия, г. Тула, проспект Ленина, д. 92.
2 ООО «Консультант Фарм». 300041, Россия, г. Тула, ул. Коминтерна, д. 20.
About the authors:
1 Valeriy G. Volkov — MD, PhD, Professor, Head of the Department of Obstetrics and Gynecology, ORCID iD 0000-0002-7274-3837;
2 Natal’ya E. Malykh — MD, PhD, doctor of highest category, ORCID iD 0000-0002-5137-1202.
1 Tula State University. 92, Lenin Ave., Tula, 300012, Russian Federation
2 Tula Multidisciplinary Medical Center “Consultant Farm”. 20, Kominterna str., Tula, 300041, Russian Federation.
Список литературы Свернуть Развернуть
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Читайте также:
