Аппендэктомия у детей. Операция при инвагинации кишечника у детей
Добавил пользователь Алексей Ф. Обновлено: 28.01.2026
Городская Ивано-Матренинская детская клиническая больница, Иркутск;
Иркутская государственная медицинская академия последипломного образования
Городская Ивано-Матренинская детская клиническая больница, Иркутск;
Иркутский государственный медицинский университет;
Иркутская государственная медицинская академия последипломного образования
1. Городская Ивано-Матренинская детская клиническая больница, Иркутск;
2. Иркутский государственный медицинский университет;
3. Иркутская государственная медицинская академия последипломного образования
Городская Ивано-Матренинская детская клиническая больница, Иркутск
Центр хирургии и реанимации новорожденных, МУЗ «Ивано-Матренинская детская клиническая больница», Иркутск
Иркутский государственный медицинский университет, Иркутск
Эндохирургическое лечение мальротации кишечника у новорожденных и младенцев
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2016;(4): 34‑39
Введение. Мы сообщаем результаты сравнения лечения мальротации кишечника у новорожденных и младенцев с использованием лапароскопии и лапаротомии. Материал и методы. В период между январем 2004 г. и декабрем 2013 г. было выполнено 34 операции Ледда. В исследовании сообщаются данные детей, которые подвергнуты лапароскопической (17 пациентов - 1-я группа) и стандартной (17 больных - 2-я группа) операции. Результаты. Группы имели одинаковые демографические и другие предоперационные параметры. Были обнаружены значимые различия в длительности операции между лапароскопическими и открытыми операциями (61 мин против 70 мин). Пациенты начинали раньше питание после миниинвазивного способа лечения (1,5 сут против 3 сут) и имели меньшее время перехода на полное энтеральное питание (4,2 сут против 6,9 сут). Продолжительность пребывания в стационаре была меньше в 1-й группе (7,7 сут против 10,2). Количество ранних послеоперационных осложнений не отличалось в группах. Число поздних осложнений было больше в группе лапаротомии, однако различия не были достоверны. Заключение. Исследование демонстрирует, что эндохирургическая коррекция врожденных аномалий вращения кишечника дает лучшие послеоперационные результаты, чем открытая хирургия, и может быть широко использована у маленьких детей.
Цель настоящего исследования - продемонстрировать возможность и преимущества лапароскопического лечения мальротации кишечника в группе больных, чей возраст не превышает 3 мес жизни.
Материал и методы
Мы выполнили ретроспективный анализ результатов всех операций Ледда, произведенных в Центре хирургии новорожденных Иркутской детской клинической больницы на протяжении 11 лет, с января 2004 г. по декабрь 2013 г. Исследование было одобрено этическим комитетом больницы. Лапароскопия была внедрена для лечения мальротации в 2004 г. и с тех пор стала постепенно превращаться в предпочтительный подход для коррекции этого состояния. За все время исследования процедура Ледда выполнена 34 детям: 17 - лапароскопические операции (1-я группа) и 17 - открытые хирургические вмешательства (2-я группа). Конверсия к лапаротомии стала необходимой у 2 больных 1-й группы и была обусловлена нарастанием гемодинамических расстройств на фоне заворота и ишемии кишечника. Из исследования были исключены также пациенты с врожденной диафрагмальной грыжей, гастрошизисом, омфалоцеле.
В обеих группах было по 11 мальчиков и 6 девочек. Средний возраст больных 1-й группы составил 13,1±9,6 сут (здесь и далее M±SD означает среднее ± стандартное отклонение), 2-й - 12,9±9,6 сут. Средняя масса тела к моменту операции была равна 3326±426 г в 1-й и 3351±407 г во 2-й группе.
Наиболее распространенные клинические симптомы заболевания включали боль или беспокойство, являющееся аналогом болевых ощущений у маленьких детей (59%), эпизодическую рвоту (100%) и кровь в стуле (33%).
В нашем исследовании диагноз мальротация устанавливался на основании нескольких рентгенологических и визуальных до- и интраоперационных критериев: расположение дуоденоеюнального перехода справа от средней линии, размещение слепой кишки под печенью или в центральных отделах брюшной полости.
Современным методом диагностики мальротации, позволяющим определить не только морфологию кишечника, но и его функциональные расстройства, являлось ультразвуковое исследование брюшной полости. Мы придаем большое значение оценке двух ультразвуковых признаков - толщины корня брыжейки тонкой кишки и кровотока в верхней брыжеечной артерии. Определение заворота первоначально основывалось на измерении размера корня брыжейки, который в случае ротации «средней» кишки вокруг верхней брыжеечной артерии превышал 50% окружности брюшной полости. Ультразвуковые критерии синдрома Ледда, сопровождающегося заворотом кишечника, включали симптом «штопора» или «водоворота» - графическое выражение направления кровотока в верхней брыжеечной артерии.
Дооперационный диагноз, основанный на данных рентгенологического и ультразвукового исследований, был установлен у 79% пациентов. У остальных 21% больных мальротация выявлена во время эксплоративной операции на органах брюшной полости, произведенной в связи с подозрением на высокую кишечную непроходимость.
Техника операции Ледда. Пациента размещали на операционном столе в положении, обратном положению Тренделенбурга. Выполняли правосторонний поперечный разрез в правом подреберье или полукруглый разрез в околопупочной области. Принципиальной находкой, определяющей вид реконструкции, являлся заворот, сопровождающийся некрозом обширного сегмента тонкой кишки. В этом случае производили резекцию некротически измененного сегмента и соединение жизнеспособных кишечных сегментов с помощью анастомоза.
В стандартных ситуациях, не сопровождающихся некрозом кишечной трубки, применяли классическую операцию Ледда, которую начинали с устранения заворота вокруг корня брыжейки по часовой стрелке или против нее (в зависимости от направления торсии). Затем рассекали перидуоденальные спайки, деформирующие просвет двенадцатиперстной кишки. Дуоденолиз выполняли до тех пор, пока не достигали полного выпрямления двенадцатиперстной и начального отдела тощей кишки. Корень брыжейки обнажали так, чтобы визуально определялась пульсация верхней брыжеечной артерии. Толстую кишку перемещали в левую половину брюшной полости. Размещенные слева слепую кишку и восходящий отдел ободочной кишки фиксировали к левой половине ободочной кишки. Производили аппендэктомию инвагинационным способом. После окончания основных этапов операции Ледда послойно ушивали разрез брюшной стенки.
Лапароскопический вариант операции Ледда осуществляли с использованием трехпортового доступа. Ребенка размещали на операционном столе в положении, обратном положению Тренделенбурга с поворотом операционного стола на 30° в левую сторону. Использовали карбоперитонеум с «мягкими» параметрами - поток 2 л/мин, давление 8 мм рт.ст. Выполняли лапароцентез и устанавливали 3 порта: первый - в левой подвздошной области (оптический), второй - в левом верхнем квадранте (инструментальный), третий - в правой подвздошной области (инструментальный). Расположение лапароскопа в нижнем отделе брюшной полости обеспечивает лучшую визуализацию порока развития кишечника у новорожденных. При таком размещении портов создается рабочее пространство, достаточное для выполнения операции Ледда. Однако у пациентов, чей возраст превышал 3 мес жизни, размер брюшной полости позволяет размещать оптический троакар в области пупка.
Выполняли ревизию брюшной полости, чтобы подтвердить диагноз. Для этого с помощью атравматических зажимов приподнимали слепую и поперечную ободочную кишку с целью идентификации связки Трейтца. Если эта связка отсутствовала, то диагноз мальротации не вызывал сомнения и служил показанием к выполнению операции Ледда. Дальнейшие действия хирурга зависели от того, сопровождался ли синдром Ледда заворотом и некрозом «средней» кишки. При идентификации необратимых нарушений кровообращения в ротированной кишке выполняли конверсию к открытой операции, которая заключалась в резекции пораженного сегмента кишки с наложением анастомоза.
Если заворот «средней» кишки не сопровождался некрозом, то последующие этапы хирургического вмешательства повторяли шаги, которые используются при открытом варианте этой процедуры. Устраняли заворот, разделяли перидуоденальные спайки, перемещали слепую кишку в левую половину брюшной полости и фиксировали ее к сигмовидной кишке (см. рисунок). Использовали технику no touch (от англ. - без соприкосновения), т. е. без захвата стенки кишки, который может привести к ее травме. Конверсию к лапаротомии выполнили в 2 (12%) наблюдениях из-за недостаточной визуализации ключевых структур брыжейки на фоне заворота и нарушений мезентериального кровотока.
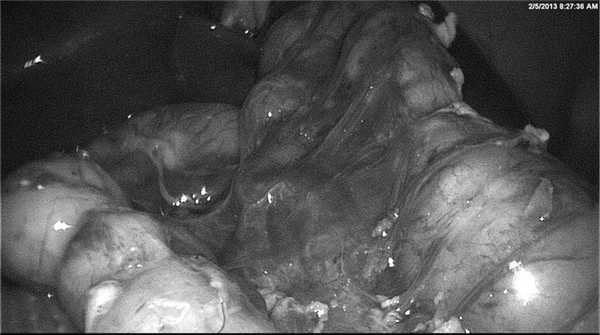
Интраоперационная фотография. Вид органов брюшной полости после выполнения операции Ледда. Слева находится выпрямленная двенадцатиперстная кишка, справа - толстая кишка, перемещенная в левую половину брюшной полости.
Энтеральное кормление больных после операции начинали с того момента, когда объем потерь по желудочному зонду снижался до 10 мл/кг/сут. После нормализации нутритивного статуса пациентов переводили в хирургическое отделение для послеоперационного лечения. Пациентов выписывали на основании внутрибольничного протокола, предусматривающего их полную адаптацию к вскармливанию и положительный баланс весоростовых показателей на фоне стабильного гомеостаза. Контрольные осмотры проводили через 1, 3, 6 и 12 мес после выписки.
По окончании наблюдения за детьми проведено сравнение демографических данных, интраоперационных параметров, ближайших и отдаленных результатов операции. Выполнено статистическое сравнение групп пациентов. Проанализированы дооперационные показатели (пол, возраст и масса тела ко дню операции). Проведено сравнение интра- и послеоперационных параметров - длительности операции, наличия заворота, времени начала энтерального питания и времени перехода на полное энтеральное питание, продолжительности нахождения в стационаре, частоты послеоперационных осложнений - ранних (раневая инфекция) и поздних (повторный заворот, спаечная кишечная непроходимость), а также летальности. Для оценки средних значений в группах использовали U-тест Манна-Уитни, для оценки категориальных переменных - c 2 -тест с поправкой Йетса или точный критерий Фишера. Уровнем доверительной значимости принимали p
Результаты и обсуждение
Пациенты в обеих группах не имели значимых различий по полу (р=1,0), возрасту (р=0,946) и массе тела (р=0,892).
Во время операции заворот «средней» кишки обнаружен у 13 (76,5%) детей 1-й группы и у 14 (82,4%) детей 2-й группы, различия недостоверны (р=1,0). Резекция кишки потребовалась в 2 (11,8%) наблюдениях в каждой группе. Средняя продолжительность операции была меньше у пациентов эндохирургической группы (61 мин против 70 мин; р=0,0005).
Послеоперационные данные показали несколько существенных различий между двумя группами. Среднее количество дней, отражающих начало и достижение полного энтерального питания, было достоверно меньше в 1-й группе по сравнению со 2-й: 1,5 сут против 3 сут (р=0,001) и 4,2 сут против 6,9 сут (р=0,001) соответственно. Раневая инфекция регистрировалась значительно чаще во 2-й группе (11,8% против 0), однако различия не были достоверны (р=0,484).
Продолжительность послеоперационного пребывания в больнице также была значительно больше в группе открытой операции (7,7 сут против 10 сут; р=0,001).
Хирургические операции не сопровождались летальным исходом в раннем послеоперационном периоде. Летальные исходы имели место только в отдаленном периоде наблюдений в группе открытого лечения (11,8% против 0; р=0,484) и были связаны в основном с необратимым повреждением печени на фоне длительного парентерального питания и полиорганными расстройствами вследствие синдрома «короткой кишки».
Последующее наблюдение было доступно у 15 пациентов 1-й группы и у 10 пациентов 2-й группы на протяжении от 6 мес до 10 лет после операции. Ни у одного из этих детей в отдаленном периоде не возник повторный заворот кишечника. У 3 больных после открытой операции развилась спаечная кишечная непроходимость через 6-12 мес после операции Ледда, однако это различие не было статистически значимо (17,6% против 0; р=0,227).
Врожденные нарушения ротации в 75% наблюдений проявляются в течение 1 мес и в 90% - в течение 1 года жизни [14, 16, 23]. Популяционная частота аномалий вращения достоверно не известна. Эмбриональный механизм возникновения этого заболевания изучен и заключается в следующем [6]. Примитивный кишечный тракт начинает формироваться приблизительно к 4-й неделе беременности. В 10 нед беременности «средняя» кишка подвергается вращению против часовой стрелки на 270° вокруг оси верхней брыжеечной артерии. К 12-й неделе внутриутробного развития «средняя» кишка становится фиксированной к задней стенке брюшной полости с помощью брюшинных сращений, обеспечивающих ее стабилизацию на протяжении от связки Трейтца до слепой кишки. Изменения в этой последовательности вращения и фиксации «средней» кишки приводят к мальротации и аномалиям брыжейки, предрасполагающим к завороту. Непроходимость кишечника может развиться как вследствие заворота и некроза всей «средней» кишки, так и в результате наружного сдавления двенадцатиперстной кишки.
Быстрая постановка точного диагноза нарушения вращения кишечника и своевременное хирургическое лечение крайне важны для предотвращения катастрофических последствий. С этой целью используют ультразвуковое исследование [19] и ирригографию [16]. Не менее важные симптомы могут быть отмечены при проведении контрастной гастродуоденографии. Следует учитывать вероятность получения ложноположительных и ложноотрицательных результатов [5], которые могут привести к напрасной операции или упущенной возможности предотвращения заворота. Другая проблема связана с выявлением бессимптомных форм заболевания, случайно обнаруженных при рентгенологических исследованиях или в ходе операций, выполняющихся по поводу других заболеваний [23]. Риск заворота у этих пациентов не может быть точно предсказан.
Критериями благоприятного восстановления больных после лапароскопии являются раннее возобновление функции пищеварения и сокращение длительности пребывания младенца в больнице. Среднее время, необходимое для перехода на полное энтеральное питание больных после эндохирургической коррекции мальротации, по данным некоторых авторов, составляет 1-4 дня [3, 4, 18]. Сообщается также, что средняя продолжительность нахождения пациентов в больнице составляет 5-7 дней [3, 4, 7, 22]. Имеются данные о том, что пациентам после лапароскопии требуется меньшее количество анальгетиков, чем пациентам после открытых операций [3, 4, 7].
Другое потенциальное преимущество лапароскопической операции Ледда заключается в снижении частоты формирования перитонеальных адгезий. Показатель спаечной кишечной непроходимости после открытой операции Ледда составляет от 2 до 15% [4, 8, 27]. Некоторые хирурги полагают, что абдоминальные спайки важны для фиксации тонкой кишки в состоянии нонротации, что предотвращает заворот в будущем [13, 14], но это мнение не нашло всеобщей поддержки.
Итак, лапароскопия как менее агрессивная хирургическая техника предполагает альтернативный подход, заключающийся в минимально травматичном доступе и раннем восстановлении пациентов после операции. В нашей больнице эндохирургия используется на протяжении 11 лет и стала предпочтительным методом для коррекции мальротации. В настоящей работе мы изложили свой взгляд на место минимально инвазивной хирургии в лечении аномалий вращения кишечника и провели сравнение результатов открытых и эндоскопических операций, выполненных 34 пациентам. Данные, представленные в исследовании, подтверждают и закрепляют результаты нескольких других, меньших по количеству пациентов серий исследований, посвященных лечению мальротации. Сокращение длительности операции, раннее послеоперационное восстановление пациентов стали самыми значимыми факторами, которые способствовали уменьшению продолжительности пребывания пациентов в госпитале. Кроме того, нами было установлено, что лапароскопия сопровождается снижением показателей осложнений и летальности.
Таким образом, в ходе сравнительного исследования результатов открытой и лапароскопической операции Ледда было установлено, что лапароскопия является выполнимой, безопасной и эффективной технологией лечения детей с мальротацией. Мы полагаем, что минимально инвазивная хирургия предоставляет превосходную альтернативу открытой хирургии у новорожденных и младенцев без подозрения на заворот. Кроме того, учитывая наш опыт использования лапароскопического подхода в лечении мальротации, сопровождающейся заворотом и нарушением мезентериального кровообращения, мы полагаем, что срочная лапаротомия в этой группе является методом выбора, позволяющим выполнить самый быстрый доступ к кишечнику и минимизировать риск развития его некроза.
Инвагинация кишечника у детей
Инвагинация кишечника - смешанный вариант кишечной непроходимости, обусловленный изоперистальтическим внедрением проксимального участка кишки в дистальный (крайне редко - наоборот).

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Наиболее распространенная - илеоцекальная инвагинация - представлена слепо-ободочной - внедрение слепой кишки в восходящую ободочную с последующем вовлечением в инвагинат подвздошной кишки с Баугиниевой заслонкой («головка инвагината» - слепая кишка) и подвздошно-ободочной - внедрение подвздошной кишки в восходящую ободочную через Баугиниеву заслонку («головка инвагината» - подвздошная кишка).
Этиология и патогенез
У детей грудного возраста причиной инвагинации кишечника чаще всего является функциональное нарушение координации кишечной моторики с преобладанием сокращений циркулярного мышечного слоя кишечной стенки. К некоординированному сокращению мышечных слоев могут привести изменения режима питания, введение прикорма, воспалительные заболевания кишечника. У детей старше года сравнительно часто наблюдаются механические причины инвагинации (полипы, дивертикулы, опухоли кишечной стенки).
Нарушение координации сокращения гладкой мускулатуры кишки приводят к внедрению ее участка в нижележащий по ходу перистальтики и формированию «инвагината» (обтурация кишечника). Поскольку за кишечной трубкой внедряется и соответствующая часть брыжейки, возникает странгуляция кишечника (нарушение кровообращения в кишке). Дальнейшее изоперистальтическое продвижение инвагината усугубляет циркуляторные нарушения в кишке. Развивается венозный застой и отек кишечной стенки, сопровождающийся отложением фибрина с адгезией брюшинных поверхностей цилиндров инвагината. Дальнейшие циркуляторные нарушения ведут к некрозу кишечной стенки и развитию перитонита. При тонкокишечных инвагинациях некроз кишки можно ожидать через 12 - 24 часа, при подвздошно-ободочном варианте инвагинации - через 6 - 12 часов, при слепо-ободочном и толстокишечном вариантах - через 36 - 48 часов.
Эпидемиология
Инвагинация кишечника является самым частым видом острой кишечной непроходимости у детей и может возникать в любом возрасте. Чаще инвагинация кишечника встречается в возрасте от 4 до 9 месяцев (85 - 90% случаев).
Диагностика
• Рекомендовано выполнить осмотр врачом-хирургом не позднее 1 часа от момента поступления в стационар.
Уровень убедительности рекомендации D (уровень достоверности доказательств 4)
Клиническая картина инвагинации кишечника зависит от её анатомического типа, возраста ребенка и срока, прошедшего от начала заболевания.
Поскольку, в большинстве случаев, инвагинация кишечника является илеоцевальной, то клиническую картину этой формы инвагинации у грудных детей можно считать типичной.
• Рекомендовано выяснить у больного и/или его родителей, имеются ли жалобы на повторяющиеся приступы беспокойства, анорексию, боли в животе, тошноту, рвоту, наличие примеси крови в стуле.
Коментарии: в классическом варианте, клиническая картина илеоцекальной инвагинации включает несколько компонентов:
• приступообразное беспокойство ребенка, обусловленное болевой импульсацией с ущемленной брыжейки - 85 % детей. Заболевание начинается внезапно, ребенок начинает резко беспокоиться, кричать, сучить ножками. Лицо становиться бледным, иногда покрывается холодным потом. Ребенок отказывается от груди. Длительность болевого приступа, как правило 3 - 7 минут, затем приступ прекращается также внезапно. Ребенок успокаивается, поведение его становиться обычным. Через несколько минут (от 5 до 20) приступ боли повторяется вновь. Постепенно приступы боли теряют свою остроту, но общее состояние ребенка ухудшается;
• рвота, которая в начальной стадии заболевания обусловлена висцеро-висцеральным рефлексом, а с течением времени является проявлением кишечной непроходимости - 73% детей;
• стул с примесью крови, как результат диапедеза эритроцитов в просвет кишки - 61% детей. Впервые часы заболевания у ребенка может быть самостоятельный стул без патологических примесей. Через 3 - 6 часов от начала заболевания у ребенка появляется стул с примесью темной крови без каловых масс, но с примесью слизи. Иногда выделения из прямой кишки имеют характер кровянистой желеобразной массы (стул по типу «малинового желе»).
Важно помнить, что в 15 - 20% случаев отсутствует важный анамнестический критерий - приступообразное беспокойство! В этом случае ребенок вял, адинамичен, имеет выраженные нарушения микроциркуляции в виде бледности кожи и слизистых.
• пальпируемое объемное образование (инвагинат) в брюшной полости, чаще всего определяемый в правом подреберье. Инвагинат пальпируется в виде продолговатого гладкого умеренно подвижного валика мягко-эластичной консистенции. При беспокойстве ребенка получить достоверные пальпаторные ощущения при осмотре живота бывает трудно.
• симптом Dance (симптом пустого правого подвздошья), что обусловлено вовлечением слепой кишки в инвагинат и продвижением слепой кишки в восходящую ободочную по ходу перистальтики.
• Клиническая картина тонкокишечной инвагинации имеет некоторые отличия. Первым признаком начала заболевания так же будет сильное беспокойство, обусловленное болевым приступом за счет патологической импульсации с брыжейки кишки, ущемленной в инвагинате. Однако, продолжительность беспокойства и крика ребенка короче; в промежутках между приступами типичный «светлый» промежуток не наступает. Ребенок по прежнему отказывается от груди, соску не берет. Состояние ребенка прогрессивно ухудшается, повторяется рвота. Стул длительное время остается нормальным, кровянистые выделения из прямой кишки появляются через 12 - 24 часа от начала заболевания или позже. Пальпаторно инвагинат определяется реже, чем при илеоцекальной инвагинации. Определяется он в параумбиликальной области, подвижен и небольших размеров.
• Клинические симптомы толстокишечной инвагинации менее выражены, чем при других видах инвагинации кишечника. Беспокойство ребенка нерезкое и непродолжительное. Общее состояние страдает в меньшей степени. При осмотре удается пальпировать инвагинат, который в данном случае располагается в левом подреберье или в левом подвздошье.
• В редких случаях инвагинации изоперистальтическое продвижение инвагината приводит к выпадению головки инвагинированной кишки через заднепроходное отверстие (эвагинация). Слизистая оболочка эвагинированной кишки синюшна, отечна с участками кровоизлияний.
Комментарии: при КИ общее состояние страдает незначительно, но может ухудшаться при развитии некроза ущемленной кишки, за счет присоединения явлений ОНК и перитонита.
• При осмотре и пальпации рекомендовано обратить внимание на наличие опухолевидного образования в брюшной полости, пассивного напряжения мыщц передней брюшной стенки, симптомов раздражения брюшины.
• При отсутствиии самостоятельно стула рекомендуется выполнить очистительную клизму - с оценкой наличия и характера стула.
Комментарии: после тщательного сбора анамнеза, который позволяет с высокой степень обоснованности заподозрить наличие инвагинации кишечника, необходимо приступить к пальпаторному исследованию брюшной полости.
• определить наличие инвагината (чаще в правом подреберье). Пальпацию живота необходимо проводить между приступами беспокойства ребенка. Если тщательная пальпация живота затруднена из-за выраженного беспокойства ребенка, необходимо осмотреть ребенка в состоянии неглубокого наркоза, для чего ребенок должен быть госпитализирован в стационар.
• при поздней диагностике заболевания, когда имеются признаки некроза кишки и перитонита живот становиться вздутым, напряженным и болезненным во всех отделах. В такой ситуации пальпаторное определение инвагината без наркоза сомнительно.
• пальпируемое объемное образование (инвагинат) в брюшной полости, чаще всего определяется в правом подреберье. Инвагинат пальпируется в виде продолговатого гладкого умеренно подвижного валика мягко-эластичной консистенции.
• может определяться симптом Dance (симптом пустого правого подвздошья), что обусловлено вовлечением слепой кишки в инвагинат и продвижением слепой кишки в восходящую ободочную по ходу перистальтики.
• При тонко-тонкокишечной инвагинации инвагинат пальпаторно определяется реже, чем при илеоцекальной инвагинации. Определяется он в параумбиликальной области, подвижен и небольших размеров.
• При толсто-толстокишечной КИ пальпируемый инвагинат чаще всего располагается в левом подреберье или в левой подвздошной области.
• В купе с типичным анамнезом, пальпаторное обнаружение инвагината делает диагноз инвагинации кишечника очевидным и позволяет перейти к лечению пациента.
Диагноз инвагинации кишечника устанавливается на совокупности данных анамнеза, осмотра и ряда инструментальных способов диагностики
Комментарии: В анализе крови, особенно при позднем поступлении,может определяться лейкоцитоз до 10-15х10⁹, палочкоядерный сдвиг, ускорение скорости оседания эритроцитов (СОЭ).
• В качестве предоперационного обследования рекомендовано определение группы крови и Rh-фактора, биохимического анализа крови с определением показателей кислотно-щелочного состояния, электролитного состава крови.
• Рабочая группа рекомендует использовать УЗИ для инструментальной диагностики кишечной инвагинации у детей.
Комментарии: основным методом в дополнительной диагностике инвагинации кишечника является УЗИ органов брюшной полости. Этот метод обладает 100-процентной диагностической достоверностью и специфичностью в отношении инвагинации кишечника. УЗ-признаками инвагинации кишечника является обнаружение симптома «мишени» или «псевдопочки». Симптом «мишени» заключается в наличии на поперечном срезе двух колец низкой эхоплотности, разделенных гиперэхогенным кольцом. Симптом «псевдопочки» виден на продольном срезе и представляет собой наслаивающиеся друг на друга гипер- и гипоэхогенные слои.
Диагностическая ценность ультразвукового исследования при подозрении на инвагинацию кишечника у детей подтверждена в ходе многих многоцентровых контролируемых исследований (Ko HS, Schenk JP, Tröger J, Rohrschneider WK.Current radiological management of intussusception in children.EurRadiol 2007; 17:2411; Hryhorczuk AL, Strouse PJ.Validation of US as a first-line diagnostic test for assessment of pediatric ileocolic intussusception.PediatrRadiol 2009; 39:1075).
• Для дополнительной диагностики инвагинации кишечника рекомендуется использование рентгенографии (рентгеноскопии).
Комментарий: для дополнительной диагностики инвагинации кишечника допустимо использование рентгенографии (рентгеноскопии). При инвагинации кишечника на обзорных рентгенограммах органов брюшной полости, выполненных в вертикальном положении может отмечаться малое газонаполнение правого нижнего квадранта живота и признаки кишечной непроходимоти - расширенные петли кишечника с уровнями жидкости. В случае перфорации стенки ущемленной кишки и развитии перитонита - определяется свободный газ в брюшной полости (серповидная полоска просветления над печенью). Однако подобная рентгенологическая картина неспецифична для инвагинации кишечника. Более полные сведения при подозрение на инвагинацию кишечника дает контрастная ирригография. В качестве контраста в случае подозрения на инвагинацию кишечника целесообразно использование воздуха (пневмоирригография). При выполнении пневмоирригографии ребенка укладывают на стол рентгенологического аппарата в горизонтальном положении. Нагнетание воздуха в ампулу прямой кишки производят баллоном Ричардсона через катетер. Воздух в кишку нагнетают медленно и осторожно. По мере заполнения воздухом толстой кишки головка инвагината определяется в виде гомогенной тени с четкими контурами. Расположение тени зависит от анатомического типа внедрения. Равномерное заполнение толстой кишки воздухом и проникновение его в начальный отдел подвздошной кишки позволяет исключить наличие инвагината в этом отделе кишечника, но не снимает диагноза тонкокишечного внедрения.
Комментарии: дифференцировать инвагинацию кишечника необходимо с заболеваниями, сопровождающимися приступами боли в животе, рвотой, кровянистыми выделениями из прямой кишки, наличием опухолевидного образования в брюшной полости.
Для дизентерии не характерно столь острое начало заболевания с приступами боли в животе и «светлыми» промежутками, что типично для инвагинации. Для дизентерии характерно слизи в каловых массах с примесью комочков гноя и сгустков крови. В отличие от этого при инвагинации из заднего прохода выделяется томная кровь, смешанная со слизью. Пальпируемое в брюшной полости колбасовидное образование подтверждает диагноз инвагинации. Ректальное исследование при инвагинации кишечника позволяет определить головку инвагината, пустую ампулу прямой кишки, сниженный тонус сфинктера. В отличие от этого при дизентерии выявляет спазм анального сфинктера. В любом случае следует учитывать нередкое сочетание инфекционной патологии с инвагинацией кишечника.
Абдоминальный синдром при болезни Шейнлейна-Геноха может иметь сходные с инвагинацией проявления: внезапные приступы боли в животе, рвота и стул с примесью крови. Для абдоминального синдрома при болезни Шейнлейна-Геноха характерно непостоянство и нестойкость симптомов, тогда, как при инвагинации они держаться стойко и нарастают. У детей может быть рвота с примесью крови, что нехарактерно для инвагинации. Кишечное кровотечение при болезни Шейнлейна-Геноха бывает вместе с каловым стулом, а при инвагинации присутствует кровь со слизью.
У старших детей инвагинацию приходиться дифференцировать с острым аппендицитом. Симптомы инвагинации кишечника у детей старшего возраста выражены обычно менее ярко, чем у грудных детей. В отличие от аппендицита при инвагинации боль в животе носит схваткообразный характер со светлыми промежутками. Признаки непроходимости кишечника также нехарактерны для острого аппендицита. При инвагинации кишечника живот долгое время остается мягким, в отличие от острого аппендицита, при котором напряжение мышц живота - один из основных признаков заболевания.
При пептической язве дивертикула Меккеля кишечное кровотечение является первым и основным симптомом. В отличие от инвагинации кровотечению не предшествуют болевые приступы, ребенок остается спокойным. Выделяемая кровь при язве дивертикула Меккеля не содержит слизи, что характерно для инвагинации кишечника. Пальпаторно не выявляется опухолевидное образование.
Полипоз толстой кишки часто сопровождается массивным кровотечением. Однако болевой синдром у таких детей не наблюдается, стул остается каловым с примесью алой или более темной крови со сгустками. Выражена анемия.
Эвагинацию приходится дифференцировать с выпадением прямой кишки. В отличие от инвагинации выпадение прямой кишки не сопровождается болевым приступом и рвотой. Кроме того, при осмотре выпавшей кишки определяется, что слизистая кишки переходит в кожу вокруг заднепроходного отверстия. При эвагинации между выпавшей кишкой и кольцом заднего прохода имеется борозда, через которую можно провести палец или зонд в ампулу прямой кишки.
Инвагинация кишечника - симптомы и лечение
Что такое инвагинация кишечника? Причины возникновения, диагностику и методы лечения разберем в статье доктора Чепрасова Владимира Дмитриевича, детского хирурга со стажем в 6 лет.
Над статьей доктора Чепрасова Владимира Дмитриевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Инвагинация кишечника — это внедрение одной части кишки в другую, в результате которого развивается кишечная непроходимость.
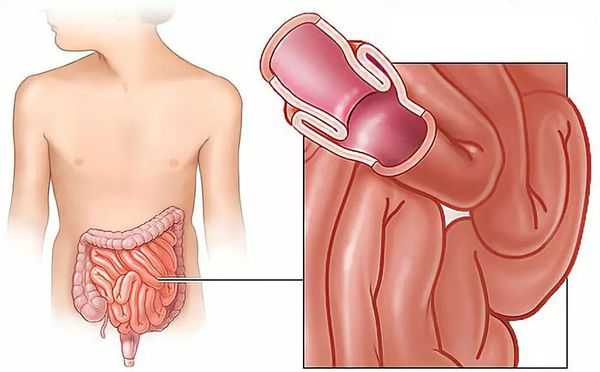
Данное заболевание является комбинированным видом механической непроходимости,так как оно сочетает в себе элементы обтурации (закрытия просвета кишки инвагинатом) и странгуляции (сдавления сосудов, питающих кишку).
Чаще всего к причинам возникновения инвагинации кишечника относят:
- возрастные особенности соединительной ткани у младенцев (крайне подвижный купол слепой кишки и недостаточность илеоцекального клапана, отделяющего тонкую кишку от толстой);
- незрелость нервной системы, которая просто даёт сбой — нарушается баланс между сокращениями продольных и круговых мышц кишки, а также возникает спазм вышележащего и парез (полное расслабление) нижележащего отдела кишки.
Дополнительными факторами риска могут стать:
- вирусные и кишечные инфекции;
- усиленная моторика (например, в ответ на приём слабительных);
- кишечная форма аллергии;
- муковисцидоз;
- туберкулёз брюшины и кишечника.
Также есть предположение, что инвагинацию кишечника может провоцировать именно аденовирусная или ротавирусная инфекция. [2] [3] Они поражают сначала Пейеровы бляшки кишечника, а затем мезентериальные лимфоузлы (лимфоузлы брыжейки тонкой кишки), где происходит размножение вируса. Этот тезис правильнее соотнести с большинством вирусных инфекций, например, с семейством пикорновирусов (вирус Коксаки, энтеровирусы).
Инвагинация кишечника встречается у абсолютно здоровых младенцев в возрасте 4-9 месяцев и является основной причиной кишечной непроходимости (в 85-90% случаев). [1]
У детей старшего возраста эта патология проявляется реже и часто имеет органическое происхождение:
- эмбриональные спайки Лейна (мембрана Джексона);
- энтероптоз — расположение петлей кишечника ниже нормы;
- дивертикул Меккеля — врождённая аномалия подвздошной кишки;
- полипы толстой кишки;
- кишечные удвоения;
- болезнь Геноха (геморрагический васкулит);
- гиперплазия (увеличение) лимфоидной ткани;
- новообразования, в том числе злокачественные.
Мальчики страдают данной патологией чаще девочек почти в два раза.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы инвагинации кишечника
Проявления инвагинации зависят от её вида и продолжительности нарушения. К основным симптомам можно отнести:
- боль в животе;
- плач, беспокойство;
- отказ от еды;
- рвоту;
- выделение из заднего прохода розоватой слизи — симптом "малинового желе".
Заболевание начинается всегда внезапно с выраженного беспокойства, плача и болей в животе: ребёнок поджимает ножки, плачет, отказывается от пищи, игр и предлагаемых предметов. Так же неожиданно боли прекращаются, и ребёнок даже может продолжить играть, принимать пищу, но через некоторое время приступ повторяется.
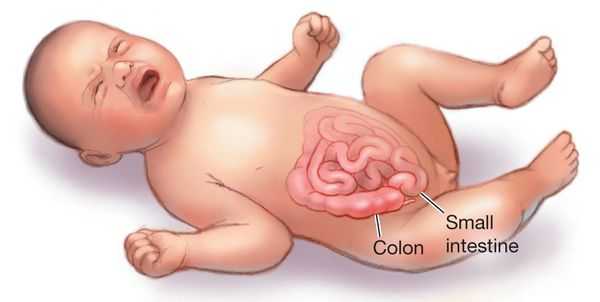
Такой волнообразный характер болей объясняется движением волны кишечной перистальтики: при сокращении круговых мышц влагалища (ущемляющей части) инвагината в стенке (ущемлённой части) инвагината возникает гипоксия, вследствие чего появляется боль. На данном этапе возможна одно- или двукратная рвота рефлекторного характера (на высоте болевого синдрома). У ребёнка может быть нормальный стул, температура, как правило, не поднимается.
Если в период первых приступов ребёнок останется без квалифицированной медицинской помощи, то процесс инвагинации будет развиваться дальше:
- интервалы между "схватками" будут всё короче;
- боль постепенно станет постоянной;
- ребёнок будет бледным, истощённым, плаксивым, адинамичным, станет отказываться от пищи и игр;
- возникнет рвота, которая принесёт кратковременное облегчение или вовсе не облегчит состояние.
ВАЖНО: через некоторое время после приступов вид и поведение ребёнка не будут соответствовать слабому болевому синдрому — такое состояние следует расценивать как крайне тяжёлое, так как при отмирании стенки кишки боль прекращается, а патологический процесс прогрессирует. На этом этапе важным симптомом будет выделение из заднего прохода слизи, окрашенной в розовый цвет. Этот специфичный признак обнаруживается:
- в 70% случаев в первые 12 часов от начала заболевания (причём в 40% случаев — спустя 4 часа);
- в 30% случаев спустя 12 часов после начала заболевания.
В некоторых случаях симптом "малинового желе" не возникает ни в один из периодов болезни. В основном такое бывает в случае слепо-ободочной формы инвагинации. Это связано с отсутствием ущемления и преобладанием закрытия просвета кишки инвагинатом.
Проявления заболевания при слепо-ободочной и толстокишечной формах инвагинации невыразительны:
- нет выраженного беспокойства;
- приступы боли в животе становятся менее интенсивными и протекают с длительными "светлыми" промежуткам;
- рвота возникает только у 20-25% маленьких пациентов.
Патогенез инвагинации кишечника
Инвагинация кишечника чаще всего представляет собой внедрение проксимальной (ближней) части кишки в дистальную (дальнюю). По сути, это нарушение одновременно является и ущемлением части кишки, и закупоркой кишечной трубки, которые в дальнейшем становятся причиной патологических изменений в стенке кишки.
Механизм внедрения одной кишки в другую
В стенке кишки есть Мейсснерово и Ауэрбахово нервные сплетения [5] [6] , которые отвечают за то, чтобы мышцы кишки сокращались и расслаблялись. При введении в пищу незнакомого продукта — прикорма (например, фруктового сока или нового пюре) — происходит раздражение стенок кишки и вышеописанных нервных сплетений. В результате этого возникает спазм вышележащего отдела и парез (расслабление, невозможность сократиться) нижележащего отдела, которые в совокупности дают старт формированию инвагината: под воздействием спастических сокращений стенка кишки постепенно начинает втягиваться в её просвет.
Поскольку вместе с кишечной стенкой внедряется и её питающая часть — брыжейка — возникает замедление и полная остановка кровотока в венозном русле кишки, т. е. венозный стаз. В итоге данные процессы приводят к отёку, артериальной ишемии стенки и отмиранию поражённой кишки. Поэтому крайне важно вовремя распознать нарушения и обратиться к врачу.
Классификация и стадии развития инвагинации кишечника
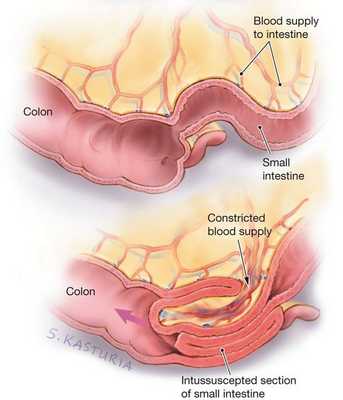
Инвагинация может образоваться на любом отрезке кишечника. По классификации J. Waldschmidt (1990), обычно выделяют три анатомических вида инвагинации кишечника:
- илеоцекальная — внедрение тонкой кишки в ободочную (встречается в 94% случаев);
- тонко-тонкокишечная — внедрение тонкой кишки в тонкую (встречается в 5% случаев);
- толсто-толстокишечная — внедрение толстой кишки в толстую (встречается в 1% случаев).
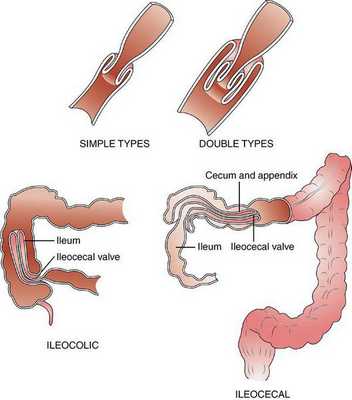
Илеоцекальная инвагинация, в свою очередь, можно разделить на два подвида:
- слепо-ободочная инвагинация — внедрение слепой кишки в восходящую ободочную ("головка" инвагината — слепая кишка);
- подвздошно-ободочная инвагинация — внедрение подвздошной кишки в восходящую ободочную через Баугиневу заслонку ("головка" инвагината — подвздошная кишка).
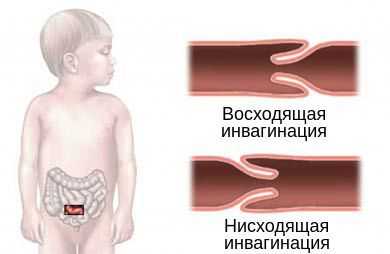
По направлению внедрения инвагината выделяют два типа инвагинации:
- нисходящая инвагинация — вышележащий участок входит в нижележащий (встречается редко);
- восходящая инвагинация — нижележащая часть кишки входит в вышележащую.
Инвагинация может протекать по трём клиническим типам:
- острое течение (в 98,8% случаев) — внедрение кишок, возникающее впервые, с характерным острым началом, сопровождающееся явными проявлениями кишечной непроходимости;
- рецидивирующее течение (в 0,7% случаев) — повторное внедрение кишок с острым началом;
- хроническое течение (в 0,5% случаев) — длительное внедрение кишок, при котором признаки клинической непроходимости выражены слабо.
Осложнения инвагинации кишечника
При длительном закрытии просвета кишки и закупорки сосудов возникнет кишечная непроходимость, а затем некроз (отмирание) стенки ущемлённой кишки. Некроз стенки ущемленной кишки может наступить через:
- 6-12 часов при подвздошно-ободочной инвагинации;
- 12-24 часа при тонкокишечной инвагинации;
- 36-48 часов при толстокишечной инвагинации.
Этот процесс в дальнейшем способен привести к перфорации — образованию отверстия в кишечнике.
Некроз и перфорация кишечника могут стать причиной развития перитонита. На это осложнение будут указывать такие симптомы, как:
- выраженный болевой синдром;
- сначала беспокойство, а потом полное безразличие ребёнка;
- вздутие живота;
- отсутствие отхождения газов и стула;
- выраженное ухудшение общего состояния.
Однако наличие отверстия в кишке редко приводит к развитию перитонита, так как ущемленная и уже некротизированная кишка находится внутри другой здоровой кишки.
Диагностика инвагинации кишечника
Диагностика инвагинации кишечника не вызывает трудностей и включает в себя осмотр, который производится детским хирургом, и инструментальное обследование.
Золотым стандартом считается проведение ультразвукового исследования (сонографии) органов брюшной полости, так как оно является неинвазивным, быстрым, безопасным, безболезненным и высоко информативным методом. [9] [10] При помощи сонографии можно диагностировать инвагинат не только на типичных, но и на атипичных участках кишечника, что повышает точность установления и верификации диагноза.
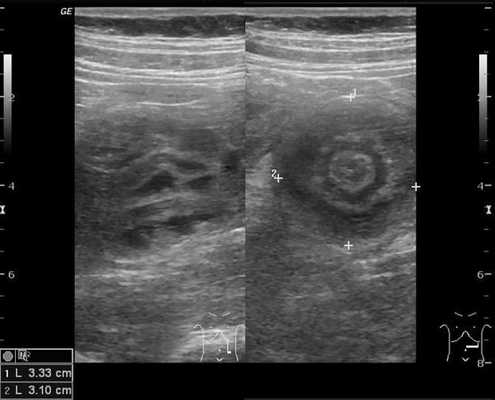
В момент УЗ-исследования врач может определить один из симптомов:
- симптом мишени (за счёт внедрения одной кишки в другую инвагинат на срезе выглядит как мишень);
- симптом "почки с завоздушенным центром".
При осмотре хирург прощупывает живот пациента. Таким образом он может обнаружить характерный симптом слепо-ободочной инвагинации (симптом Данса) — "исчезновение" купола слепой кишки и выявление как бы пустой области правой подвздошной ямки. Дополнительным признаком может быть пальпаторное определение инвагината в брюшной полости в качестве дополнительного образования.
Очень важно произвести ректальное пальцевое исследование. Оно может быть очень информативным, так как с его помощью выявляются такие признаки инвагинации, как:
- расслабленные сфинктеры ануса — симптом Гиршпрунга;
- пальпируемая головка инвагината (при его расположении в сигмовидной кишке);
- эвагинация — выпадение головки инварианта через атоничные сфинкстеры ануса (возникает в тяжёлых случаях при толстокишечной инвагинации).
Также необходимо произвести осмотр содержимого прямой кишки и вышележащих отделов: при инвагинации можно обнаружить слизь малиновой окраски и кровь.
Дополнительными методами могут служить рентгенография органов брюшной полости, компьютерная томография и ирригография.
Лечение инвагинации кишечника
Лечение инвагинации кишечника подразумевает дезинвагинацию — высвобождение ущемленной кишки. Согласно Приказу Министерства здравоохранения РФ № 203 "Об утверждении критериев оценки качества медицинской помощи", лечение инвагинации кишечника должно производится не позже, чем через час после установления диагноза. [7] Дело в том, что патологический процесс в стенке ущемлённой кишки очень опасен. Поэтому важно как можно раньше и максимально быстро произвести дезинвагинацию.
Выделяют два основных принципа лечения инвагинации: хирургический (оперативный) и консервативный.
В случае тяжёлого общего состояния ребёнка необходимо произвести предоперационную подготовку:
- восстановить водно-электролитный баланс;
- снизить гипертермию;
- улучшить микроциркуляцию;
- как можно раньше ввести антибактериальные препараты.
Консервативная терапия
Лечение инвагинации кишечника длительное время было исключительно хирургическим, так как уровень диагностики был низким. На данный момент при отсутствии убедительных данных за перитонит и некроз ущемлённой кишки проводится консервативное лечение с помощью специальной манипуляции — дезинвагинации воздухом. [8] Эта процедура выполняется под общей анестезией и не причиняет ребёнку боль. Суть её заключается в ведении специальной трубки — ректального зонда с подключенной к нему системой нагнетания воздуха и манометром (ректоскопом с подсоединённым баллоном Ричардсона). Под определённым давлением воздух нагнетается в кишечник, и при помощи давления газа инвариант расправляется.
Данный метод считается золотым стандартом консервативного лечения инвагинации кишечника. Его эффективность подтверждена множеством мультицентровых исследований. [11] [12] [13] [14] [15]
Также существует метод гидродезинвагинации, основанный на воздействии гидростатического давления на инвагинат. Он подразумевает применение клизмы с нагнетанием тёплого физраствора или бариевой взвеси под контролем рентген-установки, которая ведёт непрерывную съёмку.
Стоит отметить, что метод с бариевой взвесью, по мнению авторов, имеет один плюс: барий является достаточно плотным и тяжёлым веществом, что может дать больше шансов для консервативной дезинвагинации. Однако в настоящее время данная взвесь не применяется, так как может привести к грозному осложнению: если во время дезинвагинации произойдет прорыв стенки кишки, то бариевая взвесь попадёт в брюшную полость, откуда удалить её будет крайне сложно, что даст толчок к развитию тяжёлого перитонита.
Сама по себе гидродезинвагинация в Федеральных клинических рекомендациях указана как дополнительный метод лечения, но она менее предпочтительна. [8]
Оперативное лечение
Хирургическое лечение инвагинации кишечника проводится значительно реже. Для его проведения существуют чётко сформулированные показания:
- наличие перитонита и верифицированного диагноза "Инвагинация кишечника";
- более 24-48 часов с момента начала заболевания;
- отсутствие эффективности от трёх попыток консервативной дезинвагинации (пневмодезинвагинации).
При наличии соответствующего оборудования и достаточной квалификации хирурга инвагинация устраняется через лапароскопический доступ. Если нет возможности произвести лапароскопическую дезинвагинацию, прибегают к открытой методике, которая уступает лишь в части послеоперационной реабилитации.
Сроки реабилитации крайне индивидуальны и зависят от многих факторов. Принято считать, что после лапароскопического высвобождения ущемлённой кишки реабилитация протекает проще и быстрее за счёт уменьшенного болевого синдрома.
Прогноз. Профилактика
В случае своевременного обращения за медицинской помощью и вовремя проведённого лечения прогноз благоприятный. Скорее всего, о данной проблеме через 1-2 года родители (а уж ребёнок и подавно) не вспомнят, так как последствий никаких нет.
Обычно после пневмодезинвагинации требуется, чтобы ребёнок находился в стационаре в течение 24 часов. Однако если инвагинация кишечника произошла на фоне, например, кишечной инфекции, то необходимо пройти курс стационарного лечения по поводу заболевания, которое привело к инвагинации, так как не устранив проблему можно спровоцировать рецидив инвагинации.
В тяжёлых случаях с некрозом кишки выполняется удаление отмершего участка и производится наложение кишечной стомы (выведение кишки на переднюю брюшную стенку и формирование противоестественного ануса). В этой ситуации прогноз будет зависеть от тяжести исходного и послеоперационного состояния и тяжести септического процесса.
Специфической профилактики инвагинации кишечника не существует, так как её причины обусловлены детским возрастом. Однако снизить риск возникновения данной патологии может правильное введение прикорма. [8]
Аппендэктомия у детей. Операция при инвагинации кишечника у детей
Под нашим наблюдением с 2011 по 2017 год находилось 386 детей с инвагинацией кишечника в возрасте от 4 месяцев до 7 лет. Пациенты проходили стационарное лечение в хирургическом отделении педиатрического корпуса Самарской областной клинической больницы им. В.Д. Середавина. Абсолютное большинство составили дети грудного возраста (224). Из 386 пациентов 251 ребенок поступил в первые сутки заболевания, 96 - на 2-е сутки, 33 - на 3-и, и 6 - на 4-е сутки от начала развития патологии. Кроме клинического обследования, применены ультразвуковое и рентгенологическое исследования. У 314 пациентов успешным оказалось консервативное лечение, у 72 выполнены хирургические вмешательства. 48 больных прооперированы с использованием лапароскопического доступа, 24 пациентам проведена дезинвагинация при лапаротомии. Одному ребенку с подвздошно-ободочной инвагинацией произведена резекция подвздошной кишки в связи с некрозом последней. В двух наблюдениях причиной инвагинации являлся Меккелев дивертикул, у остальных пациентов органических причин не выявлено. Все дети выписаны в удовлетворительном состоянии. Летальных исходов не наблюдалось. Из 386 пациентов у 15 больных отмечалось наличие рецидивирующей инвагинации после проведенного ранее консервативного расправления.
1. Детская хирургия: национальное руководство / под ред. Ю.Ф. Исакова, А.Ф. Дронова. - М.: ГЭОТАР-Медиа, 2009. - 1168 с.
2. Барская М.А. Диагностика и лечение приобретенной кишечной непроходимости у детей: учебное пособие для студентов мед. вузов / Федеральное агентство по образованию; Федеральное агентство по здравоохранению и социальному развитию; Гос. образовательное учреждение высш. проф. образования «Самарский гос. мед. ун-т». - Самара, 2005. - C. 107.
3. Гераськин А.В. Инвагинация кишечника у детей / А.В. Гераськин, А.Ф. Дронов // Медицинский вестник Северного Кавказа. - 2009. - № 1. - С. 25.
5. Юсуфов А.А. Ультразвуковая диагностика инвагинации кишечника / А.А. Юсуфов, Г.Н. Румянцева, В.Н. Карташев // Медицинский вестник Северного Кавказа. - 2009. - Т. 13. - № 1. - С. 99.
Инвагинация кишечника является самым частым видом приобретенной кишечной непроходимости у детей, при этом в абсолютном большинстве данная патология встречается у пациентов грудного возраста 1. Инвагинация кишечника относится к смешанной форме механической непроходимости (сочетание обтурации и странгуляции). К данной патологии приводит дискоординация кишечной перистальтики с образованием участков спазма, что способствует внедрению одного участка кишечника в другой, при этом чаще внедрение происходит по ходу перистальтики. У детей грудного возраста эта патология развивается на фоне анатомо-физиологических особенностей, к которым относятся подвижность подвздошной и слепой кишки, незрелость Баугиниевой заслонки [2; 3]. Именно с этими особенностями связано то, что инвагинация у детей до года чаще всего развивается в области илеоцекального угла. Кроме того, развитию данной патологии способствует возрастная физиологическая незрелость ферментативного аппарата кишечника. Значительная роль в возникновении инвагинации принадлежит нарушению режима вскармливания ребенка и факторам, способствующим изменению перистальтики кишечника - кишечным инфекциям [3].
К инвагинации кишечника приводят и различные органические причины: полипы кишечника, опухоли, удвоение различных отделов кишечника и т.п.
В диагностике кишечной инвагинации, кроме клинического исследования, большое значение отводится ультразвуковому исследованию, которое практически в 100% выявляет данную патологию [4].
Лечение инвагинации у большинства пациентов удается выполнить консервативными методами 4 Показания к операции: наличие перитонита, тонко-тонкокишечной инвагинации и безуспешность консервативного лечения [5].
Цель настоящего исследования - анализ результатов диагностики и лечения инвагинации кишечника у детей.
Материал и методы исследования
В основу работы включен анализ наблюдений за 386 детьми с инвагинацией кишечника в возрасте от 4 месяцев до 7 лет включительно, находящихся на лечении в хирургическом отделении педиатрического корпуса Самарской областной клинической больницы им. В Д. Середавина с 2011 по 2017 год. Мальчиков было 247, девочек - 139 (табл. 1). Наиболее часто инвагинация развивалась у детей до 1 года (224 человека, 58,0%).
Распределение наблюдаемых больных по полу и возрасту
Сроки госпитализации наших пациентов в хирургический стационар значительно колебались. В первые 6 часов от начала заболевания было госпитализировано лишь 11 (2,8%) человек, от 6 до 12 часов - 102 (26,4%) ребенка, от 12 до 24 часов - 138 (35,8%) детей, от 24 до 48 часов 96 (24,9%) детей, и позже 72 часов без хирургической помощи оставались 6 (1,6%) пациентов (рис. 1).
Рис. 1. Давность заболевания к моменту госпитализации в хирургический стационар
Всем больным проводилось клиническое обследование, применялись лабораторные, рентгенологические и ультразвуковые методы исследования.
При сборе анамнеза выявлено наличие погрешности в питании у 48 детей (12,4%). В 23 (6%) наблюдениях инвагинация развилась на фоне острой респираторной инфекции, у 29 (7,5%) пациентов - на фоне кишечной инфекции.
Клинические проявления кишечной инвагинации практически во всех наблюдениях были ярко выраженными.
Приступообразные боли в животе, которые выражались периодическим беспокойством, отмечались у 383 (99%) пациентов. Приступы болей длились от 5 до 15 минут. Промежутки времени между приступами были равны 10-20 минутам. У 322 (83%) больных наблюдалась повторяющаяся рвота, в начале заболевания - содержимым желудка, затем - с примесью желчи, у 11 пациентов отмечалась рвота застойным содержимым. В 86 наблюдениях (22%) отмечалось повышение температуры тела до субфебрильных значений. У 47 (12%) больных наблюдалось выделение крови из заднего прохода, причем у большинства - в виде «малинового желе».
При поступлении в детское хирургическое отделение состояние 45 детей (11,7%) было расценено как удовлетворительное, у 305 (79,0%) - средней тяжести. 39 (10,1%) пациентов поступили в стационар в тяжелом состоянии. Тяжелое состояние отмечено у детей, поступивших в стационар в сроки от начала заболевания более 48 часов.
Вздутие живота определялось у 115 детей (29,8%). Инвагинат пальпировался в виде опухолевидного подвижного, цилиндрической формы, умеренно болезненного образования в 223 наблюдениях (57,8%). Наличие симптома Данса отмечено в истории болезни 89 детей (23%). У 350 (90,6%) больных живот при пальпации был мягким, у 36 (9,4%) детей определялось напряжение мышц передней брюшной стенки.
В общем анализе крови у 331 ребенка количество лейкоцитов не превышало 10,0х109/л, у 21 пациента отмечался лейкоцитоз от 12,0 до 15,0х109/л, в 34 наблюдениях - от 16,0 до 25,0 х109/л (эти дети поступили в стационар позже 48 часов от начала заболевания, при этом 6 больных из них поступили позже 72 часов).
Всем наблюдаемым детям выполнено ультразвуковое исследование органов брюшной полости. 312 пациентам (81%) ультразвуковое исследование было дополнено рентгенологическим - ирригографией.
На рисунках 2 и 3 отображена ультразвуковая картина кишечной инвагинации.
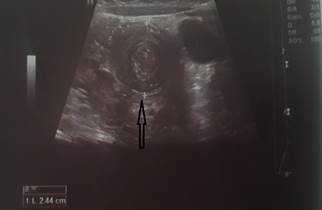
Рис. 2. Симптом «мишени»
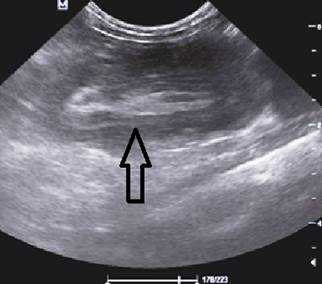
Рис. 3. Симптом «псевдопочки»
На рисунках 4 и 5 представлена картина кишечной инвагинации при рентгенологическом исследовании.
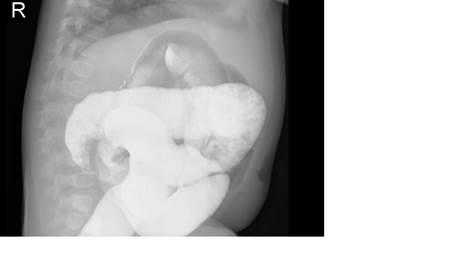
Рис. 4. Ирригограмма при тугом наполнении взвесью сульфата бария - симптом «клешней рака»
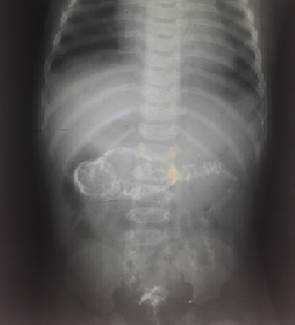
Рис. 5. Ирригограмма после опорожнения толстой кишки - симптом «кокарды»
ЛЕЧЕНИЕ. У 312 больных (80,8%) кишечная инвагинация устранена консервативно, у 2 больных (0,5%) инвагинация расправилась самопроизвольно. 72 ребенка (18,7%) оперированы. Показания к оперативному лечению были следующими:
- клинические признаки перитонита;
- тонко-тонкокишечная инвагинация (диагностирована при УЗИ);
- безуспешность консервативного лечения.
У 187 детей дезинвагинация произошла во время выполнения ирригографии.
В 125 наблюдениях инвагинация устранена при нагнетании в толстую кишку воздуха с контролем создаваемого давления. Этот метод используется нами у детей любого возраста. Для введения в прямую кишку воздуха мы применяем интубационную трубку (трубку для интубации трахеи), размер которой подбирается в зависимости от возраста ребенка. Трубка с помощью переходника соединяется с манометром и баллоном Ричардсона (рис. 6). Преимуществом данного устройства является наличие манжетки, которая позволяет создать герметизм при нагнетании воздуха в толстую кишку.
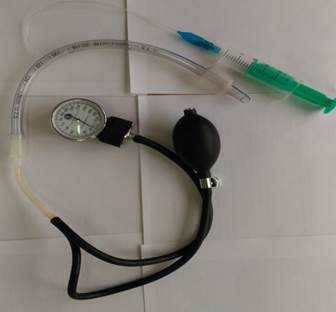
Рис. 6. Устройство для консервативного расправления инвагинации
Консервативная дезинвагинация проводится в операционной под общим обезболиванием. Перед манипуляцией необходимо произвести пальпацию живота для определения инвагината. Затем в прямую кишку пациента вводится интубационная трубка, после чего раздувается манжетка с целью создания герметизма во время нагнетания в кишку воздуха.
С помощью баллона Ричардсона начинается нагнетание воздуха, при этом отслеживается поступление воздуха в толстую кишку: в начале наблюдается асимметрия живота при прохождении воздуха до инвагината, при дальнейшем нагнетании воздуха при условии расправления инвагината живот становится симметричным в связи с прохождением воздуха в проксимальные отделы кишечника. В это время пальпаторно инвагинат перестает определяться. Затем от трубки отсоединяется баллон Ричардсона для удаления избыточного воздуха из кишечника. Ребенок помещается в палату. После полного пробуждения пациента выполняется обзорная рентгенография брюшной полости, на которой отмечается наличие газа как в толстой, так и в тонкой кишке.
В 26 наблюдениях консервативная дезинвагинация была безуспешной. Эти дети оперированы.
У 15 детей после пневмодезинвагинации и у 24 пациентов после дезинвагинации посредством ирригографии отмечен рецидив инвагинации. Эти дети оперированы.
Читайте также:
