Диагностика и дифференциация гигантизма. Лечение гипофизарного гиганта
Добавил пользователь Алексей Ф. Обновлено: 02.02.2026
Обслуживание на двух языках: русский, английский.
Оставьте свой номер телефона, и мы обязательно перезвоним вам.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначить только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Статья проверена врачом-эндокринологом, к.м.н. Мирной С.С., носит общий информационный характер, не заменяет консультацию специалиста.
Для рекомендаций по диагностике и лечению необходима консультация врача.
Акромегалия и гигантизм — хронические заболевания, возникающие вследствие чрезмерной секреции гипофизом гормона роста.
Акромегалия развивается преимущественно у взрослых людей; гигантизм проявляется уже в детском возрасте.
Причины и патогенез акромегалии и гигантизма
Итак, основная причина заболеваний — повышенный синтез гипофизом гормона роста соматотропина. Это может быть обусловлено как патологией самого гипофиза (опухоль, в том числе аденома, аномальное разрастание и др.), так и нарушениями его функций при поражении близко расположенных тканей (опухоли, метастазы).
Среди факторов риска развития акромегалии и гигантизма — инфекционные заболевания, черепно-мозговые травмы, хроническое воспаление носовых пазух, наследственность.
Симптомы акромегалии и гигантизма
Акромегалия характеризуется прогрессирующим патологическим увеличением различных частей тела — кистей, стоп, грудной клетки, нижней челюсти, внутренних органов, огрубением черт лица, утолщением кожи.
Рост больных гигантизмом достигает 2 метров и более при непропорциональном телосложении; обычно удлиняются конечности.
Избыточная секреция гормона роста вызывает изменения в костях, мягких тканях, сказывается на метаболизме.
Пациенты жалуются на нарушение зрения, головную боль, головокружение, повышенную потливость, боли в суставах, снижение потенции, нарушение менструального цикла и др. Голос становится хриплым и низким, развивается гипертония, сердечная недостаточность, тиреотоксикоз, мышечная слабость, артрозы.
Диагностика и лечение акромегалии и гигантизма в Клиническом госпитале на Яузе
Опытный специалист может определить патологию по внешнему виду пациента.
Но для уточнения диагноза необходимы лабораторная и инструментальная диагностики:
- общий и биохимический анализы крови
- общий анализ мочи
- комплекс гормональных исследований (ТТГ, СТГ, ИФР-1, пролактин и др.)
- ЭХО-КГ (эхокардиография)
- МРТ-головы
- Rg-графия черепа в двух проекциях, позвоночника, кистей и стоп
Для лечения акромегалии и гигантизма, целью которого является достижение стойкой ремиссии, специалисты отделения эндокринологии нашей клиники применяют самые современные лекарственные препараты, способные отсрочить оперативное вмешательство.
Цены на услуги Вы можете посмотреть в прайсе или уточнить по телефону, указанному на сайте.
Цены на услуги эндокринолога
- Стандартные консультации
- Прием (осмотр, консультация) врача-эндокринолога первичный 3 900 руб.
- Прием (осмотр, консультация) врача-эндокринолога повторный 3 500 руб.
- Первичный прием врача-эндокринолога Катамадзе Н. Н. 2 300 руб.
- Консультации экспертов
- Прием (осмотр, консультация) ведущего врача-эндокринолога первичный 5 900 руб.
- Прием (осмотр, консультация) ведущего врача-эндокринолога повторный 5 500 руб.
- Телеконсультации
- Удаленная консультация врача-эндокринолога первичная 2 500 руб.
- Удаленная консультация врача-эндокринолога повторная 2 500 руб.
- Обследования
- Установка датчика мониторирования глюкозы, с учетом стоимости датчика FreeStyle Librе 7 000 руб.
- Проведение мониторирования глюкозы с установкой датчика, обучением пользованию, расшифровкой и анализом данных системой FreeStyle Libre (7 дней), без стоимости сенсора 10 000 руб.
- Проведение мониторирования глюкозы с установкой датчика, обучением пользованию, расшифровкой и анализом данных системой FreeStyle Libre (14 дней), без стоимости сенсора 15 000 руб.
- Биоимпедансометрия 3 000 руб.
- Эндоскопия
- Капсульная эндоскопия 60 000 руб.
Внимание! Цены на сайте могут отличаться.
Пожалуйста, уточняйте актуальную стоимость у администраторов по телефону.
Наши специалисты:

КимЕкатерина Игоревна Врач-эндокринолог
Стоимость приема: 3900 ₽

КатамадзеНино Николаевна Врач-эндокринолог
Стоимость приема: 2300 ₽

МирнаяСветлана Сергеевна Врач-эндокринолог Кандидат медицинских наук
Стоимость приема: 5900 ₽

БелозерскаяНина Петровна Врач-эндокринолог, диетолог
Стоимость приема: 3900 ₽
Опухоли гипофиза
Опухоли гипофиза - группа доброкачественных, реже - злокачественных новообразований передней доли (аденогипофиза) или задней доли (нейрогипофиза) железы. Опухоли гипофиза, по статистике, составляют около 15% новообразований внутричерепной локализации. Они одинаково часто диагностируются у лиц обоих полов, обычно в возрасте 30-40 лет. Подавляющее большинство опухолей гипофиза составляют аденомы, которые подразделяются на несколько видов в зависимости от размеров и гормональной активности. Симптомы опухоли гипофиза представляют собой сочетание признаков объемного внутримозгового процесса и гормональных нарушений. Диагностика опухоли гипофиза осуществляется проведением целого ряда клинических и гормональных исследований, ангиографии и МРТ головного мозга.
Общие сведения
Опухоли гипофиза - группа доброкачественных, реже - злокачественных новообразований передней доли (аденогипофиза) или задней доли (нейрогипофиза) железы. Опухоли гипофиза, по статистике, составляют около 15% новообразований внутричерепной локализации. Они одинаково часто диагностируются у лиц обоих полов, обычно в возрасте 30-40 лет.
Гипофиз является железой внутренней секреции, осуществляющей регулятивно-координирующую функцию в отношении некоторых других эндокринных желез. Гипофиз расположен в ямке турецкого седла клиновидной кости черепа, анатомически и функционально связан с отделом головного мозга - гипоталамусом. Вместе с гипоталамусом гипофиз составляет единую нейроэндокринную систему, обеспечивающую постоянство гомеостаза организма.
В гипофизе выделяют две доли: переднюю - аденогипофиз и заднюю - нейрогипофиз. Гормонами передней доли, вырабатываемыми аденогипофизом, являются: пролактин, стимулирующий секрецию молока; соматотропный гормон, влияющий на рост организма через регуляцию белкового обмена; тиреотропный гормон, стимулирующий метаболические процессы в щитовидной железе; АКТГ, регулирующий функцию надпочечников; гонадотропные гормоны, влияющие на развитие и функцию половых желез. В нейрогипофизе образуются окситоцин, стимулирующий сократительную способность матки, и антидиуретический гормон, регулирующий процесс реабсорбции воды в канальцах почек.
Аномальное разрастание клеток железы приводит к образованию опухолей переднего или заднего отдела гипофиза и нарушению гормонального баланса. Иногда в область гипофиза прорастают менингиомы - опухоли мозговых оболочек; реже железа поражается метастатическими отсевами злокачественных новообразований других локализаций.
Причины опухолей гипофиза
Достоверные причины развития опухолей гипофиза до конца не изучены, хотя известно, что некоторые виды новообразований могут быть обусловлены генетически.
В число факторов, предрасполагающих к развитию опухолей гипофиза, входят нейроинфекции, хронические синуситы, черепно-мозговые травмы, гормональные изменения (в том числе вследствие длительного применения гормональных препаратов), неблагоприятное воздействие на плод в период беременности.
Классификация опухолей гипофиза
Опухоли гипофиза классифицируются с учетом их размеров, анатомического расположения, эндокринных функций, особенностей микроскопического окрашивания и т. д. В зависимости от размера новообразования выделяют микроаденомы (менее 10 мм в максимальном диаметре) и макроаденомы (при наибольшем диаметре более 10 мм) гипофиза.
По локализации в железе различают опухоли аденогипофиза и нейрогипофиза. Опухоли гипофиза по топографии относительно турецкого седла и окружающих его структур бывают эндоселлярными (выходящими за границы турецкого седла) и интраселлярными (расположенными в пределах турецкого седла). С учетом гистологической структуры опухоли гипофиза подразделяются на злокачественные и доброкачественные новообразования (аденомы). Аденомы исходят из железистой ткани передней доли гипофиза (аденогипофиза).
По функциональной активности опухоли гипофиза делятся на гормонально-неактивные («немые», инсиденталомы) и гормонально-активные аденомы (вырабатывающие тот или иной гормон), которые встречаются в 75% случаев. Среди гормонально-активных опухолей гипофиза выделяют:
- соматотропная аденома
- соматотропинома - опухоль гипофиза, синтезирующая соматотропин - гормон роста;
- пролактиновая аденома
- пролактинома - опухоль гипофиза, синтезирующая гормон пролактин;
- кортикотропная аденома
- кортикотропинома - опухоль гипофиза, секретирующая АКТГ, стимулирующий функцию коры надпочечников;
- тиротропная аденома
- тиротропинома - опухоль гипофиза, секретирующая тиротропный гормон, стимулирующий функцию щитовидной железы;
Фоллтропинпродуцирующие или лютропинпродуцирующие аденомы (гонадотропные). Эти опухоли гипофиза секретируют гонадотропины, стимулирующие функцию половых желез.
Гормонально-неактивные опухоли гипофиза и пролактиномы встречаются наиболее часто (в 35% случаев соответственно), соматотропинпродуцирующие и АКТГ-продуцирующие аденомы - в 10-15% случаев от всех опухолей гипофиза, другие виды опухолей образуются редко. По особенностям микроскопии различают хромофобные опухоли гипофиза (гормонально-неактивные аденомы), ацидофилиные (пролактиномы, тиротропиномы, соматотропиномы) и базофильные (гонадотропиномы, кортикотропиномы).
Развитие гормонально-активных опухолей гипофиза, продуцирующих один или несколько гормонов, может приводить к развитию центрального гипотиреоза, синдрома Кушинга, акромегалии или гигантизма и т. д. Повреждение гормонопродуцирующих клеткок при росте аденомы может вызывать состояние гипопитуаризма (гипофизарной недостаточности). У 20% пациентов отмечается бессимптомное течение опухолей гипофиза, которые обнаруживаются лишь при аутопсии. Клинические проявления опухолей гипофиза зависят от гиперсекреции того или иного гормона, размеров и скорости роста аденомы.
Симптомы опухолей гипофиза
По мере увеличения опухоли гипофиза развиваются симптомы со стороны эндокринной и нервной систем. Соматотропинпродуцирующие аденомы гипофиза приводят к возникновению акромегалии у взрослых пациентов или гигантизма, если они развиваются у детей. Пролактинсекретирующие аденомы характеризуются медленным ростом, проявляются аменореей, гинекомастией и галактореей. Если такие опухоли гипофиза продуцируют неполноценный пролактин, то клинические проявления могут отсутствовать.
АКТГ-продуцирующие аденомы стимулируют секрецию гормонов коры надпочечников и ведут к развитию гиперкортицизма (болезни Кушинга). Обычно такие аденомы растут медленно. Тиротропинпродуцирующие аденомы нередко сопровождают течение гипотиреоза (функциональной недостаточности щитовидной железы). Они могут вызывать упорный тиреотоксикоз, чрезвычайно устойчивый к медикаментозному и хирургическому лечению. Гонадотропные аденомы, синтезирующие половые гормоны, у мужчин приводят к развитию гинекомастии и импотенции, у женщин - к нарушению менструального цикла и маточным кровотечениям.
Увеличение размеров опухоли гипофиза ведет к развитию проявлений со стороны нервной системы. Поскольку гипофиз анатомически соседствует с перекрестом зрительных нервов (хиазмом), то при увеличении размеров аденомы до 2 см в диаметре развиваются зрительные нарушения: сужение полей зрения, отек сосочков зрительного нерва и его атрофия, ведущие к падению зрения, вплоть до слепоты.
Аденомы гипофиза больших размеров вызывают сдавление черепных нервов, сопровождающееся симптомами поражения нервной системы: головные боли; двоение в глазах, птоз, нистагм, ограничение движений глазных яблок; судороги; упорный насморк; деменцию и изменения личности; повышение внутричерепного давления; кровоизлияния в гипофиз с развитием острой сердечно-сосудистой недостаточности. При вовлеченности в процесс гипоталамуса могут наблюдаться эпизоды нарушения сознания. Злокачественные опухоли гипофиза встречаются крайне редко.
Диагностика опухолей гипофиза
Необходимыми исследованиями при подозрении на опухоль гипофиза являются тщательное офтальмологическое и гормональное обследования, нейровизуализация аденомы. Исследование мочи и крови на содержание гормонов позволяет установить вид опухоли гипофиза и степень ее активности. Офтальмологическое обследование включает оценку остроты и полей зрения, позволяющих судить о вовлеченности в процесс зрительных нервов.
Нейровизуализацию опухоли гипофиза позволяет осуществить рентгенография черепа и зоны турецкого седла, МРТ и КТ головного мозга. Рентгенологически могут определяться увеличение размеров турецкого седла и эрозия его дна, а также увеличение нижней челюсти и пазух носа, утолщение костей черепа, и расширение межзубных промежутков. С помощью МРТ головного мозга возможно увидеть опухоли гипофиза диаметром менее 5 мм. Компьютерная томография подтверждает наличие аденомы и ее точные размеры.
При макроаденомах ангиография сосудов головного мозга указывает на смещение сонной артерии и позволяет дифференцировать опухоль гипофиза с внутричерепной аневризмой. В анализе спинномозговой жидкости может определяться повышенный уровень протеинов.
Лечение опухолей гипофиза
На сегодняшний день в лечении опухолей гипофиза эндокринология применяет хирургический, лучевой и лекарственный методы. Для каждого вида опухолей гипофиза существует специфический, наиболее оптимальный вариант лечения, который подбирается эндокринологом и нейрохирургом. Наиболее эффективным считается хирургическое удаление опухоли гипофиза. В зависимости от размеров и локализации аденомы проводится либо ее фронтальное удаление через оптический прибор, либо резекция через клиновидную кость черепа. Оперативное удаление опухолей гипофиза дополняется лучевой терапией.
Гормонально-неактивные микроаденомы лечатся с помощью лучевой терапии. Проведение лучевой терапии показано при наличии противопоказаний к оперативному лечению, а также пожилым пациентам. В послеоперационном периоде проводится гормонозаместительная терапия (кортизоном, тиреоидными или половыми гормонами), при необходимости - коррекция электролитного обмена и инсулинотерапия.
Из лекарственных препаратов используют агонисты дофамина (каберголин, бромокриптин), вызывающие сморщивание пролактин- и АКТГ-секретирующих опухолей гипофиза, а также ципрогептадин, понижающий уровень кортикостероидов у пациентов с синдромом Кушинга. Альтернативным методом лечения опухолей гипофиза является замораживание участка ткани железы при помощи зонда, введенного через клиновидную кость.
Прогноз при опухолях гипофиза
Дальнейший прогноз при опухолях гипофиза во многом определяется размерами аденом, возможностью их радикального удаления и гормональной активностью. У пациентов с пролактиномами и соматотропиномами полное восстановление гормональной функции наблюдается в четверти случаев, при адренокортикотропинпродуцирующих аденомах - в 70-80% случаев.
Макроаденомы гипофиза размером более 2 см полностью удалить невозможно, поэтому возможны их рецидивы в течение 5-летнего срока после операции.
Гигантизм
Гигантизм - патологическая высокорослость, обусловленная чрезмерной выработкой гормона роста (соматотропного гормона) передней долей гипофиза и проявляющаяся уже в детском возрасте. Наблюдается увеличение роста свыше 2 м, непропорциональность телосложения с преимущественным удлинением конечностей, при этом голова кажется очень маленькой. У больных наблюдается расстройство физического и психического состояния, половой функции. При гигантизме трудоспособность ограничена, высок риск бесплодия. Основным диагностическим критерием гигантизма, помимо яркой клинической картины, является выявление повышения СТГ в крови.
Гигантизм (или макросомия) развивается у детей с незавершенными процессами окостенения скелета, чаще встречается у подростков мужского пола, определяется уже в возрасте 9-13 лет и прогрессирует на протяжении всего периода физиологического роста. При гигантизме скорость роста ребенка и его показатели намного превышают анатомо-физиологическую норму и к концу пубертатного периода достигают более 1,9 м у женщин и 2 м у мужчин при сохранении относительно пропорционального телосложения. Частота встречаемости гигантизма составляет от 1 до 3 случаев на 1000 населения.
Родители пациентов, страдающих данной патологией, обычно нормального роста. Гигантизм следует дифференцировать с наследственной высокорослостью.
Классификация гигантизма
Современная эндокринология выделяет следующие варианты развития гигантизма:
- Акромегалический - гигантизм с признаками акромегалии;
- спланхномегалия или гигантизм внутренних органов - сопровождается увеличением размеров и массы внутренних органов;
- евнухоидный - гигантизм у пациентов с гипогонадизмом (гипофункцией или полным прекращением функций половых желез), проявляется непропорционально удлиненными конечностями, открытыми зонами роста в суставах, отсутствием вторичных половых признаков;
- истинный - характеризуется пропорциональным увеличением размеров тела и отсутствием отклонений со стороны физиологических и психических функций;
- парциальный или частичный - гигантизм с увеличением отдельных частей тела;
- половинный - гигантизм, сопровождающийся увеличением одной половины туловища;
- церебральный - гигантизм, вызванный органическим поражением головного мозга и сопровождающийся нарушением интеллекта.
Причины гигантизма
Гигантизм и акромегалия являются двумя возрастными вариациями одних и тех же патологических процессов: гиперплазии и гиперфункции клеток гипофиза, продуцирующего соматотропный гормон (гормон роста). Повышенная секреция гормона роста может наблюдаться при поражениях гипофиза в результате опухолей железы (аденомы гипофиза), интоксикации, нейроинфекций (энцефалита, менингита, менингоэнцефалита), черепно-мозговых травм.
Нередко причиной гигантизма служит понижение чувствительности эпифизарных хрящей, обеспечивающих рост костей в длину, к воздействию половых гормонов. В результате этого кости долго сохраняют способность увеличения в длину, даже в постпубертатном периоде. Гиперсекреция соматотропина после закрытия зон роста костей и завершения окостенения скелета приводит к акромегалии.
Симптомы гигантизма
Скачок увеличения длины тела при гигантизме происходит в 10-15 лет. Пациенты отличаются высоким ростом и темпами его увеличения, жалуются на быструю утомляемость и слабость, головокружения, головные боли, ухудшение зрения, боли в суставах и костях. Снижение памяти и работоспособности ведет к ухудшению успеваемости в школе. Гигантизм характеризуется гормональными нарушениями, расстройством психической и половой функции (инфантилизм). У женщин при гигантизме развивается первичная аменорея или раннее прекращение менструальной функции, бесплодие, у мужчин - гипогонадизм. Другими гормональными проявлениями гигантизма служат несахарный диабет, гипо- или гипертиреоз, сахарный диабет. Отмечается сначала увеличение мышечной силы, а затем мышечная слабость и астения.
При гигантизме возможно развитие артериальной гипертензии, миокардиодистрофии, сердечной недостаточности, эмфиземы легких, дистрофических изменений печени, бесплодия, сахарного диабета, нарушений функции щитовидной железы.
Диагностика гигантизма
Диагноз гигантизма устанавливается на основании внешнего осмотра пациента, результатов лабораторных, рентгенологических, неврологических и офтальмологических исследований. При гигантизме лабораторно определяется высокое содержание СТГ в крови.
Для выявления опухолей гипофиза проводится рентгенография черепа, КТ и МРТ головного мозга. При наличии аденомы гипофиза определяется увеличенное турецкое седло (ложе гипофиза). Рентгенограммы кистей рук показывают несоответствие между костным и паспортным возрастом. При офтальмологическом обследовании пациентов с гигантизмом выявляется ограничение зрительных полей, застойные явления в глазном дне.
Лечение гигантизма
Принципы лечения гигантизма аналогичны лечению акромегалии. Для нормализации уровня гормона роста при гигантизме применяются аналоги соматостатина, для более быстрого закрытия зон роста костей - половые гормоны. Этиологическое лечение гигантизма при аденомах гипофиза предусматривает применение лучевой терапии или их оперативное удаление в сочетании с медикаментозной поддержкой агонистами дофамина.
При евнухоидном типе гигантизма лечение направлено на устранение полового инфантилизма, ускорение окостенения скелета и прекращение его дальнейшего роста. Лечение частичного гигантизма включает ортопедическую коррекцию при помощи пластических операций. Применяемое эндокринологами комбинированное лечение гигантизма сочетает гормональную и лучевую терапию и позволяет добиться положительных результатов у значительного числа пациентов.
Прогноз и профилактика гигантизма
При адекватной терапии гигантизма прогноз для жизни относительно благоприятный. Однако, многие пациенты не доживают до старости и погибают от осложнений заболевания. Большинство пациентов, страдающих гигантизмом, бесплодны, их трудоспособность резко снижена.
Обеспокоенность родителей должно вызывать резкое, значительное увеличение роста ребенка в период полового созревания по сравнению с его сверстниками. Своевременное медицинское вмешательство позволит предотвратить осложнения.
Гипофизарный нанизм (карликовость) - симптомы и лечение
Что такое гипофизарный нанизм (карликовость)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скворцовой Ольги Викторовны, детского эндокринолога со стажем в 9 лет.
Над статьей доктора Скворцовой Ольги Викторовны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Гипофизарный нанизм, или гипопитуитаризм — это заболевание, при котором частично или полностью прекращается выработка гормона роста — соматотропина (соматотропного гормона) [1] . Оно сопровождается нарушением роста скелета, из-за чего мужчины не вырастают выше 130 см, а женщины — выше 120 см. В связи с этим характерным проявлением болезнь также называют карликовостью.
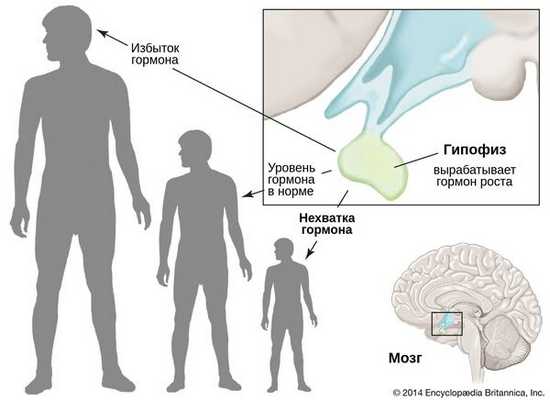
Наиболее частые причины гипофизарного нанизма:
- Наследственность — мутации в гене соматотропного гормона (GH1) или его рецепторах. Частота встречаемости врождённого гипопитуитаризма колеблется от 1:4000 до 1:10000 [5] .
- Дефекты развития гипоталамо-гипофизарной системы — области головного мозга, где вырабатывается соматотропный гормон:
- гипоплазия (недоразвитие) гипофиза;
- полное отсутствие гипофиза. При этом дефицит гормона роста сочетается с нехваткой других гормонов, которые вырабатываются в гипофизе. Такое состояние называется пангипопитуитаризмом. Оно проявляется надпочечниковой недостаточностью, ухудшением работы щитовидной железы (гипотиреозом), несахарным диабетом, гипогонадотропным гипогонадизмом (отсутствием полового развития и дефицитом гормона роста).
- Опухоли гипофиза:
- краниофарингиома — доброкачественная опухоль гипофизарной области, одна из самых распространённых в детском возрасте;
- гамартома — редкий вид доброкачественной опухоли;
- герминома — редкий вид опухоли, чаще всего бывает злокачественной — и др.
- Травмы головного мозга с повреждением гипофиза, возникшие до того, как человек достиг социально приемлемого роста — 155-170 см (например, родовая травма).
- Инфекционные заболевания — менингиты, энцефалиты и др.
- Облучение головы и шеи.
- Токсические последствия химиотерапии.
Теоретически, спровоцировать развитие гипофизарного нанизма может любое заболевание, которое будет затрагивать работу гипофиза.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гипофизарного нанизма
Гипофизарный нанизм проявляется по-разному. Симптоматика зависит от причин дефицита гормона роста.
Основной симптом — отставание в темпах линейного роста [2] . Такие дети вырастают менее чем на 4 см в год. Нарушение динамики роста будет заметно уже в первые месяцы жизни ребёнка. Если повреждение гипоталамуса или гипофиза возникло в более позднем возрасте, то отставание в росте будет отмечаться позднее. Также для детей с гипофизарным нанизмом характерно отставание костного (биологического) возраста от паспортного (фактического) более чем на 2-3 года.
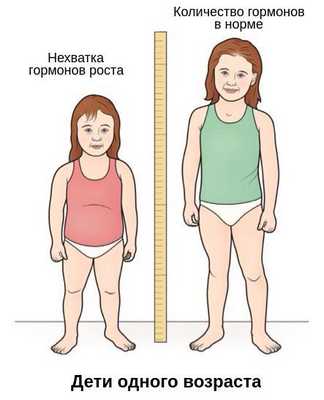
При нехватке гормонов роста телосложение остаётся пропорциональным. Это важный диагностический критерий: он позволяет исключить разные формы скелетных дисплазий [9] .
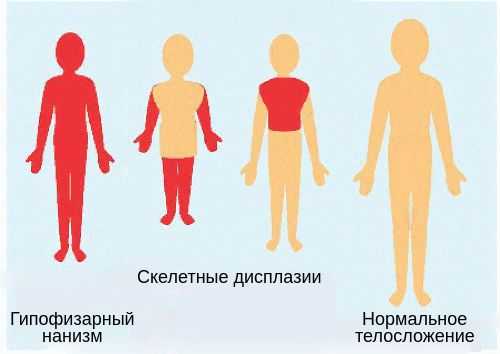
Симптомами врождённого гипофизарного нанизма у новорождённых являются:
- гипогликемия — низкий уровень глюкозы в крови натощак. Это физиологическое состояние может встречаться и у здоровых детей из-за незрелости поджелудочной железы. Дети с нанизмом сталкиваются с ним гораздо чаще, особенно на первом году жизни, поскольку гормон роста участвует в регуляции углеводного обмена;
- позднее закрытие большого родничка;
- задержка костного созревания;
- истончение кожи — может быть связано со снижением функции щитовидной железы;
- медленный рост ногтей и волос;
- высокий голос.
Часто у детей с гипопитуитаризмом встречается множественный кариес зубов. Это объясняется задержкой окостенения скелета и снижением обменных процессов в костной ткани.
Психоинтеллектуальное развитие у детей с гипофизарным нанизмом, как правило, не страдает, но возможны некоторые психологические проблемы: повышенная потребность в родительской опеке, снижение самооценки, трудности в общении со сверстниками.
Патогенез гипофизарного нанизма
В зависимости от причин дефицита соматотропного гормона есть несколько вариантов механизмов развития заболевания. При этом в основе патогенеза всегда будет лежать нарушение выработки гормона роста. В дальнейшем его нехватка станет причиной нарушения работы органов и систем, на которые он оказывает влияние: костной, мышечной и соединительной ткани, жирового углеводного обмена. В некоторых случаях первоначально будут развиваться гипоталамические нарушения, а недостаточность соматотропного гормона станет вторичным проявлением.
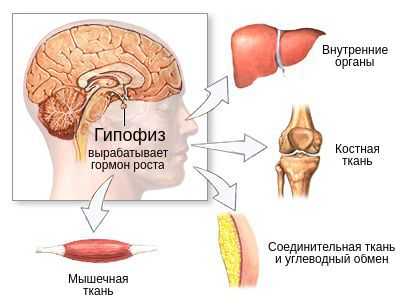
Молекулярной основой изолированного дефицита гормона роста является мутация определённого гена, которая не даёт организму синтезировать гормон. От видов генетических мутаций зависит, будет ли дефицит соматотропного гормона изолированным, или же он будет сочетаться с нехваткой других гормонов гипофиза, которые лежат в основе других патологий:
- дефицит тиреотропного гормона — вторичный гипотиреоз;
- дефицит пролактина — гипопролактинемия;
- дефицит гонадотропинов — аменорея и недоразвитие половых органов у женщин, снижение потенции и либидо у мужчин;
- дефицит АКТГ — вторичная недостаточность надпочечников;
- дефицит вазопрессина — несахарный диабет;
- дефицит кортизола — гипокортицизм.
У некоторых пациентов с мутацией конкретных генов выявляется гиперплазия передней доли гипофиза (аденогипофиза). В процессе жизни может произойти её атрофия вплоть до формирования синдрома "пустого турецкого седла" — недостаточности области головного мозга, где расположен гипофиз. Данный синдром приводит к внедрению мягкой мозговой оболочки в полость турецкого седла, сдавлению и уменьшению гипофиза, что нарушает или полностью прекращает его работу.
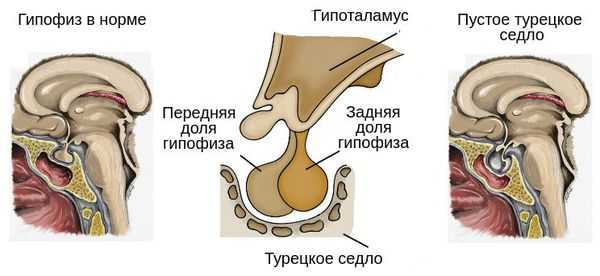
В подобных случаях дефицит гормона роста и других гормонов гипофиза будет возникать постепенно [3] .
Классификация и стадии развития гипофизарного нанизма
Единой, общепринятой классификации гипофизарного нанизма не существует. Наиболее удобной для практикующих врачей является классификация, основанная на причинах заболевания. Она выделяет две большие группы: врождённый и приобретённый гипопитуитаризм [4] .
Врождённый гипофизарный нанизм делится на три подгруппы:
- Наследственный:
- изолированный дефицит гормона роста: мутации гена самого гормона (GH1) или мутации гена рецептора к соматотропину (GHRHR);
- множественный дефицит гормонов передней доли гипофиза: мутации гена PIT-1 или гена PROP1.
- Идиопатический (незафисимый) дефицит СТГ-релизинг гормонов, которые стимулируют выработку гормонов передней доли гипофиза.
- Дефекты развития гипоталамо-гипофизарной системы:
- патология срединной трубки;
- нарушение развития гипофиза: врождённая аплазия (отсутствие гипофиза), гипоплазия (недоразвитие), эктопия (неправильное расположение).
Приобретённый гипофизарный нанизм включает в себя девять причин развития болезни:
- Опухоли гипоталамуса и гипофиза: краниофарингиома, гамартома, нейрофиброма, герминома, аденома гипофиза.
- Опухоли других отделов мозга: глиома зрительного перекреста.
- Травмы: черепно-мозговая, хирургическое повреждение ножки гипофиза.
- Инфекционные заболевания: вирусный, бактериальный энцефалит и менингит, неспецифический гипофизит (воспаление гипофиза).
- Супраселлярные арахноидальные кисты — полые опухоли, заполненные жидкостью (ликвором), которые распространяются в полость черепа.
- Сосудистые нарушения: аневризмы сосудов гипофиза, инфаркт гипофиза.
- Облучение головы и шеи по поводу лейкемии, медуллобластомы, ретинобластомы; общее облучение всего тела (при пересадке костного мозга).
- Токсические последствия химиотерапии.
- Инфильтративные болезни: саркоидоз, гистиоцитоз.
Осложнения гипофизарного нанизма
Осложнения заболевания связаны с утратой воздействия гормона роста на органы и системы. Они развиваются вследствие несвоевременной диагностики.
У новорождённого с дефицитом соматотропина относительную опасность может представлять гипогликемическое состояние, поскольку этот гормон играет важную роль в регуляции углеводного обмена. Клинически гипогликемия проявляется бледностью, потливостью, повышенным аппетитом, беспокойством ребёнка, иногда наблюдается судорожный синдром [5] .

Так как сомтатотропин усиливает синтез белка и тормозит его распад, у детей с дефицитом этого гормона может снизиться уровень общего белка в организме и его фракций. Это сказывается на общем физическом развитии: снижается иммунитет, повышается риск присоединения других гормональных сопутствующих нарушений.
Значительная часть эффектов гормона роста передаётся через ИПФР-I (инсулиноподобный фактор роста-I). Он вырабатывается в печени под действием соматотропина и стимулирует рост внутренних органов. Вследствие дефицита соматотропного гормона рост и своевременное развитие органов может частично нарушиться. Это приводит к нарушению работы печени, почек, сердечно-сосудистой системы. Такое осложнение встречается нечасто.
При дефиците гормона роста совместно с другими гормонами гипофиза (пангипопитуитаризме) будет развиваться недостаточность других эндокринных желёз — щитовидной железы, надпочечников, репродуктивной системы. Несвоевременная диагностика этих нарушений после рождения опасна для жизни, а также может стать причиной необратимым нарушений психического или интеллектуального развития.
Диагностика гипофизарного нанизма
Диагностика заболевания начинается с оценки линейного роста ребёнка и скорости прибавки в росте. Для этого врачи сравнивают фактические параметры ребёнка с предполагаемым ростом и среднестатистической скоростью роста. Подставив все данные в специальную формулу, они вычисляют коэффициент стандартного отклонения. Если у ребёнка отставание в росте больше двух сигмальных отклонений, плохая скорость прибавки роста, то проводится дальнейшее обследование.
Затем врачи определяют костный возраст. Сделать это можно с помощью рентгена или УЗИ запястья. В норме костный возраст может отставать или опережать паспортный на два года.
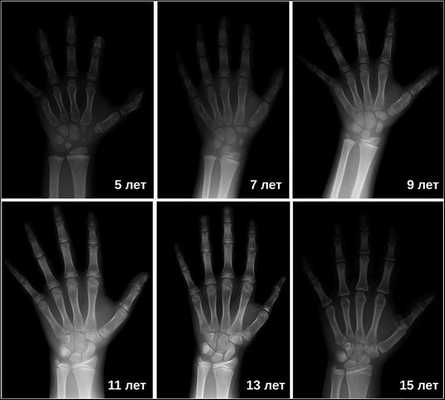
Также важно провести оценку гормонального профиля:
- уровень тиреотропного гормона (ТТГ) и свободного тироксина (Т4) — проверка работы щитовидной железы;
- уровень кортизола и АКТГ (кортикотропина) — исключение нарушений работы надпочечников [10] ;
- уровень лютеинизирующего гормона (ЛГ) и фоллитропина (ФСГ) — исключение гипогонадотропного гипогонадизма в возрасте, когда должно начаться половое созревание;
- инсулиноподобный фактор роста-I (ИПФР-I) — оценка уровня гормона роста.
Прямая оценка уровня соматотропина, как правило, не проводится. Гормон роста в течение суток выделяется в разном количестве, поэтому узнать его истинный уровень невозможно.
При необходимости проводится МРТ головного мозга и гипофиза с контрастированием [6] . Она позволяет исключить или подтвердить наличие объёмных образований области гипофиза и головного мозга.
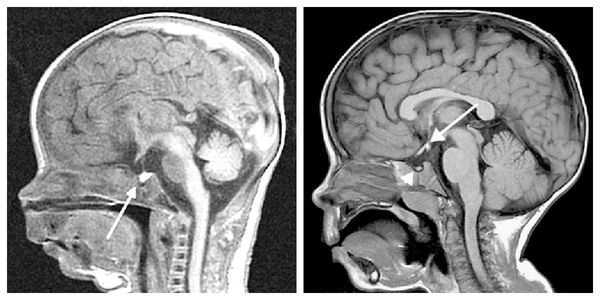
Для дифференциальной диагностики задержки роста, не связанной с гормоном роста, исключают дефицит железа, дефицит витамина D, общего белка и другие дефицитные состояния, т. к. их наличие может отрицательно влиять на скорость линейного роста. Рентгенография черепа в данном случае не информативна.
Для исключения определённых генетических синдромов может потребоваться консультация генетика.
При подозрении на истинный дефицит гормона роста проводятся пробы на стимуляцию соматотропина. Эти провокационные тесты стимулируют выброс гормона роста при введении определённых препаратов. Они проводятся только после исключения других возможных причин низкорослости. На основании этих проб, при отсутствии должного выброса гормона роста, будет установлен диагноз "гипопитуитаризм".
Лечение гипофизарного нанизма
Лечение проводится рекомбинантным гормоном роста, который получают методом генной инженерии. Он назначается после исключения активных злокачественных новообразований и тяжёлых сопутствующих заболеваний (как физических, так и психических). Эти состояния являются противопоказанием к использованию данного препарата.
Если имеются другие дефициты гормонов гипофиза, то перед лечением их также нужно компенсировать. Иначе должного эффекта от применения гормона роста не будет.
Цели лечения:
- ускорить темп роста и нормализовать рост;
- стимулировать начало периода полового созревания с нормальным ростом;
- достичь генетически прогнозируемого роста ребёнка или опередить его;
- улучшить качество жизни;
- повысить минеральную плотность костей;
- снизить факторы риска сердечно-сосудистых заболеваний.
Противопоказания к назначению рекомбинантным гормоном роста:
- закрытые зоны роста, за счёт которых происходит линейный рост (при их закрытии человек перестаёт расти);
- активные злокачественные новообразования;
- прогрессирующий рост внутричерепных опухолей;
- аллергия на препарат.
Прекращают терапию гормоном роста при:
- закрытии зон роста;
- плохой скорости прибавки роста — менее 2 см в год;
- достижении социально приемлемого роста.
Крайне редко возможны побочные эффекты и осложнения при терапии гормоном роста:
- доброкачественная внутричерепная гипертензия — повышение внутричерепного давления;
- боли в суставах — обычно наблюдаются при значительном ускорении линейного роста;
- возможно усугубление заболеваний, связанных с недифференцированными дисплазиями соединительной ткани (сколиозов);
- отёки — связано с функцией гормона роста задерживать жидкости в организме;
- пубертатная гинекомастия — увеличение грудных желёз за счёт разрастания железистой ткани у мальчиков [7] .
Прогноз. Профилактика
Прогноз заболевания при своевременной диагностике и проведении должного лечения, как правило, благоприятный. Дети достигают своего генетически прогнозируемого роста и иногда даже опережают его.
Если дефицит гормона роста сочетается с дефицитом других гормонов гипофиза, то для достижения желаемого эффекта, профилактики ухудшения состояний и более лёгкой социальной адаптации ребёнка необходимо лечение других дефицитов.
Также очень важен чёткий и своевременный контроль во время лечения гормоном роста: оценка динамики линейного роста, гормонального статуса и костного возраста. Особое внимание необходимо уделять режиму лечения и своевременной коррекции дозы препарата с учётом прибавки в росте и весе. При применении соматотропного гормона доза препарата будет увеличиваться. При несвоевременной прибавке дозы динамика роста может ухудшится [8] .
Мониторинг детей, находящихся на лечении, проводится раз в полгода, при других сопутствующих дефицитах гормонов гипофиза — по показаниям.
Вопрос профилактики данного заболевания сложен, т. к. речь идёт о генетических нарушениях. В первую очередь важен ответственный подход будущих родителей к рождению ребёнка:
- своевременное обследование и лечение заболеваний;
- восполнение дефицитов при планировании беременности;
- отказ от вредных привычек.
Для профилактики дефицита гормона роста, который возникает вследствие другого заболевания (инфекции, опухоли, травмы), следует проводить профилактики первоисточника.
Диагностика и лечение акромегалии и гигантизма
Акромегалия - нейроэндокринное заболевание, вызванное хронической избыточной секрецией гормона роста (СТГ) у лиц с законченным физиологическим ростом и характеризующееся патологическим диспропорциональным периостальным ростом костей, хрящей, мягких тканей, внутренних органов, а также нарушением функционального состояния сердечно-сосудистой, легочной системы, периферических эндокринных желез, различных видов метаболизма) [1].
Гигантизм - нейроэндокринное заболевание, вызванное хронической избыточной секрецией гормона роста, возникающее у детей и подростков с незаконченным физиологическим ростом, характеризующееся пропорциональным ростом костей скелета в длину, приводящее к значительному увеличению роста субъекта [1].
I. ВВОДНАЯ ЧАСТЬ
Название протокола: Диагностика и лечение акромегалии и гигантизма
Код протокола:
Код МКБ-10: Е-22
Сокращения, используемые в протоколе:
СТГ - соматотропный гормон
ИФР-1 - инсулиноподобный фактор роста
МРТ - магнитно-резонансная томография
КТ - компьютерная томография
ОГТТ - оральный глюкозотолерантный тест
Дата разработки протокола: апрель 2013.
Категория пациентов: больные акромегалией и гигантизмом
Пользователи протокола: врачи-эндокринологи поликлиник и стационаров, нейрохирурги, врачи ПМСП, невропатологи, окулисты, врачи других специальностей, выявившие акромегалию впервые.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Классификация
По этиологическому принципу
Спорадическая опухоль гипофиза (соматотропинома)
Эктопическая секреция гормона роста:
- эндокраниальная (опухоль глоточного кольца и сфеноидального синуса)
- экстракраниальная (опухоли поджелудочной железы, легких и средостения)
Эктопическая секреция соматолиберина:
- эндокраниальная (гамартромы, ганглиоцитомы)
- экстракраниальная (карциноид поджелудочной железы, бронхов, ЖКТ)
Синдромы генетических нарушений:
- синдром Мак-Кьюна-Олбрайта
- синдром МЭН-1 (синдром Вермера)
- комплекс Карни
- изолированная семейная низкорослость
Классификация соматотропином по морфофункциональным характеристикам
Моногормональная опухоль гипофиза (соматотропинома):
- плотногранулированная
- редкогранулированная
Плюригормональная опухоль гипофиза:
- продуцирующая СТГ и пролактин (соматопролактинома)
- продуцирующая СТГ и другие гормоны аденогипофиза (смешанные опухоли гипофиза) (1)
По размеру
- микроаденомы (менее 10 мм.) и макроаденомы (более 10 мм.).
По характеру роста
- эндоселлярная,
- экстраселлярная с пара- или супраселлярным ростом (без зрительных нарушений или со зрительными нарушениями),
- инфраселлярная,
- гигантская.
В клинике акромегалии различают: активную стадию и стадию ремиссии, прогрессирующее и торпидное течение [1,2,3].
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
Основные диагностические мероприятия
Амбулаторно:
- Определение базального уровня СТГ в сыворотке крови 2-3 раза
- Определение в крови уровня пролактина.
- Определение в крови уровня ИРФ-1 (соматомедина-С)
- Компьютерная, либо магнитно-резонансная томография области турецкого седла с контрастированием.
- Оценка состояния глазного дна, области перекреста зрительных нервов, периметрия Голдмана.
В стационаре:
- ОГТТ с 75 г глюкозы с определением СТГ на 0, 30, 60, 90, 120 мин (проводится только у пациентов, не страдающих сахарным диабетом!).
- МРТ или КТ органов грудной клетки и брюшной полости для выявления эктопированной опухоли (при наличии показаний)
Дополнительные диагностические мероприятия
Амбулаторно:
- Определение в крови уровня ТТГ, св. Т4
- Гликемия натощак
- Коагулограмма
- Время свертывания крови
- Кровь на ВИЧ
- Кровь на гепатит «В», «С»
- Кровь на RW
- Липидный спектр крови (холестерин, триглицериды, ЛПНП, ЛПВП)
- Креатинин крови
- АЛТ, АСТ крови
- УЗИ органов брюшной полости и малого таза
- Рентгенография органов грудной клетки
- Определение величины толщины мягких тканей стопы в области пяточной кости. Норма у мужчин до 21 мм, у женщин до 20 мм.
- ЭКГ
В стационаре
- Определение в крови уровня АКТГ, кортизола, ФСГ, ЛГ
- ОГТТ
- ЭХО-кардиография
- Колоноскопия (при наличии показаний)
Диагностические критерии
Жалобы и анамнез:
- укрупнение черт лица, кистей и стоп,
- длительные головные боли,
- ночные апноэ.
Анамнез, как правило, длительный. От момента появления первых симптомов заболевания до постановки диагноза акромегалии проходит от 5 до 15 лет) [1,2].
Физикальное обследование:
Основные клинические проявления [1,2,3]:
- Изменение внешности (укрупнение носа, губ, языка, утолщение кожи, увеличение надбровных дуг), увеличение верхней и нижней челюсти, прогнатия, расширение межзубных промежутков - диастема, увеличение конечностей.
- Увеличение внутренних органов - спланхномегалия
- Себорея, гипергидроз, акне
- Признаки объем ного образования хиазмально-селлярной области: головная боль, нарушения полей зрения, парезы черепно-мозговых нервов, гиперпитуитаризм, гиперпролактинемия
- Парестезии, артралгии, корешковые и туннельные синдромы
- Артериальная гипертензия, кардиомегалия
- Нарушение менструального цикла, галакторея, снихение либидо, потенции
- Нарушение толерантности к глюкозе, сахарный диабет
- Гиперхолестеринемия, гипрертриглицеридемия
- Склонность к новообразованиям (полипы ЖКТ, узловой зоб, миома матки)
Лабораторные методы исследования [1,2,3]:
- Повышение базального уровня СТГ в сыворотке крови в 2-3 и более раз
- Через 2 часа на фоне ОГТТ с 75 г глюкозы уровень СТГ >1 нг/мл (проводится только у пациентов, не страдающих сахарным диабетом!)
- Повышение уровня ИРФ-1 (соматомедина-С) в крови
- Повышение уровня пролактина в сыворотке крови при соматомамматропиномах
Инструментальные методы исследования:
- Наличие аденомы гипофиза при проведении компьютерной, либо магнитно-резонансной томографии с контрастированием.
- Наличие эктопированной опухоли, секретирующей СТГ или соматолиберин
- Увеличение толщины мягких тканей стопы в области пяточной кости. Норма у мужчин до 21 мм, у женщин до 20 мм.
- Изменения на глазном дне и гемианопсия, выявляемые при оценке состояния глазного дна, области перекреста зрительных нервов, периметрии Голдмана.
Показания для консультации специалистов:
- Окулист - оценка состояния глазного дна, полей зрения, зрительных нервов
- Консультация нейрохирурга для решения вопроса об оперативном лечении
- Консультация онколога для исключения новообразований прямой кишки
Дифференциальный диагноз
Дифференциальный диагноз акромегалии [1,2]
| Заболевания | Клиническме проявления акромегалии или гигантизм | Секреция СТГ и ИФР 1 ↑ | Аденома гипофиза | Секреция других гормонов |
| Гипофизарная акромегалия | + | + | + | _ |
| Внегипофизарная акромегалия | + | + | _ | _ |
| Акромегалоидизм | +_ | | - | |
| Гипотиреоз | +_ | _ | _ | ТТГ ↑ Т4↓ |
| Пахидермопериостоз | Изменения кожи, суставов | _ | _ | _ |
| Болезнь Педжета | Изменения костей и суставов | _ | _ | _ |
| Синдром Мак-Кьюна- Олбрайта | Костно-фиброзная дисплазия, локальная дерматопатия, изменения внешности | Повышена у 20% | Аденомы редко | _ |
Лечение
Цели лечения:
- ликвидация (или блокирование) источника гиперсекреции СТГ
- нормализация или снижение до безопасного уровня секреции СТГ и ИФР-1
- устранение клинических симптомов заболевания
- улучшение качества жизни пациентов
Тактика лечения
В настоящее время применяются хирургический, медикаментозный и реже - лучевой методы лечения акромегалии.
Основные факторы, определяющие выбор метода лечения:
- Состояние зрения
- Размеры и характер роста аденомы
- Степень функциональной активности аденомы
- Возраст больного
- Наличие тяжелых сопутствующих соматических нарушений
- Желание больного [2,3,4,5]
При больших размерах аденом гипофиза используется комплексное многоэтапное лечение.
Немедикаментозная терапия:
Стол 9.
Режим щадящий, противопоказан тяжелый труд и пребывание на солнце.
Медикаментозная терапия
В качестве медикаментозной терапии используются два класса препаратов - аналоги соматостатина и агонисты дофамина.
Препараты первого ряда - аналоги соматостатина длительного действия
Ланреотид длительного действия 60 - 120 мг 1 раз в 28 дней, п/к (6,7,8)
Октреотид длительного действия 10-30 мг 1 раз в 28 дней в/м(9,10)
Аналог соматостатина короткого действия октреотид в дозе 100 мкг 3 раза в день п/к используется редко (для непродолжительного лечения).
Показания к терапии аналогами соматостатина длительного действия (1,4,5,7)
1. При неэффективности хирургического лечения
2. После хирургического лечения и (или) лучевой терапии до реализации эффекта от облучения
3. Как монотерапия при наличии противопоказаний или отказе больного от оперативного лечения
4. Для предоперационной подготовки с целью улучшения состояния больного и уменьшения размеров опухоли в течение 6 и более месяцев
Аналоги соматостатина длительного действия нормализуют СТГ и ИФР-1 у 60 -70% больных [2,,4,5,6]. Эффективность действия препаратов нарастает по мере увеличения срока применения.
Побочные эффекты: покраснение и болезненность в месте инъекции, повторный жидкий стул в первые 2-3 дня после введения препарата, встречаются редко и по мере увеличения срока терапии проходят. У части пациентов отмечается застой желчи и камнеобразование.
Препараты 2 ряда - агонисты дофамина
Агонисты дофамина показаны при относительно невысокой активности заболевания и обязательно назначаются при сопутствующей гиперсекреции пролактина [2,3,4,5].
В РК применяются агонисты дофамина:
Бромкриптин от 10 до 20 мг/сут в 2-4 приема, эффективно снижает секрецию СТГ только 10% пациентов.
Каберголин в дозе от 0,5 мг 3 раза в неделю до 0,5 мг ежедневно, нормализует секрецию СТГ только у 30% [4,5]
Консервативная терапия чаще применяется как дополнительная к хирургическому и (или) лучевому лечению. Проводится длительно, часто пожизненно.
Другие виды лечения
Лучевая терапия
В последние годы показания к лучевой терапии сузились, применяется только при неудовлетворительном эффекте от хирургического и медикаментозного лечения [2,3,4,5]
Стереотоксическая гамматерапия - гамма-нож,* облучение одномоментное в дозе до 90 грей.
Протонотерапия *- одномоментное облучение области гипофиза потоком тяжелых протонных частиц в дозе 50-70 Грей, применяется при опухолях размером не более 1,5 см и позволяет достичь ремиссии заболевания у 39-46 % больных в сроки от 1 до 5 лет.
Возможно повторное проведение облучения (не ранее, чем через 1 год) при наличии роста аденомы гипофиза.
Осложнения лучевой терапии: гипопитуитаризм, постлучевая энцефалопатия, неврологические нарушения, постлучевые некрозы, снижение качества жизни [2,3,4,5]
Эффект от лучевой терапии наступает через 5-10 лет у 60-70% больных [3,4].
Хирургическое лечение - метод первого выбора в терапии акромегалии.
Преимущество этого метода - быстрота наступления эффекта: уже в раннем послеоперационном периоде в случае полного удаления аденомы отмечается нормализация секреции гомона роста.
В подавляющем большинстве случаев применяется транссфеноидальная аденомэктомия под контролем нейронавигации. Транскраниальный доступ применяется редко.
Выбор метода определяется размером аденомы и степенью экстраселлярного распространения. При необходимости последовательно применяются оба метода. Хирургический метод позволяет достичь ремиссии заболевания в 30-50% случаев удаления макроаденомы, и в 70-80% - в случае удаления микроаденом гипофиза [1,2,3].
АЛГОРИТМ ЛЕЧЕНИЯ АКРОМЕГАЛИИ
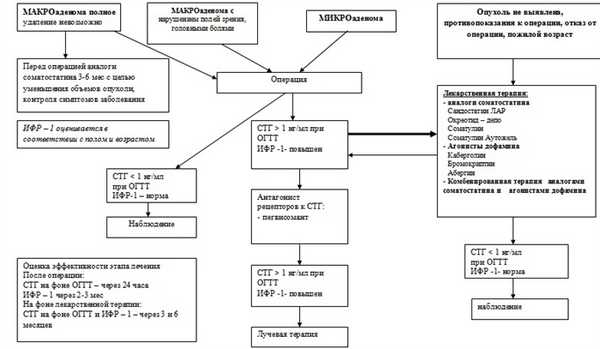
Профилактические мероприятия:
Методы первичной профилактики акромегалии неизвестны.
Дальнейшее ведение:
После оперативного лечения и лучевой терапии пациент наблюдается и при необходимости получает медикаментозную терапию у эндокринолога по месту жительства.
Эффективность хирургического вмешательства контролируется определением ИРФ-1 или проведением ОГТТ с определением СТГ в раннем послеоперационном периоде - на 5-8 сутки и через 3, 6 и 12 месяцев.
Один раз в год проводится определение ТТГ, свТ4, кортизола, половых гормонов.
Эффективность лучевой терапии с исследованием ИРФ-1 или проведением ОГТТ с определением СТГ оценивается не ранее, чем через 6 месяцев.
Эффективность лечения аналогами соматостатина должна контролироваться каждые 3-4 месяца (ИФР-1 или ОГТТ с определением СТГ).
У пациентов с медикаментозной ремиссией для определения остаточной функции гипофиза через 1-2 года после начала терапии необходимо прервать лечение на 1 - 2 месяца с контролем ИФР-1. При сохранении нормального уровня ИФР-1 лечение прекращают.
Наблюдение нейрохирурга, КТ и МРТ через 6-12 месяцев. Осмотр окулиста 1 раз в год.
Критерии ремиссии акромегалии [1,2,,4,5]
Полная ремиссия
- Отсутствие клинических признаков активности
- СТГ базальный < 0,4 нг/мл
- Минимальный уровень СТГ на фоне ОГТТ < 1 нг/мл (< 2,7 мЕд/л).
- Нормальный уровень ИРФ-1 соответственно полу и возрасту
Неполная ремиссия
- Отсутствие клинических признаков активности.
- СТГ базальный > 0,4 нг/мл
- Минимальный уровень СТГ на фоне ОГТТ > 1 нг/мл (> 2,7 мЕд/л).
- Повышенный уровень ИРФ-1 соответственно полу и возрасту.
Отсутствие ремиссии
- Имеются клинические признаки активности.
- Минимальный уровень СТГ на фоне ОГТТ > 1 нг/мл (> 2,7 мЕд/л).
- Повышенный уровень ИРФ-1.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе
- Увеличение процента больных, выявленных на ранних стадиях акромегалии
- Увеличение количества больных, достигших ремиссии и неполной ремиссии.
- Уменьшение количества больных с осложнениями после оперативного лечения
Препараты (действующие вещества), применяющиеся при лечении
| Бромокриптин (Bromocriptine) |
| Каберголин (Cabergoline) |
| Ланреотид (Lanreotide) |
| Октреотид (Octreotide) |
Госпитализация
Показания для госпитализации с указанием типа госпитализации
1. Необходимость верификации диагноза акромегалии и определения тактики ведения - плановая госпитализация в региональное специализированное эндокринологическое отделение (7 - 14 дней)*
2. Оперативное лечение в условиях оказания ВСМП, трансназальная аденомэктомия под контролем нейронавигации, - плановая госпитализация в профильные нейрохирургические отделения. Сроки госпитализации от 14 до 21 дня.
3. Динамическое наблюдение и лечение осложнений акромегалии - плановая госпитализация в региональное специализированное эндокринологическое отделение (5-14 дней)*
4. Проведение больному курса гамма-терапии - плановая госпитализация в специализированное радиологическое отделение НИИ онкологии или региональные онкоцентры (6-7 недель)
*Для пациентов, проживающих в региональных центрах, где имеются оснащенные медицинские диагностические центры, возможно амбулаторное обследование и лечение.
Информация
Источники и литература
- Протоколы заседаний Экспертной комиссии по вопросам развития здравоохранения МЗ РК, 2013
- 1. Дедов И.И., Мельниченко Г.А., Акромегалия, М., 2009, 117. 2. Дедов И.И., Мельниченко Г.А., Эндокринология национальное руководство, Под. Ред. Дедова И.И., Мельниченко Г.А.,Москва, «ГЭОТАР - Медиа», 2012, 633 - 646., 3. Генри М. Кроненберг, Шломо Мелмед, Кеннет С., Полонски К., П.Рид Ларсен. Эндокринология по Вильямсу. Нейроэндокринология,Москва, Рид Элсивер, 2010, 277 - 311. 4. Melmed S, Colao A, Barkan A et al (2009) Guidelines for Acromegaly Management: An Update. J Clin Endocrinol Metab 94:1509-1517 5. Laurence Katznelson, John L.D. Atkinson, David M. Cook, Shereer Z. Ezzat, Amir H. Hamrahium, Karen K. Miller. Medical Guidelines for clinical practice for the diagnosis and treatment of acromegaly - 2011 UPDATE. Endocrine Practice. Vol 17 (Suppl 4), July/ august, 2011. 6. Maiza JC, Vezzosi D, Matta M, Donadille F, Loubes-Lacroix F, Cournot M, Bennet A, Caron P (2007) Долговременное (вплоть до 18 лет) воздействие на гиперсекрецию ГР/ ИФР-1 и величина новообразования при первичном приеме аналога соматостатина (SSTa) у пациентов с ГР. Clin Endocrinol (Oxf) 67:282-288 7. Cozzi R, Montini M, Attanasio R, Albizzi M, Lasio G, Lodrini S, Doneda P, Cortesi L, Pagani G (2006) Первичное лечение акромегалии с применением октреотида LAR: длительное (до девяти лет) перспективное исследование эффективности препарата в регуляции активности заболевания и уменьшения новообразования. J Clin Endocrinol Metab 91:1397-1403
Информация
III. ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола
1. Базарбекова Р.Б. - д.м.н., профессор, зав. кафедрой эндокринологии РГКП «Алматинский государственный институт усовершенствования врачей»
2. Косенко Т.Ф. - к.м.н., доцент кафедры эндокринологии РГКП «Алматинский государственный институт усовершенствования врачей»
3. Досанова А.К. - к.м.н., ассистент кафедры эндокринологии РГКП «Алматинский государственный институт усовершенствования врачей»Рецензенты: д.м.н., профессор кафедры эндокринологии КазНМУ имени С.Д. Асфендиярова Нурбекова А.А.
Указание на отсутствие конфликта интересов - отсутствует
Указание условий пересмотра протокола: данный протокол подлежит пересмотру каждые три года, либо при появлении новых доказанных данных по проведению процедуры реабилитации.
Читайте также:
- Взаимодействие вируса с клеткой. Характер взаимодействия вирус-клетка. Продуктивное взаимодействие. Вирогения. Интерференция вирусов.
- Формирование мышц шеи эмбриона. Развитие мышц головы плода
- Диагностика рака толстой кишки: скрининг на рак кишки, ранняя диагностика
- Глубокая трихофития волосистой части головы
- Заворот желудка
