Доступ и ход операции удаления эхинококковой кисты печени
Добавил пользователь Дмитрий К. Обновлено: 22.01.2026
ГКП на ПХВ «Мангистауская областная больница», Актау, Казахстан, ГБОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Лапароскопическая эхинококкэктомия при прорыве кисты печени в брюшную полость
Журнал: Эндоскопическая хирургия. 2016;22(6): 48‑51
Цистный эхинококкоз является паразитарным заболеванием, вызванным Echinococcus granulosus, и характеризуется образованием жидкостных кист в различных органах и тканях. Поражаются преимущественно печень и легкие.
Кисты печеночной локализации осложняются в 5—40% случаев. Среди осложнений наблюдаются формирование цистобилиарных свищей, прорыв кисты в желчные протоки или сдавление их с развитием механической желтухи, инфицирование и нагноение кисты, развитие различных аллергических реакций, прорыв кисты в брюшную полость, развитие мембранного гломерулита и др. [1—4].
По D. Lewall и S. McCorkell (1986), различают 3 типа прорыва кисты: contained — прорыв в фиброзную полость (при этом повреждена лишь хитиновая оболочка, гидатидная жидкость остается в пределах фиброзной полости); communicating — разрыв хитиновой оболочки и прорыв в фиброзную полость, сообщающуюся с желчными или бронхиальными путями; direct — прорыв в плевральную, брюшную или другие полости в связи с разрывом хитиновой оболочки и фиброзной капсулы [5].
Прорыв кист печени в брюшную полость, по разным оценкам, наблюдается в 1—16% случаев [2, 5—12]. Основными факторами риска прорыва кист в брюшную полость считаются молодой (травмоопасный) возраст пациента, диаметр кисты более 10 см, быстрый рост кисты с высоким интракистозным давлением, а также поверхностное расположение кисты [4, 7, 9].
Клинически прорыв может протекать как бессимптомно [13], так и с яркой клинической картиной, включающей абдоминальную боль с перитонитом и развитие анафилактической реакции [4]. Наиболее характерными симптомами прорыва эхинококковой кисты в брюшную полость являются боли в животе, крапивница и другие аллергические реакции, тошнота и рвота [6]. Аллергические реакции можно наблюдать, по разным данным, в 16,7—25% случаев [5]. Описаны летальные исходы в связи с анафилактическим шоком при прорыве эхинококковой кисты.
Верификация прорыва кисты в брюшную полость основана на данных УЗИ, КТ или МРТ. Критериями прорыва при эхинококкозе печени являются наличие свободной жидкости и эхинококковых кист в брюшной полости, наличие отслоившейся оболочки в полости кисты, изменение формы кисты с наличием внекистозной жидкости [5].
Прорыв кист в брюшную полость — один из ведущих факторов развития послеоперационного рецидива [14]. Частота рецидивов после интраперитонеального разрыва эхинококковых кист печени может достигать 21% [10]. Использование альбендазола для предотвращения вторичного (рецидивного) перитонеального эхинококкоза рекомендуется всеми авторами, однако нет единого мнения относительно продолжительности лечения. Минимальная продолжительность лечения, рекомендуемая большинством авторов, — 3 мес [15].
При прорыве эхинококковой кисты в брюшную полость развивается паразитарный перитонит, который может протекать абортивно. Однако нередко перитонит прогрессирует с формированием развернутой клинической картины разлитого гнойного процесса. В связи с этим большинство авторов при прорыве кист в брюшную полость рекомендуют экстренное хирургическое вмешательство [6, 8]. Но, как показывают отдельные клинические наблюдения, возможно и отсроченное проведение хирургического вмешательства с благоприятным исходом [16, 17].
При хирургическом лечении эхинококкоза печени, осложненного прорывом кисты в брюшную полость, отмечен высокий уровень послеоперационных осложнений и летальности. Публикаций с анализом этих проблем мало, однако в отдельных работах сообщается о летальности 11,8% и уровне осложнений 10—23,5% [5]. Летальность, как правило, связана с развитием развернутой картины перитонита.
Радикальные вмешательства (перицистэктомия, резекция печени) редко применяются в случаях прорыва эхинококковых кист в брюшную полость. В подобных случаях чаще используются так называемые консервативные хирургические методы: наружное дренирование, частичная перицистэктомия, тампонада полости и др., разумеется, включая санацию брюшной полости.
Лапароскопическая эхинококкэктомия и чрескожное дренирование эхинококковых кист, хотя и приобретают популярность в последнее десятилетие, тем не менее в случаях порыва кист в брюшную полость они не практикуются [5].
Мы имели 3 случая успешного проведения лапароскопической эхинококкэктомии из печени у больных в раннем периоде (12—36 сут) после прорыва кисты в брюшную полость. Всем после операции проведено противорецидивное лечение альбендазолом. Срок послеоперационного наблюдения за пациентами составил 5—17 мес. Рецидивы заболевания не выявлены.
Приводим выписку из истории болезни одного из пациентов.
Больной П., 39 лет, госпитализирован в отделение видеоэндоскопической хирургии ГКП на ПХВ «Мангистауская областная больница» (г. Актау, Казахстан) с подозрением на острый живот. При поступлении жаловался на боли в правом подреберье. За несколько часов до поступления был сильный кашель (во время приема пищи больной поперхнулся), в момент которого появились резкие боли в правом подреберье. Через 10—15 мин боли в правом подреберье значительно стихли и постепенно сместились в правую подвздошную область. Больной отмечает, что небольшая припухлость в правом подреберье, отмечаемая им ранее, в настоящее время исчезла. Ранее у больного был диагностирован эхинококкоз печени в 5—7-м сегментах СЕ1-типа, по классификации ВОЗ, размерами 6×8 см (рис. 1), по поводу чего готовился к плановой операции.
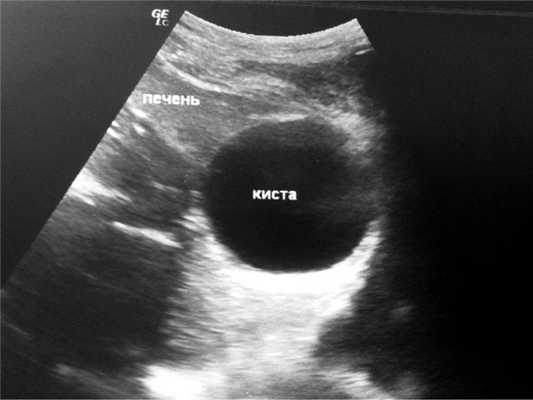
Рис. 1. Больной П., 39 лет. Эхинококковая киста в проекции 5—7-го сегментов печени до прорыва.
При поступлении в стационар общее состояние больного удовлетворительное, небольшая тахикардия (ЧСС до 85 уд/мин), гипотонии нет, дыхание не страдает, аллергических кожных проявлений нет. Живот не вздут, несколько болезненный при пальпации в правой половине, преимущественно в правом подреберье и в правой подвздошной области. Там же отмечается небольшое напряжение мышц передней брюшной стенки.
Выполнено УЗИ брюшной полости: в проекции 5—7-го сегментов печени визуализируется эхинококковая киста овальной формы с отслоившейся кутикулой (СЕ3-типа по классификации ВОЗ) размерами 5,5×7,0 см и анэхогенным жидкостным компонентом (рис. 2). В малом тазу свободная анэхогенная жидкость в небольшом количестве.
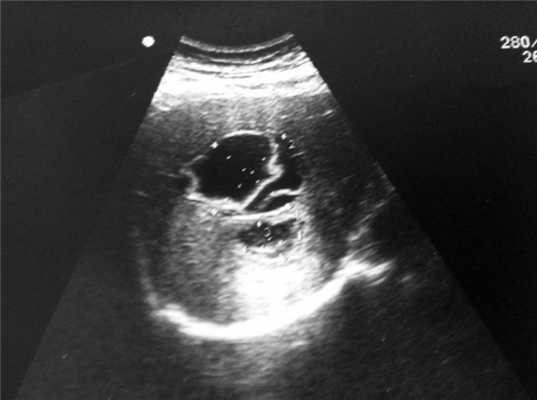
Рис. 2. Больной П., 39 лет. Эхинококковая киста в проекции 6—7-го сегментов печени после прорыва.
Для уточнения тактики лечения решено провести лапароскопию.
Протокол операции. Пневмоперитонеум 10 мм рт.ст. Порт для видеолапароскопа (порт № 1) установлен в верхней точке Калька. При осмотре брюшной полости обнаружены единичные сформировавшиеся спайки сальника с дном желчного пузыря. Рыхлые и плотные спайки с диафрагмой купола кисты на передней поверхности 5—7-го сегментов печени (рис. 3). Киста багрового цвета, размерами 6×8 см. При инструментальной пальпации киста не напряжена. В малом тазу серозный выпот объемом не более 100 мл.
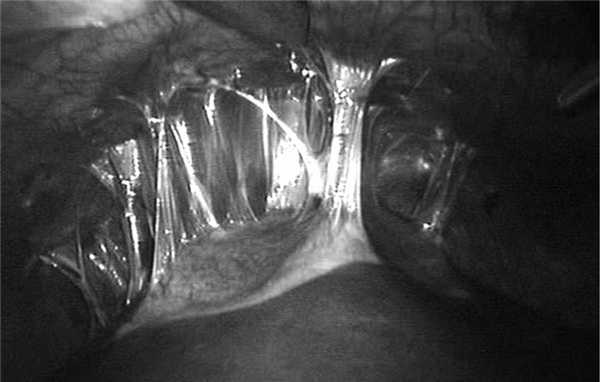
Рис. 3. Лапароскопия: киста 5—7-го сегментов печени при состоявшемся прорыве в брюшную полость. Рыхлые спайки с диафрагмой и спавшаяся киста.
При рассечении спаек в области 7-го сегмента выявлена линейная трещина в перикистозной ткани печени длиной 4 см и шириной 0,25 см, в котором просматривается белесовато-серая кутикула эхинококковой кисты. В области разрыва перикистозной ткани небольшие фибриновые слизеподобные наложения и рыхлые спайки с диафрагмой.
Обнаруженная картина расценена как прорыв эхинококковой кисты печени в брюшную полость с неполным опорожнением кисты за счет прикрытия дефекта фиброзной капсулы кутикулярной оболочкой. Учитывая удобную локализацию кисты и достаточно высокую локализацию зоны перфорации, а также отсутствие данных за прогрессирование перитонита, решено выполнить эхинококкэктомию печени и санацию брюшной полости лапароскопическим доступом.
Установлены дополнительные порты: порт № 2 для 10 мм троакара на 1 см правее и ниже точки Кера, порт № 3 по средней линии чуть ниже мечевидного отростка и порт № 4 под правой реберной дугой для 5 мм троакаров. К месту прорыва кисты подведена турунда, смоченная гипертоническим раствором. Туда же установлен наконечник аспиратора. Пункционная лапароскопическая игла, подсоединенная к аспиратору, проведена через порт № 2. Для пункции выбрана точка на 3 см выше места прорыва и максимально близко к порту № 2. Киста пунктирована при постоянном контроле за подтеканием жидкости из места прорыва. По мере опорожнения кисты края фиброзной капсулы в месте прорыва захвачены зажимами, что обеспечило контроль за содержимым кисты и последующую ревизию остаточной полости через место прорыва кисты. Дальнейшие этапы проведения лапароскопической эхинококкэктомии не отличались от стандартных. Стенки фиброзной полости обработаны тампонами, смоченными 80% раствором глицерина и 70% этиловым спиртом.
После проведения всех этапов обработки эхинококковой кисты выполнено промывание брюшной полости большим количеством (до 2 л) раствора фурацилина. Антипаразитарный раствор для промывания брюшной полости не использовался.
Контрольный осмотр проводился через 1, 2 и 3 мес (по завершении каждого курса противорецидивного лечения). Больной лечение перенес хорошо. Дальнейшее наблюдение осуществлялось каждые 6 мес с проведением УЗИ брюшной полости. Через 17 мес после прорыва кисты контрольные УЗИ не выявили данных за рецидив заболевания. Последние результаты ИФА на эхинококкоз положительные в титре 1:200.
Результаты оперативного лечения эхинококкоза печени лапароскопическим и открытым способом
Введение. Эпидемиологическое и социально-экономическое значение эхинококкоза печени вызвано его широкой распространенностью в Кыргызской Республике, разнообразием клинической манифестации, тяжестью осложнений, стабильными показателями инвалидизации и летальности, финансовыми издержками в секторе здравоохранения 3.
Современная тенденция развития гепатохирургии отличается внедрением инновационных технологий, которые разработаны для улучшения качества и результатов диагностики и оперативного лечения, сохраняя радикальность и малоинвазивность [4, 6, 7]. Развитие эндовидеохирургии, разработка высококачественных видеосистем, а также технологий бескровного рассечения и гемостаза печени расширили возможности лапароскопии и определяют ее роль как приоритетного метода в лечении очаговых патологий, в частности ЭКП 6.
Большое количество публикаций, посвященных сравнительным анализам результатов лапаротомных и лапароскопических операций свидетельствует о существенных преимуществах эндовидеохирургии (короткий послеоперационный период, малоинвазивность, минимальные операционные осложнения, ранняя активизация и медико-социальная реабилитация больных [4, 5, 7].
Несмотря на широкую популяризацию эндовидеохирургии, в лечении ЭКП унификация показаний к лапароскопической эхинококкэктомии (ЛЭЭ), методологические и технические аспекты операции, профилактика интра- и послеоперационных осложнений, основанных на анализе первоначального опыта, остаются недостаточно изученными и имеющими большой научно-практический интерес. Все эти вопросы лапароскопической хирургии печени явились основанием для проведения настоящего исследования.
Цель исследования: повышение эффективности оперативного лечения ЭКП на основе оптимизации методологии ЛЭЭ.
Материал и методы. Дизайн исследования: одноцентровое ретроспективное и проспективное нерандомизированное исследование 108 больных с ЭКП.
Критерии включения больных в исследование: 1) больные с ЭКП с локализацией в S 2-7; 2) размеры кист не более 10 см.
Критерии исключения больных из исследования: 1) локализация кисты в S8 печени; 2) размеры кисты более 15 см; 3) полная интрапаренхиматозная локализация кисты; 4) рецидивный эхинококкоз печени; 5) больные с выраженным спаечным процессом в брюшной полости; 6) больные с декомпенсированными кардиореспираторными и метаболическими патологиями (бронхиальная астма, хроническая обструктивная болезнь легких (ХОБЛ), желудочковая экстрасистолия, ожирение с индексом массы тела (ИМТ) ≥ 40кг/м 2 ); 7) отказ больного от включения в исследование.
Медиана возраста 108 больных составила 30 лет (14-67). Преобладали лица женского пола - 71 (65,7%) с медианой возраста 32 года (14-67). Мужчины составили 37 (34,3%) человек с медианой возраста 29 лет (14-65).
В зависимости от метода операции все больные были разделены на 2 группы. Первую (основную) группу составили 57 (52,8%) больных, которым эхинококкэктомия была выполнена лапароскопическим методом. Вторая (контрольная) группа составлена из 51 (47,2%) пациента, оперированного лапаротомным методом. Пациенты обеих групп сопоставимы по полу и возрасту (разницы статистически нерепрезентативны). Следует отметить, что из всех 108 больных 86 (79,6%) были в возрасте до 50 лет (43 (75,4%) больных 1- группы и 43 (84,3%) больных 2-группы).
Все больные были госпитализированы в плановом порядке после полного клинического обследования.
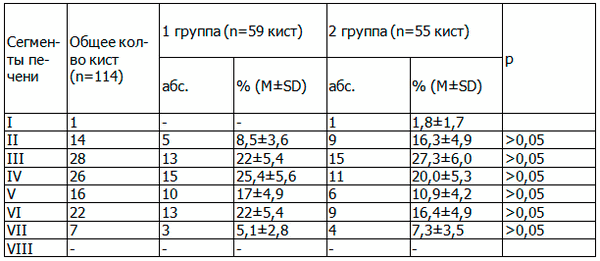
У всех 108 больных было в целом установлено 114 ЭКП: в 1-группе - 59 кист (у 2 больных по 2 кист), а во 2-группе - 55 кист (у 2 больных по 2 кист и у одного - 3 кист) (таблица 1).
Таблица 1. Сегментарная локализация ЭКП
Размеры ЭКП колебались от 17 до 140 мм: в первой группе - 17-140 мм (медиана 50 мм), во второй группе - 20-100 мм (медиана 58 мм).
В 27 (25%) наблюдениях ЭКП осложнились нагноением (у 17 (29,8%) больных 1-группы и у 10 (19,6%) больных 2-группы).
Из всех больных у 51 (47,2%) были установлены 99 сопутствующих терапевтических патологий органов и систем, среди которых превалировали заболевания пищеварительной системы.
Для проведения лапароскопической операции использовалась стандартная лапароскопическая стойка фирмы «ЭФА-МЕДИКА» (Санкт-Петербург, Россия) и «KARL STORZ» (Германия).
Во второй группе (n = 51) подреберная лапаротомия была применена у 18 (35,3%) больных с 20 кистами. Верхне-срединный лапаротомный доступ был использован у 33 (64,7%) больных с 35 кистами (2 кисты у одного пациента). В данной группе больных были выполнены атипичные резекции печени (4 больных) и эхинококкэктомии (ЭЭ) (47 больных) со следующими способами ликвидации остаточной полости печени (ОПП): с абдоминизацией (9 больных, 17,6%), с оментопластикой (3 больных, 5,9%), с капитонажем (6 больных, 11,8%), с гепатизацией (13 больных, 25,5%), полузакрытая ЭЭ (16 больных, 31,4%).
В обеих группах гермицидную обработку ОПП производили 33% раствором NaCl или 0,02 раствором декасана.
При выявлении желчных свищей у 6 (11,7%) больных второй группы производили их ушивание синтетической нерассасывающейся нитью на атравматической игле № 4/0 или 5/0 кисетным швом.
Для определения показаний к ЛЭЭ использовалась классификация ультразвуковых изображений ЭКП по H.A. Charbi (1981) в модификации ВОЗ (WHO-IWGE, 2003) (таблица 2).
Таблица 2. Распределение ЭКП по классификации WHO-IWGE (2003)
Показаниями для ЛЭЭ явлились: ЭКП типа CL, CE1, CE2 размерами до 150 мм; ЭКП типа СЕ3, СЕ4 и СЕ5 малых размеров (до 50-100 мм); локализация ЭКП в передних сегментах печени (S II, III, IVb, V,VI); субкапсулярное расположение ЭКП; отсутствие цистобилиарных фистул.
Вопрос количества рабочих троакаров решали индивидуально в зависимости от локализации ЭКП, использовали 3-4 троакаров. Они устанавливались после достижения уровня карбоксиперитонеума в режиме 10-12 мм.рт.ст. Траекторию установки троакаров ориентировали с наклоном в сторону ЭКП по правилу «треугольника», согласно которому троакары устанавливаются в области основания треугольника, верхушкой которого является киста печени (рисунок 1).
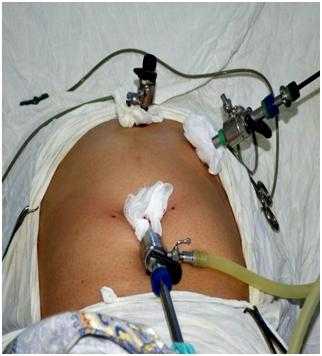
Рис. 1. Расположение троакаров при локализации ЭКП в левой доле печени.
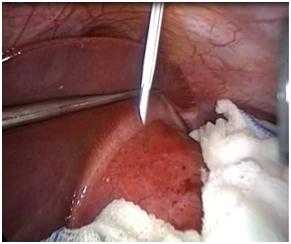
Рис. 2. Пункция эхинококковой кисты при ЛЭЭ (эндофото собственного наблюдения).
После полного опорожнения в полость ЭКП вводили гермицидный раствор для обеззараживания элементов паразита (30% раствор хлорида натрия (36 больных) и 0,02% декасана (21 больной)) с экспозицией 10 минут. После гермицидной обработки ЭКП антисептический раствор аспирировали и по пункционной игле вскрывали фиброзную капсулу (ФК). Данный этап операции проводился под постоянной аспирацией электроотсосом. После расширения раны ФК наконечник электроотсоса заменяли на 10-мм, с помощью которого возможно было более активно эвакуировать более густую массу (детрит, остатки хитина и дочерние пузыри). Затем зажимами хитиновую оболочку помещали в эндоконтейнер, который герметично закрывали (рисунок 3).
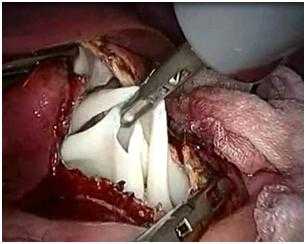
Рис. 3. Удаление хитиновой оболочки эхинококковой кисты в эндоконтейнер (эндофото собств. наблюдения).
В последующем в ОПП вводили лапароскоп и проводили эндовидеоцистоскопию на предмет исключения или диагностики цисто-билиарных желчных свищей и оценки полноты удаления хитиновой оболочки, дочерних пузырей и детрита. По сравнению с осмотром ОПП при лапаротомном доступе эндовидеоцистоскопия показала такие преимущества, как детализация ревизии при 12-кратном увеличении цифрового изображения на мониторе, широкий диапазон обзора за счет боковой оптической системы, расправление стенки ОПП в условиях газовой инсуффляции, малая инвазивность.
Были использованы следующие способы ликвидации ОПП при ЛЭЭ: оментопластика (21 больной, 36,8%), абдоминизация (17 больных, 30%), дренирование ОПП (15 больных, 26,2%) и сочетание оментопластики с дренированием ОПП (4 больных, 7%).
Статистическая обработка полученных результатов проводилась с использованием программы «STATISTICA 6.0». Достоверность различий между группами определяли с помощью параметрического t-критерия Стьюдента. Различия считали достоверными при уровне p
Результаты и обсуждение. В первой группе перехода на конверсию не было. Все 57 операций начаты и были завершены эндовидеохирургическим доступом. По многим объективным параметрам лапароскопические технологии продемонстрировали лучшие непосредственные и отдаленные результаты перед открытой методикой оперативного лечения ЭКП.
Одним из показателей сравнительного анализа результатов и эффективности использованных хирургических методов лечения является длительность операции. В наших наблюдениях разница в длительности операций как лапароскопическим, так и лапаротомным способами достоверно не отличалась (р>0,05). Это связано с тем, что в период освоения лапароскопических технологий эндовидеохирургические операции были длительными. В последующем по мере накопления опыта продолжительность ЛЭЭ заметно сократилась, составляя в среднем 47,4±6,6 минут.
В послеоперационном периоде в первой группе осложнения имели место в 2 (3,5%) наблюдениях в виде желчеистечения из ОПП, которое самостоятельно прекратилось на 12 и 20 сутки после операции. Суточный дебит желчи по дренажу составил в среднем 60-80 мл. А у остальных 55 (96,5%) больных после ЛЭЭ желчеистечения не было и сроки дренирования ОПП составили в среднем 3,9±2,5 суток. Во второй группе послеоперационные осложнения наблюдались в 14 (27,4%) случаях (нагноение ОПП - 5, формирование желчного свища - 4, нагноение операционной раны - 2, экссудативный плеврит - 2, пневмония - 1).
Сроки дренирования ОПП в первой группе составили в среднем 3,9±2,5 суток, а в контрольной - 22,5±5,8 суток (р<0,01).
Интенсивность послеоперационного болевого синдрома в обеих группах больных была оценена методом визуально-аналоговой шкалы. После ЛЭЭ болевой синдром был минимальным, составляя 3,3±1,2 мм, а во второй группе болевой синдром (7,6±1,3 мм) был основным фактором, влияющим на активизацию больных, развитие послеоперационных осложнений и длительность пребывания в стационаре. Эти больные нуждались в ежедневной анальгезии обезболивающими препаратами, а в первые сутки даже - наркотическими средствами.
В первой группе больные активизировались уже в среднем через 5,3±1,6 часов после операции, а больные второй группы активизировались только через 18,5±2,4 часов после операции (р<0,001). После ЛЭЭ пассаж кишечника восстанавливался через 11,3±3,4 часов после операции, а после открытой ЭЭ - через 34,7±3,6 часов (р<0,001). Среднее пребывание больных первой группы составило 6,0±3,1 койку-дней, а в контрольной группе - 9,4±4,0 (р>0,05). Восстановление трудоспособности после ЛЭЭ наступало с высокой достоверностью раньше, чем после операции лапаротомным методом (р<0,001).
Одним из немаловажных сравнительных критериев эффективности методов оперативного лечения является косметичность доступа, что указывает на степень травматичности. На рисунке 4 наглядно показана высокая косметичность лапароскопических доступов в хирургическом лечении ЭКП.
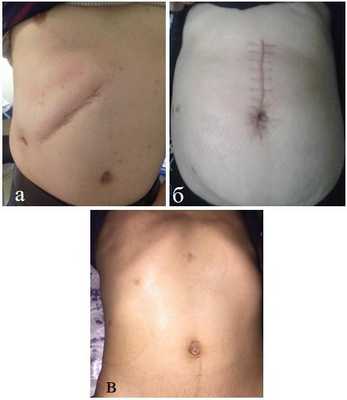
Рис. 4. Вид операционных рубцов после подреберной (а), верхне-срединной (б) лапаротомии и ЛЭЭ (в).
Таким образом, проведенное исследование показывает, что по многим сравниваемым объективным параметрам лапароскопические технологии демонстрируют более лучшие непосредственные результаты перед открытой методикой оперативного лечения ЭКП.
Отдаленные результаты были изучены у всех больных первой группы и у 42 (82,3%) больных контрольной группы, остальные 9 (21,4%) пациентов этой группы были упущены из поля наблюдения в силу разных причин (миграция и т.д.). Сроки наблюдения от 1 года до 7 лет. Для объективизации исследования оценки отдаленных результатов были разделены на 3 группы: хорошие, удовлетворительные и неудовлетворительные.
В целом при оперативном лечении ЭКП хорошие результаты были достигнуты у 78 оперированных больных, что составило 78,8%. Удовлетворительный результат констатирован в 18 наблюдениях (18,2%) и неудовлетворительный - в 3 (3%).
Анализ отдаленных результатов исследуемых двух групп оперированных по поводу ЭКП больных показал, что лучшие исходы хирургического лечения были достигнуты при использовании лапароскопических технологий. У большинства больных (86%) первой группы был получен хороший результат и у 14% - удовлетворительный. Рецидивов эхинококкоза и других, требующих оперативного лечения, состояний в первой группе не было. У 8 (14%) больных с удовлетворительным результатом в отдаленном послеоперационном периоде сонографически были установлены ОПП размерами до 2-4 см с гомогенным эхонегативным содержимым, которые клинически никак себя не проявляли. При динамическом исследовании в сроки до 4-6 месяцев наступила полная инволюция ОПП с формированием неправильной формы эхоплотного фиброзного очага. ЛЭЭ у этих 8 больных была завершена дренированием ОПП без ее ликвидации. Причиной выбора дренирования ОПП были большие размеры гидатидозной кисты печени (3 больных), а также при первых случаях использования лапароскопии в оперативном лечении ЭКП (5 больных).
Во второй группе больных отдаленные результаты оперативного лечения прослежены у 42 (82,3%) из 51 больного. При этом хорошие результаты были получены в 29 (69%) наблюдениях. Из них у 4 (13,8%) больных были выполнены резекционные вмешательства, каких-либо проблем с процессом заживления паренхимы печени не было. Хорошие результаты были также и у 4 (13,8%) пациентов, перенесших ЭЭ с абдоминизацией ОПП. А у остального 21 (72,4%) больного хороший результат был получен после следующих операций ЭЭ: с оментопластикой ОПП (2 из 3), капитонажем ОПП (3 из 5), полным ушиванием ОПП (гепатизация) (2 из 7), полузакрытой ЭЭ (3 из 6).
У 10 (23,8%) больных результат расценен как удовлетворительный, так как имелись ОПП размерами до 3,5-5 см. Из них у 5 больных ОПП нагноились, что потребовало интервенционного подхода - пункционно-аспирационное лечение под контролем УЗИ. В этих 10 наблюдениях с удовлетворительным отдаленным результатом у одного ликвидация ОПП была осуществлена методом капитонажа, еще у одного после полного ушивания ОПП, у 8 больных была выполнена полузакрытая ЭЭ.
Из изученных 42 больных второй группы у 3 (7,2%) отдаленные результаты хирургического лечения ЭКП нами были расценены как неудовлетворительные. У 2 из них развился рецидив болезни через 3,5 и 5 месяцев. Они были повторно оперированы методом полузакрытой ЭЭ. В одном наблюдении после ЭЭ с оментопластикой развилась спаечная болезнь брюшной полости, которая разрешалась консервативными мерами. Следует отметить, что представленные результаты изучения отдаленных исходов оперативного лечения ЭКП традиционным, лапаротомным доступом не являются репрезентативными ввиду малого числа наблюдений, и это не входило в наши задачи.
Диагностика и лечение нагноившихся кист, расположенных в зоне 7-8 сегментов печени
Введение. К одной из самых сложных локализаций паразитарных кист относят 7 и 8 сегменты печени [1,2]. Это связано с тем, что при этом расположении кист заболевание длительное время ничем себе не проявляет и только с увеличением размеров, а затем с присоединением такого осложнения как нагноение, появляются признаки поражения печени [4,5]. Основным методом диагностики является ультразвуковое исследование (УЗИ), а в затруднительных случаях многие исследователи рекомендуют выполнять компьютерную томографию, которая существенно помогает уточнить диагноз, избрать наиболее адекватный оперативный доступ и наметить план операции [6,7].
К настоящему времени детально разработана техника операции, особенности выполнения всех этапов операции, но, несмотря на достижения, частота послеоперационных осложнений после эхинококкэктомии при осложненных формах эхинококкоза печени поддиафрагмальной локализации (зона 7-8 сегментов) остается на высоком уровне [2,4].
Цель работы - представить результаты оперативного лечения нагноившихся паразитарных кист печени с локализацией в зоне 7-8 сегментов.
Материалы и методы исследования. Под наблюдением находилось 152 больных с поддиафрагмальной локализацией кист, осложненных нагноением, из них у 76 (50%) кисты локализовались в зоне 7 и 8 сегментов печени. Больные оперированы в период с 2009 по 2014 г. включительно. Чаще поступали женщины в сравнении с мужчинами (соответственно 42 и 34), возраст в обеих группах колебался от 18 до 62 лет. Давность заболевания составляла от двух недель до 5 лет.
В обследовании больных использовали общий анализ крови, показатели функционального состояния печени и почек (билирубин, тимоловая проба, трансаминазы, общий белок, мочевина, креатинин), УЗИ по общепринятой методике и компьютерная томография по показаниям. Пациентам с первичным эхинококкозом ставили кожно-аллергическую реакцию Казони с апирогенным антигеном разработанным Б.А.Акматовым и соавт. [3].
При поступлении основными жалобами больных были слабость, повышение температуры, боли в правом подреберье и в области грудной клетки, усиливающиеся при глубоком вдохе, одышку (12 чел.). При объективном обследовании у 56 отмечено увеличение границ печени, особенно вверх, у 22 пальпировалась резко болезненная печень.
Основным методом диагностики было УЗИ, при котором определяли размеры кист, их количество и локализацию. Из 76 одиночные кисты обнаружены у 62, а у 14 с локализацией кист в 7-8 сегментах также выявлены кисты в других отделах печени. УЗИ выполняли до операции и в послеоперационном периоде для своевременного выявления осложнений (поддиафрагмальный, подпеченочный абсцесс, плеврит).
До операции выполняли рентгенографию грудной клетки в двух проекциях (прямую и боковую), при этом определяли уровень стояния диафрагмы, состояние легких и наличие объемного образования в печени при обызвествлении от отдельных участков фиброзной капсулы.
При нагноении кист при УЗИ выявляли утолщение стенки кист с наличием негомогенного содержимого и нередко (13 чел.) с воспалением окружающих кисты тканей. Из 76 диагноз эхинококкоза был поставлен 70, а у 6 - для уточнения диагноза выполнена компьютерная томография, которая позволила уточнить не только характер заболевания, но и связь кисты с сосудистыми и протоковыми структурами и избрать наиболее оптимальный оперативный доступ. При УЗИ мы определяли размер кисты, характер содержимого, локализацию, высоту стояния диафрагмы, соотношение кисты к поверхностям и краям печени, измеряем прослойку истонченной части паренхимы над кистой, определяли подвижность диафрагмы. Если кисты располагались в зоне 7-8 сегментов, толщина паренхимы печени над кистой 1-2 см, диафрагма подвижна, то эхинококкэктомию выполняли из разреза по Федорову или Кохеру с рассечением связок печени. Если кисты располагались в зоне 7-8 сегментов печени, диафрагма неподатлива и ее уровень до 3-4 ребра, что свидетельствует о сращении печени с диафрагмой и паренхимы печени над кистой не более 1 см, то использовали торакальный доступ. Придерживаясь этих критериев выборы доступа, мы не наблюдали сложностей при выполнении эхинококкэктомии при поддиафрагмальной локализации кист.
Результаты и их обсуждение. В результате выполненых исследований у 76 определен характер заболевания эхинококкоз поддиафрагмальной локализации. На протяжении 2-3 дней проводилась предоперационная подготовка, которая включала инфузионную терапию (реополиглюкин, глюкозу, комплекс витаминов). После непродолжительной подготовки все пациенты оперированы под эндотрахеальным наркозом.
Особое внимание было обращено на выбор оперативного доступа. При больших и гигантских нагноившихся кистах выполняли торакальный доступ (22 чел.), он обеспечивал тщательную обработку кисты, удаление содержимого, выявление желчных свищей и ликвидацию полости фиброзной капсулы.
В тех случаях, когда поддиафрагмальная локализация кист сочеталась с другой локализацией (14 чел.) и при одиночных кистах с подвижной диафрагмой, что указывало на отсутствие сращений кист с диафрагмой - мы использовали подреберный доступ по Федорову с пересечением связок печени (44 чел.), это создавало возможность выполнить обеззараживание плодоносных элементов кист и ликвидацию полости фиброзной капсулы.
При открытом способе мы стремились уменьшить объем полости фиброзной капсулы путем наложения ряда швов, а затем в полость подводили связку дренажей (2-3, иногда 4) и выводили через дополнительные разрезы и сразу подключали активную аспирацию содержимого полости. Один-два раза в сутки через дренажи вводили озонированный раствор для санации полости и через час после введения вновь осуществляли активную аспирацию. Это предотвращало закупорку дренажей и позволяло добиться санации полости с последующей ее облитерацией. Кроме дренирования полости фиброзной капсулы обязательно дренировали поддиафрагмальное пространство, из которого дренаж удаляли на 2-3 сутки. Дренажи из полости фиброзной капсулы удаляли последовательно: на 4 сутки один дренаж, на 5-6-е сутки еще один и последний дренаж удаляли после полного прекращения выделения отделяемого. Через 1-2 дня выполняли УЗИ, чтобы проследить за состоянием полости.
У 14 больных кисты поддиафрагмальной локализации сочетались с расположением кист в других сегментах печени, у них для ликвидации полости фиброзной капсулы использовали способ абдоминизации, сущность которого заключалась в иссечении капсулы кисты выступающей над печенью до ткани печени, накладываем на края иссеченной капсулы обвивной гемостатический шов, осматриваем полость, при наличии желчных свищей ушиваем их (2 чел) и полость оставляем открытой, но к ней касательно подводим один-два страховых дренажа. Послеоперационный период при использовании абдоминизации протекал благоприятно, лишь у одного больного на 3 сутки из страхового дренажа стала выделяться серозная жидкость с примесью желчи, но затем выделение прекратились, дренаж удален, при контрольном УЗИ скопление жидкости не обнаружено, он был выписан в удовлетворительном состоянии. При обследовании через 3 месяца патологии не обнаружено.
Для профилактики осложнений за 30 минут до операции вводили внутривенно 1,0 цефазолина и к концу операции повторяли введение, а затем после операции продолжали вводить антибиотик еще 4-5 дней, а также выполняли инфузионную терапию, направленную на нормализацию функции печени ( реополиглюкин, гептрал, комплекс витаминов, раствор глюкозы и др.).
После операции осложнения возникли у 6 больных, что составило 7,8%. На 3 сутки после операции выявлен плеврит у 3 больных, выполняли плевральную пункцию, затем накопление жидкости прекратилось. К моменту выписки при контрольном УЗИ выпота в плевральной полости не было. У одной больной на 4-е сутки после операции через дренаж, стоявший в полости фиброзной капсулы, стала выделяться серозно-геморрагическая жидкость с примесью желчью, но постепенно количество отделяемого уменьшилось, и когда выделение прекратилось, дренаж был удален. При УЗИ - патологии не обнаружено. У одной больной течение послеоперационного периода осложнилось пневмонией, была усилена противовоспалительная терапия. У одного больного в области операционной раны выявлен инфильтрат, который под влиянием физиотерапии был излечен.
При выписке из стационара всем выполнено УЗИ, при котором у одного обнаружена остаточная полость размером 2,5х3,0 см, но без наличия жидкости. Все оперированные выписаны в удовлетворительном состоянии. Среднее пребывание в стационаре составило 8,8±1,2 койко-дня.
В процессе работы мы проследили и за динамикой функционального состояния печени и почек (табл. 1).
Таблица 1. Показатели функционального состояния печени и почек у больных с поддиафрагмальной локализаций кист (n=76)
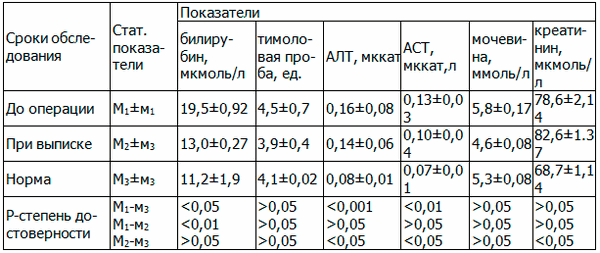
Примечание: АЛТ - аланинаминотрансфераза; АСТ - аспартатаминотрансфераза.
При анализе полученных данных отмечено, что до операции имело место повышения уровня билирубина и трансаминаз, а функциональное состояние почек не нарушено. К моменту выписки из стационара отмечен нормальный уровень билирубина, тимоловой пробы и показателей функции почек, были достоверные различия лишь в показателях трансаминаз, они оказались повышенными в сравнении с нормой. Следовательно, при нагноившемся эхинококкозе поддиафрагмальной локализации имеет место нарушения функции печени, к моменту выписки показатели улучшились, но не достигают нормы.
Таким образом, наши наблюдения показали, что при локализации паразитарных кист в зоне 7-8 сегментов печени с нагноением, улучшения результатов лечения можно добиться использованием индивидуального подхода к выбору доступа, способа ликвидации полости фиброзной капсулы и выполнения мер профилактики осложнений.
Доступ и ход операции удаления эхинококковой кисты печени
Представлены результаты лечения 44 больных с эхинококкозом печени. Выделены 2 группы больных: основная — 18 пациентов и сравнения — 26 пациентов. Ведение пациентов основывалось на разработанном алгоритме диагностики и лечения больных с эхинококковыми кистами печени. В основной группе лечение заключалось в чрескожной пункции и дренировании эхинококковых кист печени под ультразвуковым наведением. В группе сравнения выполнены хирургические вмешательства, используя трансабдоминальный доступ.
Surgical treatment of patients with hepatic echinococcosis
Results of treatment of 44 patients with hepatic echinococcosis during the period of 1997-2011 years are presented. Two groups of patients were allocated: the basic — 18 patients, and comparison group — 26 patients. Management of patients was based on the developed algorithm of diagnostic and treatment of hepatic echinococcosis. The basic group treatment consisted of transcutaneous puncture and drainage of hydatid hepatic cysts under ultrasound directing. In the comparison group performed surgery interferences using transabdominal access.
В настоящее время общепризнано, что основным и наиболее эффективным в лечении больных с эхинококковыми кистами печени (ЭКП) остается хирургический метод [1, 2]. Вместе с тем в последнее десятилетие традиционному оперативному методу лечения больных с ЭКП появилась альтернатива, основанная на малоинвазивных технологиях, заключающаяся в чрескожной пункционно-аспирационной эхинококкэктомии под УЗ наведением 1.
Задача исследования заключалась в улучшении результатов хирургического лечения больных с эхинококкозом печени.
Материалы и методы
В период с января 1997 г. по декабрь 2011 г. в клинике хирургических болезней № 1 КГМУ на базе отделения абдоминальной хирургии РКБ МЗ РТ находились на лечении 44 пациента с эхинококкозом печени: 18 пациентов составили основную группу, 26 — группу сравнения. В группе сравнения выполнялись традиционные хирургические операции, в основной группе чрескожные пункции и дренирование эхинококковых кист печени под УЗ наведением.
Традиционное хирургическое лечение проведено 26 пациентам с гидатидозным эхинококкозом печени. Возраст больных от 16 до 79 лет, из них женщин — 16 (61,5%), мужчин — 10 (38,5%). Одиночные паразитарные кисты печени наблюдались в 19 случаях (73%), две и более — в 7 (27%), размеры варьировали от 2.0 до 24.0 см в диаметре. При солитарном эхинококкозе печени поражение правой доли печени отмечалось у 17 (65,4%) больных. Первичный эхинококкоз был выявлен у 20 (77%) больных, рецидив — у 5 (19,2%), резидуальный — у 1 (3,8%) больного.
При хирургических вмешательствах производили эхинококкэктомию (16), эхинококкотомию (3), резекцию пораженной части печени (3), правостороннюю гемигепатэктомию (3), марсупиализацию (1), чаще из срединного доступа (22). У 4 (15,3%) больных одновременно с операцией на печени были выполнены эхинококкэктомия из брюшной полости — 1 (3,8%), холецистэктомия — 2 (7,7%), спленэктомия — 1 (3,8%).
Атипичная (клиновидная) резекция печени выполнена у 3 (11,5%) пациентов с периферическим расположением небольшой эхинококковой кисты, что является радикальным хирургическим вмешательством. При тотальном и множественном поражении одной из долей печени выполняли гемигепатэктомию — 3 наблюдения (11,5%). Эхинококкотомия произведена 3 (11,5%) больным. Однако эту операцию не всегда удается выполнить ввиду высокой вероятности повреждения крупных сосудов и желчных протоков. Вынужденная марсупиализация остаточной полости выполнена 1 (3,8%) больному с осложненным эхинококкозом печени.
Комбинированная эхинококкэктомия применялась при множественном поражении печени у 3 (11,5%) пациентов, когда количество паразитарных кист было более двух. Наружное дренирование остаточной полости выполняли при внутрипеченочном расположении солитарных эхинококковых кист неправильной формы, при невозможности устранения остаточной полости ушиванием, ввиду технических трудностей и опасностью повреждения важных анатомических структур печени. После эхинококкэктомии, производили дренирование остаточной полости полихлорвиниловой трубкой 24-27 Fr с боковыми отверстиями. После операции через дренажную трубку проводилась фистулография для контроля динамики облитерации. Дренажная трубка удалялась после полной облитерации остаточной полости в среднем через 1,5-2 месяца.
Поддиафрагмальное расположение эхинококковых кист печени является наименее удобным для выполнения оперативных вмешательств. Именно при такой локализации эхинококковых кист в послеоперационном периоде часто отмечаются застой раневого отделяемого и формирование поддиафрагмальных абсцессов, что обуславливает необходимость широкого дренирования поддиафрагмального пространства.
Анализ результатов хирургического лечения пациентов с эхинококкозом печени показал отсутствие специфических ранних послеоперационных осложнений (РПО) у больных, которым была выполнена «идеальная эхинококкэктомия». Наибольшее количество послеоперационных осложнений наблюдалось у больных, которым произведены эхинококкотомия и резекция печени.
При анализе результатов традиционного хирургического лечения эхинококкоза печени установлено, что осложнения общего характера наблюдались у 3 больных (11,5%), а местные осложнения 8 (30,8%). Причиной развития в 2 наблюдениях экссудативного плеврита послужило поддиафрагмальное расположение эхинококковой кисты и наличие сращений фиброзной капсулы с диафрагмой. Показаниями к повторной операции у 2 (7,7%) пациентов послужили внутреннее кровотечение и подпеченочный абсцесс.
Средняя длительность пребывания в стационаре в группе сравнения составила 29,6±5,4 койко-дня. В ходе проведенного исследования нами проанализированы отдаленные результаты лечения. К рецидивам нами были отнесены случаи повторного заболевания в сроки до 3 до 5 лет, после перенесенного оперативного вмешательства. Более поздние рецидивы, расценивались как реинвазия эхинококка. Среди 26 оперированных больных случаев рецидивного эхинококкоза было 3 (11,5%), что согласуется с данными Ф.Г. Назырова (1999) и Б.И. Альперовича (2010) [4, 5].
На основании анализа результатов хирургического лечения пациентов с эхинококкозом печени, следует отметить, что до настоящего времени традиционный хирургический метод лечения остается основным. Данное оперативное пособие рекомендуется при больших эхинококковых кистах печени с множественными дочерними пузырями, при поверхностно расположенных кистах с риском разрыва, при осложненных кистах, при кистах, сдавливающих жизненно важные органы.
С 2001 года в РКБ МЗ РТ аспирационная эхинококкэктомия под УЗ наведением выполнена 18 больным (основная группа) с ЭКП в возрасте от 16 до 79 лет. Мужчин было 8 (44,4%), женщин — 10 (55,6%). Средний возраст больных составил 43,4±1,8 года.
Размеры эхинококковых кист в основной группе варьировали от 3,5 до 10 см. У 12 (66,7%) больных было поражение правой доли, у 6 (33,3%) — левой. Рецидивная форма эхинококкоза печени установлена у 3 (16,7%) человек, в 18 (100%) наблюдениях интрапаренхиматозная локализация эхинококковой кисты. У 10 (55,6%) пациентов эхинококковые кисты были с признаками нагноения.
Показаниями для данного вмешательства были изолированные эхинококковые кисты, не превышающие в диаметре 100 мм, расположенные в толще паренхимы, особенно у ослабленных больных, отказывающихся от проведения традиционного хирургического лечения, пациенты с высоким операционно-анестезиологическим риском, нагноившиеся формы эхинококкоза печени.
Оперативные вмешательства под ультразвуковым (УЗ) наведением выполнялись под местной анестезией или внутривенным потенцированием. После проведения обзорного ультразвукового исследования (УЗИ) выбирается траектория движения инструмента, которая может быть линейной или «ломаной». Применялась техника PAIR-PD (puncture, aspiration, injection, reaspiration, percutaneous drainage) [6]. Для дренирования кисты использовали метод стилет-катетер. После попадания в полость ЭКП стилет извлекали, а дренаж фиксировали к коже. Использовали изогнутые дренажные катетеры 12-18 Fr, а также типа «свиной хвост». Через катетер производили максимальную аспирацию содержимого кисты. Далее полость неоднократно промывали раствором NaCl (30%). Интраоперационных осложнений не было. В раннем послеоперационном периоде у одного пожилого пациента развилась правосторонняя нижнедолевая пневмония, еще в одном наблюдении произошло нагноение остаточной полости. В наших наблюдениях у 8 больных с нагноившейся ЭКП достигнута полная эвакуация хитиновой оболочки во время выполнения манипуляции. Сроки полной эвакуации хитиновой оболочки при нагноившихся формах ЭКП в среднем составили 16,3±2,4, а в остальных случаях — 22,2±3,4 дня. Средний срок пребывания больных в стационаре при чрескожных вмешательствах составил 13±2,1 койко-дня. Летальных исходов в данной группе больных не было.
Специфическое медикаментозное лечение проводили альбендазолом в дозе 10-13 мг/кг в сутки. Для профилактики рецидива препарат назначали, как правило, одним курсом продолжительностью 28 дней. В отдельных наблюдениях проводили либо непрерывный курс 56-60 дней, либо 3 последовательных курса по 28 дней с межкурсовым интервалом 7-10 дней. Для лечения первичных и рецидивных кист назначали не менее 3 курсов по 28 дней.
Средний срок пребывания больных в стационаре при чрескожных вмешательствах составил 13,0±2,1 койко-дня. На основании оценки отдаленных результатов (6 месяцев — 5 лет) применения чрескожной пункционно-аспирационной эхинококкэктомии под УЗ наведением удовлетворительный результат был отмечен у всех пациентов. Данных за рецидив заболевания не обнаружено. При УЗИ у 15 больных (83,3%) отмечена полная инволюция кисты, а у 3 (16,7%) — сохранились небольшие остаточные полости.
Методы малоинвазивных вмешательств имеют большое преимущество перед традиционными операциями: малая травматичность, ранняя активизация больных, снижение количества послеоперационных осложнений, уменьшение пребывания пациентов в стационаре. Особое значение малоинвазивные технологии приобретают в лечении ЭКП у пожилых больных, страдающих тяжелыми сочетанными заболеваниями, высоком операционном риске. В то же время считаем, что ошибочно преувеличивать значимость этих методов, как основного пособия, при лечении больных с данной патологией. На современном этапе развития хирургии возникает необходимость в переосмыслении и унификации тактики при применении традиционных вмешательств, с учетом внедрения в практику новых технологий. Накопленный нами опыт использования пункционно-аспирационной эхинококкэктомии позволяет рекомендовать данный метод лечения к более широкому применению по строго обоснованным показаниям, а также при дальнейшем совершенствовании техники операций и её инструментального обеспечения.
А.П. Толстиков, А.В. Абдульянов, М.А. Бородин
Казанский государственный медицинский университет
Толстиков Алексей Петрович — ассистент кафедры хирургических болезней № 1
Литература:
1. Вишневский В.А., Кахаров М.А., Камолов М.М. Радикальные операции при эхинококкозе печени // Актуальные вопросы хирургической гепатологии: Сб. тезисов XII Международного конгресса хирургов-гепатологов стран СНГ. — Ташкент, 2005. — С. 106.
2. Рудаков В.А., Полуэктов Л.В. Криохирургия в лечении эхинококкоза и непаразитарных кист печени // Анналы хир. гепатол. — 1997. — № 2. — С. 20-24.
3. Борисов А.Е. Руководство по хирургии печени и желчевыводящих путей. — СПб: Предприятие ЭФА, 2002. — 448 с.
4. Назыров Ф.Г., Исмаилов Д.А., Леонов В.Ф. Эхинококкоз. — Ташкент, 1999. — 207 с.
5. Альперович Б.И. Хирургия печени / Б.И. Альперович. — М.: ГЭОТАР Медиа, 2010. — 352 с.
6. Гаврилин А.В., Кунцевич Г.И., Вишневский В.А. Пункционный метод лечения эхинококковых кист печени под контролем ультразвукового исследования // Хирургия. — 2002. — № 8. — С. 39-46.
Эхинококкэктомия печени
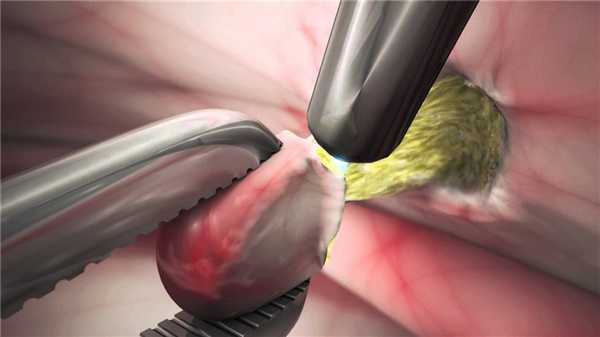
Эхинококкэктомия печени - операция предпринимаемая по поводу эхинококкоза печени-паразитарного ее заболевания, заключающаяся в удалении паразитарной хитиновой оболочки и обработки полости паразитарной кисты.
Лучшим методом лечения эхинококкоза печени многие годы остается эхинококкэктомия. Полную эхинококкэктомию, при которой удаляется киста без дополнительного вскрытия ее просвета, используют редко - при краевом расположении и небольших размерах кисты. Зачастую кисту удаляют вместе с хитиновой и герминативной оболочкой после проведенной пункции полости кисты, аспирации содержимого и дальнейшей обработки полости различными противопаразитарными средствами. Этот метод позволяет избежать при выделении разрыва кисты, тем самым предотвратив диссеминацию зародышей эхинококка.
Фиброзную оболочку после удаления кисты дополнительно обрабатывают раствором глицерина (концентрированным, 85%) или раствором хлорида натрия (20%). После чего полость кисты ушивается изнутри отдельными швами и внутри полости вворачиваются наружные края фиброзной капсулы. В стенках толстой и плотной фиброзной капсулы зачастую остаются мелкие дочерние пузыри. Поэтому при нормальных анатомических условиях рекомендуется проводить перицистэктомию - полное иссечение фиброзной капсулы, что сделает операцию крайне радикальной, но более опасной и трудной для выполнения.
Читайте также:
