Эффективность вакцин. Эпидемиологические методы оценки эффективности вакцинации.
Добавил пользователь Алексей Ф. Обновлено: 01.02.2026
Данная статья публикуется в рамках серии публикаций ВОЗ «Все о вакцинах», посвященной различным аспектам создания и применения вакцин. В серии публикаций ВОЗ «Все о вакцинах» вы узнаете о том, как действуют вакцины, как их производят и как обеспечивается их безопасность и справедливое распределение.
Доказано, что вакцины против COVID-19 безопасны, эффективны и могут спасти жизнь. Как и любые другие вакцины, они не гарантируют полной защиты, и пока неизвестно, в какой степени они позволяют предотвратить передачу вируса привитыми людьми окружающим. Поэтому, помимо вакцинации, для борьбы с пандемией мы должны продолжать соблюдать остальные профилактические меры.
Эффективность вакцины в контролируемых и реальных условиях
Все вакцины против COVID-19, одобренные ВОЗ для применения в условиях чрезвычайной ситуации, прошли рандомизированные клинические испытания, в ходе которых были проверены их качество, безопасность и эффективность. Для получения одобрения вакцина должна продемонстрировать высокие показатели эффективности на уровне не ниже 50% в ходе контролируемых испытаний. После одобрения вакцин их безопасность и эффективность в реальных условиях являются объектом непрерывного мониторинга. Но в чем разница между эффективностью в контролируемых и реальных условиях?
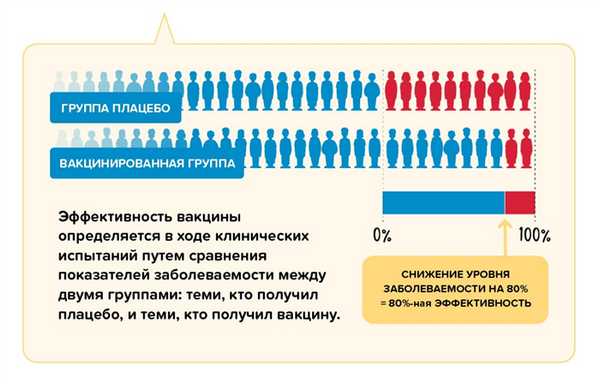
Эффективность вакцины в контролируемых условиях клинических испытаний измеряется путем сравнения количества людей, которые получили вакцину и у которых наступил т.н. «интересующий исход» (как правило, заболевание), с количеством людей, получивших плацебо (фиктивную вакцину), у которых наступил тот же исход. По завершении исследования сравнивается число заболевших в обеих группах, и рассчитывается относительный риск заболевания в случае вакцинации и в случае ее отсутствия. Так мы получаем показатель эффективности вакцины в контролируемых условиях - то, в какой мере вакцина позволяет снизить риск заболевания. Если в группе, получившей вакцину, заболело намного меньше людей, чем в группе, получившей плацебо, делается вывод о высокой эффективности вакцины.
Например, предположим, что у нас есть вакцина с доказанной эффективностью на уровне 80%. Это означает, что среди участников клинического исследования у получивших вакцину риск заболеть был на 80% ниже, чем у тех, кто получил плацебо. Этот показатель рассчитывается путем сравнения числа случаев заболевания в группе привитых и в группе получивших плацебо. Показатель эффективности 80% не означает, что 20% из группы вакцинированных непременно заболеет.
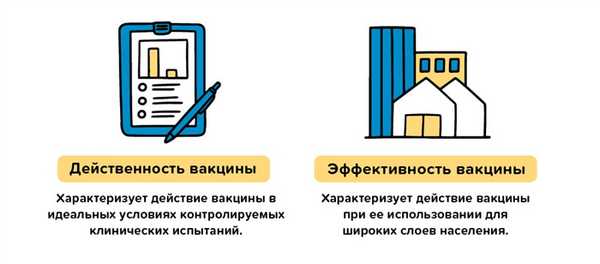

Эффективность вакцины в реальных условиях описывает то, насколько эффективно вакцина действует на практике. В клинических исследованиях участвует широкая выборка людей разных возрастных групп, обоих полов, разной этнической принадлежности, а также лица с хроническими заболеваниями, однако даже такая широкая выборка не может быть идеальной моделью всего населения. В условиях клинических испытаний оценивается эффективность препарата в отношении определенных исходов. В реальных же условиях оценивается то, насколько успешно вакцинация позволяет защитить здоровье населения в целом. Показатель эффективности в реальных условиях может отличаться от показателя эффективности, полученного в контролируемых условиях, поскольку невозможно заранее предсказать, насколько эффективной будет вакцинация намного более широкой и разнообразной массы населения на практике.
Уровень и скорость формирования иммунитета
Вакцины формируют сильный иммунитет, но для этого требуется определенное время. Для получения полной защиты необходимо сделать все обязательные дозы прививки. При использовании двухкомпонентных вакцин одна доза обеспечивает только частичную защиту, поэтому для повышения иммунитета к болезни требуется введение второй дозы. Для выработки максимального иммунного ответа требуется определенное время - несколько недель после второй прививки. В случае использования однокомпонентной вакцины максимальный иммунитет формируется через несколько недель после вакцинации.

Защита, обеспечиваемая вакцинацией, и риск заражения
Вакцины защищают от заболевания COVID-19 большинство привитых, но не каждого.
Даже в случае полной вакцинации и по прошествии нескольких недель, необходимых для формирования стойкого иммунитета, вероятность заражения вирусом сохраняется. Вакцины не обеспечивают полной (100%) защиты, поэтому иногда, несмотря на полный курс вакцинации, случаи заражения вирусом все-таки случаются.
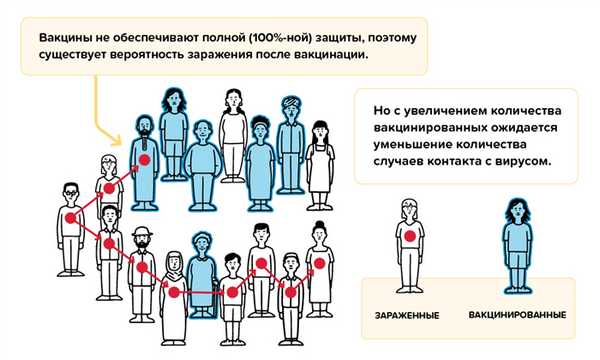
В случае заражения у прошедших вакцинацию отмечаются, как правило, только легкие симптомы болезни, и в целом привитые пациенты очень редко тяжело болеют или умирают от инфекции.
Защита, обеспечиваемая вакцинацией, и риск передачи инфекции
Вакцинация против COVID-19 - важнейшее средство борьбы с пандемией, которое защищает от тяжелых форм болезни и смерти. Вакцинация обеспечивает, по крайней мере, некоторую защиту от заражения и передачи инфекции, однако уровень этой защиты не так высок, как уровень защиты от тяжелых форм болезни или смерти. Чтобы точно определить, в какой мере вакцины защищают от заражения и передачи инфекции, требуется больше данных.
После вакцинации необходимо продолжать соблюдение таких простых мер предосторожности и профилактики, как физическое дистанцирование, ношение масок, проветривание помещений, отказ от посещения мест массового скопления людей, мытье рук и респираторный этикет (прикрывание рта и носа при кашле локтевым сгибом или салфеткой). Если вам кажется, что вы нездоровы, пройдите тестирование, даже если вы прививались против COVID-19. Следуйте рекомендациям местных органов здравоохранения. Соблюдайте все профилактические меры!

Защита, обеспечиваемая вакцинацией, и новые варианты вируса
В условиях роста заболеваемости и ускорения распространения вируса повышается вероятность возникновения новых опасных и более заразных вариантов вируса, способных более легко передаваться между людьми или вызывать более тяжелое заболевание.
Исходя из имеющихся на сегодняшний день данных, вакцины демонстрируют эффективность против известных вариантов вируса, особенно в том, что касается профилактики тяжелого заболевания, госпитализации и смерти. Однако перед лицом некоторых вариантов вируса обеспечиваемая вакцинами защита от легких форм заболевания и заражения несколько снижается.
Вакцины, скорее всего, остаются по-прежнему эффективными против новых вариантов вируса ввиду вызываемого ими широкого иммунного ответа, и поэтому изменения или мутации вируса едва ли приведут к полной потере вакцинами своей эффективности.
ВОЗ продолжает постоянно анализировать новые данные и будет обновлять свои рекомендации по мере поступления новой информации. Узнать актуальную информацию о том, что мы знаем о новых вариантах COVID-19, можно в еженедельных эпидемиологических сводках ВОЗ, а также в пояснительном материале «Варианты вируса и их влияние на вакцины против COVID-19».
Один из лучших способов защиты от новых вариантов вируса - продолжать соблюдать проверенные профилактические меры и расширять охват вакцинацией. Все вакцины против COVID-19, одобренные ВОЗ для применения в условиях чрезвычайной ситуации, прошли тщательные испытания, в ходе которых была доказана их способность формировать высокий уровень защиты от тяжелых форм заболевания или смерти. В условиях появления более опасных вариантов вируса крайне важно при первой возможности привиться от COVID-19.
Критерии оценки эффективности вакцинации
Что такое иммунологическая и эпидемиологическая эффективность вакцинации? Какие показатели используются при оценке эпидемиологической эффективности вакцинации? В каких случаях при оценке эффективности вакцинации используют когортный метод и метод «с
Что такое иммунологическая и эпидемиологическая эффективность вакцинации?
Какие показатели используются при оценке эпидемиологической эффективности вакцинации?
В каких случаях при оценке эффективности вакцинации используют когортный метод и метод «случай-контроль»?
Эффективность иммунопрофилактики многих инфекционных болезней доказана многолетней мировой практикой. Сегодня представляется бесспорным тот факт, что вакцинопрофилактика является наиболее мощным методом борьбы с инфекционной патологией. Накопленные данные убедительно свидетельствуют о том, что риск неблагоприятных реакций на введение современных вакцин несоизмеримо ниже, чем при возникновении соответствующей инфекции. Триумфом вакцинации явилась эрадикация оспы во всем мире. После определенного периода «благополучия» наблюдается увеличение заболеваемости многими хорошо и давно известными инфекционными болезнями (чума, холера, дифтерия, туберкулез, малярия и др.); за последние 20 лет открыто около 30 новых возбудителей и болезней человека. Причиной «возвращения» многих болезней следует считать неблагоприятное влияние комплекса социально-экономических и экологических факторов, среди которых не последнее место занимает и свертывание программ иммунизации населения. В частности, применительно к России можно говорить о наличии неоправданно большого числа противопоказаний для вакцинации детей, необоснованных отказов и отводов от прививок, широкой кампании в прессе против вакцинации, массовом использовании препаратов с уменьшенным содержанием антигенов, несоблюдении «холодовой цепи». Все это привело к формированию низкой иммунной прослойки населения и росту заболеваемости рядом инфекционных болезней, управляемыми средствами иммунопрофилактики. Страна пережила эпидемию дифтерии, крупную вспышку полиомиелита, повысилась заболеваемость корью, коклюшем, эпидемическим паротитом. Такое неблагополучие нельзя объяснить только социальными переменами последних лет — «прослойка» невакцинированных детей формировалась в течение последних двух десятилетий.
Вакцинация относится к числу мероприятий, требующих значительных материальных затрат, поскольку предусматривает охват прививками широких слоев населения. В связи с этим важно иметь правильное представление об эффективности иммунизации. Эффективность иммунизации оценивается по трем группам критериев:
- показатели документированной привитости (охват прививками),
- показатели иммунологической или клинической эффективности,
- показатели эпидемиологической или полевой эффективности.
Показатели охвата прививками позволяют косвенно оценить возможное состояние популяционного иммунитета. Объективными критериями качества вакцинного препарата, а также состояния защищенности коллектива против того или иного инфекционного заболевания являются показатели иммунологической (клинической) и эпидемиологической (полевой) эффективности. По степени иммунологической эффективности можно судить о том, «работает» ли вакцина, в то время как эпидемиологическая эффективность позволяла сделать вывод, «помогает ли прививка людям» [5, 7]. Иными словами, иммунологическая эффективность вакцины и эффективность иммунизации как профилактического мероприятия — разные понятия. Если под иммунологической эффективностью вакцины принято понимать способность препарата вызывать выработку иммунитета у привитого человека, то эффективность иммунизации оценивается на основании различия в заболеваемости в группе привитых и непривитых лиц [3, 4].
Сбор сведений о вакцинированности осуществляется на уровне педиатрического участка по данным журналов профилактических прививок (ф. 064-у), карт профилактических прививок (ф. 063-у), истории развития ребенка (ф. 112-у), сертификата о профилактических прививках (ф. 156-у). Эта информация передается в территориальные центры Госсанэпиднадзора, последние анализируют ее по территориям и переадресуют вышестоящим учреждениям. Оценка привитости проводится на основании изучения величины охвата прививками лиц декретированного возраста в соответствии с действующим календарем профилактических прививок, утвержденным приказом МЗ РФ № 375 от 18.12.1997 г. Нормативными показателями охвата прививками в возрастных группах детей до трех лет следует считать 95%, в старших возрастных группах — 97-98%. Опыт борьбы с оспой показал, что 80-90%-ный охват прививками недостаточен для ликвидации инфекции. Оспу удалось ликвидировать лишь тогда, когда было привито 99% населения. Это обстоятельство важно учитывать при решении задачи ликвидации других инфекций.
Среди болезней, с которыми реально можно бороться средствами активной иммунизации, видное место занимают корь, краснуха и паротит. Вакцинопрофилактика привела к существенному снижению показателей заболеваемости этими инфекциями; среди заболевших уменьшился удельный вес детей прививаемых возрастов, снизились очаговость и пораженность детских дошкольных учреждений. Особенно заметные успехи в этом плане достигнуты в ряде стран за последние два-три десятилетия, что позволило прогнозировать ликвидацию данных заболеваний. В России в последние годы отмечается рост заболеваемости этими инфекциями.
Оценка иммунологической эффективности осуществляется выборочно среди различных групп населения и прицельно в индикаторных группах населения (получающих в соответствии с возрастом прививки), а также в группах риска (детские интернаты, дома ребенка и др.). Основные требования, предъявляемые к иммунологическим исследованиям, сводятся к следующему:
- короткий промежуток времени, в течение которого исследуются все сыворотки;
- стандартность диагностических препаратов, сыворотки и диагностикумов;
- высокая чувствительность иммунологического теста для определения антител [4]. Для этого используется весь арсенал серологических исследований (РНГА, РТГА, ИФА и др.). Выбор теста для оценки иммунологической эффективности вакцины зависит от характера иммунитета при данной инфекции. Например, для столбняка, дифтерии, кори, паротита критерием эффективности вакцины является определение уровня циркулирующих антител, а для туберкулеза, туляремии и бруцеллеза — клеточные реакции, например кожные пробы замедленного типа. К сожалению, для большинства инфекций, в основе которых лежит клеточный иммунитет, защитные уровни клеточных реакций не установлены.
Изучение иммунологической эффективности вакцин проводится путем сопоставления титров специфических антител в сыворотке крови привитых до и в разные сроки после иммунизации, а также путем сравнения этих результатов с данными уровня антител, полученными в те же сроки при обследовании лиц, которым вводили плацебо или препарат сравнения. Плацебо помещают в точно такие же ампулы или флаконы, как и изучаемую вакцину. В ряде случаев целесообразно, исходя из этических соображений, использовать вместо плацебо вакцины, предназначенные для профилактики других инфекционных заболеваний. При этом схема иммунизации, дозировка и место введения препарата должны быть такими же, как и в группе испытуемых.
Необходимость проведения подобных исследований определена неоднозначностью понятий «привит» и «защищен». Имеющийся опыт свидетельствует о том, что эти понятия далеко не всегда совпадают. Это было отмечено рядом авторов, когда речь шла о дифтерии, кори и эпидемическом паротите. Как показали исследования, проведенные сотрудниками НИИ вирусных препаратов РАМН [2] в ряде детских коллективов Москвы и в других районах страны, около 40% детей дошкольного и младшего школьного возраста не имели антител к вирусу эпидемического паротита и, таким образом, были подвержены значительному риску развития этого заболевания.
Иммунологическая активность вакцины может отражать ее профилактическую эффективность в том случае, если известен защитный уровень иммунологических показателей при данной инфекции. Защитный уровень антител устанавливается заранее в опытах с однонаправленным препаратом. Для каждой инфекции определяется свой защитный титр антител: для кори, паротита и гриппа он равен 1:10; для столбняка 1:20; для дифтерии 1:40 по РПГА; для коклюша 0,03 МЕ/мл; гепатита В 0,01 МЕ/мл по иммуноферментному анализу и т. д. При инфекциях, в отношении которых не установлен защитный уровень антител, приходится проводить испытания профилактической эффективности вакцин по показателям заболеваемости данной инфекцией.
Наиболее объективную оценку иммунологической эффективности вакцин можно получить при вакцинации серонегативных к специфическим антигенам людей. Из таких лиц формируют опытную и контрольную группы. Оценку иммуногенности вакцинного препарата осуществляют на основе определения разницы в числе лиц, имеющих антитела в этих двух группах. Коэффициент иммунологической эффективности определяют по следующей формуле:
КЭ — коэффициент иммунологической эффективности;
А — число привитых испытуемым препаратом, у которых исследовали парные сыворотки крови;
Б — то же в контрольной группе лиц;
α — число привитых с возникшим иммунологическим сдвигом;
β — то же в контрольной группе.
Сформировать группы лиц, у которых не определялись бы антитела к широко распространенным возбудителям (грипп, гепатит А и др.), подчас бывает довольно сложно. В таких случаях нередко эффективность препаратов оценивают по нарастанию титров специфических антител до и после вакцинации как в основной, так и в контрольной группе. Иммунологические сдвиги, возникающие при вакцинации, оцениваются также по проценту сероконверсии. Вакцина считается высокоэффективной, если процент сероконверсии составляет 90% и выше. Кроме того, важное значение имеет продолжительность сохранения поствакцинального протективного иммунитета. После введения вакцины против желтой лихорадки она составляет 10-15 лет, брюшнотифозной (вакцины вианвак и Vi тифин) — 3 года, гепатита В — не менее 7-10 лет. Опубликованы результаты исследований о сохранении антител к вирусу краснухи от 9 до 21 года после прививки, причем серонегативность обнаруживалась только у 1% привитых вакциной рудивакс [9].
Для оценки и наблюдения за уровнем популяционного иммунитета проводится плановый серологический (иммунологический) контроль. Он позволяет выявить группы людей, наиболее подверженных риску заболевания, оценить степень защищенности лиц, привитых с нарушением схемы иммунизации или не имеющих документов о вакцинации, дать оценку и составить прогноз изменения эпидемиологической ситуации на конкретной территории. Отбор лиц для обследования в целях изучения иммуноструктуры осуществляется на основе кластерной выборки, рекомендованной ВОЗ. Экстренный серологический контроль проводится в очагах инфекционных заболеваний с целью выявления неиммунных лиц, которые контактировали с источником инфекции и подлежат срочной активной или пассивной иммунизации. Он также показан среди лиц с неясным прививочным анамнезом, при оценке вакцинального процесса у детей из групп риска развития поствакцинальных осложнений и привитых щадящими методами. Исследования иммунологической (клинической) эффективности вакцин могут определять, является ли вакцина иммуногенной и защищает ли она тех, кто привит. В то же время исследования относительной иммуногенности не могут определять, какая из схем вакцинации обеспечивает лучшую защиту, и результаты испытаний клинической эффективности трудно экстраполировать на условия рутинного применения вакцины в общей популяции. Таким образом, хотя исследования иммунологической эффективности вакцин необходимы, они часто не в состоянии помочь правильно оценить преимущества вакцинации.
В условиях плановой вакцинации контролируемые испытания представляются как непрактичными, так и неэтичными. Поэтому применяются обычные эпидемиологические исследования, детально описанные Оренштейном и соавт. [8]. Исследования эпидемиологической (полевой) эффективности прививки прямо отвечают на вопрос, помогает ли прививка людям. Оценка эпидемиологической эффективности предусматривает сбор информации об уровне заболеваемости, проявлениях эпидемического процесса во времени, в пространстве и среди различных групп населения. Кроме того, сопоставляются данные о заболеваемости на территории, где иммунизацию проводили, и там, где ее не проводили, при условии одинакового уровня заболеваемости на этих территориях в течение нескольких предыдущих лет.
В качестве примера можно привести программу всеобъемлющей иммунизации вакциной M-M-R II в Финляндии. Через несколько лет после начала реализации программы заболеваемость корью, краснухой и паротитом уменьшилась более чем на 90%, а к концу 12-летней программы местные случаи кори, паротита и краснухи были ликвидированы. Кроме того, заболеваемость энцефалитами у детей снизилась на треть, и прекратился рост заболеваемости диабетом I типа среди детей 5-9 лет, что также может являться результатом кампании иммунизации [14].
Основными критериями оценки эффекта массовой иммунизации служат показатели не только заболеваемости, но и смертности; изменения в характере очаговости, сезонности и цикличности, возрастной структуре болеющих, а также клиническом течении соответствующей вакцине инфекционной болезни, которые учтены за достаточно длительный период времени до и после проведения прививок. Предусматривается определение индекса эффективности, коэффициента (показателя) защищенности, коэффициента тяжести клинического течения болезни.
Коэффициент защищенности (Е) определяется по формуле:
α — заболеваемость среди лиц, получивших препарат;
β — заболеваемость среди лиц, не получивших препарат.
По показателю защищенности можно определить, какой процент людей из числа получающих вакцинный препарат защищен от заболевания. Показатель защищенности может с известной долей достоверности выводиться из показателя непосредственного риска, определяемого в ходе когортного эпидемиологического исследования.
Индекс эффективности показывает, во сколько раз заболеваемость среди лиц, получивших препарат, ниже заболеваемости среди лиц, его не получивших. Он определяется по формуле.
Индекс эффективности вакцинации равен показателю относительного риска.
Следует также отметить, что вакцинация представляет собой весьма результативное в экономическом плане мероприятие. Согласно данным специалистов Центра по контролю за инфекционными болезнями (США, Атланта), 1 долл., вложенный в вакцинации против кори, дает прибыль, равную 11,9 долл. Прибыль при иммунизации против полиомиелита равна 10,3 долл., паротита - 6,7 долл. Известно, что на 1 долл., вложенный сегодня в вакцинацию против краснухи, приходится 7,7 долл., которые сейчас тратятся на борьбу с этим заболеванием. Экономический эффект удваивается, если используется тривакцина (корь-краснуха-паротит). Иммунопрофилактика коклюша и инфекций, вызываемых гемофильной палочкой, приносит прибыль, соответственно равную 2,1-3,1 и 3,8 долл. На ликвидацию оспы было затрачено 313 млн. долл., величина предотвращенного ущерба ежегодно составляет 1-2 млрд. долл. Ни одна отрасль народного хозяйства не дает такой впечатляющей отдачи. Все затраты на мероприятия, проведенные под эгидой ВОЗ по ликвидации оспы, окупились в течение одного месяца после провозглашения ее ликвидации.
Литература
Сегодня является бесспорным тот факт, что вакцинопрофилактика это наиболее мощный метод борьбы с инфекционной патологией. Вместе с тем, вакцинация относится к числу мероприятий, требующих значительных материальных затрат, поскольку предусматривает охват прививками широкие слои населения. В связи с этим важно иметь правильное представление об эффективности иммунизации. Вакцинопрофилактика как мероприятие оценивается по 3 группам критериев: показатели документированной привитости (охват прививками), уровень иммунологической или клинической эффективности (efficacy) и эпидемиологическая или полевая эффективность (effectiveness). Показатели охвата прививками позволяют косвенно оценить возможное состояние популяционного иммунитета. Объективными критериями качества вакцинного препарата, а также состояния защищенности коллектива против того или иного инфекционного заболевания являются показатели иммунологической (клинической) и эпидемиологической (полевой) эффективности. Иммунологическая эффективность отвечает на вопрос «работает ли вакцина?», в то время как эпидемиологическая - «защищает ли прививка людей?» [3,5]. Иными словами, иммунологическая эффективность вакцины и эффективность иммунизации как профилактического мероприятия - разные понятия. Если под иммунологической эффективностью вакцины принято понимать способность препарата вызывать иммунный ответ у привитого, то эффективность иммунизации - различия в заболеваемости в группе привитых и непривитых лиц [1,2].
Сбор сведений о привитости осуществляется на уровне педиатрического участка по данным журналов профилактических прививок (ф.064-У), карт профилактических прививок (ф.063-у), истории развития ребенка (ф.112-у), сертификата о профилактических прививках (ф.156-у). Эта информация передается в территориальные центры Госсанэпиднадзора, последние анализируют ее по территориям и передают в соответствующие ведомства. Оценка привитости проводится на основании изучения величины охвата прививками лиц декретированного возраста в соответствии с действующим календарем профилактических прививок, введенным Приказом МЗ РФ №375 от 18.12.97. Нормативными показателями охвата прививками в возрастных группах детей до 3-х лет следует считать 95,0%, в старших возрастных группах - 97-98%. Опыт борьбы с оспой показал, что 80-90% охват прививками недостаточен для ликвидации инфекции. Оспу удалось ликвидировать лишь при охвате 99% населения прививками. Это обстоятельство важно учитывать при решении задачи ликвидации других инфекций.
Оценка иммунологической эффективности осуществляется выборочно среди различных групп населения и прицельно в индикаторных группах населения (получающих в соответствии с возрастом прививки), а также в группах риска (детские интернаты, дома ребенка и др.). Основные требования к иммунологическим исследованиям сводятся к следующему: 1) короткий промежуток времени, в течение которого исследуются все испытуемые сыворотки; 2) стандартность используемых диагностических препаратов; 3) высокая чувствительность иммунологического теста [2]. Выбор теста для оценки иммунологической эффективности вакцины зависит от характера иммунитета при данной инфекции. Например, для таких инфекций как столбняк, дифтерия, корь, паротит критерием эффективности вакцины является определение уровня циркулирующих специфических антител, а для туберкулеза, туляремии и бруцеллеза и др. - клеточные реакции (например, кожные реакции замедленной гиперчувствительности). К сожалению, для большинства инфекций, при которых основой защиты является клеточное звено иммунитета, уровни иммунных клеточных реакций не установлены.
Изучение иммунологической эффективности вакцин проводится путем сопоставления титров специфических антител в сыворотке крови привитых до и в разные сроки после иммунизации, а также путем сравнения этих результатов с определяемыми уровнями антител, полученными в те же сроки при обследовании лиц, которым вводили плацебо или препарат сравнения. Плацебо помещают в точно такие же ампулы или флаконы, в которых содержится изучаемая вакцина. Первые сыворотки собираются непосредственно перед вакцинацией, последующие - обычно через месяц после введения препарата. При однократной вакцинации одновременному исследованию подлежат парные сыворотки крови. При двукратной - тройные сыворотки и т.д. Очень важно, чтобы сыворотки, собранные в разные сроки, титровались одновременно. В случае хранения сывороток, взятых в более ранние сроки, может произойти снижение их активности, в результате чего показатели иммуногенности будут искусственно завышены. Сыворотки следует хранить в замороженном состоянии, причем замораживанию должны быть подвергнуты все образцы как ранее собранных сывороток, так и свежих. В этом случае если и наблюдается снижение активности сывороток, то данный факт имеет равное значение для сывороток, полученных в разные сроки.
Необходимость проведения подобных исследований определена неоднозначностью понятий «привит» и «защищен». Имеющийся опыт свидетельствует, что эти понятия далеко не всегда совпадают (рядом авторов это отмечено при дифтерии, кори и эпидемическом паротите). Иммунологическая активность вакцин может отражать ее профилактическую эффективность в том случае, если известен защитный уровень иммунологических показателей при данной инфекции. Защитный уровень антител устанавливается заранее на основании результатов опытов с однонаправленным препаратом. Для каждой инфекции определяется защитный титр антител (для кори, паротита и гриппа он равен 1:10, столбняка 1:20, дифтерии 1:40 в РПГА; для коклюша 0,03 МЕ/мл, гепатита В 0,01 МЕ/мл в иммуноферментной реакции и т.д.). Для инфекций, при которых не установлен защитный уровень антител, приходится проводить испытания профилактической эффективности вакцин по показателям заболеваемости данной инфекцией.
Наиболее объективную оценку иммунологической эффективности вакцин можно получить при вакцинации серонегативных к специфическим антигенам людей. Из таких лиц формируют опытную и контрольную группы. Оценку иммуногенности вакцинного препарата осуществляют на основе определения разницы в числе лиц имеющих антитела в этих двух группах. Коэффициент иммунологической эффективности определяют по следующей формуле:
КЭ - коэффициент иммунологической эффективности;
А - число привитых испытуемым препаратом, у которых исследовали парные сыворотки крови;
Б - то же в контрольной группе лиц;
а - число привитых с возникшим иммунологическим сдвигом;
б - то же в контрольной группе.
Сформировать группы лиц, у которых не определялись бы антитела к широко распространенным возбудителям (грипп, гепатит А и др.) подчас бывает довольно сложно. В таких случаях нередко эффективность препаратов оценивают по нарастанию титров специфических антител до и после вакцинации как в основной, так и в контрольной группе. Иммунологические сдвиги, возникающие при вакцинации, оцениваются также по проценту сероконверсии. Вакцина считается высоко эффективной, если процент сероконверсии составляет 90% и выше. Кроме того, важное значение имеет длительность поствакцинального протективного иммунитета, которая после введения, например, вакцины против желтой лихорадки составляет 10-15 лет, брюшного тифа (вакцины Вианвак и Тифим Ви) - 3 года, гепатита В не менее 7-10 лет. Опубликованы результаты исследований о сохранении антител к вирусу краснухи от 9 до 21 г. после прививки, причем серонегативность обнаруживалась только у 1% привитых вакциной Рудивакс [7].
Для оценки и слежения за уровнем популяционного иммунитета проводится плановый серологический (иммунологический) контроль. Он позволяет выявить группы людей, наиболее подверженных риску заболевания, оценить степень защищенности лиц, привитых с нарушением схемы иммунизации или не имеющих документов о вакцинации, дать оценку и составить прогноз изменения эпидемиологической ситуации на конкретной территории. Отбор лиц для обследования в целях изучения иммуноструктуры проводится на основе кластерной выборки, рекомендованной ВОЗ. Экстренный серологический контроль проводится в очагах инфекционных заболеваний с целью выявления неиммунных лиц, которые контактировали с источником инфекции и подлежат срочной активной или пассивной иммунизации. Он также показан для лиц с неясным прививочным анамнезом, при оценке вакцинального процесса у детей из групп риска, привитых щадящими методами, а также при развитии поствакцинальных осложнений. Результат оценки иммунологической (клинической) эффективности вакцин может дать представление, является ли вакцина иммуногенной и защищает ли она тех, кто привит. В то же время исследования относительной иммуногенности не могут дать ответ, какая из схем вакцинации обеспечивает лучшую защиту, и результаты испытаний клинической эффективности будут трудны для экстраполирования на условия рутинного применения вакцины в популяции. Таким образом, хотя исследования иммунологической эффективности вакцин необходимы, они часто не могут дать четкий ответ о выгоде, связанной с вакцинацией.
Среди исследований эпидемиологической (полевой) эффективности ретроспективный вид анализа наиболее распространен. Один из простых подходов, разработанных в середине 1980-х является скрининговый метод, широко применяющийся в оценочных программах вакцинации не только в развивающихся, но и в развитых странах. Скрининг-исследование требует только два типа данных контроля относительно каждой популяции: соотношение прошедших вакцинацию (PPV) и соотношение пациентов, которые были привиты, но заболели (PCV). Эффективность вакцинации рассчитывается с использованием алгебраического производного классического уравнения VE = 1 - относительный риск (5). Была разработана простая номограмма, позволяющая скрининг-исследованию быть легко применимым. Скрининг имеет два важных ограничения: для того, чтобы исследование было точным, частично привитые пациенты должны быть исключены из опыта, помимо этого большие погрешности могут иметь место всякий раз, когда PPV или PCV очень низки или очень высоки. Тем не менее, метод очень полезен, потому что, подобно всем скрининг-исследованиям, он показывает, являются ли клиническая (иммунологическая) и эпидемиологическая (полевая) эффективность вакцинации приемлемыми или требуют дальнейшего изучения.
В условиях плановой вакцинации применяют обычные эпидемиологические исследования, детально описанные Оренштейном и соавт. [6]. Исследования эпидемиологической (полевой) эффективности прививки прямо отвечают на вопрос, «защищает ли прививка людей?». Оценка эпидемиологической эффективности предусматривает сбор информации об уровне заболеваемости, проявлениях эпидемического процесса во времени, в пространстве и среди различных групп населения. Основными критериями оценки эффекта массовой иммунизации служат не только показатели заболеваемости, но и смертности, изменения в характере очаговости, сезонности и цикличности, возрастной структуре болеющих, а также клинического течения соответствующего инфекционного заболевания. Эти критерии учитываются за достаточно длительный период времени до и после проведения прививок. Предусматривается определение индекса эффективности, коэффициента (показателя) защищенности, коэффициента тяжести клинического течения болезни.
Коэффициент защищенности (Е) определяется по формуле
a - заболеваемость среди лиц, получивших препарат;
б - заболеваемость среди лиц, не получивших препарат.
По показателю защищенности можно определить, каков удельный вес людей из числа получающих вакцинный препарат защищенных от заболевания. Показатель защищенности может с известной долей достоверности выводиться из показателя непосредственного риска, определяемого в когортном эпидемиологическом исследовании.
Принципы и система организации полевых испытаний эпидемиологической эффективности вакцин
Одним из основных и наиболее объективных показателей, характеризующих эффективность вакцин, является оценка их профилактической эффективности, т.е. определение количественных параметров защиты от заболевания той инфекцией, для профилактики которой предназначен препарат.
Профилактическая эффективность вакцин оценивается по двум основным показателям: коэффициенту эффективности и (или) индексу эффективности. При этом первый показатель (коэффициент эффективности) характеризует удельный вес лиц из числа привитых, защиту которых обеспечивает вакцинация; второй показатель (индекс эффективности) отражает соотношение заболеваемости в группе привитых и непривитых, т.е. во сколько раз заболеваемость среди привитых окажется ниже таковой среди лиц не получавших вакцину.
Испытания эпидемиологической эффективности вакцин проводятся в рамках работ по регистрации вновь разработанных вакцин по специально разработанной программе, которая утверждается Главным государственным санитарным врачом Российской Федерации.
Оценка показателей профилактической эффективности вакцин проводится только в условиях специально организованных полевых контролируемых эпидемиологических опытов, для чего формируются основная и контрольная группы.
Основная группа привитых препаратом и контрольная группа, получающая плацебо (в качестве плацебо обычно используется «наполнитель» вакцины без активного его компонента) должны представлять равноценные по всем критериям части одних и тех же коллективов и находиться под наблюдением в одно и то же время.
В ряде случаев при оценке профилактической эффективности препарата целесообразно, исходя из этических соображений, использовать вместо плацебо вакцины предназначенные для профилактики других инфекционных заболеваний. При этом схема иммунизации, дозировка и место введения препарата, предназначенного для вакцинации лиц, вошедших в состав контрольной группы, должны быть идентичны группе испытуемой вакцины. Естественно, что при выборе препарата используемого вместо плацебо, необходимо учитывать эпидемиологическую целесообразность его применения на территориях выделенных для оценки профилактической эффективности вакцины.
В условиях контролируемого эпидемиологического опыта суммируются материалы наблюдения среди различных коллективов, территорий, характеризующихся различным уровнем заболеваемости, поэтому необходимо численное равенство наблюдаемых групп, а также идентичность этих групп по половым и возрастным характеристикам.
Равноценность основной и контрольной группы достигается при одинаковой методике их отбора с помощью случайно-выборочного метода.
При формировании основной и контрольной групп особое значение имеет показатель, характеризующий единицу выборки. Чаще за единицу выборки принимается один человек, т.е. в одном и том же коллективе один человек получает вакцину, другой - плацебо. Однако в отдельных случаях за единицу выборки можно принимать группу лиц, находящихся в одних и тех же условиях, например, группу детей в детских дошкольных учреждениях, класс - в школах и т.д. Групповая выборка возможна при условии одинаковой интенсивности распространения инфекции в тех или иных коллективах. Следует иметь в виду, что при вакцинации «через одного» (единица выборки - один человек) в наблюдаемом коллективе создается т.н. 50% иммунная прослойка. Это, естественно, влияет на интенсивность распространения инфекции в контрольной группе. В связи с этим искусственно занижаются показатели профилактической эффективности вакцины.
Поэтому при определении единицы выборки необходимо учитывать особенности инфекции с учетом путей передачи, интенсивности проявления ее в различных коллективах, а также возможность реализации путей передачи не только в одном коллективе (например, в классе школы), но и целом ряде коллективов или отдельно взятых учреждениях. Естественно, при широко распространенных инфекциях, особенно характеризующихся воздушно-капельным механизмом передачи, единица выборки может быть более крупной (класс, школа, детское дошкольное учреждение и т.п.).
Одним из необходимых условий, которое должно соблюдаться при организации контролируемых исследований, является шифровка вводимого препарата и плацебо. При этом медицинский персонал, который осуществляет вакцинацию и в дальнейшем проводит лабораторно-клинические обследования лиц, входящих в состав основной и контрольной групп, а так же проводит сбор и анализ заболеваемости, не должен знать, какой препарат получили те или иные контингенты.
Расшифровка всех материалов проводится только по окончанию наблюдения.
Кодирование препаратов, а так же шифровка других материалов, в частности, сывороток крови осуществляется специальной комиссией, состоящей из специалистов, которые непосредственно не принимают участия в исследованиях. Шифры хранятся в запечатанных конвертах, члены комиссии принимают участие в расшифровке материалов.
Для получения статистически достоверных данных о показателях профилактической эффективности вакцины численный состав группы привитых и получающих плацебо (соответственно основная и контрольная группа) определяется после проведения углубленного анализа с учетом заболеваемости за несколько лет инфекцией, для профилактики которой предназначен препарат. При этом необходимо исходить из минимально ожидаемой заболеваемости среди контингентов, подлежащих наблюдению.
Численный состав двух групп наблюдения (W) определяется по следующей формуле:
n - число наблюдаемых групп
m - ожидаемая минимальная заболеваемость
k - предполагаемый минимальный индекс эффективности, который может быть принят как существенный для данной вакцины.
Профилактическая эффективность вакцины оценивается путем сравнения показателей заболеваемости в группе привитых испытуемым препаратом с таковыми среди лиц, получившими плацебо.
Как видно из представленной формулы величина контингентов, включаемых в контролируемые исследования, зависит от заболеваемости и предполагаемого индекса эффективности вакцины. При этом, чем выше эти показатели, тем меньше численный состав групп необходимый для получения статистически достоверной разницы между заболеваемостью в основной и контрольной группах.
При этом сроки наблюдения обычно выбираются с учетом времени сезонного подъема данного заболевания и, в основном они должны быть не менее 10-12 месяцев.
Оценка профилактической эффективности, как указано выше, проводится путем расчета индекса эффективности (ИЭ)
Показатель заболеваемости на 1000, получивших плацебо
ИЭ = -------------------------------------------------------------------------------
Показатель заболеваемости на 1000, привитых испытуемым препаратом
и коэффициента эффективности (КЭ)
Индекс эффективности менее нагляден, чем коэффициент, и менее удобен для сопоставления эффективности нескольких препаратов. Поэтому при сравнении эффективности однонаправленных вакцин лучше пользоваться коэффициентом эффективности.
Особое место в проведении исследований по оценке профилактической эффективности вакцин занимает качественный и полный сбор данных о числе случаев заболеваний в основной и контрольной группах. При этом необходимо учитывать все случаи заболеваний, независимо от их клинического проявления.
В связи с этим количественная оценка профилактической активности препарата предполагает организацию качественной диагностики, позволяющей наиболее полно выявлять больных, в том числе стертыми и иннапарантными формами заболевания в группах наблюдения (основной и контрольной).
Одним из важных элементов эпидемиологического надзора является оценка эффективности применения различного рода вакцин в практике здравоохранения, т.е. влияния вакцинации на заболеваемость.
Эффективность вакцин при массовом применении зависит от целого ряда причин, одной из которых, естественно, является показатель профилактической эффективности препарата, т.е. потенциальные защитные свойства вакцины, охарактеризованные на этапах ее внедрения.
Однако, применение вакцин, обладающих даже высокой защитой, не всегда сопровождается заметным эпидемиологическим эффектом. В связи с этим одним из важных факторов, влияющих на эпидемиологическую эффективность вакцинации, является правильно избранная тактика применения препаратов в практике здравоохранения.
Естественно, что тактика вакцинопрофилактики базируется прежде всего на эпидемиологических особенностях проявления той или иной инфекции. При этом важное значение имеет выбор контингентов, подлежащих иммунизации, сроки проведения вакцинации, эпидемиологически обоснованный выбор территории, процент охвата вакцинацией лиц из группы высокого риска заражения и строгое соблюдение схем иммунизации. Кроме того, необходимо учитывать условия транспортировки и хранения препаратов.
В связи с этим одной из основных задач эпидемиологического надзора при оценке эффективности вакцинопрофилактики является установление причин, оказывающих негативное воздействие на реализацию защитных потенций вакцин с целью их устранения. Поэтому при планировании мероприятий по вакцинопрофилактике необходимо предусматривать перечень мер, позволяющих осуществить сбор качественной информации по оценке эффективности вакцинации.
При этом необходимо проводить полный учет и регистрацию заболеваний не только среди тех, кто был привит, но и тех, кто по каким-нибудь причинам не был вакцинирован.
Определяющее значение имеет тщательный сбор данных обо всех случаях заболевания той инфекцией, для профилактики которой предназначен препарат. При этом, естественно, необходимо отдельно анализировать заболеваемость среди привитых.
В случае заболевания привитого необходимо провести сбор следующих данных:
- сроки проведения вакцинации;
- схема вакцинации (полная или частичная);
- серия вакцины, которая была использована при иммунизации, и срок ее годности;
- где проводилась иммунизация (в том числе выделить условия хранения и доставки препарата);
- данные эпидобследования очага заболевания.
Сбор и обобщение этих данных позволит установить причины заболеваний среди привитых, т.е. оценить возможность реализации защитных свойств вакцины при массовом ее применении.
Оценканка эффективности массовой иммунизации может проводиться с использованием следующих методов:
- сопоставление заболеваемости среди привитых и непривитых, при этом более информативные данные можно получить при сравнении заболеваемости в определенных возрастных когортах и профессиональных группах в одни и те же сроки наблюдения и на одних и тех же территориях;
- использование данных ретроспективного анализа, сопоставляя заболеваемость до и после введения иммунизации;
- сопоставление заболеваемости на территории, где иммунизацию проводили, и на территории, где иммунизацию не проводили, при условии одинакового уровня заболеваемости на этих территориях в течение нескольких предыдущих лет.
При анализе этих данных следует учитывать, что по влиянию массовых прививок на эпидемический процесс, все инфекционные заболевания можно разбить на две группы:
- заболевания, при которых эффективность связана с непосредственной защитой от заболевания лишь тех, кто был иммунизирован. Это относится, прежде всего, к природно-очаговым инфекциям, например, клещевой энцефалит и др.;
- заболевания, при которых вакцинация приводит к снижению заболеваемости вследствие как непосредственной защиты от заболевания привитых, так и в результате уменьшения вероятности заболевания неиммунных лиц, за счет созданной иммунной прослойки, т.е. процента охвата вакцинацией лиц, подлежащих иммунизации.
При организации работ по оценке эффективности вакцинопрофилактики необходимо обратить особое внимание на качество диагностики, используя для этого методы, позволяющие максимально выявить не только клинически выраженные случаи заболевания, но легкие и стертые формы инфекции.
В заключение следует отметить, что оценка эффективности вновь внедренных вакцин при применении их в практике здравоохранения, т.е. так называемые постмаркетинговые наблюдения нуждаются в специальном планировании. Для получения достоверной информации, связанной как с изучением возможных осложнений при массовом использовании препарата, так и его эффективности, работы по постмаркетинговым наблюдениям следует организовывать и проводить на специально избранных территориях по специально разработанной программе.
Вопросы и ответы по оценке эффективности вакцин (часть 1)
1. Есть ли различия в оценке эффективности вакцин и других лекарств?
Нет, принципиальных различий нет; конечно, для большинства вакцин оценивается профилактическая эффективность, т.е. предупреждение болезней, тогда как для большинства лекарств - лечебная эффективность.
2. Каким путем проводится оценка иммунологической эффективности вакцин?
Иммунологическая эффективность оценивается по частоте и уровню тех изменений в иммунной системе вакцинированного, с которыми связано развитие невосприимчивости. Для инфекций, невосприимчивость к которым связана с продукцией антител, оценивается частота сероконверсии в определенные сроки после вакцинации, а также уровень антител. Для инфекций, зависящих от реакций клеточного звена иммунитета (туберкулез, бруцеллез и некоторые другие), проводится оценка выраженности кожных реакций замедленной гиперчувствительности.
3. Какими показателями оценивается профилактическая эффективность вакцин?
Для оценки степени защиты от инфекции, создаваемой вакциной, наиболее приемлемы проспективные контролируемые испытания в двух группах испытуемых - получающих вакцину и получающих плацебо. Группы создаются с использованием метода рандомизации, обеспечивающего равноценность условий в группах по максимуму параметров. Испытание проводят как двойное слепое, т.е. ни испытатели, ни испытуемые не знают, что им вводят. По уровню заболеваемости за определенный период наблюдения выводят два основных показателя.
Индекс эффективности представляет собой частное от деления заболеваемости непривитых на таковую привитых, т.е. он говорит, во сколько раз вакцинация снизила заболеваемость у привитых. Этот показатель фактически совпадает с показателем относительного риска заболевания у непривитых по сравнению с привитыми.
Другой показатель - коэффициент эффективности (коэффициент защиты) - высчитывается в процентах: разницу в заболеваемости двух групп соотносят с заболеваемостью непривитых. Этот показатель удобно использовать при сопоставлении эффективности разных вакцин против одной инфекции.
4. Всегда ли необходимо проведение контролируемых испытаний вакцин?
Для вакцин, уже применяемых в плановом порядке, возможно изучение профилактической эффективности методом «случай-контроль». Для этого изучается доля привитых данной вакциной среди заболевших соответствующей инфекцией (случаи) и среди подобранных по основным параметрам не заболевших в группе контроля. Чем меньшую часть среди заболевших составляют привитые, тем выше эффективность вакцины.
5. Исчерпывают ли эти показатели возможности оценки программ вакцинации?
Нет, приведенные выше показатели говорят лишь о способности вакцины защитить привитого, однако эпидемиологическая эффективность вакцинации зависит от многих параметров, таких, как принятая схема вакцинации, ее своевременность, уровень охвата целевого населения прививками, техника вакцинации, сохранность качества при хранении и транспортировке вводимой вакцины и т.д. Для оценки эпидемиологической эффективности принятой программы вакцинации учитывается уровень заболеваемости данной инфекцией (и смертности от нее) за ряд лет (до и после начала вакцинации), изменения в характере очаговости, сезонности.
6. Как расценить изменение возрастного состава заболевших корью и паротитом - сдвиг заболеваемости на подростковый и молодой возраст?
Этот сдвиг, отмеченный в последнее десятилетие, позволил убедиться в недостаточности однократной вакцинации против этих инфекций на втором году жизни (как и выборочной ревакцинации против кори по данным серологического исследования перед поступлением в школу). Эта ситуация явилась обоснованием изменений внесенных в Национальный прививочный календарь - в частности, введения, двух прививок против кори и паротита, что позволяет снизить до минимума процент восприимчивых к этим инфекциям подростков, снизив заболеваемость в этом возрасте. Двукратная вакцинация против кори с охватом минимум 95% (этот уровень уже достигнут в России) положена в основу стратегии ВОЗ по элиминации кори к 2007 г.
7. Используется ли для оценки эффективности вакцинации снижение тяжести клинического течения болезни?
Да, в отношении ряда инфекций это очень важный показатель. В частности, эпидемиологическая эффективность профилактических мероприятий при коклюшной инфекции проявляется не только в снижении заболеваемости, но особенно в резком снижении частоты тяжелых форм, протекающих с лейкоцитозом. Для оценки эффективности вакцинации против туберкулеза БЦЖ-вакциной (она не превышает в целом, 80-85%) важно учесть прежде всего снижение частоты генерализованных форм болезни (милиарного туберкулеза и туберкулезного менингита).
8. Целесообразно ли проведение рутинных массовых серологических обследований населения для оценки качества программ вакцинации, как это нередко практикуется в ряде регионов России?
Согласно рекомендациям ВОЗ массовые серологические исследования должны преследовать цель совершенствования тактики вакцинопрофилактики. В частности, в программе по элиминации кори может понадобиться определение величины восприимчивой прослойки населения. Во время недавней эпидемии дифтерии такое исследование показало высокую долю восприимчивых лиц в ряде возрастных групп, что позволило менять тактику и стратегию массовых прививок.
Однако в ситуации планового применения проверенных вакцин высокого качества кривые заболеваемости и данные об уровне охвата прививками определенных возрастов позволяют достаточно точно прогнозировать эпидемиологическую ситуацию. Поэтому ВОЗ не рекомендует рутинное серологическое наблюдение за иммунным статусом, настоятельно призывая затратить расходуемые на эти цели ресурсы (достаточно большие) на закупку вакцин и повышение охвата целевого населения прививками.
Читайте также:
