Формирование слезного аппарата глаза. Развитие уха эмбриона
Добавил пользователь Алексей Ф. Обновлено: 21.01.2026
Слёзный аппарат состоит из слёзных желез, слёзных точек, верхних и нижних слёзных канальцев, слёзных мешков и носослёзных протоков. В статье проанализированы данные об анатомическом и гистологическом строении, иннервации, кровоснабжении и развитии составляющих органов слезного аппарата. Отдельно рассмотрены функции слезной железы и слезоотводящих путей. Также в статье обозреваются аномалиях строения и патологии развития органов слезного аппарата. Рассмотрены методы исследования нарушений работы слезного аппарата, одним из которых является дакриоцистография. Основываясь на информации, которая представлена в статье, можно сделать заключение о том, что на сегодняшний день для диагностики и лечения патологии слёзопродуцирующего и слёзоотводящего аппаратов необходимо получить информацию с помощью дакриоцистографа. Дакриоцистограф дает трехмерное представление о строении слезной системы человека. Полученные результаты необходимо сопоставлять с результатами других методов исследований, это позволит уточнить семиотику заболеваний слезного аппарата. В связи с этим адекватное знание анатомии, гистологии и физиологии слёзных желез, слёзных канальцев, слёзных мешков и носослёзных протоков, секреции и оттока слез является основой для правильной диагностики.
1. Костиленко Ю.П., Мыслюк И.В., Девяткин Е.А. Структурно-функциональные единицы слюнной и слезной желез. Архив анатомии, гистологии и эмбриологии. 1986; 91: 80-86.
2. Пилюгин А.В., Тихонова Л.О., Рогуля В.А. Структурная организация экскреторных протоков слезной железы человека. Світ медицини та біології. 2008;81-83.
4. Dvoriantchikova G., Tao W., Pappas S., et al. Molecular profiling of the developing lacrimal gland reveals putative role of Notch signaling in branching morphogenesis. Invest Ophthalmol Vis Sci. 2017; 58: 1098-1109.
5. Farmer D.T., et al. Defining epithelial cell dynamics and lineage relationships in the developing lacrimal gland. Development. 2017;144:2517-2528.
6. Hirayama M., et al. Functional lacrimal gland regeneration by transplantation of a bioengineered organ germ. Nature communications. 2013;4:2497.
7. Maliborski A, Różycki R. Diagnostic imaging of the nasolacrimal drainage system. Part I. Radiological anatomy of lacrimal pathways. Physiology of tear secretion and tear outflow. Med Sci Monit. 2014;20(20):628-38.
9. Paulsen F., Langer W., Hoffmann W., Berry M., Human lacrimal gland mucins. Cell Tissue Res. 2004; 316(2):167-77.
10. Repka MX, Melia BM, Beck RW, Chandler DL, Fishman DR, Goldblum TA, Holmes JM, Perla BD, Quinn GE, Silbert DI, Wallace DK. Primary treatment of nasolacrimal duct obstruction with balloon catheter dilation in children younger than 4 years of age. Pediatric Eye Disease Investigator Group. J AAPOS. 2008;12(5):451-5.
11. Stevenson W., Pugazhendhi S., Wang M. Is the main lacrimal gland indispensable? Contributions of the corneal and conjunctival epithelia. Surv Ophthalmol. 2016;61(5):616-627.
К слёзному аппарату (apparatus lacrimalis) относятся слёзные железы, слёзные точки, верхние и нижние слёзные канальцы, слёзный мешок и носослёзный проток.
Функция. Слёзные железы (glandulae lacrimales) производят слёзную жидкость — прозрачная жидкость слабощелочной реакции с удельным весом 1,001 - 1,008. На 97,8% она состоит из воды и только около 2% из липидов, воды и муцинов, причем вода имеет большую толщину. Вода образуется основной слёзной железой, вспомогательными слёзными железами Краузе и Вольфринга. Мейбомиевы железы и железы Цейса выделяют липидный компонент слёзной плёнки, который предотвращает чрезмерное испарение слезной жидкости. Клетки Гоблета и Манца, крипты Генле, бокаловидные клетки Бехера продуцируют муцин. Тонкая слёзная плёнка сглаживает микроскопические неровности поверхности роговицы, поддерживает здоровую гомеостатическую среду на поверхности глаз, способствует правильному преломлению в ней лучей света, участвует в дыхании и питании роговицы, также в составе слёзной жидкости содержится фермент лизоцим, который обладает бактериостатическим свойством [6.11].
Развитие. Ткани слезной железы развиваются из поверхностной эктодермы (наружного слоя зародыша). Формирование железы начинается на втором месяце внутриутробной жизни, когда в области будущего виска появляются выросты базальных клеток конъюнктивального эпителия. В дальнейшем из них формируются ацинусы железы.
К третьему месяцу клетки в середине тяжей становятся вакуолизированными, из них в последующем возникнут протоки. Когда заканчивается эмбриогенез, начинается ветвление протоков. Их конечные отделы открываются в конъюнктивальный мешок. Особый фактор роста - эпидермальный - стимулирует работу железы, приводит к повышению количества простагландинов в вырабатываемой жидкости. Последние оказывают влияние на движение жидкой части секрета из межклеточного пространства. К рождению работа клеток железы еще недостаточно налажена, нормальное выделение слезы начинается к двухмесячному возрасту, а у 10% детей - в более поздние сроки.
Слезоотводящая система начинает формироваться на той стадии развития, когда размеры эмбриона не превышают 7 мм. На месте небольшого вдавления между верхнечелюстным и носовым отростками начинается интенсивное деление клеток, и образуется слезно-носовой желобок, который внутри заполнен эпителием. Движение клеточных масс идет в двух направлениях: к носу и к глазному яблоку. Край, направленный к глазу, разветвляется на две части: первая идет к верхнему веку, вторая - к нижнему. В дальнейшем эти части смыкаются со слезным мешком. В это время из окружающих клеток начинает формироваться костная основа носослезного канала.
Когда длина эмбриона человека достигает 32-35 мм, начинается канализация желобка (т.е. появляется просвет). Изначально эпителиальные клетки пропадают в центральной части, а его концы долгое время остаются закрытыми тонкими мембранами. Постепенно отмирающий эпителий середины тяжа скапливается в отделе, расположенном ближе к носу (из-за этого у новорожденных с плохой дренажной функцией слезного канала возможно развитие дакриоцистита). Верхняя мембрана обычно к рождению уже открыта, а нижняя в половине случаев сохраняется. Повышение гидростатического давления во время первого крика приводит к ее разрыву. Если этого не происходит, наблюдается непроходимость канала и слезотечение [4,5].
Гистологическое строение. Паренхима слёзной железы состоит из тубуло-ацинарных желёз, имеющие слизистый характер. Секреторные клетки железы плотно заполняются внутрицитоплазматическими секреторными гранулами и многочисленными скоплениями слизи разных размеров [8,9].
Стенки слёзных канальцев выстланы многослойным плоским эпителием, над ним находится слой эластических мышечных волокон, способствующих продвижению слезы по канальцам. Слизистая оболочка слёзного мешка так же покрыта многослойным плоским эпителием. Подслизистый слой богат аденоидной тканью. Наружные слои состоят из плотной фиброзной ткани, содержащей эластические волокна. Нижние отделы передней стенки слёзного мешка бедны эластической тканью, в связи, с чем в этом месте при дакриоциститах происходит растяжение и выпячивание стенки мешка. Слизистая оболочка носослёзного канала выстлана цилиндрическим эпителием с бокаловидными клетками, продуцирующими слизь. Эти клетки способны накапливать гранулы специального вещества — муциногена, которое может абсорбировать воду. Благодаря этому клетки постепенно набухают, а муциноген превращается в муцин — основной компонент носовой слизи. Слизь в носовой полости выполняет следующие функции: проведение воздуха из внешней для организма среды к носоглотке и в обратном направлении, очистка воздуха от пылевых частиц крупных и средних размеров, увлажнение воздуха, разведение химических раздражающих веществ, частичное обеззараживание воздуха [1].
Кровоснабжение слёзной железы осуществляется ветвями внутренней сонной артерии: отходящая от arteriae ophthalmica слёзная артерия (а. lacrimalis) проходит между верхней и латеральной прямыми мышцами глаза. Венозный отток обеспечивается через v.lacrimalis, которая впадает в v. ophtalmica superior.
Иннервация. Слёзная железа получает три типа иннервации: чувствительную, секреторную парасимпатическую и секреторную симпатическую. Чувствительную иннервацию железы обеспечивает nervus lacrimalis ветвь nervus ophthalmicus от nervi trigemini. Парасимпатическая иннервация берёт начало от ядра промежуточного нерва (nucleus salivatorius superior). Преганглионарные волокна nervus petrosus major идут в составе n.intermedius до ganglion pterygopalatinum. От этого узла начинаются постганлионарные волокна, которые в составе nervus maxillaris и далее по его ветвям достигают слёзной железы. Симпатические постганлионарные волокна исходят из верхнего шейного сплетения и доходят до слёзной железы в составе plexus caroticus internus.
Патологии развития. Обструкция носослезного канала (ОНСК) или дакреостеноз является наиболее распространенным расстройством слезной системы. Приблизительно у 6-20 % новорожденных проявляются некоторые симптомы. Как правило, ОНСК чаще встречается в первые недели или месяцы жизни с симптомами, начинающимися при нормальной продукции слез, в виде чрезмерного выделения слезной жидкости или синдрома сухих глаз. Эритема периорбитальной кожи, верхних и нижних век может быть результатом раздражения и трения, вызванных капанием слез и происходит из-за недостаточного дренажа. В результате состояние может проявляться как хронический односторонний конъюнктивит. Большинство случаев разрешалось спонтанно или с минимальным вмешательством на первом году жизни; однако нерешенные случаи нуждаются во внимании педиатрического офтальмолога, в зависимости от результатов исследования может потребоваться хирургическое вмешательство. У детей младше 6 месяцев консервативный подход является типичным руководством. Обычно используются массаж слезного мешка, глазные капели и местные антибиотики, а хирургическое лечение показано для пациентов, симптомы которых сохраняются после 12-месячного возраста.
Диагностика. Чрезмерное орошение глаза является распространенным состоянием в офтальмологической практики. Это может быть результатом чрезмерного производства слезной жидкости или обструкции и недостаточности эфферентных слезных путей. Дифференциация между обструкцией и недостаточностью слезных путей остается клинически сомнительной. В диагностическом процессе необходимо проводить клинические испытания, и часто требуется дополнительная диагностическая визуализация. Все чаще новые методы используются при диагностической визуализации слезных путей, такие как компьютерная томография, МРТ и изотопные методы. Дакриоцистография является главным критерием для диагностирования слезной обструкции. Дакриоцистография - рентгенологический метод исследования слезоотводящих путей с применением контрастного вещества. Это может помочь прояснить причину и точное место препятствия и предоставить информацию для планирования лечения, особенно хирургического [7].
Заключение. Основываясь на вышеизложенных сведениях и фактах можно сделать вывод о том, что на сегодняшний день, для диагностики и лечения патологии слёзопродуцирующего и слёзоотводящего аппаратов необходимо получить информацию о трехмерном строении слезной системы человека и сопоставить результаты с результатами других методов исследований, это позволит уточнить семиотику заболеваний слезного аппарата. В связи с этим адекватное знание анатомии и физиологии слезной системы, секреции и оттока слез является основой для правильной диагностики.
Формирование слезного аппарата глаза. Развитие уха эмбриона
ЛОР-болезни:
Популярные разделы сайта:
Эмбриогенез органа слуха. Развитие и формирование уха у плода
Формирование органа слуха является одним из самых сложных процессов органообразования у человека. В дифференциации тканей висцерального скелета на 4-й неделе внутриутробной жизни появляется зачаток внутреннего уха, а в последующем, к 7-й неделе, и элементы среднего уха.
Внутреннее ухо развивается на основе образования утолщения эктодермальной пластинки («плакода») с дальнейшим ее погружением в мезодерму и образованием слухового пузырька, заполненного эндолимфой. Из верхнемедиального отдела пузырька последовательно отшнуровываются эндолимфатический ход и элементы лабиринта. Нижние части пузырька дают начало формированию улитки.
Постепенно возникают чувствительные рецепторы и первоначально единственный ganglion acusticum распадается на два нервных образования ganglion vestibulare и ganglion cochleare. Окостенение лабирипта в целом, которое происходит к 5-му месяцу внутриутробной жизни, процесс сложный и постепенный. Если отделы внутреннего уха, составляющие собственно лабиринт, проходят период превращения хряща в кость через спонгиозную стадию, то окостенение улитки происходит без предварительного перехода в хрящ.
Процесс развития внутреннего уха человека неразрывно связан с образованием другого, не менее важного по значению для функции слуха разделом анализатора, — формированием среднего уха. В конце 1-го месяца внутриутробной жизни из дорсального углубления первого внутреннего эктодермального кармана образуются барабапная полость и слуховая труба, которые носят в этот период общее наименование — recesses tube — tympanicus.
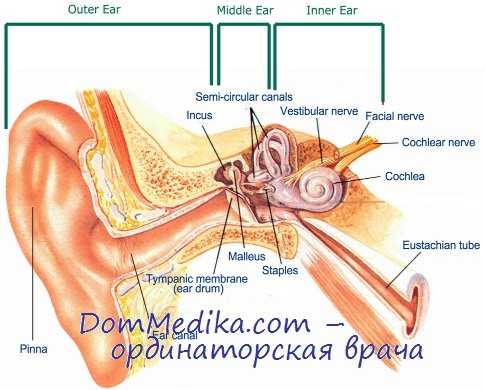
He менее сложным является процесс пневматизации височной кости, начало которой отмечается с момента образования recessus tubo-tympanicus. Антральная полость формируется па 21-й неделе утробной жизни плода. У новорожденных antrum выполнен миксоидной ткапыо, которая вскоре после рождения рассасывается, образуя воздухоносную полость. Постепеппо путем сложных превращений различных по строепию тканей происходит возникновение новых воздухоносных полостей уже на первом году ЖИЗНИ ребенка. Основной этап развития сосцевидного отростка с его ппевматизациой завершается у большинства детей к 3—5 годам жизни [Выренков Ю. Е.].
Известно, что наружное ухо формируется из элементов, окружающих первую жаберную щель. Образование cavi-tas conchae и окружающих ее шести бугорков относится ко 2-му месяцу утробной жизни. Эпителиальная трубка, являющаяся продолжением cavum conchac, образует в дальнейшем наружный слуховой проход. Одновременно появляется и барабапная перепонка, которая возникает из ментальной пластинки первичного слухового прохода. К моменту рождения ребенка костный отдел слухового прохода еще отсутствует и окончательное его формирование происходит в течение последующих 1— 1,5 лет [Кручинский Г. В.].
Таким образом, эмбриональное развитие органа слуха является сложным и продолжительным процессом, в котором участвуют разнообразные по строению и происхождению ткани. Длительность периода формирования наружного, среднего и внутреннего уха, сложность превращения тканей на различпых этапах создают множество условий для нарушений развития органа слуха, разнообразных по характеру и тяжести.
ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России
Особенности архитектоники структур полости носа и хоанальной зоны у детей с врожденными пороками развития глаз
Журнал: Вестник оториноларингологии. 2021;86(1): 63‑67
В статье приведены данные об эмбриогенезе глазного яблока, носослезного канала и полости носа. Отмечено нередкое сочетание врожденной атрезии хоан и аномалий развития глаз, по всей видимости, связанное с временным и топографическим параллелизмом внутриутробного развития данных анатомических областей. С целью оценки состояния полости носа и хоанальной области при врожденной патологии глаз были обследованы 43 ребенка с офтальмологическими пороками развития. У 32 (74,4%) детей по данным эндоскопического обследования выявлены изменения анатомии хоанальной области с изменением ее размеров в виде неполной атрезии. Полученные результаты позволяют авторам рекомендовать всем детям с врожденными офтальмологическими пороками развития осмотр и наблюдение у врача-отоларинголога с проведением эндоскопического исследования полости носа и носоглотки.
Дата принятия в печать:
Врожденные пороки в структуре младенческой заболеваемости и смертности занимают одно из первых мест. По данным популяционных исследований и сведений ВОЗ, частота встречаемости врожденных пороков развития составляет в среднем от 3 до 6% [1], а у новорожденных детей колеблется в широких пределах — от 11,5:1000 до 32:1000 [2]. Сочетание пороков развития лица и черепа с другими видами аномалий выявляется у 60% детей [3].
Этиология пороков и аномалий развития до конца не изучена. Взаимодействие множества разнообразных причинных факторов (тератогенов) определяет многофакторный характер врожденных аномалий развития носа и глаз. Эффект воздействия проявляется в виде физиологических, модифицирующих и повреждающих явлений [4]. Достаточно часто выявляются сочетанные пороки формирования полости носа и хоанальной зоны с пороками развития глаз, что обусловлено течением гестационного периода жизни.
Различные исследования, посвященные эмбриогенезу риноорбитальной зоны, свидетельствуют о крайне тесной взаимосвязи развития структур латеральной стенки полости носа, околоносовых пазух и носослезного канала [8—11]. Уже на 5-й неделе эмбрионального развития еще в первичной полости носа между латеральным и верхнечелюстным отростками прослеживается слезная пластинка, из которой на 7-й неделе гестации образуется слезный шнур. Затем, на 10-й неделе внутриутробного развития, в слезном шнуре проявляется просвет, так называемый истинный носослезный канал. К 20-й неделе заканчивается формирование костной трубки, окружающей носослезный канал [8, 12—14]. В связи с вышеуказанным считаем справедливым анатомо-топографически и клинически разделять у детей два понятия: «носослезный канал», представляющий собой костную структуру, и «носослезный проток», являющейся мягкотканым образованием. Воздействие негативных факторов окружающей среды на эмбрион в различные сроки гестации, по мнению W. Katowitz и соавт., может привести к появлению врожденных аномалий и пороков развития слезоотводящих путей, например стенозу носослезного канала [15].
Среди пороков развития носа и околоносовых пазух у детей наиболее часто хирургические вмешательства производят по поводу врожденной атрезии хоан. Имеются многочисленные наблюдения сочетания врожденной атрезии хоан с аномалиями развития других органов, в том числе при различных синдромах и расстройствах как часть сложного фенотипа [16, 17]. В наших наблюдениях более чем у 1 /2 детей с врожденной атрезией хоан (n=144), а именно у 76 (52,8%), выявлены сопутствующие пороки развития. При этом у 30 (20,8%) детей обнаружена врожденная патология со стороны органа зрения: в несиндромальных случаях сочетанного поражения — у 14 (9,7%) детей и с синдромальной патологией, в том числе при CHARGE-синдроме, — у 16 (11,1%). Чаще всего врожденная атрезия хоан ассоциировалась с такими пороками развития глаз, как колобома радужки или сетчатки (11 (7,6%) пациентов); у 1 ребенка двусторонняя врожденная атрезия хоан сочеталась с врожденным двусторонним стенозом носослезных каналов.
Нередкое сочетание врожденной атрезии хоан и аномалий развития глаз, по всей видимости, связано с тем, что формирование структур полости носа, носоглотки у эмбриона идет параллельно с закладкой структур органа зрения как во временных рамках, так и топографически. Воздействие различных потенциально тератогенных факторов в период с 3-й по 10—12-ю неделю внутриутробного периода может оказать влияние на закладку и полости носа, и глаз, и слезоотводящих путей.
Цель исследования — оценка состояния полости носа и хоанальной области при врожденной патологии глаз.
Пациенты и методы
Обследованы дети, наблюдающиеся с данной патологией в детской глазной консультативной поликлинике при Морозовской детской клинической больнице и в отделении офтальмологии Российской детской клинической больницы. Обследование проводилось амбулаторно на клинической базе кафедр оториноларингологии и офтальмологии — ОСП РДКБ ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России. Всего осмотрены 43 ребенка с врожденными аномалиями развития глаз от 2 до 14 лет, средний возраст обследуемых детей 6 лет.
Клиническое обследование больных включало в себя анализ жалоб, сбор анамнеза, проведение стандартных оториноларингологического и офтальмологического осмотров, эндоскопическое исследование полости носа и носоглотки по стандартной методике. Жалобы на частые риниты, затруднение носового дыхания предъявляли 10 пациентов, у 1 ребенка отмечалось нарушение оттока слезы, остальные жалоб не предъявляли.
Результаты. Структура патологии представлена в таблице, из которой видно, что наибольшее число детей в нашем исследовании (21 (48,8%) ребенок) имели колобому радужки, которая имеет форму перевернутой капли, связанной со зрачковой областью, и возникает вследствие незаращения щели глазного бокала. При колобоме радужки дефект локализовался у 16 детей на 6 ч, у 1 ребенка на 7 ч, у 4 детей в зоне 5—7 ч (рис. 1 на цв. вклейке). Микрофтальм наблюдался у 2 детей. При этом у 1 ребенка колобома радужной оболочки правого глаза сочеталась с левосторонним микрофтальмом и косоглазием.
Распределение детей по типу выявленной врожденной офтальмологической патологии
Зрение у детей
Нормальное функционирование зрительной системы ребенка — необходимое условие не только для обеспечения самого зрительного процесса, но и для развития всех органов и систем организма, т. к. глаз — это не только орган зрения, но и «потребитель» световой энергии. Благодаря стимулирующему действию света в организме железами внутренней секреции вырабатываются гормоны гипофиза, надпочечников, щитовидной железы, половых желез и др. Более быстрая адаптация организма новорожденного к внешним условиям, его правильное развитие и рост в большой степени зависят от правильного функционирования зрительной системы. Именно поэтому зрительный анализатор у детей формируется достаточно быстро. Рост и развитие глаза у ребенка в основном завершаются к 2-3 годам, а в последующие 15-20 лет происходит меньше изменений, чем за первые годы.
Особенно важным для дальнейшего нормального функционирования зрительной системы ребенка является правильная закладка и развитие органа зрения еще до рождения. Существуют особые критические периоды развития, когда закладка того или иного органа становится особенно чувствительной к различным повреждающим факторам. Результаты клинических наблюдений свидетельствуют о том, что нарушения в развитии глаза могут вызываться:
- авитаминозом А (слепота);
- влиянием хлорида лития (циклопия, анофтальм) и роданида натрия (гидрофтальм);
- гипоксией (катаракта, недоразвитие);
- диагностической рентгенографией беременных (микрофтальм, катаракта, слепота);
- инфекционными болезнями, избыточным или длительным введением препаратов при сахарном диабете (аплазия зрительного нерва, слепота, катаракта) и т. д.
Однако изменения могут быть обусловлены и влиянием врожденно-наследственных факторов. К моменту рождения глаз ребенка, в случае нормального дородового развития, имеет все оболочки, однако существенно отличается по размерам, массе, гистологической структуре, физиологии и функциям от глаза взрослого.
Глаз новорожденного
Глаз новорожденного имеет значительно более короткую, чем у взрослого, переднезаднюю ось (ок. 16-18 мм) и, соответственно, более высокую (80,0-90,9D) преломляющую силу. К году переднезадний размер глазного яблока ребенка увеличивается до 19,2 мм, к 3-м годам — до 20,5 мм, к 7-ми — до 21,1 мм, к 10-ти — до 22 мм, к 15-ти годам составляет около 23 мм и к 20-25 — примерно 24 мм. Однако, величина и форма глазного яблока зависят от вида и величины того или иного вида рефракции (нарушения рефракции — миопия, гиперметропия, нормальная рефракция — эмметропия). Размеры глазного яблока ребенка имеют большое значение при оценке вида и стадии глазной патологии (врожденная глаукома, близорукость и др.).
Как правило, у детей при рождении и в младшем возрасте глаз имеет гиперметропическую рефракцию — дальнозоркость (по данным исследований она выявлена в 92,8% всех исследованных глаз в возрасте до 3 лет, нормальная рефракция и близорукость в этом возрасте — соответственно 3,7 и 2%). Степень дальнозоркости составляет в среднем 2,0-4,0D. По мере роста глаза его рефракция смещается в сторону нормальной. В первые 3 года жизни ребенка происходит интенсивный рост глаза, а также уплощение роговицы и особенно хрусталика.
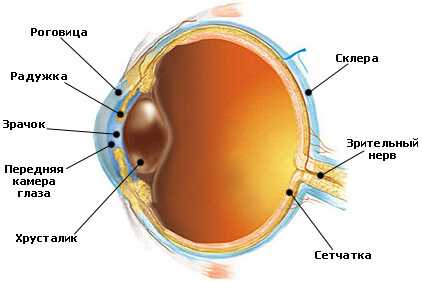
Роговица
Роговица — это основная преломляющая структура глаза. Ширина (или горизонтальный диаметр) роговицы у новорожденных в среднем 8-9 мм, к году — 10 мм, к 11 годам — 11,5 мм, что почти соответствует диаметру роговицы у взрослых. Рост роговицы, увеличение ее размеров происходит за счет растягивания и истончения ткани. Толщина центральной части роговицы уменьшается в среднем с 1,5 до 0,6 мм, а по периферии — с 2,0 до 1,0 мм. Радиус кривизны передней поверхности роговицы новорожденного равен в среднем 7,0 мм, с возрастом происходит некоторое ее уплощение и к 7 годам кривизна составляет в среднем 7,5 мм, как и у взрослых (кривизна роговицы может варьироваться от 6,2 до 8,2 мм, в зависимости от вида и величины рефракции глаза). Преломляющая сила роговицы изменяется в зависимости от возраста обратно пропорционально радиусу кривизны: у детей первого года жизни она составляет в среднем 46-48 D, а к 7 годам, как и у взрослых, — около 42-44 D. Сила преломления роговицы в вертикальном меридиане почти всегда примерно на 0,5 D больше, чем в горизонтальном, что и обуславливает, так называемый, "физиологический" астигматизм.
В первые месяцы жизни ребенка роговица малочувствительна вследствие еще не закончившегося функционального развития черепных нервов. В этот период особенно опасно попадание в конъюнктивальный мешок инородных тел, которые не вызывают раздражения глаз, боли и беспокойства ребенка и, следовательно, могут привести к тяжелым повреждениям роговицы (кератиту) вплоть до ее разрушения. В дальнейшем чувствительность роговицы повышается и у годовалого ребенка она почти такая же, как и у взрослого. См. строение роговицы глаза.
Радужная оболочка
Радужная оболочка — это передняя часть сосудистой оболочки глаза, образует вертикально стоящую диафрагму с отверстием в центре — зрачком, регулирующим поступление света внутрь глаза в зависимости от внешних условий. Радужная оболочка может иметь различную окраску — от голубой до черной. Цвет ее зависит от количества содержащегося в ней пигмента меланина: чем больше пигмента, тем темнее радужная оболочка; при отсутствии или малом количестве пигмента эта оболочка имеет голубой или светло-серый цвет. У детей в радужной оболочке мало пигмента, поэтому у новорожденных и детей первого года жизни она голубовато-сероватая. Окончательно цвет радужки формируется к 10-12 годам. У детей грудного возраста плохо развиты мышечные волокна, расширяющие зрачок и поэтому зрачок узкий (2-2,5 мм). К 1-3-ем годам зрачок приобретает размеры, характерные для взрослых (3-3,5 мм).
Хрусталик
Хрусталик — вторая важнейшая оптическая система, на долю которой приходится около одной трети преломляющей силы глаза (до 20,0 D). Хрусталик обладает свойством изменять кривизну своей передней поверхности и приспосабливать глаз к ясному видению предметов, расположенных на различных расстояниях (функция аккомодации). Форма и величина хрусталика существенно меняется с возрастом. У новорожденных форма хрусталика приближается к шаровидной, его толщина составляет примерно 4 мм, диаметр — 6 мм, кривизна передней поверхности — 5,5 мм. В зрелом и пожилом возрастах толщина хрусталика достигает 4,6 мм, а диаметр — 10 мм, при этом радиус кривизны передней поверхности увеличивается до 10 мм, а задней — до 9 мм. Соответственно меняется и преломляющая сила хрусталика: если у детей она составляет порядка 43,0 D, то у взрослых — 20,0 D.
Сетчатка
Сетчатка — важнейшая составляющая зрительного анализатора, являющаяся его периферическим звеном. Сложнейшая структура позволяет сетчатке первой воспринимать свет, обрабатывать и трансформировать световую энергию в нервный импульс, который далее по цепочке нейронов передается в зрительные центры коры головного мозга, где и происходит восприятие и переработка зрительной информации. Сетчатка является внутренней оболочкой глазного яблока, выстилающей глазное дно. Самым важным местом сетчатки является так называемое желтое пятно (macula) с центральной (0,075 мм) областью (fovea centralis). Эта область наилучшего восприятия зрительных ощущений.
У новорожденного сетчатка состоит из 10 слоев:
- пигментного эпителия;
- слоя палочек и колбочек;
- наружной пограничной мембраны;
- наружного ядерного слоя;
- наружного плексиформного (сетчатого) слоя;
- внутреннего ядерного слоя;
- внутреннего плексиформного слоя;
- слоя ганглиозных и мультиполярных клеток;
- слоя нервных волокон;
- внутренней пограничной мембраны.
Первые четыре слоя относятся к светочувствительному аппарату сетчатки, а остальные составляют мозговой отдел. После первого полугодия и по мере роста глаза растягиваются и истончаются не только наружные, но и внутренние слои сетчатки. В связи с этим значительные изменения претерпевает сетчатка в макулярной и особенно фовеолярной (центральной) области: здесь остаются лишь 1-й, 2-й, 3-й и 10-й слои, что и обеспечивает в будущем высокую разрешающую зрительную способность этой зоны. См. строение сетчатки.
Передняя камера глаза
Передняя камера глаза ограничена спереди задней поверхностью роговицы, по периферии (в углу) — корнем радужки, ресничным телом, сзади — передней поверхностью радужки, а в зрачковой области — передней капсулой хрусталика. К моменту рождения ребенка передняя камера глаза уже сформирована, однако по форме и размерам она значительно отличается от камеры у взрослых. Это объясняется наличием короткой передне-задней оси глаза, своеобразием формы радужной оболочки и шаровидной формой передней поверхности хрусталика. Важно знать, что задняя поверхность радужной оболочки тесно контактирует с межзрачковой областью передней капсулы хрусталика.
У новорожденного глубина передней камеры в центре (от роговицы до передней поверхности хрусталика) достигает 2 мм, а угол камеры острый и узкий, к году камера увеличивается до 2,5 мм, а к 3 годам она почти такая же, как у взрослых, т. е. около 3,5 мм; угол камеры становится более открытым. Во внутриутробном периоде развития угол передней камеры закрыт мезодермальной тканью, однако к моменту рождения эта ткань в значительной мере рассасывается. Задержка в обратном развитии мезодермы может привести к повышению внутриглазного давления еще до рождения ребенка и развитию гидрофтальма (водянка глаза).
Около 5% детей рождаются с закрытым отверстием слезно-носового канала, но под влиянием слезной жидкости ткань («пробка») в первые дни почти всегда рассасывается, и начинается нормальное отведение слезы. В противном случае, прекращается отток слезы, образуется ее застой и возникает дакриоцистит новорожденных.
Глазница
После рождения ребенка зрительный анализатор проходит определенные этапы развития, среди которых основные пять:
Читайте также:
- Клиника и диагностика рака шейки матки
- Рубцовый выворот века глаза: причины, диагностика, лечение
- Синдром Эйкора-Смита (Achor-Smith)
- Пример абдоминального парагонимоза. Острый живот при парагонимозе
- Врожденное сужение артериального конуса левого желудочка. Сочетанные пороки сужения артериального конуса
