Гломусангиома среднего уха. Лечение гломусангиомы
Добавил пользователь Валентин П. Обновлено: 21.01.2026
Гломусные опухоли (параганглиомы, нехромаффинная параганглиома, хемодектома) - это медленно растущие доброкачественные опухоли головного мозга, происходящие из параганглиозных клеток области расширения внутренней яремной вены. Их частота составляет 0,6 % от всех внутричерепных опухолей.
Женщины болеют в 6 раз чаще мужчин. Средний возраст пациентов 55 лет.
Гломусные опухоли могут обнаруживаться как экстракраниально так и интракраниально.
Патогенез (что происходит?) во время Гломусных опухоли (параганглиом):
Параганглиома развивается из широко распространенных в организме нехромаффинных параганглиев симпатической и парасимпатической нервной системы, а также из гломусных телец. Исходная ткань состоит из хеморецепторных клеток, исходящих из первичного неврального гребешка. Гломусные тельца выглядят в виде небольших узелков васкуляризированной ткани параганглия. Они являются частью бранхиомерной интравагальной парасимпатической нервной системы.
Гломусные опухоли представляют собой сосудистые переплетения с включениями гломусных клеток, часто вовлекающие в свой рост каудальные черепные нервы и кровеносные сосуды. В состав гломусных опухолей также входят хромофинные клетки, что в 1% случаев сопровождается активной секрецией катехоламинов.
Скопление гломусных телец отмечается в глазнице, гортани, трахее, средостении, забрюшинном пространстве, органах желудочно-кишечного тракта и др. В области головы и шеи каротидные тельца расположены в области бифуркации общей сонной артерии и в височной кости.
Симптомы Гломусных опухоли (параганглиом):
Наиболее частыми симптомами является снижение слуха, звон в ушах, парез лицевой мускулатуры, лабильное артериальное давление. В запущенных случаях выявляются симптомы компрессии ствола мозга.
Диагностика Гломусных опухоли (параганглиом):
Диагностика солитарных гломус-ангиом в типичных случаях не представляет труда за счет характерных симптоматики и локализации очагов поражения. При множественной врожденной форме заболевания для верификации диагноза обычно приходится прибегать к предварительному гистологическому исследованию.
Основными методами диагностики являются МРТ и КТ, иногда для уточнения диагноза необходимо проведение магнитно-резонансной или рентгеновской ангиографии.
Гломусные опухоли следует дифференцировать от гемангиомы, голубого невуса, дерматофибромы, невриномы, лейомиомы, меланомы.
Лечение Гломусных опухоли (параганглиом):
Лечение гломусных опухолей представляет собой сложную задачу из-за обильного кровоснабжения опухолей, локализации в области крупных венозных сосудов, а также инвазивного характера роста. В настоящее время возможности лечения заключаются в микрохирургической резекции, радиохирургии, эмболизации, лучевой терапии и комбинации этих методов. Хотя целью хирургии является тотальная резекция, из-за выраженной васкуляризации опухоли и вовлечения критических структур, тотальное удаление этих опухолей связано с большим количеством осложнений. Частота послеоперационных осложнений в виде поражения черепных нервов колеблется от 22 до 100%, ишемических инсультов в 10-20 %, в 10 % имеется риск послеоперационной ликвореи. Смертность после операций может достигать 4 %.
Применение лучевой терапии в лечении гломусных опухолей ограничено тем, что при использовании низких доз отмечается частое рецидивирование, а при увеличении дозы радиации отмечается высокий процент лучевых осложнений. Эти осложнения включают в себя мастоидиты, нарушения вкуса, облучение, поражения слизистых и кожи. Также описаны парезы мышц лица из-за поражения лицевого нерва, потерю слуха, некроз височной кости и твердой мозговой оболочки, сопровождающийся ликвореей.
К каким докторам следует обращаться если у Вас Гломусные опухоли (параганглиомы):
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Гломусных опухоли (параганглиом), ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Гломусангиома среднего уха. Лечение гломусангиомы
Кафедра оториноларингологии Российского университета Дружбы народов, Москва
Кафедра челюстно-лицевой хирургии и хирургической стоматологии Российского национального медицинского университета им. Н.И. Пирогова Минздравсоцразвития России, Москва
Кафедра оториноларингологиии Российского университета дружбы народов, Москва, Россия, 117198
Этиология и патогенез гломусных опухолей (хемодектом) основания черепа
Журнал: Вестник оториноларингологии. 2016;81(3): 26‑29
Цель работы — описать историю развития этиологии и патогенеза гломусной опухоли (хемодектомы) основания черепа. В работе приведены хронологические таблицы развития исследований этиологии, патогенеза, хирургического лечения при данном заболевании, анализ и обсуждение спорных мест номенклатуры.
Локализация и функции гломусов головы и шеи
В 1941 г. S. Guild [1] описал сосудистую ткань на луковице яремной вены и на мысе улитки, которую он назвал гломусной тканью. Новообразования, которые возникали из этой ткани, в различные периоды времени получали название рецептом, хемодектом, нехромафинных опухолей, экстраадреналовых гломусных опухолей, а также опухолей, напоминающих каротидное тельце (carotidbodyliketumors).
Гломусная опухоль (хемодектома) — это новообразование из органов эндокринной системы, которые способны продуцировать биогенные амины, а также выполнять хеморецепторную функцию — реагировать на изменения концентрации О 2 , СО 2 и рН крови и передавать информацию об этом в бульбарные центры головного мозга [2, 3]. Гломусы имеют общее происхождение с мозговым слоем надпочечника и возникают из эмбриональных симпатических клеток нервной ткани [4]. Другими словами — это совокупность нейроэктодермальных клеток экстраадреналовой локализации. На этапе внутриутробного развития данная система как эндокринный орган функционирует до тех пор, пока не завершится формирование мозгового вещества надпочечников — основного источника катехоламинов. Функции клеток гломусов идентичны таковым в мозговом веществе надпочечников. Как и надпочечники, они могут содержать катехоламины и выделять их по изменениям нейрональных или химических сигналов наподобие обычных эндокринных органов.
Самым крупным органом из этой группы принято считать само мозговое вещество надпочечника, вторым по размеру — аортальный гломус [4]. Остальные гломусы, локализация которых представлена в табл. 1, имеют значительно меньшие размеры в пределах 0,6—4 мм в диаметре.

Таблица 1. Гломусные опухоли (хемодектомы) и места их исходного роста в организме человека
Таким образом, гломусные опухоли (хемодектомы) могут возникать во всех местах нервной системы. Остановимся только на тех, которые локализуются в области головы и шеи.
Блуждающие, яремные и барабанные гломусы представляют собой цепочку, идущую по ходу ветвей языкоглоточного и блуждающего нервов с локализацией:
— в области нижнего, среднего и верхнего узлов блуждающего нерва;
— в адвентиции луковицы яремной вены;
— в области мыса улитки;
— по ходу барабанной ветви IX нерва (нерва Якобсона);
— по ходу заднеушной ветви X нерва (нерва Арнольда).
История изучения и проблемы терминологии
История исследования опухолей, растущих из гломусов основания черепа, сравнительно невелика. Впервые барабанный и яремный гломус описал в 1941 г. S. Guild [1]. Опухоль, возникающую из них, впервые обнаружил в 1945 г. H. Rosenwasser [5].
С момента первого описания опухоли ее название неоднократно изменялось. До настоящего времени специалисты, занимающиеся этой патологией, называют ее по-разному. Часто при микроскопии ставят диагноз гемангиомы [6, 7]. В хронологической последовательности история терминологии гломусных опухолей представлена в табл. 2 [8].

Таблица 2. Хронология изменения терминов гломусных опухолей
Название хемодектомы или рецептомы предполагает функциональную роль гломусов только в качестве рецепторных образований.
Однако установлено, что помимо рецепторной функции, они обладают эндокринной активностью и могут секретировать биологически активные вещества, например катехоламины или серотонин. Немаловажным моментом может являться то, что с этими опухолями имеют дело и общие хирурги-онкологи, и сосудистые хирурги, и оториноларингологи [9], которые в своих работах чаще всего обозначают их как гломусные или хемодектомы. Термин «параганглиома» для них достаточно редкий. Однако иногда гломусными опухолями называют новообразования барорецепторов (тельца Барре—Масона и т. д.) [9], не имеющих отношения к симпатико-адреналовой системе. Термин «нехромаффинная параганглиома», периодически используемый и сейчас, основан на реакции осаждения солей хромовой кислоты клетками опухоли, что дает возможность судить о наличии или отсутствии их симпатической активности. В настоящее время эта реакция представляет только исторический интерес. Соответственно, устарел и термин.
Деление гломусных опухолей (хемодектом) по классификации ВОЗ на симпатические и парасимпатические представляется недостаточно обоснованным, поскольку не учитывается возможность существования неактивных форм. Могут существовать также опухоли, секретирующие множество биогенных аминов, как относящихся к парасимпатическому или симпатическому отделу нервной системы, так и не относящихся ни к одному из них.
Другая часть термина указывает либо на исходную локализацию (яремная, барабанная или вагусная гломусная опухоль), либо на зону поражения — среднее ухо, сосцевидный отросток или блуждающий нерв) [5].
Даже при небольшом объеме новообразования поражаются как пирамида височной кости, так и яремное отверстие. У многих больных зона распространения захватывала основание черепа, верхние отделы шеи, а также головной мозг. Поэтому имеет смысл остановиться на термине гломусная опухоль (хемодектома). Например, гломусная опухоль (хемодектома) основания черепа с ростом в заднюю черепную ямку или с распространением в заднюю черепную ямку и паравертебрально. Исходную локализацию при распространенной опухоли можно определить на основании детального анализа хронологии симптомов заболевания [10].
Этиология гломусных опухолей
Этиология гломусных опухолей (хемодектом) основания черепа в настоящее время неизвестна. Анализ данных литературы, а также собственных наблюдений показал, что в 75% наблюдений этим заболеванием страдают лица женского пола в возрасте 40—45 лет. Вероятно, этиологическим моментом служит перестройка гормональной системы организма. В молодом возрасте фактором, вызывающим рост опухоли, может явиться беременность. В возрасте 20—30 лет чаще встречаются гормонально-активные формы.
Если сделать небольшой экскурс в историю, то можно вспомнить, что существуют уницентрическая [11] и мультицентрическая теории возникновения опухолей [12]. По первой теории, новообразование под воздействием различных онкогенов может возникать из одного зачатка, в частности из гломуса. Согласно второй, онкогенный фактор может быть общим для нескольких гломусов сразу. Возможно, этим фактом объясняется наличие множественных фopм опухолей [13—18], двусторонних яремных гломусных опухолей, сочетание опухоли яремного гломуса с забрюшинной феохромоцитомой, диссеминированных форм и т. д. [19]. Гломусные опухоли могут сочетаться с невриномой слухового нерва [20]. Описан единственный случай сочетания гломусной опухоли (хемодектомы) с арахноидальной кистой задней черепной ямки [21]. Иногда гломусные опухоли могут быть первично-множественными. Первично-множественные гломусные опухоли (хемодектомы) бывают синхронными и метахронными. Первично-множественные синхронные новообразования в пределах височной кости и основания черепа могут восприниматься как один распространенный процесс, а первично-множественные метахронные новообразования этой локализации — как рецидив опухоли после ранее возникшего удаленного очага [10, 12, 13, 18].
Некоторые исследователи связывают образование гломусных опухолей с хронической гипоксией. При ней наблюдалась гипертрофия гломусов в ответ на длительную кислородную недостаточность [22], например при врожденных пороках сердца.
Генетический аспект гломусных опухолей
Имеются данные о роли наследственного фактора в возникновении гломусных опухолей, передача которого происходит по аутосомно-доминантному типу [23]. Существует семейные формы этих опухолей [24, 25], составляющие, по данным литературы, менее 1—2% от общего числа наблюдений.
Анализ генома хемодектом выявил значительную разницу между наследственными и спорадическими опухолями по наличию или отсутствию хромосомы 11q23 соответственно. Другими словами, если наличие данной хромосомы установлено, то гломусные опухоли (хемодектомы) могут передаваться по наследству. Если ее нет, то опухоль, если когда-нибудь возникнет, то спорадически, как и любое другое новообразование. Таким образом, ранняя идентификация 11q23 может служить индикатором наследственного фактора онкогенеза данного вида опухолей [26, 27].
В заключение следует отметить, что гломусные опухоли (хемодектомы) основания черепа были описаны сравнительно недавно — в 1945 г. Они возникают из гломусов, расположенных в среднем ухе или яремной ямке, и относятся к экстраадреналовой эндокринной системе. Способны реагировать на изменения концентрации СО 2 , информируя об этом бульбарные центры головного мозга, а также продуцировать биогенные амины. Могут расти как экстра-, так и интракраниально. Возникают в период эндокринных изменений организма. Причиной также могут служить хроническая гипоксия и наследственная предрасположенность. О наследственном характере хемодектом можно судить только в тех случаях, если больному меньше 18 лет, а также в случае билатеральных или множественных опухолей и положительного тестирования на указанные выше гены. Наследование происходит по аутосомно-доминантному типу. Тестирование на определенные гены позволяет определить спорадический или генетически детерминированный характер гломусной опухоли (хемодектомы).
Наблюдается в различном возрасте, без различия пола.Составляют 1-2% от всех опухолей мягких тканей.Опухоль органоидного типа, развивается из стенок канала Суке-Гойера, являющегося функциональной частью клубочковидного артерио-венозного анастомоза.Он имеет узкий просвет, выстлан эндотелиоцитами и окружен несколькими рядами гломусных клеток, которые рассматриваются как видоизмененные гладкомышечные клетки, изменяющие просвет анастомоза. Клубочки богато иннервированы.
В норме клетки (гломусы) участвуют в регуляции температуры тела и кровяного давления. Гломусы сконцентрированы преимущественно на акральных участках (ладони, подошвы, пальцы кистей и стоп), что определяет преобладающую локализацию опухолей в этих зонах. Однако развиваются и экстраакрально, возможно из миофибробластов, происходящих от стволовых клеток неврального гребешка эмбрионов.
Этиология не установлена. В основном опухоли появляются спорадически, в небольшой части случаев прослежена связь с травмами, беременностью. Множественные поражения могут быть врожденными или наследоваться аутосомно-доминантно с неполной пенетрантностью и варибельной экспрессивностью.
Выделяют 2 формы:
- изолированная (солитарная)
- акральная
- экстраакральная
- нодулярная
- бляшковидная
Изолированная (солитарная) форма
![]()
Солитарные опухоли являются наиболее частыми (90% всех случев) с преобладающей локализацией на акральных участках, особенно субунгвально на пальцах кистей. Подногтевые опухоли наблюдаются в виде узелков розового - пурпурного цвета, размерами 3-10 мм в диаметре, редко крупнее. Они просвечивают через ногтевую пластинку, вызывают ее истончение, появление продольной или поперечной исчерченности. Такие опухоли наблюдаются чаще у женщин в возрасте 20-40 лет. На других акральных и экстраакральных участках (чаще на конечностях) новобразования более крупные (до 2 см и более), мобильные, хорошо ограниченные, куполообразные. Узлы плотные, розового - красно-фиолетового цвета, болезненные при пальпации, располагаются в коже или подкожной клетчатке, иногда приобретают грибовидную форму.
Экстраакральные гломусные опухоли располагаются на голенях, бедрах, туловище, а в ряде случаев имеют необычную локализацию.
- полость рта
- периуретрально у женщин, сопровождающиеся изъязвлением и вагинальным кровотечением
- головка полового члена или кавернозные тела, часто с возникновением приапизма
- пояснично-крестцовый отдел с возникновением кокцидинии
Классическая триада симптомов включает болезненную пальпацию опухолей, повышенную чувствительность к воздействию низких температур и интенсивные спонтанные боли, возникающие пароксизмально с длительностью до 1 минуты, но в течение суток эпизоды могут повторяться многократно и вызывать у больных состояние тревоги и эмоциональной неуравновешенности.
Множественная диссеминированная форма
Множественные опухоли составляют примерно 10% случев. В отличие от солитарных опухолей, они бывают семейными, наследуемыми аутосомно-доминатно, врожденными и очень редко приобретенными. Возникая в детском возрасте, они становятся более выраженными к подростковому периоду.
Расположение множественных гломус-опухолей может быть локализованным, сегментарным или диссеминированным. Наиболее часто поражаются туловище и верхние конечности, реже вовлекаются лицо, волосистая часть головы, половые органы, иногда слизистые рта (десны, внутренняя поверхность губ) и мышцы.
- При нодулярной форме клинические проявления мало отличаются от солитарных гломус-опухолей. Опухоли более мягкие, имеют розовую, темно-голубую, фиолетовую окраску, иногда гиперкератотическую поверхность. Начинаясь с одиночных узлов, они медленно становятся мультифокальными, количество их со временем достигает от нескольких десятков до сотни. У некоторых больных диссеминация происходит на протяжении всей жизни.
- Бляшковидная форма - более редкая, преимущественно врожденная, характеризуется плоскими более крупными опухолями с постепенным изменением окраски до темных оттенков.
Особенностью обеих форм является малая болезненность при пальпации или даже ее отсутствие, сохраняются малоболезненные ощущения только у 40-60% больных. Возможны висцеральные поражения.
Диагноз ставится на основании клинических проявлений, при множественной форме показана биопсия одного из элементов.
Солитарный узел гломус-ангиомы состоит из большого количества мелких сосудов, просветы которых выстланы одним слоем уплощенных эндотелиоцитов. К периферии от них располагаются в несколько слоев гломусные клетки, имеющие слабоэозинофильную цитоплазму и крупные овальные ядра, темноокрашенные гематоксилином, напоминающие эпителиальные элементы. Во многих участках отмечаются их полиморфизм, а также дистрофические изменения. Строма опухоли скудная, представлена аргирофильными волокнами и тонкими коллагеновыми пучками, иногда гиалинизи-рованными. При импрегнации нитратом серебра выявляется большое число нервных волокон, чаще безмиелиновых.
Множественные гломус-ангиомы не имеют капсулы и состоят из более крупных сосудистых щелей неправильной формы. Так же, как и в солитарном узле, сосудистые щели выстланы одним слоем уплощенных эндотелиоцитов, но число гломусных клеток, располагающихся к периферии от эндотелиальных, значительно меньше, а местами они отсутствуют. Увеличения числа нервных волокон не наблюдается. Подобная структура напоминает строение кавернозной гемангиомы.
При иммуногистохимическом исследовании клетки опухоли экспрессируют a-SMA, виментин, MSA, D2-40, фокально - CD34; не окрашиваются на цитокератины, S-100, хромогранин, синаптофизин.
- Невромы
- Ангиолейомиома
- Гранулема инородного тела
- Голубой пузырный невус
- Голубой невус
- Гемангиомы
- Ангиолипома
- Гемангиоперицитома
- Эпидермальня киста
- Метастазы злокачественных опухолей
- Саркоидоз
- Эккринная спираденома
- Меланома
При солитарных формах целесообразно хирургическое иссечение, тем не менее рецидивы развиваются в 12-33% случаев, а у некоторых больных оно сопровождается появлением множественных опухолей. Для удаления мелких, поверхностно расположенных новообразований используют лазеротерапию (СО2, аргоновый, Nd:YAG лазеры).
При множественных опухолях применяется склерозирующая терапии (введение тетрадецил сульфата натрия, полидоканола, гипертонического раствора) или поэтапное хирургическое иссечение
Отделение оториноларингологии-хирургии головы и шеи Центральной дорожной больницы ЗОО Азербайджанской Дороги, Баку, Азербайджан, AZ 1117
кафедра оториноларингологии Российского национального исследовательского медицинского университета им. Н.И. Пирогова, Москва, Россия, 117997
Параганглиома среднего уха. Ретроспективный анализ результатов хирургического лечения
Журнал: Вестник оториноларингологии. 2016;81(2): 26‑29
Цель исследования — анализ результатов и обобщение опыта диагностики и хирургического лечения больных параганглиомой среднего уха (ПСУ). Представлены данные 5 больных (все женщины) ПСУ, у 2 из которых степень распространения соответствовала классу А, а у 3 — классу В согласно классификации U. Fisch. Всем больным с опухолью класса А и 2 больным класса В проведена операция с применением ретроаурикулярно-эндомеатального подхода. У одной больной с опухолью класса В, учитывая распространение опухоли в инфралабиринтное пространство, а также подозрение на разрушение опухолью наружной стенки канала внутренней сонной артерии или вторжение ее в канал, применен ретроаурикулярно-эндомеатально-трансмастоидальный подход. Катамнестическое наблюдение показало отсутствие рецидива опухоли в отдаленные сроки после операции (более 3 лет). У всех больных была отмечена сохранность слуховой функции.
Параганглиома (гломусная опухоль) среднего уха (ПСУ) развивается из гломусных телец (ГТ), расположенных на промонториальной стенке барабанной полости, и по своим клинико-морфологическим особенностям относится к доброкачественным опухолям (злокачественное преобразование — явление крайне редкое). Имея широкую сеть месторасположения ГТ в структурах головы и шеи, параганглиомы могут развиваться также в глазнице, гортани, трахее, яремной ямке, на развилке общей сонной артерии и возвратном нерве. Частота ПСУ составляет 12% среди всех параганглиом головы и шеи [1—5].
Скопление ГТ в среднем ухе чаще всего отмечается вдоль ушного разветвления блуждающего нерва (нерв Арнольда) [4—6] и барабанного разветвления языкоглоточного нерва (нерв Якобсона) [1, 2, 7]. Изредка опухоль может развиваться из ГТ, расположенных вдоль сонно-барабанных канальцев или части лицевого канала [4, 7, 8].
Обладая экспансивным ростом, ПСУ зачастую приводит к патоморфологическим изменениям мягких тканей (барабанной перепонки) и деструкции костных структур — нижней стенки барабанной полости, задней поверхности пирамиды височной кости и наружной стенки канала внутренней сонной артерии (ВСА). При распространении опухоли на близлежащие анатомические области может наблюдаться также поражение некоторых сосудистых и нервных структур. Следовательно, знание анатомо-топографических особенностей ПСУ имеет большое значение как для раннего распознавания опухоли, так и для выбора адекватного метода лечения больных.
Оптимальным методом лечения больных с ПСУ является хирургический, который обычно осуществляется путем отомикрохирургического вмешательства. При этом одни авторы как метод выбора применяют эндомеатальный подход [9—11], другие для обеспечения подхода к опухоли предварительно производят расширение костной части наружного слухового прохода проведением либо межхрящевого разреза по Heerman [12], либо заушного разреза [10, 13—19], а некоторые отдают предпочтение трансмастоидальному подходу [10, 15—17, 19].
Несмотря на определенные успехи, достигнутые в хирургическом лечении больных с ПСУ, вопросы применения эффективного хирургического вмешательства при данной патологии не теряют своей актуальности.
Цель исследования — ретроспективный анализ результатов хирургического лечения больных с ПСУ.
Пациенты и методы
В течение 25 лет (1986—2012 гг.) под нашим наблюдением находились 5 больных с ПСУ (средний возраст 53 года) — 4 женщины и 1 мужчина.
Всем больным наряду с общим клиническим обследованием производили отомикроскопию, камертональное исследование, аудио- и тимпанометрию, КТ и/или МРТ.
Из радиологических методов исследования отдавали предпочтение КТ, данные которой обладают большей информативностью для распознавания раннего процесса развития опухоли и очагов деструкции костных структур (нижней стенки барабанной полости, задней поверхности пирамиды и/или наружной стенки канала ВСА) при распространении опухоли. Были запрограммированы следующие параметры КТ: толщина томографического среза 5 мм, шаг стола томографа 1—1,5 мм. МРТ проводили при подозрении на опухолевую экспансию в анатомические структуры среднего уха и соседние с ней области.
Степени распространения опухоли определяли по классификации U. Fisch и соавт. [17], согласно которой у исследуемых были констатированы опухоли класса, А (опухоль располагается на промонториуме) и В (опухоль возникает в гипотимпануме, распространяется на другие отделы среднего уха и вторгается в сосцевидный отросток).
При удалении ПСУ почти во всех случаях была проведена операция с применением ретроаурикулярно-эндомеатального подхода (РЭП). Только при распространении опухоли в некоторые структуры среднего уха и/или подозрении на вторжение ее в ряд структур сосцевидного отростка и височной кости с целью предотвращения возможных осложнений была произведена расширенная операция с применением ретроаурикулярно-эндомеатально-трансмастоидального подхода (РЭТП). Во всех случаях диагноз был подтвержден патогистологическим исследованием.
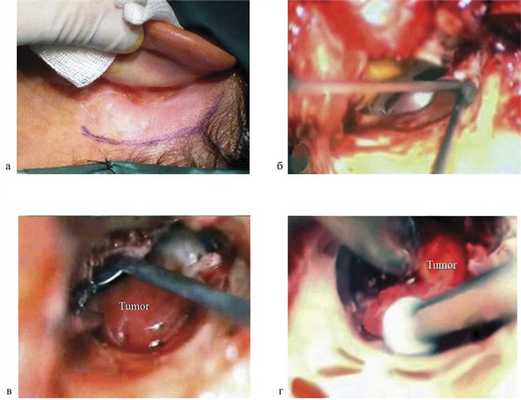
Основные этапы операции с применением РЭП (рис. 1, а—г):
![]()
Рис. 1. Основные этапы операции с применением РЭП при удалении параганглиомы среднего уха класса, А (объяснение в тексте).
— заушный кожный разрез с рассечением наружного слухового прохода (см. рис. 1, а);
— далее под микроскопом: сепарирование и мобилизация тимпаномеатального лоскута на ножке до визуализации опухоли (см. рис. 1, б, в);
— расширение костного наружного слухового прохода бором (здесь может понадобиться дезартикуляция наковальне-стременного сочленения) (см. рис. 1, г);
— удаление опухоли от промонториума с последующей репозицией тимпаномеатального лоскута.
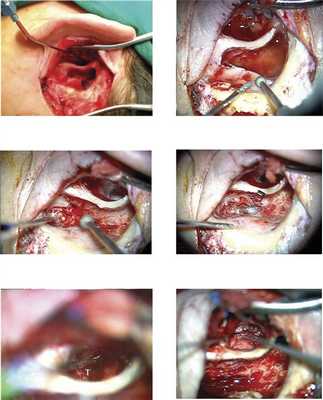
Расширенная операция, осуществляемая РЭТП, наряду с вышеуказанными этапами включала также заднюю тимпанотомию с сохранением задней стенки наружного слухового прохода (рис. 2, а—е):
![]()
Рис. 2. Основные этапы операции с применением РЭТП при удалении параганглиомы среднего уха класса В (объяснение в тексте).
— мастоидэктомия и аттикотомия (расширенная задняя тимпанотомия с сохранением задней стенки слухового прохода) (см. рис. 2, а);
— обнажение сигмовидного синуса (см. рис. 2, б) до места прикрепления заднего брюшка двубрюшной мышцы (см. рис. 2, в);
— удаление нижней стенки барабанной полости до обнажения луковицы яремной вены (здесь также может понадобиться скелетирование канала ВСА) (см. рис. 2, г);
— сепарирование и удаление опухоли из гипотимпанума (см. рис. 2, д);
— устранение дефекта гипотимпанума при помощи свободного височного мышечно-фациального лоскута с последующей репозицией тимпаномеатального лоскута (см. рис. 2, е).
Все больные предъявляли жалобы на медленно развивающийся пульсирующий шум в ухе и прогрессирующую одностороннюю тугоухость. У 4 больных опухоль локализовалась слева, а у одной больной — справа. Отомикроскопически у всех больных за барабанной перепонкой обозревалась опухоль малинового (или красного) цвета, которая выпирала центральную часть барабанной перепонки в просвет наружного слухового прохода.
Из 5 больных с ПСУ у 2 опухоль локализовалась на промонториуме (класс А), у 3 она распространялась на анатомические структуры среднего уха и/или сосцевидного отростка (класс В). Так, у 2 больных с опухолью класса В опухоль занимала мэзо- и гипотимпанум, а у одной больной также распространялась и в сосцевидный отросток — инфралабиринтное пространство. Несмотря на разрешающие диагностические способности КТ и МРТ, в последнем случае не удалось устранить сомнений относительно сохранности нижней стенки барабанной полости и возможной деструкции наружной стенки канала ВСА. Поперечные размеры опухоли колебались от 5 до 6 мм у больных с опухолями класса, А и от 6,5 до 7,5 мм — класса В.
При аудио- и тимпанометрии у всех больных был установлен кондуктивный тип снижения слуха и регистрировано наличие тимпанограммы типа В (отсутствовала величина пика), что свидетельствовало об ограничении подвижности барабанной перепонки (или цепи слуховых косточек).
Из 5 больных с ПСУ у 4 при удалении опухоли был применен ретроаурикулярно-эндомеатальный подход. Только у одной больной с распространением опухоли в инфралабиринтное пространство (класс В) была проведена операция с применением РЭТП.
Результаты и обсуждение
У всех больных было достигнуто полное удаление опухоли. Потеря крови во время операции умеренная (средний объем кровопотери составил 50,5 мл). У одной больной с опухолью класса В, у которой был применен РЭТП, в связи с инфильтрацией опухолью инфралабиринтных ячеек все нижележащие клетки были удалены до достижения коркового слоя нижней стенки барабанной полости. Учитывая подозрение на разрушение опухолью наружной стенки канала ВСА (по данным КТ и МРТ) и возможного вторжения ее в канал, произведено частичное удаление стенки последнего, что позволило устранить все сомнения относительно экспансии опухоли.
Катамнестическое наблюдение показало отсутствие рецидива опухоли в отдаленные сроки после операции (более 3 лет). У всех больных отмечена сохранность слуховой функции: пороги воздушного и костного звукопроведения находились в пределах 10—15 дБ.
В качестве клинического примера, потребовавшего применения РЭТП при удалении опухоли класса В, приводим собственное наблюдение.
Больная Х., 61 года, обратилась с жалобами на снижение слуха и пульсирующий шум в левом ухе, появление которых заметила за 3 мес до обращения.
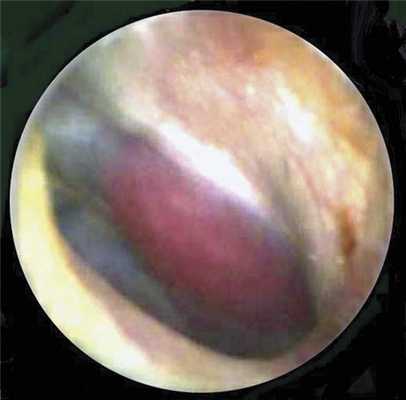
Отомикроскопически за барабанной перепонкой (слева) выявлена малинового цвета пульсирующая опухоль, которая, сдавливая барабанную перепонку, смещала ее центральную часть в просвет наружного слухового прохода (рис. 3).
![]()
Рис. 3. Отомикроскопическая картина параганглиомы левого среднего уха. Опухоль малинового цвета в барабанной полости, сдавливает барабанную перепонку и отодвигает ее центральную часть в просвет наружного слухового прохода.
При КТ височной кости слева обнаружено наличие мягкотканного образования барабанной полости, локализующегося на промонториуме. Опухоль частично занимала гипотимпанум и распространялась в сосцевидный отросток — инфралабиринтное пространство. Наличие выявленного феномена «изъеденность молью» вызывало сомнение в интактности как кортикального слоя нижней стенки барабанной полости, так и наружной стенки канала ВСА (рис. 4). Поперечный размер опухоли составлял 7,5 мм.
Рис. 4. Компьютерная томограмма височной кости больной параганглиомой левого среднего уха. а — опухоль локализуется на промонториуме; б — распространяется в гипотимпанум и проникает в инфралабиринтное пространство; в — выявленный феномен «изъеденность молью» (объяснение в тексте).
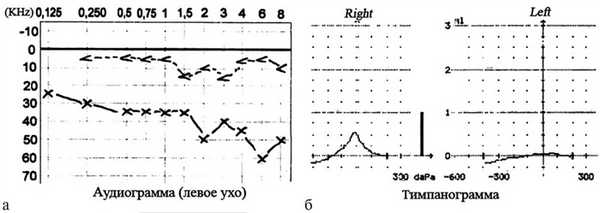
По данным аудио- и тимпанометрии выявлены кондуктивный тип снижения слуха (воздушно-костный интервал увеличен более 20 дБ) и ограничение подвижности барабанной перепонки (отсутствие пика) по типу В, которые, несомненно, были обусловлены наличием опухоли в среднем ухе (рис. 5).
![]()
Рис. 5. Аудио- и тимпанометрическая картина больной параганглиомой левого среднего уха. а — наличие кондуктивного типа снижения слуха; б — ограниченная подвижность барабанной перепонки (и/или цепи слуховых косточек) по типу В (отсутствие пиков).
Клинический диагноз: новообразование левого среднего уха, предположительно параганглиома (класс В), пульсирующий субъективный шум в ухе, вторичная кондуктивная тугоухость слева.
Больной произведена операция — удаление опухоли с применением РЭТП. Энуклеация опухоли сопровождалась умеренным кровотечением, которое остановилось после ее полного удаления (объем кровопотери составил 55 мл).
Макропрепарат: округлой формы опухоль размером 5×2,5 мм, имеет мягкую консистенцию и ровную поверхность. Патогистологическое заключение: элементы нехромаффинной параганглиомы.
При обследовании через 8 мес после операции больная жалоб не предъявляет, рецидив опухоли не обнаружен. Аудиометрическое исследование свидетельствовало о сохранности слуховой функции: пороги воздушного и костного звукопроведения находились пределах 10—15 дБ.
Заключение
В отличие от некоторых параганглиом головы и шеи (каротидная хемодектома, параганглиома яремного отверстия, вагальная параганглиома), зачастую требующих мультидисциплинарного подхода в лечении (с привлечением онкологов, нейрохирургов, сосудистых хирургов и радиологов), при ПСУ преобладает монодисциплинарный подход, предусматривающий отомикрохирургическую операцию.
Анализируя представленные результаты, можно констатировать, что применение РЭП позволяет осуществить полное удаление почти всех ПСУ (классы, А и В), существенно не нарушая функции органа слуха. В случаях проникновения опухоли в сосцевидный отросток — инфралабиринтное пространство (класс В) и возникающих при этом сомнениях в интактности нижней стенки барабанной полости и наружной стенки канала ВСА, предпочтительна расширенная операция с применением РЭТП. С нашей точки зрения, данная операция может обеспечить адекватный подход к некоторым анатомическим структурам среднего уха (нижней стенки барабанной полости), сосцевидного отростка (инфралабиринтное пространство) и височной кости (наружной стенки канала ВСА) при подозрении на опухолевую экспансию.
Параганглиома среднего уха ( Гломангиома среднего уха , Гломусная опухоль среднего уха , Нехромаффиннная параганглиома среднего уха , Хемодектома среднего уха )
Параганглиома среднего уха - это доброкачественная опухоль, сформированная из нехромаффинных параганглиев, расположенная на медиальной стенке барабанной полости. К основным клиническим проявлениям заболевания относятся снижение слуха, пульсирующий шум в ушах, неврологическая симптоматика. Высокой информативностью в диагностике параганглиомы обладают микроотоскопия, рентген и компьютерная томография височной кости, магнитно-резонансная томография. Основное лечение включает проведение хирургического вмешательства, лучевой терапии. В случаях, когда операция не показана, могут быть назначены симптоматические средства (НПВС, анальгетики).
МКБ-10
![Параганглиома среднего уха]()
Общие сведения
Параганглиома (гломусная опухоль, нехромаффиннная параганглиома, хемодектома, гломангиома) среднего уха - одна из доброкачественных опухолей головы и шеи, поражающая преимущественно барабанную полость, сосуды, нервы. Впервые была описана в 1941 году американским профессором анатомии С. Гилдом. Гломусная опухоль встречается с частотой 1:300000, является одним из самых распространённых доброкачественных образований среднего уха. Известно, что женщины болеют в 5-7 раз чаще мужчин. Основные симптомы заболевания манифестируют в возрасте 55-60 лет, у детей и подростков такая патология обнаруживается крайне редко.
Причины
В настоящее время причины развития гломангиомы достоверно неизвестны. Выявлено, что она может возникать спонтанно под действием внешних воздействий среды на организм человека или же наследоваться по аутосомно-доминантному типу от родителей. За развитие наследственных форм болезни отвечают мутации генов, участвующих в кодировании B, C, D ферментно-митохондриального комплекса сукцинат-дегидрогеназы. Опухоль может входить в структуру генетических заболеваний (синдром МЭН 2А типа, болезнь Гиппеля-Линдау).
Спорадическая хемодекома формируется у людей в возрасте 40-50 лет. На её развитие могут оказывать влияние инфекционные заболевания, бесконтрольный приём стероидов и гормональных контрацептивов, аутоиммунные болезни. Также причиной возникновения образования из параганглиев могут стать любые состояния, приводящие к изменению работы эндокринной системы. К ним относят беременность, патологии яичников, щитовидной железы.
Патогенез
Параганглиома образуется из гломусных телец, которые располагаются во внешней оболочке луковицы яремной вены, в области мыса, по ходу ветвей языкоглоточного, блуждающего нерва, а также в пирамиде височной кости. Эти клетки представляют собой хеморецепторы и реагируют на различные стимулы путем синтеза гормонов. При развитии опухолевого перерождения клеток образование биологически активных веществ происходит постоянно.
Элементы АПУД-системы могут продуцировать катехоламины и пептидные гормоны. В процессе роста доброкачественное образование проникает в барабанную полость, заполняет её, постепенно нарушая целостность барабанной перепонки, повреждая прилежащие сосуды и нервы. По мере разрастания гломусная опухоль может выступать в наружный слуховой проход.
При гистологическом исследовании выявляются крупные округлые клетки с явлениями секреторной активности (образование в цитоплазме вакуолей, наличие в ней гранул). Клетки опухоли формируют клубочки, вдающиеся в просвет сосудов. Соединительная ткань параганглиомы представлена коллагеновыми волокнами, синусоидными капиллярами. Участки между клетками заполнены мелкозернистым веществом, образующим гомогенную массу.
Симптомы
У большинства пациентов с параганглиомой среднего уха клиническая картина развивается постепенно и связана с повреждением внутричерепных нервов. Больные жалуются на снижение остроты слуха, периодически возникающий звон в ушах. Он имеет пульсирующий характер, может усиливаться при наклонах вниз или резких движениях головой. Эти симптомы связаны не только с разрушением лабиринта, но и с компрессией улиточной части преддверно-улиткового нерва.
Если опухоль выходит в просвет слухового прохода, она часто травмируется, что сопровождается незначительными кровянистыми выделениями, которые остаются на подушке и волосах после сна. В некоторых случаях пациенты жалуются на периодическое повышение артериального давления. Это напрямую связано с избыточным образованием биологических веществ, увеличивающих тонус сосудов.
Общая неврологическая симптоматика при гломусном новообразовании характеризуется развитием постоянных головных болей диффузного характера, слабостью, усталостью. Наблюдается снижение работоспособности, ухудшается память и концентрация. При поражении преддверной части VIII черепного нерва страдает вестибулярный аппарат. Развивается нистагм, могут возникать головокружения и обморочные состояния.
Осложнения
Без лечения гломангиома прогрессирует, что способствует потере слуха, развитию псевдобульбарного синдрома, неврита лицевого нерва. Это может привести к тяжёлым неврологическим расстройствам. Находящееся в просвете слухового прохода образование легко травмируется, в области повреждения может возникнуть инфекция. При нарушении целостности сосудов гломусной опухоли возникает внутреннее кровотечение в полость черепа. В редких случаях (менее 5%) происходит перерождение доброкачественной опухоли в злокачественную с последующим метастазированием.
Диагностика
Диагноз параганглиомы среднего уха ставится на основании жалоб больного, данных осмотра врача-отоларинголога, инструментальных и лабораторных исследований. В рамках диагностических мероприятий показана консультация невролога. К основным методикам, применяемым для верификации диагноза, относят:
- Физикальное обследование. При осмотре в наружном слуховом проходе обнаруживается образование, напоминающее полип, которое обладает контактной кровоточивостью. Показательным является положительный симптом пульсации при введении воронки в слуховой проход. Использование микроотоскопии позволяет выявить контуры параганглиомы в виде бордового пятна за барабанной перепонкой.
- Неврологические исследования. Для определения характера поражения нервов используется электронейромиография: она регистрирует снижение скорости проведения нервных импульсов. Функцию вестибулярного аппарата оценивают с помощью обертовой пробы, пробы Ромберга.
- Исследование функции органов слуха. С этой целью проводятся камертональные пробы. Чаще выявляется нейросенсорная тугоухость, связанная с повреждением слухового нерва. Аудиометрия позволяет оценить остроту слуха, снижающуюся при развитии доброкачественной хемодектомы.
- Генетическое обследование. У всех пациентов с параганглиомой обязательно собирается семейный анамнез, чтобы установить наследственную предрасположенность и составить родословную. Полимеразная цепная реакция с ДНК пациента обнаруживает мутации в геноме, отвечающие за развитие опухолевого процесса.
- Лабораторные исследования. Биохимическое исследование крови и мочи позволяет оценить уровень метаболитов катехоламинов. Их повышение указывает на избыточное образование этих биологических веществ и является косвенным доказательством наличия нехромаффинного образования.
- Инструментальные исследования. Чтобы определить характер поражения, размеры и локализацию патологического образования, используют рентгенографию, КТ височной кости. Магнитно-резонансное исследование позволяет определить степень повреждения венозных и артериальных сосудов головы . Ангиография используется непосредственно перед оперативным вмешательством и выявляет источники кровоснабжения гломангиомы.
Дифференциальный диагноз параганглиомы на начальной стадии проводится с отосклерозом, аневризмой сонной артерии, средним отитом. При повреждении нервов патологию необходимо дифференцировать с параличом гортани, гемангиомой, невритом лицевого нерва. Реже дифдиагностика осуществляется с невриномой преддверно-улиткового нерва, холестеатомой среднего уха, черепно-мозговой травмой.
Лечение параганглиомы среднего уха
Хирургическое лечение хемодектомы проводится в отделении отоларингологии. Больному необходимо соблюдать палатный режим, а также придерживаться диеты с большим содержанием белков, витаминных и минеральных комплексов. К основным методам лечения относятся:
- Лучевая терапия. Использование гамма-ножа, кибер-ножа, линейного и протонного ускорителя позволяет удалить опухолевые клетки и предотвратить дальнейший рост образования. Радиохирургия может быть использована в качестве дополнения к хирургическому лечению или в форме монотерапии у пожилых пациентов.
- Хирургическое вмешательство. Операция проводится как традиционным открытым методом, так и с помощью эндоскопического оборудования. Перед ней осуществляется эмболизация источников кровоснабжения опухоли, способствующая деваскуляризации патологического образования. Гломангиома полностью или частично удаляется вместе с изменёнными тканями, восстанавливается целостность височной кости. При необходимости осуществляется реконструкция барабанной перепонки.
- Симптоматическая терапия. При неоперабельной параганглиоме с целью облегчения общего состояния пациентам назначают анальгетики, нестероидные противовоспалительные препараты. Для компенсации тугоухости используются классические слуховые аппараты.
Прогноз и профилактика
При своевременном удалении параганглиомы среднего уха прогноз для жизни и здоровья пациента благоприятный. Уже в первую неделю после оперативного вмешательства наблюдается исчезновение основных симптомов, нормализуется слух. При необоснованном отказе от хирургического лечения существует вероятность развития опасных для пациента осложнений. Профилактика развития параганглиомы сводится к проведению генетического исследования у людей, входящих в группу высокого риска, а также к защите организма от неблагоприятных воздействий внешней среды в течение жизни.
1. Хирургическое лечение параганглиом пирамиды височной кости/ Гуляев Д.А., Чеботарев С.Я., Яковенко И.В.// Креативная хирургия и онкология. - 2011.
2. О диагностике и тактике лечения гломусных опухолей с интракраниальным ростом/ Мустафин Х.А., Смагулов Ф.Х., Бердиходжаев М.С., Шпеков А.С., Толбаева Г.К., Сыздыкбаева Ш.М.// Нейрохирургия и неврология Казахстана. - 2012.
3. Гломусная опухоль (параганглиома) уха. Современное состояние проблемы. Литературный обзор/ Аникин И.А. , Комаров М.В.// Российская оториноларингология - 2010 - № 4.
Читайте также: