Грибковые осложнения антибиотикотерапии. Кандидоз на фоне лечения антибиотиками
Добавил пользователь Alex Обновлено: 28.01.2026
Влагалищный микоз является одним из наиболее распространенных, но и наиболее неприятных побочных эффектов антибиотикотерапии. Почему при приеме антибиотиков развивается грибковая инфекция и как с ней бороться?
Чтобы ответить на этот вопрос, сначала нужно узнать, как работают антибиотики. Антибиотики — это вещества, которые вырабатываются определенными микроорганизмами — бактериями и грибками, которые уничтожают другие микроорганизмы. Их открытие является одним из величайших достижений медицины, поскольку оно помогает бороться со многими опасными заболеваниями, лечение которых ранее не было известно и которые наносили урон на протяжении веков.
Влияние антибиотиков на микрофлору влагалища
К сожалению, при антибиотикотерапии уничтожаются не только патогенные микроорганизмы, но и полезные бактерии, которые являются частью физиологической флоры человека. Бактериальная флора является основой многих иммунных процессов — она предотвращает инфекции и помогает синтезировать витамины. Когда ее баланс нарушается, вредные микроорганизмы, которые могут вызвать интимные инфекции, выходят на первый план.
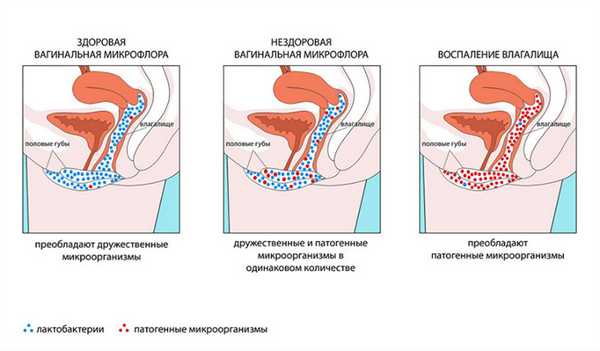
Влияние антибиотиков на микрофлору влагалища
Candida albicans, вызывающая микоз влагалища (молочница, кандидоз), присутствует в организме человека в безопасном количестве, но в случаях ослабления иммунитета, что часто возникает во время антибактериальной терапии, она начинает размножаться. Кроме того, антибиотики уничтожают колонии полезных пробиотических бактерий, таких как Lactobacillus, которые защищают женщину от влагалищного микоза.
Микоз влагалища после приема антибиотика — что его вызывает?
Влагалищный микоз после приема антибиотиков развивается не у всех пациенток. Ему подвергаются женщины, прошедшие длительную антибактериальную терапию, имеющие общие иммунные нарушения, страдающие диабетом, дефицитом витаминов, гормональными нарушениями или соблюдающие диету, богатую углеводами.
Влагалищный микоз после антибиотика — симптомы
Симптомами влагалищного микоза при антибиотикотерапии чаще всего являются сильный зуд в интимных зонах, а также жжение и боль во время полового акта. Также могут быть обильные водянистые или сыроподобные выделения.
Сильный зуд в интимной зоне
Как лечить микоз влагалища после приема антибиотика?
Антибиотики действуют против бактерий, но не против грибков. Таким образом, вагинальный микоз требует отдельной медицинской консультации во время антибиотикотерапии. Ваш гинеколог, вероятно, назначит лечение вагинального микоза в форме таблеток или мазей — нистатин или клотримазол. Если симптомы очень тяжелые или длительные, а инфекция обширная, может потребоваться лечение флуконазолом.
В терапии вагинального микоза на фоне приема антибиотиков врач может назначить местный иммуномодулятор ГЕПОН®. В основе препарата — олигопептид из 14 аминокислот, который оказывает комплексное иммуномодулирующее и противовирусное действие на клетки организма.
Назначение иммуномодулятора ГЕПОН® не требует предварительного определения чувствительности к различным видам грибов. Препарат обладает противовоспалительным и иммуномодулирующим эффектом и позволяет:
- увеличить функциональную активность клеток, которые защищают организм от грибов, бактерий и вирусов;
- усилить синтез альфа- и бета-интерферонов;
- подавить размножение вирусов.
Исследования подтверждают, что у 83% пациенток неприятные симптомы микоза влагалища — зуд, жжение, отек — проходят уже через два дня после начала приема препарата. ГЕПОН® назначают не только в терапевтических, но и в профилактических целях.
Очень важным элементом, поддерживающим лечение микоза влагалища после приема антибиотика, является диета. Сладости, сладкие напитки и продукты, богатые углеводами, должны быть ограничены.
В интернете можно прочитать, что восстановить естественную бактериальную флору можно, используя пробиотики. Натуральные пробиотики присутствуют в кисломолочных продуктах. В аптеке продаются готовые пробиотические препараты, которые помогут бороться с инфекцией. Но важно понимать, что сами по себе пробиотики не могут вылечить микоз — это всего лишь дополнительный метод, входящий в комплексное лечение.
Кандидоз и этиотропная терапия
Н.В. БЕЛОБОРОДОВА, доктор медицинских наук, профессор, главный научный сотрудник академической группы академика РАМН Ю.Ф. Исакова.
При участии Ж.И. АРХИПОВОЙ, кандидата медицинских наук, НИИ детской гематологии. Серьезные экологических изменения, происходящие на планете в последние десятилетия, не могли не сказаться на состоянии микроэкологии и иммунореактивности современного человека.
В этом - одна из глобальных причин роста грибковых заболеваний, которыми сегодня, по данным Всемирной организации здравоохранения, страдает каждый пятый житель планеты. Чаще проявлениями грибковых заболеваний являются различные локальные поражения кожи, ногтей, слизистых оболочек полости рта, кишечника, уретры и влагалища, однако при серьезных нарушениях иммунореактивности организма может наступить генерализация процесса, и тогда грибковые заболевания приобретают жизнеугрожающий характер.
На фоне достижений современной медицины, увеличения продолжительности жизни наиболее ослабленных больных (глубоконедоношенные дети, пациенты с опухолями и иммунодефицитами) в лечебных учреждениях наблюдается широкое распространение инвазивных микозов, которые составляют до 12% в этиологической структуре внутрибольничных инфекций и до 40% в структуре инфекционной летальности. Ученые из Центра контроля заболеваемости (Атланта, США) называют кандидоз внутрибольничной эпидемией последнего десятилетия, так как заболеваемость им иммунокомпрометированных больных возросла в 11 раз.
Колонизация слизистых грибами Candida у практически здоровых людей колеблется от 15 до 40% и может возрасти до 80% на фоне какой-либо патологии в условиях длительной госпитализации, но инвазивный микоз у них не развивается благодаря большому количеству защитных механизмов против грибковой инфекции. Защитные механизмы, не связанные с иммунной системой, включают барьеры в виде кожи и слизистых, а также конкурентные взаимодействия с нормальными бактериями, которые обеспечивают защиту от кандидоза и других микозов посредством соревнования за пищу и, возможно, посредством локальной продукции веществ с антифунгальной активностью. Само по себе разрушение барьеров химической травмой, ожогом или операцией, как и нарушение нормального биоценоза кишечника после длительного применения антибиотиков широкого спектра действия, крайне редко приводит к развитию системного микоза, но вызывает предпосылки для этого в виде локального избыточного накопления грибов в тех местах, где действие физиологических барьеров нарушено.
Общеизвестными факторами риска возникновения грибковой инфекции являются длительная антибиотикотерапия и снижение защитных сил организма. В нормальном организме нейтрофилы, макрофаги и эозинофилы фагоцитируют и убивают бластоспоры кандид, а альвеолярные макрофаги и нейтрофилы способны блокировать прорастание спор аспергилл. Нейтрофилы и моноциты уничтожают также псевдогифы Candida и гифы Aspergillus. Поэтому первыми кандидатами на развитие диссеминированного кандидоза и аспергиллеза являются больные с количественными и функциональными дефектами нейтрофилов, особенно в условиях депрессии Т-клеточного звена иммунной сиcтемы. К специфическим условиям относится лекарственная нейтропения на фоне лечения цитостатиками, особенно глубокая (14 дней нейтрофилы
У пациентов с онкогематологическими заболеваниями к появлению специфических факторов риска инвазивного микоза приводит терапия. На современном этапе она обязательно включает мощные цитостатики, глюкокортикоиды и антибиотики широкого спектра действия. Помимо возникновения нейтропении цитостатики приводят к разрушению кожных и слизистых барьеров, глюкокортикоиды угнетают Т-лимфоциты и макрофаги, антибиотики нарушают биоценоз кишечника. Неудивительно, что в онкогематологических стационарах инвазивные микозы становятся все возрастающей проблемой.
Барьер №1 - конкурентное взаимодействие грибов с бактериями нормальной микрофлоры хозяина
Барьер №2 - целостность кожи и слизистых
Барьер №3 - фагоцитоз и иммунологические реакции
Основные факторы, способствующие разрушению барьеров
№1 - неадекватная (избыточная) антибиотикотерапия
№2 - повреждение эпителия (механическое, токсическое, воспалительное), замедление регенерации, авитаминоз
№3 - снижение иммунореактивности под влиянием цитостатиков, стероидных гормонов
Еще в 80-е годы грибковые инфекции возникали в основном на фоне длительной госпитализации, продолжительной антибиотикотерапии и повторных курсов химиотерапии. Средняя продолжительность периода от момента установления диагноза онкогематологического заболевания до развития грибкового осложнения составляла 19 месяцев. В настоящее время все чаще грибковые инфекции стали наблюдаться на ранних этапах лечения цитостатиками. Это связано как с агрессивностью режимов полихимиотерапии, так и с широким применением современных супермощных антибиотиков.
Важно отметить, что инвазивные грибковые поражения могут развиваться не только у больных при явнымх дефектах иммунореактивности, но и у пациентов с любыми хирургическими заболеваниями в случае осложненного течения послеоперационного периода, реанимационных мероприятий, интенсивной терапии, длительной искусственной вентиляции легких. Мы наблюдали таких пациентов после тяжелых комбинированных травм, после повторных операций по поводу абдоминального сепсиса, после кардиохирургических, нейрохирургических операций и др. В этих случаях предрасполагающим моментом является совокупность факторов, снижающих барьерную функцию слизистых оболочек (стресс, нарушения гемодинамики, гипоксия, длительная невозможность энтерального питания и др.) в сочетании с массивной комбинированной антибиотикотерапией, к сожалению, необходимой у больных высокого риска по жизненным показаниям. Забегая вперед, следует отметить, что даже при выделении грибов из крови или очагов инфекции при проведении целенаправленной противогрибковой терапии у таких пациентов не представляется возможным отказаться от одновременного введения антибиотиков в связи с высокой опасностью септического шока.
Самым частым видом микоза является кандидоз. В списке возбудителей кандидоза лидирующее место занимает Candida albicans. Этим видом грибов вызывается более 80% кандидозов. Однако инфекция может быть вызвана и другими видами: С. tropicalis, С. parapsilosis, С. krusei, С. lusitaniae, Torulopsis glabrata.
Кандидоз в зависимости от степени поражения может быть классифицирован как поверхностный и глубокий. Поверхностный кандидоз включает кожный, орофарингеальный, мочеполовой и характеризуется поражением соответствующих слизистых. Наиболее опасен глубокий кандидоз, составляющий основной спектр кандидозных инфекций у иммунокомпрометированных больных, который может быть классифицирован как фунгемия, диссеминированный кандидоз и кандидоз отдельных органов.
Инвазивное кандидозное поражение желудочно-кишечного тракта (ЖКТ). Считается общепризнанным, что ЖКТ является основным эндогенным резервуаром Candida, откуда происходит проникновение грибов в кровь (феномен транслокации) и последующее распространение инфекции по организму. Однако у больного с агранулоцитозом локальное поражение ЖКТ грибами рода Candida не ограничивается хорошо описанной в литературе ролью "ворот" для диссеминации, а само по себе может вызвать жизнеугрожающие состояния: прогрессирование поражения быстро приводит к множественной инфильтрации или некрозам всей толщи стенки пищеварительного канала, вызывая такие тяжелые осложнения, как кишечная непроходимость, перитонит, желудочно-кишечное кровотечение, вплоть до летального исхода.
Поражение легких. Грибы рода Candida часто высеваются из респираторных секретов, однако клиническое значение таких высевов в большинстве случаев невелико, так как колонизация ротовой полости и верхних дыхательных путей приводит к контаминации мокроты. Более того, легочная инфекция грибами Candida обычно возникает в результате гематогенного распространения, и мокрота у таких больных не отделяется вовсе. Симптомы кандидозной пневмонии схожи с клиническими проявлениями бактериальной пневмонии, но носят более непостоянный характер. Обращает на себя внимание несоответствие выраженных нарушений дыхания скудным аускультативным и рентгенологическим признакам. Рентгенологические нарушения могут ограничиваться изменениями корня и усилением сосудистого рисунка, почти в половине случаев наблюдается рентгенонегативная кандидозная пневмония. В финале заболевания может развиться диссеминация по обоим легочным полям. Рентгенологически этот процесс характеризуется появлением множественных "мигрирующих" облаковидных теней. Сегодня для диагностики поражения легких у иммунокомпрометированных больных наиболее широко используется бронхоальвеолярный лаваж с последующим микробиологическим исследованием.
Поражение кожи встречается в 5-10% случаев острого диссеминированного кандидоза. Классически оно имеет вид плотных, приподнимающихся над поверхностью узлов 0,5-1 см в диаметре, розово-красного цвета, не исчезающих при надавливании. Однако у большинства больных изменения на коже представляют собой просто папулезную или пятнисто-папулезную сыпь, часто неотличимую от медикаментозной.
Изменения на коже и инфильтраты мягких тканей часто становятся информативным материалом для идентификации возбудителя, так как поверхностное расположение делает их удобными для биопсии. Сочетание посева с гистологическим исследованием значительно увеличивает этот показатель. Следует иметь в виду, что поражения кожи при кандидозе затрагивают дерму, в то время как поверхностный слой эпидермиса остается интактным, поэтому клиницист должен быть очень внимателен при заборе материала. При гистологическом исследовании обычно находят псевдомицелий грибов, фибрин и небольшие геморрагии в сочетании с отеком стенки сосудов и периваскулярной ткани.
Поражение ЦНС. Кандидозный менингит встречается относительно редко, наиболее характерен для новорожденных и недоношенных детей, а также как вторичное осложнение при шунтирующих нейрохирургических вмешательствах. В случае развития у имунокомпрометированных больных имеет исключительно агрессивное течение. Поражение оболочек головного мозга характеризуется достаточно ярко выраженными общемозговыми и менингеальными симптомами, а также нейтрофильным или лимфоцитарным плеоцитозом в ликворе - в зависимости от степени нейтропении. Candida имеет низкую высеваемость из ликвора, при морфологическом исследовании ликвора друзы гриба или псевдомицелий обнаружить, как правило, не удается, клинические симптомы (лихорадка, головная боль) не специфичны, поэтому грибковая природа менингита у больных с нейтропенией редко распознается при жизни. Внутримозговые абсцессы, связанные с Candida, могут вызывать очаговую неврологическую симптоматику, соответствующую их локализации.
Поражение сердца. Клиника кандидозного эндокардита не отличается от клиники бактериального, сопровождается длительной лихорадкой и формированием вегетаций на клапанах сердца. Особенностью этой локализации является частое сочетание с фунгемией: хотя бы однократный высев Candida из крови имеют до 80% больных кандидозным эндокардитом. На фоне иммунодефицита могут развиваться грибковые микроабсцессы в миокарде, что иногда проявляется аритмиями. Возможна закупорка грибковыми тромбоэмболами кардиальных артерий с развитием ишемии и сердечной недостаточности.
Хронический диссеминированный кандидоз (ХДК). Наиболее важный маркер ХДК - поражение печени и селезенки. Именно микроабсцессы в этих органах определяют хронический характер течения болезни. Термины "ХДК" и "гепатолиенальный кандидоз" в литературе являются синонимами. Клинически ХДК проявляется увеличением печени и селезенки на фоне длительной лихорадки. Иногда заболевание сопровождается желтухой или болями в правом подреберье. В крови отмечаются высокий лейкоцитоз и выраженная гипербилирубинемия (в основном за счет прямой фракции) в среднем у половины больных. Уровень трансаминаз повышается непостоянно и не более, чем в 3 раза. Наблюдения позволяют сказать, что в целом у большинства больных поражение печени грибами выглядит как холестатический гепатит. Такая особенность приводит к тому, что ХДК часто ошибочно принимается за токсическое поражение цитостатиками, особенно при отсутствии характерных изменений на УЗИ. Кандидозные микроабсцессы в паренхиматозных органах выглядят при ультразвуковом исследовании и компьютерной томографии как гипоэхогенные очаги, поэтому многие клиницисты считают обнаружение этих характерных изменений диагностическим критерием, подтверждающим инвазивную грибковую инфекцию.
Кандидемия. Многие авторы утверждают, что Candida spp., высеянная из крови, редко является контаминантом и должна быть принята во внимание как патоген практически во всех случаях. Фунгемия обнаруживается примерно в 30% случаев диссеминированного кандидоза и имеет важное диагностическое значение, так как служит основным прижизненным доказательством инвазивного кандидоза. Повторная (стойкая) кандидемия может быть результатом инфицирования центрального венозного катетера или проявлением деструктивного поражения глубоких тканей.
С момента возникновения проблемы грибковых инфекций в 60-70-е гг. огромные усилия медиков всего мира были направлены на разработку методов диагностики этих опасных осложнений, так как ранняя диагностика остается основным критическим моментом, определяющим успех в ведении больного с инвазивной инфекцией. Однако до настоящего времени от 20 до 75% случаев инвазивных микозов диагностируется лишь на аутопсии.
Кроме классических микробиологических методов серьезным подспорьем в лабораторной диагностике сегодня является определение маркеров кандидоза - Д-арабинитола и маннозы - методом газовой хроматографии. Даже при трудной локализации очага, недоступного для биопсии и посева, обнаружение высокого уровня маркеров в крови или спинномозговой жидкости позволяет подтвердить диагноз кандидоза, кроме того, в динамике объективно оценить эффект противогрибковой терапии.
Профилактика и лечение. Широко распространено мнение о необходимости одновременно с антибиотиками принимать нистатин, что гарантирует от грибковых осложнений. Действительно, нистатин препятствует массивному размножению кандид на слизистых ЖКТ. Однако крайне важно учитывать, что этот препарат не всасывается при приеме внутрь, то есть не способен воздействовать на клетки грибов, находящиеся вне просвета кишечника. Поистине революционным событием в этиотропной терапии кандидоза следует считать появление препарата флуконазола, наиболее известного под торговым названием дифлюкан. Хорошая биодоступность препарата обеспечивает высокую эффективность практически при любой локализации процесса - от распространенных кожных поражений до менингита. Почти всегда рекомендуется прием препарата внутрь за исключением редких случаев крайне тяжелого состояния больного, когда препарат вводят внутривенно. Благодаря отсутствию токсичности и низкой частоте побочных реакций флуконазол применяется даже у недоношенных детей. Очень важно правильно соблюдать режимы дозирования (см. табл.).
| Пациенты | Показания и дозы флуконазола | ||
| Новорожденные и дети раннего возраста | кандидоз кожи и слизистых 5-6 мг/кг 1 раз в день 5 дней | грибковый сепсис 10 мг/кг 1 раз в день 10-14 дней | грибковый менингит 15 мг/кг 1 раз в день 10-14 дней |
| Взрослые | кандидоз кожи и слизистых 50 мг 1 раз в день 5 дней | вагинальный кандидоз 150 мг однократно (!) | кандидемия, диссеминированный кандидоз 200-400 мг 1 раз в день 2-4 недели |
Когда терапия флуконазолом не дает эффекта, следует думать о кандидозе, вызванном природно резистентными видами кандид, например C.krusei. В этих случаях рекомендуется противогрибковая терапия эффективным, но потенциально токсичным препаратом амфотерицин В (относительно менее высокой токсичностью характеризуется препарат с торговым названием фунгизон). Лечение проводится только в стационаре под тщательным лабораторным контролем. Дозы амфотерицина В из-за опасности нефротоксических реакций не должны превышать 0,5-1 мг/кг в сутки внутривенно один раз в день или через день. При наличии микроабсцессов в печени, головном мозге и других органах наиболее эффективными являются липосомальные формы амфотерицина В (амфоцил и др.), которые, однако, малодоступны из-за высокой стоимости.
Таким образом, в настоящее время актуальность своевременной диагностики и раннего лечения кандидоза чрезвычайно высока.
Современные аспекты лечения вульвовагинального кандидоза
Вульвовагинальный кандидоз (ВВК) - одно из наиболее часто встречающихся заболеваний, с которыми на практике приходится сталкиваться акушерам и гинекологам. Вульвовагиниты, обусловленные грибковой инфекцией, занимают, по данным разных авторов, от 30 до 40% в структуре инфекционных поражений наружных половых органов (вульвы и влагалища) и их число неуклонно увеличивается. Причем ВВК является одной из наиболее частых причин обращения женщин за медицинской помощью. Чаще им страдают женщины репродуктивного возраста. ВВК представляет собой значительную социальную проблему, существенно снижает качество жизни женщины, может привести к осложнениям беременности.
Существует ряд известных факторов, предрасполагающих к развитию ВВК:
- • изменение гормонального фона (беременность, постменопауза). Риск развития вагинального кандидоза изменяется в соответствие с фазами менструального цикла, причем пик заболеваемости приходится на вторую фазу цикла. Это связано с повышением содержания гликогена в эпителиоцитах, сдвигом рН и угнетением механизмов иммунной защиты;
- • лечение некоторыми лекарственными препаратами может быть осложнено развитием вагинального кандидоза (антибиотики, иммунодепресанты, кортикостероиды, контрацептивы и спермициды). Антибиотики широкого спектра действия подавляют нормальную вагинальную флору, включая лактобактерии (Lactobacterium acidophillus). Нарушение структуры нормальной бактериальной флоры может изменять кислую pH влагалища и уменьшать конкуренцию за нутриенты, такие как гликоген. Эти факторы облегчают пролиферацию кандиды во влагалище, что приводит к развитию инфекции.
Развитию ВВК способствуют хронические заболевания женских половых органов, как воспалительные, так и дисгормональные. Также важно состояние желудочно-кишечного тракта (качество пищи, нерегулярное питание, различные диеты, которые приводят к дисбактериозу кишечника).
ВВК - болезнь современной цивилизации, его развитию способствуют ношение белья из синтетических тканей, плотно облегающих тело. В этих условиях создается микроклимат с повышенной влажностью и температурой, что приводит к мацерации рогового слоя кожи, возникновению термостатных условий для развития местной микрофлоры, в частности грибов.
Необходимо отметить неадекватное спринцевание (контрацепция, самостоятельное лечение), применение современных интимных средств гигиены, которые являются триггером развития реакции гиперчувствительности и предрасполагают к колонизации грибковой инфекции.
Также важную роль в развитии ВВК играет сексуальное поведение: орогенитальные контакты, высокая частота половых сношений [12].
Вульвовагинальный кандидоз чаще всего вызывается избыточным ростом дрожжевого гриба Candida albicans, который в норме находится в вагинальной флоре. С. albicans является единственной причиной вагинального кандидоза в 85-90% случаев, на остальные виды Candida (C. glabrata, C. krusei, C. tropicals, C. parapsilosis, C. lusitaniae) остается 10-15%.
C. albicans - нормальный компонент флоры влагалища, кожи и кишечника. Более 40% женщин имеют C. albicans в составе вагинальной флоры без симптомов болезни. В нормальных условиях Candida не вызывает заболевания. Тем не менее все виды C. albicans - оппортунистические патогены, и при определенных условиях под действием экзогенных и/или эндогенных факторов, они могут расти, становятся патогенными и вызывают заболевание.
Причинами возникновения ВВК являются трансформация сапрофитной формы дрожжеподобных грибов в вирулентную и аутоинфицирование из экстрагенитальных очагов кандидоза (преимущественно из кишечника) [2].
В развитии патологического процесса большое значение имеет колонизационная резистентность слизистой оболочки влагалища, которая определяет устойчивость ее эпителия к колонизации условно-патогенными и патогенными микроорганизмами [1].
Триггером развития ВВК является не изменение свойств возбудителя, а снижение резистентности организма-хозяина.
Грибы рода Candida нередко участвуют в микробных ассоциациях и могут являться маркерами воспалительных заболеваний мочеполовых органов, вызванных возбудителями инфекций, передающихся половым путем.
Способ заражения и пути передачи возбудителя при кандидозном вульвовагините остаются предметом дискуссии.
Несмотря на то что партнеры могут быть носителями одного и того же штамма возбудителя, половой путь передачи заболевания в настоящее время не считается значимым. У 5-25% половых партнеров женщин с вагинальным кандидозом выявляют носительство грибов [3].
В случаях хронического, рецидивирующего заболевания женщин следует исследовать половые органы и сперму их партнеров. При обнаружении грибов, а чаще это те же виды, что и у женщины, следует провести лечение независимо от клинического состояния партнера.
Стоит отметить основные факторы защиты макроорганизма, препятствующие развитию ВВК, такие как нормальный состав микрофлоры влагалища, местные противогрибковые и противомикробные факторы, синтезируемые слизистой влагалища и иммунная система, причем основная роль антител заключается в блокировании Candida-рецепторов и литических ферментов возбудителя. Необходимо помнить о собственных механизмах грибов рода Candida: смена фаз роста, возможность существования при разной температуре и РН среды, структура их клеточной стенки, которая позволяет избежать многих противогрибковых факторов, протеиназы и каталаза грибов противостоят фунгицидным факторам макрофагов и системы перекиси водорода [13].
В настоящее время выделяют три формы кандидозной инфекции [4]:
- грибы рода Candida могут быть выделены из влагалища практически здоровых женщин при отсутствии клинических признаков ВВК, что подразумевает носительство;
- острый кандидозный вульвовагинит: длительность заболевания не превышает 2 мес. В клинической картине преобладают выраженные признаки местного воспаления вульвы и влагалища (гиперемия, отек, творожистые серо-белые выделения, зуд и жжение);
- хронический (рецидивирующий) кандидозный вульвовагинит: длительность заболевания составляет более 2 мес., при этом на слизистых оболочках вульвы и влагалища выражены инфильтрация, лихенизация и атрофия. Нередко в патологический процесс вовлекается мочевая система с развитием клинических проявлений цистита и уретрита.
Нозологическая дифференцировка целесообразна с точки зрения выбора рациональной этиотропной терапии [10].
Для диагностики ВВК используется микроскопическое исследование, позволяющее определить наличие гриба, его спор, мицелия, количество лейкоцитов, облигатно анаэробных бактерий и лактобацилл. Для видовой идентификации гриба обязательно культуральное исследование.
В связи с выраженной тенденцией к распространению ВВК особую важность приобретает проблема его лечения. Причем значительные трудности возникают при лечении рецидивирующей формы кандидозной инфекции. Проблемы этиотропной терапии ВВК зависят от особенностей возбудителей, от неспособности некоторых препаратов обеспечить полную эрадикацию Candida spp. во влагалище [9]. Это наблюдается при наличии устойчивости к противомикробной терапии, чаще для системных антимикотиков, и неконтролируемой концентрации местных противогрибковых препаратов с большой дозировкой и очень коротким курсом лечения.
Часто болезнь протекает длительно и без желаемого эффекта от проводимой терапии. Одной из причин этого является необоснованное использование лекарственных средств, так как часто пациентки занимаются самолечением. После завершения курса лечения, несмотря на отрицательные результаты культурального исследования, эрадикация микроорганизма может быть неполной, что может привести к развитию рецидивов.
Вопросы лечения ВВК представляют собой большие трудности. Одновременно с антимикотической терапией необходимо проводить коррекцию состояний, приводящих к развитию ВВК [10]. Согласно клиническим рекомендациям, при назначении лечения, необходимо, во-первых, достигнуть элиминации возбудителя, во-вторых, устранить факторы, поддерживающие рецидивирующий характер заболевания, и, в-третьих, проводить лечение сопутствующих заболеваний, утяжеляющих урогенитальный кандидоз.
Выделяют следующие этапы развития инфекционного процесса при проникновении в организм грибов рода Candida:
- прикрепление (адгезия) грибов к поверхности слизистой оболочки и ее колонизация;
- внедрение (инвазия) в эпителий;
- преодоление эпителиального барьера слизистой оболочки, проникновение в соединительную ткань собственной пластинки;
- преодоление тканевых и клеточных защитных механизмов;
- проникновение в сосуды;
- гематогенная диссеминация с поражением различных органов и систем.
При ВВК инфекционный процесс затрагивает чаще только поверхностные слои эпителия влагалища; если макроорганизм полностью не способен элиминировать возбудитель, инфекция персистирует десятки лет [10]. Также на поверхности слизистой оболочки влагалища грибы рода Candida вступают во взаимодействие с различными представителями микрофлоры. Бактерии в большинстве случаев тормозят рост грибов и их прикрепление к эпителиоцитам влагалища за счет секреции антифунгальных веществ и конкуренции за рецепторы на эпителиоцитах влагалища. Огромную роль играют лактобациллы: они вырабатывают вещества, тормозящие рост грибов и их прикрепление к эпителиоцитам влагалища.
Применение местных препаратов патогенетически обосновано, так как они наиболее безопасны, высокоэффективны, имеют широкий спектр действия и несклонны к формированию устойчивости.
С появлением новых препаратов разрабатываются новые схемы лечения ВВК, особенно его хронической, рецидивирующей формы. Так как причинами рецидивирующего ВВК чаще являются изменения в локальном и клеточном иммунитете на уровне слизистой влагалища [10], целесообразно применение местных препаратов с курсом лечения не менее 5-7 дней.
При лечении ВВК используют как системные, так и интравагинальные антимикотические средства, сопоставимые по эффективности [1, 2, 9-11).
Лекарственное средство должно удовлетворять ряду требований:
- обладать высокой эффективностью;
- безопасностью;
- удобством в применении;
- оптимальным соотношением "цена-качество".
Лечение показано при наличии клинической картины заболевания, подтвержденной микроскопически и/или культурально. Вопрос о необходимости фармакотерапии при бессимптомном носительстве в настоящее время до конца не решен. Перед предстоящими диагностическими вмешательствами возможно назначение противогрибковых лекарственных средств [1, 7].
Адгезии грибов Candida к эпителию влагалища способствует, в частности, уменьшение резидентной микрофлоры влагалища и изменение рН вагинального секрета. Характерным отличием кандидозной инфекции от кандидоносительства является инвазия дрожжеподобных грибов в эпителиальную клетку, обуславливающая развитие тканевой реакции [8]. Санация влагалища при вагинитах может быть достигнута с помощью местно-действующих препаратов, обладающих активностью в отношении дрожжеподобных грибов.
Результаты нескольких клинических исследованиях свидетельствуют о том, что интравагинальный путь введения антимикотических препаратов остается востребованным практикующими врачами и пациентками и обладает рядом преимуществ (возможность создания высокой концентрации действующего вещества при его минимальной системной абсорбции, что позволяет избежать нежелательные явления и лекарственные взаимодействия) [11].
Необходимо помнить, что проводя системное лечение ВВК во время и/или после антибиотикотерапии, мы повышаем нагрузку на органы элиминации. При случайном (чаще самостоятельном) лечении, при неуточненной беременности местные препараты менее опасны.
Для лечения ВВК в настоящее время используются полиеновые антибиотики, производные имидазола, триазолы. Препараты с фунгицидным действием (чаще ими являются лекарственные средства местного действия) оказывают непосредственное повреждающее воздействие на клетку гриба. Фунгистатическое действие - нарушение синтеза разных компонентов мембраны клетки гриба и ингибирование роста клетки - характерно для системной терапии.
В связи с этим целесообразно использовать лекарственное средство, обладающее и фунгистатическим и фунгицидным эффектом. Таким препаратом из группы азолов является кетоконазол - синтетическое диоксолановое производное имидазола. Нарушение синтеза мембраны лежит в основе фунгистатического действия этого препарата. При очень высоких концентрациях препарата, достигаемых только при местном применении, тяжелые повреждения мембраны дают фунгицидный эффект.
Другим механизмом действия кетоконазола является угнетение тканевого дыхания на уровне цитохром С оксидазы. Причем нарушенная деятельность мембранных ферментов приводит к подавлению синтеза хитина клеточной стенки.
Кетоконазол в виде таблеток проявляет преимущественно фунгистатический эффект, но в местных формах (кремы, вагинальные суппозитории) его концентрации (1-2%) достаточны для развития фунгицидного действия.
В состав вагинальных суппозиториев "Ливарол", помимо кетоконазола, входит полиэтиленоксидная основа, которая способствует увлажнению слизистых оболочек и улучшает взаимодействие активного компонента препарата с вагинальными эпителиоцитами.
Кетоконазол в виде вагинальных суппозиториев "Ливарол" назначается по 1 суппозиторию (400 мг) в сутки в течение 5 дней при остром ВВК, при хроническом ВВК предлагается удвоенная дозировка (по 1 суппозиторию - 400 мг - 2 раза в день) в течении 7 дней и последующая интермиттирующая превентивная терапия по 1 суппозиторию (400 мг) в сутки 5 дней перед менструациями в течение 6 мес. [9].
Результаты проведенных клинических исследований препарата "Ливарол" [9, 11, 12], свидетельствуют о высоком уровне чувствительности к нему микрофлоры пациенток с ВВК и его безопасности, так как не выявлено ни одного случая непереносимости препарата или возникновения нежелательных явлений при его применении.
Учитывая данные клинических исследований, подтвердившие высокий антимикотический эффект препарата, в связи с достаточно равномерно распределенной концентрацией лекарственного средства, его безопасностью, удобством применения, отсутствием побочных явлений и системного воздействия, "Ливарол" рекомендуется для широкого использования в практике акушеров-гинекологов.
Выбор лекарственного препарата в каждом конкретном случае должен зависеть от тяжести клинического течения заболевания, наличия микстинфекции и сопутствующих заболеваний. Только комплексный подход к данной проблеме позволит повысить эффективность лечения ВВК, снизить процент и частоту рецидивирования.
ЛИТЕРАТУРА
1. Серов В.Н. Рациональная терапия влагалищной инфекции. Гинекология, 2005; 2 (7).
2. Ткаченко Л.В., Жукова С.И. Преимущества комбинированной терапии хронического рецидивирующего кандидозного вульвовагинита. Гинекология, 2006; 2 (7).
3. Jack D. Sobel Epidemiology and pathogenesis of recur-rent vulvovaginal candidiasis. Am J Obst Gynecolol 1995.
4. Прилепская В.Н., Анкирская А.С., Байрамова Г.Р., Муравьева ВВ. Вагинальный кандидоз. М., 1997.
5. Романовская ТА. Современная практика и вопросы стандартизации терапии кандидозного вульвовагинита. Гинекология, 2004; 1.
6. Kent HL. Epidemiology of vaginitis. Am J Obstet Gynecol 1999; 165: 1168-75.
7. Рациональная фармакотерапия в акушерстве и гинекологии, 2005.
8. Кисина ВИ. Комбинированная терапия смешанных инфекций влагалища. Consilium Medicum 2005; 7 (5).
9. Романовская Т.А., Сергеев ЮВ. Хронический вагинальный кандидоз: новые возможности терапии. Иммунопатол., аллергол., инфектол. 2005; 1.
10. Тихомиров АЛ. Варианты терапии острого и хронического кандидозного вульвовагинита. Гинекология. 2005; 3 (7).
11. Мирзаболаева А.К., Долго-Сабурова Ю.В., Колб ЗК и др. Опыт применения вагинальных суппозиториев "Ливарол" у больных ОКВВ. Гинекология. 2006; 2 (8).
12. Байрамова Г.Р ВВК. Рациональная фармакотерапия. Гинекология. Экстравыпуск. 2006.
13. Хамаганова И.В. Кандидозный вульвовагинит. Леч. врач. 2007; 3: 50-3.
14. Савичева АМ. Диагностика и лечение урогени-тального кандидоза Трудн. пациент. 2006; 9 (4): 28-33.
15. Прилепская ВН., Байрамова ГР. Вульвовагиналь-ный кандидоз - современные пути решения проблемы. Трудн. пациент. 2006; 9 (4): 33-7.
16. Тихомиров АЛ. Основные принципы лечения кандидозного вульвовагинита. Consilium Medicum 2006; 6 (8): 58-62.
Молочница после приема антибиотиков у женщин
Антибиотики давно стали привычным для нас способом лечения многих сложных заболеваний. Ангины, отиты, воспаления и многое другое легко поддается лечению с их помощью. Однако неправильная дозировка, длительный курс лечения и самолечение могут привести к неожиданным последствиям в виде осложнений. С точки зрения женского здоровья одним из самых частых осложнений становится развитие вагинального кандидоза после приема антибиотиков. Важно знать, почему это происходит, можно ли избежать появления молочницы после антибиотиков и как лечить данное заболевание.
Признаки кандидоза и его причины
Вагинальный кандидоз, или, проще говоря, молочница, — заболевание, с которым рано или поздно сталкиваются многие девушки и женщины. Его неприятные симптомы знакомы многим: зуд, жжение, покраснение и отек половых органов, боль и дискомфорт, обильные белые выделения — мало кому захочется вновь пережить эти ощущения. Появление болезни может происходить в совершенно различных ситуациях, что вызывает множество вопросов. Самые распространенные из них — это какова же причина возникновения молочницы, какие дополнительные факторы могут ухудшить ситуацию, как осуществить грамотное лечение и какие меры профилактики предпринять в дальнейшем при приеме антибиотиков.
Причиной появления молочницы считается массовое размножение грибка рода Кандида на слизистой влагалища, огромные колонии грибка нарушают правильную и естественную микрофлору, вследствие чего и проявляются многочисленные симптомы болезни. Как ни странно, но этот грибок не является инородным для нашей слизистой. В нормальном организме любой женщины дрожжеподобные грибки присутствуют как один из множества представителей условно-патогенной микрофлоры слизистой, но их размножение сдерживается тем, что преобладающими являются не патогенные бактерии.
Антибиотики и флора организма
Как связан прием антибиотиков и размножение условно-патогенной флоры на слизистой? Механизм воздействия антибиотиков заключается в том, что они подавляют рост и размножение всех бактерий и грибов, не разбираясь, полезные они для нас или нет. Не стоит забывать, что антибиотики оказывают не локальное, а комплексное влияние на наш организм. В итоге иммунитет человека становится угнетенным, так как теряет своих помощников в лице здоровой микрофлоры и не может дать адекватный иммунный ответ новому заболеванию. Это осложняется и тем, что условно-патогенная флора очень быстро становится резистентной к лекарственным препаратам и лечение существенно осложняется. После курса антибиотиков может возникнуть целый ряд осложнений: проблемы с желудочно-кишечным трактом, кожные реакции и аллергии.
Женские проблемы и их решение
У женщин на фоне сниженного иммунитета и длительного курса сильных антибиотиков нередко может появиться вагинальный кандидоз. Распознать его не составляет труда, поскольку симптомы кандидоза остаются такими же: постоянный зуд и жжение в области половых органов, неприятные болевые ощущения во время интимной близости, обильные творожистые выделения из влагалища, часто с кислым кефирным запахом. Как только эти признаки появились — скорее всего, у вас началась молочница и необходимо сразу начинать лечение.
Чем лечить молочницу после антибиотиков? Кардинально методы лечения молочницы разного происхождения (будь то следствие приема антибиотиков, угнетение иммунитета или другая причина) не отличаются. Важно обратиться к врачу, который назначит подходящее вам лечение: это могут быть как таблетки, так и свечи или крем, в том числе Ломексин — эффективный препарат на основе фентиконазола. Заниматься самолечением, как и в случае антибиотиков, и увлекаться разнообразными народными советами и средствами не стоит — вы можете не достичь желаемого результата, а болезнь перейдет в более глубокую хроническую форму, лечить которую сложнее и дороже, чем острую форму молочницы.
Заботиться о здоровье
Помимо лекарственной терапии, необходимо предпринять меры по укреплению иммунитета организма в целом и восстановления нормальной микрофлоры слизистых. В первую очередь — это нормализация режима дня и питания. Ваш сон должен быть полноценным, достаточным для восстановления сил. В еде придерживайтесь умеренности, постарайтесь исключить лишний сахар — пончики, пирожные и лишняя шоколадка принесут больше проблем, чем удовольствия. Отдавайте предпочтение сезонным фруктам и овощам и дополнительно принимайте поддерживающие иммунитет природные витамины и добавки.
Стоит также уделить особое внимание личной гигиене. Откажитесь от тесного и полностью синтетического белья — это вызывает лишний дискомфорт и может спровоцировать возникновение заболеваний нижнего отдела женских половых путей. Интимная гигиена помогает поддерживать флору половых органов в нормальном состоянии, не забывайте принимать душ регулярно, желательно с использованием средств, специально разработанных для интимной гигиены — их кислотно-щелочной баланс не нанесет вреда слизистым.
Молочница, вызванная антибиотиками, хорошо поддается лечению, так же как и вызванная другими причинами. Важно сразу распознать ее симптомы и начать грамотное лечение под наблюдением врача, а в дальнейшем уделить максимум внимания и заботы вашему организму — ему потребуется ваша помощь, чтобы полностью восстановить силы.
Вагинальный кандидоз (молочница) - симптомы и лечение
Что такое вагинальный кандидоз (молочница)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Сосниной Анастасии Сергеевны, гинеколога со стажем в 15 лет.
Над статьей доктора Сосниной Анастасии Сергеевны работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Вагинальный кандидоз (кандидозный вагинит) — поражение слизистой оболочки влагалища дрожжеподобными грибами рода Candida. В быту эту болезнь называют молочницей .
Краткое содержание статьи — в видео:
Candida — это условно-патогенные микроорганизмы, факультативные анаэробы (организмы, способные жить как в присутствии кислорода, так и без него). Они обладают тропизмом — направлением роста на клетки богатые гликогеном, в частности клетки слизистой оболочки влагалища. Самый распространённый вид возбудителя, который встречается в 70—90 % случаев, — Candida albicans.
В последние годы растёт заболеваемость кандидозом, вызванным другими представителями рода Candida. Наиболее часто выявляются:
- С. glabrata (15 %);
- C. dubliniensis (6 %);
- C. tropicalis (3—5 %);
- C. parapsilosis (3 %);
- C. krucei (1—3 %).
Распространение новых видов микроорганизмов связано в первую очередь с бесконтрольным самолечением пациенток, приводящем к возрастающей устойчивости грибов к препаратам [3] [4] .
Частота кандидозного вагинита среди инфекционных заболеваний влагалища и вульвы составляет 30—45 %. Патология занимает второе место среди всех инфекционных заболеваний влагалища и является крайне распространённым поводом для обращения женщин за медицинской помощью. По данным J. S. Bingham (1999):
- к 25 годам около 50 % женщин репродуктивного возраста сталкивались с хотя бы одним диагностированным врачом эпизодом вагинального кандидоза;
- к началу периода менопаузы — около 75 % [17] .
Кандидозный вагинит редко наблюдается в постменопаузе, за исключением тех пациенток, которые получают гормональную заместительную терапию.
Предрасполагающими факторами заболевания являются:
- Механические — ношение синтетического белья, первый половой контакт, травматическое повреждение тканей влагалища, длительное применение внутриматочной спирали.
- Физиологические — беременность, менструация.
- Эндокринные — гипотиреоз, сахарный диабет.
- Иммунодефицитные состояния.
- Ятрогенные (приём антибиотиков, кортикостероидов, иммуносупрессоров, лучевая терапия, химиотерапия, онкологические заболевания, оральные контрацептивы).
- Прочие (авитаминоз, аллергические заболевания, хронические патологии гениталий и желудочно-кишечного тракта).
Заболевание, как правило, не передаётся половым путём, но установлено, что оно связано с характером половых контактов: анально-вагинальным и орогенитальным. Также не исключается вероятность развития кандидозного баланопостита у половых партнёров пациенток с вагинальным кандидозом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вагинального кандидоза
Основные симптомы при вагинальном кандидозе:
- жжение и зуд в области влагалища и вульвы;
- творожистые выделения из влагалища;
- расстройства мочеиспускания;
- боль при половом акте.
Зуд может усиливаться после водных процедур, полового акта, ночью во время сна и в период менструации [1] .
В целом симптомы вагинального кандидоза нарастают перед менструацией. При беременности проявление болезни также усугубляется, это связано со снижением иммунитета у беременных женщин.
Объективные признаки вагинального кандидоза:
- отёк и гипермия слизистой оболочки влагалища и наружных половых органов;
- белые или зеленовато-белые наложения на стенках влагалища;
- покраснение слизистой влагалища.
При осложнённом кандидозе на коже наружных половых органов появляются везикулы — пузырьки, возвышающиеся над уровнем кожи или слизистой и заполненные прозрачным или мутным содержимым, которые могут вскрываться и образовывать эрозии. При вагинальном кандидозе также могут наблюдаться трещины слизистой вульвы, задней спайки и перианальной области [2] .
Патогенез вагинального кандидоза
Грибы рода Candida относятся к условно-патогенной микрофлоре, которая присутствует как в окружающей среде, так и на поверхности кожных покровов и слизистых оболочках здорового человека (в полости рта, кишечнике, влагалище). При снижении защитных сил организма возможно повышение адгезивных свойств (способности прилипать) грибов с прикреплением их к клеткам эпителия влагалища, колонизацией слизистой оболочки и развитием воспалительной реакции [7] .
Вагинальный кандидоз зачастую затрагивает только поверхностные слои эпителия влагалища без проникновения возбудителя в более глубокие слои слизистой оболочки. Однако в редких случаях эпителиальный барьер преодолевается и происходит инвазия в подлежащую ткань с последующей гематогенной диссеминацией (распространением возбудителя инфекции из первичного очага заболевания по всему органу или организму посредством кровотока) [8] [9] .
Основные этапы патогенеза:
- Адгезия (прилипание) грибов на слизистой и колонизация.
- Инвазия (проникновение) в эпителий.
- Преодоление эпителиального барьера.
- Проникновение в соединительную ткань.
- Преодоление защитных механизмов ткани.
- Попадание в сосуды.
- Гематогенная диссеминация.
При вагинальном кандидозе воспаление происходит в верхних слоях эпителия влагалища. Причина состоит в том, что поддерживается динамическое равновесие между грибом, который не может проникнуть в более глубокие слои, и организмом, который сдерживает его распространение. Соответственно инфекция может долго развиваться в одном месте, проявляясь творожистыми выделениями из влагалища. Обострение заболевания происходит при сдвиге равновесия между развитием грибов и защитными силами организма.
Классификация и стадии развития вагинального кандидоза
Согласно национальным клиническим рекомендациям [18] , выделяют две формы вагинального кандидоза:
- острую — до трёх обострений в год;
- хроническую (рецидивирующую) — не менее четырёх обострений в год.
По классификации, предложенной D.A. Eschenbach, вагинальный кандидоз подразделяют на два типа:
У женщин различают три формы заболевания:
- вагинит (воспаление влагалища); (воспаление влагалища и вульвы); (воспаление шейки матки).
У мужчин выделяют:
- баланит (воспаление головки полового члена);
- баланопостит (воспаление крайней плоти и головки полового члена); (воспаление мочеиспускательного канала).
Для острой формы вагинального кандидоза характерны выраженные симптомы: обильные выделения из влагалища, жжение и зуд во влагалище и наружных половых органах. На фоне таких симптомов нередко снижается трудоспособность пациентки и развиваются неврозы. Острая форма вагинального кандидоза встречается наиболее часто и формируется в результате увеличения количества грибов рода Candida во влагалище на фоне снижения иммунитета пациентки.
Рецидивирующий вагинальный кандидоз — встречается у 10—15 % женщин репродуктивного возраста и проявляется четырьмя и более обострениями за год [11] .
Неосложнённая форма заболевания предполагает впервые выявленный или возникающий менее четырёх раз в год вагинальный кандидоз с умеренными проявлениями вагинита у пациенток без сопутствующих факторов риска (сахарный диабет, приём глюкокортикоидов, цитостатиков и др.).
При осложнённом вагинальном кандидозе наблюдаются яркие объективные симптомы: покраснение, отёк, образование язв, трещин слизистых оболочек и кожи перианальной области. Также характерны рецидивы четыре и более раз в год. Заболевание часто возникает на фоне сахарного диабета, ВИЧ-инфекции, терапии глюкокортикоидами и цитостатиками. Возбудителем заболевания в данном случае являются как C. albicans, так и другие грибы рода Candida.
Осложнения вагинального кандидоза
К осложнениям вагинального кандидоза у женщин относятся:
- стеноз влагалища;
- воспалительные патологии органов малого таза — сальпингит, оофорит и другие;
- заболевания мочевыделительной системы — цистит, уретрит[2] .
Стеноз влагалища развивается при воспалении стенок влагалища. При этом просвет влагалища сужается, а стенки влагалища становятся плохо растяжимы. Пациентки испытывают боль при половом акте.
Сальпингит — инфекционно-воспалительное заболевание фаллопиевой (маточной) трубы. Возникает при переходе инфекции восходящим путем из влагалища, не исключен также и гематогенный путь передачи. Сальпингит чаще всего протекает в сочетании с оофоритом — воспалением яичника. Поражение может быть как односторонним, так и двусторонним. Пациентки испытывают боль в области придатков, внизу живота слева или справа, повышается температура тела, возникает общее недомогание, слабость, а иногда и тошнота со рвотой. При несвоевременном лечении данного осложнения высок риск бесплодия, наступления внематочной беременности, возникновения спаечного процесса, приводящего к оперативному вмешательству, инфицированию органов брюшины и малого таза. Сальпингит особенно опасен в случаях, когда с кандидозом сочетаются другие инфекции [1] .
Уретрит — воспаление слизистой мочеиспускательного канала. Проявляется болезненным мочеиспусканием, чувством жжения в области уретры, выделением с мочой крови или гноя, дискомфортом при соприкосновении с бельём, слипанием краёв уретры, покраснением области вокруг мочеиспускательного канала.
Цистит — воспаление мочевого пузыря. Патология возникает при попадании возбудителя восходящим путём через уретру в мочевой пузырь. Симптомы цистита схожи с симптомами уретрита, однако есть некоторые отличия: частые позывы к мочеиспусканию при небольшом количестве мочи, чувство неполного опорожнения мочевого пузыря, боль, резь в конце мочеиспускания, помутнение мочи, повышение температуры тела, боли внизу живота.
На фоне вагинального кандидоза возрастает частота осложнений при беременности, а также увеличивается риск инфицирования плода.
Кандидоз плода может вызвать его внутриутробную гибель или приводить к преждевременным родам. После родов у женщин возможно развитие кандидозного эндометрита — воспалительного процесса в тканях, выстилающих внутреннюю полость матки.
Диагностика вагинального кандидоза
Диагностика вагинального кандидоза основывается на характерных жалобах пациентки, данных анамнеза, клинических проявлениях, выявленных при гинекологическом осмотре. В зеркалах видна гиперемия, отёк слизистой, белые налёты на стенках влагалища.
Независимо от этих признаков, подтверждение диагноза должно основываться на лабораторных данных:
- Микроскопия мазков вагинального отделяемого — позволяет выявить споры и мицелий гриба.
- Культуральный метод — посев влагалищного содержимого на искусственные питательные среды. Метод определяет количество, видовую принадлежность, чувствительность к противогрибковым препаратам, а также характер и степень заселения другими микроорганизмами. Культуральный метод дополняет микроскопию.
- Серологическая диагностика (РСК). Определяет антитела против антигенов грибов рода Candida. Такая диагностика имеет значение при генерализации процесса.
- Молекулярно-биологические методы. Направлены на обнаружение специфических фрагментов ДНК Candida spp. Применяют метод полимеразной цепной реакции (ПЦР).
- Иммунофлюоресцентная диагностика (Candida Sure Test) проводится в случае рецидивирующего течения вагинального кандидоза [15] .
К дополнительным методам диагностики относятся: изучение микробиоценоза кишечника, обследование на инфекции, передаваемые половым путём, внутривенный тест на толерантность к глюкозе [16] .
Дифференциальную диагностику проводят со следующими заболеваниями:
- генитальным герпесом; ;
- аэробным вагинитом;
- кожными заболеваниями (экземой, красным плоским лишаём, склеродермией, болезнью Бехчета и др.).
Лечение вагинального кандидоза
Показаниями к назначению терапии вагинального кандидоза являются жалобы пациентки, клинические проявления и лабораторное подтверждение наличия грибов рода Candida. Лечение не требуется при обнаружении грибов без каких-либо клинических проявлений (кандидозоносительство). Это правило обусловлено тем, что грибы рода Candida могут содержаться в небольшом количестве во влагалище и являются частью нормальной микрофлоры, если их количество не превышает пороговое значение 10 4 .
Механизм действия противогрибковых препаратов — нарушение синтеза эргостерола (вещества в составе клеточных мембран грибов), что приводит к образованию дефектов в мембране микроорганизма. В зависимости от дозы антимикотики проявляют фунгистатическое (замедление роста) или фунгицидное (полное уничтожение) действие [15] .
Существуют различные группы препаратов для лечения вагинального кандидоза:
- антибиотики (пимафуцин, амфотерицин В, нистатин, леворин);
- имидазолы (клотримазол, сертаконазол, кетоконазол, гино-певарил, миконазол);
- триазолы (итраконазол, флуконазол);
- комбинированные препараты ("Тержинан", "Полижинакс", "Пимафукорт", "Клион Д", "Макмирор комплекс");
- препараты разных групп (флуцитозин, гризеофульвин, дафнеджин, нитрофунгин, йодат поливинилпирролидон).
Лечение подбирается гинекологом индивидуально для каждой пациентки, учитывая клиническую картину, форму заболевания и степень выраженности симптомов. Но важно отметить, что при лечении молочницы при беременности флуконазол противопоказан, так как он может негативно повлиять на развитие плода [19] [20] .
При лечении острых форм вагинального кандидоза назначают местное лечение. Препарат не всасывается в системный кровоток, а действует в области влагалища и слизистой. Примеры схем лечения:
- 150 мг в виде вагинальных свечей один раз в сутки в течение трёх дней; один аппликатор крема на ночь вагинально в течение трёх дней; одна свеча на ночь один раз в сутки в течение восьми дней; одна таблетка на ночь в течение 10 дней.
При хроническом кандидозе наряду с местным лечением применяют системные антимикотики:
- 150 мг один раз внутрь; 200 мг внутрь два раза с интервалом 12 часов в течение одного дня или 200 мг в сутки в течение трёх дней.
- Операция Бокштейн на ухе. Техника операции Бокштейн
- Полнота нозогнозии. Согласие на лечение как уступка окружающим
- Прогрессирующий семейный внутрипеченочный холестаз (ПСВХ)
- Больные шизофренией в семье. Влияние семьи на больных шизофренией
- Синдромы Шая-Дрейджера, Хорнера. Физиология двигательной нервной системы
При рецидивирующей форме заболевания (более четырёх эпизодов в год) применяют схему:
- 150 мг внутрь три раза с интервалом 72 часа в 1,4 и 7 день лечения.
Для купирования рецидивов препарат применяют в дозировке 150 мг один раз в неделю в течение шести месяцев.
В последние годы всё больше исследуется способность C. albicans формировать биоплёнки — вещества на поверхности колонии микроорганизмов, которые служат барьером для проникновения лекарственных средств и обеспечивают выживание. Основным полисахаридом, определяющим развитие резистентности к антибиотикам, является глюкан. Его рассматривают как одну из причин формирования резистентности к антимикотическим препаратам. Этим объясняется отсутствие эффекта при лечении у некоторых больных. Таким пациенткам можно порекомендовать препарат фентиконазол 600 мг в сутки с интервалом в три дня. Лекарство отличается от других способностью преодолевать биоплёнки, тем самым повышая эффективность лечения при резистентности к другим препаратам.
Прогноз. Профилактика
При своевременном обращении пациентки к врачу, лабораторном обследовании и отсутствии самолечения прогноз благоприятный. Самолечение опасно из-за риска рецидива заболевания, его хронизации и возникновения резистентности к препарату, неверно выбранному пациенткой или при неадекватной дозе.
Чтобы повысить эффективность терапии пациентки должны следовать схеме лечения, индивидуально назначенной гинекологом. Во время лечения и диспансерного наблюдения необходимо соблюдать половой покой или применять барьерные методы контрацепции. Повторно обратиться к врачу для контроля анализов следует через 7-10 дней [12] .
Читайте также:
