История лечения вестибулярного головокружения
Добавил пользователь Евгений Кузнецов Обновлено: 08.01.2026
В последнее время интерес к проблемам головокружения и расстройства равновесия значительно возрос. Это связано не только с ростом числа пациентов, обращающихся к врачу с подобными жалобами, но и с появлением
В последнее время интерес к проблемам головокружения и расстройства равновесия значительно возрос. Это связано не только с ростом числа пациентов, обращающихся к врачу с подобными жалобами, но и с появлением новых методов диагностики, созданием как специфических фармакологических препаратов, так и методов реабилитационной терапии. Для врача по-прежнему очень важно точно установить причину развития заболевания и его формы с целью дальнейшего назначения адекватной терапии. На основании опыта работы, накопленного в течение пяти лет в специализированном центре по головокружению и расстройствам равновесия, мы сделали вывод, что у более чем у 50% пациентов на момент обращения появление подобных симптомов обусловливается целым комплексом причин. Это объясняется сложным строением системы равновесия и вестибулярной системы.
Для практикующего врача важно детально ознакомиться с жалобами, предъявляемыми пациентом, и анамнезом развития заболевания. Использование дополнительных современных методов диагностики и консультации у специалистов значительно повышают эффективность диагностики. Прежде всего, из дополнительных методов диагностики следует отметить вестибулометрию и постурографию (возможно, стабилометрию). Если первый метод, представляющий собой комплекс тестов с компьютерной обработкой данных, позволяет ответить на вопросы о функциональном состоянии вестибулярной системы, в том числе об изменениях в вестибулярном рецепторе, центральных вестибулярных структурах, стволе мозга, мозжечке; состоянии глазодвигательной системы; шейных рецепторов и др., то постурография дает возможность оценить состояние равновесия (функциональный состав компонентов — зрения, вестибулярной системы, проприорецепторов), в том числе и для индивидуального подбора и проведения реабилитационной терапии. Ультразвуковое дуплексное исследование магистрального кровотока транскраниального и шейного отделов позволяет кроме обычных процедур проводить исследования с функциональными пробами и получать информацию о венозном кровотоке. В сочетании с поворотными столами этот метод дает возможность получить информацию о повышении внутричерепного давления.
В практике мы сталкиваемся с вестибулярной патологией, которая может быть условно разделена на периферический, центральный и смешанный вестибулярные синдромы. Выбор лечащего врача при существующей системе оказания специализированной помощи чаще всего происходит следующим образом. Если у пациента имеется кохлеовестибулярный синдром, то он направляется к врачу сурдологу; вестибулярный синдром без изменений слуха — к неврологу. На наш взгляд, на первом этапе обследования обязательны консультации у невролога и отоневролога (оториноларинголога), так как периферический вестибулярный синдром без аудиологических симптомов может быть причиной развития заболеваний внутреннего уха, на которых следует остановиться подробнее.
Группу заболеваний внутреннего уха без изменений слуха составляют: доброкачественное пароксизмальное позиционное головокружение (отолитиаз), вестибулярный нейронит, фистула лабиринта, вестибулярная форма болезни Меньера и вторичный гидропс лабиринта.
Доброкачественное пароксизмальное позиционное головокружение (ДППГ) — одна из часто встречающихся причин головокружения, связанных с патологией внутреннего уха. У больных с этой патологией развиваются кратковременные приступы головокружения и нистагма (обычно длящиеся менее 30 с) при изменении положения тела и головы: обычно при повороте в кровати, укладывании и вставании с кровати, сгибании и выпрямлении или вытягивании шеи, чтобы посмотреть вверх.
Основные признаки ДППГ и связанного позиционного нистагма были описаны Робертом Барани (Barany, 1921), но такого термина не существовало до 1952 г., когда Дикс и Холлпайк описали провоцирующий позиционный тест и четко определили синдром (Dix и Hallpike, 1952).
Диагноз ДППГ по-прежнему основывается на обнаружении характерного нистагма положения (который называется также как пароксизмальный позиционный нистагм) у больного с типичным анамнезом позиционного головокружения. Нистагм может наблюдаться при визуальном осмотре в пробе Дикса-Холлпайка, однако так как он возникает вследствие патологии вестибулярного рецептора (т. е. является периферическим), то подвержен угнетению при фиксации взора, поэтому диагностика предполагает применение очков Френзеля или видеонистагмографии. В настоящее время нами накоплен опыт терапии более чем 100 пациентов с подобной патологией. Лечение позволяет перемещать частицы из полукружных каналов в преддверие лабиринта и таким образом купировать головокружение. Эффективность процедур, согласно нашим и зарубежным источникам, колеблется в пределах 90—95%.
Острый вестибулярный нейронит
Это заболевание с пока еще неизвестной этиологией. Наиболее популярна гипотеза о вирусной этиологии. Для него характерны приступы вестибулярного головокружения, часто сопровождающиеся вегетативными реакциями (тошнотой и рвотой). Любые движения головой усиливают ощущение головокружения. Длительность заболевания колеблется от нескольких часов до нескольких суток. Важным признаком является отсутствие, как и при всех заболеваниях этой группы, изменений слуха. При проведении обследования можно наблюдать на фоне асимметричного поражения типичный вестибулярный периферический нистагм, который будет сочетаться с соответствующим отклонением рук и позы при выполнении статокинетических проб. Лечение, как правило, симптоматическое с применением вестибулярных супрессантов на первом этапе. Отдельно следует упомянуть токсический нейронит, вызванный воздействием аминогликозидных антибиотиков, особенно если речь идет о гентамицине. Введение гентамицина, одно—двухкратное, через барабанную перепонку, по своей эффективности с успехом заменяет операцию по разрушению лабиринта (если таковую необходимо выполнить при абсолютной неэффективности других методов лечения).
Не меньшие сложности в диагностике может представлять фистула лабиринта. Это заболевание характеризуется появлением сообщающегося отверстия или канала между средним и внутренним ухом, вследствие чего происходит истечение жидкости из внутреннего уха в полость среднего. Нарушается система гидродинамики, а затем и состояние сенсорных клеток. Чаще всего фистула формируется при баротравме (например, при нырянии, кашле, чихании). Характерный признак — это появление головокружения при пробе Вальсальвы (или аналогичных нагрузках — натуживании или поднятии тяжестей). Фистулы имеют тенденцию к самостоятельному закрытию, однако вследствие часто образующегося повышенного внутрилабиринтного давления (гидропса) могут перейти в хроническую форму. Электрофизиологические, рентгенологические и другие методы исследований не могут дать достоверный ответ на вопрос о наличии фистулы. Поэтому после проведения обследования при определенных результатах тестов решается вопрос о диагностической миринготомии (хирургической отсепаровки барабанной перепонки для ревизии барабанной полости). При обнаружении фистулы производится ее пластика.
Вестибулярной форме болезни Меньера посвящены отдельные исследования, проводившиеся в основном за рубежом. Для типичной болезни Меньера характерны следующие признаки. Обычно заболевание начинается в возрасте 25—45 лет, чаще болеют мужчины. Заболевание сопровождается приступами вестибулярного головокружения, длительностью до 6—12 ч, шумом в ушах, флюктуирующем снижением слуха по сенсоневральному типу с тенденцией к прогрессированию степени тугоухости, ощущением дискомфорта, распирания в пораженном ухе.
Обращает внимание существование большого количества пациентов с вторичным гидропсом лабиринта. Термин «вторичный» предполагает, что увеличение внутрилабиринтного давления происходит вследствие причин, имеющих системную распространенность, и происходящее во внутреннем ухе отражает проявление этих изменений. В одном из номеров «Лечащего Врача» (№9, 2000) мы подробно останавливались на особенностях диагностики и лечения этой патологии.
Подобные изменения предполагают проведение соответствующей терапии, включающей по крайней мере два компонента: нормализацию состояния венозного оттока и терапию гидропса лабиринта. На этом этапе работа с пациентом должна также проводиться при непосредственном участии невролога-вертебролога (мануального терапевта) и отоневролога. Индивидуальное сочетание физических и физиотерапевтических методов, а также комбинированная терапия гидропса (дегидратация, вестибулярная супрессия, вазоативное воздействие на регионарный кровоток во внутреннем ухе) позволяют добиваться излечения пациента. Методом этапной оценки состояния давления во внутреннем ухе также остается электрокохлеография.
Последние исследования в области иммунологии внутреннего уха свидетельствуют, что гидропс лабиринта может быть следствием аутоиммунного поражения внутреннего уха. Морфологические изменения характеризуются: дегенерацией клеток спирального ганглия, атрофией органа Корти, артериитом вокруг кохлеарного нерва и сосудистой полоски, развитием эндолимфатического гидропса. Для вестибулярных расстройств головокружение не является постоянным признаком. Если же оно присутствует, то схоже с меньероподобными головокружениями, сочетающимися с атаксией и приступами внезапного падения. При вестибулометрическом исследовании определяется двухсторонняя симметричная периферическая вестибулярная дисфункция. В клинической картине заболевания встречаются как различные сочетания слуховых и вестибулярных симптомов, так и полное их отсутствие на фоне только внезапных падений. Для практикующего врача возможность установить причину развития патологии внутреннего уха служит указанием для назначения кортикостероидной противовоспалительной терапии.
Лечение периферического вестибулярного синдрома можно условно разделить на две стадии — активного проявления заболевания и подострого состояния. На первом этапе важно проведение патогенетической терапии в комплексе с назначением вестибулярных супрессантов и противорвотных препаратов при сочетании головокружений с вегетативными проявлениями.
В лечении головокружений основное место занимают вестибулярные супрессанты. Термин «вестибулярный супрессант» является собирательным: так обычно называют препараты, которые уменьшают нистагм и ощущение головокружения, вестибулярную неустойчивость или купируют болезнь движения (укачивание).
По крайней мере четыре основных нейромедиатора вестибулярной системы вовлечены в формирование вестибулоокулярного рефлекса: глутамат, ацетилхолин, гамма-аминомасляная кислота и глицин, гистамин.
Антихолинергические средства оказывают воздействие на мускариновые рецепторы. Важной особенностью для этой группы препаратов является то, что они не проникают через гематоэнцефалический барьер и поэтому неэффективны в лечении болезни движения. Также, в отличие от антигистаминных средств, антихолинергические препараты неэффективны, если их применять после того, как головокружение уже началось.
Все антихолинергические средства, используемые для купирования головокружения, имеют побочные эффекты: расширенние зрачков и седативный. Наиболее часто из препаратов этой группы применяются скополамин и атропин.
Имеются данные, указывающие на то, что центрально действующие антигистаминные препараты предотвращают болезнь движения и уменьшают выраженность вестибулярных проявлений, даже если симптомы уже появились. Большинство антигистаминных препаратов также обладает блокирующим эффектом кальциевых каналов. Однако седативный эффект, которым обладают антигистаминные препараты, оказывает неблагоприятное влияние на процессы вестибулярной адаптации, поэтому данную группу препаратов не следует рекомендовать пациентам для длительного применения.
Бензодиазепиновые препараты — GABA-модуляторы — действуют центрально для подавления вестибулярных реакций. Данные препараты применяются в малых дозах. Их основные недостатки — это привыкание, ухудшение памяти, повышенный риск падений и отрицательное воздействие на вестибулярную компенсацию.
Удачным сочетанием свойств патогенетического препарата с эффектом подавления ощущения головокружения характеризуется бетасерк (бетагистина дигидрохлорид). При воздействии на две группы Н-рецепторов одновременно происходят увеличение кровотока в лабиринтной артерии и супрессия информации, идущей через вестибулярные ядра. Бетасерк можно рассматривать как препарат выбора. В зависимости от патогенеза заболевания бетасерк может сочетаться с другими терапевтическими средствами (за исключением антигистаминных препаратов, сочетание с которыми приводит к ослаблению терапевтического действия обоих лекарственных средств).
Периферическая вестибулярная патология на фоне не проходящей атаксии в дальнейшем, как правило, компенсируется самостоятельно. Однако в целях скорейшего выздоровления пациента может быть использована вестибулярная реабилитация. Это комплекс упражнений, выполняемых самостоятельно или на специальных установках (постурографах или стабилографах) с биологической обратной связью. Включение вестибулярной реабилитации в комплексную терапию периферического вестибулярного синдрома, по нашему мнению, оправдано и должно выполняться под контролем врача. Рекомендуется подобные упражнения назначать после окончания применения пациентом вестибулярных супрессантов. Возможно, бетасерк является исключением, так как в последнее время в отечественной литературе появились работы, свидетельствующие об эффективности вестибулярной реабилитации при использовании бетасерка. С возрастом происходит ухудшение системы равновесия из-за изменений в структуре сенсорных систем и нервной ткани. Поэтому у пожилых людей, даже при наличии периферического вестибулярного синдрома, рекомендуется применять вестибулярную реабилитацию.
В заключение хочу подчеркнуть, что успех работы с пациентами, страдающими головокружениями и расстройствами равновесия, зависит от диагностических возможностей лечебного учреждения, взаимодействия врачей различных специальностей и использования всех средств, эффективных для лечения и реабилитации пациентов.
О. А. Мельников, кандидат медицинских наук
АНО «ГУТА-Клиник», Москва
История лечения вестибулярного головокружения
1. Поликлиника восстановительного лечения №7;
2. Кафедра неврологии и нейрохирургии Российского национального исследовательского медицинского университета им. Н.И. Пирогова;
3. Окружные неврологические отделения Москвы
Опыт лечения вестибулярного головокружения и синдрома Меньера в амбулаторных условиях
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2012;112(12): 36‑40
Костенко1 Е.В., Петрова1 Л.В., Торгованова14 Е.А., Ганжула3 П.А., Лисенкер3 Л.Н., Отческая3 О.В., Хозова3 А.А., Лебедева2 А.В., Бойко2 А.Н. Опыт лечения вестибулярного головокружения и синдрома Меньера в амбулаторных условиях. Журнал неврологии и психиатрии им. С.С. Корсакова. 2012;112(12):36‑40.
Kostenko1 EV, Petrova1 LV, Torgovanova14 EA, Ganzhula3 PA, Lisenker3 LN, Otcheskaia3 OV, Khozova3 AA, Lebedeva2 AV, Boĭko2 AN. Treatment of vestibular vertigo and Ménière syndrome in outpatient clinics. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2012;112(12):36‑40. (In Russ.).
Цель исследования - оценка клинической эффективности и переносимости препарата тагиста при симптоматическом лечении вестибулярного головокружения (вертиго) и синдрома Меньера. Наблюдали 32 больных, 16 женщин и 16 мужчин, в возрасте от 25 до 67 лет. В 17 случаях головокружение было обусловлено хронической ишемией головного мозга, в 14 оно было связано с дисциркуляцией в вертебрально-базилярной системе на фоне остеохондроза шейного отдела позвлночника, и в 1 случае был диагнотирован синдром Меньера. Препарат тагиста назначался в течение 4 нед в дозе 48 мг в сутки (по 24 мг 2 раза) в комбинации с ранее назначенной базисной медикаментозной терапией, лечебной физкультурой и стабилотренингом. Получены статистически достоверные показатели, свидетельствующие о положительном влиянии изучавшегося препарата на основные проявления заболевания (частоту, продолжительность, интенсивность приступов головокружения и др.) и его хорошей перносимости, что послужило основанием для его рекомендации к применению в неврологической практике.
Головокружение — одна из самых распространенных жалоб больных, встречающихся во врачебной практике.
У амбулаторных больных, обращающихся к врачам всех специальностей, головокружение является основной жалобой в 2—5% случаев. В последние годы отмечается значительный рост частоты (до 5—10%) этого симптома во всех развитых странах [8, 9]. Головокружение может быть как физиологической реакцией, так и проявлением патологии. Оно возникает при разных заболеваниях среднего и внутреннего уха (воспалительного и невоспалительного характера), патологии центральной нервной системы, органов шеи, в том числе при дегенеративно-дистрофических изменениях шейного отдела позвоночника, метаболических и гематологических отклонениях, приеме ряда лекарственных веществ, инфекционных поражениях, кардиогенных расстройствах и т.д. Нередко встречается сочетание нескольких причин [4, 6, 14]. Во всех случаях головокружение приводит к ухудшению качества жизни пациента, вплоть до стойкой утраты трудоспособности и инвалидности [8, 14].
Причины головокружения не всегда понятны и легко устранимы. Поэтому основное значение в терапии больных с головокружением приобретает патогенетическое и симптоматическое лечение. Накопленный клинический опыт показывает, что предлагаемые на сегодняшний день лекарственные средства для лечения больных с головокружением относятся к разным фармакологическим группам и имеют различную эффективность и переносимость. Наибольшей эффективностью при лечении головокружения обладают средства, действующие на уровне вестибулярных рецепторов или центральных вестибулярных структур [4, 16, 17].
На сегодняшний день установлено, что передача импульсации от вестибулярных рецепторов и вестибулярных ядер обеспечивается преимущественно гистаминергическими нейронами. Основным источником гистаминергической иннервации является задний гипоталамус, главным образом туберомамиллярное ядро, нейроны которого связаны практически со всеми структурами диэнцефальной области и конечного мозга, включая базальные ганглии и кору, а также со стволом и, в частности, с комплексом вестибулярных ядер. При периферических вестибулярных расстройствах наблюдается усиление спонтанной импульсации нейронов ипсилатеральных вестибулярных ядер, главным образом медиального. Одновременно отмечается снижение экспрессии рецепторов ГАМК, что ведет к преобладанию возбуждающих гистаминергических влияний. Гистаминергическая система также обеспечивает передачу возбуждения между вестибулярными ядрами и рвотным центром [15].
Поскольку важную роль в функционировании вестибулярных структур играет гистаминергическая система, в качестве базового средства лечения синдрома головокружения используется гидрохлорид бетагистина, имеющий структурное сходство с гистамином. Бетагистин реализует свое действие через центральные и периферические гистаминовые рецепторы. Центральная активность бетагистина в отношении вестибулярного аппарата способствует развитию компенсации, периферическая активность увеличивает кохлеарный кровоток [17].
Одним из препаратов бетагистина является тагиста. Это средство имеет структурное сходство с гистамином. Вследствие блокады Н3-рецепторов и стимуляции H1-рецепторов тагиста увеличивает высвобождение нейромедиаторов из нервных окончаний пресинаптической мембраны, оказывает ингибирующий эффект в отношении вестибулярных ядер ствола мозга и улучшает кровоснабжение внутреннего уха.
Цель данного исследования — оценка клинической эффективности и переносимости препарата тагиста при симптоматическом лечении вестибулярного головокружения (вертиго) и синдрома Меньера.
Материал и методы
В исследование были включены 32 пациента, 16 женщин и 16 мужчин, в возрасте от 25 до 67 лет (средний — 53,4±10,7 года) с вестибулярным головокружением и синдромом Меньера, наблюдавшихся в 5 окружных неврологических отделениях Москвы.
В исследование включались пациенты с системным постоянным или приступообразным головокружением установленной этиологии; с частыми (не реже 3 раз в неделю) приступами любой степени выраженности и общей продолжительностью более 1 мес.
Критериями исключения больных из исследования служили: наличие головокружения неустановленной этиологии; декомпенсация соматических заболеваний; язвенная болезнь желудка и двенадцатиперстной кишки, эрозивный гастрит в стадии обострения; феохромоцитома; бронхиальная астма в стадии обострения; установленные заболевания внутреннего и среднего уха воспалительного характера, в том числе после оперативного вмешательства; повышенная чувствительность к бетагистину или вспомогательным компонентам исследуемых препаратов; беременность и лактация; злоупотребление алкоголем; эндогенные психические расстройства.
Во время исследования запрещался прием других ноотропных и метаболически активных препаратов, а также средств, влияющих на головокружение: антигистаминных, антидепрессантов, транквилизаторов, нейролептиков. В случае, если пациент принимал препараты вышеперечисленных групп, производилась их отмена не менее чем за 4 нед до включения в исследование.
Основными причинами головокружения являлись хроническая ишемия головного мозга — у 17 (53,1%) человек; дисциркуляция в вертебрально-базилярной системе на фоне остеохондроза шейного отдела позвоночника — у 14 (43,75%); у 1 (3,15%) больного диагностирована болезнь Меньера.
Головокружение отразилось на работоспособности у 22 (68,7%) пациентов; 8 (25%) человек сменили работу, в 4 (12,5%) случаях головокружение стало причиной стойкой инвалидизации. За последние 3 мес в связи с острым головокружением 8 (25%) человек неоднократно вызывали бригаду скорой медицинской помощи (в среднем 3,75 раза в месяц). По поводу головокружения 16 (50%) пациентов обращались к терапевту в среднем 2,7 раза в месяц; к неврологу — 31 (96,9%) пациент в среднем 3,7 раза в месяц. Двое (6,25%) больных были выписаны из неврологического стационара, где проводилась коррекция вестибулярных нарушений. На амбулаторном лечении с оформлением документа о нетрудоспособности в связи с головокружением находились 4 человека (средняя длительность нетрудоспособности 7,3±4,8 дня).
Для оценки эффективности терапии исследовалась динамика неврологических симптомов, а также использовался ряд дополнительных методик [5]: вестибулярные тесты: нистагм — спонтанный, оптокинетический, позиционный; вестибулоспинальные пробы: проба Ромберга, шаговая проба Унтерберга, указательная проба Барани; шкала головокружения; методика оперативной оценки самочувствия, активности и настроения (САН) в модифицированном варианте В.А. Доскина; шкала общего клинического впечатления (CGI), которая используется для дополнительной количественной оценки возможного ухудшения или улучшения психического состояния пациента в процессе терапии. Оценки по этой шкале варьируют от 1 до 7 баллов: 1 — «очень значительное улучшение», 2 — «существенное улучшение», 3 — «минимальное улучшение»; 4 — «нет изменений», 5 — «минимальное ухудшение», 6 — «умеренное ухудшение», 7 — «значительное ухудшение». Кроме того, использовали балльную оценку переносимости и эффективности препарата (0—4 балла).
При неврологическом осмотре у большинства больных выявлялись координаторные (50%) и чувствительные (28,12%) расстройства, нарушения мышечного тонуса — у 8 (25%) человек. Изменения слуха наблюдались у 23 (71,9%) пациентов в виде субъективного шума, треска в ухе, снижения слуха.
Наиболее часто пациентов беспокоили головокружения в виде вращения, уплывания, проваливания, качания, кроме того, их беспокоили проявления в виде шаткости при ходьбе, укачивания в транспорте, шума или звона в ушах, понижения слуха, головной боли, слабости, усталости, ухудшения памяти.
При проведении вестибулоспинальных проб неустойчивость в позе Ромберга выявлена в 22 (68,75%) случаях. Отклонения в пробе Унтерберга — у 18 (56,25%) человек, указательной пробе Барани — у 14 (43,75%) больных. Спонтанный и оптокинетический нистагм зафиксирован у 13 (40,6%) пациентов.
Артериальная гипертония была у 12 (37,5%) больных, ишемическая болезнь сердца — у 6 (18,75%). У 8 (25%) имелись соматические заболевания: мочекаменная болезнь, хронический холецистит, хронический гастрит, хронический пиелонефрит, катаракта. Один пациент наблюдался отоларингологом в связи с хроническим отитом. Сопутствующую терапию, не противоречащую критериям включения в исследование, получали 17 человек.
Всем больным препарат тагиста назначался в дозе 48 мг в сутки (2 таблетки по 24 мг 2 раза в день). Он входил в состав комплексной терапии: пациенты продолжали принимать базовую гипотензивную терапию, дезагреганты, назначались также лечебная гимнастика и стабилотренинг с биологически-обратной связью на стабилоплатформе — 10 процедур по стандартной методике. Длительность лечения составляла 4 нед. Состояние пациентов изучали до и после курса лечения.
Результаты исследований заносились в индивидуальную регистрационную карту пациента и подвергались статистической обработке на персональном компьютере с использованием стандартизованных функций программ Excel, Epi и Statistica 6.0. Достоверность различий средних величин определяли с помощью параметрического метода (t-тест Стьюдента) и непараметрической статистики (критерий &khgr; 2 ). Различия считались статистически достоверными при р
Лечение головокружения у пожилых пациентов с хронической цереброваскулярной патологией
Дума С.Н.
Научно-исследовательский институт терапии и профилактической медицины - филиал ФГБОУ«Федеральный исследовательский центр Институт цитологии и генетики Сибирского отделения Российской академии наук»,
Новосибирск, Россия 630089, Новосибирск, ул. Бориса Богаткова, 175/1
У пожилых пациентов головокружение может быть вызвано различными причинами, возможности лекарственной терапии ограничены, наиболее часто используется бетагистина дигидрохлорид.
Цель исследования - изучение эффективности и безопасности комплексной терапии препаратом Мексидол ® и бетагистином у пациентов с головокружением по данным шкалы глобальной оценки эффективности лечения.
Пациенты и методы. В исследование включено 89 пожилых пациентов (средний возраст - 73,7 года) с хронической цереброваскулярной патологией и жалобами на головокружение. У всех пациентов оценивали неврологический, отоневрологический (пробы ортостатическая, с форсированной гипервентиляцией, Дикса-Холлпайка, Тинетти, визуальная аналоговая шкала головокружения), соматический, когнитивный и эмоциональный статус. Пациенты были рандомизированы на две группы. В основную группу вошли пациенты, получавшие бетагистин 48 мг/сут, Мексидол ® 5,0 мл внутривенно в течение 10 дней, затем таблетки по 375 мг/сут 50 дней; в группу сравнения - больные, использовавшие только бетагистин 48 мг/сут на протяжении 60 дней. Оценку эффективности лечения проводили по глобальной шкале на 60-й день терапии в обеих группах с учетом мнения врача и пациента. Результаты. У пожилых пациентов головокружение в большинстве случаев (75%) было вызвано несколькими причинами. В группе комбинированного лечения (бетагистин + Мексидол ® ) отмечено более существенное (более чем в два раза) уменьшение симптомов головокружения, чем в группе сравнения.
Заключение. У пожилых пациентов с хроническим цереброваскулярным заболеванием и головокружением комбинированная терапия препаратом Мексидол ® и бетагистином, обладающим нейропротективными свойствами, улучшает результаты лечения.
Ключевые слова: головокружение; пожилой возраст; хроническая ишемия головного мозга; Мексидол ® .
Для ссылки: Дума С.Н. Лечение головокружения у пожилых пациентов с хронической цереброваскулярной патологией. Неврология, нейропсихиатрия, психосоматика. 2018;10(1):55-59.
Treatment of vertigo in elderly patients with chronic cerebrovascular disease
Duma S.N.
Research Institute of Internal and Preventive Medicine, Branch, Federal Research Center, Institute of Cytology and Genetics, Siberian
Branch, Russian Academy of Sciences, Novosibirsk, Russia 175/1, Boris Bogatkov St., Novosibirsk 630089
Трудно найти более разнообразно трактуемый симптом, чем головокружение, которое может существенно ухудшать качество жизни пожилого пациента, быть причиной падений и травм, приводить к инвалидизации [1, 2]. Обычно врачи неохотно берутся за лечение пожилых пациентов, у которых «кружится голова», так как диагностика этого состояния трудоемка и требует времени и есть множество причин для возникновения головокружения. В нашей стране очень мало специализированных центров, в которых проводятся диагностика и лечение головокружения. В амбулаторной неспециализированной практике в качестве причины головокружения обычно рассматривается хроническое цереброваскулярное заболевание, определяемое как хроническая ишемия головного мозга (ХИГМ) [3]. При описании своих ощущений пациенты говорят не столько об истинном вращении, сколько о покачивании, неуверенности при ходьбе и т. п. Неопределенное описание жалоб связано с тем, что система равновесия опирается на взаимодействие сразу нескольких сенсорных систем: зрительной, вестибулярной и мышечно-суставной. Большой объем информации, поступающей в мозг, обеспечивает высокую надежность и приспособляемость системы ориентировки. В то же время дисфункция одной из трех сенсорных систем порождает настолько разные ощущения, что описания пациентами с одинаковым заболеванием своего состояния редко совпадают. Обычно в условиях непродолжительного амбулаторного приема врач оценивает симптомы вестибулярной дисфункции по времени их возникновения и выраженности.
Вестибулярное головокружение носит вращательный характер, сопровождается нистагмом, тошнотой, рвотой, чувством страха и другими вегетативными нарушениями. Наиболее распространенные причины вестибулярного головокружения у пожилых пациентов - доброкачественное пароксизмальное позиционное головокружение (ДППГ), болезнь Меньера, инсульт или транзиторная ишемическая атака (ТИА). При инсульте или ТИА головокружение, как правило, возникает остро и сопровождается другими очаговыми неврологическими симптомами; редко (0,4-0,7% случаев) встречается изолированное вестибулярное головокружение [1]. Головокружение как симптом ортостатической гипотензии наблюдается при болезни Аддисона, амилоидозе почек, при использовании лекарственных препаратов (ганглиоблокаторы, гипотензивные и противопаркинсонические средства), при заболеваниях сердца (аортальный стеноз, желудочковые аритмии) 6. Нарушение устойчивости, обусловленное церебральной микроангиопатией (сосудистая лейкоэнцефалопатия), отмечается почти у половины пациентов (40%) с когнитивными нарушениями [7, 8]. Неустойчивость и падения в пожилом возрасте ассоциированы также с другими соматическими заболеваниями, такими как сахарный диабет, остеопороз, сердечная недостаточность. Множественная сенсорная (мультисенсорная) недостаточность - частая причина жалоб у пациентов с головокружением, она вызвана сочетанием множественной патологии: зрительных расстройств, проприоцептивных нарушений, снижения слуха [1].
Тревога и страх падения усугубляют заболевание и ухудшают адаптацию пожилых пациентов путем избегания рисков (мелкие шаги, медленные движения). Головокружение нередко вызвано тревожными расстройствами [9]. Диагностика психогенного головокружения часто затруднительна в связи с тем, что психопатологические симптомы нередко отрицаются пожилыми пациентами, а головокружение связывается с колебаниями артериального давления (АД) [8, 10, 11]. При наличии подобных жалоб у пожилых пациентов на приеме у невролога часто наблюдается гипердиагностика когнитивных нарушений вплоть до деменции, а терапевты в большом числе случаев интерпретируют эти жалобы как проявление ХИГМ с астено-невротическим синдромом [12].
Выделяют фобическое постуральное головокружение, при котором несистемное головокружение - основная и часто единственная жалоба [9]. В дальнейшем заболевание было переименовано в «персистирующее постурально-перцептивное головокружение», которое ВОЗ включила в МКБ-11 [13].
Лечение головокружения проводится в зависимости от его причины. Например, в случае ДППГ эффективны репозиционные маневры [2, 9]. При вестибулярном головокружении наиболее часто используется бетагистин. В нашей стране у таких пациентов широко применяются ноотропные средства, однако нередко они вызывают раздражительность, слабость и нарушение сна [14]. Пациентам с диагнозом ХИГМ нередко назначают этилметилгидроксипиридина сукцинат (Мексидол ® ), который обладает антиоксидантными, анксиолитическими, антиагрегантными и вегетотропными свойствами [14], что позволяет рассматривать его как патогенетически обоснованное средство в комплексной терапии пациентов с ХИГМ и головокружением. Мексидол ® мало токсичен, не оказывает седативного, миорелаксирующего, стимулирующего, эйфоризирующего действия. Применение одного нейропротективного препарата, обладающего несколькими механизмами действия и минимальным количеством побочных эффектов, крайне важно в лечении пожилых пациентов [14].
Цель исследования - изучение эффективности и безопасности Мексидола ® в комплексной терапии пожилых пациентов с ХИГМ и жалобами на головокружение.
Пациенты и методы. В открытое сравнительное контролируемое исследование было включено 89 пожилых пациентов (49 женщин и 40 мужчин) в возрасте 70-85 лет (средний возраст - 73,7 года) с диагнозом «хроническая ишемия мозга», ведущей жалобой у которых было головокружение. По МКБ-10 ХИГМ квалифицируется как «Другие уточненные поражения сосудов мозга с гипертензией» (рубрика I67.8) [5]. Диагноз ХИГМ подтверждали или устанавливали на основании результатов стандартизированного клинического неврологического обследования, а также лабораторных данных (общий анализ мочи и крови, биохимическое исследование крови трехмесячной давности) и инструментальных исследований (дуплексное сканирование сонных артерий, магнитно-резонансная томография - МРТ - головного мозга), представленных в амбулаторной карте пациента.
Критерии включения в исследование: I-II стадия ХИГМ в соответствии с классификацией сосудистых поражений головного мозга Е.В. Шмидта и соавт. (1985).
Критерии исключения: III стадия ХИГМ с наличием деменции по классификации Е.В. Шмидта и соавт.; нестабильные сопутствующие заболевания, требующие лечения изменяющимися дозами лекарств; наличие признаков депрессии (>7 баллов по шкале Гамильтона) и деменции ( < 24 баллов по краткой шкале оценки психического статуса, КШОПС).
Характер головокружения оценивали с помощью специализированного опроса (табл. 1).
Таблица 1. Вопросы, позволяющие выяснить характер головокружения
- Кружились ли предметы вокруг вас?
- Как они кружились?
- Можете ли вы воспроизвести головокружение и указать рукой его скорость и направление?
- Как долго длилось головокружение?
- Был ли этот приступ головокружения первый?
- Связано ли головокружение с колебаниями АД и пульса?
- Беспокоила ли вас головная боль одновременно с головокружением или после него?
- Были ли у вас «пелена перед глазами», дурнота, обмороки?
- Возникали ли слуховые симптомы в это время?
- Был ли гул или свист?
- Было ли ощущение заложенности ушей и глухоты?
Таблица 2. Причины головокружения у пожилых пациентов (n=89)
| Причина головокружения | Частота, % |
| Сердечно-сосудистые заболевания | 39 |
| Побочные эффекты препаратов 14 Периферические вестибулярные нарушения (ДППГ, болезнь Меньера и др.) | 18,6 |
| Психические заболевания (психогенное головокружение) | 17,2 |
| Нейросенсорная тугоухость I-II стадии | 11,2 |
| Снижение остроты зрения (катаракта, макулодистрофия I-II стадии) | 68,2 |
| Несколько причин | 74,8 |
Выясняли анамнез заболевания, а также какие лекарственные средства принимал пациент (по поводу других заболеваний). Оценивали соматический статус: АД, частоту сердечных сокращений и дыхания. Когнитивный статус определяли по КШОПС. Для характеристики психического статуса использовали шкалу Гамильтона. Неврологический статус изучали с использованием стандартного набора провокационных проб на головокружение и равновесие. Проводили ортостатическую пробу и ее стандартизированную оценку, форсированную гипервентиляцию в течение 3 мин для диагностики панических атак [15]. Применяли следующие тесты: резкие повороты во время ходьбы, тандемную ходьбу или круговое вращение в вертикальном положении (фрагмент шкалы Тинетти), пробу Дикса-Холлпайка [15]. Использовали визуальную аналоговую шкалу (ВАШ) 10 см для субъективной оценки пациентом выраженности головокружения в 1-й и на 60-й день терапии.
Все пациенты были рандомизированы на две группы, между которыми не было статистически значимых различий по полу и возрасту. Основная группа включала 50 пациентов, которым назначали бетагистин по 48 мг/сут в сочетании с препаратом Мексидол ® 5,0 мл внутривенно в течение 10 дней, а затем перорально по 375 мг/сут еще 50 дней. Группу сравнения составили 49 пациентов, которые получали только бетагистин по 48 мг/сут на протяжении 60 дней. Всем пациентам дополнительно проводили антигипертензивную терапию под контролем АД.
Все участники исследования подписали информированное согласие на участие в нем.
Результат лечения оценивал врач по глобальной шкале эффективности лечения в обеих группах (в %): очень хороший; хороший; минимальный; нет изменений; минимальное ухудшение. Проводилась также оценка лечения пациентом по шкале общего впечатления: значительное улучшение; улучшение; незначительное улучшение; минимальное улучшение (с момента начала исследования). Кроме того, регистрировали побочные эффекты.
Для статистической обработки данных используемых тестов и шкал применяли компьютерную программу SPSS версия 11.5. Для обработки данных использовали непараметрический критерий Уилкоксона-Манна-Уитни. При сравнении вариационных рядов учитывали достоверные различия (р<0,001). Различие долей в группах рассчитывали по критерию Пирсона.
Результаты. Все пациенты предъявляли жалобы на головокружение: флюктуирующая неустойчивость в форме приступов (секунды или минуты) или иллюзорное нарушение устойчивости тела (часы или минуты) при ходьбе. Головокружение возникало спонтанно, но чаще было связано с такими провоцирующими факторами, как повороты в постели и подъем с нее, подъем по лестнице, пребывание в лифте, метро и т. д.). Пациенты часто указывали на ощущение «тумана в голове», чувства легкого опьянения; головокружение имело место в положении стоя и во время ходьбы.
Наиболее частыми (39%) причинами головокружения у пожилых пациентов были сердечно-сосудистые заболевания, которые сопровождались колебаниями АД, нарушением ритма сердца, ортостатическими состояниями (табл. 2). На втором месте по распространенности были побочные эффекты лекарственных препаратов. Причиной ортостатических нарушений часто являлась ятрогенная гипотензия (прием гипотензивных препаратов в сочетании с другими средствами, усиливающими артериальную гипотензию), вызывающая постуральное головокружение и падения у пожилых. К артериальной гипотензии приводил прием комбинации гипотензивных препаратов (чаще всего бета-адреноблокатор + диуретик, сартан + диуретик - 3% случаев) или комбинации гипотензивного препарата с миорелаксантами, противопаркинсоническими средствами, нитратами, анксиолитиками или снотворными (11% случаев). На рецидивирующие периферические вестибулярные нарушения приходилось 18,6% причин головокружения; на психогенное головокружение (после перенесенного ранее периферического вестибулярного головокружения) - 17,2%. Неустойчивость могла быть вызвана снижением слуха (11,2% пациентов) и (или) зрения (68,2%). Более чем 74,8% пациентов имели несколько причин головокружения.
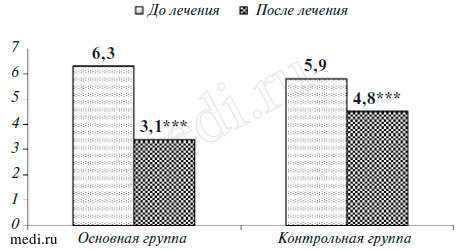
Рис. 1. Выраженность головокружения по ВАШ (в баллах) в 1-й и на 60-й день терапии в основной и контрольной группах.
Здесь и на рис. 2: *** - р
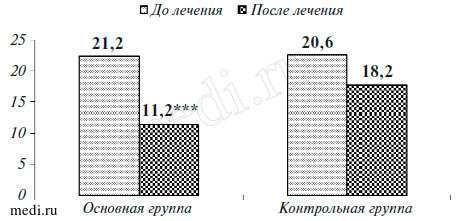
Рис. 2. Динамика тревожности по шкале Гамильтона (в баллах)
Оценка результатов лечения (к 60-му дню) врачом была следующей. В основной группе очень хороший результат зафиксирован у 24,5% пациентов, хороший - у 42,4%, минимальное улучшение - у 27,6%, не отмечено изменений у 5,5%; в контрольной группе очень хороший результат отмечен у 18,4% больных, хороший - у 36,4%, минимальное улучшение - у 32,6%, не было изменений у 12,6%. По мнению пациентов (на 60-й день лечения), в основной группе существенное улучшение наблюдалось в 27,8% случаев, незначительное улучшение - в 44,5%, состояние не изменилось в 27,7%; в контрольной группе на существенное улучшение указали 19,2% обследованных, на незначительное улучшение - 37,5%, не отметили изменений 42,3% и сообщил о незначительном ухудшении 1%. Суммарно положительная динамика на фоне лечения зафиксирована в основной группе, по мнению врача, у 66,9% пациентов, а по мнению пациентов - у 72,3% (в контрольной группе - соответственно у 54,8 и 56,7%). Переносимость препарата была хорошей. Связанных с препаратом нежелательных явлений не отмечено.
В настоящее время у пациентов с вестибулярным головокружением в качестве лекарственной терапии используется бетагистин, который наиболее эффективен при болезни Меньера [2, 9]. Результаты нашего исследования показывают, что у пожилых пациентов с хроническим цереброваскулярным заболеванием и головокружением присоединение к бетагистину препарата Мексидол ® , оказывающего нейропротективное действие, улучшает результаты лечения. Фармакологические эффекты Мексидола ® , по мнению авторов, позволяют рассматривать его как патогенетически обоснованное средство в комплексной терапии пациентов с ХИГМ и головокружением.
Заключение. Таким образом, нейропротективный препарат Мексидол ® , обладающий антиоксидантным, анксиолитическими, антиагрегантным и вегетотропным эффектом, в комбинации с бетагистином улучшает результаты лечения у пожилых пациентов, страдающих хроническим цереброваскулярным заболеванием и головокружением.
ЛИТЕРАТУРА
Декларация о финансовых и других взаимоотношениях
Публикация статьи поддержана ООО «Векторфарм». Автор несет полную ответственность за предоставление окончательной версии рукописи в печать. Окончательная версия рукописи была одобрена автором.
Больной М., 53 лет, поступил в приемное отделение городской больницы с жалобами на головокружение с ощущением вращения окружающих предметов, усиливающееся при движении, тошноту и рвоту. Из-за головокружения пациент не мог ходить без поддержки. Головокружение появилось 3 часа назад. Накануне был эпизод кратковременного (в течение нескольких секунд) головокружения с небольшой тошнотой, самостоятельно регрессировавшего. За неделю до появления головокружения перенес ОРВИ.
При обследовании в приемном отделении больницы отмечался горизонтальный нистагм, направленный влево. В пробе Ромберга пациент отклонялся вправо. Другой очаговой неврологической симптоматики не было.
Головокружение продолжалось еще около 5 часов, постепенно ослабевая. Однако из-за неустойчивости и усиливающейся при движении тошноты почти не мог ходить; несколько шагов делал только с поддержкой. На протяжении следующих двух недель состояние постепенно улучшалось: приступы системного головокружения не возобновлялись, неустойчивость возникала только при резких движениях, быстром вставании с постели.
Возникновение острого вестибулярного головокружения у больного, перенесшего несколько дней назад ОРВИ, отсутствие очаговой неврологической симптоматики за исключением горизонтального нистагма и вестибулярной атаксии, течение заболевания в виде постепенно (в течение нескольких часов) уменьшающегося головокружения и вестибулярной атаксии, сохраняющейся на протяжении нескольких недель и также постепенно регрессирующей, позволило диагностировать у пациента вестибулярный нейронит.
Какова тактика лечения вестибулярного нейронита в остром периоде, какой должна быть реабилитация, и какова вероятность рецидива?
Клиническая картина вестибулярного нейронита была впервые описана Эриком Руттином в 1909 году, а затем более подробно Карлом Ниленом в 1924 году. Термин «вестибулярный нейронит» предложен Чарльзом Халлпайком в 1949 году. Вестибулярный нейронит - третья по частоте причина острого вестибулярного головокружения после доброкачественного пароксизмального позиционного головокружения и болезни Меньера.
Заболевание преимущественно встречается в возрасте 30-60 лет, мужчины и женщины болеют одинаково часто.
Этиология и патогенез
Этиология и патогенез вестибулярного нейронита до конца не ясны. Заболевание связывается с избирательным воспалением (вирусного или инфекционно-аллергического генеза) вестибулярного нерва, на что указывают результаты немногочисленных патоморфологических исследований. В пользу вирусной этиологии (чаще всего вирус простого герпеса первого типа) вестибулярного нейронита свидетельствуют нередкое развитие заболевания после перенесенной респираторной вирусной инфекции, эпидемический характер болезни с пиком заболеваемости, приходящимся на конец весны и начало лета, а также описанные в литературе случаи одновременного заболевания нескольких членов семьи. Роль вируса герпеса подтверждают случаи развития герпетического энцефалита при вестибулярном нейроните.
При вестибулярном нейроните обычно поражается верхняя ветвь вестибулярного нерва, иннервирующая горизонтальный и передний полукружные каналы, а также эллиптический мешочек преддверья лабиринта, на что указывает нередкое сочетание вестибулярного нейронита с доброкачественным пароксизмальным позиционным головокружением, которое обычно обусловлено отолитиазом заднего полукружного канала, иннервируемого нижней ветвью вестибулярного нерва. Значительно реже встречается поражение нижней ветви вестибулярного нерва.
Клиника и диагноз
Вестибулярный нейронит проявляется внезапным и продолжительным приступом системного головокружения, сопровождающегося тошнотой, рвотой и нарушением равновесия. Заболеванию может предшествовать респираторная вирусная инфекция. Иногда за несколько часов или дней до развития острого вестибулярного приступа больные испытывают кратковременные эпизоды головокружения или неустойчивости.
Симптомы вестибулярного нейронита усиливаются при движениях головы или изменении положения тела. Головокружение может уменьшаться при фиксации взора. Характерен спонтанный нистагм, быстрая фаза которого направлена в сторону здорового уха. Мнимое вращение предметов вокруг больного также в типичном случае направлено в сторону здорового уха. В пробе Ромберга больной отклоняется в сторону пораженного уха. Слух не снижается. При неврологическом исследовании отсутствуют симптомы поражения ствола или других отделов головного мозга.
Длительность головокружения колеблется от нескольких часов до нескольких суток. Спонтанный нистагм сохраняется 3-5 дней, нистагм при отведении глаз в сторону здорового уха в очках Френзеля (то есть при выключении фиксации взора) наблюдается еще в течение 2-3 недель. После прекращения головокружения больные на протяжении нескольких суток или недель продолжают испытывать неустойчивость.
Сроки восстановления вестибулярной функции зависят от степени повреждения вестибулярного нерва, скорости центральной вестибулярной компенсации и выполнения больным вестибулярной гимнастики. У многих больных быстрые движения головой могут вызывать осциллопсию и легкую непродолжительную неустойчивость в течение длительного времени после перенесенного вестибулярного нейронита. По данным Okinaka с соавт., через год после заболевания вестибулярная функция полностью восстанавливалась у 40% больных, частично - у 20-30% больных, а в остальных случаях сохранялась односторонняя вестибулярная арефлексия. Тем не менее даже при отсутствии или неполном восстановлении вестибулярной функции больные обычно не испытывают существенных изменений в повседневной активности за счет вестибулярной компенсации. У многих больных, перенесших вестибулярный нейронит, жалобы на головокружение отражают имеющееся соматоформное расстройство.
Вестибулярный нейронит редко (в 2% случаев) рецидивирует, при повторном заболевании поражается «здоровый» вестибулярный нерв. Если у больного, которому был поставлен диагноз вестибулярного нейронита, повторяются приступы вестибулярного головокружения, то следует искать другие причины головокружения, среди которых наиболее часто встречаются болезнь Меньера, доброкачественное пароксизмальное позиционное головокружение и вестибулярная мигрень.
Диагноз вестибулярного нейронита основывается на клинической картине заболевания: острое и относительно длительное (от нескольких часов до нескольких суток) вестибулярное головокружение, сопровождающееся неустойчивостью, горизонтальным или горизонтально-ротаторным спонтанным нистагмом с осциллопсией, тошнотой и рвотой.
Диагноз можно подтвердить с помощью калорической пробы, выявляющей вестибулярную гипо- или арефлексию на стороне поражения. При редко встречающемся поражении нижней ветви вестибулярного нерва калорическая проба отрицательная, но вестибулярный нейронит подтверждают изменения вызванных вестибулярных потенциалов. Косвенные признаки вестибулярного нейронита можно выявить при использовании высоко разрешающей магнитно-резонансной томографии (МРТ) головного мозга с гадолинием.
Дифференциальный диагноз проводят с другими состояниями, проявляющимися длительным вестибулярным головокружением. В отличие от вестибулярного нейронита, острый лабиринтит часто возникает на фоне системной инфекции или острого среднего отита и сопровождается снижением слуха. Перилимфатическая фистула обычно возникает после черепной травмы, баротравмы, сильного кашля или натуживания, сопровождается снижением слуха, подтверждается фистульной пробой. Инсульт в вертебро-базилярной системе сопровождается другими очаговыми неврологическими расстройствами, центральным нистагмом, поражением головного мозга по данным МРТ. Вестибулярный нейронит часто бывает трудно отличить от первого приступа болезни Меньера, которая более вероятна, если головокружение сопровождается шумом в ушах, ощущением распирания в ухе и снижением слуха.
Лечение
Лечение направлено на уменьшение головокружения, тошноты и рвоты (симптоматическое лечение) и ускорение вестибулярной компенсации.
Симптоматическое лечение включает использование препаратов, относящихся к группе вестибулярных супрессантов. Препарат выбора - дименгидринат в дозе 50-100 мг каждые 6 часов. Вместо дименгидрината можно применять метоклопрамид, бензодиазепиновые транквилизаторы и фенотиазины. При рвоте используют парентеральный путь введения (диазепам в/м, метоклопрамид в/м, тиэтилперазин в/м или ректально в свечах). Длительность применения вестибулярных супрессантов определяется длительностью и тяжестью головокружения; как правило, их не используют более трех дней, поскольку эти препараты замедляют вестибулярную компенсацию.
Для ускорения восстановления вестибулярной функции рекомендуют вестибулярную гимнастику, включающую упражнения, при которых движения глаз, головы и туловища приводят к сенсорному рассогласованию. Эти упражнения стимулируют центральную вестибулярную компенсацию. Однако выполнение их на первых порах может быть сопряжено со значительным дискомфортом. Тактика вестибулярной реабилитации и характер упражнений зависят от стадии заболевания, что отражает содержание таблицы 1.
У больных с вестибулярным нейронитом применение в первые трое суток заболевания метилпреднизолона (в начальной дозе 100 мг с последующим снижением дозы на 20 мг каждые трое суток) приводит к более высокой частоте восстановления вестибулярной функции через год с момента заболевания. Несмотря на предположительно вирусную природу заболевания, применение у больных противогерпетических препаратов (отдельно или в комбинации с метилпреднизолоном) не улучшает процесс восстановления.
Для ускорения вестибулярной компенсации в сочетании с вестибулярной гимнастикой можно использовать бетагистина дигидрохлорид (Бетасерк 24 мг) по 48 мг в сутки (1 таблетка 24 мг 2 раза в сутки). Этот препарат, блокируя НЗ-рецепторы центральной нервной системы, увеличивает высвобождение нейромедиаторов из нервных окончаний пресинаптической мембраны (гистамин препятствует высвобождению медиаторов), оказывая ингибирующий эффект в отношении вестибулярных ядер ствола мозга. Экспериментальные исследования показали, что бетагистин ускоряет вестибулярную компенсацию. В эксперименте на животных Бетасерк оказывал дозозависимый эффект на электрическую активность полисинаптических нейронов в вестибулярных ядрах.
Литература
1. Albera R., Ciuffolotti R., Di Cicco M. et al. Double-blind, randomized, multicenter study comparing the effect of betahistine and flunarizine on the dizziness handicap in patients with recurrent vestibular vertigo ‘// Acta Otolaryngol. -2003. - Vol.123. -P. 588-593.
2. Arbusow V, Schulz P, Strupp M et al. Distribution of herpes simplex virus type I in human geniculate and vestibular ganglia: implications for vestibular neuritis. Ann Neurol-1999.-v.46.-p.416-419
3. Baloh R.W Vestibular neuritis. N Engl J Med. -2003. -v348. -p. 1027-1032.
4. Bartal-Pastor J. Vestibular neuritis: etiopathogenesis // Rev Laryngol Otol Rhinol (Bord). -2005. - Vol.126: 279-281.
5. Brandt T. Vertigo. Its Multicensory Syndromes. - 2nd Ed. - London, 2000.
6. Fetter M, Dichgans J. Vestibular neuritis spares the inferior division of the vestibular nerve. Brain 1996. -Vol. 119:755-763.
7. Domingues M.O. Treatment and rehabilitation in vestibular neuritis // Rev Laryngol Otol Rhinol (Bord). 2005. - Vol. 126: 283-286.
8. Gacek RR, Gacek MR The three faces of vestibular ganglionitis. Ann Otol Rhinol Laryngol -2002. -v.lll. -p. 103-114.
9. Godemann F., Siefert K. et al. What accounts for vertigo one year after neuritis vestibularis - anxiety or a dysfunctional vestibular organ? // J Psychiatr Res - 2005.-Vol. 39:529-534.
10. Halmagyi G.M., Aw S.T., Karlberg M. Et al. Inferior vestibular neuritis // Ann N Y Acad Sci. 2002. -Vol. 956: 306-313.
11. Heinrichs N., Edler C. et al. Predicting continued dizziness after an acute peripheral vestibular disorder // Psychosom Med -2007. - Vol 69: 700-707.
12. Huppert D, Strupp M., Theil D., et al. Low recurrence rate of vestibular neuritis: a long-term follow-up. Neurology. -2006. -v.67. -N10. -p. 1870-1871.
13. Karlberg M., Annertz M, Magnusson M. Acute vestibular neuritis visualized by 3-T magnetic resonance imaging with high-dose gadolinium // Arch Otolaryngol Head Neck Surg -2004. - Vol. 130: 229-232.
14. Okinaka Y, Sekitani T, Okazaki H et al Progress of caloric response of vestibular neuronitis. Acta Otolaryngol. -1993. -v.503. -p. 18-22.
15. Philpot S.J., Archer J.S. Herpes encephalitis preceded by ipsilateral vestibular neuronitis // J Clin Neurosci. -2005. - Vol.12: 958-959.
16. Strupp M., Zingler VC, Arbusow V. et al Methylprednisolone, valacyclovir, or the combination for vestibular neuritis. N Engl J Med. -2004. -v. 351. - 354-361.
Читайте также:
- Диагностика коронарной недостаточности. Двухступенчатая проба Мастера
- Врожденная патология плода и новорожденного. Врожденные заболевания плода в картинках
- Гломусангиома среднего уха. Лечение гломусангиомы
- Острая перемежающаяся порфирия (пирролопорфирия, шведская порфирия): причины, диагностика, лечение
- КТ при портальной гипертензии и варикозном расширении вен
