История создания химиопрепаратов - химиотерапии
Добавил пользователь Дмитрий К. Обновлено: 28.01.2026
Одна из основных статей расходов нашего фонда — покупка лекарств противоопухолевой терапии. Так, за 2017 год расходы на их покупку для клиник составили более 313 миллионов рублей — и это не считая адресной помощи.
Дело в том, что противоопухолевая терапия — очень динамично развивающаяся отрасль. Ежегодно в арсенале онкологов и онкогематологов возникают новые лекарства. Какие-то из них позволяют излечивать тех больных, которым раньше ничто не помогало. Какие-то не излечивают полностью, но существенно продлевают жизнь и улучшают ее качество. И почти все новые лекарства, увы, очень дороги. Потом они становятся более доступными, но на рынок выходят новые препараты, которые могут спасти новых пациентов. И вновь это очень дорогостоящие лекарства. Но их цена — это цена многих жизней.
При этом интересно, что химиотерапия — сравнительно молодая область. До начала XX века основным и фактически единственным инструментом онколога был скальпель хирурга. Чуть больше ста лет назад появился еще один метод — лучевая терапия. Но лишь с появлением химиотерапии многие онкологические заболевания из смертельных стали излечимыми или хорошо контролируемыми.
Может быть, пора оглянуться назад и посмотреть, какой огромный путь прошла лекарственная терапия онкологических заболеваний за последние 70 с лишним лет. И как врачи-исследователи, переходя от надежды к отчаянию и снова к надежде, одерживали победы над опухолями с 40-х годов XX века и до наших дней.
1. Рождение химиотерапии
Есть красивая легенда о том, как возникла идея химиотерапии. Эта легенда связана с известным событием Второй мировой войны: в 1943 году немецкая авиация разбомбила военные суда союзников в гавани итальянского города Бари. Бомбардировке подвергся и транспорт с грузом иприта — известного боевого отравляющего вещества. Из-за утечки иприта пострадали или погибли тысячи людей. Медики, обследуя пострадавших, заметили, что у них резко снижено число лейкоцитов, особенно лимфоцитов. И якобы именно это наблюдение подвигло ученых на то, чтобы изучать применение аналогов иприта для лечения таких опухолей, как лимфомы.
В действительно все было не так. Исследования противоопухолевой активности производных иприта уже велись ко времени бомбардировки Бари. Но это были секретные разработки, и первые результаты были опубликованы только в 1946 году. Американские химики Альфред Гилман и Луи Гудмен синтезировали препарат «Эмбихин», успешно испытали его на мышах, а затем и на человеке с лимфомой, добившись несомненного (но, увы, недолгого) улучшения. Сейчас этот высокотоксичный препарат практически не применяется, но свою роль он сыграл: впервые было показано, что химическое вещество может тормозить развитие опухоли, и это вызвало огромный интерес медиков и химиков.
2. Сидни Фарбер и его роль
Несмотря на открытие Гилмана и Гудмена, основоположником современной химиотерапии считают другого человека — американского педиатра Сидни Фарбера. Он основал Фонд исследований рака у детей и вел систематические исследования эффективности различных препаратов. Вероятно, самым известным достижением Фарбера явился препарат «Метотрексат», синтезированный по его просьбе гениальным химиком Суббарао: это лекарство, которое до сих пор является одним из ключевых химиопрепаратов, впервые позволило добиться ремиссии (исчезновения признаков болезни) при самом распространенном онкозаболевании у детей — остром лимфобластном лейкозе. Более того, разработка «Метотрексата» была основана на очень важной концепции, которая впоследствии позволила изобрести еще несколько противоопухолевых лекарств: его действие основано на том, что он очень похож на вещество, необходимое для деления клеток при этом варианте лейкоза, и позволяет «обмануть» делящиеся клетки, что приводит к их гибели.
3. Новые препараты. Оптимизм и пессимизм
В 50-е и начале 60-х годов XX века велся широкий поиск, и именно тогда появились многие противоопухолевые лекарства, которые хорошо нам знакомы и по сей день. Так, исследование противоопухолевого действия антибиотиков привело к открытию «Космегена», изучение растительных препаратов — к открытию «Винкристина». Были синтезированы и испытаны «Меркаптопурин», «Тиогуанин», «Фторурацил», «Цитозар» и другие лекарства. Бурный интерес к новой области привел и к росту финансирования: противораковой терапией заинтересовались и государства, и филантропы.
Однако, несмотря на многочисленные достижения, врачи в то время все более скептически смотрели на перспективы химиотерапии. Ни одно из лекарств не могло дать полного излечения: практически у всех пациентов болезнь через некоторое время «приспосабливалась» к препарату, возвращалась и оказывалась фатальной. И многие специалисты считали, что новые лекарства лишь продлевают мучения больных… Тем более что эти лекарства очень тяжело переносились: ведь побочные эффекты химиотерапии всем известны.
4. Полихимиотерапия. Первые выжившие
Прорыв произошел в 1965 году. Он был связан с именами трех врачей и исследователей — Эмиля Фрая, Эмиля Фрайрайха и Джеймса Холланда. Именно они впервые предположили, что для повышения эффективности лечения можно и нужно использовать сразу несколько лекарств с разными механизмами действия — тогда опухоли труднее будет к ним приспособиться.
Эта идея шла вразрез со всеми тогдашними представлениями: если пациент тяжело переносит один токсичный препарат, как можно давать ему сразу три или четыре? Но терять было нечего: лейкозы и лимфомы в те времена были абсолютно смертельными заболеваниями. И первые пациенты получили терапию сразу несколькими лекарствами — то, что сейчас называется полихимиотерапией. Еще одна идея состояла в том, что терапия должна длиться достаточно долго, даже когда признаки болезни вроде бы уже исчезли — чтобы уничтожить остатки опухолевых клеток и не дать им возможности вновь размножиться.
Эффект был потрясающим. Впервые появились не просто больные, у которых наступало кратковременное облегчение симптомов, а случаи длительных ремиссий, фактически равносильных выздоровлению. Шанс на долгую полноценную жизнь получили сразу десятки процентов детей с острым лимфобластным лейкозом и взрослых с лимфомой Ходжкина. Это и сейчас одни из самых излечимых онкологических заболеваний.
5. Адъювантная и неоадъювантная химиотерапия, сопроводительная терапия
И с этого момента представление о лечении химиотерапией стало приближаться к нашему современному пониманию. Не только разрабатывались новые препараты, но и изменялась концепция их использования. Возникло понятие протокола, который описывает, когда, в каких сочетаниях и в каких дозах должны вводиться химиопрепараты. Врачи также задумались над тем, как снизить опасность от токсического воздействия препаратов на больных, и стала развиваться сопроводительная терапия, без которой сейчас невозможно представить себе противораковое лечение: антибиотики и противогрибковые препараты для борьбы с инфекционными осложнениями, переливания компонентов крови, антидоты для некоторых конкретных лекарств…
Инфузоматы - автоматизированные приспособления для химиотерапии
Далее, врачи поняли, как сочетать химиотерапию и хирургическое лечение при солидных опухолях — то есть не лейкозах или лимфомах, а заболеваниях, где есть локальная масса опухолевых клеток. Использование пред- и послеоперационной (говоря по-научному, неоадъювантной и адъювантной) химиотерапии позволило добиться победы во многих случаях рака груди или кишечника у взрослых, нефробластомы и сарком у детей, при целом ряде других опухолей.
«Традиционная» химиотерапия за десятки лет достигла существенных успехов. Но в целом, хотя по сей день появляются новые лекарства и новые протоколы, есть ощущение, что во многом она уже достигла своего потолка. И современные магистральные пути развития уже основаны не просто на препаратах, которые блокируют деление любых быстро делящихся клеток, а на лекарствах, действие которых учитывает особенности каждой конкретной опухоли.
6. Таргетная терапия
Хронический миелоидный лейкоз еще сравнительно недавно считался болезнью, которая очень плохо поддается терапии: шанс больным давала только трансплантация донорского костного мозга. Но именно с этой болезнью был связан первый и самый значимый успех нового подхода: в конце 90-х годов XX века для борьбы с ней был разработан иматиниб («Гливек»). Это лекарство учитывает конкретные молекулярные механизмы, которые управляют делением опухолевых клеток именно при хроническом миелоидном лейкозе, и целенаправленно блокирует их. Новый подход получил название таргетной терапии, от английского target — мишень, цель.
С появлением «Гливека» практически фатальная болезнь превратилась в хорошо контролируемую: человек может полноценно жить многие годы, просто принимая таблетки (которые к тому же менее токсичны, чем традиционная химиотерапия). Другие лекарства учитывают молекулярные механизмы развития других опухолей и используются, например, при некоторых саркомах и лимфомах, раке почки, легких, других органов.
Особая разновидность таргетной терапии, также возникшая около 20 лет назад, — использование иммунопрепаратов на основе моноклональных антител. Речь идет об особых белках, которые связываются с клетками конкретной опухоли и тем самым способствуют их уничтожению. Например, ритуксимаб («Мабтера», «Ацеллбия») успешно используется при ряде лимфом, а трастузумаб («Герцептин») очень эффективен при определенных типах рака молочной железы.
Эти успехи вдохновили исследователей на новые разработки. Сейчас уже известны десятки таргетных препаратов, которые заметно улучшили результаты лечения при целом ряде опухолей. Разработка новых лекарств активно ведется и сейчас.
7. Современная противоопухолевая иммунотерапия
В последние несколько лет внимание онкологов всего мира приковано к новому направлению в лекарственной терапии злокачественных опухолей. Речь идет о том, чтобы *стимулировать иммунную систему самого организма на борьбу с раком*. Для этого, как выяснилось, необходимо блокировать те молекулярные механизмы, которые опухоль использует, чтобы защититься от атаки иммунных клеток. Углубленное понимание этих сложнейших механизмов (которые сейчас интенсивно изучаются) уже привело к разработке таких лекарств, как «Ервой», «Опдиво», «Китруда», «Тецентрик» и другие. Благодаря им уже сейчас удалось спасти целый ряд пациентов с меланомой, лимфомами и некоторыми другими онкозаболеваниями, но, по общему мнению, потенциал этих новейших лекарств пока еще раскрыт далеко не полностью и в самом скором времени нас ждут новые достижения.
В 2018 году за разработку этого класса лекарств ученым Джеймсу Эллисону и Тасуко Хондзе была присуждена Нобелевская премия по физиологии и медицине.
Перемены на Западном фронте: история химиотерапии

12 июля 1917 года около бельгийского городка Ипр немецкая армия впервые пустила в ход отравляющее вещество, названное по месту сражения ипритом. Оказалось, новое оружие можно обратить против опухолей.
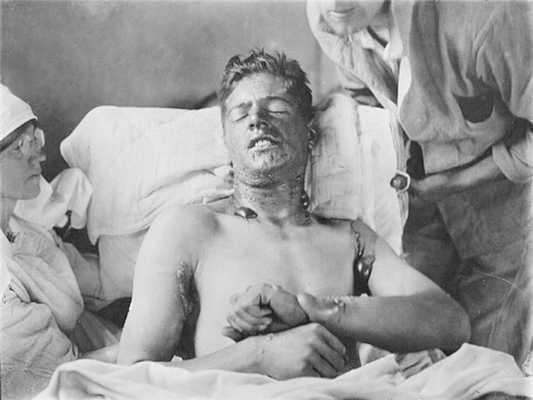
Волдыри и нарывы от иприта возникают прежде всего там, где кожа нежнее — на шее, под мышками, на запястьях.
Страшный яд оказывал действие, которого не ожидали даже сами немцы. Изучая последствия применения иприта, врачи придумали важнейший метод лечения рака — химиотерапию.
Как водится, новое оружие применили, не зная толком, с чем имеют дело. Весной 17-го года немецкое командование осознало, что силы на исходе. В дело шли все ресурсы без разбора, лишь бы удержать вражеское наступление. Химики предложили маслянистую жидкость, пары которой оказывали удушающее действие и раздражали глаза, судя по опытам на обезьянах. Отравляющее вещество с запахом горчицы, прозванное «горчичный газ», плохо разлагалось и заражало местность надолго. Для отличия начинённые им снаряды помечали жёлтым крестом.
Когда химический завод в Адлергофе выдал первую партию таких снарядов, в цеху произошёл взрыв. При тушении пожара и расчистке завалов никто не погиб. Военные решили, что новая отрава не так уж сильна, и не хотели принимать её на вооружение. Но деваться было некуда: англичане собрали под Ипром ударную группировку, которую надо было хоть чем-нибудь остановить. Для пробы артиллеристы обстреляли загон с кошками. Все кошки погибли, значит, «жёлтый крест» в качестве яда вполне пригоден. Отчего умерли животные, никто особо не разбирался. В 22 часа 12 июля немцы начали артобстрел и за ночь обрушили на противника 50 тысяч снарядов со 125 тоннами «горчичного газа».
Англичане ощутили сильный запах. Он чувствовался всего несколько минут. На самом деле это грозный симптом — если человек «принюхался» и более не слышит запаха, значит, началось отравление. Тогда этого ещё не знали. От нового газа немного першило в горле, но не сильней, чем от порохового дыма. Маслянистые лужи под ногами выглядели вполне безобидно. Проведя на всякий случай полчаса в газовых масках, британцы сочли, что ничего страшного нет, поснимали противогазы и легли спать. Сон их был крепок и спокоен. Но к утру они совершенно ослепли. Кожа по всему телу чесалась, в паху и под мышками ощущалась жуткая боль. Кричать и даже говорить сил не было: лёгкие заполнила пена, и каждый вдох давался так тяжело, что казался последним.
Задыхающиеся люди с повязками на глазах — они были не в силах выносить солнечный свет — держась друг за друга, брели в тыл, ведомые медсёстрами. Из 6000 готовых наступать бойцов пострадало 2143, умерло 95. К большинству остальных вернулось зрение, но ожоги и нарывы по всему телу не заживали месяца три. Эти-то не поддающиеся лечению нарывы и были сюрпризом для всех.

«Отравленные газом», картина американского живописца Джона Сингера Сарджента (1856-1925). Изображает британских и американских солдат, пострадавших на германском фронте от иприта. Эскизы выполнены в июле 1918 года с натуры, картина закончена в марте 1919-го.
Немцы при опытах на шимпанзе и кошках не удосужились посмотреть, что творится у них под шерстью. До 12 июля 1917 года лишь один человек испытал на себе все прелести иприта. Это был не кто иной, как Николай Зелинский, в будущем великий химик и создатель противогаза. 30 лет назад, в 1886 году, молодой Зелинский был на практике в Гёттингенском университете. Научный руководитель Виктор Мейер поручил ему синтезировать вещество, которое как раз и оказалось ипритом. Зелинский случайно облился своим продуктом и еле выжил. Он едва дышал, надолго ослеп и три месяца со страшными язвами пролежал в местной клинической больнице. Мейер послал остатки иприта в больницу на исследование. Лабораторные кролики демонстрировали те же симптомы, что и пострадавший. Когда же раздражение появилось на коже лаборанта, эксперименты сразу прекратили. Потом о них вообще забыли, и потеряли журнал.
В 1917 году немцам уже некого было спросить: Зелинский на стороне противника, а Мейер двадцать лет назад впал в депрессию и принял цианистый калий. Только после боевого применения все бросились изучать иприт. Британские врачи установили, что у отравленных падает уровень лейкоцитов в крови. Вскоре на фронт прибыл американский хирург Эдвард Крамбхаар, в будущем знаменитый кардиолог и историк медицины. С ним была его супруга Хелен, женщина-врач, верный помощник и ассистент. Постоянно оперируя, они урывали время ото сна, чтобы внимательно изучить тела отравленных.
Рассматривая под микроскопом их костный мозг, Крамбхаар заметил, что деления клеток совершенно не видно. Между тем в костном мозге этот процесс должен происходить активно — там из бластов вырабатываются новые клетки крови. Вот почему так трудно лечить причинённые «горчичным газом» язвы: иприт останавливает митоз, а значит, и любую регенерацию.
Этот вывод сразу же применили на практике. Немцы часто использовали смеси газов. Если анализ показывает снижение числа лейкоцитов и активности митоза, значит, пациент пострадал от иприта. Всего по обе стороны фронта таких отравленных насчитывалось около миллиона двухсот тысяч человек, из них до конца войны скончалась 91 тысяча. Остальные в массе своей не дожили до старости, умирая от инфекций дыхательных путей.
После войны на смену «горчичному газу» пришли в пять раз более ядовитые азотистые иприты. Перспектива их применения казалась сомнительной: теперь газ стоял на вооружении всех армий, и никто мечтать не мог о монополии на иприт, которая была у немцев целый год с лета 1917-го.
Но после Перл-Харбора стало ясно, что от японцев можно ждать всего. С декабря 1941 года в Йельском университете фармакологи Луис Гудман и Алфред Гилман стали по заказу военных искать антидот к азотистому иприту. А как проверить, действует ли антидот? Вспомнили работу Крамбхаара — если митоз идёт, значит, иприт нейтрализован. Активнее всего делятся раковые клетки, вот на них и можно проверять. Тут Гудмана осенило: да ведь инъекция иприта должна останавливать рост опухоли!
Если на опыты в интересах вооружённых сил изводили стаи кроликов, то для проверки этой гипотезы у Гилмана была всего одна мышь. У неё вызвали лимфому, затем ввели ей иприт — опухоль исчезла. Через две недели случился рецидив, после новых инъекций опухоль опять уменьшилась, однако теперь её клетки стали резистентными к яду, и мышь всё-таки умерла от рака. Но она прожила целых 84 дня, то есть на порядок больше, чем без лечения. Этот результат сообщили хирургу-онкологу Густаву Линдскогу. Он решился предложить такую химиотерапию кому-нибудь из безнадёжных пациентов больницы Нью-Хейвен. По счастливой случайности, первым согласился пациент с формой лейкоза, чувствительной к иприту. Будь у него другая патология, химиотерапия возникла бы на много лет позже.
История болезни была засекречена, потому что дело касалось применения боевого отравляющего вещества. В медицинской карточке вместо словосочетания «азотистый иприт» значится «субстанция X». Врачебная тайна до сих пор запрещает публиковать имя, фамилию и биографию больного.
Мы мало знаем об этом замечательном человеке, который вошёл в историю медицины под инициалами «J.D». Родился он в 1894 году в Российской империи, на территории современной Польши. В 1912 году эмигрировал в США. Семьи у него не было, он в одиночку снимал четырёхкомнатный дом в Меридене, штат Коннектикут, где работал на шарикоподшипниковом заводе. Вот, собственно, и всё.
К врачам он обратился в феврале 41-го, по поводу увеличения лимфоузлов и болезненных ощущений. Диагностировали лимфосаркому, облучали с некоторым результатом. После рецидива оперировали, затем опять облучали. Летом 42-го рост опухоли возобновился. Она мешала открывать рот и как следует дышать. Шея настолько распухла, что не давала повернуть голову, а спать «J.D.» мог только в кресле.
На предложение попробовать инъекции иприта больной согласился, понимая, что терять уже нечего. В 10 утра 27 августа 1942 года ему ввели внутривенно первую дозу яда. На четвёртый день химиотерапии опухоль спала, «J.D.» стал способен есть ложкой и спать в постели. За неделю внешние симптомы исчезли полностью, а через месяц наступила ремиссия — анализ крови показал отсутствие раковых клеток.
Конечно же, наблюдалась и характерная для отравленных ипритом лейкопения, то есть падение числа лейкоцитов в крови. Начались кровоизлияния и замещение костного мозга жировой тканью. Через некоторое время вернулась опухоль, и новые инъекции не свели её на нет. Спустя 96 дней после начала химиотерапии «J.D.» умер от побочных эффектов лечения. Но его фотографии, приложенные к этой публикации, произвели глубокое впечатление на врачей.
К 1946 году, когда работу рассекретили, азотистый иприт получили уже 67 онкобольных в разных городах Америки. Появилась статистика, которая с тех пор неуклонно улучшается. Лейкоз перестал быть смертным приговором: современная химиотерапия позволяет добиться стойкой ремиссии у 75% больных. «Горчичный газ», с которого всё началось, для медицины уже в далёком прошлом. Теперь остаётся исключить его использование по прямому назначению.
Химиотерапия: выдержать и выздороветь

Самочувствие и настрой пациентов при проведении химиотерапии несомненно сказываются на эффективности онкологического лечения. Правильный подбор препаратов поможет избежать развития серьезных побочных эффектов, связанных с приемом цитостатиков: больные будут чувствовать себя лучше, а лечение будет более результативным.
Кому и зачем назначают химиотерапию
Химиотерапия — важный этап лечения онкологических заболеваний. В зависимости от характера опухоли, стадии развития и агрессивности процесса, больным назначают различные комбинации препаратов, наиболее эффективно справляющиеся с опухолью. Химиотерапия может назначаться как до хирургического вмешательства или лучевой терапии, так и после проведения операции. Для достижения необходимого результата больным необходимо пройти несколько последовательных химиотерапевтических курсов. Лекарственные препараты, которые используются для проведения химиотерапии, нередко оказываются токсичны для пациентов. Они вызывают ряд побочных эффектов — тошноту, рвоту, диарею, потерю аппетита, повышенную утомляемость. Это не лучшим образом влияет как на физическое, так и на эмоциональное состояние людей, вынужденных бороться с тяжелым заболеванием.
Осложнения при химиотерапии
Одним из серьезных осложнений, связанных с приемом цитостатических препаратов, является нейтропения — уменьшение уровня нейтрофилов в крови. Падение концентрации нейтрофилов снижает устойчивость организма к вирусным, бактериальным и грибковым инфекциям. Такие последствия приема цитостатиков нередко приводят к вынужденному увеличению промежутка между химиотерапевтическими курсами, снижению дозы препаратов или же отмене лечения. Это негативным образом сказывается на эффективности лечения и выживаемости пациентов.
Что принимать при осложнениях
Для того чтобы снизить иммунодепрессивное, гепатотоксичное и нефротоксичное действие химиотерапевтических препаратов, рекомендован прием азоксимера бромида. Улучшить состояние больных поможет короткий курс препарата, продолжительность которого не превышает 10 дней.
При необходимости профилактики иммунодепрессивного влияния опухоли, для улучшения состояния пациентов после проведения операции по удалению опухоли, а также в период восстановления после химиотерапевтического лечения и лучевой терапии назначают более длительный курс азоксимера бромида, который может длиться от 2 месяцев до года.
Действие азоксимера бромида
Препарат хорошо переносится онкобольными и может назначаться с цитостатиками, антибиотиками и другими лекарствами. Включение азоксимера бромида в комплексную терапию онкологических пациентов позволит проводить лечение без изменения назначенной врачом схемы химиотерапии из-за развития инфекционных осложнений и других побочных эффектов.
Химиотерапия
Химиопрепараты разделяются на алкилирующие цитостатики, антиметаболиты, антибиотики и другие. Торможение роста опухоли гормонами, антигормонами или регуляторами их выработки также относят к химиотерапии.
Что такое химиотерапия?
Химиотерапия злокачественных опухолей - это один из методов нехирургического лечения онкологических заболеваний. Суть его заключается в применении препаратов, оказывающих токсическое действие на быстро делящиеся раковые клетки. Негативное влияние на здоровые клетки организма должно отсутствовать или быть минимальным. Существует важное отличие химиотерапевтических препаратов от других противоопухолевых медикаментов (таргетная терапия, иммунотерапия, гормональная терапия): они «убивают» раковые клетки, нарушая их деление.
В каких случаях назначают химиотерапию?
В зависимости от цели различают следующие виды химиотерапии:
- лечебная - для уничтожения новообразования.
- индукционная - перед операцией или радиотерапией, увеличивающая эффективность последующих процедур. Зачем назначают химиотерапию вместе с операцией? Лечение противоопухолевыми препаратами делает новообразование компактнее. Уменьшение опухоли дает возможность сократить объем хирургического вмешательства или сделать неоперабельную опухоль операбельной.
- адъювантная (химиотерапия после операции) - снижает риск рецидива.
- паллиативная - помогает контролировать симптомы у больных, которым невозможно провести радикальную операцию.
Химиотерапия у детей
Лечение онкологических заболеваний у детей часто включает химиотерапию. За некоторыми исключениями, эффективность для маленьких пациентов гораздо выше, чем для взрослых. Ребенок обычно также легче переносит препараты. Однако сочетание с радиотерапией нередко сопровождается отдаленными побочными эффектами. В этом случае рекомендуется мониторинг состояния здоровья на протяжении всей жизни.
Премедикация перед химиотерапией
Премедикацией называют введение лекарственных средств, которые помогают организму лучше переносить саму химиотерапию. Выбор медикаментов зависит от прогнозируемых побочных действий. Премедикация может включать дексаметазон, димедрол, ранитидин, тавегил и другие препараты.
Как проходит курс химиотерапии?
Прием химиотерапевтических препаратов происходит несколькими курсами. Перерывы между ними дают возможность здоровым тканям восстановиться и свести к минимуму количество и тяжесть побочных эффектов. Курс лечения можно проходить дома, амбулаторно или в процессе госпитализации. Здесь все зависит от способа введения препаратов, необходимости дополнительных процедур и общего состояния пациента. Схемы химиотерапии составляется индивидуально и могут включать один или несколько препаратов. Главная задача врача при подборе лекарств - обеспечить разумный баланс между эффективностью препаратов и минимально возможным вредом для здоровья. Как долго необходимо проводить лечение, будет зависеть от индивидуальных особенностей пациента.
Способ введения препаратов может быть различным:
- внутривенным (с постоянным катетером и без);
- пероральным (таблетки, капсулы);
- в виде подкожных или внутримышечных инъекций (редко, поскольку возможен некроз тканей в месте инъекции).
В особую категорию стоит выделить способ лечения, получивший название гипертермическая интраперитонеальная химиотерапия (ГИПХ, HIPEC). Она применяется для терапии некоторых новообразований органов брюшной полости; состоит из нескольких этапов. Первый - хирургическое удаление опухоли. Затем при помощи специального прибора в брюшную полость вводят подогретый до 42-43 градусов раствор химиопрепарата. Через некоторое время его откачивают и рану зашивают.
Расчет дозы при химиотерапии
Дозу химиопрепаратов обычно рассчитывают не на массу тела, а на его поверхность. Имеют значение возраст, тип заболевания, необходимость комбинирования с другими методами лечения и/или лекарствами.
При последовательной высокодозной химиотерапии (секвенс) больному назначают 2-4 препарата в максимальной дозировке. Каждый из них пропивается отдельным курсом. Высокодозную химиотерапию применяют при онкологических заболеваниях крови, в случае рецидива или отсутствия положительной реакции на ранее применяемые химиотерапевтические препараты.
Побочные действия после химиотерапии
Почему химиотерапия так плохо переносится? Раковая клетка обладает способностью к быстрому делению. Это одно из свойств, которое отличает ее от нормальных и делают особо уязвимой для химиопрепаратов. Лекарства не различают здоровые и мутировавшие клетки. Из-за этого помимо раковых страдают и нормальные ткани, в особенности те, клетки которых в норме быстро делятся (пищеварительный тракт, кровь, волосяные фолликулы, кожа). Поэтому основные побочные эффекты связаны с этими системами:
- усталость;
- тошнота, потеря аппетита;
- выпадение волос;
- анемия;
- подверженность инфекционным заболеваниям;
- повышенная кровоточивость;
- проблемы с памятью и концентрацией;
- понос или запор;
- стоматит;
- потеря сексуального влечения;
- бесплодие.
Щадящая химиотерапия оказывает минимальное влияние на здоровые клетки, но все же большинство пациентов испытывают те или иные из них. Основываясь на свойствах химиопрепаратов врач способен предположить наиболее вероятные побочные эффекты. Основываясь на этой информации он назначает поддерживающие лечение и дополнительные, которые существенно улучшают качество жизни.
Восстановление после химиотерапии
Реабилитация после химиотерапии может занять некоторое время. Ее продолжительность будет зависеть от типа препаратов, их дозы, общего состояния здоровья и индивидуальной переносимости лечения. Она может включать:
- диету;
- физические упражнения;
- психологическую поддержку;
- занятия, помогающие снизить стресс (медитация, дыхательная гимнастика).
Некоторые люди чувствуют себя истощенными. Если они работают, то им рекомендуется перейти на частичную занятость или взять больничный. Дополнительно необходимо периодически сдавать анализы, помогающие оценить своё общее состояние.
Сколько живут после химиотерапии?
Химиотерапия при онкологии может помочь победить рак или значительно улучшить качество и продолжительность жизни. Результат лечения будет зависеть прежде всего от вида опухоли, стадии рака, общего состояния здоровья человека и его возраста. Поэтому прогноз необходимо обсуждать со своим лечащим врачом.
Об этапах создания противоопухолевых препаратов

Еще во времена, когда онкологические заболевания диагностировались на последней, терминальной стадии, предпринимались попытки их лечения. Использовались средства с натуральным составом и токсичными химическими веществами. В относительно недавно обнаруженном папирусе, датированном 1500 годом до н. э., описывались способы уменьшить размеры злокачественного образования с помощью соединений мышьяка. После создания современных препаратов рак перестал считаться неизлечимой патологией. Купить в аптеке противоопухолевые препараты можно в любое время.
Об истоках развития химиотерапии
Парацельс и другие врачеватели древних времен предпринимали попытки лечить опухоли, поражающие кожу или внутренние органы. Но из-за их эмпирического характера успехом они не увенчались. Ведь в основе методов лечения был только жизненный опыт, наблюдение за развитием патологии, эффективностью применяемых средств, а не научные теории, результаты доклинических исследований.
П. Эрлих, считающийся основоположником химиотерапии, впервые употребивший этот термин в своих трудах, придавал ей совершенно иной смысл. Так он обозначал комплексную терапию химическими веществами болезней, спровоцированных паразитами. Под ними он понимал не только гельминты, но и патогенные и условно-патогенные грибки, бактерии, простейшие, вирусы. То есть изначально термином «химиотерапия» обозначалось лечение любой патологии, вызванной внедрением в организм человека инфекционных возбудителей, червей-паразитов.
Несколько позже так стали называть и терапию онкологических заболеваний. В свое время П. Эрлих предложил выполнять систематический скрининг химических соединений для выявления у них свойств, полезных для остановки роста опухоли с дальнейшим уменьшением ее в размерах. И уже на основе его результатов разрабатывать методики использования химиотерапевтических средств в клинической практике.
Историческая справка

История противоопухолевой химиотерапии как раздела медицины, включающего разработку и исследования новейших фармакологических препаратов, сравнительно короткая. Это объясняется, в том числе и относительно недавней возможностью правильно диагностировать онкологические заболевания, отслеживать динамику проводимого лечения. До 40-х годов прошлого века противоопухолевая активность была обнаружена у небольшой группы органических и неорганических соединений. Способность замедлять деление генетически измененных клеток исследователи выявили у таких веществ:
определенных соединений мышьяка;
алкалоида колхицина и других митотических ядов.
Немецкий биохимик О. Варбург, лауреат Нобелевской премии в области физиологии и медицины 1931 года, подстегнул интерес к разработке противоопухолевых препаратов. Этот выдающийся ученый двадцатого века совершил прорыв в области цитологии. В процессе изучения опухолевых и нормальных тканей он обнаружил их существенные различия. Результаты этих исследований в последующем были взяты за основу не только при создании лекарственных средств, но и при разработке лабораторной диагностики рака.
О первых эффективных противоопухолевых средствах
Первые успешные попытки лечения онкологических патологий с помощью химиотерапевтических препаратов отмечены в 40-х годах прошлого века. Предпосылки к ним гуманными назвать нельзя. Все началось с изучения влияния на организм человека отравляющих веществ, которые использовались во время боевых действий. Это иприт и его азотистое производное — трихлорэтиламин. О том, что последний способен провоцировать быстрое развитие лейкопении и аплазии костного мозга, было известно еще в начале 20-го века.
В ходе дальнейшего проведения исследований были выявлены и полезные свойства трихлорэтиламина. В тщательно подобранных дозах он тормозит деление злокачественных клеток лимфоидных тканей. На начальном этапе противоопухолевая активность химического вещества тестировалась на мышах с лимфосаркомой. Вскоре она была подтверждена и результатами клинического исследования с привлечением добровольцев.
На основе трихлорэтиламина создавались разнообразные противоопухолевые средства. Например, выраженную цитостатическую активность проявляли его производные — бис- амины. Они постепенно усовершенствовались, в том числе уменьшалась их токсичность к неизмененным клеткам человеческого организма.
История современных противоопухолевых препаратов

Скидка на противоопухолевые препараты предлагается в нашей аптеке. Эффективность химиотерапии значительно повысилась после синтезирования и успешной апробации этилениминов, алкилированных сульфонатов, триазунов. А вскоре были созданы первые антиметаболиты, в основе механизма действия которых лежит ингибирование определенных биохимических процессов. Их торможение отрицательно сказывается на митозе мутировавших клеток. Эти препараты по структуре напоминают фолиевую кислоту, но их действие более мощное.
Первый представитель клинико-фармакологической группы антиметаболитов — Метотрексат — до сих пор востребован в онкологической практике. Лечению им хорошо поддаются многие виды рака, но особенно хориокарционама, лейкемия в острой форме. Вскоре группа антиметаболитов пополнилась аналогами пурина (Меркаптопурином, Тиогуанином), пиримидина (Фторурацилом, Цитарабином).
В дальнейшем для лечения рака начали применяться антибиотики как противоопухолевые средства — Адриамицин, Дактиномицин, а также средства с растительным активным составом — Винбластин, Винкристин. Прорывом в химиотерапии стало синтезирование препаратов на основе платины. В химиотерапии гормональнозависимых новообразований востребованы эстрогенные, андрогенные и гестагенные средства, антагонисты эстрогенов (Тамоксифен) и андрогенов (Флутамид). Поиск противоопухолевых препаратов по нашему каталогу интуитивно понятен и не занимает много времени.
Читайте также:
