Как сделать блокаду подбородочного нерва
Добавил пользователь Алексей Ф. Обновлено: 22.01.2026
Лечебная блокада при остеохондрозе - самый эффективный и безопасный способ обезболивания. Инъекцию с анестетиком делают непосредственно в очаг боли. В результате интенсивность болевого синдрома быстро снижается, и постепенно болезненность в области пораженного позвонка проходит совсем.
Эффект от блокады непродолжительный, поэтому ее проводят курсами - от 2 до 15 уколов. После такого лечения пациент быстро возвращается к работе и привычной деятельности, к тому же качество жизни пациента значительно улучшается.
Самая распространенная причина обращения к врачу (80 %) - боль в спине. По статистике, каждый четвертый взрослый житель планеты страдает от периодического появления болевого синдрома, а около 90 % хотя бы один раз в жизни испытывали эпизод длительной боли. При чем остеохондроз выявляли у 50 % обратившихся.
Это заболевание характеризуется развитием дегенеративно-деструктивных изменений в межпозвонковом диске и деформацией близлежащих позвонков. В начальной стадии происходит постепенная деформация хрящевой ткани диска, его обезвоживание и разделение на волокна. В результате он становится более тонким, теряет упругость и перестает выполнять амортизационные функции. При этом расстояние между позвонками сужается. Но на этой стадии болевых ощущений пока не возникает.
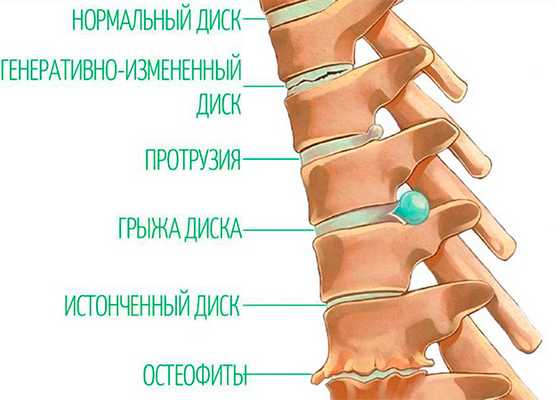
Со временем происходят следующие изменения:
- деформация диска приводит к появлению протрузий - образованию выпуклости (выпиранию студенистой сердцевины);
- со временем внешняя оболочка диска прорывается и формируется межпозвонковая грыжа;
- позвонок утолщается, на нем появляются остеофиты - костные наросты, сначала их немного, но по мере прогрессирования болезни их количество значительно увеличивается;
- форма позвонка меняется, он теряет высоту или становится конусообразным (в зависимости от отдела позвоночника, в котором находятся поврежденные позвонки).
Боли при остеохондрозе возникают на стадии необратимых изменений в хрящевой и костной ткани позвоночного столба. Деформация приводит к компрессии нервных корешков остеофитами или межпозвонковой грыжей. В результате происходит раздражение болевых рецепторов и возникновение болевого импульса.
Блокада нижнего альвеолярного нерва
Блокада нижнего альвеолярного нерва, так же именуемая, мандибулярной анестезией, является наиболее часто используемой (после инфильтрации) и, возможно, самой сложной инъекционной методикой в стоматологии. К сожалению, она также оказывается и с самым высоким процентом клинических неудач даже при правильном применении.
Это особенно полезная техника для обезболивания квадранта. Дополнительная блокада (щечного нерва) необходима только тогда, когда необходимо обезболить мягкие ткани щеки. В редких случаях может потребоваться супрапериостальная инъекция (инфильтрация) в область нижнего резца для коррекции частичной анестезии, вызванной перекрытием чувствительных волокон с контралатеральной стороны. Интралигаментарная анестезия может стать необходимой, когда изолированные участки зубов нижней челюсти (обычно мезиальный корень первого моляра) остаются чувствительными после успешного выполнения мандибулярной анестезии. Внутрикостная анестезия является дополнительной техникой, обычно используемой на молярах, когда проводниковая анестезия оказалась неэффективной, в первую очередь, в зубах с необратимым пульпитом.
В последующем описании блокады нижнечелюстного альвеолярного нерва отмечается, что место инъекции немного выше, чем это обычно изображается.
Эффективность радиочастотной денервации позвоночных сегментов
Методика радиочастотной деструкции фасеточных нервов является высокоэффективной и безопасной. Это подтверждается так же материалами многочисленных «клиник боли», в которых данный метод является основным в лечении хронической вертеброгенной боли.
Актуальность
Боль в спине - это не только страдания людей, но и большие социально-экономические потери. Согласно данным эпидемиологических исследований, проведенных в странах с развитой экономикой и медициной, более 70 % пациентов на первичном приёме жалуются на недомогание, связанное с заболеванием позвоночника. Это вызвано широкой распространённостью патологических состояний позвоночника, именуемых врачами как остеохондроз, спондилоартроз, спондилез и др. В последние десятилетия у врачей различных специальностей значительно вырос интерес к проблемам вертеброгенной боли, методам её изучения, способам профилактики и лечения. С одной стороны разработка новых инструментов, имплантов, методов хирургической коррекции патологически измененного позвоночника позволяет хирургии находится на вершине технического прогресса, а с другой - вертебролог сегодня сталкивается с проблемой выбора оптимального для пациента метода хирургического лечения [2,3].
Оперативное вмешательство по поводу вертеброгенной боли в настоящее время почти исключительно сводится к спондилодезу. Однако, в декабре 2001 года Шведская научная группа по изучению поясничных болей (Swedish Lumbar Spin study Group) опубликовала результаты проспективного рандомизированного исследования. Было обследовано 294 пациента с хроническими болями дегенеративной этиологии, исключая случаи специфических рентгенологических диагнозов, таких как спондилолистез. В этом исследовании было обнаружено, что у пациентов получавших оперативное лечение в виде спондилодеза, через 2 года после операции функциональная оценка была ниже, а болевая - выше, чем у неоперированных пациентов. В свете этого встаёт вопрос о целесообразности проведения объёмных оперативных вмешательств пациентам с вертеброгенной болью [2].
За прошедшие годы был предложен ряд малоинвазивных методов лечения спондилогенного болевого синдрома путём разрушения нервной ткани, в том числе, метод радиочастотной денервации (РЧД). Этот метод в настоящее время является альтернативой травматичным медицинским вмешательствам на шейном, грудном и поясничном отделах позвоночника при возникновении у пациентов вертеброгенной боли и неэффективности консервативной терапии.
Материалы и методы
Под нашим наблюдением находились 245 пациентов ( 150 женщин и 95 мужчин ) в возрасте от 21 до 69 лет (средний возраст - 54,3 года). Поводом для обращения к врачу являлись жалобы на боли в шейном ( 18 больных), грудном ( 19 больных ) и поясничном ( 208 больных ) отделах позвоночника.
Всем больным проводилось лучевое обследование, включающее рентгенографию позвоночника в двух проекциях (при боли в шее и поясничной боли дополнительно проводились функциональные пробы), в сомнительных случаях для исключения диско - радикулярного конфликта назначалась МРТ или КТ пораженного отдела. На рентгенограммах в случае дегенеративных изменений межпозвонковых дисков и суставов выявлялся субхондральный склероз замыкательных пластин позвонков, снижение высоты межпозвонкового промежутка, склерозирование и деформация суставных поверхностей, нарушение их конгруэнтности, возможно развитие унко-вертебрального артроза [4], (рис. 1).
Оценка интенсивности болевого синдрома проводилась при помощи карты болевого аудита, максимальный уровень боли в которой соответствует 100 баллам.
Также пациентам проводилось исследование биомеханики шейного и поясничного отделов позвоночника при помощи трёхмерного анализатора движений Zebris 3-D Motion Analyzer (Zebris medizintechnik, Германия) (рис. 2). У пациентов было обнаружено нарушение биомеханики шейного и поясничного отделов позвоночника, что выражалось в ограничении разгибания и асимметрии амплитуды наклонных и ротационных движений.
На основании клинического и рентгенологического обследования в этих группах больных было установлено, что причиной болевого синдрома являлись дегенеративные изменения в фасеточных (дугоотросчатых) суставах, т.е. диагноз формулировался как спондилоартроз определенных сегментов (в шейном отделе чаще были поражены сегменты от С3 до С6 (97%), в грудном отделе - от Тh5 до Тh12 (96 %), в поясничном отделе - сегменты L3-4, L4-5, L5-S1 (97%). Уменьшение или полное купирование болевого синдрома после параартикулярной диагностической блокады 2% раствором лидокаина на уровне поражения позволило окончательно установить, что боль исходит из компрометированного сустава.
Учитывая тот факт, что не все клиницисты признают роль патологии межпозвонковых суставов в генезе боли в спине, следует более подробно остановиться на клинике «фасет - синдрома». Часто начало боли связано с разгибанием и ротацией позвоночника и другими торзионными перегрузками. У всех пациентов в группе с заболеванием шейного отдела позвоночника отмечается боль (иногда очень выраженная) и ограничение движений. Боль зачастую иррадиирует в надплечье, плечевой сустав, плечо. В отличие от корешковой боли, вызванной компрессией соответствующего нерва грыжей диска, боль не должна локализоваться в предплечье и пальцах кисти. Осматривая пациента, обращает на себя внимание вынужденное положение головы, асимметрия надплечий, напряжение паравертебральных и мышц воротниковой зоны с одной или двух сторон. Как правило, ограничены движения в шейном отделе позвоночника, особенно разгибание и ротация головы. При изолированном поражении межпозвонковых суставов врач не найдет патологических изменений в рефлекторной и чувствительной сфере на верхних конечностях. Исходящая отраженная боль из фасеточных суставов грудного и поясничного отделов позвоночника носит латерализованный, диффузный, трудно локализуемый, склеротомный характер распространения и, как правило, не спускается ниже колена. Она ограничивается грудной или пояснично-крестцовой областью над соответствующим дугоотросчатым суставом, иррадиирует в ягодичную область и верхнюю часть бедра (при поясничной локализации). Фасеточная боль может быть более или менее схваткообразной, усиливаться при длительном стоянии, разгибании, особенно если оно сочетается с наклоном или ротацией в больную сторону, при перемене положения тела из лежачего в сидячее и наоборот. Характерно появление кратковременной утренней скованности и нарастание болевых ощущений к концу дня. Разгрузка позвоночника - легкое его сгибание, принятие сидячего положения, использование опоры (стойка, перила) - уменьшает боль. При физикальном исследовании можно выявить сглаженность поясничного лордоза, ротацию или искривление позвоночника в грудном, грудо-поясничном или пояснично-крестцовом отделах, напряжение паравертебральных мышц и/или квадратной мышцы спины на больной стороне, мышц подколенной ямки, ротаторов бедра. Характерна локальная болезненность при пальпации фасеточного сустава. Как правило, не бывает каких-либо неврологических чувствительных, двигательных и рефлекторных расстройств. Не характерны и симптомы «натяжения» нервных корешков, ограничение движений как таковых. Иногда, в хронических случаях выявляется некоторая слабость выпрямителей позвоночника и мышц подколенной ямки. Боль от сустава L5-S1 отражается в область копчика, тазобедренного сустава, задней поверхности бедра, иногда - в паховую область. Раздражение сустава L4-5 характеризуется болью, иррадиирующей от места раздражения в ягодицу, заднюю поверхность бедра и тазобедренного сустава и, лишь изредка, в копчик. От сустава L3-4 боль распространяется в грудную область, боковую поверхность живота, пах, достигает передней поверхности бедра и очень редко - копчика и промежности. Раздражение фасеточных суставов более высокого уровня (Th12-L1, L1-2, L2-3) ограничивается появлением болезненных ощущений в верхних отделах спины и живота, грудном и даже в шейном отделах. Боль от суставов Тh3-4-5 часто иррадиирует в межлопаточную, подлопаточную область [1,4].
Всем больным проводилось консервативное лечение в амбулаторных условиях. В терапевтический комплекс включалось медикаментозное лечение (нестероидные противовоспалительные препараты, витаминотерапия, биостимуляторы и т.д.), параартикулярные блокады - с диагностической и лечебной целью (с обязательным введением стероидоных препаратов - дипроспан 1,0 мл), физиотерапия, массаж, корсетотерапия, психотерапия. При недостаточной эффективности консервативной терапии или кратковременности эффекта больным была выполнена радиочастотная деструкция фасеточных нервов. Учитывая особенности клинических проявлений дегенерации межпозвонковых суставов, нами были определены следующие показания для изолированной радиочастотной деструкции фасеточных нервов: длительная боль в шейном/грудном/поясничном отделе позвоночника (более 6 месяцев); обострение боли в позвоночнике после разгибания и ротации головы/туловища, длительного фиксированного положения головы/туловища (например, работы на компьютере); усиление боли в позвоночнике при глубокой пальпации суставов; отсутствие признаков компрессии корешков (неврологического дефицита); отсутствие улучшения после физиотерапии; значительное уменьшение боли в шее/пояснице после параартикулярной блокады на одном или нескольких уровнях; соответствие клиники рентгенологическим находкам (спондилоартроз); интенсивность боли по шкале болевого аудита более 15 баллов.
Также нами были определены общие противопоказания для выполнения РЧД: зависимость от наркотических и седативных препаратов, алкоголя, наличие социальных и психологических факторов, определяющих восприятие боли, возрасте моложе 18 и старше 80 лет, перенесенные ранее операции на позвоночнике, расстройства спинального кровообращения в анамнезе [2].
Манипуляция выполнялась в условиях операционной. В положении больного на животе при РЧД на грудном и поясничном уровнях и на спине при выполнении РЧД на шейном уровне, под местной анестезией раствором новокаина 0,5% - 10,0 мл под контролем электронно-оптического преобразователя производилась пункция параартикулярной области в зоне нахождения нервов, идущих к суставной капсуле. Как правило, одномоментно проводили пункцию на трех - четырех уровнях (рис. 3). Положение иглы контролировалось в двух проекциях (рис. 4).
Затем, для идентификации корректного положения иглы, с помощью радиочастотного генератора Stryker Interventional spine MultiGen RF Console (рис. 5) или генератора RFG-3C PLUS фирмы RADIONICS проводилась электростимуляция фасеточных нервов с частотой 50 Гц. Пациент должен был испытывать ощущения покалывания в области соответствующего фасеточного сустава в диапазоне между 0,4 и 0,6 В. Далее частоту снижали до 2 Гц и наблюдали мышечные сокращения в конечностях, отсутствие которых указывало на корректное положение электрода. С целью анестезии в зону предполагаемой деструкции вводилось 0,5 % раствора новокаина (не более 2,0 мл) и осуществлялась собственно радиочастотная деструкция.
Больные манипуляцию переносили хорошо. В течение тридцати минут после денервации они соблюдали постельный режим, в это время проводилась противовоспалительная терапия (ксефокам 8 мг в/м). Затем больным разрешалось вставать. Пациенты выписывались под амбулаторное наблюдение невролога в этот же день. На амбулаторном этапе проводилось восстановительное лечение (лечебная гимнастика верхних и нижних конечностей), противовоспалительная терапия. В течение 4-6 недель рекомендовалось исключение тяжёлых физических и спортивных нагрузок. Больным рекомендовалось приступить к работе через 7 - 14 дней после манипуляции.
Результаты лечения пациентов методом радиочастотной денервации сравнивались с результатами консервативного лечения пациентов со спондилоартрозом позвоночника. В данную группу входило 106 пациентов (64 женщины и 42 мужчины) в возрасте от 24 до 65 лет. 8 пациентам проводилось лечение по поводу болей в шейном отделе, 9 - в грудном, 89 - в поясничном отделе позвоночника. В комплекс консервативного лечения входило применение медикаментозных препаратов: НПВС (диклофенак, мелоксикам, лорноксикам), мышечные релаксанты (мидокалм), антидепрессанты, витамины. Всем пациентом проводилось физиотерапевтическое лечение, ЛФК, массаж.
Результаты
Мы не отметили никаких осложнений ни во время операции, ни в раннем, ни в позднем послеоперационном периодах. После радиочастотной деструкции в течение 1-2 недель в 79 % случаев пациенты на фоне значительного уменьшения интенсивности болевого синдрома продолжали жаловаться на чувство тяжести в зоне манипуляции. Через 3-6 недель это чувство исчезало.
Эффект от денервации мы оценивали перед выпиской больного на работу, через 1 месяц, 6 месяцев, 1 год и 1,5 года с момента РЧД.
Результаты манипуляции были разделены на три группы: хороший - отсутствие боли, удовлетворительный - отсутствие боли в покое, значительное снижение её интенсивности при движениях, отсутствие необходимости приема анальгетиков и неудовлетворительный - сохранение интенсивности болевого синдрома на прежнем уровне.
При оценке результатов в ранний срок после манипуляции во всех случаях было отмечено уменьшение болевого синдрома, в среднем, на 36 баллов по шкале болевого аудита как в соответствующем отделе позвоночника, так и в конечностях. Через месяц хороший исход заболевания был отмечен у 101 (41 %), удовлетворительный - у 137 (56 %), неудовлетворительный - у 7 (3 %) пациентов. Таким образом, через месяц после манипуляции улучшение состояния наступило у 97 % больных. Через 6 месяцев распределение исходов заболевания осталось примерно таким же. Через год проведен анализ результатов лечения у 195 больных: хороший исход отмечен у 62 (32 %), удовлетворительный - у 117 (60 %), неудовлетворительный - у 16 (8 %) пациентов. Положительные результаты сохранились у 92 % больных, хотя снизилась доля хороших и увеличилась доля удовлетворительных оценок. Через 1.5 года мы наблюдали 180 больных, у 143 из них боли возобновились практически с прежней интенсивностью.
По шкале оценки боли установлено, что до операции интенсивность болевых ощущений составляла 47,1 ± 6,9 балла, через 3 дня - 11,4 ± 3,5 балла, через 1 месяц - 6,9 ± 4,1 балла, через 6 месяцев - 7,7 ± 3,8 балла, через 1 год - 8,5 ± 4,3 балла, через 1,5 года - 37,7 ± 3,3 балла. По всей видимости, произошла реинервация позвоночных сегментов и в эти сроки возможно повторение радиочастотной деструкции. Повторно манипуляция была выполнена 47 пациентам с выраженным положительным эффектом.
В свою очередь, в группе контроля до проведения консервативной терапии интенсивность боли составляла 46,3 ± 5,3 балла, по окончании лечения - 21,7 ± 4,2 балла, через 6 месяцев - 39,5 ± 3,2 балла, через 1 год - 45,4 ± 5,6 балла (рис. 6).
Таким образом, очевидным является не только более высокая по сравнению с консервативной терапией эффективность РЧД, но и более длительный период ремиссии после выполнения процедуры.
Исследование биомеханики шейного и поясничного отделов позвоночника до и через месяц после операции показало, что в значительной степени увеличивается амплитуда и скорость движений в позвоночных сегментах.
Заключение
Наш опыт показывает, что методика радиочастотной деструкции фасеточных нервов является высокоэффективной и безопасной. Это подтверждается так же материалами многочисленных «клиник боли», в которых данный метод является основным в лечении хронической вертеброгенной боли. Главными преимуществами радиочастотной денервации являются: контролируемый размер деструкции; контроль термического воздействия за счет постоянного мониторинга нагревания и электрического сопротивления тканей на конце иглы; подтверждение правильности расположения иглы методом электростимуляции; проведение манипуляции под местной анестезией в амбулаторных условиях; короткий восстановительный период после проведения денервации; низкая частота осложнений; возможность повторного проведения деструкции.
Радиочастотную денервацию можно рассматривать как паллиативное лечение, но стойкость ее эффекта, возможность проведения повторных операций делает ее привлекательной как для врачей, так и для пациентов. Данный метод является эффективным при лечении вертеброгенной боли, локализованной в одном дерматоме, когда последняя не поддаётся консервативному лечению. РЧД - это весьма привлекательное дополнение к комплексной консервативной терапии, позволяющее улучшить исходы заболевания и продлить стойкость эффекта. Любая «радикальная» операция подразумевает длительное оперативное вмешательство, фиксацию позвоночных сегментов (т.е. нарушение биомеханики позвоночника), возможность интра- и послеоперационных осложнений, высокую стоимость лечения. Радиочастотная же деструкция выгодно отличается от всех известных неинвазивных методов своей высокой эффективностью, а от инвазивных - подкупающей безопасностью.
Несомненно, радиочастотная денервация позвоночных сегментов при лечении вертеброгенного болевого синдрома имеет большое будущее и требует дополнительных исследований для определения наиболее продуктивного сочетания с другими методиками консервативного лечения [5].
Литература
Назаренко Г.И., Черкашов А.М., Кузьмин В.И., Назаренко А.Г., Горохов М.А., Шарамко Т.Г.
Статья опубликована в журнале Вестник травматологии и ортопедии им. Н.Н. Приорова, 2013.-N 2.-С.26-31.
Блокада подбородочного нерва
Такой способ блокады осуществляют при операциях на нижней губе, подбородке и резцовых зубах. Положение подбородочного отверстия у лошади, через которое выходит одноименный нерв, устанавливают путем пальпации через кожу приблизительно на два пальца ниже угла рта, предварительно сместив вверх сухожилие опускателя нижней губы, частично прикрывающее отверстие. Через иглу, введенную под углом спереди назад с таким расчетом, чтобы конец ее проник к верхнему контуру отверстия, впрыскивают 5 мл 3% раствора новокаина. Обезболивание распространяется на зону нижней губы (кожа и слизистая) и подбородка, кроме десен и резцов, которые иннервирует лежащий глубоко в костном канале луночковый резцовый нерв. Для блокады последнего (при зубных операциях) иглу продвигают через подбородочное отверстие в направлении спереди назади внутрь в канал на глубину 1,5 см и инъицируют дополнительно 5—10 мл раствора. При глубоком проникании раствора в канал можно получить и анестезию премоляров.
У крупного рогатого скота отверстие лежит на ширину пальца ниже угла рта; в остальном техника операции такая же, как и у лошади.
У собак отверстие прощупывают со стороны слизистой оболочки преддверия рта, после отведения пальцем губы вниз, на уровне второго пре-моляра. На инъекцию требуется 1,5—2 мл раствора новокаина (рис. 132).
Блокада подглазничного нерва
Блокада подглазничного нерва необходима при операциях на спинке носа, верхней губе, носовом дивертикуле, ноздре и резцовых аубах.
Концевые ветви подглазничного нерва—наружный и передний носовые и верхний губной нервы (при операциях в носогубной области)—блокируют раствором новокаина непосредственно у подглазничного отверстия. Это отверстие находят у лошади вблизи пункта пересечения двух линий: первой, идущей от внутреннего угла глаза параллельно скуловому гребню, и второй—перпендикулярной к первой, проецируемой от конца того же гребня (рис. 132). Мускул, покрывающий отверстие, отводят вверх; иглу продвигают спереди назад, по направлению к отверстию, до кости. Трехпроцентного раствора новокаина инъицируют 5—10 мл.
У крупного рогатого скота анестезию производят так же, как и у лошади. Подглазничное отверстие отыскивают в точке пересечения линии, проходящей от наружного угла орбиты параллельно спинке носа, и перпендикуляра к этой линии от переднего края первого премоляра верхней челюсти.
У собак подглазничное отверстие легко обнаруживают, предварительно отодвинув вверх подниматель верхней губы, под кожей на уровне третьего коренного зуба, в форме щели.
При операциях на резцах, премолярах и окружающей их десне приходится блокировать, кроме концевых ветвей подглазничного нерва, и верхний резцовый нерв. С этой целью иглу вводят на глубину 3—4 см через подглазничное отверстие в канал, т. е. до места отхождения верхнего резцового нерва от подглазничного. Во избежание повреждения сосудов и нерва иглу продвигают вдоль нижней стенки подглазничного канала. Доза на инъекцию составляет 10 мл 3% раствора новокаина (во время инъекции прижимают ткани в области отверстия пальцами, чтобы жидкость не вытекала за пределы канала). У собак проникают иглой в подглазничный канал на глубину 1—2 см со стороны слизистой оболочки преддверия рта, приподняв верхнюю губу животного, и инъицируют 3—5 мл 2% раствора новокаина.
Обезболивание в области щечного нерва
При широко открытом рте больного вкол иглы делают в слизистую оболочку щеки, направляя шприц с противоположной стороны. Местом вкола является точка, образованная пересечением горизонтальной линии, проведенной на уровне жевательной поверхности верхних больших коренных зубов и вертикальной линии, являющейся проекцией переднего края венечного отростка на слизистую оболочку щеки. Иглу продвигают на глубину 1 — 1,5 см до переднего края венечного отростка, где щечный нерв пересекает его, выходя из крыловидно-височного клеточного промежутка или из толщи височной мышцы, и располагается по наружной поверхности щечной мышцы. Вводят 1—2 мл раствора анестетика.
Обезболивание в области язычного нерва
Язычный нерв блокируют при проведении; анестезии у отверстия нижней челюсти и на нижнечелюстном валике. Кроме того, на него можно воздействовать в челюстно-язычном желобке. Техника проведения. Для этого язык отводят шпателем в противоположную сторону, Вкол иглы делают в слизистую оболочку в наиболее глубокой части челюстно-язычного желобка на уровне середины коронки третьего нижнего большого коренного зуба. В этом месте язычный нерв залегает очень поверхностно. Вводят анестетик.
Обезболивание в области подбородочного нерва
Подбородочный нерв и резцовая ветвь нижнего луночкового нерва являются его конечными ветвями, на которые он разделяется после подбородочного отверстия. Подбородочный нерв выходит из подбородочного отверстия и, разветвляясь на более мелкие ветви, заканчивается в слизистой щеки, десне, коже подбородка и нижней губы. Резцовая ветвь проходит в губчатом слое кости к фронтальной группе зубов, иннервируя эти зубы, периодонт, кость, надкостницу в области подбородка с соответствующей стороны.
Показанием к использованию блокады подбородочного нерва являются вмешательства на мягких тканях нижней губы (биопсия, наложение швов и т.д.)
Для проведения анестезии в области резцов нижней челюсти следует проводить её и с противоположной стороны инфильтрационным способом. У пожилых пациентов из-за выраженного склероза костных отверстий эффективность инфильтрационной анестезии значительно снижена.
Для выполнения анестезии необходимо определить расположение подбородочного отверстия. Оно располагается на уровне верхушек корней клыков и премоляров. Чаще всего оно находится на уровне середины альвеолы нижнего второго малого коренного зуба или межальвеолярной перегородки между вторым и первым малыми коренными зубами и на 12—13 мм выше основания тела нижней челюсти. Более точное расположение можно определить по рентгенограмме или при пальпации альвеолярного отростка нижней челюсти указательным пальцем, в области верхушек корней премоляров определяется характерная неровность.
Существуют внеротовой и внутриротовой способы блокады подбородочного нерва.
Внеротовой метод. Этот метод широко проводился ранее вследствие малой эффективности анестетиков и необходимостью в связи с этим введения иглы и анестетика в канал.
При проведении анестезии на правой половине нижней челюсти врач располагается справа и сзади больного, а на левой половине - справа и кпереди от больного.
Указательным пальцем прижимают на коже точку проекции подбородочного отверстия, затем делают вкол на 5 мм выше и кзади от его проекции. Продвигают её до соприкосновения с костью и вводят анестетик, затем находят подбородочное отверстие и продвигают иглу в канал на глубину 3-5 мм и вводят основную часть раствора. Через 5 мин наступает анестезия.
Блокада двигательных волокон нижнечелюстного нерва
Показание к применению:
- наличие воспалительной контрактуры нижней челюсти в сроки до 10 дней после развития
По Берше - выключение жевательного нерва.
Вкол иглы делают перпендикулярно кожным покровам под нижний край скуловой дуги, отступя кпереди от козелка ушной раковины на 2 см. Иглу продвигают горизонтально к средней линии на глубину 2—2,5 см через вырезку нижней челюсти. Вводят раствор анестетика. Через 5-10 мин определяется эффект анестезии. Выражается он в расслаблении мышц, поднимающих нижнюю челюсть.
По П. М. Егорову - позволяет блокировать не только жевательный нерв, но и остальные двигательные ветви нижнечелюстного нерва.
Депо из раствора анестетика создается на уровне основания переднего ската суставного бугорка у наружной поверхности подвисочного гребня, что позволяет инфильтрировать клетчатку крыловидно-височного, крыловидно-нижнечелюстного пространств и подвисочной ямки. Это технически достаточно сложный способ анестезии, требующий соответствующих мануальных навыков.
Читайте также:
