Клиника отравления глифозатом-сурфактантом (Roundup)
Добавил пользователь Morpheus Обновлено: 21.01.2026
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Сурфактант-БЛ
Лиофилизат для приготовления эмульсии для ингаляционного введения в виде спрессованной в таблетку массы или порошка белого или белого с желтоватым оттенком цвета, приготовленная эмульсия белого с кремоватым или белого с желтоватым оттенком цвета, однородная, в которой не должны наблюдаться хлопья или твердые частицы.
| 1 фл. | |
| сурфактант | 25 мг |
Флаконы стеклянные вместимостью 10 мл (2) - пачки картонные (5) - коробки картонные с вкладышем.
Фармакологическое действие
Высокоочищенный природный сурфактант, полученный из крупного рогатого скота.
Комплекс веществ из смеси фосфолипидов и сурфактант-ассоциированных белков; снижает поверхностное натяжение легочных альвеол, предотвращая их коллапс и развитие ателектазов. Восстанавливает содержание фосфолипидов на поверхности альвеолярного эпителия, стимулирует вовлечение в дыхание дополнительных участков легочной паренхимы; способствует удалению вместе с мокротой токсических веществ из альвеолярного пространства. Повышает активность альвеолярных макрофагов и угнетает экспрессию и экскрецию цитокинов полиморфноядерными лейкоцитами; стимулирует синтез эндогенного сурфактанта альвеолоцитами II типа и защищает альвеолярный эпителий от повреждений химическими и физическими агентами.
При ингаляционном введении не оказывает влияния на ССС, не оказывает местнораздражающего действия, не влияет на состав крови и кроветворение за исключением кратковременной (1 сут после прекращения введения препарата в дозах 200 и 400 мг/кг) лимфопении и агранулоцитоза за счет увеличения числа палочко- и сегментоядерных нейтрофилов. В дальнейшем состав периферической крови полностью нормализуется. Не влияет на биохимические параметры крови, мочи и свертывающую систему крови, не вызывает патологических изменений функций и структуры внутренних органов.
У недоношенных новорожденных с респираторным дистресс-синдромом эндотрахеальное введение препарата при ИВЛ улучшает газообмен в легочной ткани. Через 30-120 мин после введения уменьшаются признаки гипоксемии, повышается парциальное давление кислорода в артериальной крови и насыщение Hb кислородом, а также уменьшается гиперкапния (парциальное давление углекислого газа), что позволяет перейти на более физиологичные параметры ИВЛ (снизить токсические концентрации кислорода во вдыхаемой газовой смеси до 40%, а также уменьшить общую продолжительность аппаратного дыхания). Значительно снижает летальность и частоту осложнений у новорожденных с респираторным дистресс-синдромом.
Фармакокинетика
Через 6-8 ч после однократного интратрахеального введения концентрация сурфактанта в легких снижается и достигает исходной величины через 12 ч.
Препарат полностью утилизируется в легких и не кумулирует в организме.
Показания активных веществ препарата Сурфактант-БЛ
Респираторный дистресс-синдром новорожденных; синдром острого повреждения легких и респираторный дистресс-синдром у взрослых (в т.ч. на фоне множественной травмы, сепсиса, аспирации желудочного содержимого, эндогенной интоксикации, массивной кровопотери и множественных гемотрансфузий, применения АИК в ходе кардиохирургических операций, тяжелой пневмонии).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Респираторный дистресс-синдром новорожденных, находящихся на ИВЛ : эндотрахеально (распылением микроструйно через эндотрахеальную трубку и боковой адаптер) и ингаляционно (в виде аэрозоля с помощью бронхоальвеолярного небулайзера). Микроструйно вводят медленно - дозу 75 мг в объеме 2.5 мл в течение 60-90 мин, в виде аэрозоля через альвеолярный небулайзер - в той же дозе в течение 2-3 ч. Препарат вводят 1-2 раза в дозе 75 мг/кг в виде 3% эмульсии (30 мг в 1 мл 0.9% раствора натрия хлорида). В случае тяжелого респираторного дистрсс-синдрома (2-го типа, обусловленного смешанной этиологией - незрелость легких и наличие инфекций) - 100 мг/кг. Повторно препарат вводят с интервалом 6-10 ч, при необходимости - через несколько суток.
Правила приготовления эмульсии
Непосредственно перед введением 75 мг лиофилизированного порошка разводят 2.5 мл 0.9% раствора натрия хлорида д/и. Для этого вносят во флакон 2.5 мл теплого (36°С) 0.9% раствора натрия хлорида и дают флакону постоять 2-3 мин, затем суспензию осторожно перемешивают во флаконе, не встряхивая, набирают эмульсию в шприц тонкой иглой, выливают обратно во флакон по стенке несколько раз (4-5) до полного равномерного эмульгирования, избегая образования пены. Флакон нельзя встряхивать. После разведения образуется молочного цвета эмульсия, лишенная хлопьев или твердых частиц.
Новорожденного предварительно интубируют и непосредственно перед введением Сурфактанта-БЛ аспирируют мокроту из дыхательных путей и эндотрахельной трубки. Через адаптер с дополнительным боковым входом в трахею с помощью шприцевого насоса или капельно, в течение 60-90 мин, проводят инфузию приготовленного препарата. Для равномерного распределения сурфактанта по различным отделам легких, во время инфузии препарата ребенку, если позволяет тяжесть состояния, на несколько минут осторожно меняют положение тела: поворот на правый-левый бок, подъем головного конца. Заканчивают процедуру несколькими принудительными вдохами больного. Желательно не проводить санацию трахеи в течение нескольких часов после введения сурфактанта.
Аэрозольное введение осуществляют с помощью небулайзера, включенного в контур аппарата ИВЛ максимально близко к эндотрахеальной трубке для уменьшения потерь препарата. Желательно использовать аппараты, позволяющие подавать аэрозоль сурфактанта синхронно с вдохом. Для получения аэрозоля и введения препарата необходимо использовать только не УЗ-бронхоальвеолярные небулайзеры, т.к. сурфактант разрушается при обработке эмульсии УЗ.
Синдром острого повреждения легких и респираторного дистресс-синдрома взрослых : эндобронхиально, с помощью фибробронхоскопа, в дозе 12 мг/кг массы тела в сутки, разделенной на 2 введения по 6 мг/кг, выполняемых через 12-16 ч. Препарат вводится в виде 1.5% эмульсии (15 мг в 1 мл 0.9% раствора натрия хлорида).Может потребоваться многократное введение препарата (4-6 введений) до стойкого улучшения газообмена (до увеличения индекса оксигенации более 300 мм рт.ст.), рентгенологической картины и возможности проведения ИВЛ с FiO2 менее 40%.
В большинстве случаев продолжительность курса применения Сурфактанта-БЛ не превышает двух суток. У 10-20% пациентов назначение препарата не сопровождается нормализацией газообмена (особенно больных с выраженной полиорганной недостаточностью). Если в течение 2 дней не происходит улучшение оксигенации, введение препарата прекращают.
75 мг лиофилизированного порошка разводят так же, как для новорожденных, в 2.5 мл 0.9% раствора натрия хлорида. Полученную эмульсию разводят дополнительно 0.9% раствора натрия хлорида до 5 мл, получая 1.5% эмульсию препарата (15 мг в 1 мл 0.9% раствора натрия хлорида).
Эндобронхиальному введению препарата предшествует тщательная санационная бронхоскопия, проводимая по стандартной методике, в конце которой в каждое легкое вводится равное количество эмульсии препарата. Наилучший эффект достигается при введении эмульсии в каждый сегментарный бронх. Объем вводимой эмульсии определяется дозой препарата.
Интратрахеальная инстилляция показана в случае отсутствия возможности проведения бронхоскопии. Эмульсия готовится по описанному выше способу. До введения препарата необходимо провести тщательную санацию трахеобронхиального дерева, предварительно приняв меры для улучшения дренирования мокроты (вибромассаж, постуральная терапия, муколитики при отсутствии противопоказаний к их назначению). Эмульсию вводят через катетер, устанавливаемый в эндотрахеальную трубку так, чтобы конец катетера располагался ниже отверстия эндотрахеальной трубки, но обязательно выше киля трахеи. Эмульсию необходимо вводить в 2 приема (разделив дозу пополам), с интервалом 10 мин.
При туберкулезе (после подбора многокомпонентной антимикобактериальной терапии) - ингаляционно до или через 1.5-2 ч после приема пищи в дозе 25 мг 5 раз в неделю первые 2 нед, затем 3 раза в неделю в последующие 6 нед. Продолжительность курса - 8 нед, 28 ингаляций.
Побочное действие
Новорожденные: кратковременный рефлюкс (ретроградный выброс эмульсии препарата), который устраняется несколькими принудительными вдохами воздуха или кислородно-воздушной смеси (при использовании аэрозольного способа введения таких явлений не наблюдается); кровотечения в легких через 1-2 сут после введения у недоношенных детей с низкой массой тела при рождении; ретинопатия - при быстром и значительном повышении парциального напряжения кислорода в крови; кратковременная гиперемия кожных покровов (требует оценки адекватности параметров ИВЛ для исключения гиповентиляции вследствие транзиторной обструкции дыхательных путей).
Взрослые: специфических побочных эффектов не выявлено. При эндобронхиальном введении - ухудшение газообмена продолжительностью 10-60 мин, связанное с собственно процедурой бронхоскопии.
Противопоказания к применению
Внутрижелудочковые кровоизлияния III-IV ст. у новорожденных; пневмоторакс; пневмомедиастинум; интерстициальная эмфизема; нарушения газообмена, связанные с недостаточностью ЛЖ и бронхообструкцией.
Клиника отравления глифозатом-сурфактантом (Roundup)
1. Аллахвердиева А.И. Современные тренды инноваций средств реанимации // Международный журнал экспериментального образования. -2016 - № 3 (часть1) - С.40-41
2. Госенова Х.Я. Токсикологические аспекты «здорового питания» //Успехи современного естествознания. - 2014. - № 6 - С.87.
3. Доника А.Д. Чрезвычайные ситуации в проблемном поле текущего национального законодательства: медицинский аспект // Международный журнал экспериментального образования - 2015 - № 3-3 - С.295-296.
4. Доника А.Д. Использование методик оценки нервно-психической устойчивости для диагностики донозологического статуса в экстремальных условиях. - Успехи естественного естествознания . - 2015, - № 9 - С.45-49.
5. Кастури Р. Отравления грибами: этиология и симптомы //Успехи современного естествознания. - 2014. - № 6 - С.89.
6. Меркешкина Р.С. Экотоксиканты в проблемном поле токсикологии //Успехи современного естествознания. - 2014. - № 6 - С.91.
7. Полищук А.Е. Контаминация пищи как проблема безопасности питания //Успехи современного естествознания. - 2014. - № 6 - С.93.
8. Пуренкова М.С. Пестициды: токсикологическая угроза мирного времени// Международный студенческий вестник. - 2016. - № 4-1. - С.106-107.
9. Donika A.D. The study of professional deformations of doctors as deviations of their professional role // International Journal of Emergency Mental Health. 2015. Т. 17. № 4. С. 714-716.
Актуальность
Вопрос о токсическом действии веществ, которые попадают в организм человека из-за нарастающего загрязнения окружающей среды, интересует не только врачей, но и биологов, генетиков и, в целом имеет государственное значение, поскольку влияет на общее здоровье нации [2, 6]. Неслучайно 2017 год объявлен в России годом экологии. Особый интерес представляют вещества, которые используются в сельском хозяйстве, а, следовательно, могут влиять на «токсикологическое меню» россиян непосредственно [3, 7, 8].
Цель исследования: провести комплексный анализ токсикологических характеристик гербицидов на примере глифосата и оценить степень их опасности как экотоксикантов для безопасности жизнедеятельности.
Материалы и методы
Полученные результаты и их обсуждение
Отравления гербицидами и пестицидами в последнее время носят характер латентной экологической чрезвычайной ситуации. В то же время аварии на промышленных объектах, где в циклах производства включены рассматриваемые токсические вещества или их предикторы, могут стать причиной техногенной чрезвычайной ситуации, обусловленной розливом химического вещества в следствии нарушения техники безопасности или транспортных (чаще железнодорожных) аварий. В период между 1901 и 2016 годами, по данным всемирных организаций, в мире произошло 1 125 техногенных катастроф, затронувших около 4,5 миллионов человек, из которых около 49 000 человек погибли. Общий ущерб был оценен в 225 миллиардов долларов. Такие чрезвычайные ситуации чаще всего возникали в Азии (651 случай) и гораздо реже в Европе (199) и Северной и Южной Америке (177). По некоторым оценкам, ежегодно сотни тысяч техногенных инцидентов происходят в мире, убивая сотни людей и нанося значительный ущерб, превышающий десятки тысяч долларов США.
По данным ООН, техногенные катастрофы занимают третье место по числу жертв после стихийных бедствий, вызванных метеорологическими или геологическими факторами. Статистика CRED показывает, что число техногенных катастроф неуклонно растет с конца 1970-х годов. Эксперты считают, что основной причиной такого роста являются все более сложные инженерные системы, используемые людьми, а также значительное увеличение числа выполняемых ими функций (автоматизация), а уровень знаний и подготовки тех, кто разрабатывает такие системы, и тех, кто производит и управлять ими, не соответствует стандартам работы на всех этапах их жизненного цикла.
Статистика CRED показывает, что транспортные аварии, особенно в море и на реках, стали особенно частыми. Поскольку Европа и Северная Америка имеют надежную и безопасную транспортную и промышленную инфраструктуру, самые большие потери в таких авариях поддерживаются бедными странами Азии и Африки. Россия занимает в этой статистике промежуточное положение.
В то же время наибольший интерес представляют именно латентные чрезвычайной ситуации с участием гербицидов и пестицидов, поскольку несмотря на то, что медицинские последствия характеризуются неопределенностью (отсутствуют массовые острые отравления), они имеют серьезные отдаленные последствия, обуславливая хроническую заболеваемость и существенно влияя на качество жизни населения.
Среди наиболее обсуждаемых в последнее время является глифосат (N-(фосфонометил)-глицин, C3H8NO5P), который используется в большинстве коммерческих гербицидов. В немецком университете на содержание глифосата тестировали образцы мочи, взятой у городского населения, и было показано, что его концентрация превышала предельно допустимый порог установленный для питьевой воды в 5-20 раз [10].
В целом характер и тяжесть отравления, а также конкретных токсикологических эффектов возрастают с увеличением воздействия, определяемым дозой, продолжительностью и частотой попадания глифосата в организм человека, в рамках отношения «доза-ответ». Помимо дозы, факторы, которые могут влиять на токсикологический эффект, включают в себя путь воздействия на вещество, генетическую восприимчивость, физиологическое состояние, пол и возраст.
Токсикологические последствия могут быть краткими или длительными, немедленными или отсроченными, обратимыми или необратимыми, единичными или множественными, неприятными или недееспособными или даже опасными для жизни. Токсикологический эффект при отравлении глифосатом носит безпороговый характер. По определению предполагается, что непороговые эффекты происходят на любом уровне воздействия вещества. Однако, вполне может быть «практический» порог, например, в случае генотоксических эффектов, которые являются отражением взаимодействия между генотоксичностью и механизмами восстановления клеточной ДНК.
Возникает ли эффект - функция вероятности, и хотя вероятность будет уменьшаться по мере уменьшения уровня воздействия, предполагается, что уровень воздействия, для которого вероятность равна нулю, отсутствует. В отсутствие реального альтернативного механизма, поддерживаемого экспериментальными данными, мутагенность и генотоксическая канцерогенность в настоящее время считаются не пороговыми эффектами.
Сегодня оценка новых малоизученных веществ, таких, как глифосат, токсическое действие которых считается не имеющим порога, требует тщательной оценки имеющейся информации, в том числе результатов биологических анализов in vitro и in vivo и достоверных прогнозируемых оценок SAR, для определения веса доказательств канцерогенности или зародышей человека клеточной мутагенности.
В целом в механизме действия глифосата отмечаются эмбиротоксические и тератогенные эффекты, как бесплодие и нарушения эмбрионального развития человека и животных. Кроме того, отрвления глифосатом связывают с увеличением риска заболеваний лимфатической системы и рака кожи.
Клинические рекомендации по физиологической оценке тяжести интоксикации
Градации тяжести отравлении по степени
Симптомы стимулирующего действия
Симптомы депрессивного действия
возбуждение, беспокойство, потоотделение, гиперрефлексия, мидриаз, тремор
Отравление фосфорорганическими веществами
Отравление фосфорорганическими веществами — это острая интоксикация, возникающая при ингаляционном, трансдермальном или пероральном поступлении в организм некоторых инсектицидов (карбофос, хлорофос, тиофос) или боевых отравляющих веществ (зарин, зоман, ВИ-газы). Основные признаки: миоз, боль в области глаз, рвота, усиленное потоотделение, абдоминалгия и болезненность в груди, брадикардия, атаксия, паралич дыхания, судороги. Патология диагностируется на основании анамнеза, клинической картины и информации, полученной в ходе лабораторного обследования. Лечение включает холинолитики, реактиваторы холинэстеразы, симптоматическую терапию.
МКБ-10

Общие сведения
ФОВ — фторангидриды фосфорной или метилфосфоновой кислоты. Отравления ими составляют 1-2% от общего числа острых экзотоксикозов. Яд способен проникать сквозь кожу, не повреждая ее. При высоких концентрациях ксенобиотика патологическая симптоматика возникает уже через несколько минут. Распыленные в воздухе фосфорорганические соединения образуют стойкое облако, расположенное около поверхности земли, которое сохраняется на протяжении 4-6 часов. Военные отравляющие вещества способны удерживать токсическую концентрацию нескольких дней. Летальные дозы сильно различаются в зависимости от свойств конкретного соединения.
Причины
Абсолютное большинство случаев связано с нарушением правил техники безопасности при обработке полей или помещений от насекомых. Отравление фосфорорганическими веществами возникает при отказе от использования противогаза, недостаточной герметичности защитных костюмов, направлении распылителя на людей. Подобные интоксикации обычно бывают легкими или среднетяжелыми, поскольку доза полученного средства сравнительно мала. Другие возможные причины:
- Токсикомания. Пик встречаемости приходился на 80-90-е годы XX века. Сегодня отмечается устойчивая тенденция к снижению числа подобных случаев. Производные фосфорной кислоты способны вызывать галлюцинации и измененное состояние сознания, что до определенного момента делает их востребованными среди наркозависимых лиц.
- Военные действия. При проведении военных кампаний и террористических актов могут использоваться боевые отравляющие вещества: зоман, зарин. Отравление тяжелое, поскольку применяются стойкие, способные к долговременному поддержанию высокой концентрации формы ФОВ. Полулетальная доза зарина — 1,7 г, зомана — 60 мг.
- Суицид. Попытки покончить с собой с помощью фосфорорганических соединений сравнительно редки, их частота не превышает 3-4% от общего количества суицидов. Как правило, используются распространенные инсектициды, обладающие средней или малой токсичностью: карбофос, хлорофос, бромофос и демуфос, поэтому эффективность способа не слишком высока.
Патогенез
Основным патогенетическим механизмом действия ФОВ является подавление активности холинэстеразы на 30-80%, нарушение процессов синтеза и гидролиза ацетилхолина. Отравление фосфорорганическими веществами крайне тяжелой степени приводит к 100% ингибированию фермента. Происходит накопление АЦХ в синапсах, что сопровождается их перевозбуждением, нарушением работы головного мозга, сердца, гладкой и поперечнополосатой мускулатуры. Полное восстановление ЦНС наступает через 147 суток, системы крови — через 48 суток.
Токсикант обладает и прямым возбуждающим влиянием на холинергические структуры, поэтому тяжесть интоксикации не всегда соответствует количеству заблокированной холинэстеразы. Также ФОВ сенсибилизирует холинорецепторы организма к собственной ХЭ, что ведет к рецидиву симптоматики после полного очищения от отравляющего вещества. Последний механизм включает ускоренное высвобождение накопившегося ацетилхолина, что провоцирует его чрезмерное накопление на пресинаптических мембранах.
Классификация
Отравление фосфорорганическими веществами может подразделяться по наименованию токсиканта (зарин, карбофос, зоман); путям поступления яда (ингаляционный, трансдермальный, пероральный); механизму возникновения (непредумышленное поражение, суицид, военные действия); периоду интоксикации (скрытый, острый, осложнений и последствий). В клинической практике распространена классификация по степени тяжести:
- Легкая. Заблокировано не более 20-30% холинэстеразы. Ведущими являются следующие синдромы: невротический, миотонический, кардиальный, желудочно-кишечный, нарушения дыхания. Возникает при кратковременном пребывании на зараженном участке, чаще при неаккуратном применении бытовых инсектицидов.
- Средней тяжести. Объем заблокированного фермента варьируется от 30 до 80%. Основные синдромы: психоневротический, бронхоспастический. Возможно появление признаков, соответствующих легкой интоксикации. Встречается при попытках суицида с применением малотоксичных веществ или при длительном пребывании в зоне, обработанной инсектицидами.
- Тяжелое и летальное. Основу клинической картины составляет судорожно-паралитический синдром. Присутствует выраженное нарушение дыхания, гемодинамики. Развивается при попадании в зону действия боевых газов, пероральном или ингаляционном приеме высокотоксичных ФОВ. Сопровождается ранними и поздними осложнениями.
Симптомы отравлений ФОС
Отравление фосфорорганическими веществами проявляется симптоматикой поражения нескольких органов и систем. Со стороны респираторного аппарата отмечается бронхоспазм, экспираторная одышка, кашель с отделением большого количества мокроты, диспноэ, отек легких. Нарушение работы ЖКТ приводит к возникновению рвоты, тошноты, схваткообразных абдоминальных болей, непроизвольной дефекации. Потовые и слюнные железы реагируют увеличением секреции - наблюдается слюнотечение, повышенная потливость.
Поражение сердечно-сосудистой системы сопровождается брадикардией, ослаблением гемодинамики, транзиторным ростом уровня АД с его последующим падением. Реакция органов зрения заключается в появлении миоза, анизокории, спазма аккомодации (пострадавший теряет способность видеть на большом расстоянии). При тяжелых интоксикациях определяется резкая слабость, непроизвольные подергивания изолированных групп мышц, параличи и парезы. Возможны судороги, угнетение сознания вплоть до комы, признаки подавления активности дыхательного и сосудодвигательного центра.
Осложнения
Все осложнения подразделяются на ранние и поздние. Ранние возникают на 1-2 сутки с момента интоксикации. Поздние могут быть диагностированы с 3 до 150-200 дня. К первым относятся центральный паралич дыхания, обусловленный поражением соответствующего центра головного мозга, рецидивирующий бронхоспазм, острая пневмония, миокардиодистрофия, интоксикационный психоз, нефропатия и гепатопатия с развитием полиорганной недостаточности. Частота встречаемости ранних осложнений составляет около 5-7%.
На поздних сроках может формироваться периферический паралич дыхательной мускулатуры, токсическая энцефалопатия, полиневрит, астеновегетативный синдром. У некоторых пациентов определяются сохраняющиеся парезы и гемипарезы конечностей, поражение нервов, сопровождающееся нарушением функции внутренних органов, недержание кала, мочи. Также возможен рецидив клинической картины интоксикации. Отравление фосфорорганическими веществами осложняется поздними патологическими явлениями в 3-4% случаев.
Диагностика
Основа диагностики — клиническая картина и анамнез пациента. Постановкой диагноза занимается врач скорой помощи или токсиколог специализированного центра (при самостоятельном обращении пострадавшего). Требуются консультации гастроэнтеролога, невролога и других специалистов. Патологию дифференцируют с отравлением наркотиками, нейротоксическими ядами, веществами, способными воздействовать на активность холинэстеразы (ингибиторы овуляции, миорелаксанты, мышьяк, глюкокортикостероиды). Методы обследования:
- Физикальные. Отмечается спутанность сознания, заторможенность, кома. При осмотре — цианоз или бледность кожи, спонтанные подергивания отдельных групп мышц или клонико-тонические судороги. АД выше или ниже нормы, дыхание затруднено, пульс урежен. При аускультации легких могут выслушиваться влажные хрипы, присутствует продуктивный кашель.
- Лабораторные. Изменение цвета индикатора при лабораторной пробе составляет 22-40 минут. Отмечается сдвиг pH крови в кислую сторону, нарушение электролитного баланса. Парциальное давление кислорода снижено, нарастает содержание углекислого газа. При поражении почек накапливается мочевина, креатинин. На фоне печеночной патологии отмечается повышение АСТ, АЛТ.
- Аппаратные. Используются преимущественно для диагностики осложнений. Отек легкого проявляется летучими тенями на рентгенограмме, при бронхоспазме резко снижен объем форсированного выдоха. На ЭКГ — мерцательная аритмия, тахикардия, обусловленная непосредственным поражением миокарда или гипотонией.
Лечение отравлений ФОС
До прибытия медиков следует эвакуировать пострадавшего из зоны химического загрязнения, уложить, обеспечить приток свежего воздуха. Если токсикант попал на незащищенную кожу, этот участок необходимо протереть 10% раствором аммиака. Случаи поражения глаз требуют промывания 2% натрия гидрокарбонатом с последующим закапыванием атропина. Последствия перорального употребления яда можно уменьшить, если сразу после контакта с ним промыть желудок беззондовым методом и дать активированный уголь. Доза сорбента рассчитывается по формуле 1 таблетка на 10 кг веса.
Первая помощь
Первую помощь оказывают бригады СМП. Основным мероприятием считается введение атропина, который нейтрализует влияние фосфорорганических соединений. Препарат вводят внутривенно, при выраженной тахикардии - внутримышечно по 1 мл 0,1% раствора каждые 15 минут. При пероральных интоксикациях проводится зондовое промывание желудка, введение энтеросорбентов, инфузия солевых средств. Симптоматическая терапия включает антиконвульсанты, прессорные амины, бронхолитики, диуретики. При нарушении сознания и дыхания осуществляется интубация трахеи с последующим переводом на ИВЛ.
Стационарное лечение
Основой терапевтической схемы являются реактиваторы холинэстеразы и холинолитики. К числу последних относится атропин. Пациенты получают его с интервалом 15 минут. Оценочный критерий достаточного объема антидотной терапии — возникновение атропинового делирия, для этого может потребоваться 20-30 мл препарата. Реактиваторы ХЭ (изонитрозин, дипироксим) используют на всех этапах отравления. Схема подбирается индивидуально, зависит от тяжести патологии и категории пациента (дети, взрослые, старики).
Для борьбы с возникающими нарушениями больной получает симптоматическое лечение. Назначаются препараты янтарной кислоты, стимуляторы дыхания, антидепрессанты, нейролептики, антиоксиданты, противосудорожные медикаменты, блокаторы кальциевых каналов. Для ускоренного выведения ксенобиотика используется метод форсированного диуреза и стимуляция кишечника (солевые слабительные). При необходимости осуществляется реанимационное пособие (интубация, ИВЛ, гемодиализ, титрованное введение дофамина, мониторинг).
Реабилитация
После выписки пациенту назначается амбулаторное долечивание. Он должен тщательно отслеживать свое состояние, регулярно посещать врача общей практики или терапевта. Медикаментозная поддержка предусматривает прием ноотропов, антипсихотических и сердечных средств. Рекомендуется посещение санаторно-курортных учреждений, расположенных в хвойных лесах. При наличии парезов требуется наблюдение невролога, прием лекарств, улучшающих нервно-мышечную проводимость, лечебная физкультура.
Прогноз и профилактика
Полное восстановление занимает около двухсот дней. На протяжении этого периода могут возникать отсроченные осложнения. Время госпитализации больных с легкой и средней степенью поражения обычно не превышает 10-15 суток. Длительность стационарного лечения тяжелых пострадавших зависит от течения соматической стадии экзотоксикоза и регенеративных возможностей организма. Смертность составляет 12,9%. Основная причина летальных исходов — паралич центра дыхания, несвоевременно оказанная медицинская помощь.
Чтобы предотвратить отравление фосфорорганическими веществами, необходимо строго соблюдать требования техники безопасности. Во время работы с пестицидами и гербицидами используются изолирующие противогазы, одежда, не позволяющая токсиканту попасть на кожу. Солдаты, принимающие участие в боевых действиях, должны быть обучены навыкам распознавания химической опасности и обеспечены средствами защиты. Дома ФОВ нужно хранить в закрытых помещениях, куда не имеют доступа дети и люди с нестабильной психикой.
3. Руководство по скорой медицинской помощи/ Багненко С.Ф., Мирошниченко А.Г., Верткин А.Л., Хубутия М.Ш. — 2007.
Медведев О.С., факультет фундаментальной медицины МГУ имени М.В. Ломоносова,
Национальный исследовательский центр «Здоровое питание»
Вопрос о безопасности использования ГМО-продуктов для здоровья человека остается ареной споров и дискуссий как в обществе, так и в научных кругах. Имеются сторонники взгляда об их безопасности для здоровья (1, 2) и убежденные противники использования этих продуктов (3).
По мнению многих исследователей требуется больше времени для получения научно-обоснованного ответа на этот вопрос. Всемирная Организация Здравоохранения (ВОЗ) разрабатывает методологию для проведения подобных исследований по безопасности генно-модифицированных продуктов (4).
Однако следует рассматривать не только сами продукты питания, произведенные с использованием ГМО-технологий, но и технологические процессы производства таких продуктов. В качестве примера приведем опубликованные данные о современной технологии выращивания генно-модифицированных сои, кукурузы и других культур и использования гербицидов для уничтожения сорняков.
Впервые гербициды на основе глифосата, созданные американской фирмой «Монсанто», появились в 1974 году. Глифосат представляет собой аналог аминокислоты глицина, который способен в растениях блокировать работу фермента EPSP синтазы, что сопровождается угнетением синтеза ароматических аминокислот, и как следствие - синтеза белка, хлорофилла, в результате чего растения погибают. Это вещество является действующим началом широко известного гербицида RoundUp. До 2000 года действовал патент фирмы «Монсанто», а после этого другие компании стали выпускать гербициды, содержащие глифосат. Особенно широко стали использовать подобные гербициды для борьбы с сорняками после создания генно-модифицированных растений (сои, кукурузы, хлопка, сахарной свеклы и других) - “Roundup Ready”, устойчивых к действию глифосата. Со временем у сорняков развивается устойчивость к действию глифосата, что требует более частого применения гербицида (5). Если в 1987 году по частоте использования глифосат был в мире на 17-м месте, то уже в 2001 году он вышел на первое место (6). Ежегодная потребность в глифосате составляет около 500 тыс. тонн (7), а продажи в 2011 году составили 5.6 миллиарда долларов (8).
Глифосат применяется несколько раз во время роста и созревания возделываемой культуры, а также для подсушивания урожая перед уборкой. Производители гербицидов постоянно подчеркивают экономическую необходимость их использования в сельском хозяйстве, т.к. при их применении производство кормовых культур, пшеницы, сои повышается на 4.3 - 7.1%, а если их запретить, то потери для экономики только Европейского Союза составят 1.4 млрд долларов (9).
В США разрешен довольно высокий максимальный уровень глифосата в питьевой воде - 700 мкг/л, в Австралии еще выше - 1000 мкг/л, тогда как в Европе допустимый уровень поллютанта - менее 0.1 мкг/л (10).
В связи с широким использованием гербицидов на основе глифосата неудивительно, что его небольшие количества обнаруживаются в кормах и продуктах питания (11, 12), в питьевой воде за счет стекания воды с полей в реки и водоемы, проникновения в грунтовые воды (13), человек может получить его с пищей, питьевой водой или в процессе применения RoundUp при борьбе с сорняками. (14). Фирмы - производители гербицидов на основе глифосата в течение длительного времени убеждали общественность, что токсичность таких гербицидов для человека очень низка за счет того, что у человека и других млекопитающих отсутствует фермент EPSP синтаза, на который направлено действие глифосата в растениях. Однако исследования последних лет не подтверждают такую точку зрения. Оказалось, что изучение самого глифосата (в основном на грызунах) недостаточно, так как в состав конечного продукта входят дополнительные вещества - адьюванты, ускоряющие всасывание глифосата и усиливающие его гербицидное действие. Сравнительные исследования глифосата и конечного продукта (RoundUp) показали, что в опытах in vitro на клетках человека токсичность глифосата составила 2 г/л, тогда как токсичность RoundUp 400 и 450 составила 0.001 г/л (15).
Острые отравления глифосатом
В литературе описаны случаи острого отравления гербицидами на основе глифосата. Симптомами острого отравления обычно являются гастроэнтерит, нарушения дыхания, нарушения сознания, снижение артериального давления, почечная недостаточность и шок (16). В подобных случаях суточные дозы глифосата и АМРА составляют или превышают 125 и 5 мкг/кг/день, соответственно (17). В Индии описан случай, когда у человека, проглотившего 75 мл раствора гербицида, содержащего 40.6% глифосата, развился отек легкого (18). Смертельный исход отмечается в среднем в 3.2% случаев, наступает через 20 часов и связан с развитием сердечно-дыхательной недостаточности (19).
Эффекты хронического воздействия глифосата и комплекса RoundUp на здоровье
В опытах как на клеточных культурах, так и на животных (in vivo) была установлена способность глифосата и RoundUp вызывать окислительный стресс даже в небольших концентрациях. Это связано с их способностью связывать ряд ионов (марганца, меди, кобальта, железа, цинка, кальция и магния, что ведет к нарушению функций митохондрий, нарушению процесса окислительного фосфорилирования и образованию больших количеств активных форм кислорода (23). Наиболее характерным для пищевых токсикантов является поражение почек и печени. Это подтверждается исследованием фермеров в Шри Ланке, которые применяли RoundUp без защитных масок и пили воду с повышенным содержанием глифосата (24). Детальный анализ хронического потребления воды (2 года) с низким содержанием глифосата (0.1 ppb) или RoundUp (45 ng/L глифосата, смешанного с адьювантами) выявил нарушения функций печени и почек к 15 месяцу исследования (3). Повреждение клеток печени включает угнетение активности цитохромоксидазных ферментов CYP1A1/2 and CYP3A, участвующих в метаболизме многих ксенобиотиков. Следствием также может быть снижение концентрации активной формы витамина D-25-гидрокси-витамин-D. Обнаруженные изменения в экспрессии ряда генов отражали нарушения жирового обмена в печени и почках, соответствовали процессам развития фиброза, некроза, нарушениям функции мембран митохондрий и ишемии (3).
В ряде исследований обнаружено негативное влияние глифосата на репродуктивную функцию млекопитающих. Отмечено изменение уровня ароматазы в яичках и нарушения структуры ядра в сперматозоидах крыс, а также нарушения сперматогенеза (25, 26).
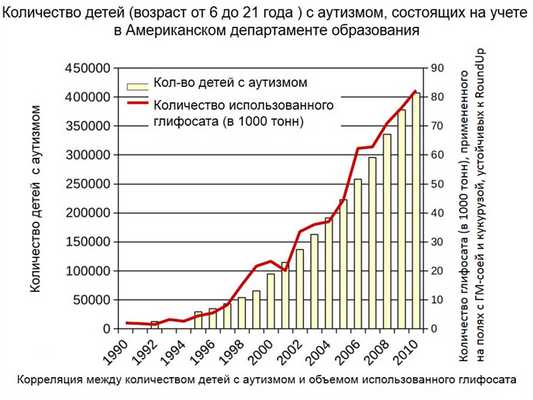
Целый ряд эпидемиологических исследований выявил тесную корреляцию между возросшим применением глифосата при производстве устойчивых к RoundUp генно-модифицированных растений и повышением частоты выявления таких нарушений со стороны нервной системы, как развитие аутизма и старческого слабоумия (Таблица 1) (22). Авторы связывают это со способностью глифосата вызывать состояние окислительного стресса не только в периферических органах, но и мозгу.
Коэффициент корреляции R
Заболевания, частота выявления которых коррелирует с повышением использования глифосата в сельском хозяйстве США
Сюрванта ® (Survanta)
Произведено:
Упаковка и выпускающий контроль качества:
Форма выпуска, упаковка и состав препарата Сюрванта ®
Суспензия для эндотрахеального введения в виде молочно-белой жидкости от почти белого до светло-коричневого цвета.
| 1 мл | |
| экстракт легких быка, содержащий липиды легких быка (берактант) в пересчете на: | |
| общее содержание фосфолипидов | 25.0 мг |
| динасыщенный фосфатидилхолин | 11.0-15.5 мг |
| свободные жирные кислоты | 1.4-3.5 мг |
| триглицериды | 0.5-1.75 мг |
Вспомогательные вещества: натрия хлорид - q.s. до 9.0 мг, натрия гидроксид - q.s. до pH 6.2-7.6, хлористоводородная кислота - q.s. до pH 6.2-7.6, вода д/и - до 1.0 мл.
4 мл - флаконы бесцветного стекла (1) - пачки картонные.
8 мл - флаконы бесцветного стекла (1) - пачки картонные.
Механизм действия берактанта основан на снижении поверхностного натяжения альвеолярных стенок при дыхании и предотвращении спадания альвеол в конце выдоха (экспираторной фазы). Дефицит легочного сурфактанта вызывает респираторный дистресс-синдром (РДС) у недоношенных новорожденных.
Берактант восполняет количество сурфактанта и восстанавливает поверхностную активность легких у недоношенных новорожденных.
После эндотрахеального введения берактант быстро распределяется по альвеолярному пространству, что приводит к стабилизации альвеол и повышению их сопротивляемости спаданию во время дыхания, что, в конечном счете, улучшает альвеолярное дыхание.
В клинических исследованиях с участием недоношенных новорожденных с респираторным дистресс-синдромом после введения одной дозы берактанта наблюдалось улучшение оксигенации.
Также у этих детей наблюдалось снижение потребности в кислороде, а также повышение артериально-альвеолярного коэффициента оксигенации (а/АрО 2 ). Кроме того, наблюдалось значительное снижение потребности в респираторной поддержке, что подтверждалось более низкими значениями среднего сопротивления дыхательных путей. В большинстве случаев эти явления сохранялись в течение не менее 72 часов после введения одной дозы берактанта.
Показания активных веществ препарата Сюрванта ®
Профилактика и лечение респираторного дистресс-синдрома (РДС, болезнь гиалиновых мембран) у недоношенных новорожденных.
Только для эндотрахеального введения.
Препарат, содержащий берктанат, должен применяться врачами, имеющими опыт проведения интубации, искусственной вентиляции легких и ухода за недоношенными новорожденными, или под его наблюдением.
Значительное улучшение оксигенации может быть достигнуто в течение нескольких минут после введения, для предотвращения гипероксии необходим тщательный медицинский контроль и мониторинг системной оксигенации.
Доза составляет 100 мг/кг массы тела, исходя из массы тела на момент рождения.
Со стороны сердечно-сосудистой системы: 11.9% - транзиторная брадикардия.
Со стороны дыхательной системы: 9.8% - снижение сатурации кислорода.
В ходе процедуры введения: менее 1% - рефлюкс препарата в эндотрахеальную трубку, бледность, вазоконстрикцию, снижение АД, закупорку эндотрахеальной трубки, повышение АД, гипокапнию, гиперкапнию и апноэ.
При анализе всех контролируемых клинических исследований различий в частоте внутричерепных кровоизлияний выявлено не было. Однако в одном исследовании, в котором берактант вводился однократно в лечебных целях, и в другом исследовании профилактического многократного введения препарата распространенность внутричерепных кровоизлияний была значительно выше среди пациентов, получавших берактант (63.3% против 30.8%, Р=0.001; и 48.8% против 34.2%, Р=0.047 соответственно).
Применение при беременности и кормлении грудью
Применение у детей
Применяется по показаниям.
Отсутствует опыт применения берактанта у пациентов с массой тела менее 600 г и более 1750 г.
Применение у пожилых пациентов
Особые указания
Берактант способен быстро оказать воздействие на оксигенацию и поверхностную активность легких. В связи с этим, препарат, содержащий берактант, следует применять только в условиях высокоспециализированных отделений, где работают специалисты, имеющие опыт проведения интубации, ИВЛ и ухода за недоношенными новорожденными. При лечении барктантом необходим частый мониторинг системных показателей кислорода и углекислого газа в артериальной крови или при чрескожном измерении.
В ходе введения берактанта были отмечены случаи транзиторной брадикардии и снижения сатурации кислорода. В случае развития этих нежелательных реакций, процедуру следует прекратить, и принять надлежащие меры по улучшению состояния ребенка. После стабилизации состояния ребенка следует возобновить процедуру.
Отсутствует опыт применения берактанта у пациентов с массой тела менее 600 г и более 1750 г, а также в сочетании с другими методами лечения РДС (например, высокочастотная искусственная вентиляция легких или экстракорпоральная мембранная оксигенация).
В контролируемых клинических исследованиях у новорожденных, получавших лечение берактантом, был отмечен повышенный риск развития внутрибольничного сепсиса. Повышенный риск развития сепсиса у детей, получавших лечение берактантом, не был ассоциирован с увеличением смертности среди этих детей. Возбудители были сходными в группе детей, получавших лечение, и в контрольной группе. По распространенности других инфекционных заболеваний значимых различий между группами отмечено не было.
Читайте также:
