КТ, МРТ при синоназальном плоскоклеточном раке
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Вам поставили диагноз: опухоль полости носа и околоносовых пазух?
Наверняка Вы задаётесь вопросом: что же теперь делать?
Предлагаем Вашему вниманию краткий, но очень подробный обзор данного онкологического заболевания.
Его подготовили высоко квалифицированные специалисты Отделения лучевого и хирургического лечения заболеваний верхних дыхательных путей МРНЦ имени А.Ф. Цыба - филиала ФГБУ «НМИЦ радиологии» Минздрава России под редакцией заведующего отделением к.м.н. Феликса Севрюкова.
Данная брошюра содержит информацию о диагностике и лечении опухоли полости носа и околоносовых пазух. Здесь собраны основные методики лечения данного заболевания, в том числе, последние разработки отечественных и зарубежных ученых-онкологов.
Филиалы и отделения, где лечат опухоль полости носа и околоносовых пазух
МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России.
МРНЦ им. А.Ф. Цыба - филиал ФГБУ «НМИЦ радиологии» Минздрава России.
1. Введение
Особенностями опухолей полости носа и околоносовых пазух является их локализация, тесная, а иногда интимная, связь с жизненно важными органами и системами (головной мозг, глаз, среднее ухо, магистральные сосуды и т.д.).
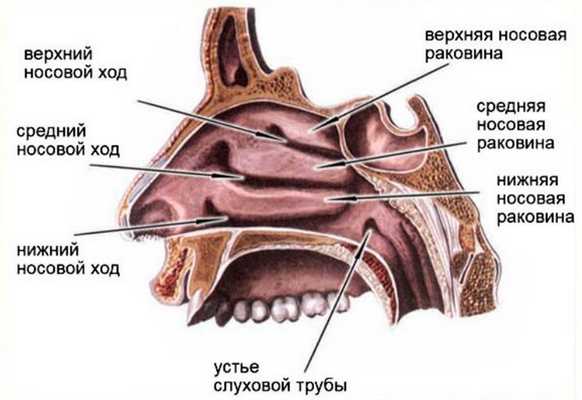
Полость носа состоит из носовых ходов (нижний, средний, верхний и общий); перегородки носа, делящей полость носа на две половины; и носовых раковин (нижняя, средняя и верхняя). Кзади полость носа посредством хоан сообщается с полостью носоглотки. На боковой стенке полости носа имеется выводные отверстия околоносовых пазух: верхнечелюстной, лобной, пазухи основной кости и клеток решетчатого лабиринта или решетчатой кости. Все элементы полости носа и околоносовых пазух покрыты слизистой оболочкой, элементы которой в большинстве случаев служат основой для возникновения опухолей данной локализации.
2. Статистика опухоли полости носа и околоносовых пазух (эпидемиология)
Злокачественные опухоли полости носа и околоносовых пазух встречаются приблизительно в 3% от всех злокачественных опухолей и до 20% от опухолей верхних дыхательных путей, после опухолей гортани, гортанноглотки и ротоглотки. Наиболее часто поражаются опухолью верхнечелюстные пазухи и собственно полость носа. Реже встречаются опухоли решетчатого лабиринта, лобной и основной пазух. Наиболее часто распространенные опухоли данной локализации поражают глазницу, включая все ее стенки и собственно глазное яблоко, кости основания черепа, иногда распространяясь и в полость черепа, особенно при поражении лобной, основной пазух и клеток решетчатого лабиринта. Опухоли данной локализации приблизительно в 2 раза чаще встречаются среди мужчин, чем у женщин, при этом заболевают чаще в наиболее трудоспособном возрасте - 40-60 лет, однако имеет место заболеваемость как в более раннем, так и старшем возрастах.
Мы хотим Вам помочь победить рак!
3. Морфологическая классификация опухоли полости носа и околоносовых пазух
Среди злокачественных опухолей полости носа и околоносовых пазух наиболее часто встречаются раковые опухоли разной степени дифференцировки.
• Плоскоклеточный ороговевающий рак - 50% и более,
• Плоскоклеточный неороговевающий - 10-13%,
• Низкодифференцированный рак 7-8%.
• Опухоли другого морфологического строения (саркомы, меланомы, цилиндромы, эстезионейробластомы, малигнизированные переходно-клеточные папилломы и др.) - 28%&
4. Стадии и симптоматика опухолей полости носа и околоносовых пазух
Подавляющее большинство пациентов имеют распространенные формы рака полости носа и околоносовых пазух. Так, пациенты с распространенностью опухоли T3N0M0 составили 22% случаев, T3N1-3M0 - 3,4%, T4N0 - 32,0% и с T4N1-3 - 9,6%. Только у 4,6% больных распространенность опухолевого процесса классифицировалась как T1-2N0.
Перечень симптомов, позволяющих заподозрить опухолевое поражение полости носа и околоносовых пазух:
1. быстро нарастающее одно редко двухстороннее нарушение носового дыхания;
2. упорные серозно-гнойные или кровянистые выделения из полости носа, чаще односторонние;
3. снижение обоняния;
4. нарушение конфигурации лица;
5. нарушение чувствительности кожи щеки или зубов верхней челюсти (как правило - одностороннее);
6. усиливающаяся подвижность зубов верхней челюсти;
7. смещение глазного яблока;
8. безболезненная припухлость щеки;
9. нарастающее нарушение зрения;
10. изменение конфигурации твердого неба или альвеолярного отростка верхней челюсти;
11. появление неприятного запаха.
5. Причины возникновения опухоли полости носа и околоносовых пазух и факторы риска
Как и для всех опухолей, причина возникновения злокачественных опухолей полости носа и околоносовых пазух, достоверно не установлена. Можно предполагать, что возникновению опухолей данной локализации способствуют ряд факторов, таких как хронические болезни полости носа и околоносовых пазух, полости рта, в частности зубов, производственные вредности, особенно пыль, в частности - асбестовая, древесная, вдыхание паров горюче-смазочных материалов, дыма - в частности, при сварочных работах, у работников никелевой промышленности и кожевенного производства.
Развитию опухолей может способствовать различные травмы (бытовые, производственные, спортивные и т.д.). К факторам риска может быть отнесена - генетическая предрасположенность, а также хроническая травма, например при пользовании зубными протезами.
6. Диагностика опухоли полости носа и околоносовых пазух
Перечень диагностических процедур подразделяется на обязательные и дополнительные. При этом особое значение имеет тщательный сбор анамнеза заболевания и анализ данных эндоскопического обследования ЛОР органов и данных СКТ и МРТ-исследований. Морфологическое подтверждение заболевания является обязательной процедурой для диагностики как первичной опухоли, так и ее метастазов. При этом особое значение имеют иммуноморфологические данные.
Перечень обязательных диагностических процедур:
•анкетные данные больного и анамнез заболевания
•врачебный осмотр (включающий ЛОР-осмотр)
•назофаринголарингоскопия
•ультразвуковое исследование шеи, печени, с пункцией лимфоузлов увеличенных более 1 см.
ультразвуковое исследование опухоли при разрушении опухолью костных структур и выходом в мягкие ткани лица
•СКТ головы с контрастированием (включая оценку инвазии в головной мозг) и шеи (до биопсии, шаг 3 мм)
•биопсия опухоли с последующим гистологическим, цитологическим исследованием, через полость носа, путем гайморотомии с использованием видеоассистированной техники, трепонобиопсии.
•рентгенологическое исследование органов грудной клетки при Т1-2 КТ грудной клетки при Т3 - Т4, или при подозрении на метастазы в легкие при рентгеновском снимке Т1-2
•ЭКГ стандартная
•консультация стоматолога
•совместный консилиум с участием ОНКОЛОГА, радиотерапевта, химиотерапевта
•консультация терапевта
•консультация анестезиолога для пациентов, планируемых для хирургического лечения
Дополнительные процедуры
•пункция лимфатических узлов шеи с последующим цитологическим исследованием (при подозрении на метастатическое поражение)
•гастроскопия
•КТ/МРТ шеи (до биопсии, шаг 3 мм) (по показаниям)
•компьютерная томография органов грудной клетки (при подозрении на метастатическое поражение легких)
•компьютерная томография органов брюшной полости (при подозрении на метастатическое поражение печени)
•магнитно-резонансная томография головного мозга (при наличии очаговой неврологической симптоматики)
•сцинтиграфия костей (при подозрении на метастатическое поражение)
•позитронно-эмиссионная томография /ПЭТ-КТ (при III-IV стадиях процесса, по показаниям)
•консультация специалистов (по показаниям)
•флуоресцентная диагностика (по показаниям)
•ЭХО-КГ, Холтеровское мониторирование - по показаниям
Специфических онкомаркеров для диагностики злокачественных опухолей данной локализации не существует. Скрининговых программ для диагностики этой патологии нет.
7. Лечение опухоли полости носа и околоносовых пазух
Основным методом лечения злокачественных опухолей полости носа и околоносовых пазух является хирургический. При этом объем хирургического вмешательства зависит от распространенности и локализации опухолевого поражения, которые определяются в результате клинического и инструментального обследований.
При начальных стадиях (Т1, Т2) опухолевого роста возможно выполнение щадящих органосберегающих хирургических вмешательств. При операбельных распространенных процессах (Т3, Т4), как правило, проводятся различные по объему расширенные, комбинированные операции, с включением в блок удаляемого препарата близ расположенных органов и тканей (глаз, стенки и ткани глазницы, клетчатка подвисочной и крылонебной ямок, скуловая кость, кожа и др.). Одновременно или отсрочено выполняются различные реконструктивно-пластические вмешательства, позволяющие минимизировать функциональные и косметические потери (пластики перемещенными кожно-жировыми и кожно-мышечными лоскутами, фрагментами мало-берцовой кости или гребня подвздошной кости на сосудистой ножке и др.). Наиболее часто изготавливаются либо разделительные пластины обеспечивающие разобщение возникшего послеоперационного дефекта и полости рта, или замещающие протезы с восстановленным зубным рядом.
Практически во всех случаях используется послеоперационная лучевая терапия в дозе ≈ 50-60 Гр. Предоперационное облучение применяется реже. Самостоятельная лучевая терапия проводится только в случаях неоперабельности опухоли или отказе пациента от хирургического лечения.
Лекарственная противоопухолевая терапия самостоятельного значения не имеет и применяется либо с предоперационной целью (неоадъювантная терапия), либо в послеоперационном периоде (адъювантное лечение), либо в сочетании с лучевой терапией (химиолучевое лечение). Применяются в основном препараты платины в сочетании с 5-фторурацилом, лучший эффект получается при использовании в данной схеме таксанов (таксотер и др.).
В предоперационном периоде проводится 2-3 цикла химиотерапии каждые 3 недели. В послеоперационном периоде возможно проведение до 6 циклов ПХТ (полихимиотерапии). При химиолучевом лечении применяется, в основном, цисплатин в дозе 100 мг/м2 1 раз в 3 недели или в дозе 75 мг/м2 каждую неделю. Для получения лучшего результата химио- или химиолучевой терапии иногда применяются таргетные препараты, в частности - Эрбитукс (Цетуксимаб).
8. Осложнения противоопухолевого лечения и их коррекция
Как уже было отмечено, хирургическое лечение злокачественных опухолей полости носа и околоносовых пазух ведет прежде всего к косметическим и функциональным нарушениям и касается в основном, возникновением обширных послеоперационных дефектов, разговорной речи и акта приема пищи. С целью минимизации таких осложнений осуществляются различные реконструктивно-пластические вмешательства, как неотсроченные (во время основного хирургического вмешательства), так и отсроченные (в разные периоды после операции), а также сложное зубное и разобщающее протезирование.
При проведении лучевой терапии при данной патологии наиболее часто возникают острые лучевые реакции (дерматиты) и поздние постлучевые осложнения (постлучевые отеки мягких тканей, фиброзы, постлучевые язвы и некрозы). При возникновении острых лучевых реакций проводятся в основном, противовоспалительные и противоотечные мероприятия. Возможно, при необходимости, назначение обезболивающих препаратов. Как правило, данные реакции купируются в течение 10-12 дней. Поздние лучевые осложнения требуют более сложных и длительных лечебных мероприятий, а иногда и сложных хирургических вмешательств.
При химиотерапии данной патологии наиболее частым нежелательным явлением оказывается возникновение гематологической токсичности разной степени выраженности, заключающейся в нарушении нормального кроветворения (анемии, нейтропении, тромбоцитопении и т.д.), приводящие к развитию инфекционных осложнений, кровотечениям (преимущественно носовым). Проводимое лечение может сопровождаться выпадением волос, развитием воспаления слизистой оболочки полости рта, глотки, желудка и кишечника. Вовремя и в необходимом объеме проведенные лечебные мероприятия позволяют купировать эти нежелательные явления и полностью завершить запланированный объем лечения.
9. Использование уникальных методик
В последнее время достаточно широкое применение получили такие методики как гипертермия (локальное нагревание опухоли СВЧ- или УВЧ - излучением); фотодинамическая терапии (либо при начальных формах опухолей, либо на ложе удаленного новообразования); химиоэмболизация питающих опухоль сосудов, видеоэндоскопическое удаление новообразований и др.
10. Особенности реабилитации
Как уже отмечалось, практически все больные с злокачественными опухолями полости носа и околоносовых пазух в той или иной степени требуют различных по сложности реабилитационных мероприятий. Эти мероприятия проводятся как в клиниках, занимающихся лечением данной категории больных, так и в специализированных учреждениях, занимающихся реконструктивно-пластическими операциями.
11. Прогноз заболевания
Прогноз эффективности лечения зависит как от локализации опухолевого поражения, так и от распространенности, морфологического строения опухоли, так и от проведенного лечения.
При правильном лечении у больных с начальными формами злокачественных опухолей полости носа и околоносовых пазух возможно излечение в течении 5 лет практически у 100% пациентов.
При распространенности опухоли Т3 излечение в этот период времени возможен более чем в 70% случаев, в зависимости от примененного вида лечения. Безусловно, лучший результат имеет место при использовании комбинированного лечения (операция + лучевое и химиолучевое лечение).
При опухолях, распространенностью Т4, 5-летний результат лечения не превышает 30-40% наличия метастазов в зонах регионарного метастазирования ухудшает результаты проводимой терапии.
Филиалы и отделения, в которых лечат опухоль полости носа и околоносовых пазух
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Рак носоглотки - симптомы и лечение
Что такое рак носоглотки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Опря Анны Николаевны, онколога со стажем в 12 лет.
Над статьей доктора Опря Анны Николаевны работали литературный редактор Вера Васина , научный редактор Татьяна Остринская и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Рак носоглотки (Nasopharyngeal cancer) — это злокачественная опухоль верхней части глотки. На ранних стадиях болезнь протекает бессимптомно или маскируется под другие заболевания, например под острые респираторные инфекции. Одним из первых проявлений рака носоглотки могут стать увеличенные шейные лимфоузлы.

В 70 % случаев в носоглотке развивается плоскоклеточный рак — опухоль, исходящая из клеток эпителия слизистой оболочки [3] .
Но могут встречаться и другие злокачественные новообразования:
- исходящие из малых слюнных желёз (аденокарцинома);
- из мягких тканей (саркома);
- из лимфоидной ткани (лимфома);
- из нейроэпителия (эстезионейробластома) [1] .
Распространённость рака носоглотки
В России на рак носоглотки приходится 0,1-0,2 % от всех онкологических болезней. Самая высокая заболеваемость в двух возрастных группах: в 15-25 и 40-60 лет. Мужчины болеют раком носоглотки примерно в пять раз чаще, чем женщины [2] [3] .
Причины рака носоглотки
Причины заболевания до конца не изучены, но известно, что основным фактором развития болезни является вирус Эпштейна — Барр [6] . Этим вирусом заражено более 90 % населения планеты, зачастую заболевание протекает без симптомов и не вызывает осложнений. Лишь у немногих заражённых инфекция становится хронической, что впоследствии может привести к раку [15] .
К другим факторам развития рака носоглотки относятся:
- Хронические воспалительные процессы, вызывающие гиперплазию и метаплазию слизистой оболочки носоглотки, т. е. разрастание и преобразование тканей.
- Анатомические особенности некоторых рас. Рак носоглотки чаще встречается среди народов Юго-Восточной Азии, Африки и Индокитая.
- Профессиональные факторы. Риск развития заболевания выше при работе, связанной с воздействием тепла, пара и пыли. Чаще заболевают сварщики, печники, пекари, кочегары, кузнецы, операторы кузнечных прессов, работники деревообрабатывающей и текстильной промышленности [6] .
- Частое потребление солёной консервированной рыбы. Предположительно, если есть её ежедневно, риск развития рака повышается в несколько раз. Потребление других консервированных продуктов также может повышать риск развития болезни [6] .
В исследовании, проведённом в США, две трети случаев рака носоглотки I типа были связаны с курением, но для II и III типа такую взаимосвязь не выявили [6] . Также не доказано, что рак носоглотки чаще возникает при употреблении алкоголя.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы рака носоглотки
На ранних стадиях рак носоглотки протекает бессимптомно или скрывается под маской острых респираторных инфекций, ринофарингита и аденоидных вегетаций. Кроме того, опухоль не видна и не прощупывается, поэтому часто её выявляют только на поздних стадиях.
Симптомы рака носоглотки зависят от расположения опухоли и направления её роста.
Можно выделить следующие проявления болезни:
- Со стороны полости носа — периодические носовые кровотечения, примесь крови в слюне и прогрессирующая заложенность носа.
- Ушные — пощёлкивание и боли, заложенность уха, ухудшение слуха, односторонний рецидивирующий средний отит.
- Офтальмологические — выпячивание и смещение глазного яблока, опущение верхнего века, косоглазие, снижение остроты зрения и двоение в глазах.
- Расстройство глотания и произношения звуков, провисание мягкого нёба, гнусавость.
- Неврологические — поражение черепно-мозговых нервов может привести к онемению лица, неподвижности половины гортани, отклонению языка в сторону и другим симптомам, связанным с параличом черепно-мозговых нервов. Чаще всего поражаются 3, 5, 6 и 12-й черепные нервы [1][16] .
Боль и затруднения при глотании, возникающие при других видах рака головы и шеи, редко встречаются на ранней стадии рака носоглотки, поскольку очаг находится выше ротоглотки.
Для рака носоглотки характерны метастазы, поражающие шейные лимфоузлы. Нередко первым и единственным симптомом становится их увеличение с одной или обеих сторон шеи, по поводу таких лимфоузлов пациент и обращается к врачу.
Неврологические, офтальмологические и другие симптомы, как правило, возникают на III-IV стадиях. К поздним проявлениям также относят спазм жевательной мускулатуры и головную боль [16] .
Патогенез рака носоглотки
Вирус Эпштейна — Барр связан с несколькими злокачественными опухолями: раком носоглотки, лимфомой и карциномой желудка. Инфекция передаётся через жидкости организма, особенно через слюну, а также половым путём.
Считается, что ядерный антиген вируса Эпштейна — Барр, т. е. его специфический белок, может поражать эпителиальную оболочку носоглотки и приводить к злокачественному перерождению тканей [16] .

Раковые опухоли носоглотки, связанные с вирусом Эпштейна — Барр, представляют собой недифференцированные карциномы с выраженной лимфоидной инфильтрацией — это означает, что опухоль содержит много лимфоцитов . Взаимодействие раковых клеток с лимфоцитами приводит к тому, что клетки опухоли распространяются через лимфоток и развиваются метастазы [1] .
Чаще всего ведущая роль в развитии рака носоглотки при вирусе Эпштейна — Барр принадлежит геномным изменениям, при которых активируется сигнальный путь NF-κB [5] . Этот путь связан с развитием воспаления, делением клеток и программируемой клеточной гибелью. Особую роль он играет в развитии B-лимфоцитов: при недостаточной активности NF-κB созревающие лимфоциты гибнут раньше времени, а при повышенной — могут развиваться злокачественные опухоли.
Вирус Эпштейна — Барр способен активировать путь NF-κB, а также механизмы уклонения от иммунитета, что приводит к неконтролируемому делению клеток и развитию рака [5] .
Связь потребления солёной рыбы с развитием рака объясняется тем, что консервирование в соли неэффективно и может приводить к частичному разложению рыбы. В результате в ней накапливаются нитрозамины. Считается, что они вызывают повреждение ДНК и хроническое воспаление в слизистой оболочке носоглотки, что способствует развитию рака [17] . Такая рыба содержит и другие вещества, которые активируют вирус Эптштейна — Барр и могут повышать риск развития рака [6] .
Классификация и стадии развития рака носоглотки
Согласно классификации Всемирной организации здравоохранения, выделяют три подтипа карциномы носоглотки:
- Ороговевающая плоскоклеточная карцинома, или кератинизирующий плоскоклеточный рак. В 85 % этот тип рака связан с вирусом Эпштейна — Барр.
- Неороговевающая плоскоклеточная карцинома. Бывает дифференцированной и недифференцированной, причём второй тип такой карциномы — самая распространённая форма рака носоглотки.
- Базалоидная плоскоклеточная карцинома — редкий тип опухоли [1][16] .
Международная классификация рака носоглотки по системе TNM (2017 г.) [7]
Наглядно это можно показать так:

Осложнения рака носоглотки
Характер осложнений зависит от распространения рака:
- При прорастании опухоли в область глазницы пациент может потерять зрение.
- При опухолях в области ротоглотки возникает спазм жевательных мышц, нарушается жевание и глотание, что способствует истощению и потере веса.
- Распространение опухоли в кости черепа и головной мозг может вызывать сильную головную боль. При сдавливании нервной ткани может нарушиться дыхание и речь.
- Массивная опухоль проявляется интенсивными носовыми кровотечениями. При распаде опухоли появляется неприятный гнилостный запах изо рта.
- При выраженном поражении шейных лимфоузлов затруднена подвижность шеи, возникает боль в ней, из-за чего нарушается сон[4] .
При распространённом онкологическом процессе, наряду с сильной болью в области головы и/или шеи, может развиться кахексия, анорексия и анемия, что проявляется, прежде всего, выраженной слабостью [18] [19] .
Диагностика рака носоглотки
Лабораторная диагностика
При первичной диагностике, а также для дальнейшей оценки эффективности лечения может проводиться анализ крови на вирус Эпштейна — Барр (количественное определение ДНК методом ПЦР) [9] . С помощью этого анализа можно быстро и недорого оценить эффективность лечения.
Инструментальная диагностика
- Эндоскопия носоглотки — для постановки диагноза проводится осмотр первичной опухоли. Наилучший обзор достигается с помощью гибкого или жёсткого носового эндоскопа. При заполнении опухолью всей полости носоглотки наиболее информативен осмотр через полость рта с помощью 30 ° или 70 ° жёсткого гортанного эндоскопа [1] . Если эндоскопа нет, может использоваться носоглоточное зеркало [11] .

- МРТ (предпочтительно) и/или КТ носоглотки с контрастом — позволяют оценить распространение опухоли и определить стадию болезни.
- УЗИ шейных лимфоузлов — можно выявить изменённые лимфатические узлы. В сочетании с биопсией позволяет подтвердить или исключить метастазы в лимфоузлах.
- УЗИ брюшной полости и забрюшинного пространства — позволяет выявить метастазы в печени и сопутствующие патологии (кисту, мочекаменную болезнь, аденому надпочечников, цирроз печени и др.). Если обнаружены узловые образования, то для уточнения их характера проводится КТ или МРТ брюшной полости с контрастом.
- КТ грудной клетки — позволяет выявить или исключить метастазы в лёгких и сопутствующие болезни (туберкулёз, пневмонию, саркоидоз и др.).
- ПЭТ-КТ — показана при подозрении на распространённый процесс. Также это обследование проводят после лучевой или химиолучевой терапии, чтобы подтвердить полное рассасывание метастазов, выявить возможный рецидив и понять, нужна ли операция по удалению лимфоузлов (лимфаденэктомия) [1][3] .
Биопсия
Для гистологического подтверждения диагноза выполняется биопсия. Образец ткани берут через нос или через рот.
Консультации других врачей
До и после лечения пациентам потребуются консультации смежных специалистов:
- Стоматолог — обучает правильной гигиене полости рта и при необходимости проводит лечение зубов и дёсен. Санация полости рта, проведённая до начала лучевой терапии, позволяет снизить частоту и тяжесть лучевых мукозитов. При выраженном мукозите приходится делать перерыв в лучевой терапии, что плохо влияет на результаты лечения.
- Эндокринолог — консультация проводится после лучевой терапии. Она необходима, потому что после лечения, в среднем через 6-12 месяцев, может развиться постлучевой гипотиреоз. Врач оценивает уровень тиреотропного гормона (ТТГ) через 6, 12,18, 24 месяца после лечения. Также может потребоваться УЗИ щитовидной железы.
- Репродуктолог — консультирует молодых пациентов перед химиотерапией по вопросам фертильности [11] .
По показаниям может потребоваться консультация офтальмолога, оториноларинголога, сурдолога и логопеда.
Оценка нутритивного статуса
Нутритивная поддержка — это лечебное питание, цель которого обеспечить организм всеми необходимыми веществами. Нутритивная поддержка позволяет скорректировать уровень макро- и микронутриентов, улучшить переносимость и ослабить побочные эффекты химио- и лучевой терапии, повысить качество жизни.
Онколог оценивает нутритивный статус как до лечения, так и на всех этапах терапии.
Необходимость нутритивной поддержки определяется по следующим показателям: индекс массы тела (ИМТ) меньше 20, похудение более чем на 5 % за полгода, невозможность есть через рот, среднее или тяжёлое поражение тонкого кишечника, уровень белка в плазме крови менее 60 г/л, уровень альбумина менее 30 г/л. При лечении эти показатели желательно оценивать раз в 7 дней.

Дифференциальная диагностика
Рак носоглотки следует отличать:
- от плоскоклеточной и инвертированной папилломы;
- доброкачественных и злокачественных заболеваний малых слюнных желёз (онкоцитомы, полиморфной аденомы, аденокарциномы, цистаденокарциномы);
- доброкачественных и злокачественных новообразований мягких тканей (юношеской ангиофибромы, нейрофибромы, шванномы, хемодектомы, фибросаркомы, рабдомиосаркомы, нейрофибросаркомы);
- опухолей лимфоидной и кроветворной ткани (лимфосаркомы, ретикулосаркомы, плазмоцитомы, болезни Ходжкина);
- опухолей смешанного происхождения (солидной тератомы, дермоидной кисты, гипофихарной аденомы, менингиомы, хордомы, краниофарингиомы); ;
- эстезионейробластомы;
- метастазов других опухолей в носоглотку, но такие случаи очень редки;
- опухолеподобных состояний (псевдоэпителиальной гиперплазии, онкоцитарной метаплазии и гиперплазии, кисты, гемангиомы, фиброматоза, амилоидоза, инфекционной гранулёмы, гранулёмы Стеварта, гранулематоза Вегенера); и полипозного риносинусита [4] .
Лечение рака носоглотки
Злокачественные опухоли носоглотки высокочувствительны к химио- и лучевой терапии, поэтому эти методы предпочтительны для первичного лечения [11] .
При I стадии рака носоглотки показана лучевая терапия [3] . На этой стадии её проводят без химиотерапии: не доказано, что химиолучевое лечение повышает выживаемость по сравнению с лучевой терапией, но побочных эффектов возникает больше.
При II-IVA стадиях рекомендуется провести химиолучевую терапию с последующей химиотерапией или химио-, а затем химиолучевую терапию [3] . Если после проведённого лечения останутся метастазы в шейных лимфоузлах, потребуется операция. Хирургически удалить опухоль носоглотки очень сложно, поэтому в качестве первичного лечения операция не рассматривается [1] .
При IVB стадии (наличии отдалённых метастазов) назначается химиотерапия с препаратами платины [8] . После химиотерапии может проводиться лучевая и химиолучевая терапия, симптоматическое лечение, операция (при единичном метастазе) [3] .
Основной побочный эффект лучевой терапии в области головы и шеи — это мукозит (эпителиит), который проявляется болью и воспалением слизистой оболочки полости рта. При заболевании затруднён приём пищи, тяжело говорить, иногда трудно открывать рот. Полностью предотвратить это осложнение нельзя, но его течение можно облегчить. Для этого до лечения нужно обратиться к стоматологу, чтобы провести санацию полости рта, а также соблюдать рекомендации врача во время терапии.
Самым грозным осложнением лучевой терапии является остеомиелит. Как правило, заболевание развивается при удалении зуба после лучевой терапии. Удалять плохие зубы нужно за 14 дней до лучевой терапии, в течение двух лет после лечения следует избегать манипуляций, затрагивающих кость челюсти.
Прогноз. Профилактика
Прогноз зависит от времени постановки диагноза, степени распространения опухоли в носоглотке и наличия метастазов [16] . Пятилетняя выживаемость при I стадии составляет 98 %, при II стадии — 92 %, при III стадии — 83 %, при IVA стадии —71 % [12] .
Высокие изначальные или сохраняющиеся к концу лучевой терапии уровни ДНК вируса Эпштейна — Барр являются признаком неблагоприятного прогноза [14] [16] .
Профилактика рака носоглотки
Первичная профилактика. В некоторых исследованиях выявлено, что риск развития рака носоглотки снижается при употреблении фруктов и овощей: моркови, китайской капусты, зелёных листовых овощей, свежих соевых продуктов, апельсинов и мандаринов. Также риск развития болезни был ниже при приёме витаминов Е, С, А по отдельности или в сочетании. Защитное действие фруктов и овощей можно объяснить тем, что они оказывают антиоксидантный эффект и предотвращают образование нитрозаминов [6] .
При наличии профессиональных факторов риска снизить вероятность развития рака носоглотки можно с помощью средств защиты.
Не существует стандартных скрининговых тестов для определения рака носоглотки. Скрининг с тестом на антитела к вирусу Эпштейна — Барр или на ДНК вируса не помог снизить смертность от рака носоглотки [13] .
Вторичная профилактика заключается в знании симптомов, своевременном обращении за медицинской помощью и онконастороженности врачей — повышенной бдительности к симптомам, которыми может проявляться рак.
Во время лечения важно предотвратить развитие побочных эффектов, чтобы не пришлось прерывать цикл терапии. При прохождении химиотерапии рекомендуется заниматься ЛФК, будет полезна психологическая поддержка и курс массажа для уменьшения слабости. Также следует лечить стоматит, гематологические осложнения, ксеростомию и спазм жевательных мышц [3] [10] [20] .
Курильщикам необходимо бросить курить, а бывшим курильщикам воздержаться от курения [11] .
После завершения лечения нужно посещать врача:
- в первый год — раз в 1-3 месяца;
- во 2-й год — раз в 2-6 месяцев;
- на 3-5-й год — каждые 4-8 месяцев, далее раз в год.
При возникновении новых симптомов необходимо сразу же обратиться к врачу.
Алгоритм обследования пациентов со злокачественными опухолями полости рта и ротоглотки
Актуальность проблемы. Злокачественные опухоли полости рта и ротоглотки составляют по данным разных авторов около 2-5% от всех злокачественных новообразований и число новых случаев растет. Морфологически 90% таких опухолей приходится на плоскоклеточный рак (ПКР). Соотношение мужчин и женщин - 3:1. Средний возраст больных - 60 лет [1,2].
Несмотря на визуальную локализацию, диагностика злокачественных опухолей орофарингеальной зоны представляет определенные трудности. Оценка распространенности опухолевого процесса в полости рта производится при визуальном осмотре и пальпаторном исследовании, которое не позволяет оценить распространенность опухолевого инфильтрата за пределы видимых изменений слизистой [3]. Для оценки размера первичной опухоли, ее местного распространения в мышечную ткань и на слизистую оболочку, а также в шейные лимфатические узлы, клиническое обследование бывает недостаточным, т.к. часто недооценивается объем опухоли, особенно в случае поздней стадии заболевания ввиду склонности таких опухолей к распространению по подслизистой основе. В большинстве случаев сложно оценить поражение костных структур, протяженность поражения по нижней челюсти [4,5,6]. Изучение возможностей мультиспиральной компьютерной томографии (МСКТ), МСКТ с болюсным внутривенным контрастированием и магнитно-резонансной томографии (МРТ) при диагностике новообразований орофарингеальной зоны необходимо для долечебного стадирования опухолевого процесса, создания концепции консервативного (химиолучевого) лечения, а также дальнейшего планирования тактики и объема оперативного вмешательства. Также существует потребность в доработке и усовершенствовании алгоритма обследования пациентов с данной патологией.
Цель исследования. Оценить возможности МСКТ с внутривенным контрастированием и МРТ в выявлении и долечебном стадировании рака полости рта и ротоглотки. Усовершенствовать алгоритм лучевого обследования больных с опухолевым поражением орофарингеальной зоны.
Материалы и методы. МСКТ-исследования полости рта и ротоглотки проводились на аппарате Bright Speed 16 (General Electric). Сканирование выполнялось в спиральном режиме с толщиной томографического среза 2,5 мм, с шагом томографирования 2,5 мм до и поcле внутривенного болюсного введения контрастного вещества. Контрастное усиление достигалось путем введения 100 мл неионного контрастного вещества при скорости введения 3 мм/сек, время задержки сканирования 40 секунд. Зона сканирования включала в себя область от основания черепа до яремной вырезки. Сырые данные повторно реконструировали с шагом реконструкции 1.25 мм. В последующем выполнялось построение многоплоскостных реформаций изображений (МРR) на рабочей станции. МРТ проводилась на аппарате «Excelart Vantage» 1,5 Т (Toshiba). Исследования дна полости рта методом МРТ проводилось в режимах Т1-ВИ, Т2-ВИ, STIR в сагиттальной, коронарной и трансверзальной проекциях с толщиной среза 5 мм с использованием шейной катушки. В исследовании участвовали 50 пациентов (45 мужчин, 5 женщин) в возрасте от 41 до 73 лет. Результаты во всех случаях сопоставлялись с данными, полученными при патогистологических и интраоперационных исследованиях.
Результаты. Из 50 пациентов у 12 человек (24%) опухоль располагалась в области языка, у 15 пациентов (30%) в области дна полости рта, на миндалинах у 16 человек (32%), мягком небе - 5 человек (10%), слизистая щеки - 1 пациент (2%), альвеолярный отросток - 1человек (2%). По распространенности опухолевого процесса 29 пациентов были с Т3 стадией (58%), 7 пациентов с Т4 (14%), 12 пациентов с Т2 (24%), 2-с Т1(4%). По степени поражения лимфатических узлов 14 человек с N1(28%) стадией, 10 - с N2(20%), у 2 человек - N3 стадия (5%). В 2 случаях (4%) было выявлено поражение нижней челюсти.
Анализ результатов МСКТ и МРТ у больных с установленным диагнозом рака орофарингеальной зоны включал оценку размеров опухоли, распространенности опухолевого процесса по мышцам и костным структурам, переход за среднюю линию, степень инфильтрации межмышечной и подкожной клетчатки, поражение лимфатических узлов. Было установлено, что МСКТ - семиотика плоскоклеточного рака полости рта и ротоглотки соответствует МРТ-семиотике и включает в себя прямые и косвенные признаки. Прямыми признаками злокачественной опухоли являлись объемное разрастание патологической ткани, истончение жирового слоя или полная облитерация жировых пространств, инфильтрация мышечной ткани и костная деструкция. Косвенными признаками были структурная неоднородность ткани (при наличии некроза), изменение показателей плотности после введения контрастного вещества при МСКТ - исследовании и изменение сигнала при МРТ.
С помощью КТ сложно было выявлять опухоли малых размеров (Т1стадия) и их границы в результате низкой контрастности, а также новообразования с поверхностным распространением (рис. 1). Вместе с тем, 72,0% обследованных больных имели Т3, Т4 стадии опухолевого процесса и после болюсного введения контрастного вещества контрастность опухоли повышалась. С увеличением размера опухоли отмечалась неоднородность усиления из-за наличия некроза (рис. 2). Жировые пространства подъязычной области в нормальном состоянии представляют собой симметричную зону низкой плотности между челюстно-подъязычной и подбородочно-подъязычной мышцами. Облитерация жировых пространств подъязычной области служила основным показателем опухолевого поражения при выявлении небольших образований дна полости рта (рис. 3,4).

Рис.1. Пациент Ж., 58 лет. МСКТ ротоглотки в аксиальной проекции: А - нативное исследование, В - с внутривенным болюсным контрастированием. Небольшая инфильтративная опухоль ротоглотки (левой небной миндалины Т1 стадии). Границы опухоли не дифференцируются, накопление контраста слабое (показатели плотности в нативной фазе исследования 45 ед.Н, после внутривенного болюсного усиления - 56 ед.Н). Определяется смещение левой стенки ротоглотки, сглаженность контура (стрелки)
Рис. 2. Пациент К., 65 лет. МСКТ полости рта с внутривенным болюсным контрастированием в аксиальной проекции. Опухоль передних отделов дна полости рта Т4 стадии. Выявляется опухолевое образование размерами 4,5х3,5 см (стрелки) неоднородной структуры. Отмечается инвазия опухоли в нижнюю челюсть
Рис.3. Пациент Ч.,54 года. МСКТ в аксиальной проекции с внутривенным болюсным контрастированием. Небольшая опухоль дна полости рта с переходом за среднюю линию (стрелки). Инфильтрация жировых пространств дна полости рта
Рис.4. Пациент П., 48 лет. МСКТ полости рта с внутривенным болюсным контрастированием. В передних отделах дна полости рта центрально и слева дифференцируется участок низкой плотности размерами 0,8х0,4 см (стрелки). Накопление контраста слабое, показатели плотности 65-67 ед.Н. Границы опухоли четко не определяются, при этом распространения за среднюю линию не обнаружено. Отмечается облитерация жировой клетчатки подъязычной области слева. Справа жировые прослойки дифференцированы, мышцы не изменены. Лимфатические узлы шеи не увеличены
Сложно было выявлять опухоли малых размеров (Т1,Т2 стадии), расположенные в передних отделах дна полости рта из-за расположенных рядом костных тканей, зубов, наличия пломбировочного материала вследствие выраженных артефактов от плотных структур. В ряде случаев визуализацию облегчало наличие язвенного дефекта в структуре опухоли (рис. 5). При всех опухолях Т3, Т4 стадии определялось повышение плотности после введения контрастного вещества, их края четко визуализировались относительно окружающих тканей. Во всех случаях Т3, Т4 стадии удавалось определить размер опухоли и оценить инфильтрацию и распространение в соседние зоны, а также за среднюю линию (рис. 6).
Особенностью МРТ являлась высокая контрастность мягких тканей. Плотные костные ткани или зубоврачебный материал не создавали артефактов, что давало возможность получать четкое изображение опухоли полости рта, определять распространение в мягкие ткани, глубокие отделы орофарингеальной зоны, в область неба. На Т1-ВИ все опухоли имели ту же интенсивность сигнала, как у окружающих мышц или слабее (рис.7).
Рис. 5. Пациент З.,61 год. МСКТ ротоглотки в аксиальной проекции с внутривенным болюсным контрастированием. Опухоль Т2 стадии левой боковой поверхности языка в средней трети. Щелевидная язва, окруженная ободком повышенной плотности (стрелки)
Рис.6. Пациент З., 73года. МСКТ полости рта, ротоглотки в аксиальной проекции с внутривенным болюсным контрастированием. В области корня языка и средней трети визуализируется опухолевый узел размерами 6,4х4,5 см без признаков некроза, с инфильтрацией жировых пространств справа (стрелки). Опухоль накапливает контраст, повышая плотность до 80 ед.Н
Рис.7. Пациент С., 55 лет. МРТ ротоглотки в сагиттальной проекции в режиме Т1-ВИ. Опухоль дна полости рта с переходом на нижнюю поверхность языка (стрелки)
После введения контрастного вещества все опухоли показывали усиление сигнала. При локализации опухолевого процесса в области языка (12 пациентов) границы опухоли визуализировались более четко. В режиме Т2-ВИ опухолевые узлы проявлялись более высокой интенсивностью сигнала, чем у окружающих мышц (рис. 8).
Сложно было с помощью МРТ визуализировать опухоли любых размеров с поверхностным распространением, не выходящие за пределы слизистой оболочки. Опухоли малых размеров (Т1 стадия) в 2 наблюдениях были однородны, не имели центральной зоны некроза и сливались с мышцами. С увеличением размера опухолевого узла отмечалась неоднородность структуры. В наших исследованиях удалось выявить небольшие опухоли Т1 и Т2 стадий, локализованные в области языка и дна полости рта. В 9 наблюдениях опухоли Т2 стадии, не накапливающие контраст при МСКТ исследовании, хорошо визуализировались при МРТ в режимах Т2-ВИ, STIR, проявляясь сигналом высокой интенсивности. Можно было четко видеть границы опухоли и оценить ее размеры (рис. 9,10).
Рис. 8. Пациент П., 76 лет. МРТ полости рта в сагиттальной проекции в режиме Т2-ВИ. Опухоль языка, высокая интенсивность сигнала на фоне окружающих мышц (стрелки)

Рис. 9. Пациент А., 66 лет. МРТ дна полости рта в сагиттальной проекции в режиме Т2-ВИ. Опухоль дна полости рта размерами 2,0х1,8 см с распространением на основание языка Т1N0M0 (стрелки). Границы опухоли четко визуализируются, структура однородная
Не возникало сложностей в выявлении опухолевых узлов Т3, Т4 стадий, имевших все отмеченные выше признаки в различных сочетаниях в 36 исследованиях (рис. 11). Из 50 обследованных с помощью МСКТ и МРТ пациентов у 26 (52,0%) были выявлены метастазы в лимфатических узлах шеи. Поражались преимущественно лимфатические узлы I-II уровня. Признаками метастаза плоскоклеточного рака в лимфатических узлах были: увеличение размера лимфатического узла более 1,0 см, изменение формы лимфатического узла с бобовидной на округлую, структурные нарушения в узле, нечеткость наружных контуров узла, уплотнение окружающей жировой ткани на КТ или изменение сигнала на МРТ.
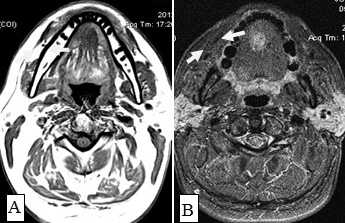
Рис. 10. А. Пациент Е., 52 года. МРТ полости рта, ротоглотки в аксиальной проекции, Т1-ВИ. Опухоль языка небольших размеров, границы визуализируются с трудом за счет перифокального отека (стрелки); В. Тот же пациент. МРТ в аксиальной проекции, Т2 с подавлением сигнала от жировой ткани. Визуализируются границы опухолевого узла, размеры опухоли языка четко определяются (стрелки)
Рис. 11: А. МРТ полости рта, ротоглотки в аксиальной проекции. Рецидив опухоли языка размерами 6,0х6,5 см с распространением на дно полости рта, правую боковую стенку ротоглотки (стрелки). Выявляется переход за среднюю линию; В. Тот же больной. МРТ полости рта, ротоглотки в коронарной проекции. Опухолевый узел показан стрелками. Просвет ротоглотки сужен, деформирован. Опухоль имеет низкий сигнал на Т1-ВИ, аналогичный сигналу от окружающих мышц, при этом размеры опухолевого узла, его объемные характеристики позволяют четко отграничить от интактных тканей. Также отмечается структурная неоднородность патологического образования за счет некроза
Большинство пораженных метастазами лимфатических узлов имели размеры более 1,0 см, округлую форму (рис. 12). Внутривенное контрастирование при оценке изменений в лимфатическом узле являлось обязательным условием для уточнения внутренней структуры и выявления зон некроза. В результате гипоксии и распада ткани формируется центральная зона некроза, не накапливающая контрастный препарат при внутривенном болюсном усилении. При этом отмечается повышение плотности в периферических отделах лимфатического узла (рис. 13).
Рис. 12. Пациент П., 68 лет. МРТ полости рта, ротоглотки в коронарной проекции. Выявляется увеличенный подчелюстной лимфатический узел округлой формы, неоднородной структуры (стрелки)
Рис. 13. Пациентка К.,64 года. МСКТ ротоглотки, шеи в аксиальной проекции с внутривенным болюсным контрастированием. Рак языка с метастазами в лимфатические узлы средней яремной группы. Отмечается контрастирование пораженных лимфатических узлов по периферии, низкой плотности центральная зона некроза (стрелки). Билатеральное поражение
Рис. 14. Пациент К., 56 лет. МСКТ полости рта в аксиальной проекции в костном режиме. Выявленная в мягкотканном режиме опухоль дна полости рта слева прилежит к слизистой оболочке альвеолярного края нижней челюсти. В костном режиме выявляется очаг деструкции кортикального слоя нижней челюсти слева
Клиническая оценка инвазии опухоли в нижнюю челюсть проводилась на основании клинических симптомов и признаков, а также выполняли пальпацию двумя руками для оценки степени подвижности опухоли относительно нижней челюсти. При этом результаты клинического осмотра всегда требовали корреляции с данными визуализирующих исследований. От степени распространения опухоли зависит объем резекции в соответствии с онкологическими требованиями.
В наших исследованиях у 4 пациентов (3,0%) с первично установленным диагнозом опухолевого поражения полости рта выявлена деструкция нижней челюсти. Очаги лизиса были представлены на КТ-изображениях в виде участков нарушения целости или эрозий кортикального слоя. Признаком поражения костного мозга при КТ была замена низкой плотности нормальной жировой ткани на плотность мягких тканей (рис. 14).
При МРТ-исследованиях оценка инфильтрации костной ткани проводилась по следующим показателям: отсутствие типичного гипоинтенсивного сигнала от кортикального слоя на Т1-ВИ и Т2-ВИ, появление сигнала высокой или средней интенсивности на Т1-ВИ и Т2-ВИ, соответствующего опухолевой ткани, появление гипоинтенсивного сигнала на Т1, гиперинтенсивного сигнала на Т2 или Т2 с подавлением сигнала от жировой ткани, что демонстрировало поражение костного мозга (рис. 15).
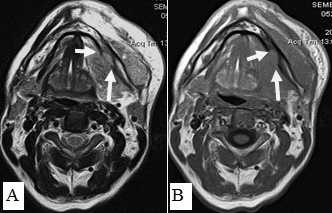
Рис. 15. Пациент С.,52 г. МРТ полости рта в аксиальной проекции в режиме Т2-ВИ (А) и Т1-ВИ (В). Рак дна полости рта с распространением на нижнюю челюсть, инфильтрацией мягких тканей щечной, подбородочной области слева. Выявляется деструкция кортикального слоя нижней челюсти слева, поражение костного мозга (стрелки)
Выводы. МСКТ и МРТ являются высокоэффективными методами в обнаружении опухолей полости рта и ротоглотки, а также в оценке степени распространения опухолевого процесса. Алгоритм лучевого обследования пациентов с опухолевым процессом данной локализации должен включать обязательное МСКТ-исследование с внутривенным болюсным контрастированием. МРТ следует рассматривать как метод выбора у пациентов с опухолями малых размеров, в случаях низкой контрастности опухоли на МСКТ-изображениях, а также при наличии выраженных артефактов от зубоврачебного материала, костей. Использование предложенного алгоритма обследования позволяет получать всю необходимую информацию за короткое время одного исследования, не удлиняя период обследования онкологического больного.
Список использованных источников:
1. Аксель Е.М. Злокачественные новообразования в странах СНГ// Матер. III съезда онкологов и радиологов СНГ. - Минск, 2004. - Ч. 1. - С. 210-211.
2. Чиссов В.И., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2007 году. - М. - 2009. - 244 с.
3. Lenz M., Greess H., Baum U., Dobritz M., Kersting-Sommerhoff B. Oropharynx, oral cavity, floor of the mouth: CT and MRI// Eur J Radiol. 2000 Mar;33(3):203-15.
4. Mukherji S.K., Isaacs D.L., Creager A., Shockley W., Weissler M., Armao D. CT detection of mandibular invasion by squamous cell carcinoma of the oral cavity// Am J Roentgenol. 2001 Jul;177(1):237-43.
5. Lenz M., Hermans R. Imaging of the oropharynx and oral cavity. Part II: pathology// Eur. Radiol. 1996;6:536-49.
6. Yuasa K., Kawazu T., Nagata T et al. Computed tomography and ultrasonography of metastatic cervical lymph nodes in oral squamous cell carcinoma// Ultrasound Q. 2010; 26(1):45-51.
Подписано в печать: 07.05.2013
Плоскоклеточный рак
Плоскоклеточный рак, или плоскоклеточная карцинома - это гистологический тип злокачественных опухолей, такой диагноз устанавливают по результатам биопсии после исследования образца опухолевой ткани под микроскопом. Новообразование формируется из плоских клеток эпидермиса, которые выглядят как чешуйки. Оно может возникать на коже, в полости рта, в гортани, трахее, бронхах, пищеводе, на половых органах, в прямой кишке.
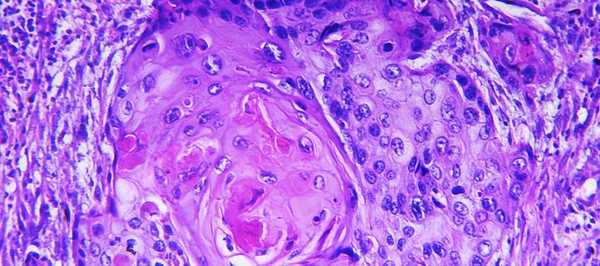
В «Евроонко» диагностикой и лечением плоскоклеточного рака занимаются врачи экспертного уровня, за плечами которых обширный опыт работы в ведущих онкологических центрах Москвы. С пациентом работает команда, в которую входят онкологи, дерматоонкологи, хирурги, химиотерапевты, радиотерапевты и другие специалисты. Мы применяем инновационные методы лечения, препараты последнего поколения, проводим противоопухолевую терапию в соответствии с ведущими международными рекомендациями. «Евроонко» - первый российский частный онкологический центр, в котором можно получить эффективное паллиативное лечение на поздних стадиях, даже в случаях, когда от пациента отказались в других клиниках.
Причины возникновения плоскоклеточного рака
Причины плоскоклеточного рака те же, что и для других типов злокачественных опухолей. В клетках происходят определенные мутации, которые приводят к злокачественному перерождению. «Неправильные» клетки утрачивают внешние черты и функции нормальных, начинают бесконтрольно размножаться, приобретают способность распространяться в организме.
Основные факторы риска плоскоклеточного рака:
- На коже такие опухоли часто возникают из-за действия ультрафиолетовых лучей. Наиболее уязвимы открытые участки тела.
- Плоскоклеточный рак половых органов, головы и шеи вызывают некоторые типы вируса папилломы человека.
- Риск развития плоскоклеточного рака повышен у курильщиков и людей, которые употребляют много алкоголя.
- Вероятность развития онкологического заболевания повышается с возрастом, так как в клетках тела накапливаются мутации.
- Шрамы, ожоги, хронический воспалительный процесс.
- Воздействие некоторых канцерогенных веществ, например, если человек работает на производстве и контактирует с химикатами.
- Снижение иммунитета.
Ни один из этих факторов не приводит гарантированно к заболеванию - каждый из них лишь в определенной степени повышает вероятность.
Какие бывают виды плоскоклеточного рака?
Злокачественные новообразования данного гистологического типа встречаются на разных частях тела. В зависимости от локализации, могут несколько различаться их свойства, подходы к диагностике и лечению, прогноз для пациента.

Рак кожи
Злокачественные опухоли кожи представлены плоскоклеточным раком примерно в 20% случаев. Намного чаще пациенты страдают базальноклеточным раком, который происходит из клеток, находящихся в нижнем слое эпидермиса.
Плоскоклеточный рак более агрессивен по сравнению с базальноклеточным. Он с большей вероятностью прорастет в глубокие слои кожи, будет распространяться в организме с образованием отдаленных метастазов. Тем не менее, это происходит довольно редко. Чаще всего опухоль удается обнаружить и удалить на ранней стадии.
Как правило, плоскоклеточный рак возникает на коже лица, ушей, шеи, тыльной стороне рук, реже - в области половых органов. Нередко новообразование развивается там, где находятся шрамы и хронические повреждения.

Плоскоклеточный рак красной каймы губ
Злокачественные опухоли губ составляют не более 1-3% от всех онкологических заболеваний. В большинстве случаев (95%) они представлены плоскоклеточным раком, который бывает двух типов:
- Плоскоклеточный ороговевающий рак ведет себя не так агрессивно, медленно растет, редко образует отдаленные метастазы.
- Плоскоклеточный неороговевающий рак растет быстро, раньше приводит к изъязвлению и чаще метастазирует.
Исследования показывают, что у мужчин этот тип рака встречается в 3-13 раз чаще, чем у женщин. Вероятно, это связано с тем, что представители мужского пола чаще подвергаются воздействию солнечных лучей на рабочем месте, среди них более распространено курение, употребление алкоголя.
Рак полости рта
Раком ротовой полости называют злокачественные опухоли, которые возникают на слизистой оболочке губ, щек, десен, передних двух третей языка, неба, дна ротовой полости (находится под языком). В 90% случаев они представлены плоскоклеточным раком, из них 5% - плоскоклеточный ороговевающий рак, который менее агрессивен, реже прорастает в окружающие ткани, распространяется в лимфатические узлы и метастазирует.
Рак пищевода
Слизистая оболочка пищевода выстлана многослойным плоским эпителием, и из него может развиваться плоскоклеточный рак. Чаще всего такие опухоли находятся в шейном отделе пищевода и верхних двух третях грудного отдела. В нижней трети органа чаще встречаются аденокарциномы - злокачественные опухоли из железистых клеток.
Рак гортани
При раке гортани опухоль практически всегда развивается из плоского эпителия и представляет собой плоскоклеточную карциному. Обычно возникновению опухоли предшествуют предраковые изменения - дисплазия. Клетки, которые находятся в очаге, внешне не похожи на нормальные, но отличаются и от раковых. В ряде случаев дисплазия не приводит к развитию рака и даже проходит самостоятельно, особенно если устранена ее причина, например, человек бросил курить. Но у некоторых людей предраковые изменения приводят к возникновению «рака на месте» (in situ), а затем инвазивной опухоли.

Рак трахеи и бронхов
Плоскоклеточный рак - наиболее распространенный тип злокачественных опухолей в трахее. Обычно он возникает в нижней части трахеи, довольно быстро растет, прорастает ее стенку, приводит к изъязвлениям и кровотечению. Это редкий тип рака, его основной причиной является курение.
Наиболее распространенным раком легкого является немелкоклеточный рак - он встречается в 80% случаев и в 30% случаев представлен плоскоклеточной карциномой. Нередко эти опухоли находятся в бронхах.
Рак шейки матки
Шейка матки состоит из двух частей. Экзоцервикс находится снаружи, во влагалище, это то, что видит гинеколог во время осмотра. Эндоцервикс - канал шейки матки, он соединяет матку с влагалищем. В норме экзоцервикс выстлан плоским эпителием, а эндоцервикс - железистым. Место, где они встречаются, называется зоной трансформации.
Плоскоклеточным раком представлены 90% злокачественных опухолей шейки матки. Чаще всего новообразование возникает в области зоны трансформации. Раки, которые развиваются из железистых клеток эндоцервикса, называются аденокарциномами.
В редких случаях в шейке матки встречается железисто-плоскоклеточный рак.
Рак вульвы
Вульвой называют наружные женские половые органы: преддверие влагалища, большие и малые половые губы, клитор. Большинство типов рака, которые развиваются в этой области, представлены плоскоклеточным раком (70-90%). Они делятся на две группы:
- Большая группа - опухоли, происхождение которых неизвестно. Чаще всего их диагностируют у женщин старшего возраста.
- Меньшая группа - злокачественные опухоли, вызванные вирусом папилломы человека.
Рак прямой кишки
В большинстве случаев злокачественные опухоли прямой кишки представлены аденокарциномами - железистым раком. Плоскоклеточный рак в этом органе встречается очень редко и составляет от 10 до 25 случаев на каждые 100 тысяч случаев колоректального рака.
Плоскоклеточный рак составляет 90% от всех злокачественных новообразований анального канала - узкого прохода, который соединяет прямую кишку с анусом.
Рак миндалин
У человека есть четыре вида миндалин: небные (при их воспалении развивается тонзиллит), трубные (находятся в глотке возле отверстий слуховых труб), язычная (позади языка) и глоточная (у детей из-за нее бывают аденоиды). Чаще всего злокачественные опухоли развиваются в небных миндалинах. В большинстве случаев это плоскоклеточный рак. Его сложно диагностировать, поэтому зачастую он выявляется на поздних стадиях.

Виды диагностики заболевания
Врач-онколог назначает пациенту те или иные виды диагностики, в зависимости от того, в каком органе находится злокачественная опухоль:
Место локализации рака
Методы диагностики
- Осмотр дерматолога.
- Дерматоскопия.
- В «Евроонко» применяется современная дерматоскопическая установка — ФотоФайндер. Она позволяет составить «карту родинок» и выявить мельчайшие изменения на коже.
- Осмотр ЛОР-врача.
- Фарингоскопия.
- Ларингоскопия.
- Бронхоскопия.
- Эзофагоскопия.
- Исследование на ВПЧ.
- Эндоскопическое исследование, в том числе эндоУЗИ.
- Рентгенография с контрастным усилением.
- КТ, МРТ.
- Рентгенография грудной клетки.
- Бронхоскопия.
- Осмотр гинеколога
- Осмотр гинеколога.
- Кольпоскопия.
- Осмотр врача-проктолога.
- Проктоскопия.
- Колоноскопия.
- Анализ кала на скрытую кровь.
Во всех случаях, когда обнаружено патологическое образование, проводят биопсию - исследование, во время которого получают фрагмент подозрительной ткани и отправляют в лабораторию для гистологического и цитологического исследования. Биопсия - самый точный метод диагностики рака. Она помогает не только достоверно установить диагноз, но и определить гистологический тип новообразования.Для того чтобы проверить степень распространения рака в организме и уточнить стадию, врач может назначить дополнительные исследования:
- компьютерную томографию, МРТ;
- рентгенографию грудной клетки, костей;
- ПЭТ-сканирование;
- УЗИ и эндоскопические исследования органов, в которые мог прорасти рак.
Лечение плоскоклеточного рака
Лечение зависит от локализации, стадии рака, общего состояния пациента, наличия у него сопутствующих заболеваний и других факторов.
Лучевая терапия
Ионизирующее излучение повреждает опухолевые и другие быстро размножающиеся клетки. Этот вид лечения плоскоклеточного рака может быть назначен до или после операции, либо на поздних стадиях в паллиативных целях.

Хирургия
Радикальные операции возможны, если нет метастазов, и не произошло сильное прорастание рака в окружающие ткани. В одних случаях таким пациентам показано только хирургическое лечение, в других его дополняют противоопухолевыми препаратами, лучевой терапией - это помогает снизить риск рецидива.
При запущенном плоскоклеточном раке может быть выполнено паллиативное хирургическое вмешательство, направленное на ликвидацию симптомов, восстановление проходимости и функции пораженного органа.
Медикаментозное лечение плоскоклеточного рака
Химиотерапия при плоскоклеточном раке может быть адъювантной (после операции), неоадъювантной (до хирургического вмешательства) или применяется в качестве самостоятельного метода лечения на поздних стадиях.
Если опухоль обладает определенными молекулярно-генетическими характеристиками, назначают таргетную терапию. Таргетные препараты прицельно воздействуют на молекулы, которые помогают раку расти и поддерживать свою жизнедеятельность.
Врачи «Евроонко» применяют при плоскоклеточном раке оригинальные противоопухолевые препараты последнего поколения, назначают их в соответствии с современными международными протоколами.
Симптоматическое лечение при плоскоклеточном раке
Лечение при плоскоклеточном раке и любых других злокачественных новообразованиях должно быть направлено не только на борьбу с самой опухолью, но и на купирование симптомов, улучшение состояния пациента. В «Евроонко» пациент может получить все виды симптоматической терапии при раке:
- Купирование болевого синдрома в соответствии с трехступенчатой схемой ВОЗ.
- Восстановление проходимости пищевода, кишечника, дыхательных путей.
- Устранение кровотечений, при необходимости - переливание крови.
- Купирование тошноты.
- Устранение сдавления опухолью внутренних органов, нервов, сосудов.
- Лечение экстренных состояний в условиях палаты интенсивной терапии, оснащенной современной аппаратурой.
- Контроль и коррекция нутритивного статуса.
- Поддерживающая терапия помогает комфортно перенести курс химиотерапии, предотвратить и купировать побочные эффекты.

Прогноз выживаемости при плоскоклеточном раке
Прогноз зависит от того, в каком месте начался рост рака, на какой стадии установлен диагноз и начато лечение. Например, зачастую выживаемость при раке кожи и красной каймы губ стремится к 100%, потому что такие опухоли, как правило, удается обнаружить достаточно рано, и они не очень агрессивны. Если появились отдаленные метастазы, шансы на ремиссию становятся крайне низкими. Но таким пациентам все еще можно помочь: затормозить прогрессирование плоскоклеточного рака, продлить жизнь, улучшить общее состояние, купировать мучительные симптомы.
Мы в «Евроонко» считаем, что безнадежных больных не бывает. Помочь можно всегда. Никогда не стоит сдаваться. Мы знаем, как помочь.
Читайте также:
