Лечение рака шейки матки у беременных - тактика
Добавил пользователь Валентин П. Обновлено: 21.01.2026
Рак шейки матки занимает первое место в структуре заболеваемости злокачественными опухолями женских половых органов. По сводным данным, среди злокачественных опухолей у беременных на первом месте стоит рак шейки матки: от 0,17 до 4,1 %.
Среди форм рака преобладают экзофитные и смешанные формы роста опухоли (в 74,3 %), с расположением в области эктоцервикса (в 89,2 %), кровоточащие (в 68,2 %).
Симптомы Рака шейки матки при беременности:
Одним из ведущих проявлений опухолевой прогрессии является снижение степени ее дифференцировки. Другой неблагоприятный фактор - глубокая инвазия опухоли в ткани шейки матки.
Снижение дифференцировки опухоли и ее глубокая инвазия способствуют быстрому распространению за пределы органа. Во время операции по поводу сочетания рака шейки матки и беременности в 2 раза чаще обнаруживают метастазы в регионарных лимфатических узлах таза.
Результаты исследования клеточного иммунитета указывают на угнетение клеточного иммунитета уже в I триместре беременности у больных с I стадией заболевания.
Диагностика Рака шейки матки при беременности:
В I триместре беременности симптом маточного кровотечения нередко расценивается как начинающийся выкидыш, во II и III триместрах - как акушерская патология: предлежание или преждевременная отслойка плаценты. Во многих случаях у беременных не производят тщательного осмотра шейки матки при помощи зеркал; редко применяют цитологическое исследование и кольпоскопию. Положение усугубляется из-за необоснованной боязни биопсии. Осуществление цитологического скрининга позволяет получить сведения о частоте выявления рака шейки матки среди беременных (у 0,34 %). При этом частота преинвазивного рака составляет 0,31 %, инвазивного - 0,04 %.
В настоящее время основой для выявления ранних форм рака шейки матки считается двухэтапная система диагностики:
- цитологический скрининг при гинекологическом осмотре;
- углубленная комплексная диагностика при выявлении визуальной или цитологической патологии.
По мнению многих клиницистов, беременность большого срока и послеродовой период оказывают неблагоприятное влияние на клиническое течение рака шейки матки.
Лечение Рака шейки матки при беременности:
Врачебную тактику при лечении беременных, больных раком шейки матки, трудно ограничить жесткими рамками определенной схемы. Нельзя согласиться с принципом: лечить рак, учитывая стадию и игнорировать беременность. Необходим строго индивидуальный подход, причем существенную роль играет срок беременности.
При раке insitu шейки матки в I триместре беременности и после родов лечение заключается в прерывании беременности и конусовидной эксцизии шейки матки. Во II и III триместрах осуществляется диагностическое кольпоскопическое и цитологическое наблюдение. Через 2-3 мес после родоразрешения производят конусовидную эксцизию шейки матки.
При II стадии заболевания в I, II триместрах беременности и после родов производят экстирпацию матки с верхней третью влагалища.
При IА стадии в I, II триместрах беременности и после родов осуществляется расширенная экстирпация матки; в послеоперационном периоде при глубокой инвазии и регионарных метастазах проводят дистанционное облучение. В III триместре беременности производят кесарево сечение с последующей расширенной экстирпацией матки. В послеоперационном периоде используют дистанционную лучевую терапию.
При IВ стадии в I, II, III триместрах беременности производят расширенную экстирпацию матки с последующим дистанционным облучением. После родов лечение заключается в предоперационном облучении; в выполнении расширенной экстирпации матки и проведении в послеоперационном периоде при глубокой инвазии и регионарных метастазах дистанционного облучения.
При II стадии заболевания в I триместре беременности и после родов проводят сочетанное лучевое лечение (внутриполостное и дистанционное). Не следует стремиться к искусственному прерыванию беременности в I триместре при II и III стадиях заболевания, поскольку самопроизвольные выкидыши наступают на 10-14-й день от начала лучевой терапии. Если ПВ стадия заболевания диагностирована во II и III триместрах беременности, производят кесарево сечение и сочетанное лучевое лечение в послеоперационном периоде.
При III стадии заболевания в I триместре беременности и после родов лечение начинают с сочетанно-лучевой терапии (внутриполостное и дистанционное облучение). Во II и III триместрах беременности лечение начинают с кесарева сечения с последующей сочетанной лучевой терапией.
У женщин, страдающих пре- и микроинвазивным раком шейки матки и желающих иметь детей, возможно осуществление функционально-щадящих методов лечения: электроконизации, криодеструкции, ножевой и лазерной ампутации шейки матки. В этом случае беременность и роды не оказывают неблагоприятного влияния на течение основного заболевания. Частота рецидивов после органосохраняющего лечения начальных форм рака шейки матки составляет 3,9 %; частота рецидивов в популяции - 1,6-5,0 %.
Частота наступления беременности после органосохраняющего лечения начальных форм рака шейки матки составляет от 20,0 до 48,4 %.
Пролонгирование беременности целесообразно не ранее 2 лет после функционально-щадящего лечения патологии шейки матки. Ведение родов через естественные родовые пути не противопоказано. Отмечено повышение частоты невынашивания беременности и преждевременных родов по сравнению со здоровыми женщинами. Наблюдается более высокий уровень перинатальной смертности (11,5 %). Повышение частоты преждевременного прерывания беременности после органосохраняющего лечения патологии шейки матки свидетельствует о необходимости применения профилактических мероприятий (спазмолитики, токолитики, антиагреганты, постельный режим). Родоразрешение путем кесарева сечения осуществляют лишь по акушерским показаниям. Диспансерное наблюдение после перенесенного функционально-щадящего лечения начальных форм рака шейки матки включает в себя обследование в 1-й год не реже 6 раз; во 2-й - 4 раза; в последующие - 2 раза в год.
К каким докторам следует обращаться если у Вас Рак шейки матки при беременности:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Рака шейки матки при беременности, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Рак шейки матки при беременности
Рак шейки матки при беременности — это злокачественное новообразование, которое происходит из трансформационной зоны, экзоцервикса, эндоцервикса и выявляется в период беременности. Более чем в двух третях случаев протекает бессимптомно. При манифестном течении проявляется контактной кровоточивостью, спонтанными влагалищными кровотечениями, лейкореей, болью внизу живота, нарушением функции тазовых органов. Диагностируется на основании данных гинекологического осмотра, ПЦР, цитологического анализа, кольпоскопии, гистологии биоптата. Для лечения используют органосохраняющие и радикальные хирургические вмешательства, лучевую и химиотерапию.
МКБ-10
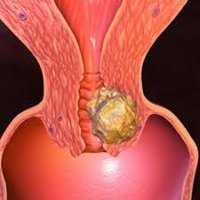
Общие сведения
Рак шейки матки (РШМ) — самая распространенная онкопатология, выявляемая у беременных. 1-3% расстройства диагностируется именно в гестационном периоде. В зависимости от региона распространенность заболевания составляет от 1,2 до 10 случаев на 10 000 беременностей. Гестация наступает у 3,1% пациенток с ранее установленным диагнозом РШМ. Болезнь чаще выявляют у сексуально активных курящих женщин, которые начли интимную жизнь до 16 лет, имеют более 2-3 половых партнеров в год, инфицированы вирусом папилломатоза человека (ВПЧ, HPV), а зачастую и другими генитальными инфекциями (хламидиозом, трихомонозом, сифилисом, гонореей, уреаплазмозом).

Причины
В подавляющем большинстве случаев злокачественное перерождение слизистой экзо- и эндоцервикса начинается задолго до гестации. Неоплазия ассоциирована с вирусами папилломатоза человека, передаваемыми при половых контактах. ДНК-содержащие папилломатозные вирусы определяются у 95% пациенток с подтвержденным диагнозом рака шейки матки. В 65-75% случаев провоцирующим фактором считаются вирусные агенты 16 и 18 серотипов, реже — HPV 31, 33, 35, других типов высокого и среднего риска. Инфицированность ВПЧ в женской популяции составляет 5-20%. У большинства пациенток вирус длительно персистирует без каких-либо клинических проявлений.
Факторы, способствующие повышению его патогенности и началу онкопроцесса, пока не выявлены. Несмотря на теоретическую возможность ускорения канцерогенеза на фоне физиологического снижения иммунитета при беременности, убедительные данные о негативном влиянии гестации на течение злокачественного процесса в шейке матке на сегодняшний день отсутствуют. Более того, по наблюдениям специалистов в сфере онкогинекологии, у двух третей беременных отмечается регресс предраковых состояний.
Обнаружению РШМ в период гестации благоприятствует ряд обстоятельств. Во-первых, многие пациентки из группы риска вне беременности крайне редко посещают медицинские учреждения с профилактической целью. Постановка на учет в женской консультации с целью получения медицинской помощи и социальных выплат предполагает регулярное наблюдение специалиста и выполнение скрининговых обследований, в ходе которых может быть обнаружен рак. Во-вторых, к 20-й неделе гестационного срока у большинства беременных происходит смещение кнаружи зоны трансформации и стыка цилиндрического шеечного эпителия с плоским влагалищным. В результате участок слизистой шейки, чаще всего поражаемый раком, становится хорошо заметным и доступным для проведения цитологического скрининга, кольпоскопии и других исследований.
Патогенез
Хотя вероятность заражения папилломавирусной инфекцией достигает 75%, у 90% женщин иммунная система быстро элиминирует возбудителя. В 10% случаев вирусные частицы персистируют в базальных эпителиальных клетках и могут регрессировать. Лишь у некоторых пациенток под влиянием неустановленных факторов ВПЧ начинает прогрессировать. ДНК вирусов встраивается в геном клеток эпителия шейки, что приводит к нарушению механизмов апоптоза и злокачественной морфологической трансформации — от легкой и умеренной дисплазии до выраженных диспластических изменений и карциномы in situ. Вирусные гены Е5 и Е6 оказывают блокирующий эффект на антионкогены p53 Rb нормальных клеточных элементов шейки матки.
Из-за инактивации опухолевого супрессора запускается бесконтрольная пролиферация опухолевых клеток. Кроме того, под влиянием белка, в синтезе которого участвует ген Е6, активируется теломераза, что способствует возникновению бессмертных клеточных клонов и развитию опухолей. Одновременно за счет блокирования циклинзависимой киназы р21 и р26 белком, производимым геном Е7, начинается активное деление поврежденных клеток. В последующем раковые клетки распространяются со слизистой на другие ткани маточной шейки, опухоль прорастает в смежные органы и метастазирует.
Классификация
Систематизация форм рака шейки матки при беременности основана на тех же критериях, что и у небеременных пациенток. С учетом типа пораженного эпителия опухоли могут быть экзофитными плоскоклеточными, происходящими из экзоцервикса (выявляются у 53,6% беременных), эндофитными аденокарциноматозными, образованными клетками эндоцервикса (диагностируются у 25,7% пациенток). В 20,7% случаев неоплазия шейки при гестации является смешанной. Для разработки оптимальной тактики ведения беременности важно учитывать стадию рака:
- Стадия 0. При прекарциноме (опухоли in situ) процесс локализован в эпителиальном слое, атипия клеток соответствует пограничному состоянию между дисплазией III степени и истинной злокачественной неоплазией. Прогноз для вынашивания беременности наиболее благоприятен, после родов возможны малоинвазивные операции.
- СтадияI. Рак не выходит за пределы шейки. Опухолевый очаг определяется микроскопически (IA, микроинвазивный рак) или макроскопически (IB). Возможно продолжение гестации и естественное родоразрешение по согласию пациентки с выполнением консервативных или радикальных вмешательств в послеродовом периоде.
- СтадияII. Карцинома распространилась на тело матки, верхнюю часть влагалища (IIA) и параметрий (IIB). Стенки таза и нижняя треть вагины в процесс не вовлечены. При гестационном сроке свыше 20 недель беременность можно пролонгировать не более чем на 8 недель до достижения плодом жизнеспособности и завершить кесаревым сечением.
- СтадияIII. Рак распространился на нижнюю треть влагалища (IIIA), доходит до стенок таза, возможно блокирование почки и возникновение гидронефроза (IIIB). Лечение рекомендуется начинать как можно раньше. В 1 триместре беременность прерывают, во 2-3 —выполняют кесарево сечение с расширенной экстирпацией матки.
- СтадияIV. В онкопроцесс вовлечена слизистая прямой кишки и мочевого пузыря либо опухоль вышла за пределы таза (IVA), имеются отдаленные метастазы (IVB). При беременности встречается редко. Обнаружение неоперабельной опухоли является основанием для проведения кесарева сечения при жизнеспособном плоде с последующей лучевой и химиотерапией.
Симптомы РШМ при беременности
Преинвазивные и малоинвазивные формы неоплазии, выявляемые у 70% беременных, протекают бессимптомно. У женщин с начальными стадиями инвазивного рака (IB, IIA) отмечаются контактные кровянистые выделения после вагинального осмотра, полового акта. Кровотечения из поврежденных сосудов неоплазии в I триместре часто ошибочно расцениваются как угрожающий спонтанный выкидыш, во II-III — как преждевременная отслойка или предлежание плаценты. Возможно появление прозрачных белей. При опухолях с распадом выделения становятся зловонными.
Боль в нижней части живота, принимаемая за угрозу прерывания беременности, возникает редко. Появление болезненности в пояснично-крестцовой области, ягодице, задней поверхности бедра обычно свидетельствует об инфильтрации тазовой клетчатки. При сдавливании опухолью мочеточников нарушается отток мочи, при прорастании мочевого пузыря, прямой кишки наблюдаются появление примесей крови в моче и кале, их отхождение через вагину.
Осложнения
При инвазивных видах рака повышается вероятность самопроизвольного прерывания гестации выкидышем или преждевременными родами. Значительная деформация органа опухолью может спровоцировать развитие истмико-цервикальной недостаточности. У пациенток, имеющих кровоточащие неоплазии, сильнее выражена анемия беременных. Уровень перинатальной смертности повышается до 11,5%. Завершение беременности естественными родами при наличии крупного объемного новообразования существенно увеличивает вероятность разрывов маточной шейки, массивных послеродовых кровотечений, гематогенного метастазирования рака. Поэтому в таких случаях рекомендовано кесарево сечение.
Диагностика
Основные задачи диагностического поиска — исключение или подтверждение злокачественности патологического процесса и точное определение стадии рака. В период гестации рекомендуется использовать методы обследования, не представляющие угрозы для плода, что усложняет постановку правильного диагноза. Наиболее информативными являются:
- Осмотр на кресле. Исследование в зеркалах позволяет обнаружить макроскопически видимые изменения экзоцервикса, трансформационной зоны, обнаружить новообразования, выступающие в полость влагалища из цервикального канала. Возможно выявление контактной кровоточивости неоплазии.
- ПЦР скрининг на ВПЧ. Хотя инфицированность вирусом папилломы не свидетельствует об опухоли шейки, получение положительного анализа повышает онконастороженность. ПЦР-диагностика дает возможность определить спектр серотипов возбудителя, провести их типирование.
- Цитология соскоба шейки матки. При беременности забор материала проводится с осторожностью, чтобы предупредить кровотечение, сохранить шеечную пробку, исключить повреждение плодных оболочек. Исследование направлено на определение дисплазии, атипии, малигнизации.
- Кольпоскопия. Дополняет результаты цитологического теста. Расширенная кольпоскопия производится при наличии лабораторных признаков предракового или ракового состояния для обнаружения в слизистой оболочке шейки патологического очага перед выполнением прицельной биопсии и контроля над забором материала.
- Гистологическое исследование биоптата. Применяется для определения вида опухоли и степени ее дифференцировки. Для снижения травматизации маточной шейки и уменьшения вероятности кровотечения беременным обычно проводят клиновидную биопсию. По мнению многих акушеров-гинекологов, забор материала не следует осуществлять ранее 2 триместра.
Для оценки состояния прямой кишки, тазовой клетчатки, мочевого пузыря, регионарных лимфоузлов могут быть рекомендованы УЗИ малого таза, цистоскопия, ректороманоскопия, МРТ отдельных органов, МРТ лимфатических узлов. При подозрении на метастазы предпочтительным методом обследования является МРТ всего тела. Лучевые методы диагностики беременным женщинам с подозрением на рак маточной шейки назначают ограниченно из-за возможного повреждающего воздействия на плод. Заболевание дифференцируют с эрозиями, полипами, кондиломами, кистами, цервицитом, эктопией, эктропионом, дисплазией, опухолями влагалища, спонтанным выкидышем, предлежанием плаценты. Пациентку осматривает онкогинеколог, по показаниям — уролог, проктолог.
Лечение РШМ при беременности
Рак III-IV стадии является показанием для прерывания гестации на любом сроке. До 20-й недели назначается наружная лучевая терапия, провоцирующая спонтанный выкидыш при дозе 4000 сГр. После 20-недельного срока выполняется кесарево сечение и субтотальная резекция матки независимо от жизнеспособности плода. Основные методы лечения при раке маточной шейки у беременных такие же, как и вне гестационного периода:
- Органосохраняющие операции. Показаны молодым пациенткам с карциномой in situ и раком IA стадии (при проникновении в строму не глубже 3 мм), желающим сохранить фертильность. Конизация выполняется спустя 4-8 недель после медицинского аборта или через 7-9 недель после влагалищных или абдоминальных родов.
- Простая гистерэктомия. Удаление матки с сохранением придатков рекомендовано женщинам с преинвазивным и малоинвазивным раком, которые не имеют репродуктивных планов. Операция проводится как самостоятельное вмешательство в I-м триместре и одномоментно с кесаревым сечением при решении выносить беременность.
- Расширенная гистерэктомия. Является операцией выбора при раке IB-II стадий. В 1-м триместре осуществляется, в том числе, для прерывания беременности, во 2 и 3-м производится одновременно с хирургическим родоразрешением. Спустя 2-3 недели женщине рекомендована адъювантная лучевая терапия.
- Сочетанная химиолучевая терапия. Применяется при злокачественном новообразовании шейки матки III-IV стадий. Внешнее облучение позволяет не только воздействовать на опухолевый процесс, но и прервать гестацию до 20 недели. Химиопрепараты и радиометоды не используют при решении женщины сохранить плод.
Прогноз и профилактика
При диагностике у беременной рака шейки матки прогноз всегда серьезный. Наилучших результатов удается достичь при неинвазивных формах неоплазии. Пятилетняя выживаемость пациенток с раком I стадии, выявленным во время беременности, не отличается от аналогичного показателя для небеременных женщин и достигает 88%. При опухоли II стадии на протяжении 5 лет выживает до 54% онкобольных (против 60-75% женщин с диагностированным раком маточной шейки вне беременности), при III стадии — до 30-45%. При инвазивных опухолях отсрочка лечения в связи с желанием сохранить беременность ухудшает прогноз выживаемости на 5% на каждый месяц пролонгированной гестации.
После органосохраняющих операций рак рецидивирует у 3,9% пациенток, а новая беременность наступает у 20,0-48,4%. Отдаленными последствиями конизации являются истмико-цервикальная недостаточность, бесплодие, формирование ректовагинальных, уретро- и пузырно-влагалищных свищей. Профилактика предусматривает соблюдение правил сексуальной гигиены с использованием методов барьерной контрацепции, отказом от беспорядочных половых связей, регулярное диспансерное наблюдение ВПЧ-инфицированных пациенток, своевременное лечение предраковых состояний.
1. Инвазивный рак шейки матки и беременность. Клинические рекомендации ESGO, 2017)/ Жорданиа К.И., Паяниди Ю.Г., Хохлова С.В., Козаченко В.П., Адамян Л.В.// Онкогинекология. - 2018 - №2.
2. Гинекологический рак в сочетании с беременностью/ Урманчеева А.Ф.// Практическая онкология. - 2009 - Т.10, №4.
3. Фоновые заболевания, предрак и рак шейки матки у беременных женщин/ Степанова Р.Н., Коломеец Е.В., Тарасова Л.П.// Ученые записки Орловского государственного университета. - 2011 - №3.
4. Методы диагностики и лечения предрака шейки матки, ассоциированного с беременностью/ Доброхотова Ю.Э. , Венедиктова М.Г. , Боровкова Е.И. , Данелян С.Ж., Саранцев А.Н. , Морозова К.В. , Оруджова К.Ф.// РМЖ.Мать и дитя. - 2017 - №15.
Лечение рака шейки матки у беременных - тактика
Рак шейки матки (РШМ) является одним из наиболее распространенных злокачественных новообразований, диагностируемых во время беременности. Частота его достигает 1,5 случая на 10 000 родов. Во время гестации стадирование и лечение заболевания должны соответствовать современным стандартам и быть идентичными тактике ведения больной вне беременности. Основными методами терапии инвазивного РШМ являются оперативный и медикаментозный (химиотерапия). Выбор лечебной тактики определяется сроком гестации на момент постановки диагноза, стадией заболевания, размером опухоли, а также вовлеченностью в процесс регионарных лимфатических узлов. При постановке диагноза до 20 нед. на выбор метода терапии влияет желание женщины сохранить беременность. При IА2 и IB1 стадиях и опухоли до 2 см проводится атипичная конизация шейки матки с лимфаденэктомией. В случае поражения лимфатических узлов в сроке до 22 нед. рекомендовано прерывание беременности. При желании пациентки сохранить беременность проводится неоадъювантная химиотерапия. После 22 нед. выполнение лимфаденэктомии технически сложно, стадирование проводится по результатам гистологического исследования. Химиотерапия проводится по стандартной методике с применением цисплатина в монорежиме или в комбинации с паклитакселом.
Ключевые слова: беременность, рак шейки матки, клинические рекомендации, конизация, неоадъювантная химиотерапия.
Managing invasive cervical cancer in pregnancy
Yu.G.Payanidi 1 , E.I. Borovkova 2 , Yu.E. Dobrohotova 2 , A.M. Arutunyan 2
1 Blokhin Cancer Research Center, Moscow, Russian Federation
2 Pirogov Russian National Research Medical University, Moscow, Russian Federation
Cervical cancer is one of the most common cancers diagnosed during the pregnancy. Its incidence is 1.5 cases per 10 000 births. During gestation, cancer staging and treatment should meet current standards and be similar to the treatment strategy in non-pregnant women. Key treatment approaches to the invasive cervical cancer are surgery and pharmacotherapy (chemotherapy). Treatment strategy is determined by the gestational period when the condition was diagnosed, cancer stage, tumor size, and regional lymph nodes involvement. When diagnosed up to 20 weeks, treatment approach choice depends on the decision of whether to proceed a pregnancy or not. In cervix cancer stage ІА2 and stage IB1 and in tumor size less than 2 cm, conization and lymph node dissection are recommended. In case of lymph node involvement in a women who is pregnant less than 22 weeks, abortion is recommended. If a woman decides to proceed her pregnancy, neoadjuvant chemotherapy is recommended. At 22 weeks pregnancy, lymphadenectomy is challenging; cancer staging is performed by histological examination. Standard chemotherapeutic strategy involves cisplatin monotherapy or cisplatin plus paclitaxel.
Keywords: pregnancy, cervical cancer, clinical guidelines, conization, neoadjuvant chemotherapy.
For citation: Payanidi Yu.G., Borovkova E.I., Dobrohotova Yu.E., Arutunyan A.M. Managing invasive cervical cancer in pregnancy. Russian Journal of Woman and Child Health. 2019;2(2):135-138.
В статье представлена тактика ведения беременных с инвазивным раком шейки матки.
Введение
Рак шейки матки (РШМ) является одним из наиболее распространенных злокачественных новообразований у беременных и встречается с частотой от 0,8 до 1,5 случая на 10 000 родов. Во время беременности и в течение первого года после родов верифицируется до 3% случаев болезни [1, 2].
Крупных рандомизированных исследований, на материалах которых можно основывать рекомендации по ведению беременных с РШМ, не проводилось. И при лечении этой категории больных применяются рекомендации, основанные на материалах исследований с участием небеременных пациенток. При этом дополнительно тактика ведения беременных с РШМ определяется сроком гестации, стадией опухолевого процесса и желанием пациентки сохранить беременность. Лечение должно быть индивидуальным, своевременным, с минимальным риском для женщины и плода [2].
Во время беременности РШМ в большинстве случаев диагностируется на ранних стадиях, а средний гестационный срок составляет 19,5 нед. [3, 4]. Клинические проявления РШМ во время беременности зачастую отсутствуют или могут быть приняты за акушерские осложнения (влагалищное кровотечение, тазовые боли, боли по ходу седалищного нерва, анемия).
Тактика лечения пациенток с РШМ
Тактика лечения пациенток с РШМ определяется стадией заболевания, сроком гестации, а также вовлеченностью в процесс регионарных лимфатических узлов. Основными методами лечения являются хирургический и медикаментозный (химиотерапия) 5 (табл. 1).
Согласно приказу Минздрава России № 572н от 1 ноября 2012 г. все беременные подлежат обязательному цитологическому скринингу, что позволяет своевременно поставить диагноз. При выявлении признаков, подозрительных в отношении микроинвазивного процесса, проводится атипичная конизация шейки матки с высотой конуса не более 1,5 см. Во время беременности не производится выскабливание цервикального канала в связи с высоким риском прерывания беременности после данной манипуляции. Конизация шейки матки может быть выполнена в любом сроке гестации, но не менее, чем за 4 нед. до предполагаемых родов. При IA1 стадии (инвазия до 3 мм и протяженность по горизонтали до 7 мм без сосудистой инвазии) конизация является оптимальным и безопасным методом лечения. Риск метастазирования составляет 0,8% при плоскоклеточном раке и 1,5% при аденокарциноме. При подозрении на поражение тазовых лимфатических узлов показано проведение тазовой лимфаденэктомии (ТЛАЭ) или биопсии сторожевого лимфатического узла [8].
Ведение пациенток до 22 нед. гестации с IА2 и IB1 стадией и опухолью до 2 см.
На первом этапе проводится атипичная конизация шейки матки с лимфаденэктомией. Если подтверждается метастатическое поражение лимфатических узлов, должен быть рассмотрен вопрос прерывания беременности. При отсутствии поражения лимфатических узлов возможно пролонгирование беременности с проведением стандартной терапии после родов (при IА2 стадии) или неоадъювантной химиотерапии (НАХТ) (при IB1 стадии) с отсроченным стандартным лечением после родов [9] (рис. 1).
Ведение пациенток в сроке более 22 нед. с IА2 и IB1 стадией при опухоли до 2 см. В данном сроке гестации для стадирования процесса проводится атипичная конизация шейки матки. Тазовая лимфаденэктомия не выполняется в связи с техническими ограничениями, связанными с размером матки. При подтверждении IА2 стадии после родов проводится стандартное лечение, при IB1 стадии начинают неоадъювантную полихимиотерапию [9].
Ведение беременных до 22 нед. с IB1 стадией и опухолью до 2-4 см. Для уточнения распространенности процесса проводится ТЛАЭ. При подтверждении вовлечения лимфатических узлов рекомендовано прерывание беременности с последующим стандартным лечением. В случае интактности лимфатических узлов после 12 нед. начинают НАХТ [9].
Беременным в сроке гестации до 22 нед. с подтвержденным РШМ IB2 и IIA стадии рекомендовано прерывание беременности вне зависимости от вовлеченности лимфатических узлов [9]. После 22 нед. проводят несколько курсов НАХТ. Последний курс должен быть завершен не позднее 3 нед. до родов [9].
Хирургическое лечение
Диагностика РШМ основывается на гистологическом исследовании, однако прогноз заболевания определяется размером опухоли и вовлеченностью в патологический процесс лимфатических узлов. В первой половине беременности (до 22 нед.) проведение лапароскопической ТЛАЭ является безопасной и весьма информативной операцией [10]. При выявлении метастазов показано прерывание беременности и проведение химиолучевой терапии [11]. Пролонгирование беременности допустимо при интактности лимфатических узлов и начале НАХТ [11]. Проведение трахелэктомии во время беременности не рекомендовано в связи с малой эффективностью и высоким риском прерывания беременности (до 34%) [12].
Неоадъювантная химиотерапия
В случае пролонгирования беременности у пациенток с местнораспространенным РШМ проведение НАХТ позволяет стабилизировать опухолевый процесс [6]. Расчет лечебной дозы и выбор препарата идентичен таковым вне беременности. Однако необходимо учитывать, что физиологические изменения, связанные с беременностью (гемодилюция, гипопротеинемия, ускорение скорости клубочковой фильтрации, появление третьего пространства — амниотической полости), оказывают влияние на фармакокинетические свойства химиопрепаратов.
Согласно международным протоколам химиотерапия не проводится в I триместре беременности в связи с высоким риском эмбриотоксического и тератогенного действия. Во время беременности у пациенток с РШМ химиотерапию можно проводить начиная со II триместра: при IB1 стадии, отсутствии метастазов в лимфатических узлах и размерах опухоли В подавляющем большинстве случаев проведение НАХТ позволяет стабилизировать опухолевый процесс и пролонгировать беременность до периода достижения плодом жизнеспособности и зрелости. Наиболее часто схема терапии включает цисплатин (50-100 мг/м 2 ) в монорежиме или в комбинации с паклитакселом (175 мг/м 2 ). Курсы проводятся с интервалом каждые 3 нед. [13]. Реже применяется комбинация цисплатина (75 мг/м 2 ) с ифосфамидом 2 г/м 2 циклами каждые 2 нед. [12, 14].
Тактика родоразрешения беременных с РШМ
Последний курс полихимиотерапии должен быть завершен за 3 нед. до предполагаемой даты родов. Это связано с риском рождения ребенка с подавленным костным мозгом и высокой вероятностью развития у него инфекционных осложнений [14, 15]. В настоящее время рекомендовано пролонгировать беременность как минимум до доношенного срока (37 нед.), при отсутствии такой возможности — хотя бы до 34 нед. 15.
После конизации шейки матки, выполненной при IA1-IA2 стадиях, теоретически возможны влагалищные роды [9]. В случае распространенного РШМ методом родоразрешения является операция корпорального кесарева сечения с последующей операцией Вертгейма. Выбор метода родоразрешения зависит от стадии заболевания с учетом желания пациентки сохранить фертильность [1, 2, 12, 18-20].
Заключение
«Золотой стандарт» лечения РШМ у беременных еще не разработан. Следует признать, что приведенные выше клинические рекомендации ESGO, к сожалению, не могут ответить на все вопросы. Так, например, с нашей точки зрения, важным прогностическим фактором являются биологические особенности новообразования, которые в рекомендациях не учитываются. Также не ясно, какова тактика лечения при запущенных стадиях процесса и не являются ли рискованными рекомендуемые роды через естественные родовые пути при IA2 стадии заболевания и т. д. Тем не менее целесообразно следовать предложенному варианту тактических подходов, учитывая рекомендации Международного консенсусного совещания по «гинекологическим ракам», основанные на базе мирового опыта. Необходимо подчеркнуть особую роль мультидисциплинарного подхода с участием онкогинеколога, акушера-гинеколога, неонатолога, химио- и лучевого терапевтов, психолога, юриста в решении ряда важных вопросов.
Беременность и злокачественные заболевания представляют собой нестандартную и сложную клиническую ситуацию, в последние годы наблюдается тенденция к росту числа таких случаев. Это связано и с увеличением среднего возраста беременных женщин, и с большой распространенностью HPV-инфекции. В структуре гинекологических опухолей, ассоциированных с беременностью, рак шейки матки (РШМ) занимает 1-е место. Сочетание РШМ и беременности осложняется невозможностью проведения полного комплекса диагностических и лечебных мероприятий, т. к. необходимо думать о рисках со стороны матери и со стороны плода. В настоящей статье рассматриваются точки зрения отечественных и мировых экспертов, занимающихся данной проблемой, которая находится на стыке специальностей. Также в данной статье рассмотрены методы диагностики и ведения беременных пациенток с предраковыми процессами шейки матки. В последние годы наблюдается тенденция к динамическому наблюдению, если речь идет о предраковых состояниях. Также стали рассматриваться варианты органосохраняющих операций в случае микроинвазивного РШМ.
В связи с актуальностью этой проблемы целесообразно изучить оптимальные методы диагностики, ведения и лечения пациенток с предраком шейки матки, ассоциированным с беременностью.
Ключевые слова: CIN, рак шейки матки и беременность, методы ведения, диагностика.
Methods of diagnosis and treatment of cervical precancer associated with pregnancy
Dobrokhotova Yu.E. 1 , Venediktova M.G. 1 , Borovkova E.I. 1 , Danelyan S.Zh. 2 , Sarantsev A.N. 2 , Morozova K.V. 1 , Orudjova K.F. 1
1 Russian National Research Medical University named after N.I. Pirogov, Moscow
2 City Clinical Hospital № 40, Moscow
Pregnancy and malignant diseases represent a non-standard and complex clinical situation, the trend towards which has increased in recent years. This is related to the increase in the average age of pregnant women and the high prevalence of HPV infection. In the structure of gynecological tumors associated with pregnancy, cervical cancer ranks first. The combination of cervical cancer and pregnancy is complicated not by the possibility of carrying out a full range of diagnostic and therapeutic measures, as it is necessary to think about the risks on the part of both the mother and the fetus. This article examines the points of view of domestic and international experts dealing with this problem, which is at the intersection of specialties. Also this article considers the methods of diagnosis and management of pregnant women with the cervical precancer. In recent years, there has been a trend towards dynamic observation, when it comes to precancerous conditions. Also, variants of organ-preserving surgeries in the case of microinvasive cervical cancer are considered.
In connection with the urgency of this problem, it is advisable to study the optimal methods of diagnosis, management and treatment of patients with the cervical precancer associated with pregnancy.
Key words: CIN, cervical cancer and pregnancy, methods of management, diagnostics.
For citation: Dobrokhotova Yu.E., Venediktova M.G., Borovkova E.I. et al. Methods of diagnosis and treatment of cervical precancer associated with pregnancy // RMJ. 2017. № 15. P. 1084-1086.
Для цитирования: Методы диагностики и лечения предрака шейки матки, ассоциированного с беременностью. РМЖ. Мать и дитя. 2017;25(15):1084-1086.
Статья посвящена диагностике и лечению предрака шейки матки, ассоциированного с беременностью
Введение
Рак шейки матки (РШМ) занимает 1-е место среди гинекологических опухолей, ассоциированных с беременностью: от 1 до 13 случаев на 10 000 беременностей, включая послеродовой период, и 1 случай на 1000-2500 родов [1].
РШМ, обнаруженный в течение 6 мес. после прерывания беременности и 12-18 мес. после родов, относится к опухолям, ассоциированным с беременностью, т. к. клинико-морфологические проявления злокачественного процесса присутствуют уже во время беременности [1]. Так, средний возраст больных РШМ в сочетании с беременностью - 30 лет [2].
Также ряд авторов отмечают тенденцию к увеличению числа беременных, у которых были выявлены предрак шейки матки и РШМ, т. к. все чаще женщины откладывают решение о материнстве. Возраст первородящих в Европе увеличился за последнее десятилетие в среднем на два года [3].
Если речь идет о дисплазии шейки матки и РШМ, то стоит отметить, что факторы риска у беременных такие же, как и у небеременных пациенток. К таким факторам относятся раннее начало половой жизни, частая смена половых партнеров, отсутствие барьерной контрацепции, что нередко приводит к инфицированию HPV [2].
Стоит отметить, что частота хронической HPV-инфекции, которая связана с развитием цервикальной интраэпителиальной неоплазии, самая высокая среди женщин детородного возраста (20-25 лет). Но несмотря на это, современная тактика лечения за эти годы сменилась - от агрессивного хирургического воздействия до консервативного подхода [4].
Выявление патологии шейки матки на уровне цервикальной интраэпителиальной неоплазии (cervical intraepithelial neoplasia (CIN)) стало возможно благодаря профилактическим осмотрам с использованием цитологического исследования мазков с шейки матки и цервикального канала на атипические клетки. Эффективность цитологического скрининга была доказана, данный метод является «золотым стандартом» профилактики и диагностики дисплазии и РШМ. С учетом факторов риска, а также среднего возраста пациенток с данными патологическими состояниями целесообразность цитологического скрининга при постановке на учет по беременности не вызывает сомнения.
Методы диагностики дисплазии во время беременности
Преобладание цервикальной интраэпителиальной неоплазии (CIN) в популяции беременных женщин составляет примерно 1% [5]. По данным литературы, в последние годы рекомендуется цитологическое исследование в качестве рутинного метода обследования во время беременности, т. к. большинство поражений шейки матки встречается у молодых женщин в детородном возрасте [4].
В I триместре при кольпоскопии будет отмечаться наличие белесоватых точечных возвышений, связанных с физиологической гипертрофией, обширной сети сосудов. Во II и III триместрах визуально может определяться физиологическая эктопия призматического эпителия, а кольпоскопически - белые пятна метаплазированного эпителия на фоне сосудистого рисунка. Данные изменения подвергаются обратному регрессу в послеродовом периоде в течение 2-4 нед. и могут привести к гипердиагностике во время беременности [2].
Ряд авторов отмечают, что интерпретация данных РАР-теста во время беременности может быть затруднена из-за таких факторов, как эрозия, воспаление, а также наличие децидуальных клеток, которые принимаются за атипию (так называемая реакция Ариас - Стелла) [3].
Но не менее опасной в вопросах диагностики может быть гиподиагностика в связи с неоднозначным отношением клиницистов и морфологов к возможным малигнизирующим процессам в тканях шейки матки у беременных. В настоящее время доказано, что малигнизированные внутриэпителиальные процессы не имеют связи с пролиферативными процессами во время беременности. В дополнение к этому, как показали исследования F.G. Jones, частота выявления рака in situ во время беременности равна соотношению 3:10 000. Такое же соотношение было отмечено и у небеременных [2] .
После того как при цитологическом скрининге была обнаружена аномальная цитологическая картина, следует рекомендовать беременным пациенткам ряд обследований, таких как визуальный осмотр шейки матки при помощи зеркал, цитологическое исследование, кольпоскопия. Ряд авторов считают, что диагностические процедуры не должны отличаться от таковых у небеременных женщин [3].
Наблюдение в течение беременности за группой пациенток с CIN (верифицированной цитологически) необходимо проводить с помощью регулярных гинекологических осмотров, включая PAP-мазок, кольпоскопию и прицельную биопсию (по показаниям). Была доказана безопасность данных обследований, и они рекомендуются группами экспертов [4].
Американское общество кольпоскопии и патологии шейки матки (The American Society for Colposcopy and Cervical Pathology, ASCCP) рекомендует при обнаружении атипичных клеток плоского эпителия неопределенного значения (ASC-US) или клеток со слабой степенью плоскоклеточных интраэпителиальных поражений (L-SIL/CIN 1) у беременных отложить кольпоскопию на период до 6 нед. после родов, поскольку вероятность обнаружить CIN 2-3 в этих случаях после родов составляет только 3,7% [6]. Если нет никаких доказательств, подтверждающих наличие РШМ, никакое лечение не должно осуществляться во время беременности, вся терапия может быть отложена до послеродового периода. У пациенток с cаncer in situ и с микроинвазивным процессом без каких-либо изменений рекомендуется мониторинг: кольпоскопия в любом триместре, в случае подозрения в отношении прогрессии следует выполнять модифицированную конизацию шейки матки [3].
Для уточнения предполагаемого диагноза при выявлении дисплазии эпителия шейки матки умеренной или тяжелой степени без признаков воспаления, а также при подозрении на злокачественную опухоль шейки матки по данным цитологического исследования как этап углубленной диагностики целесообразно выполнение морфологического исследования ткани шейки матки. Вопрос о методе забора материала для гистологического исследования во время беременности остается дискутабельным. На данный момент рассматриваются несколько методов забора материала для гистологического исследования, такие как прицельная биопсия под контролем кольпоскопии, множественная квадрантная биопсия и модифицированная конизация шейки матки [7].
Часть авторов предлагают использовать множественную пункционную биопсию, учитывая то, что данный метод - наиболее щадящий и практически не вызывает осложнений. Но, по данным литературы, при таком способе забора материала была отмечена значительная частота ошибочных заключений - от 6 до 25% [7].
Ряд авторов придерживаются мнения о необходимости выполнения модифицированной конизации шейки матки, т. к. значительное число отклонений в репаративных процессах шейки матки возникает на стыке двух видов эпителия: плоского и цилиндрического, считают достаточной глубину конуса от 1,5 до 2,0 см вместо 3-3,5 см [7]. Используя метод модифицированной конизации, врач получает более точную информацию о патологическом процессе за счет большего числа срезов, выполненных гистологом, что дает преимущество в диагностике по сравнению с прицельной биопсией, даже выполненной из нескольких участков.
При подозрении на РШМ прицельная биопсия или модифицированная конизация может быть выполнена на любом сроке беременности, но следует помнить, что выполнение конусовидной биопсии на раннем сроке беременности и после 34 нед. может сопровождаться тяжелыми осложнениями: обильными кровотечениями, выкидышами, преждевременными родами [7].
При обследовании беременных сохраняется принцип двухэтапности диагностики ранних форм РШМ. Основным методом первичного выявления преклинического РШМ является цитологическое исследование (I этап). При сомнительных и позитивных цитологических данных применяется комплекс диагностических методов: кольпоскопия, повторное цитологическое исследование и прицельная биопсия как во время беременности, так и после (II этап). Как исключение - при подозрении на инвазивный рост опухоли и при нежелании женщины прервать беременность возможно выполнение атипичной конизации (меньшего объема по сравнению с общепринятым) или клиновидной биопсии во время беременности [2].
Лечение предрака шейки матки, ассоциированного с беременностью
Тактика ведения беременных с CIN в настоящее время выжидательная, поскольку риск прогрессирования в инвазивный рак за столь короткий промежуток времени крайне низкий - 0,0-0,4% [2]. Конизация шейки матки может быть выполнена через 6-8 нед. после завершения беременности, а именно после срочных влагалищных родов [2]. На способ родоразрешения при наличии дисплазии шейки матки разной степени тяжести могут влиять только акушерские показания.
Изменения, характерные для CIN 1, подвергаются регрессу после родов примерно в 60% случаев и остаются неизменными примерно в 30%. Прогрессирование к более сложным изменениям (CIN 3) отмечается редко - максимум у 6% пациенток. При CIN 3 процент регрессии после родов низок - около 30%, и прогрессирование наблюдается приблизительно у 10% пациенток.
Из-за низких темпов прогрессирования во время беременности в настоящее время принято считать, что для большинства пациенток будет безопасна выжидательная тактика в течение всего срока гестации, если инвазивный процесс был исключен [4].
Ряд иностранных исследователей в своих работах сообщают о значительно более высокой скорости послеродовой регрессии CIN в группе беременных, чем в группах небеременных пациенток. Некоторые авторы предположили, что у женщин с ВПЧ-инфекцией типичный гормональный фон во время беременности индуцирует активацию вируса, что впоследствии приводит к увеличению скорости спонтанной регрессии после родов [8]. В исследовании Ahdoot et al. показано, что скорость регрессии была выше у женщин, которые не подвергались биопсии шейки матки как части дородовой оценки, по сравнению с женщинами, которые подверглись биопсии (70% по сравнению с 52%) [9]. Другие исследования свидетельствуют о корреляции между CIN и способом родоразрешения, обнаружив более высокую скорость регрессии дисплазии шейки матки после влагалищных родов по сравнению с кесаревым сечением (67% по сравнению с 13%) [4]. Возможный механизм этого может быть связан с потерей диспластического эпителия шейки матки во время созревания, открытия шейки матки и прохождения плода через родовые пути [4]. Другие исследования не сообщали о каких-либо различиях в частоте регрессии среди пациенток с влагалищными родами и кесаревым сечением [4]. У беременных пациенток с диагнозом CIN 2 - CIN 3 скорость прогрессирования в инвазивный РШМ, по данным различных авторов, разная. В своих работах Ackermann et al. и Everson et al. сообщили о скорости прогрессирования 2,4% [10] и 3% [11], в то время как Coppola et al. - о более высоком уровне в 8% [4].
Выводы
Проанализировав данные исследований иностранных и российских ученых, стоит отметить, что при выполнении цитологического скрининга у беременных и в случае выявления в мазках картины, соответствующей дисплазии шейки матки умеренной и тяжелой степени и даже cancer in situ, возможно избежать конизации шейки матки, которая может привести к самопроизвольному аборту, преждевременным родам, кровотечению и другим осложнениям. Сегодня тактика ведения беременных с дисплазией шейки матки заключается в динамическом наблюдении, включающем в себя цитологическое исследование, кольпоскопическую оценку состояния покровного эпителия шейки матки с учетом физиологических особенностей, характерных для беременности. При подозрении на инвазивный процесс возможно использование более щадящих способов забора гистологического материала, таких как прицельная биопсия. Все дополнительные диагностические мероприятия целесообразно отложить на послеродовый период - проводить их не ранее, чем через 6-8 нед. после родоразрешения. Несмотря на приведенные выше данные о частоте регресса дисплазии шейки матки, данная группа пациенток требует тщательного наблюдения, поскольку в течение 2-5 лет сохраняется высокий риск рецидива дисплазии.
Рак шейки матки
Рак шейки матки - опухолевое поражение нижнего отдела матки, характеризующееся злокачественной трансформацией покровного эпителия (экто- или эндоцервикса). Специфическим проявлениям рака шейки матки предшествует бессимптомное течение; в дальнейшем появляются контактные и межменструальные кровянистые выделения, боли в животе и крестце, отеки нижних конечностей, нарушения мочеиспускания и дефекации. Диагностика при раке шейки матки включает проведение осмотра в зеркалах, расширенной кольпоскопии, исследования цитологического соскоба, биопсии с гистологическим заключением, эндоцервикального кюретажа. Лечение рака шейки матки проводят с учетом гистологической формы и распространенности с помощью хирургического вмешательства, лучевой терапии, химиотерапии или их комбинации.
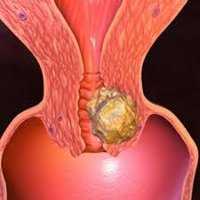

Рак шейки матки (цервикальный рак) составляет около 15% среди всех злокачественных поражений женской репродуктивной системы, занимая третье место вслед за раком молочной железы и раком эндометрия. Несмотря на то, что рак шейки матки относится к заболеваниям «визуальной локализации», у 40% женщин эта патология диагностируется на поздней (III - IV) стадии. В России ежегодно выявляется около 12000 случаев цервикального рака. Основной категорией служат пациентки в возрасте 40-50 лет, хотя в последние годы отмечается рост заболеваемости раком шейки матки среди женщин младше 40 лет.

Причины РШМ
Ключевая роль в канцерогенезе отводится папилломавирусной инфекции, обладающей тропностью к эпителию шейки матки. Серотипы ВПЧ высокого онкогенного риска (16, 18) обнаруживаются в 95% случаев рака шейки матки: при плоскоклеточном цервикальном раке чаще выявляется ВПЧ 16 типа; при аденокарциноме и низкодифференцированной форме - ВПЧ 18 типа. Серотипы ВПЧ «низкого» онкогенного риска (6, 11, 44) и среднего риска (31, 33, 35) преимущественно вызывают образование плоских и остроконечных кондилом, дисплазию и редко - рак шейки матки.
Среди других ИППП, повышающих риски развития рака шейки матки, выделяют генитальный герпес, цитомегаловирусную инфекцию, хламидиоз, ВИЧ. Из всего вышесказанного следует, что вероятность развития рака шейки матки больше у женщин, часто меняющих половых партнеров и пренебрегающих барьерными методами контрацепции. Кроме того, при раннем начале сексуальной жизни (в возрасте 14-18 лет) незрелый эпителий шейки матки обладает особой восприимчивостью к воздействию повреждающих агентов.
Факторы риска
К факторам риска по развитию рака шейки матки относят ослабление функции иммунной системы, курение, возраст старше 40 лет, диеты с малым содержанием фруктов и овощей, ожирение, недостаток витаминов А и С. Также доказано, что вероятность развития рака шейки матки увеличивается при длительном (свыше 5 лет) приеме оральных контрацептивов, многочисленных родах, частых абортах. Одним из факторов позднего обнаружения рака шейки матки является низкая медицинская культура, нерегулярное прохождение женщинами профилактических осмотров с исследованием мазка из цервикального канала на онкоцитологию.
К фоновым заболеваниям, предрасполагающим к развитию рака шейки матки, в гинекологии относят лейкоплакию (интраэпителиальную неоплазию, CIN), эритроплакию, кондиломы, полипы, истинную эрозию и псевдоэрозию шейки матки, цервициты.
По гистологическому типу, в соответствии с двумя видами эпителия, выстилающего шейку матки, различают плоскоклеточный цервикальный рак с локализацией в эктоцервиксе (85-95%) и аденокарциному, развивающуюся из эндоцервикса (5-15%). Плоскоклеточный рак шейки матки, в зависимости от степени дифференцировки, может быть ороговевающим, неороговевающим и низкодифференцированным. К редким гистотипам рака шейки матки относятся светлоклеточная, мелкоклеточная, мукоэпидермоидная и др. формы. С учетом типа роста различают экзофитные формы рака шейки матки и эндофитные, встречающиеся реже и имеющие худший прогноз.
Для оценки распространенности в клинической гинекологии используются классификации рака шейки матки по двум системам: FIGO, принятой Международной федерацией акушеров и гинекологов, и ТNМ (где T - распространенность опухоли; N - вовлеченность регионарных лимфоузлов; M - наличие отдаленных метастазов).
Стадия 0 (FIGO) или Тis (ТNМ) расценивается как преинвазивный или внутриэпителиальный рак шейки матки (in situ).
Стадия I (FIGO) или T1 (ТNМ) - опухолевая инвазия ограничивается шейкой матки, без перехода на ее тело.
- I A1 (T1 А1) - микроскопически определяемый рак шейки матки с глубиной инвазии до 3 мм с горизонтальным распространением до 7 мм;
- I A2 (T1 А2) - прорастание опухоли в шейку матки на глубину от 3 до 5 мм с горизонтальным распространением до 7 мм.
- I B1 (T1 В1) - макроскопически определяемый цервикальный рак, ограниченный шейкой матки, либо микроскопически выявляемые поражения, превышающие IA2 (T1А), не превышающее в максимальном измерении 4 см;
- I B2 (T1 В2) - макроскопически определяемое поражение, превышающее в максимальном измерении 4 см.
Стадия II (FIGO) или T2 (ТNМ) характеризуется распространением рака за пределы шейки матки; нижняя треть влагалища и стенки таза интактны.
- II A (T2 А) - опухоль инфильтрирует верхнюю и среднюю треть влагалища или тело матки без прорастания параметрия;
- II B (T2 В) - опухоль инфильтрирует параметрий, но не доходит до стенок таза.
Стадия III (FIGO) или T3 (ТNМ) характеризуется распространением рака за пределы шейки матки с прорастанием параметрия до стенок таза либо вовлечением нижней трети влагалища, либо развитием гидронефроза.
- III A (T3 А) - опухоль захватывает нижнюю треть влагалища, но не прорастает в стенки таза;
- III B (T3 В) - опухоль переходит на стенки таза либо вызывает гидронефроз, или вторичное поражение почки.
Стадия IV А (FIGO) или T4 (ТNМ) характеризуется распространением рака шейки матки в смежные органы либо распространением за пределы таза. Стадия IV B (T4 M1) свидетельствует о наличии отдаленных метастазов.
Симптомы рака шейки матки
Клинические проявления при карциноме in situ и микроинвазивном раке шейки матки отсутствуют. Появление жалоб и симптоматики свидетельствует о прогрессировании опухолевой инвазии. Наиболее характерным проявлением рака шейки матки служат кровянистые выделения и кровотечения: межменструальные, постменопаузальные, контактные (после полового акта, осмотра гинекологом, спринцевания и т. д.), меноррагии. Больные отмечают появление белей - жидких, водянистых, желтоватого или прозрачного цвета влагалищных выделений, обусловленных лимфореей. При распаде раковой опухоли выделения принимают гноевидных характер, иногда имеют цвет «мясных помоев» и зловонный запах.
При прорастании опухоли в стенки таза или нервные сплетения появляются боли в животе, под лоном, в крестце в покое или во время полового акта. В случае метастазирования рака шейки матки в тазовые лимфоузлы и сдавливания венозных сосудов могут наблюдаться отеки ног и наружных гениталий.
Если опухолевая инфильтрация затрагивает кишечник или мочевой пузырь, развиваются нарушения дефекации и мочеиспускания; появляется гематурия или примесь крови в кале; иногда возникают влагалищно-кишечные и влагалищно-пузырные свищи. Механическая компрессия метастатическими лимфоузлами мочеточников приводит к задержке мочи, формированию гидронефроза с последующим развитием анурии и уремии. К общим симптомам рака шейки матки относятся общая слабость, повышенная утомляемость, лихорадка, похудание.
Основу раннего выявления микроинвазивного цервикального рака составляют регулярные онкопрофилактические осмотры с цитологическим исследование соскоба шейки матки. Пап-тест (мазок по Папаниколау) позволяет выявлять предраковые процессы, раковые клетки при преинвазивном росте опухоли. Схема обследования включает:
- Осмотр шейки матки в зеркалах. Визуальный гинекологический осмотр в ранней стадии позволяет обнаружить или заподозрить РШМ по внешнем признакам: изъязвлениям, изменению окраски шейки матки. В инвазивной стадии при экзофитном типе роста рака на поверхности шейки матки определяются фибринозные наложения, опухолевидные разрастания красноватого, белесоватого, розовато-серого цвета, которые легко кровоточат при прикосновении. В случае эндофитного роста цервикального рака шейка становится увеличенной, приобретает бочковидную форму, неровную бугристую поверхность, неравномерную розово-мраморную окраску. При ректо-вагинальном исследовании в параметрии и малом тазу могут определяться инфильтраты.
- Кольпоскопия. С помощью кольпоскопии при увеличении изображения в 7,5- 40 раз возможно более детально изучить шейку матки, обнаружить фоновые процессы (дисплазию, лейкоплакию) и начальные проявления рака шейки матки. Для исследования зоны трансформации эпителия используют проведение пробы с уксусной кислотой и Шиллер-теста (йодной пробы). Атипия при раке шейки матки выявляется по характерной извитости сосудов, менее интенсивному окрашиванию патологических йоднегативных очагов. При подозрении на рак шейки матки показано исследование опухолеассоциированного антигена плоскоклеточных карцином - онкомаркера SCC (в норме не превышает 1,5 нг/мл).
- Биопсия шейки матки. Кольпоскопия дает возможность выявить участок трансформации и произвести прицельную биопсию шейки матки для гистологического исследования забранных тканей. Ножевая биопсия шейки матки с выскабливанием цервикального канала обязательна при подозрении на цервикальный рак. Для определения степени инвазии рака производится конизация шейки матки - конусовидное иссечение кусочка тканей. Решающим и окончательным методом в диагностике рака шейки матки является морфологическая интерпретация результатов биопсии.
Дополнительно при раке шейки матки проводится УЗИ малого таза, позволяющее стадировать опухолевый процесс и планировать объем вмешательства. Для исключения прорастания опухоли в смежные органы и отдаленного метастазирования прибегают к выполнению УЗИ мочевого пузыря и почек, цистоскопии, внутривенной урографии, УЗИ брюшной полости, рентгенографии легких, ирригоскопии, ректоскопии. При необходимости пациентки с выявленным раком шейки матки должны быть проконсультированы урологом, пульмонологом, проктологом.

Лечение рака шейки матки
Хирургическое лечение
Все операции при раке шейки матки делятся на органосохраняющие и радикальные. Выбор тактики зависит от возраста женщины, репродуктивных планов, распространенности онкопроцесса. В онкогинекологии применяется:
- Органосохраняющая тактика. При преинвазивном раке у молодых женщин, планирующих деторождение, выполняются щадящие вмешательства с удалением начально измененных участков шейки матки в пределах здоровых тканей. К таким операциям относят конусовидную ампутацию (конизацию) шейки матки, электрохирургическую петлевую эксцизию, высокую ампутацию шейки матки. Экономные резекции при раке шейки матки позволяют соблюсти онкологическую радикальность и сохранить репродуктивную функцию.
- Радикальная тактика. При более выраженных изменениях и распространенности опухолевого процесса показано удаление матки с транспозицией яичников (выведением их за пределы таза) или с овариэктомией. При раке шейки матки в стадии I B1 стандартным хирургическим объемом является пангистерэктомия - экстирпация матки с аднексэктомией и тазовой лимфодиссекцией. При переходе опухоли на влагалище показано проведение радикальной гистерэктомии с удалением части влагалища, яичников, маточных труб, измененных лимфоузлов, парацервикальной клетчатки.
Противоопухолевое лечение
Хирургический этап лечения рака шейки матки может сочетаться с лучевой или химиотерапией, либо с их комбинацией. Химио- и радиотерапия могут проводиться на дооперационном этапе для уменьшения размеров опухоли (неоадъювантная терапия) или после операции для уничтожения возможно оставшихся опухолевых тканей (адъювантная терапия). При запущенных формах рака шейки матки выполняются паллиативные операции - выведение цистостомы, колостомы, формирование обходных кишечных анастомозов.
Прогноз
Лечение рака шейки матки, начатое на I стадии, обеспечивает 5-летнюю выживаемость у 80-90% пациенток; при II ст. выживаемость через пять лет составляет 60-75%; при III ст. - 30-40%; при IV ст. - менее 10%. При осуществлении органосберегающих операций по поводу рака шейки матки шансы на деторождение сохраняются. В случае проведения радикальных вмешательств, неоадъювантной или адъювантной терапии фертильность полностью утрачивается.
При выявлении рака шейки матки при беременности, тактика зависит от сроков гестации и распространенности опухолевого процесса. Если срок гестации соответствует II-III триместру, беременность возможно сохранить. Ведение беременности при раке шейки матки осуществляется под повышенным медицинским наблюдением. Методом родоразрешения в этом случае обычно служит кесарево сечение с одновременным удалением матки. При сроке гестации менее 3-х месяцев производится искусственное прерывание беременности с немедленным началом лечения рака шейки матки.
Профилактика
Основной профилактической мерой рака является массовый онкологический скрининг с помощью цитологического исследования соскобов с шейки матки и из цервикального канала. Обследование рекомендуется начинать после начала половой жизни, но не позднее возраста 21 года. В течение первых двух лет мазок сдается ежегодно; затем, при отрицательных результатах - 1 раз в 2-3 года.
Профилактика рака шейки матки требует раннего выявления и лечения фоновых заболеваний и половых инфекций, ограничения числа сексуальных партнеров, использования барьерной контрацепции при случайных половых связях. Пациенткам групп риска необходимо прохождения осмотра гинеколога не реже 1 раза в полгода с проведением расширенной кольпоскопии и цитологического мазка. Девочкам и молодым женщинам в возрасте от 9 до 26 лет показано проведение профилактической вакцинации против ВПЧ и рака шейки матки препаратами Церварикс или Гардасил.
Читайте также:
- Систолический шум при ДМПП. Степень расщепления II тона при ДМПП
- Показания и противопоказания для поясничной пункции. Особенности у новорожденных
- Доступ и ход операции резекции холангиокарциномы с наложением билатеральных гепатикоеюностом
- Эхокардиография при сердечной недостаточности. Объем левого желудочка
- Хирургическое лечение разрывов сетчатки, катаракты при эпимакулярной мембране (ЭММ). Рекомендации
