Доступ и ход операции резекции холангиокарциномы с наложением билатеральных гепатикоеюностом
Добавил пользователь Алексей Ф. Обновлено: 21.01.2026
Отделение гепатопанкреатобилиарной хирургии ГБУЗ Московский клинический научно-практический центр им. А.С. Логинова Департамента здравоохранения города Москвы, Москва, Россия
ГБУ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы", Москва, Россия;
ФГБОУ ВО МГУ им. М.В. Ломоносова, Москва, Россия
ФГБУ "Институт хирургии им. А.В. Вишневского" Минздрава России, Москва
Хирургический стационар №2 Центральной городской клинической больницы Реутова, Московская область
Институт хирургии им. А.В. Вишневcкого МЗ РФ, Москва
Городская клиническая больница №68, Москва
Внутрипеченочная холангиокарцинома с инвазией в сосуды: оправдано ли хирургическое лечение?
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2018;(6): 49‑57
Внутрипеченочная холангиокарцинома (ВХК) ― одна из наиболее агрессивных опухолей, ассоциированных с плохим прогнозом. Основным методом лечения в резектабельных случаях остается радикальная хирургическая операция. Наиболее трудновыполнимой она становится при местно-распространенных формах поражения, особенно при вовлечении нижней полой вены (НПВ) и воротной вены (ВВ). Цель исследования ― проанализировать безопасность выполнения обширных резекций печени, комбинированных с резекцией и реконструкцией магистральных сосудов при местно-распространенных больших и множественных поражениях холангиоцеллюлярным раком внутрипеченочной локализации. Материал и методы. С января 2014 г. по апрель 2017 г. 80 пациентам с холангиокарциномой выполнены обширные резекции печени. Среди них ― 62 были радикально оперированы по поводу воротной холангиокарциномы и 18 с ВХК. Резекция и реконструкция сосудов потребовались 4 пациентам с ВХК: в 2 случаях ― протезирование НПВ (из них 1 пациенту ― в условиях обходного вено-венозного шунтирования), в 2 случаях ― краевая и циркулярная резекции бифуркации воротной вены. Результаты. Послеоперационные осложнения класса IIIа по классификации Clavien―Dindo развились во всех 4 случаях. Сосудистые осложнения отсутствовали. Продолжительность пребывания в стационаре колебалась от 14 до 35 дней. Летальных исходов не было. Годичная выживаемость составила 50%. 25% пациентов пережили двухлетний рубеж. Все пациенты получали адъювантную химиотерапию. Вывод. Обширные резекции печени, комбинированные с резекцией НПВ и ВВ при местно-распространенной ВХК, могут быть выполнены безопасно для пациентов и в последующем позволяют провести химиотерапевтическое лечение.
Внутрипеченочная холангиокарцинома (ВХК) является одной из наиболее агрессивных опухолей, на долю которой приходится около 10―15% всех первичных злокачественных заболеваний печени [1, 2]. У пациентов, не имеющих отдаленных метастазов, примерно в 50% случаев диагностируют местно-распространенные формы с вовлечением соседних органов и магистральных печеночных сосудов [3]. Радикальная резекция остается основным методом лечения пациентов с резектабельными формами поражения [4].
В течение последнего десятилетия большинство авторов согласились, что агрессивная хирургическая тактика, включающая резекцию сосудов, оправдана, когда она позволяет выполнить R0-резекцию при условии отсутствия отдаленных метастазов [1]. Ввиду агрессивности ВХК более чем в 80% случаев пациентам требуется проведение обширной резекции печени и смежных структур ― внепеченочных желчных протоков, сосудов, в том числе нижней полой вены (НПВ), воротной вены (ВВ) или печеночной артерии (ПА) и диафрагмы [5, 8]. К сожалению, хирургическое вмешательство выполняется лишь у 40% потенциально резектабельных пациентов.
Несмотря на то что при местно-распространенных ВХК радикальная операция способна увеличить общую выживаемость, не все онкологи солидарны по поводу подобной тактики лечения и считают хирургическое лечение неоправданным [5―7].
В этой связи нами проведен анализ собственного опыта хирургического лечения у ограниченного числа пациентов с местно-распространенной ВХК с инвазией в сосуды.
Материал и методы
За период с января 2014 г. по апрель 2017 г. в отделении гепатопанкреатобилиарной хирургии Московского клинического научно-практического центра им. А.С. Логинова радикально оперированы 80 пациентов с холангиокарциномой. Среди них 62 пациента страдали воротной холангиокарциномой и 18 пациентов ― холангиокарциномой внутрипеченочной локализации. У 4 (22%) пациентов с ВХК были выполнены резекция и реконструкция сосудов.
В исследование включены 1 мужчина и 3 женщины, средний возраст которых составил 59,5±7,5 года (от 52 до 67 лет). Среди 4 случаев 1 пациент поступил в стационар с механической желтухой, и с целью предоперационной билиарной декомпрессии ему была выполнена чрескожная чреспеченочная холангиостомия.
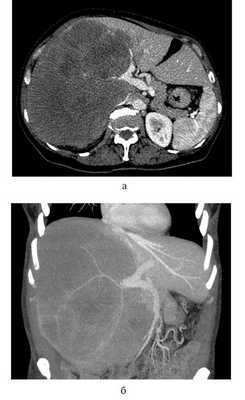
У одной пациентки 57 лет с местно-распространенной мультифокальной ВХК, вовлекающей ретропеченочный отдел НПВ, болезнь манифестировала болью в верхних правых отделах живота и синдромом нижней полой вены. Имеющиеся отеки нижних конечностей и нижней половины туловища уменьшались при положении больной на правом боку. У данной пациентки выявлено образование (ВХК, достигающая 34 см в наибольшем измерении) в V―VIII сегментах, распространяющееся на IV сегмент и хвостатую долю печени. Массив опухоли распространялся на ретропеченочный отдел НПВ (рис. 1). Рис. 1. Предоперационная К.Т. с контрастным усилением у пациентки с гигантской местно-распространенной внутрипеченочной холангиокарциномой, инвазирующей НПВ и правую ветвь ВВ. а ― в аксиальной плоскости; б ― коронарная томограмма. КТ ― компьютерная томография; НПВ ― нижняя полая вена; ВВ ― воротная вена. Во II и IV сегментах печени выявлены мелкие, менее 2 см, сателлитные очаги ВХК. Поскольку образование полностью замещало правую долю печени и распространялось на S4, объем остатка печени (S2, S3 и медиальная часть S4) составил 100%. При гепатобилиосцинтиграфии подтвержден адекватный функциональный резерв печени, позволяющий выполнить запланированное вмешательство в объеме расширенной правосторонней гемигепатэктомии.
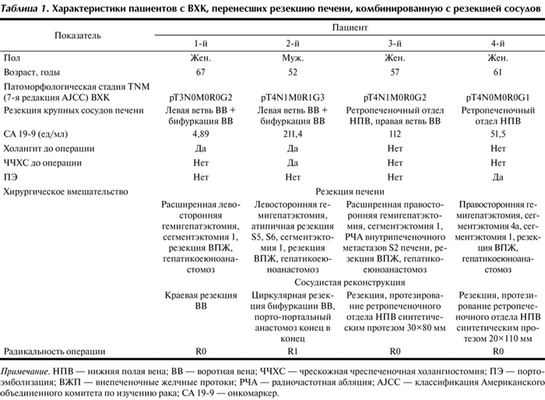
Клинико-патологические данные пациентов, включенных в исследование, представлены в табл. 1. Таблица 1. Характеристики пациентов с ВХК, перенесших резекцию печени, комбинированную с резекцией сосудов Примечание. НПВ ― нижняя полая вена; ВВ ― воротная вена; ЧЧХС ― чрескожная чреспеченочная холангиостомия; ПЭ ― портоэмболизация; ВЖП ― внепеченочные желчные протоки; РЧА ― радиочастотная абляция; AJCC ― классификация Американского объединенного комитета по изучению рака; СА 19−9 ― онкомаркер.
Стадирование и определение тактики лечения осуществлялись мультидисциплинарным консилиумом с участием хирургов, онкологов, анестезиологов и специалистов лучевой диагностики и интервенционной радиологии.
Для снижения давления в ВВ и с целью профилактики пострезекционной печеночной недостаточности интраоперационно и в течение 3 сут после вмешательства всем пациентам внутривенно вводили октреотид в дозе 1000―1200 мкг/сут.
В течение первых 5 суток послеоперационного периода рутинно осуществляли лабораторный контроль и ультразвуковое исследование с допплерографией. Все осложнения, возникшие в первые 90 дней после вмешательства, оценивали согласно классификации Clavien―Dindo [9, 10]. К тяжелым относили осложнения III класса и выше. Общая выживаемость рассчитывалась со дня хирургического вмешательства до момента смерти, наступившей от любых причин.
Резекция ВВ была произведена 2 больным: 1-му пациенту с инвазией левой ветви ВВ выполнены расширенная левосторонняя гемигепатэктомия, сегментэктомия 1 и краевая резекция бифуркации ВВ; 2-му пациенту ― левосторонняя гемигепатэктомия, атипичная резекция S5, S8, сегментэктомия 1 и резекция ствола ВВ с формированием анастомоза конец в конец. В данной серии наблюдений истинная сосудистая инвазия ВХК отмечалась у всех пациентов.
Выполнение резекции ретропеченочного отде-ла НПВ потребовалось 3-му и 4-му пациентам (табл. 2). Таблица 2. Послеоперационные осложнения, данные гистологического патоморфологического исследования и статус краев резекции у пациентов, перенесших обширные резекции печени и резекции сосудов Ввиду нетолерантности к пережатию НПВ ее протезирование 3-му пациенту осуществлено в условиях обходного вено-венозного шунтирования. В данном случае НПВ замещена сосудистым протезом из политетрафторэтилена диаметром 30 мм и длиной 80 мм (см. рис. 2). Рис. 2 . Вид операционной раны после удаления препарата и протезирования НПВ. НПВ ― нижняя полая вена. Выполне-на радиочастотная абляция сателлитного очага S2 печени.
Продолжительность выполненных операций колебалась от 595 до 740 мин (ср. 677,5 мин). У 3-го пациента, которому проводилось протезирование ретропеченочного отдела НПВ в условиях вено-венозного шунтирования, продолжительность операции достигла 720 мин. Продолжительность вмешательства у 4-го пациента, которому также выполнено протезирование НПВ, но без обходного шунтирования, достигла 740 мин ввиду выраженного адгезивного процесса в брюшной полости. Гемотрансфузия потребовалась в 2 случаях. Средняя интраоперационная кровопотеря составила 2450 мл (500―7500 мл). Оперированные пациенты в среднем нуждались в трансфузии 3 (0―7) доз эритроцитарной массы.
Во всех случаях резекция печени выполнялась в условиях интермиттирующего пережатия гепатодуоденальной связки. Средняя продолжительность Pringle-маневра составила 12 мин (0―33 мин).
Вено-венозное шунтирование при протезировании НПВ продолжалось в течение 40 мин.
Результаты
В течение 90 дней послеоперационного периода у всех 4 пациентов развились осложнения стадии IIIa―b согласно классификации Clavien―Dindo. У 2-го пациента после расширенной левосторонней гемигепатэктомии наблюдалась пострезекционная печеночная недостаточность класса, А согласно классификации International Study Group of Liver Surgery (ISGLS) [11]. В течение недели для снижения «портального удара» и лечения печеночной недостаточности больной получал октреотид в течение 5 сут в дозе 1200 мкг/сут.
Сосудистых осложнений, равно как и госпитальной летальности, в данной серии наблюдений не было. Средняя продолжительность пребывания в стационаре составила 19 дней (14―35 дней). Более подробная информация об осложнениях и данные патоморфологического исследования представлены в табл. 2.
Годичная выживаемость составила 50%, 25% пациентов пережили двухлетний рубеж, 1 пациент находится под наблюдением уже 30 мес.
До недавнего времени местно-распространенная форма ВХК, представленная массивным и/или множественным поражением, инвазией крупных сосудов, вовлечением смежных органов, а также наличием внутрипеченочных метастазов и статусом N1, являлась абсолютным противопоказанием к хирургическому лечению [7, 12, 13]. Позже попытки радикально оперировать пациентов с местно-распространенным процессом все же предпринимались, но продолжали ассоциироваться с плохим прогнозом [14].
Развитие анестезиологических и хирургических технологий в течение последних нескольких лет позволяет выполнять радикальные вмешательства в центрах, имеющих опыт гепатопанкреатобилиарной хирургии и трансплантации органов, тем самым увеличить частоту радикальных операций и продолжительность выживаемости пациентов с ВХК [15―17].
Безусловно, обширные резекции печени могут и должны выполняться пациентам с местно-распространенным холангиоцеллюлярным раком. Некоторые авторы утверждают, что радикальная операция остается основным шансом для продления жизни даже у больных, страдающих холангиокарциномой. Лучшие результаты были сообщены O. Hyder и S. Marubashi, которым удалось достичь 5-летней выживаемости в 39,8 и 40,5% случаев соответственно [18, 19].
Основываясь на анализе лечения 221 пациента, H. Bektas и соавт. сообщили, что выживаемость неоперированных радикально пациентов была значительно ниже и составила 26 и 3,4% через 1 и 3 года соответственно. Больные, включенные в исследование H. Bektas, имели значительно бόльшие по размеру опухоли, что объясняет более низкую выживаемость [20].
Хирургические вмешательства при больших и мультифокальных поражениях ВХК также оправдываются многоцентровым исследованием, проведенным в 2015 г. G. Spolverato и соавт. [21].
В настоящем исследовании проанализированы данные пациентов с несколькими критическими факторами риска, ассоциированными с неудовлетворительным прогнозом. У 2 пациентов имелись гигантские ВХК, а у 1 из них состояние осложнялось наличием внутрипеченочных метастазов (3-й пациент). Кроме того, прогноз лечения усугублялся, а вероятность выполнения радикальной операции снижалась у всех пациентов из-за наличия инвазии сосудистых структур (НПВ и ВВ). В данной серии не встречались инвазии ПА, что рассматривают в качестве дополнительного фактора риска неблагоприятного прогноза.
Всем включенным в исследование пациентам произведенные хирургические вмешательства в последующем позволили провести химиотерапию. В настоящее время выполнение радикальной операции при внутрипеченочном холангиоцеллюлярном раке стало возможным в большинстве случаев. Успех лечения зависит от мультидисциплинарного подхода к лечению и проведения подобных вмешательств в специализированных центрах.
Таким образом, наш опыт показывает, что в настоящее время тщательно отобранные пациенты с местно-распространенной ВХК, требующей резекции печени, комбинированной с сосудистой реконструкцией, должны рассматриваться в качестве потенциальных кандидатов для подобных вмешательств. Обширные резекции при местно-распространенном внутрипеченочном холангиоцеллюлярном раке с вовлечением крупных сосудов целесообразны и должны выполняться в центрах, имеющих опыт в хирургии печени. В сравнении с неоперированными пациентами радикальная операция способна увеличить продолжительность жизни и позволяет провести медикаментозное лечение.
Холангиокарцинома: стадии, лечение и прогноз
Смертность у людей, страдающих онкологией, ежегодно растет. Раковое поражение органов приводит к неутешительным прогнозам. Врачи бьют тревогу, ведь предотвратить развитие и осложнения онкологии поможет исключительно своевременное обращение и проведение диагностики на раннем этапе.
Печень - жизненно-важный орган, поэтому необходимо беречь его от негативного, канцерогенного химического воздействия извне. В случае поражения желчных протоков нарушается их основная функция - поставка пищеварительных ферментов в печень и желчный пузырь. Может начать развитие тяжелая форма рака - холангиокарцинома. Это опухоль на участках желчных протоков. Заболевание - смертельное. Даже хирургическое, паллиативное вмешательство не гарантирует положительных прогнозов для пациентов в большинстве случаев.
Что за болезнь?
Холангиокарцинома - патологический злокачественный процесс в желчных протоках с образованием опухолевидного тела. Через протоки поставляется желчь в кишечник. Процесс жизненно необходим для нормального переваривания, усвояемости поступающей пищи в организм. Каждый из протоков разделен на 2 части. Первая находиться в тканях печени, вторая - в самом органе.
Желчные протоки - 2 небольшие трубки, предназначенные для сбора желчи. На отдельном участке они сливаются между собой, образуя 2 печеночных канала: правый и левый. Общий желчный проток расположен в воротах печени.
Отличительная особенность холангиокарциномы печени - произрастание опухоли из эпителиальных клеток желчных протоков. Хотя формирование узла возможно в любом из отделов органа.
Факторы риска
Учеными не выяснены точные провоцирующие факторы, способные повлиять на развитие опухоли в желчных протоках. Есть предположения, что причиной развития карциномы может стать:
- наследственный фактор;
- заболевание Кароли;
- киста желчного протока;
- врожденное аномальное развитие протоков, системы желчевыделения;
- воздействие химикатов, диоксида тория - рентгеноконтрастного вещества;
- паразитарные инфекции (печеночная двуустка, аскариды, описторхи);
- хроническое воспаление в кишечнике;
- болезнь Крона;
- язвенный колит;
- цирроз печени;
- камнеобразование в желчных протоках;
- вирусный гепатит;
- генетическая предрасположенность к синдрому Линча, приводящая к мутациям в желчном пузыре, стенках толстой кишки.
Высокий процент заболеваемости среди жителей Азии, Японии, Дальнего Востока. Чаще холангиокарцинома развивается как железистая опухоль, реже - как недифференцированный либо плоскоклеточный рак.
Разновидности
С учетом классификации, характера, роста, месторасположения микроскопической структуры опухоль желчных протоков бывает:
- внутрипеченочная: формируется внутри печени, мелких протоков;
- внутригрудная: локализуется в печеночных воротах, в местах соединения в общий проток;
- дистальная: располагается близ тонкой кишки.
По структуре холангиокарцинома бывает: внутрипротоковая, инфильтрирующая, массивная. По характеру течения различают 4 вида опухоли:
- полиповидная: произрастает из просвета протоков, прикрепляется к стенкам на тонкой ножке;
- экзофитная: появляется во внутренней части протока, постепенно переходя на внешнюю сторону;
- инфильтративная: образуется в тканях желчного пузыря;
- смешанная: имеет признаки 2-х и более форм в совокупности.
Симптомы
Признаки напрямую зависят от месторасположения холангиокарциномы. Самые распространенные:
- бледность, желтизна покровов кожи;
- потемнение мочи;
- билирубинурия, конъюгированный билирубин в составе крови;
- зуд тела;
- колики в животе;
- тупая боль в правом квадранте печени с отдачей в спину;
- резкое снижение веса;
- диспепсические расстройства;
- отхождение бесцветного кала в случае затрудненного попадания желчи в просвет кишечника.
Заболевание не вызывает желчные колики, но желтуха прогрессирует. Сильной боли в области печени не наблюдается. Это представляет некие трудности по выявлению карциномы на начальном этапе. Зачастую пациенты слишком поздно обращаются к онкологам, когда признаки становятся явными:
- тяжесть в правом подреберье;
- увеличение печени в размерах;
- застой желчи;
- нарушение пищеварения;
- тошнота;
- диарея;
- рвота;
- резкое снижение веса, истощение организма;
- раковая интоксикация;
- повышение температуры, лихорадка.
К осложнениям стоит отнести: печеночную недостаточность, сильное кровотечение, абсцесс печеночной ткани. По мере появления метастаз и достижения опухоли внушительных размеров наблюдается сдавливание воротной вены, увеличение размера селезенки, асцит по мере накопления плевральной жидкости в животе. Симптомы становятся очевидными лишь в момент прохождения желчи по протокам из-за перекрытого просвета. Затрудняется продвижение желчного содержимого по мере увеличения новообразования в размере.
Опухоль Клацкина располагается в глубинных тканях и не распознается при визуальном осмотре и пальпации. Только проведение полноценной диагностики позволит поставить правильный диагноз.
Диагностика
Выявить холангиокарциному позволяет проведение лабораторных, инструментальных тестов. При подозрении пациентам предстоит сдать анализ крови на билирубин и щелочную фосфатазу, процентное содержание лейкоцитов, признаки анемии.
- позитронно-эмиссионная томография: позволяет выявить опухоль на участке желчных протоков путем введения контрастного вещества;
- биопсия: изучение биоматериала, гистологическое исследование;
- МРТ: безопасный, информативный метод для определения размеров и расположения опухоли, просмотра сосудистых структур и желчных протоков в трехмерном изображении;
- специальные онкомаркеры с выявлением антигена СА 19-9 высокого уровня;
- УЗИ желчного пузыря, печени и желчевыводящих путей;
- эндоскопическая, ретроградная холецистография: показывает места обструкции злокачественных видоизменений на участке фатерова сосочка.
Лечение на разных стадиях
Патология с локализацией в желчных протоках вызывает некие трудности при лечении, поскольку считается труднодоступной и неоперабельной. Однако основой лечения холангиокарциномы по сей день остается хирургическая операция или холедохотомия на раннем этапе, когда опухоль еще не проросла в стенки желчных протоков, имеет незначительные размеры.
Применима объемная операция Уиппла в случае выявления довольно крупного новообразования. Терапия заключается в удалении всех пораженных участков, отдельных фрагментов поджелудочной железы, желудка, неоплазии, печени, желчных протоков, лимфоузлов. В запущенных случаях проводится радикальная операция с удалением внушительного объема патологической ткани. Но послеоперационный период уже не гарантирует пациентам (пожилым) высокого процента выживаемости.
Один из радикальных способов при холангиокарциноме печени лечения - это пересадка органа. Сложность представляет подбор трансплантирующего органа. Если лечение радикальным путем невозможно, онкологи могут принять решение о проведении паллиативной операции путем наложения анастомоза на стенке желудка или проведения стентирования.
Операция - единственный вариант при лечении заболевания на начальном этапе, когда опухоль еще не вышла за стенки желчных протоков. Паллиативная методика проводится на 3-4 стадии рака, помогая несколько улучшить качество жизни пациентов.
Если рак прогрессирует, образуются метастазы, опухоль вышла за пределы желчных протоков в печень, единственный способ спасти жизнь больному - удалить практически весь орган, но без последующей трансплантации тогда не обойтись. В большинстве случаев летальный исход неизбежен.
Другие методы лечения
Если опухоль не подлежит удалению оперативным путем, имеет незначительные размеры или не прорастает в стенки желчных протоков, то возможно проведение:
- холедохотомии;
- лобэктомии по резекции отдельной доли печени;
- химиотерапии при холангиокарциноме печени с включением медикаментов (гемцитабин, фторурацил) для разрушения злокачественных клеток, облегчения оттока желчи, предупреждения роста опухоли.
Прогноз
При холангиокарциноме печени прогноз неутешительный. Выживаемость - не более 5 лет, если выявлен внепеченочный рак.
Выживаемость не превышает 1,5 лет даже после проведения операции в случае 3-4 стадии рака. Если опухоль неоперабельная, пациентам остается жить не более 0,5 лет.
При холангиокарциноме печени прогноз выживания зависит от наличия (отсутствия) метастазов, возраста больного, сопутствующих заболеваний, степени дифференцировки опухоли. Большинство пациентов обращается за помощью к врачам слишком поздно, когда появляются метастазы. Тогда лечение становится просто безрезультативным.
Профилактика заболевания
Меры профилактики простые, но крайне важные:
- устранение воспалительных процессов на начальном этапе;
- лечение заболеваний печени;
- выведение паразитов из организма;
- избегание контактов с химическими канцерогенными веществами;
- отказ от курения, злоупотребления алкоголем.
Холангиокарцинома - коварное заболевание, при котором даже своевременно проведенная операция по удалению опухоли не гарантирует достижение устойчивой ремиссии. Добиться выживаемости до 4-5 лет удается лишь при выявлении внепеченочной холангиокарциномы. Если появились отдаленные метастазы, то при холангиокарциноме прогноз крайне неблагоприятный. К тому же часто развиваются осложнения: сепсис, билиарный цирроз печени, асцит, сильное истощение организма.
Онкологи настоятельно рекомендуют своевременно обращаться за квалифицированной помощью. Ведь проведенная операция на раннем этапе может стать единственным спасением, значительно продлить и улучшить качество жизни.
Доступ и ход операции резекции холангиокарциномы с наложением билатеральных гепатикоеюностом
Тимофеев Илья Валерьевич
Директор Бюро по изучению рака (Россия), член Международного комитета ASCO (США), член научного комитета Колледжа Европейской Школы Онкологии (ESCO)
Рак билиарного тракта - это группа опухолей, развивающихся из эпителия внутри- и внепеченочных желчных протоков (холангиокарциномы), а также желчного пузыря [1]. Термин холангиокарцинома подразумевает 3 типа опухолей с различными факторами риска, свойствами и лечебными подходами - это внутри- и внепеченочные опухоли, а также поражение желчных протоков ворот печени, относящееся к опухолям внепеченочной локализации (опухоль Клацкина). Считается, что на опухоли билиарного тракта приходится около 3% от всех опухолей желудочно-кишечного тракта (ЖКТ), внутрипеченочные холангиокарциномы составляют около 10% случаев первичного рака печени, среди холангиокарцином на опухоль Клацкина приходится 50% случаев, из них на опухоли дистальной локализации - 40%, внутрипеченочное поражение встречается в 10% случаев [1]. В среднем заболеваемость холангиокарциномой в США составляет 1,26 случая на 100 000 населения [1,2].
Холангиокарцинома исконно считалась опухолью с печальным прогнозом. Хирургическое лечение до настоящего времени было единственным возможным более-менее эффективным подходом. Тем не менее, даже оно является вариантом лечения только 35% пациентов [3], из которых еще 35% впоследствии имеют рецидив в течение 2 лет [4]. На протяжении 10 лет стандартом первой линии терапии у больных местно-распространенной или метастатической холангиокарциномой остается химиотерапия на основе комбинации гемцитабина и цисплатина, что приводит к медиане общей выживаемости в 11,7 мес. [5]. При прогрессировании болезни на первой линии эффективных опций ранее не существовало. Попытки использовать различные химиотерапевтические режимы как в монотерапии, так и в комбинациях не увенчались успехом 7. Чтобы не оставить пациента без лечения, в качестве последующей терапии эмпирически назначаются фторпиримидины, их комбинации с оксалиплатином или иринотеканом [1].
В эпоху таргетной терапии исследователи пытались перенести ингибиторы семейств HER (ERBB), HGF/c-MET, Hedgehog, KRAS-BRAF-MEK-ERK и PI3K/AKT/mTOR, зарекомендовавшие себя при других опухолях, на лечение билиарного рака, однако ни одно из исследований не оказалось позитивным в сравнении со стандартной химиотерапией [9]. Совсем недавно ученые обратили внимание на новые молекулярные изменения в клетках холангиокарциномы - в семействе фактора роста фибробластов (FGF) и его рецепторов (FGFR), а также изоцитрат дегидрогеназы (IDH) -1 и -2.
Изменения FGFR встречаются в среднем у 7,1% всех онкологических пациентов [10], являются мишенью терапии некоторых опухолей ЖКТ, например, рака желудка [11,12]. Холангиокарцинома относится к опухолям с наиболее частыми альтерациями FGFR. Так, перестройки и слияния в генах FGFR, особенно FGFR2, были выявлены у 6,1-16% больных [10,13,14]. Следовательно, закономерным было разработать и изучить ингибиторы FGFR2 у этих пациентов.
При медиане наблюдения 17,8 мес. объективные ответы были зафиксированы у 38 больных, что составило 35,5%. У трех пациентов был достигнут полный ответ на лечение. Это соответствовало статистической гипотезе, и исследование достигло первичной конечной точки. Ответ развивался достаточно быстро - через 2,7 мес., а продолжался долго (учитывая категорию больных и тип опухоли) - 7,5 мес. Медиана выживаемости без прогрессирования составила 6,9 мес. Медиана общей выживаемости при продолжающемся наблюдении была рассчитана как 21,1 мес. Гиперфосфатемия - класс-специфическое нежелательное явление - была наиболее распространенным вариантом токсичности всех степеней с частотой 60%. 64% больных имели нежелательные явления 3 степени или выше: гипофосфатемию (12%), артралгию (6%), стоматит (5%), гипонатриемию (5%), боли в животе (5%) и усталость (5%). 45% пациентов имели серьезную токсичность: наиболее частыми были боли в животе (5%), гипертермия (5%), холангит (3%) и плевральный выпот (3%). Ни одна смерть не считалась связанной с лечением.
Имея такие результаты, несомненно, можно согласиться с решением FDA одобрить пемигатиниб для лечения столь агрессивной опухоли, продолжительность жизни больных которой, не ответивших на первые линии терапии, не превышала ранее 6,5-13,4 мес. Пемигатиниб увеличивает эту цифру не менее чем в 2 раза. В настоящее время анонсировано и продолжается исследование 3 фазы FIGHT-302 [17]. В нем пемигатиниб сравнивается с комбинацией гемцитабина и цисплатина в первой линии терапии метастатической холангиокарциномы с перестройками в гене FGFR2.
Другим направлением в таргетной терапии метастатической холангиокарциномы является ингибирование IDH. Мутация IDH встречается в клетках внутрипеченочных холангиокарцином в 10-20% случаев [20,21]. IDH имеет 3 изоформы, из которых в канцерогенезе наибольшую роль играют IDH1 и IDH2. Чаще встречаются мутации IDH1, чем IDH2. Соматические мутации IDH1/2 появляются на ранних этапах развития опухоли. Повышение активности IDH1/2 приводит к изменениям клеточного метаболизма и последующей аккумуляции метаболита 2-гидроксиглютарата как в опухолевых клетках, так и в крови, который блокирует клеточную дифференцировку и индуцирует туморогенез. Прогностического интереса мутации IDH1/2 не представляют, однако являются отличной мишенью для блокирования.
Рак желчных протоков
Рак желчных протоков (холангиокарцинома)- злокачественная опухоль, происходящая из эпителия желчных протоков. Рак внепеченочных желчных протоков встречается значительно чаще рака внутрипеченочных желчных протоков.
Акции
Полное обследование на онкологические заболевания для мужчин и женщин.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Содержание статьи:
Холангиокарцинома желчных протоков — это злокачественное новообразование, состоящее из патологически измененных клеток желчных протоков. В большинстве случаев рак желчных протоков развивается у мужчин среднего и пожилого возраста. Заболевание чаще встречается в странах, где распространены паразитарные патологии печени. Всего регистрируется 1-2 случая данного типа рака на сто тысяч населения.
Классификация холангиокарциномы
По локализации различают следующие формы патологии:
По типу роста выделяют следующие виды опухоли:
- инфильтративная;
- экзофитная;
- полиповидная;
- смешанная.
Причины рака желчных протоков и факторы риска
К сожалению, несмотря на многолетнее изучение, точные причины развития данного типа рака неизвестны. Существует ряд факторов, которые могут спровоцировать развитие заболевания. К ним относят:
- склерозирующий первичный холангит — это хроническое заболевание неясной этиологии;
- болезнь Кароли — врожденная патология, при которой происходит образование большого количества внутрипеченочных кист;
- гепатоз печени;
- аденомы;
- сахарный диабет;
- паразитарные болезни печени;
- работа на вредном производстве;
- ВИЧ-инфекция;
- синдром Линча — это наследственная патология, которая повышает риск развития онкологических заболеваний органов пищеварения;
- гепатит В, С;
- болезнь Крона — тяжелое хроническое заболевание, при котором наблюдается воспаление слизистых оболочек пищеварительного тракта;
- цирроз печени;
- вредные привычки.
Симптомы рака желчных протоков
Одним из главных симптомов холангиокарциномы является механическая желтуха, которая сопровождается сильным кожным зудом. Кал у пациента обесцвеченный. Болей перед желтухой обычно нет, приступы колики случаются редко. При быстрой закупорке просвета протока опухолью перед желтухой могут возникать приступы боли.
К симптомам и признакам рака желчных протоков также относят диспепсический синдром, снижение аппетита, потерю веса. Температура тела у части пациентов остается в пределах нормы, у части повышается. В результате застоя желчи нарушается работа печени. Она при пальпации безболезненна, увеличена, имеет гладкий край.
Одним из методов дифференциальной диагностики желтух является пальпация желчного пузыря. При этом опухоль в большинстве случаев не пальпируется, так как расположена в глубине брюшной полости и имеет небольшие размеры. При сдавливании новообразованием воротной вены развивается водянка брюшной полости.
Стадии холангиокарциномы
Выделяют четыре стадии заболевания:
Первая стадия. Новообразование находится ниже слияния печеночных протоков, без вовлечения в патологический процесс места их соединения (конфлюенса).
Вторая стадия. Опухоль по-прежнему находится ниже слияния протоков, но распространяется на место их соединения.
Третья стадия. Новообразование продолжает разрастаться и постепенно поражает левый и правый печеночный проток.
Четвертая стадия. Поражаются сегментарные протоки.
Согласно классификации по TNM выделяют следующие типы и степени заболевания:
| T0 | Никаких видимых признаков наличия новообразования нет |
| Tis | Очаг поражения локализован в пределах желчных протоков |
| T1 | Новообразование все еще находится в пределах пораженного органа, начинает прорастать в мышечную и фиброзную ткань |
| T2 | Очаг поражения распространяется за пределы протоков, опухоль начинает прорастать в близлежащие ткани печени |
| T3 | Новообразование распространяется на печеночные артерии |
| T4 | Опухоль прорастает в протоки печени либо в патологический процесс вовлекаются близлежащие сосуды |
Диагностика холангиокарциномы
Клинические признаки заболевания не являются специфическими, поэтому поставить диагноз рак желчных путей, основываясь только на данных анамнеза и клинического осмотра, не представляется возможным.
Пациенту дополнительно назначают следующие лабораторные и инструментальные диагностические исследования:
- (биохимический). Дает информацию о наличии в печени патологического процесса, но не позволяет поставить точный диагноз. В крови повышен уровень щелочной фосфатазы, билирубина. Показатели АСТ, АЛТ, а также концентрация альбуминов при данном виде онкологии обычно находятся в пределах нормы. холангиокарциномы. Имеет большое диагностическое значение. У пациентов выявляют антиген СА 19-9 (этот антиген также может синтезироваться при холангите и раке поджелудочной железы). Если уровень маркера у больных с хроническим холангитом сильно повышается (до 100 U/ml и больше), то, скорее всего, это говорит о развитии холангиокарциномы.
- УЗИ желчного пузыря и печени. Назначают на начальных этапах диагностики. При помощи данного метода можно обнаружить патологическое расширение протоков в некоторых местах, а также выявить новообразование большого размера.
- Допплерография сосудов печени. Выявляют нарушения кровотока в очаге поражения, но небольшие опухоли при помощи данной методики обнаружить не удается.
- КТ желчевыводящих путей. Более информативный метод диагностики. При помощи КТ можно увидеть опухоли небольшого размера, диагностировать увеличение регионарных лимфоузлов.
- МСКТ. Определяют степень закупорки желчевыводящих путей.
- ПЭТ КТ. Усовершенствованная методика. С ее помощью можно увидеть новообразования узлового типа размером менее одного сантиметра. Но инфильтрационные формы заболевания при помощи данной методики выявить сложно.
- Эндоскопическая ретроградная холецистография. Используется для уточнения диагноза. С ее помощью можно точно определить места закупорки желчных протоков и взять образец тканей для проведения гистологического исследования. . На сегодняшний день является наиболее информативным методом диагностики онкологических патологий желчных протоков и печени. При проведении данного исследования не используются контрастные вещества, метод неинвазивный, поэтому безопасный для здоровья пациента. На МРТ можно увидеть сосуды и желчные протоки в трехмерном изображении, правильно оценить стадию болезни, выявить новообразования небольших размеров, определить тактику дальнейшего лечения и дать прогноз.
Методы лечения холангиокарциномы
Выбор тактики терапии при раке протока желчного пузыря зависит от степени запущенности заболевания, локализации новообразования, возраста пациента, его общего самочувствия, наличия сопутствующих заболеваний.
Хирургические методы
Оперативное вмешательство при холангиокарциноме печени — это единственный вариант добиться полного выздоровления пациента. Но проведение радикальной операции возможно лишь в том случае, когда патология была выявлена на ранней стадии, опухоль имеет небольшие размеры и не вышла за пределы протоков. К сожалению, на этой стадии болезнь диагностируют крайне редко и обычно случайно, при проведении обследования по поводу другой патологии.
Вид оперативного вмешательства зависит от локализации очага поражения. При раке внутрипеченочных желчных протоков проводится частичная резекция печени. Оставшаяся часть органа пи этом продолжает функционировать.
При раке внепеченочных желчных протоков показано удаление очагов поражения, лимфоузлов, а также желчного пузыря, части печени, 12-ти перстной кишки, поджелудочной железы. Это сложная операция, которая может привести к развитию тяжелых осложнений. Поэтому выполнять ее должен хирург с большим практическим опытом проведения подобных хирургических вмешательств. Если диагностирован один узел небольшого размера, но при этом сильно нарушена работа печени (например, из-за цирроза), то проводится трансплантация.
Паллиативные операции
Проводятся, если радикальное вмешательство невозможно. Это может быть установка в желчные протоки стентов, наружно-внутренне и наружное дренирование. Специалисты нашей клиники имеют большой практический опыт проведения подобных операций.
Лучевая терапия
Может быть назначена до или после операции с целью уменьшения размеров рака желчных протоков печени и профилактики рецидивов заболевания. При запущенной онкологии радиотерапия может использоваться в качестве самостоятельного метода при проведении паллиативного лечения, направленного на облегчение самочувствия больного и повышение качества его жизни. Чаще всего используют внешние источники облучения. В ряде случаев применяют внутрибилиарную брахитерапию (пациенту в желчные пути на короткое время вводят специальный зонд, который является источником излучения).
ХИМИОТЕРАПИЯ
Также может быть назначена до или после операции либо самостоятельно, на последних стадиях холангиоцеллюлярного рака для облегчения страданий пациента. Химиотерапия может быть системной или внутриартериальной, когда растворы препаратов вводятся непосредственно в печеночную артерию. В результате в кровь попадает небольшое количество препарата, благодаря чему дозировку можно увеличить без риска развития побочных эффектов.
Химиолучевая терапия
Сочетание двух вышеперечисленных методик. Это позволяет более эффективно уничтожать клетки опухоли. Но при таком лечении велик риск развития серьезных побочных эффектов.
Прогноз при холангиокарциноме печени
Средняя продолжительность жизни при раке желчных протоков составляет два года. Пятилетняя выживаемость для дистальной формы патологии составляет 20-30%, для портальной и внутрипеченочной холангиокарциномы — 10%.
После радикального хирургического вмешательства и при отсутствии метастазов пятилетняя выживаемость при воротной холангиокарциноме составляет 30-65%, дистальной — 40-60%, внутрипеченочной — 36-43%.
Профилактика
Специфической профилактики заболевания не существует. Снизить риск развития онкологического поражения желчных протоков можно, выполняя следующие рекомендации:
- правильное питание;
- контроль веса;
- соблюдение режима труда и отдыха;
- избегание стрессовых ситуаций;
- отказ от малоподвижного образа жизни, регулярные прогулки на свежем воздухе;
- отказ от вредных привычек;
- соблюдение техники безопасности при работе на вредном производстве;
- вакцинация от вирусного гепатита;
- регулярное, не реже раза в год, прохождение профилактических осмотров, это поможет выявить возможные патологические изменения в желчных протоках на ранней стадии, что существенно облегчит лечение и улучшит прогноз.
Михайлов Алексей Геннадьевич оперирующий онколог, врач высшей квалификационной категории, к.м.н. стаж: 21 год
Информация в статье предоставлена в справочных целях и не заменяет консультации квалифицированного специалиста. Не занимайтесь самолечением! При первых признаках заболевания необходимо обратиться к врачу.
Холангиокарцинома проксимальных внепеченочных протоков, анализ хирургического лечения
Холангиокарцинома проксимальных внепеченочных протоков — это злокачественное новообразование в области бифуркации общего печеночного протока, обладающая инфильтративным ростом по ходу желчного протока и через его стенку. Заболевание актуально за счет большого количества неудовлетворительных результатов лечения, частого и прогрессирующего метастазирования и низкой выживаемостью.
Хирургическое лечение рака проксимальных желчных протоков (ПЖП) представляет особые трудности. Это объясняется расположением опухолей ПЖП в воротах печени, в непосредственной близости к воротной вене и печеночной артерии, с частой инвазией в паренхиму печени; наличием у большинства таких больных выраженной механической желтухи, часто осложненной гнойным холангитом. Вместе с тем, современные мировые тенденции в повышении радикальности операций и улучшении отдаленных результатов хирургического лечения рака ПЖП определяются все более агрессивным подходом за счет широкого использования комбинированных и обширных резекций желчных протоков и печени.
Целью работы являлся анализ выбора вида и объема оперативного вмешательства при хирургическом лечении холангиокарциномы проксимальных внепеченочных протоков.
Во время исследования проведен анализ 100 медицинских карт стационарных больных, находившихся на лечении в УЗ «9-я городская клиническая больница» г. Минск по поводу холангиокарциномы проксимальных внепеченочных протоков с 2012 по 2017 года.
В ходе проделанной работы для анализа стадии онкологического процесса использовалась стандартизированная классификация TNM для опухолей желчных протоков с локализацией в области ворот печени. Все пациенты были разделены на 4 групп согласно размеру и распространенности первичной опухоли (Т). Согласно полученным данным первая группа составила менее 2,0 %, в которую входили TX (первичная опухоль не может быть оценена), T0 (нет признаков первичной опухоли), Tis (карцинома in situ), T1(опухоль ограничена желчным протоком с вовлечением в патологический процесс мышечного или фиброзного слоев). Причем регионарные лимфатические узлы либо не могли быть оценены (NX), либо не выявлялись, тоже относилось и к отдаленным метастазам. Во вторую группу входили T2a и T2b (опухоль за пределами стенки желчного протока, распространяющаяся на окружающую жировую ткань и паренхиму печени) и составили 18 пациентов (18,0 %). Регионарные лимфатические узлы имели метастазы вдоль пузырного протока, общего желчного протока, портальной вены и печеночной артерии (N1), также отмечались случаи отдаленных метастазов (M1). В третью группу вошли 63 пациента (63,0 %), в которой наблюдалось распространение опухоли на унилатеральные ветви портальной вены и печеночной артерии (T3). Четвертая группа характеризовалась распространением опухоли на: портальную вену, ее ветви, общую печеночную артерию, ветви желчного протока; она составила 17 случаев (17,0 %) (T4). Поражение регионарных лимфатических узлов и наличие отдаленных метастазов отмечались в третьей и четвертой группах.
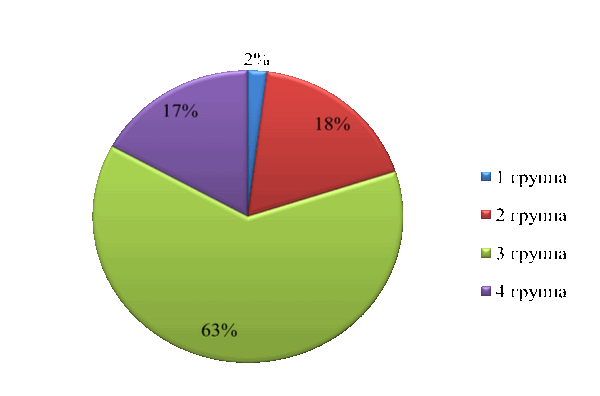
Рис. 1. Группы по классификации TNM
В результате исследования для локализации опухолевого процесса в печеночных протоках использована классификация Bismuth-Corlette, в которой все пациенты подразделены на следующие группы: холангиокарцинома I типа — (4 случая — 4,0 %); II типа — (13 случаев — 13,0 %); IIIa типа — (41 случай — 41,0 %); IIIb типа — (30 случаев — 30,0 %); IV типа — (12 случаев — 12,0 %);
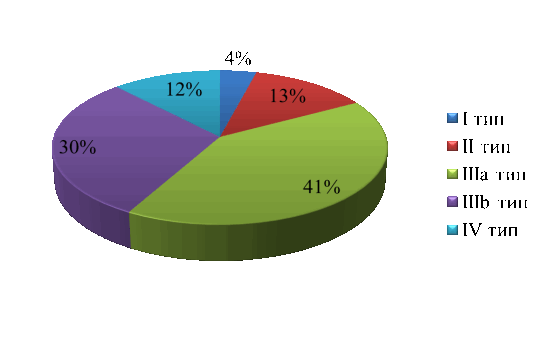
Рис. 2. Типы опухоли по Bismuth-Corlette
Из 100 пациентов только 37 (37,0 %) было проведено хирургическое лечение. Из них у 13 пациентов (35,1 %) с опухолью I и II типа выполнена резекция гепатикохоледоха с наложением бигепатикоеюноанастомоза. IIIa и IIIb типы составили 21 случай (56,8 %), у которых оперативное лечение заключалось в право- или левосторонней гемигепатэктомии, резекции гепатикохолодоха, воротной вены и регионарной лимфаденэктомии. При IIIa типе у 2 (9,5 %) пациентов была выполнена трансплантация печени. При IV типе опухоли в 3 случаях (8,1 %) произведена резекция патологических структур. У 63 пациентов (63,0 %) наблюдались неоперабельные опухоли, которым выполнялись эндоскопическое чрескожное чреспеченочное дренирование и транспапиллярное дренирование с имплантацией стента.
В заключение хотелось бы отметить, что из 100 пациентов с холангиокарциномой проксимальных внепеченочных протоков хирургическое лечение проведено у 37 (37,0 %). Объем и вид оперативного вмешательства зависит от локализации (типа) опухоли. Наиболее часто при опухоли IIIa типа (41,0 %) выполнялась право- или левосторонняя гемигепатэктомия, резекция гепатикохолодоха, воротной вены и регионарная лимфаденэктомия. Чрескожное чреспеченочное дренирование и транспапиллярное дренирование — методы паллиативного лечения при неоперабельных холангиокарциномах проксимальных внепеченочных протоков у 63,0 % пациентов.
- Bismuth, H. Intrahepatic cholangioenteric anastomosis in carcinoma of the hilus of the liver / H. Bismuth, M. B. Corlette // Surg. Gynecol. Obstet. — 1975. — Vol. 140. — P. 170-178.
- Extensive resection of the bile ducts combined with liver resection for cancer of the main hepatic duct junction: a cooperative study of the Keio Bile Duct Cancer Study Group / Y. Sugiura [et al.] // Surgery. — 1994. — Vol. 115. — P. 445-451.
- Klatskin, G. Adenocarcinoma of the hepatic duct at its bifurcation within the porta hepatis. An unusual tumor with distinctive clinical and pathological features / G. Klatskin // Am. J. Med. — 1965. — Vol. 38. — P. 241-256.
- Yasuji, S. Current surgical treatment for bile duct cancer / S. Yasuji, M. Masatoshi // World J. Gastroenterol. — 2007. — Vol. 13, N 10. — P. 1505- 1515.
Основные термины (генерируются автоматически): TNM, желчный проток, воротная вена, группа, пациент, первичная опухоль, печеночная артерия, портальная вена, проток, тип, хирургическое лечение.
Читайте также:
- Этапы и техника удаления ладонного апоневроза по Дюпюитрену (фасциоэктомии)
- Техника редукционной маммопластики с использованием круглого блока
- Пример интраперикардиальной перевязки сосудов. Трансперикардиальный доступ к сосудам при туберкулезе
- Старческие изменения желудочно-кишечного тракта, обмена веществ. Особенности
- Потенцированный наркоз под управляемым дыханием. Обеспечение операции на средостении
