Недостатки бронхографии. Дифференциация рака легкого
Добавил пользователь Cypher Обновлено: 02.02.2026
«Рак бронхов» — термин, который используется врачами редко. В медицине более распространено понятие «бронхопульмональный рак», которое объединяет злокачественные опухоли легких и бронхов. Такой подход к терминологии возник из-за того, что легочная ткань и бронхиальное дерево тесно связаны между собой, как в анатомическом, так и в функциональном смысле.
Некоторые цифры и факты, касающиеся рака бронхов:
- Заболевание чаще всего встречается у людей старшего возраста. Более чем в половине случаев оно диагностируется в возрасте старше 50 лет. Еще 25% случаев приходятся на возрастную группу 40-50 лет.
- Основная причина злокачественных опухолей бронхов — курение. До 80% больных — курильщики.
- Чаще всего опухоль возникает в верхних отделах бронхиального дерева, так как они лучше вентилируются, и канцерогены, которые содержатся во вдыхаемом воздухе, с большей вероятностью приведут к злокачественной трансформации клеток. [1,2]
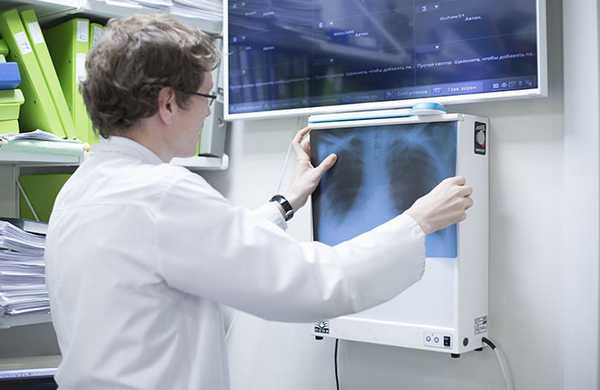
В каких бронхах возникают злокачественные опухоли?
Воздух, который вдыхает человек, проходит через нос, глотку, гортань, трахею. На уровне верхнего края пятого грудного позвонка трахея заканчивается и делится на два главных бронха. Это место называется бифуркацией трахеи. Главные бронхи — это бронхи первого порядка, они делятся на долевые (второго порядка), затем на сегментарные (третьего порядка), субсегментарные (четвертого порядка), дольковые, и, наконец, на терминальные (концевые) бронхиолы.
Все эти ветви вместе составляют бронхиальное дерево. Стенки крупных и мелких бронхов устроены одинаково: изнутри они выстланы слизистой оболочкой, под ней находится каркас — фиброзно-хрящевая оболочка, снаружи — адвентициальная оболочка.
Раком называют злокачественные опухоли, которые происходят из слизистой оболочки. Они могут возникать в любой части легкого, но чаще всего находятся в области ворот — там, где в легкое входит главный бронх. В двух третях случаев новообразование развивается в бронхах первого, второго и третьего порядка. [2,6,7]
Классификация
Гистологическая (основанная на внешнем виде опухолевых клеток под микроскопом) классификация бронхопульмонального рака включает четыре основных типа опухолей:
- Мелкоклеточный рак встречается главным образом у курильщиков, отличается высокой агрессивностью, быстро распространяется и с трудом поддается лечению. На его долю приходится около 12% всех случаев бронхопульмонального рака. [3]
- Плоскоклеточный рак вместе с двумя следующими типами объединяется в группу немелкоклеточных опухолей, которые составляют более 80% от всех случаев злокачественных опухолей легкого. Риск развития плоскоклеточного рака сильно связан с курением. [9,11]
- Аденокарцинома наиболее распространена среди женщин и некурящих людей. В отличие от плоскоклеточного рака, аденокарциномы обычно имеют более мелкие размеры и склонны к росту в периферических частях легкого. Отдельно выделяют подгруппу бронхоальвеолярных аденокарцином.
- Крупноклеточный рак состоит из крупных недифференцированных клеток. [1]
В зависимости от того, насколько сильно опухолевая ткань утратила черты нормальной, различают низкодифференцированные и высокодифференцированные опухоли. Первые более агрессивны.
При выборе лечения большое значение имеет расположение опухолевых очагов. В зависимости от этого показателя, бронхопульмональный рак делят на два типа:
- Центральный — опухоль находится в бронхах 1-3 порядка (главные долевые, сегментарные).
- Периферический — опухоль находится в более мелких бронхах. [2]
Стадии
Рак бронхов делят на стадии, в зависимости от того, насколько сильно опухоль распространилась в организме. При этом руководствуются общепринятой классификацией TNM. Буквы в ней обозначают:
- T — размеры первичного очага, степень прорастания в соседние ткани.
- N — поражение регионарных (близлежащих по отношению к первичной опухоли) лимфатических узлов.
- M — наличие отдаленных метастазов.
В зависимости от этих показателей, определяют стадию опухоли, которая обозначается римскими цифрами I-IV. [1,2]

Причины возникновения
Нормальная клетка превращается в опухолевую, когда в ее генах происходят некоторые изменения. Нельзя точно сказать, почему в том или ином случае возникли генетические дефекты, которые привели к злокачественной трансформации. Но известны факторы, которые существенно повышают риск заболевания. Их так и называют — факторы риска.
Основным фактором риска рака бронхов является курение. Вероятность того, что у человека будет диагностирована злокачественная опухоль, напрямую зависит от стажа курения, ежедневного количества выкуриваемых сигарет, возраста, в котором человек начал курить, марки сигарет (качество табака, содержание канцерогенов). Опасно не только активное, но и пассивное курение. Если в квартире постоянно кто-то курит, риск развития злокачественных новообразований бронхов повышен у всех ее жильцов. [13]
Другие факторы риска:
- Профессиональные вредности: работники шахт, заводов, производящих цемент, стекло и стекловолокно.
- Контакт с химическими реактивами, некоторыми летучими веществами, асбестом.
- Загрязнение воздуха радоном — радиоактивным газом, который естественным образом выделяется из почвы при распаде урана.
- Он может накапливаться в помещениях. [12,13]

Симптомы рака бронхов
На ранних стадиях симптомы чаще всего отсутствуют. Опухоль диагностируют случайно во время рентгенографии. В ранней диагностике помогает регулярное прохождение флюорографии. Эксперты Американского онкологического общества рекомендуют курильщикам с большим стажем рассмотреть регулярное прохождение компьютерной томографии. Такие периодические исследования, призванные диагностировать злокачественные новообразования на ранних, бессимптомных, стадиях, называются скринингом.
Возможные симптомы рака бронхов:
- Упорный хронический кашель.
- Мокрота с примесью крови.
- Одышка.
- Боли в грудной клетке.
Даже когда появляются симптомы, распознать злокачественную опухоль бронхов не всегда получается сразу. Картина может напоминать вялотекущую пневмонию, плеврит или другое заболевание. Важно внимательно относиться к своему здоровью. Если у вас появились любые необычные симптомы, если они сохраняются достаточно долго, нужно обратиться к врачу и пройти обследование.
Раковые клетки производят разные вещества, которые поступают в кровоток и могут вызывать патологические изменения в организме. Это приводит к так называемому паранеопластическому синдрому. При раке легких и бронхов опухоль часто влияет на нервную систему. Это проявляется в виде нарушения походки, удержания равновесия, координации движений, глотания, речи, памяти, зрения, сна и др. [1,2]
Методы диагностики
Обычно опухоль выявляют с помощью рентгенографии. Уточнить ее размеры, расположение, количество очагов и их степень прорастания в окружающие ткани помогает КТ, МРТ. Применяют бронхоскопию — эндоскопическое исследование, во время которого специальный инструмент в виде длинного гибкого шланга — бронхоскоп — вводят в бронхиальное дерево и осматривают слизистую оболочку бронхов.
Биопсию можно провести и другими способами: с помощью иглы, введенной в легкое через стенку грудной клетки, во время торакоскопии, плевроцентеза. Также можно провести цитологическое исследование мокроты на предмет раковых клеток.
Обнаружить мелкие метастазы помогает ПЭТ-сканирование. Во время этого исследования в организм вводят сахар со специальной радиоактивной меткой. Радиофармпрепарат накапливается в опухолевых клетках и делает очаги видимыми на снимках, сделанных с помощью специального аппарата. [1,8]
При необходимости врач может назначить другие методы диагностики.

Лечение рака бронхов
При выборе тактики лечения врач должен учитывать многие факторы: стадию и тип опухоли, ее расположение в легком, наличие поражения регионарных лимфатических узлов и отдаленных метастазов, возраст, состояние здоровья пациента, сопутствующие заболевания. [10]
Хирургическое лечение бронхопульмонального рака
Хирургическое удаление опухоли зачастую является основным видом лечения локального рака бронхов и легких, когда отсутствуют отделанные метастазы. Цель радикальной операции — полностью удалить опухолевую ткань. В зависимости от размеров и расположения очагов, прибегают к разным видам хирургических вмешательств:
- Удаление всего легкого — пульмонэктомия.
- Удаление доли легкого — лобэктомия.
- Удаление сегмента легкого — сегментарная резекция.
- Удаление опухоли с некоторым количеством окружающей здоровой ткани — клиновидная резекция.
- Удаление пораженных лимфатических узлов — лимфодиссекция, лимфаденэктомия.
Операция может быть выполнена открытым способом (через разрез) или эндоскопически (видеоассистированная торакоскопическая хирургия, или, сокращенно — VATS). [2,6]
Лучевая терапия
Лучевая терапия при раке бронхов может сочетаться с хирургическим вмешательством. Перед операцией врач может назначить неоадъювантную лучевую терапию (в том числе в сочетании с химиотерапией), это помогает уменьшить опухоль, перевести ее в операбельное состояние. После хирургического лечения применяется адъювантная химиотерапия для уничтожения оставшихся раковых клеток и снижения риска рецидива.
Если опухоль неоперабельна, лучевая терапия становится основным видом лечения. При метастатическом раке она помогает бороться с болью и другими симптомами. [1,7]
Химиотерапия
Химиопрепараты — лекарственные средства, которые уничтожают активно размножающиеся клетки. Таким образом, их мишенью в организме в первую очередь становятся опухолевые клетки, но могут поражаться и здоровые, поэтому химиотерапия часто сопровождается побочными эффектами. Современные врачи знают, как снизить их риск, и как с ними бороться.
Как и лучевая терапия, химиотерапия при раке бронхов и легких бывает адъювантной, неоадъювантной, может выступать в качестве основного метода лечения. Используют разные химиопрепараты с различными механизмами действия. Как правило, врач назначает комбинацию двух или более препаратов. Комбинации подбирают в зависимости от типа и стадии опухоли. [9]
Таргетная терапия и иммунотерапия
Таргетная терапия и иммунотерапия — это современные, наиболее молодые направления в лечении рака, появление которых стало возможным благодаря бурному развитию молекулярной генетики в последние десятилетия:
- Таргетные препараты поражают определенную молекулу-мишень, которую раковые клетки используют для выживания, бесконтрольного размножения, активации роста кровеносных сосудов. Они действуют более прицельно и избирательно по сравнению с классическими химиопрепаратами, и за счет этого более безопасны, но все же обладают некоторыми побочными эффектами.
- Из иммунопрепаратов чаще всего применяют моноклональные антитела, являющиеся ингибиторами контрольных точек — молекул, с помощью которых раковые клетки подавляют работу иммунной системы.
Обычно эти виды лечения применяют на поздних стадиях, когда имеются метастазы. Также на поздних стадиях врачам приходится бороться с таким осложнением рака бронхов и легких, как плеврит. [6,7]
Прогноз выживаемости
Вероятность успешного лечения рака бронхов зависит от многих факторов, но в первую очередь играет роль стадия и тип опухоли. При немелкоклеточном раке легкого, по данным Американского онкологического общества, выживаемость на разных стадиях составляет: [4,5]
- На I стадии — 68-92%.
- На II стадии — 53-60%.
- На III стадии — 13-26%.
- На IV стадии — менее 1%.
Показатели при мелкоклеточном раке легкого:
- На I стадии — 31%.
- На II стадии — 19%.
- На III стадии — 8%.
- На IV стадии — 2%.
На четвертой стадии прогноз зависит от того, где находятся метастазы. Например, если при немелкоклеточном раке вторичные очаги находятся в надпочечниках, прогноз лучше, чем в ситуациях, когда они локализуются в печени или в головном мозге. При мелкоклеточном раке прогноз менее благоприятный, если метастазы находятся в головном мозге, и более благоприятный, если они локализуются в костях или средостении. [3,9]
Имеет значение пол (у женщин прогноз обычно лучше), степень потери веса (плохо, если больной потерял более 5% от первоначальной массы), снижения работоспособности, наличие у опухоли бронхов тех или иных молекулярно-генетических характеристик (если в клетках есть молекулы-мишени, они будут реагировать на лечение таргетными препаратами). [7]
В «Евроонко» применяются наиболее современные методы лечения бронхопульмонального рака. Мы уверены, что помочь можно любому пациенту, даже при четвертой стадии рака. Если не удается добиться ремиссии, как правило, можно продлить жизнь, купировать боли и другие мучительные симптомы. Свяжитесь с нами, чтобы узнать больше.
Рентгенодиагностика рака легкого
Рак легкого (бронхогенная карцинома) стал одним из самых грозных заболеваний человека в последние годы. По своей частоте в промышленно развитых странах он уступает только злокачественным заболеваниям желудка.
Рак легкого (бронхогенная карцинома) стал одним из самых грозных заболеваний человека в последние годы. По своей частоте в промышленно развитых странах он уступает только злокачественным заболеваниям желудка. Удельный вес рака легкого среди онкологических заболеваний в России составляет около 15,0%. При этом у мужчин это самая распространенная локализация рака. В 35 индустриальных странах мира бронхогенная карцинома является главной причиной смерти среди онкологических больных.
Наиболее часто рак легкого выявляется на седьмой декаде жизни, при этом мужчины страдают в пять раз чаще.
В соответствии с общепринятой в России клинико-анатомической классификацией рака легкого различают следующие формы рака.
- Центральный: а) эндобронхиальный; б) перибронхиальный узловой; в) разветвленный.
- Периферический: а) круглая тень; б) пневмониеподобный; в) верхушки легкого (Панкоста).
- Атипичные формы: а) медиастинальная; б) милиарный карциноматоз.
В 1981 году была опубликована Международная гистологическая классификация опухолей легкого. Выделяют плоскоклеточный, мелкоклеточный рак, аденокарциному, крупноклеточный, железисто-плоскоклеточный рак, карциноидную опухоль, рак бронхиальных желез и прочие формы.
Наиболее часто встречается плоскоклеточный рак — по результатам различных исследований до 50 — 75%, при этом с возрастом его доля возрастает до 78%. Мужчины болеют плоскоклеточным раком почти в девять раз чаще женщин.
Как и другие виды опухолей, рак легкого все чаще стал выявляться в молодом возрасте. Это происходит прежде всего за счет увеличения доли аденокарциномы.
Среди основных лучевых методов исследования для выявления рака легких используются флюорография, рентгенография органов грудной клетки, рентгеновская компьютерная томография и реже магнитно-резонансная томография. Дополнительно могут применяться рентгеноскопия, бронхография, ангиография, диагностический пневмоторакс.
Широкомасштабное распространение в России получила флюорография органов грудной клетки. Эта методика была оптимальной в период повсеместного внедрения массовой диспансеризации населения страны. Однако необходимо признать главный ее недостаток: невысокий уровень чувствительности и точности. Опыт показывает, что доля ложноположительных и ложноотрицательных заключений достигает 30%. Кроме того, неоправданно высока лучевая нагрузка на пациентов и медицинский персонал. Поглощенная доза при флюорографии составляет более 0,25 мЗв.
Лучшей разрешающей способностью и меньшей лучевой нагрузкой (0,05 мЗв) обладает рентгенография органов грудной клетки. В клиниках стран Западной Европы и Северной Америки происходит агрессивное внедрение цифровых технологий и беспленочного производства. Дигитальная рентгенография еще более снижает лучевую нагрузку на больного. Однако целесообразность ее использования в пульмонологии до сих пор остается спорной. Доводы сторонников аналоговых изображений имеют свою сильную сторону — разрешающая способность последних в исследовании легочного рисунка выше.
Цифровые технологии постоянно развиваются. Появление плоскопанельных детекторов (flat panel detector) обещает произвести революцию в рентгенографии. С одной стороны, их разрешающая способность выше привычных аналоговых изображений, с другой — предполагается уменьшение лучевой нагрузки до 75%. Поэтому дигитальная рентгенография должна стать скрининговым исследованием органов грудной клетки в ближайшие десятилетия.
У 60% больных рак легкого имеет центральную локализацию. Известно, что он развивается из эпителия сегментарных бронхов. Затем опухоль растет проксимально, вплоть до главного бронха. Чаще, поражаются III и VI сегменты правого легкого.
Семиотические признаки центрального рака легкого при рентгенографии включают:
- наличие опухолевых масс в области корня легкого;
- гиповентиляция одного или нескольких сегментов легкого;
- признаки клапанной эмфиземы одного или нескольких сегментов легкого;
- ателектаз одного или нескольких сегментов легкого.
Рентгеновская диагностика периферического рака легкого нередко сложна вследствие схожести его семиотических признаков с другими заболеваниями. Проблема заключается не в выявлении образования, а в интерпретации полученных данных. Типичным является одиночное поражение верхней доли легкого. Структура чаще гомогенна, но на самом деле некроз возникает довольно часто. Однако длительное время дренирование бронхом остается нераспознанным. Время удвоения опухоли зависит от гистологической структуры опухоли. Так, при плоскоклеточном раке оно составляет в среднем 140 дней.
Верхушечный рак сопровождается синдромом Панкоста. Для него характерно наличие округлого образования области верхушки легкого, плевральных изменений, деструкции верхних ребер и соответствующих позвонков. Говорить о раке Панкоста можно лишь в случае, когда он имеет истинное бронхогенное происхождение.
Нередким осложнением периферического рака легких является распад опухолевого узла. При псевдокавернозной форме рака наряду с уже перечисленными семиотическими признаками выявляются дополнительные особенности, помогающие отличить его от абсцесса. Полость распада может занимать значительную часть опухолевых масс. При этом полость имеет неровный, фестончатый характер. Клинически отсутствуют признаки абсцесса легкого.
К сожалению, как и в большинстве случаев, рентгенография не позволяет определить гистологическую природу заболевания. Однако существуют некоторые закономерности, которые следует учитывать при анализе изображений. Так, аденокарцинома чаще имеет периферическую локализацию в верхних долях легких и является солитарной. Структура, как правило, неоднородная, дольковая. Контуры неровные, фестончатые.
Плоскоклеточный рак характеризуется в первую очередь локальным утолщением бронхиальных стенок, прикорневым расположением и, следовательно, возникновением ателектазов. Плоскоклеточная карцинома склонна к внутреннему распаду.
Мелкоклеточный рак также чаще бывает центральным. Первичная опухоль рентгенографически выявляется крайне редко. В то же время характерна медиастенальная лимфоаденопатия.
Крупноклеточная карцинома может иметь любую локализацию. При этом у 70% больных опухолевые массы при первичном выявлении уже превышают 4 см в диаметре.
Карциноидная опухоль является нечастой и первично злокачественной. У 80% пациентов она растет эндобронхиально и солитарно на долевом, сегментарном или субсегментарном уровне. В трети случаев дополнительно визуализируются аномалии развития бронхиального дерева.
Рак бронхиальных желез в 85-90% случаев имеет центральную локализацию. При этом он происходит из трахеи или главных бронхов и приводит к их сужению.
Вторым обязательным этапом обследования больных с подозрением на рак легкого должна быть рентгеновская компьютерная томография (РКТ). Сегодня компьютерная томография прочно и бесспорно заняла свое место среди рутинных обследований таких больных во многих клиниках России. Это объясняется высокой чувствительностью методики. Несмотря на невозможность гистологической верификации опухоли, специфичность РКТ также выше, чем у рентгенографии, и достигает 70%.
Стандартный протокол КТ-исследования включает последовательное сканирование с толщиной среза и шагом подачи стола 10 мм. При необходимости пространственное разрешение может быть улучшено использованием «срезов» толщиной 2 мм в конкретной зоне интереса. Так, это требуется для подтверждения наличия кальцинатов. Сканы толщиной в 5 мм оптимальны в исследовании корней легких для определения лимфоаденопатии и изучения узла центрального рака легкого.
Исследование может проводиться в режимах как шаговой, так и спиральной РКТ. Преимуществами второй методики в исследовании легких являются:
- возможность исследования всей зоны интереса при одно-двукратных задержках дыхания;
- исключение фактора различной глубины вдоха при исследовании, что повышает чувствительность метода.
Внутривенное контрастирование йодсодержащими препаратами (омнипак, ультравист) при проведении шаговой томографии используется не часто. Накопление контрастного вещества в ткани опухоли, как правило, не дает дополнительной диагностически значимой информации.
Иначе дело обстоит при спиральной РКТ. Принципиально новая возможность болюсного контрастирования позволяет проводить исследование на 25-30 секундах введения препарата. При этом в кубитальную вену вводится 50-60 мл препарата со скоростью 2 мл/с. Значительно улучшается идентификация сосудистых структур, их топографо-анатомическое взаимоотношение с неопластическими массами. Тем самым определяется вовлеченность в процесс сосудов корня легкого и средостения.
Анализ томограмм производится в двух режимах: средостенном и легочном. В первом случае детально изучаются мягкотканые структуры при ширине окна от 0 до 1000 HU и центре окна 50 HU. Во втором — предметом исследования является воздушная легочная ткань с шириной окна от 1500 до 500 HU и центре окна — 650 HU. В норме денситометрические показатели легочной ткани составляют около 760 HU. При этом в нижних отделах они несколько выше (на 80 — 100 HU), что объясняется гравитационным влиянием на размещение крови в сосудистом русле.
Наиболее радикальным способом лечения рака легкого остается хирургический. Компьютерная томография позволяет уточнить риск и оправданность оперативного вмешательства, оценить возможность осложнений, определить прогноз лечения больного.
При обследовании больного с раком легкого рентгеновская компьютерная томография преследует следующие задачи:
- уточнить наличие и солитарность образования, выявить возможные метастазы;
- изучить размеры, структуру, плотность (количественно в HU) и контуры опухоли;
- определить взаимоотношение неопластических масс с окружающими морфологическими структурами корня легкого и средостения;
- уточнить возможное происхождение опухоли;
- изучить изменения легочной ткани;
- выявить поражение лимфатических узлов средостения.
Обычно центральный рак характеризуется полиморфным строением, гомогенной структурой и плотностью от 40 до 70 HU. Очаги распада, как правило, появляются при значительных размерах опухоли.
Детальный анализ последовательных сканов помогает в определении локализации обструкции бронха.
С точки зрения резектабельности важным является взаимоотношение опухоли с окружающими морфологическими структурами. Велика вероятность вовлечения в неопластический процесс органов средостения, сосудов, плевры, грудной стенки. Хорошим естественным контрастным фоном является жировая клетчатка плотностью от 90 до 80 HU.
Менее информативна компьютерная томография при развитии ателектаза. Только у 20-25 % больных удается четко дифференцировать границы опухоли на фоне плотного ателектаза. Денситометрические показатели участков ателектаза варьируют от -10 до 40 HU.
Осложнением центрального рака легкого может быть выпотной плеврит, выраженность которого зависит от степени поражения плевры. Компьютерная томография выявляет минимальное, 10-15 мл, количество жидкости в полости плевры (рис. 3).
Рентгеновская компьютерная томография более чувствительна в выявлении инфильтративной формы рака, верхушечного рака, а также распада опухоли (рис. 5, 6, 7).
Рак легкого: главное, что нужно знать
Несмотря на широкую осведомленность населения о ключевых факторах риска развития рака легкого, распространенность данной патологии продолжает неуклонно расти.
Злокачественные опухоли легочной системы на протяжении многих лет остаются одной из ведущих причин смерти от онкологических заболеваний. Ежегодная смертность от рака легкого превышает совокупный показатель летальности от неопластических образований простаты, толстой кишки и молочных желез [3-пункт 1.4]. Нередко опухоль развивается бессимптомно и становится “случайной находкой” при рентгенологическом исследовании органов грудной клетки. Поэтому так важно своевременно и в полном объеме проводить скрининговые обследования легких среди населения.
Определение и классификация
Понятие рак легкого включает в себя группу заболеваний злокачественного характера, возникающих в бронхах различного диаметра и анатомических структурах легочной ткани (альвеолы). Классификацию патологии проводят по стандартной системе TNM и гистологическому типу (немелкоклеточный, мелкоклеточный, плоскоклеточный и др.). Важное значение имеют клинико-анатомические формы рака легкого:
- центральный (локализуется в крупных или средних бронхах, растет в просвет органа или вдоль его стенки);
- периферический (образуется из ткани мелких бронхов или альвеол, бывает в виде узла, пневмониеподобный вариант или рак верхушки с синдромом Панкоста).
Иногда встречается синхронный злокачественный процесс в обоих легких [3-пункт 1.2].
Этиология и патогенез
Многочисленные исследования доказывают ведущую роль активного и пассивного курения в развитии злокачественных процессов легочной системы. Именно курильщики, среди которых больше представителей сильного пола, чаще страдают данной патологией: рак легкого является лидером в структуре онкозаболеваемости среди мужского населения планеты.
Во время курения сигареты, человек не только вдыхает дым, содержащий массу канцерогенных веществ, но и обжигает нежную слизистую верхних дыхательных путей, что приводит к гибели реснитчатого эпителия и атрофическим изменениям воздухоносного тракта, и в большинстве случаев данные нарушения практически необратимы. Курильщики чаще болеют респираторными заболеваниями и туберкулезом, что способствует зарождению злокачественных новообразований в структурах бронхиального дерева и легочной ткани. Помимо курения, достоверное влияние на вероятность развития рака легкого оказывает воздействие химических соединений (асбест, бензопирен, никель и его соединения, продукты сгорания угля и т.д.), связанное с определенными видами профессиональной деятельности. Нередко злокачественные опухоли респираторной системы диагностируют у людей, которые в прошлом проходили курс облучения анатомически рядом расположенных органов (молочная или щитовидная железа, пищевод и другие). Любое иное воздействие радиации также считается фактором риска для появления данной патологии.
В некоторых случаях развитию болезни может способствовать наследственный фактор. В ходе ряда исследований были найдены определенные «поломки» ДНК, которые чаще встречались у больных раком легкого, чем у здоровых лиц [4, 3-пункт 1.3].
Клиническая картина
Симптоматика при раке легкого отличается высокой вариабельностью. Она зависит от локализации новообразования, его гистологических особенностей и характера роста (экзофитный, эндофитный или смешанный). Периферический рак легкого, как правило, длительно протекает бессимптомно, пока опухоль не достигнет большого размера. Образования, расположенные в крупнокалиберных бронхах, растущие в просвет органа, рано «заявляют» о себе, становясь преградой для потока воздуха.
Ранними симптомами, связанными с наличием самой опухоли, являются:
- кашель различного характера и интенсивности
- наличие крови в мокроте;
- одышка;
- боль в грудной клетке;
- проявления общей интоксикации организма.
При наличии метастатических очагов в регионарных лимфоузлах и/или прорастании опухоли в нервно-сосудистые пучки, пациента могут беспокоить следующие жалобы:
- осиплость голоса;
- отечность лица;
- синдром Бернара-Горнера (миоз, птоз, энофтальм);
- лихорадка;
- ломота и боль в костях и мышцах;
- синдром Мари-Бамбергера (припухлость и болезненность в суставах; утолщение и склероз трубчатых костей рук и ног, пальцы в виде «барабанных палочек»).
У ряда пациентов наблюдаются гормональные и обменные нарушения в организме. Нередко появляются признаки дерматоза или тромбофлебита.
Отдаленные очаги болезни проявляются соответствующей клинической картиной. Например, при метастатическом поражении головного мозга пациент может испытывать головные боли, головокружения, тошноту и типичные неврологические симптомы [2-стр.4, 3-пункт 2].
Диагностика
Главным исследованием в первичной диагностике рака легкого считается рентгенологический метод. В настоящее время предпочтение отдается мультиспиральной компьютерной томографии органов грудной клетки с контрастированием. Флюорография не всегда позволяет увидеть небольшие образования (менее 10 мм), поэтому не может считаться оптимальным скрининговым диагностическим методом.
В стандарт обследования пациента обязательно входит тщательный физикальный осмотр (перкуссия, пальпация и аускультация легких, оценка состояния регионарных зон лимфатического оттока, общий статус больного). Врач собирает подробный анамнез, чтобы выявить факторы риска в каждом конкретном случае. Проводится комплексная лабораторная диагностика.
Для верификации диагноза обычно назначается фибробронхоскопия (ФБС) с биопсией. При периферических образованиях может быть проведена диагностическая торакотомия со взятием материала непосредственно из патологического очага. Иногда диагноз подтверждается только после удаления опухоли и ее гистологического изучения. В последние годы все чаще применяется флюоресцентная эндоскопия, позволяющая выявить микроскопические очаги болезни.
Все измененные лимфоузлы подлежат обязательной пункционной биопсии. При наличии плеврита, производится забор жидкости из плевральной полости для определения в ней наличия атипичных клеток. Для исключения метастазов назначаются дополнительные диагностические мероприятия (УЗИ органов брюшной полости и забрюшинного пространства, МРТ головного мозга с контрастированием и др.). Наиболее информативным исследованием считается ПЭТ-КТ.
Для первичной диагностики и последующего мониторинга широко используется анализ крови на онкомаркеры (РЭА, CYFRA 21-1, HCE, SCC, СА-125). У ряда пациентов выявляются наследственные мутации гена EGFR (участки 19 и 21) и транслокации ROS1, ALK. Генетическое тестирование позволяет подобрать оптимальный таргетный препарат для лекарственной терапии рака легкого [1, 3-пункт 2].
Лечение
Каждый пациент с диагнозом рак легкого обсуждается на врачебном консилиуме. С учетом всех имеющихся данных (возраст и соматическое состояние больного, распространенность процесса, гистотип опухоли), подбирается наиболее эффективный вариант лечения. Радикальным методом борьбы с болезнью является операция. К сожалению, полностью удалить злокачественное новообразование получается лишь у 10-20% пациентов.
В большинстве случаев в терапии рака легкого применяется комплексный подход, который включает в себя несколько видов лечения (химиотерапия, таргетные препараты, иммунотерапия, облучение, хирургическое вмешательство), каждый из которых может использоваться самостоятельно. Тактика во многом определяется морфологическим вариантом опухоли (мелкоклеточный или немелкоклеточный).
В запущенных случаях или у пациентов с тяжелой сопутствующей патологией назначается симптоматическая терапия. Последняя включает в себя адекватное обезболивание по стандарту ВОЗ, восстановление нормальных показателей крови (гемоглобин и другие), борьбу с наиболее значимыми проявлениями болезни [2, 3-пункт 3].
Профилактика рака легкого
Значительно уменьшить риск развития злокачественной опухоли в бронхолегочной системе позволяет отказ от курения. Также необходимо избегать пассивного вдыхания сигаретного дыма и длительного контакта с канцерогенными летучими веществами, например, бензопиреном. Людям, у которых кровные родственники страдали раком легкого, следует пройти тестирование на присутствие генетических поломок. В целях профилактики патологии рекомендуется укреплять иммунную систему, вести здоровый образ жизни и потреблять больше свежих овощей и фруктов (морковь, грейпфрут, брокколи и т.д.). Ежегодно следует проходить контрольное рентгенологическое обследование органов грудной клетки [4].
Источники
- Усачев В.С., Смоленов Е.И., Рагулин Ю.А. Морфологическая и молекулярно-генетическая диагностика рака легкого: методики и проблемы // Исследования и практика в медицине. 2020. Т. 7 (3). С. 51-62.
- Трахтенберг А.Х., Колбанов К.И. Рак легкого // Пульмонология и аллергология. 2008. №4. C. 3-8.
- Клинические рекомендации Министерства здравоохранения Российской Федерации: Рак легкого. 2018.
- Мукерия А.Ф., Заридзе Д.Г. Эпидемиология и профилактика рака легкого // Вестник РОНЦ им. Н.Н. Блохина РАМН. 2010. Т. 21 (3). C. 3-11.
Автор: Эмилия Киселева, врач-онколог, г. Барнаул
Редактор: Ирина Буянова
Дифференциальная диагностика в онкопульмонологии
В медицинской практике важно различить одно заболевания от другого. Для этого необходимо тщательно собрать анамнез жизни и заболевания, определить патогномоничные симптомы, провести лабораторные и инструментальные исследования. Всё это входит в понятие дифференциальной диагностики — разновидности медицинской диагностики, которая подразумевает исключение того или иного заболевания для грамотного и эффективного подбора терапии.
В конечном итоге при грамотном применении дифференциально-диагностических методик, которые предполагают сочетание клинического опыта врача-диагноста и всего спектра наиболее эффективных способов определения нозологии, останется единственный диагноз, что исключает возникновение врачебных ошибок и обеспечивает максимально эффективное поддержание уровня качества жизни больного.
Использование дифференциальной диагностики заболеваний на раннем этапе в конечном итоге даёт максимальный результат. Постановка дифференциального диагноза может проходить в 5 этапов:
- Выделение главного синдрома, который объединяет несколько похожих нозологий. Если таких синдромов больше одного, то из всей совокупности вычленяют наиболее информативный.
- Проведение детального анализа ведущего синдрома (его продолжительность, стадийность, степень проявления). Также нужно охватить полную картину заболевания и учитывать симптомы, которые возникали на всём протяжении болезни.
- Сама дифференциация нозологии. Здесь сравнивается настоящая патология со всем перечнем похожих заболеваний. Для начала рассматривается сходство возникших симптомов с характерными, классическими признаками предполагаемой патологии. Кроме того, анализируют другие симптомы, которые могут склонять выбор в сторону
других нозологий. Это — самый важный этап дифференциальной диагностики. - Анализ полученной информации. К этой фазе врачи подходят творчески и используют всё имеющееся клиническое мышление. Здесь применяются несколько принципов. Например, если у больного предполагается какой-либо синдром, а некоторые симптомы прямо противоположны патогномоничным признакам, значит этот синдром исключается.
- Постановка окончательного диагноза и определение соответствующей тактики лечения.
Способы диагностики в онкологии
Применение методик дифференциальной диагностики имеет особое значение в онкологической практике, так как различные виды рака предполагают уникальные лечебные и диагностические подходы. Для того чтобы определить или исключить наличие злокачественного новообразования, применяют следующие клинические методы:
- Ультразвуковое исследование.
- Рентгенологические методы.
- Компьютерная томография.
- Позитронно-эмиссионная томография.
- Магнитно-резонансная томография.
- Анализ крови на наличие онкомаркёров.
- Гистологическое исследование биоптата.
- Эндоскопические методы.
Эти процедуры позволяют с большой долей вероятности провести дифференциальную диагностику рака не только с другими, неонкологическими, заболеваниями, но и определить точную стадию злокачественного процесса. Особенно важна в этом плане ранняя диагностика опухолей, так как чем раньше начнётся лечение рака, тем более эффективным оно будет.
Диагностика в онкопульмонологии
Актуальной задачей остаётся проведение дифференциальной диагностики первичного рака и пульмонологических заболеваний. Однако нужно помнить, что почти в половине случаев рак лёгких сопровождается как острой, так и хронической пневмонией онкологического генеза, которая маскирует проявления возникшего опухолевого процесса. Одним из главных методов, используемых при дифференциации рака лёгких и других лёгочных заболеваний (и болезней органов грудной клетки вообще), является проведение лучевой диагностики. При данных состояниях широкое применение в медицинской практике нашли крупнокадровая флюорография, прицельная и стандартная рентгенография в двух проекциях. С успехом применяется и компьютерная томография, которая позволяет оценить объём поражения лёгких, структуру патологического очага, его точную локализацию. Методы бронхоскопии и бронхографии могут использоваться при диагностике инородных тел бронхов, папилломах гортани, помогают оценить степень обтурации и оттеснения бронхов опухолью лёгких.
Центральный и периферический рак
Рак лёгких по своему расположению делится на центральный и периферический. Дифференциальное разделение этих двух форм имеет принципиальное значение для выбора хирургического метода лечения. Оба вида рака относятся к злокачественным процессам, развивающимся из эпителия бронхов разного калибра (поэтому их ещё называют бронхогенным раком). Для возникновения центрального рака лёгких в большинстве случаев имеет значение вдыхание канцерогенных веществ, поэтому он чаще является первичным злокачественным новообразованием.
Периферический рак легкого чаще является вторичным, то есть формируется в результате метастазирования других имеющихся в организме опухолей. Для него более характерно наличие сразу нескольких очагов.
Центральный рак лёгких чаще всего развивается в крупных бронхах. Сама опухоль может расти как в сторону просвета бронхов (тогда он называется эндобронхиальным), или кнаружи от него (перибронхиальный). Вначале появляется мучительный сухой кашель, особенно усиливающийся по ночам. Затем постепенно нарастает образование слизистой и слизисто-гнойной мокроты, у половины пациентов уже в ранней стадии возникает кровохарканье. Типичны боли в области грудной клетки, причём они могут быть и на стороне, противоположной поражённой. На рентгенографии можно различить округлую тень узла с характерной «дорожкой» к корню, ателектаз и усиление легочного рисунка в области поражения.
Дифференциальная диагностика периферического рака лёгкого в большинстве случаев требует применения инструментальных исследований, так как симптоматика проявляется не сразу и достаточно размыта. Из рентгенологических признаков периферического рака наиболее информативны лучистость затемнения, его бугристость, неоднородная структура (кальцинаты) и наличие плеврального выпота.

Рак лёгкого и пневмония
Не столь часто, но всё же приходится проводить в клинической практике дифференциальную диагностику периферического рака лёгких и очаговой пневмонии. Для воспалительного процесса лёгочной ткани инфекционного генеза характерны следующие признаки:
- Пневмония чаще встречается у пациентов моложе 50 лет (хотя может возникнуть в любом возрасте).
- Нет особых различий по полу пациентов (при раке — больше мужчины-курильщики).
- Начало болезни в большинстве случаев острое, с фебрильной лихорадкой.
- Одышка может отсутствовать, но при обширных поражениях лёгочной ткани появляется почти всегда (при онкологии — в далеко запущенных случаях).
- Боли могут возникать при вовлечении плевры.
- Ярко выраженные изменения в результате применения физикальных методов диагностики. Особенно изменяется дыхание, сначала оно становится жёсткое, затем появляются сухие и влажные хрипы.
- При проведении общего анализа крови можно выявить характерные признаки воспаления (рак в данном случае может характеризоваться высоким СОЭ при нормальном содержании лейкоцитов).
- На рентгенологическом снимке видны очаги воспаления гомогенной плотности, чаще — в нижних долях, с расплывчатыми границами, с усилением легочного рисунка и увеличением корней лёгкого.
Рак лёгкого и туберкулёз
Если пневмония исключена, обычно необходимо выполнить дифференциальную диагностику между раком лёгких и туберкулёзом. Схожесть симптоматики характерна для инфильтративного туберкулёза и периферического рака.
При туберкулёзе нередко можно выявить прямой контакт пациента с подтверждённым носителем микобактерий. Температура тела бывает повышенной в вечерние и ночные часы, вплоть до субфебрильной и фебрильной (в отличие от рака, при котором чаще всего температура не поднимается выше субфебрилитета). При онкологическом процессе чаще отмечается локализованный сухой кашель.
Течение туберкулёза обычно полисимптомно, но признаки выражены слабо, а при онкологическом процессе, как правило, можно явно выявить 1-2 основных симптома. При анализе мокроты патогномоничным признаком будет обнаружение возбудителей туберкулёза, а при раке — атипичных клеток (в большинстве случаев). Также специфический результат дадут подкожные туберкулиновые пробы, которые при инфицировании микобактериями дают положительный результат, а при злокачественных опухолях лёгкого — отрицательный.
Рентгенологически при туберкулёзной инфильтрации можно увидеть полисегментарные затемнения округлой или облаковидной формы, участки бронхогенного обсеменения в удалённых областях лёгкого или в другом лёгком. При ателектазе (который часто встречается при центральной форме рака) выявляется культя бронха, на фоне затемнения не видно светлых полосок бронхиального дерева (в отличие от туберкулёза).
Если сравнивать кавернозную форму туберкулёза с полостными образованиями при раке, то поначалу рентгенологически их отличить тяжело — в обоих случаях каверна имеет толстые неровные стенки с перифокальным воспалением и инфильтрацией, с наличием внутри жидкости. После отторжения некротических масс, стенки туберкулёзной каверны становятся более тонкими и ровными, само затемнение — округлое (ближе к правильной форме), а инфильтрация вокруг образования уменьшается.
Сложности могут возникнуть при дифференциальной диагностике узловой формы периферического рака и туберкуломы. Последняя имеет более чёткие округлые контуры, а рак имеет специфическую лучистость. Для туберкуломы характерны участки обызвествления и кальцификаты.
В любом случае, для дифференциального диагноза рака лёгких и туберкулёза чаще всего решающее значение имеют результаты биопсии.
Рак лёгкого и инородное тело в бронхах
Во многих случаях аспирация инородного тела в бронх проходит для взрослых незаметно. В таких ситуациях больные могут долго и безуспешно лечиться по поводу рака бронхов или лёгких. После попадания инородного тела, в большинстве случаев возникает судорожный кашель, который может пройти. Фруктовые косточки, семечки, кусочки пластмасс при нахождении в бронхах покрываются грануляцией, которая вызывает хронический воспалительный процесс. Вялотекущее воспаление в данном случае сопровождается периодическим подъёмом температуры, кашлем, сопровождающимся выделением слизистой или слизисто-гнойной мокротой, небольшой одышкой и болью в груди без чёткой локализации.
На рентгенограмме довольно чётко определяется металлическое инородное тело. В противном случае можно лишь различить неясное затемнение поражённого бронха и участок воспаления вокруг него. Поможет дифференцировать инородное тело от рака компьютерная томография, особенно если обтурирован крупный сегмент бронха. В таком случае ставится диагноз обструктивного пневмонита и рассматриваются тактики извлечения инородного тела с минимизацией ущерба для слизистой оболочки бронха.
Можно легко спутать с центральным раком лёгкого эндогенный бронхолит, который представляет собой кальцинированную часть лимфатического узла, попавшего в просвет бронха в результате бронхожелезистой перфорации. При наличии бронхолита пациенты предъявляют примерно такие же жалобы, как и при центральном раке. Дифференцировать данные состояния поможет томография, выполненная в двух проекциях.
Диагностическую ценность имеет и проведение бронхоскопии. Если бронхолит крупный, находится в просвете бронхов или частично расположен в стенке, то можно визуализировать и удалить эндогенное инородное тело. Однако если бронхолит образовался много лет назад, и полностью скрыт грануляционой тканью, то его удаление возможно только при разрушении плотной фиброзной оболочки, покрывающей его. Это чревато сильным кровотечением, так как при хирургических манипуляциях есть вероятность повредить относительно крупные бронхиальные сосуды, проходящие прямо в соединительнотканной оболочке.
При случайном обнаружении затемнения и сомнениях в выборе диагноза между центральным раком и бронхолитом имеет смысл провести бронхоскопию с биопсией. Если онкологический диагноз не подтвердился, то при отсутствии жалоб со стороны пациента можно оставить бронхолит и по необходимости проводить противовоспалительную терапию.

Рак лёгкого и сифилис
Легочное сифилитическое поражение встречается в крайне редких случаях, причём период от манифестации заболевания и появления такого осложнения может составлять 8 лет и больше. При наличии солитарной крупной сифилитической гуммы в лёгочной ткани приходится дифференцировать её с раком лёгкого.
Симптоматика болезни часто не соответствует степени поражения лёгких при сифилисе — относительно нормальное общее самочувствие может сочетаться с резко выраженной одышкой. Течение болезни длительное, часто малосимптомное. При сифилисе лёгких будут отсутствовать малые признаки рака, которые часто бывают дополнительным критерием постановки онкологического диагноза. Также следует брать во внимание длительный сифилитический анамнез, особенно если за всё время лечение было нерегулярным и неадекватным.
Сифилитические гуммы небольшого размера (милиарные, от горошины до лесного ореха), локализуются большей частью в средней и нижней долях лёгкого. Образования могут быть негомогенной структуры, распадаться с образованием каверн. Решающее значение в дифференциальной диагностике будут иметь результаты серологических исследований на сифилис и эффект таргетированного лечения препаратами йода и висмута, а также бициллинотерапии.
Рак лёгкого и метастазы
Нередко приходится различать первичные злокачественные новообразования и метастатическое поражение. На рентгенограмме обычно кардинальных различий нет, поэтому приходится опираться на клинические проявления и результаты других видов исследований.
При метастатическом поражении результаты биопсии показывают наличие атипичных клеток внелегочного генеза (рак лёгких образуется из бронхиального эпителия). Для первичного рака лёгких характерны изменения лёгочной ткани (рубцы, дисплазия, carcinoma in situ), а метастазы возникают в первоначально неизменённой паренхиме.
Поражение близлежащих регионарных лимфоузлов может быть характерным признаком рака лёгких. Метастатические очаги обычно локализуются в паренхиме, так как заносятся они лимфогенным, гематогенным или контактным путём (в этом случае они отличаются от центральной формы рака, но схожи с периферической).
Метастазы в лёгких сопровождаются паранеопластическим синдромом, который характерен для наличия опухолей в других органах. То же самое касается и онкомаркёров — при первичном раке лёгких в крови можно обнаружить специфические СА-125, CYFRA 21-1, а метастазы проявляются наличием ПСА, тиреоглобулина, СА 15-3 и других онкомаркёров (в зависимости от локализации первичного очага). После удаления метастазов хирургическим методом, эффект обычно минимальный — процесс быстро генерализируется, а при первичной онкологии лёгких генерализация происходит реже и медленнее. Метастатическое поражение лёгких, в отличие от первично возникшего рака, редко вовлекает в болезненный процесс висцеральную плевру и бронхи крупного диаметра.
Рак лёгких и саркоидоз
Саркоидоз характеризуется появлением специфических гранулём во внутренних органах и лимфатических узлах. Очень часто саркоидоз локализуется во внутригрудных лимфатических узлах и паренхиме лёгких. Клинически заболевание сначала протекает почти бессимптомно и может быть обнаружено при случайном рентгенологическом обследовании. С прогрессированием болезни появляются похожие на рак симптомы: сухой кашель, нарастающая одышка, боль в груди, общие признаки в виде утомляемости, повышения температуры, слабости, снижения аппетита. При физикальном обследовании можно обнаружить жёсткое дыхание и сухие хрипы.
Рентгенологическую картину саркоидоза тоже можно спутать с признаками рака лёгких: очаговоподобные затемнения на лёгочной ткани, инфильтрация (часто диффузная), увеличение близлежащих лимфоузлов, усиление и искажение легочного рисунка.
Однако для саркоидоза существует несколько патогномоничных признаков, выделяемых из всех рентгенологических проявлений:
- Симптом «матового стекла» — неравномерное участки затемнения и просветления на всей поверхности легочной ткани.
- Кальцинация лимфатических узлов по типу «ореховой скорлупы».
- Симптом диссеминации: множество рассеянных мелкоочаговых теней размерами от милиарных до 0,7 см, локализованные большей частью в области примыкания лёгких к плевре и в аксиллярной зоне.
Кроме того, дифференциацию поможет провести биопсия узлов — при саркоидозе обнаруживаются гигантские клетки Пирогова-Лангханса, а при опухолевом процессе — признаки атипии.
Врачи «Евроонко» ежедневно сталкиваются с необходимостью проведения дифференциальной диагностики заболеваний легкого. Благодаря узкой специализации и большому опыту работы, нам в каждом случае удается поставить верный диагноз и определить адекватную лечебную тактику.
БРОНХОЭКТАТИЧЕСКАЯ БОЛЕЗНЬ
Бронхоэктазы — это сегментарные расширения просветов бронхов, обусловленные деструкцией или нарушением нервно-мышечного тонуса их стенок вследствие воспаления, дистрофии, склероза или гипоплазии структурных элементов бронхов (И. К. Есипова, 1976). Важно
Бронхоэктазы — это сегментарные расширения просветов бронхов, обусловленные деструкцией или нарушением нервно-мышечного тонуса их стенок вследствие воспаления, дистрофии, склероза или гипоплазии структурных элементов бронхов (И. К. Есипова, 1976).
Важно разграничивать бронхоэктатическую болезнь и вторичные бронхоэктазы вследствие абсцесса легкого, туберкулезной каверны, пневмонии, инородных тел, бронхита. Наиболее обоснованным можно считать взгляд на бронхоэктатическую болезнь как на регионарное расширение бронхов обычно IV—VI порядков, превышающее просвет нормального в 2 раза и более, возникающее, как правило, в возрасте от 3 до 18 лет и проявляющееся хроническим, преимущественно эндобронхиальным нагноением.
В первые десятилетия ХХ в. было распространено мнение о преимущественно врожденной природе бронхоэктазов (F. Sauerbruch, 1927). Однако впоследствии было доказано (А. И. Струков, И. М. Кодолова, 1970), что в большинстве случаев отмечается постнатальное нарушение дифференцировки бронхиального дерева под влиянием бронхолегочной инфекции, после перенесенных в раннем детском возрасте кори, коклюша, гриппа, острых пневмоний. Подтверждением тому послужил факт расположения бронхоэктазов в тех же сегментах, что при острых пневмониях у детей.
Установлена последовательность патологического процесса — от катарального бронхита к панбронхиту, далее к перибронхиту с перибронхиальной пневмонией, затем — к деформирующему бронхиту с разрушением эластических и мышечных волокон и, наконец, к бронхоэктазам.
На основании классификации В. Р. Ермолаева (1965) различают следующие стадии заболевания: 1) легкую; 2) выраженную; 3) тяжелую; 4) осложненную. По распространенности процесса выделяют одно- и двусторонние бронхоэктазии с указанием точной локализации по сегментам. В зависимости от состояния больного, в момент обследования должна указываться фаза процесса: обострения или ремиссии. В зависимости от формы расширения бронхов, различают бронхоэктазии: а) цилиндрические; б) мешотчатые; в) веретенообразные; г) смешанные. Между ними существует много переходных форм. Кроме того, бронхоэктазии делят на ателектатические и не связанные с ателектазом, что, несомненно, удобно в практическом отношении.
Основным симптомом бронхоэктатической болезни является кашель с выделением мокроты, наиболее выраженный в утренние часы. При цилиндрических бронхоэктазах мокрота обычно отходит без затруднений, тогда как при мешотчатых и веретенообразных — нередко с трудом. При сухих бронхоэктазах, описанных С. А. Рейнбергом (1924), кашель и мокрота отсутствуют (эти бронхоэктазы проявляются лишь кровотечением, иногда угрожающим).
В период ремиссии количество слизисто-гнойной мокроты не превышает в среднем 30 мл/сут. При обострении заболевания в связи с острыми респираторными инфекциями или после переохлаждения кашель усиливается, количество мокроты увеличивается до 300 мл/сут и более, иногда достигая 1 л, она приобретает гнойный характер. Гнилостный запах мокроты не характерен для бронхоэктатической болезни и появляется лишь при абсцедировании.
Кровохарканье, по данным различных авторов, встречается у 25—34% больных. Чаще всего отмечаются прожилки крови в мокроте, но иногда возникает профузное легочное кровотечение. Считают, что источником кровохарканья и кровотечения становятся бронхиальные артерии (особенно артерии среднедолевого бронха). Кровохарканье наблюдается главным образом весной и осенью, что связывают с обострением воспалительного процесса (Д. Д. Яблоков, 1971). Обильные кровотечения могут начаться после тяжелой физической нагрузки или перегрева (А. Я. Цигельник, 1968).
Одышка и синдром бронхиальной обструкции отмечаются у 40% больных. Эти симптомы обусловлены сопутствующим хроническим обструктивным бронхитом, предшествующим образованию бронхоэктазов или возникающим вследствие нагноившихся первичных бронхоэктазов (Ю. В. Маликов и соавт., 1979). Боли в грудной клетке на стороне поражения отмечаются обычно при обострении заболевания, развитии перифокальной пневмонии и парапневмонического плеврита.
В период обострения и при тяжелом течении заболевания состояние больных значительно ухудшается. Наряду с увеличением количества гнойной мокроты, появляются признаки интоксикации: продолжительное повышение температуры тела (обычно до 38°С), потливость, слабость, недомогание. Нередко эти симптомы обусловлены перифокальной пневмонией.
При длительном течении бронхоэктатической болезни нередко наблюдаются изменения концевых фаланг пальцев рук — форма «барабанных палочек» и ногтей — форма «часовых стекол». Грудная клетка может быть деформирована вследствие пневмофиброза и эмфиземы легких.
Несмотря на яркую клиническую картину бронхоэктатической болезни, диагностировать ее удается, как правило, через много лет от начала заболевания. Больных продолжительное время лечат по поводу туберкулезной интоксикации, туберкулезного бронхоаденита и туберкулеза легких, хронической пневмонии, хронического бронхита.
Стандартное рентгенологическое исследование, дополненное иногда бронхографией, позволяет поставить правильный диагноз. В отличие от хронического бронхита, бронхоэктазы в значительной части случаев видны на обзорных рентгенограммах и томограммах. Наиболее часто бронхоэктазы встречаются в нижней доле слева и в средней доле справа.
При поражении нижней доли слева возникает характерная рентгенологическая картина (М. Г. Виннер и соавт., 1969): смещение левого корня книзу; разрежение легочного рисунка из-за вздувшейся верхней доли (компенсаторное вздутие); смещение сердца влево, сужение нижнего легочного поля; смещение книзу и кзади главной междолевой щели, что лучше видно на боковых рентгенограммах и томограммах; затемнение и уменьшение размеров самой нижней доли. При этом срединная тень сердца приобретает двойные контуры: латерально проецируется контур тени сердца, а медиально — контур уменьшенной нижней доли. Величина треугольной тени нижней доли зависит от степени ее спадения. Пятнисто-тяжистое затемнение у верхушки левого желудочка свидетельствует о наличии воспалительного процесса в нижней доле слева и язычке. При резко уменьшенной нижней доле, которая в таких случаях прячется за тенью сердца, эти патологические тени образуются воспалительным процессом в язычке. При изолированном поражении нижней доли или нижней зоны и их резком спадении, когда изображение пораженного отдела полностью располагается за тенью сердца, этих патологических изменений не видно. Также характерно затемнение в области заднего реберно-диафрагмального синуса, что видно на боковых томограммах и рентгенограммах. Этот признак является одним из самых постоянных и часто встречающихся.
При бронхографии обнаруживается, что бронхи нижней зоны или доли расширены и сближены между собой. Бронхи язычка и остальных сегментов верхней доли смещены и раздвинуты. При вовлечении в воспалительный процесс язычковых бронхов они также цилиндрически расширены и сближены между собой и с бронхами нижней доли. Бронхи верхней зоны веерообразно раздвинуты.
При поражении средней доли на обзорных рентгенограммах отчетливо определяются лишь кистовидные бронхоэктазы; другие формы отображаются в виде более или менее выраженного усиления и деформации легочного рисунка.
На томограммах в боковой или косой проекции пораженная доля бывает неоднородно затемнена, в ней наблюдаются множественные, округлые или линейные просветления, являющиеся отображением просвета расширенных бронхов в продольном, поперечном и косом сечениях.
На томограммах мешотчатые и кистовидные бронхоэктазы верхней доли отображаются в виде множественных округлых и овальных полостей с более или менее тонкими стенками, которые располагаются своей длинной осью по ходу соответствующих бронхов. В части случаев их контуры нечеткие, что обусловлено склеротическими изменениями. Иногда кистовидные бронхоэктазы сочетаются с воздушными бронхиальными кистами. Томографическая картина у них неотличима. Ценным методом, делающим возможным их распознавание, является бронхография. В отличие от воздушных бронхиальных кист, кистовидные и мешотчатые бронхоэктазы хорошо контрастируются.
При бронхоэктатической болезни важно определить истинный объем поражения, особенно при намечающейся операции. При этом бронхография обязательно должна быть двусторонней. У взрослых пациентов сделать это лучше последовательно, а у детей — одновременно, под общим обезболиванием.
Мешотчатые бронхоэктазы на бронхограммах видны в виде слепо заканчивающихся, резко расширенных бронхов IV—VI порядков, сближенных между собой и лишенных боковых ветвей (рис. 1).
Часто встречаются смешанные бронхоэктазы, когда обнаруживаются цилиндрические и мешотчатые деформации. Расположенные в верхних долях кистовидные бронхоэктазы нередко имеют туберкулезный генез и возникают в результате посттуберкулезного сужения бронха.
Бронхография, особенно в сочетании с кинематографией, позволяет выявить функциональные изменения бронхов. Нередко при этом наблюдаются парадоксальные картины: при небольших цилиндрических бронхоэктазах в части случаев видна потеря дренажной функции бронхов и, наоборот, мешотчатые полости хорошо опорожняются (Л. С. Розенштраух и соавт., 1987). Кроме того, отмечаются ригидность бронхиальных стенок, изменение углов деления и другие функциональные признаки, встречающиеся и при хроническом деформирующем бронхите, но резче выраженные.
Во время бронхоскопического исследования бронхоэктазы не видны. Бронхоскопия позволяет оценить протяженность бронхита, степень интенсивности воспаления слизистой оболочки бронхов в зависимости от стадии обострения или ремиссии бронхоэктатической болезни.
Во время бронхоскопии можно заподозрить наличие бронхоэктазов на основании признака Суля, который указывает на дистальное расширение бронхов: появление опалесцирующих пузырьков воздуха в окружности заполненных гноем устьев (рис. 2).
Для бронхоэктатической болезни в стадии ремиссии характерен частично диффузный (верхнедолевой бронх и его более мелкие ветви интактны) или строго ограниченный одно- или двусторонний бронхит I степени интенсивности воспаления (слизистая оболочка бронхов умеренно гиперемирована, отечна, секрет слизистый, жидкий или вязкий, в большом количестве).
Бронхоэктатическая болезнь в стадии обострения проявляется частично диффузным или строго ограниченным одно- или двусторонним бронхитом III степени интенсивности воспаления (слизистая оболочка бронхов ярко гиперемирована, отечна, устья сегментарных бронхов сужены до точечных, секрет гнойный, вязкий или жидкий, в очень большом количестве).
Наличие бронхоэктазов следует заподозрить на основании анамнестических сведений (кашель с выделением мокроты с детства, частые пневмонии) и выявления стойко сохраняющихся влажных хрипов в период ремиссии болезни. Однако аналогичные симптомы могут быть вызваны распространенным гнойным бронхитом или хронической пневмонией. Дифференциальная диагностика кистозных бронхоэктазов (кистозная гипоплазия) с приобретенными (мешотчатыми) бронхоэктазами, развивающимися обычно в детском возрасте, затруднительна. Обычно выделяют 3 основные группы признаков (клинико-анамнестические, рентгенологические и патоморфологические), по которым можно дифференцировать кистозную гипоплазию от сходных с нею приобретенных бронхоэктазов (Ю. Н. Левашов и соавт., 1975). О наличии ателектатических бронхоэктазов можно думать при сужении межреберных промежутков, понижении прозрачности пораженной части легкого, изменении уровня стояния диафрагмы, смещения средостения, изменения топографии междолевых щелей (Д. Л. Бронштейн, 1975). Бесспорные доказательства существования бронхоэктазов представляет, однако, лишь бронхография. При возникновении кровохарканья необходимо исключить прежде всего туберкулезный процесс, абсцесс легкого и рак бронха.
При ограниченных в пределах отдельных сегментов или даже долей бронхоэктазах без выраженного хронического обструктивного бронхита показано хирургическое лечение. Резекция легкого позволяет устранить очаг хронической инфекции, что, в свою очередь, способствует стиханию или полному разрешению хронического бронхита. Значительное улучшение состояния или выздоровление констатируют после резекции легкого у 97% больных (I. Deslauriers и соавт., 1985). Оперативное вмешательство противопоказано при хроническом обструктивном бронхите с эмфиземой легких, выраженной дыхательной и сердечной недостаточностью. Рецидивы бронхоэктазов возникают, по данным S. A. Adebonojo, O. Osinowo (1979), у 20% оперированных.
Достаточно интенсивное и своевременно начатое (особенно у детей) консервативное лечение позволяет добиться длительной ремиссии.
Методы санации бронхиального дерева принято делить на пассивные (постуральный дренаж с применением отхаркивающих средств) и активные (санационная бронхоскопия).
Обязательным считают позиционный дренаж в строгом соответствии с локализацией бронхоэктазов. При базальных бронхоэктазах секрет из бронхов удаляют путем перевешивания туловища через край кровати или значительного поднятия нижнего конца кровати. При локализации бронхоэктазов в IV и V сегментах — лежа на спине с опущенным головным концом кровати и с подложенной под больной бок подушкой.
Постуральный дренаж больным бронхоэктатической болезнью обязательно проводят по крайней мере 2 раза в день (утром после сна и вечером перед сном). При обострении болезни дренаж следует использовать многократно. Выделение мокроты значительно возрастает при сочетании перкуссии грудной клетки с постуральным дренажом. Эффект постурального дренажа может быть усилен назначением отхаркивающих средств и муколитических препаратов.
Решающее значение, однако, имеют активные методы санации бронхиального дерева. Наиболее эффективны санационные бронхоскопии.
Важное место занимает антибактериальная терапия (обязательно после бактериологического исследования с идентификацией возбудителя). Для лечения этой группы больных используют обычно полусинтетические препараты группы пенициллина, тетрациклины и цефалоспорины. Существенное значение при этом имеет путь введения антибиотика, антибактериальных средств. Принимаемые внутрь и даже вводимые парентерально препараты могут оказаться весьма эффективными при лечении перифокальной пневмонии, менее эффективными — при бронхите и вовсе неэффективными — при лечении бронхоэктазов. При бронхоэктатической болезни даже внутрибронхиальное введение антибиотика через бронхоскоп неэффективно, так как пациент откашливает его вместе с содержимым бронхиального дерева в первые же минуты после окончания бронхоскопии. В связи с этим заслуживает внимания методика интрабронхиального лимфотропного введения антибактериальных препаратов.
При двустороннем поражении на одну санацию расходуется 80—120 мл санирующего раствора, при одностороннем процессе — 60—80 мл санирующей смеси. Готовят 0,1-0,2% раствор диоксидина на 2% растворе гидрокарбоната натрия или 0,1% раствор фурагина калиевой соли на изотоническом растворе хлорида натрия. Так как у пациентов бронхоэктатической болезнью мокрота обычно очень вязкая, в санирующий раствор добавляют муколитики.
В числе первых лекарственных препаратов, влияющих на реологические свойства бронхиального секрета, применяли ферментные препараты — трипсин, химотрипсин, рибонуклеазу. В настоящее время использование протеолитических ферментов, особенно в лечении больных с хронической бронхиальной обструкцией, представляется нецелесообразным вследствие возможного развития бронхоспазма вплоть до астматического статуса, увеличения склонности к кровохарканью, аллергическим реакциям и усилению деструкции межальвеолярных перегородок при дефиците α-1-антитрипсина.
В настоящее время при заболеваниях органов дыхания, сопровождающихся образованием очень вязкой, трудно отделяемой мокроты, применяются лекарственные средства, известные как муколитики или бронхосекретолитические препараты.
Одним из наиболее распространенных препаратов этой группы является N-ацетилцистеин (флуимуцил) (Zambon Group, Италия). Свободные сульфгидрильные группы ацетилцистеина разрывают дисульфидные связи кислых мукополисахаридов мокроты. При этом происходит деполимеризация макромолекул и мокрота становится менее вязкой и адгезивной. Ацетилцистеин оказывает стимулирующее действие на мукозные клетки, секрет которых способен лизировать фибрин и кровяные сгустки.
Ацетилцистеин увеличивает синтез глутатиона, принимающего участие в процессах детоксикации. Известно, что препарат обладает определенными защитными свойствами, направленными против свободных радикалов, реактивных кислородных метаболитов, ответственных за развитие острого и хронического воспаления в легочной ткани и воздухоносных путях.
При лечебной бронхоскопии применяют 3-6 мл 5-10% раствора флуимуцила, который вводят в бронхиальное дерево в конце санации. Санационные бронхоскопии выполняют через день, 8-10 санаций на курс лечения. Желательно в год проводить 2-3 курса лечебных бронхоскопий, но уже более коротких.
Прогноз заболевания зависит от выраженности и распространенности бронхоэктазов, тяжести течения болезни и ее осложнений. Прогноз резко ухудшается при развитии у больных дыхательной недостаточности, легочной артериальной гипертензии, легочных кровотечений и особенно амилоидоза печени или почек.
Н. Е. Чернеховская, доктор медицинских наук, профессор
РМАПО, Москва
Читайте также:
