Остеосаркома верхней и нижней челюсти - лучевая диагностика
Добавил пользователь Alex Обновлено: 01.02.2026
Остеосаркома (или остеогенная саркома), которую еще иногда не совсем правильно называют раком кости, — самая распространенная злокачественная опухоль костной системы.
Некоторые цифры и факты:
- В большинстве случаев остеосаркому диагностируют в молодом возрасте — от 10 до 30 лет.
- Наиболее высока распространенность заболевания среди подростков, но это не означает, что не могут заболеть люди другого возраста.
- Каждый десятый случай остеогенной саркомы встречается у людей старше 60 лет.
- Среди прочих онкологических заболеваний остеосаркома встречается редко. У детей она составляет 2% от всех видов рака, у взрослых — еще меньше.
Чаще всего остеосаркома встречается там, где находятся зоны роста — ближе к концам длинных трубчатых костей. Излюбленные места локализации опухоли: область колена (нижний конец бедренной и верхний конец большеберцовой кости), верхняя часть плечевой кости. Намного реже встречаются поражения других костей: таза, челюстей и др. Редкие локализации в большинстве случаев обнаруживают у людей старшего возраста.
Почему возникает остеосаркома?
Точные причины возникновения опухоли не известны. Но существуют некоторые факторы риска:
- Возраст. В группе максимально высокого риска подростки и молодые люди, у которых кости интенсивно растут.
- Рост. Обычно люди, у которых возникает саркома, имеют рост выше среднего.
- Облучение костей. Риски повышены у людей, которые перенесли курс лучевой терапии высокими дозами, особенно если это было в детстве. Влияние рентгенографии и компьютерной томографии не доказано.
- Некоторые заболевания костей: болезнь Педжета, множественная наследственная остеохондрома.
- Некоторые наследственные патологии: наследственная ретинобластома, синдром Ли-Фраумени, синдром Ротмунда-Томсона, синдром Блума, синдром Вернера.
Среди факторов риска для многих онкозаболеваний большое значение имеют особенности образа жизни: масса тела, вредные привычки, характер питания, физическая активность. Можно сказать, что остеосаркома — в данном случае исключение. Для того чтобы образ жизни внёс свою лепту в возникновение злокачественной опухоли, должны пройти десятилетия, а рак костей, как мы уже знаем, наиболее распространен среди молодых людей.
Симптомы остеосаркомы
Чаще всего встречается остеогенная саркома бедренной и большой берцовой кости — в области коленного сустава. Типичный симптом заболевания — упорные боли в суставе, кости. Иногда они постоянные, а иногда то стихают, то нарастают. Болевые ощущения могут усиливаться по ночам, во время физической активности (при ходьбе, беге, занятиях спортом). Если поражена нога, человек начинает хромать.
В области опухоли можно обнаружить отек или нащупать «шишку», уплотнение. Несмотря на то что опухолевая ткань ослабляет кость, переломы случаются не так часто.
Дети, особенно маленькие, физически активны, они часто падают, ударяются, поэтому у них первые симптомы остеосаркомы легко спутать с травмой. У взрослого человека, особенно если он не занимается спортом и тяжелым физическим трудом, подобные проявления сразу должны насторожить и стать причиной для визита к врачу.
Остеосаркома челюсти чаще всего встречается в возрасте 20-40 лет, то есть в среднем на 10 лет позже, чем «обычные» остеосаркомы. Проявляется в виде болей, припухлости, деформации зубов. Иногда опухоль затрудняет глотание, дыхание.
Какие выделяют стадии остеосаркомы?
Существуют разные классификации, чаще всего врачи определяют стадию остеосаркомы в соответствии с системой MSTS. Учитывают три показателя:
- G — степень озлокачествления. Может быть низкой (G1), когда ткань опухоли похожа на нормальную, и более агрессивной высокой (G2), в которой клетки практически полностью утратили первоначальные черты.
- T — степень распространения опухоли. Она может находиться в пределах кости (T1) или прорастать в соседние ткани (T2).
- M — наличие метастазов. M0 — метастазов нет, M1 — есть.
Другая классификация — AJCC, она учитывает распространение первичной опухоли (T), метастазы в ближайших лимфатических узлах (N), метастазы в других частях тела (M) и степень озлокачествления (G).
Методы диагностики
По симптомам можно только заподозрить рак кости или другое заболевание. Для того чтобы получить точный диагноз, врач назначит обследование, которое может включать:
- Рентгенографию. Быстрый и простой метод диагностики, в некоторых случаях помогает сразу констатировать опухоль. Если есть подозрение на метастазы в легких, проводят рентген грудной клетки.
- Магнитно-резонансная томография (МРТ) и компьютерная томография (КТ) помогают более детально рассмотреть опухоль, обнаружить прорастание в соседние ткани.
- Позитронно-эмиссионная томография. В организм вводят слабое радиоактивное вещество в безопасных дозах, которое сильнее всего накапливается в опухолевых клетках. Затем делают снимки. Это позволяет не только рассмотреть основную опухоль, но и обнаружить метастазы в разных частях тела.
- Общий и биохимический анализы крови. Применяют как дополнительный метод диагностики, чтобы оценить общее состояние человека. Также они могут косвенно указывать на степень агрессивности опухоли.
- Биопсия. Самый точный метод диагностики. Её применяют всегда, даже если другие исследования уже убедительно показывают, что у пациента есть рак кости. Биопсия помогает установить окончательный диагноз, отличить остеосаркому от других опухолей, определить степень озлокачествления. Врач может взять образец ткани при помощи иглы или через разрез.

Как проводят лечение остеосаркомы?
Лечение остеосаркомы состоит из трех этапов.
Начинают с курса предоперационной, или неоадъювантной, химиотерапии. В среднем он продолжается 10 недель. Назначают комбинацию нескольких препаратов — это помогает усилить эффект. Задачи неоадъювантной химиотерапии: уменьшить размер остеосаркомы и уничтожить метастазы. Благодаря предоперационной химиотерапии и современным химиопрепаратам, выживаемость при остеосаркоме в последние годы значительно улучшилась.
Затем следует хирургическое лечение. В прошлом единственным выходом была ампутация пораженной руки или ноги. Современные хирурги чаще всего могут обойтись удалением части кости или сустава. Их можно заменить на специальный протез и практически полностью восстановить функцию конечности. Операции при остеосаркоме стали более щадящими.
Послеоперационный курс химиотерапии (адъювантная) нужен для того, чтобы удалить раковые клетки, которые могли остаться в организме после хирургического вмешательства. В среднем он продолжается 18 недель, иногда дольше.
Как лечить рецидив остеогенной саркомы? В целом схема лечения примерно та же — операция, курс химиотерапии. После рецидива прогноз намного хуже, но все еще есть шанс на выздоровление.
Прогноз при остеосаркоме
Прогнозы для онкобольных выстраивают на основе особого показателя — пятилетней выживаемости. Он обозначает процент пациентов, которые остались живы в течение пяти лет с момента установления диагноза. Конечно, многие живут и дольше. Пять лет — условный рубеж, после которого можно с достаточно высокой вероятностью предполагать, что человек выздоровел.

Наиболее благоприятен прогноз в случаях, когда опухоль локализованная — то есть не успела распространиться по организму и может быть полностью удалена во время операции. Пятилетняя выживаемость составляет 60-80%, а если опухоль чувствительна к современным таргетным препаратам — до 90%.
Если есть метастазы остеосаркомы, прогноз сильно ухудшается. Пятилетняя выживаемость падает до 15-30%. Но она может быть выше, в пределах 40%, если:
- рак успел распространиться только в легкие;
- все метастазы можно обнаружить и удалить.
Метастазы остеосаркомы чаще всего обнаруживают в легких, реже в костях, головном мозге и других местах.
Зачастую прогноз ухудшается из-за того, что человек не обратил внимания на первые симптомы и не посетил вовремя врача. Если есть хотя бы малейшее подозрение на рак, если возникли любые необычные симптомы — лучше сразу перестраховаться и пройти обследование. Иногда от этого зависит жизнь. Запишитесь на прием к врачу-онкологу, звоните:
Остеосаркома ( Остеогенная саркома )
Остеосаркома - это злокачественная опухоль, происходящая из костной ткани. Отличается склонностью к бурному течению и раннему метастазированию. На начальных стадиях проявляется локальной болью, похожей на боли при ревматизме. В дальнейшем появляется припухлость, ограничение движений в расположенном поблизости суставе. Боли становятся резкими, невыносимыми. Возникают метастазы. Патология диагностируется на основании анамнеза, результатов осмотра, рентгенографии, КТ, МРТ и других исследований. Лечение включает в себя операцию по удалению опухоли в сочетании с предоперационной и послеоперационной химиотерапией.
МКБ-10
Общие сведения
Остеосаркома (от лат. osteon кость, греч. sarkos мясо, плоть + oma опухоль) - злокачественное новообразование, возникающее из элементов кости. Для этой опухоли характерно ранее метастазирование и бурное течение. Ранее прогноз при этом заболевании был очень неблагоприятным. Пятилетняя выживаемость наблюдалась менее чем в 10% случаев. В настоящее время, в связи с появлением новых методов лечения, шансы пациентов существенно увеличились. Сегодня 5 лет после постановки диагноза переживает более 70% пациентов с локализованной остеосаркомой и 80-90% с чувствительной к химиотерапии опухолью.
По данным специалистов в сфере клинической онкологии, остеосаркома чаще наблюдается у молодых пациентов. Более двух третей всех случаев заболевания приходится на возраст 10-40 лет. При этом мужчины страдают вдвое чаще женщин. Пик заболеваемости приходится на период быстрого роста: 10-14 лет у девочек и 15-19 лет у мальчиков. После 50 лет такая опухоль встречается крайне редко.
Причины остеосаркомы
Причины развития заболевания пока не выяснены. Однако существует ряд обстоятельств, при которых риск ее возникновения увеличивается. К их числу относится лучевая терапия и химиотерапия, проводимая ранее по поводу другого онкологического заболевания. Сама по себе травма (ушиб или перелом) никак не влияет на вероятность возникновения опухоли. Тем не менее, в ряде случаев именно достаточно серьезное травматическое повреждение (патологический перелом) или необычные, сохраняющиеся в течение длительного времени после ушиба боли в пораженной области становятся причиной обращения к врачу-травматологу и последующего обнаружения остеосаркомы. В отдельных случаях остеосаркома развивается на фоне хронического остеомиелита. Риск образования опухоли также увеличивается при болезни Педжета (деформирующем остеите).
Патанатомия
Обычно заболевание поражает длинные трубчатые кости. Доля коротких и плоских костей составляет не более 20% от общего числа всех остеосарком. Нижние конечности поражаются в 5-6 раз чаще верхних. При этом около 80% от всего количества остеогенных сарком развивается в области дистального конца бедренной кости. Далее в порядке убывания по частоте располагаются большеберцовые, плечевые, тазовые и малоберцовые кости. Затем - кости плечевого пояса и локтевая кость. Кости черепа страдают редко, в основном - у детей или у пожилых людей.
Типичной локализацией остеосаркомы является область метафиза (часть кости, расположенная между суставным концом и диафизом). Тем не менее, около 10% от общего числа остеосарком бедра обнаруживаются в его диафизарной части, а метафиз при этом остается нетронутым. Кроме того у остеосаркомы существуют «излюбленные» места расположения в каждой отдельной кости. Так, у бедра обычно поражается дистальный конец, у большеберцовой кости - внутренний мыщелок, у плечевой - область, где расположена шероховатость дельтовидной мышцы.
Классификация
При постановке диагноза остеосаркома проводится стадирование - оценка распространенности процесса. С учетом распространенности все остеосаркомы делятся на две большие группы:
- Локализованные саркомы. Клетки опухоли есть только в месте ее первоначальной локализации или окружающих тканях.
- Метастатические саркомы. Выявляется метастатическое поражение других органов.
Предполагается, что у 80% больных существуют микрометастазы, которые настолько малы, что не обнаруживаются при проведении дополнительных исследований. Кроме того, выделяют мультифокальную саркому, при которой опухоли одновременно возникают в нескольких (двух или более) костях.
Остеосаркома, как и другие злокачественные опухоли, в ряде случаев возвращается после лечения. Новая опухоль может возникнуть как в месте локализации предыдущей, так и в другой части тела (в области метастазов). Такое состояние называется рецидивом. Рецидив при остеосаркоме чаще всего развивается через 2-3 года после лечения и обнаруживается в легких. В дальнейшем рецидивы тоже возможны, но вероятность их развития уменьшается.
Болезнь начинается исподволь, постепенно. Вначале пациента беспокоят тупые неясные боли, возникающие вблизи сустава. По своему характеру они могут напоминать болевой синдром при ревматических миалгиях, артралгиях, миозитах или периартритах. При этом выпот (жидкость) в суставе отсутствует. Опухоль постепенно растет, в процесс вовлекаются расположенные рядом ткани, и боли усиливаются. Пораженный отдел кости увеличивается в объеме, мягкие ткани над ним становятся припухшими, на коже возникают флебэктазии (сеть мелких расширенных вен). Формируется контрактура в расположенном рядом суставе. При локализации остеосаркомы на костях нижней конечности развивается хромота. Пальпация пораженной области резко болезненна.
Через некоторое время боли становятся нестерпимыми, лишающими сна. Они появляются как при нагрузке, так и в покое и не снимаются обычными анальгетиками. Остеосаркома продолжает стремительно расти, распространяясь на соседние ткани, прорастая мышцы и заполняя костномозговой канал. Клетки опухоли разносятся с током крови, «оседая» в различных органах и образуя метастазы. При этом чаще всего поражается головной мозг и легкие.
Диагностика
Диагноз остеосаркома выставляется на основании клинических данных, результатов инструментальных и лабораторных исследований. Врач-онколог расспрашивает пациента, обращая внимание на постепенное начало и неясные боли вблизи сустава, а также на усиление этих болей с течением времени. Припухлость в области поражения на начальных стадиях определяется всего у 25% пациентов. Флебэктазии возникают на поздних стадиях и также наблюдаются не у всех больных. Поэтому отсутствие данных симптомов не может являться поводом для исключения злокачественного новообразования.
Окончательный диагноз устанавливается на основании результатов дополнительных исследований: рентгенографии, сканировании кости и биопсии ткани, взятой из пораженного участка. Для выявления метастазов в других органах выполняется компьютерная томография и рентгенография.
В начальной стадии на рентгенограммах определяется остеопороз и смазанность контуров опухоли. В последующем выявляется дефект костной ткани. Нередко наблюдается характерная картина отслоения надкостницы с образованием «козырька». У детей часто обнаруживается игольчатый периостит - тонкие костные образования (спикулы), расположенные перпендикулярно по отношению к кости. На рентгеновском снимке такие образования создают типичную картину «солнечных лучей».
При исследовании биоптата выявляются клетки сарокоматозной соединительной ткани, часть которых образует остеоидные и атипичные костные клетки. Обнаруживаются серьезные нарушения структуры кости. Во многих случаях остеогенез (образование кости) слабо выражен и наблюдается только на периферии остеосаркомы. Остеосаркому дифференцируют с остеобластокластомой, хрящевыми экзостозами, эозинофильной гранулемой и хондросаркомой.
Лечение остеосаркомы
Тактика лечения выбирается с учетом места расположения остеосаркомы, стадии заболевания, возраста пациента, его общего состояния, наличия рецидивов и т. д. Лечение остеосаркомы проводится в отделении онкологии и включает в себя три этапа:
- Предоперационную химиотерапию для уменьшения первичной опухоли и подавления мелких метастазов. Используется ифосфамид, метотрексат, этопозид, а также препараты платины (цисплатин, карбоплатин).
- Хирургическое лечение для удаления опухоли. В прошлом при остеосаркомах выполняли ампутации и экзартикуляции. В настоящее время в большинстве случаев проводят щадящую органосохраняющую операцию - сегментарную резекцию пораженного участка с его заменой имплантатом из металла, пластика, собственной кости пациента или трупной кости. Ампутация необходима только при большом размере остеосаркомы, патологическом переломе, прорастании мягких тканей или сосудисто-нервного пучка. Хирургическим путем может удаляться не только первичная опухоль, но и крупные метастазы в легких. При поражении лимфатических узлов также выполняется их оперативное удаление (лимфоаденэктомия).
- Послеоперационную химиотерапию для окончательного подавления злокачественных клеток, которые могли остаться в области метастазов или месте расположения первичной опухоли.
Лучевая терапия при остеосаркоме малоэффективна и проводится только при наличии абсолютных противопоказаний к операции.
Прогноз и профилактика
Прогноз при остеосаркоме зависит от определенных факторов как до, так и после лечения. Факторы, влияющие на прогноз до начала лечения остеосаркомы:
- Размер и место расположения опухоли.
- Стадия остеосаркомы (локализованная опухоль, наличие метастазов в других органах).
- Возраст и общее состояние здоровья пациента.
После лечения прогноз определяется эффективностью химиотерапии и результатом операции. Более оптимистичный прогноз - при значительном уменьшении местастазов и первичного очага после химиотерапии, а также при полном удалении опухоли.
В прошлом остеосаркома относилась к числу злокачественных опухолей с наиболее неблагоприятным прогнозом. Даже при том, что в ходе лечения проводились тяжелые калечащие операции - ампутации и экзартикуляции конечностей, пятилетняя выживаемость не превышала 5-10%. В настоящее время, в связи появлением новых методов лечения и применением эффективных органосохраняющих операций, шансы пациентов на благополучный исход существенно увеличились даже при наличии метастазов в легких. Пятилетняя выживаемость при локализованной остеосаркоме в наши дни составляет более 70%, а в группе с остеогенными саркомами, чувствительными к химиотерапии, этот показатель еще выше - 80-90%.
2. Ортопедия. Руководство для практикующих врачей/ Корнилов Н.В., Грязнухин Э.Г., Осташко В.И., Редько К.Г. - 2001
Рак верхней челюсти
Рак верхней челюсти - злокачественная опухоль, поражающая верхнечелюстную кость, характеризуется инфильтративным типом роста и регионарным метастазированием. Основными симптомами неоплазии являются заложенность носа, гнойно-кровянистые выделения, постоянная боль ноющего характера, патологическая подвижность интактных зубов, деформация альвеолярного отростка. Диагноз рак верхней челюсти выставляют, базируясь на жалобах пациента, данных физикального обследования, результатах рентгенографии, цитологического и патогистологического исследований. Лечение рака верхней челюсти комбинированное, резекции верхнечелюстной кости предшествует курс химио- или лучевой терапии.
Рак верхней челюсти - первичное или метастатическое злокачественное новообразование, поражающее верхнюю челюсть. Среди пациентов, обратившихся в онкодиспансер, рак верхней челюсти диагностируют в три раза чаще, чем рак нижнечелюстной кости. На один случай саркомы верхней челюсти приходятся четыре случая рака той же локализации. Основную группу пациентов составляют люди среднего возраста (от 40 до 60 лет). В 65% случаев рак верхней челюсти выявляют после 50 лет. Наиболее часто опухоль развивается из слизистой оболочки гайморового синуса. Гистогенетически злокачественное новообразование верхней челюсти у 80% онкобольных является плоскоклеточным раком. Метастазирование рака верхней челюсти наблюдается поздно, метастазы обнаруживают у каждого третьего пациента.
Причины рака верхней челюсти
Наиболее часто причинами рака верхней челюсти являются хронические вялотекущие воспалительные заболевания гайморовых синусов. Реже злокачественная опухоль развивается непосредственно в костной ткани из эпителиальных островков Малассе, или прорастает в кость со слизистой оболочки полости рта, покрывающей небо, щеки, альвеолярный отросток. Высоки риски малигнизации в случае хронической травмы слизистой острыми краями разрушенных зубов, неотполированным базисом съемного протеза или выступающими ребристыми компонентами ортопедических или ортодонтических аппаратов.
Кроме первичного злокачественного новообразования в стоматологии описаны и вторичные формы, когда рак верхней челюсти развивался в результате метастазирования опухолей молочной, щитовидной желез, желудка у онкобольных пациентов. Метапластические изменения цилиндрического эпителия, выстилающего верхнечелюстной синус, возникают вследствие хронического гайморита. Образование гиперпластических разрастаний сопровождается малигнизацией ткани. Гистологически рак верхней челюсти в превалирующем большинстве случаев является плоскоклеточным ороговевающим. Реже обнаруживают аденокарциному, а также неороговевающий плоскоклеточный рак.
Классификация рака верхней челюсти
Различают следующие стадии рака верхней челюсти:
- 1 стадия. Опухоль локализуется в одной анатомической области. Деструктивные изменения кости отсутствуют.
- 2a стадия. Рак верхней челюсти не распространяется на соседние участки. В пределах анатомической области расположения новообразования присутствуют деструктивные изменения кости.
- 2b стадия. Рак верхней челюсти прорастает в смежные участки. На стороне поражения обнаруживают один неспаянный с окружающими тканями метастаз.
- 3a стадия. Рак верхней челюсти распространяется на орбиту, носовую полость. Признаки поражения выявляют на небе, альвеолярном отростке. Присутствует остеолиз костной ткани.
- 3b стадия. В ходе обследования выявляют односторонние или двухсторонние метастазы.
- 4a стадия. Рак верхней челюсти распространяется на носоглотку, основание черепа. На коже возникают изъязвления. Отдаленных метастазов нет.
- 4b стадия. Раком верхней челюсти поражаются смежные области. Также обнаруживают метастазы, спаянные с окружающими тканями.
Симптомы рака верхней челюсти
На начальных стадиях рак верхней челюсти протекает бессимптомно. В течение первых 2-3 месяцев больные связывают заложенность носа, наличие скудных серозных выделений с проявлениями хронического гайморита. Далее клиника рака верхней челюсти становится более явной. Симптоматика напрямую зависит от локализации патологического очага. Если злокачественное новообразование развивается в верхнем участке медиальной стенки, в патологический процесс вовлекаются слезный мешок и слезные ходы, что в дальнейшем приводит к возникновению признаков вторичного дакриоцистита. У больных отмечается усиленное слезотечение, соответствующее стороне поражения. Кожа в зоне внутреннего угла глаза становится отечной, гиперемированной.
При прогрессировании рака верхней челюсти разрушается нижнеглазничная стенка, вследствие чего развиваются экзофтальм и диплопия, падает острота зрения. Если новообразование локализуется в нижнем участке медиальной стенки, пациенты указывают на наличие бурых выделений из носа с неприятным гнилостным запахом. Присутствует ощущение тяжести, заложенности носа. Если рак верхней челюсти поражает переднюю стенку гайморового синуса, возникает выраженный болевой синдром в участке интактных премоляров или моляров. Далее присоединяется патологическая подвижность зубов.
Сильные невралгические боли наблюдаются и при локализации рака верхней челюсти в верхне-наружном квадранте. При распространении опухолевого процесса на участок жевательных мышц нарушается открывание рта. В результате компрессии венозного сплетения блокируется отток лимфы из ретробульбарной клетчатки, что в дальнейшем приводит к возникновению хемоза, экзофтальма. Стертая клиническая картина наблюдается при развитии рака верхней челюсти в нижнем участке внешней стенки гайморового синуса. Основные жалобы сходны с проявлениями хронического гайморита.
Диагностика рака верхней челюсти
Диагноз рак верхней челюсти ставят на основании жалоб пациента, данных анамнеза, результатов клинического, рентгенологического, цитологического и патогистологического исследований. На начальных стадиях клиника рака верхней челюсти сходна с хроническими гайморитом, этмоидитом. Если опухолевый процесс распространяется на костную ткань со слизистой оболочки неба, щеки или альвеолярного отростка, при обследовании врач-стоматолог выявляет исходный патологический очаг в ротовой полости.
При экзофитном типе роста опухоль представлена разрастаниями с признаками изъязвлений. Кратерообразная язвенная поверхность встречается при эндофитном росте злокачественного новообразования. На поздних стадиях рака верхней челюсти выявляют деформацию альвеолярного отростка, патологическую подвижность интактных зубов, отсутствие болевой и тактильной чувствительности в зоне локализации опухоли. Прорастание злокачественного новообразования в орбиту ведет к развитию экзофтальма, становится причиной потери зрения.
Рентгенографически при начальных стадиях рака верхней челюсти, развивающегося со слизистой оболочки гайморового синуса, выявляют завуалированность пазухи. В участке шва, соединяющего альвеолярный отросток со скуловой костью, а также в области нижнеглазничной щели обнаруживают деструктивные изменения кости, нехарактерные для хронического гайморита. На прицельной рентгенограмме определяют резорбцию костной ткани в зоне межзубных и межкорневых перегородок. На поздних стадиях резорбтивные процессы протекают по типу «тающего сахара» без признаков регенерации кости.
Для подтверждения диагноза рак верхней челюсти используют лабораторные исследования. О наличии злокачественной опухоли сигнализирует выявление в ходе цитологического анализа опухолевых клеток в промывных водах, полученных из верхнечелюстных синусов. При отсутствии дренажа через соустье гайморовой пазухи выполняют пункцию. Полученный материал направляют на патогистологическое исследование. Дифференцируют рак верхней челюсти с хроническим гайморитом, одонтогенной радикулярной кистой, хроническим остеомиелитом. Физикальное обследование проводят стоматолог-хирург, онколог, при необходимости отоларинголог.
Лечение рака верхней челюсти
Если рак верхней челюсти не распространился на основание черепа, лечение включает гамма-терапию или химиотерапию, сопровождающуюся введением лекарственных средств в регионарные артерии. Экстирпацию верхней челюсти проводят через 3 недели. После операции показана контактная лучевая терапия ложа удаленного новообразования. При подозрении на метастазирование рака верхней челюсти выполняют иссечение шейных лимфоузлов вместе с клетчаткой.
Наличие нескольких неспаянных с окружающими тканями метастазов или одного спаянного является прямым показанием к выполнению радикального вмешательства, заключающегося в удалении лимфоузлов вместе с подкожной клетчаткой, шейным отделом внутренней яремной вены, нижнечелюстной слюнной железой и грудино-ключично-сосковой мышцей. Операционный дефект восполняют с помощью пластиночного съемного протеза (при условии сохранения мягких тканей) или изготавливают эктопротез. Закрытие соустья ротовой полости с полостью носа осуществляется за счет пластинки-обтуратора. При наличии признаков вовлечения в патологический процесс основания черепа хирургическое вмешательство не осуществляют. Основой лечения рака верхней челюсти в данном случае является химиотерапия и лучевая терапия.
При раннем выявлении злокачественного новообразования прогноз благоприятный. На поздних стадиях рака верхней челюсти распространение опухолевых клеток на основание черепа сопровождается метастазированием. В этом случае прогноз для жизни неблагоприятный. После радикальной лимфаденэктомии ухудшается венозный отток, возникает стойкая деформация шеи, что негативно влияет на качество жизни пациентов.
Рак нижней челюсти

В настоящее время распространенность опухолей определяется в рамках ТNМ-классификации злокачественных опухолей, шестое издание, 2002 г. Классификация применима только для рака. Необходимо морфологическое подтверждение диагноза.
Регионарными лимфатическими узлами для нижней челюсти являются подчелюстные, глубокие шейные лимфатические узлы, расположенные вдоль сосудисто-нервного пучка шеи.
Определения R-классификации применимы ко всем локализациям опухолей головы и шеи. Эти определения следующие:
Факторы и группы риска
Диагностические критерии
I-II стадия - боли по ходу нижнечелюстного нерва, напоминающие боли при пульпите, патологическая подвижность зубов, язва на слизистой альвеолярного отростка.
Дифференциальная диагностика проводится с хроническим ларингитом, папилломой или фибромой гортани, лейкоплакией, дискератозы гортани, пахидермия.
Основаниями для консультации онколога является анамнез, клинико-рентгенологическая картина, морфологическая верификация.
III-IV стадия - боли по ходу нижнечелюстного нерва, напоминающие боли при пульпите, патологическая подвижность зубов, язва на слизистой альвеолярного отроска, деформация лица за счет инфильтрации в подбородочную, щечную области и дно полости рта, ограничение открывания рта. Наличие узлов на шее.
На R-граммах нижней челюсти - деструкция более одной анатомической части нижней челюсти с наличием патологического перелома.
9. Лабораторные исследования: общий анализ крови, биохимический анализ крови, общий анализ мочи, определение группы крови и Rh-фактора, анализ
Дифференциальный диагноз
Отсутствие болей. Множественные округлые очаги просветвления с четкими контурами, в который выстоит корень.
Грибовидное образование на слизистой альвеолярного отростка с выраженной ножкой. Костная ткань интактна.
Медленно нарастающая деформация в виде выпячивания или вздутия челюсти. Наличие очага резорбции костной ткани с четкими контурами.
Лечение
Цели лечения - ликвидация опухолевого очага и метастазов.
Общие принципы лечения
Существуют три основных метода лечения злокачественных опухолей нижней челюсти - хирургический, лучевой и их сочетание. Все методы могут быть дополнены химиотерапией. Химиотерапия, как часть комбинированного лечения, улучшает 5-летнююю выживаемость у больных с локализованным процессом на 20-60%.
Морфологическая оценка ответа опухоли после 4-6 курсов предоперационной химиотерапии дает важную прогностическую информацию.
При опухолях, соответствующих Т1, эффективность хирургического метода лечения на первом этапе, по результатам последних мировых исследований, выше, чем при лучевой терапии, достигает 85-95% излеченности, также снижается риск возникновения рецидива опухоли. При опухолях, соответствующих Т2, также лечение следует начинать с резекции нижней челюсти с последующим проведением послеоперационной лучевой терапии. При наличии у больного противопоказаний к операции лечение начинается с лучевой терапии. При распространенном злокачественном новообразовании нижней челюсти Т3-4 производят резекцию опухоли в пределах здоровых тканей с первичной костной пластикой с иссечением шейной клетчатки с послеоперационным курсом
Лечение метастазов злокачественных новообразований в лимфатических узлах шеи
Наличие регионарных метастазов не препятствует консервативному лечению, т.к. метастазы этой локализации (N1-2) часто хорошо поддаются лучевому и химиолучевому лечению. Поэтому лимфатические узлы шеи с обеих сторон следует включать в зону облучения. При необходимости облучения лимфатических узлов нижних отделов шеи больным показано использование прямого поля с блоком. Нижний край прямого поля проходит на 1 см ниже нижнего края ключиц. При поражении надключичных лимфатических узлов должны облучаться лимфатические узлы верхнего средостения.
При наличии ограниченно смещаемых или несмещаемых метастазов, лечение целесообразно начинать с неоадъювантной полихимиотерапии и последующего лучевого лечения в дозе 40 гр. Дальнейшая тактика зависит от эффективности проведенной терапии.
В случае значительной или полной регрессии метастазов или их неоперабельности после указанной дозы облучение следует довести до СОД 60-70 гр.
При недостаточной регрессии увеличенных лимфатических узлов и их операбельности после 40 гр. необходимо производить фасцально-футлярное иссечение шейной клетчатки (ФФиШК) или операцию Крайля по показаниям.
Показаниями к выполнению фасциально-футлярной лимфодиссекции является наличие Н0, N1, N2а подвижных лимфоузлов без вовлечения в процесс внутренней яремной вены и кивательной мышцы.
Показаниями к проведению операции Крайля является наличие N1, N2а, б, с неподвижных, вколоченных лимфоузлов с вовлечением в опухолевый процесс внутренней яремной вены и кивательной мышцы.
В случае спаянности регионарного метастаза на шее с сосудами шеи больному необходимо дополнительное обследование (КТ шеи и ангиография), т.к. возможно проведение операции Крайля с резекцией артерии и ее пластическим замещением.
Лечение комбинированное: оперативное лечение и пред- или послеоперационная лучевая терапия. Лучевую терапию осуществляют методом дистанционной гамма-терапии. Лучевую терапию проводят ежедневно, число полей определяют в зависимости от размеров поражения и наличия регионарных метастазов. Суммарная доза составляет 40-50 гр. Небольшие опухоли, когда процесс ограничен одной анатомической частью органа, опухоль не прорастает в надкостницу, удаляют путем резекции челюсти с первичной костной аутопластикой. При центральном раке нижней челюсти, когда опухоль не прорастает в надкостницу и нет регионарных метастазов, производят резекцию в пределах здоровых тканей и осуществляют первичную костную пластику.
При наличии метастазов, резекцию нижней челюсти производят в едином блоке с иссечением шейной клетчатки. При саркоме производят широкую резекцию нижней челюсти с удалением подчелюстной слюнной железы. При распространении опухоли на соседние анатомические структуры резекцию нижней челюсти осуществляют с широким иссечением окружающих мягких тканей. Первичное пластическое замещение дефекта производят аутотрансплантантом взятым из ребра, малоберцовой или др. кости. Также могут использоваться титановые металлоконструкции. Злокачественные опухоли нижней челюсти малочувствительны к химиопрепаратам. Однако при саркомах, фиброзной гистиоцитоме позволяют перевести местнораспространенные опухоли в операбельное состояние.
Неоадъювантная химиотерапия состоит из двух идентичных курсов с трехнедельными перерывами между ними. Однако, если после первого курса химиотерапии регрессия опухоли менее 50%, продолжение химиотерапии нецелесообразно.
При проведении как неоадъювантной, так и адъювантной полихимиотерапии при раке гортаноглотки возможно применение следующих схем и комбинаций химиопрепаратов:
Остеогенная саркома челюсти - симптомы и способы лечения
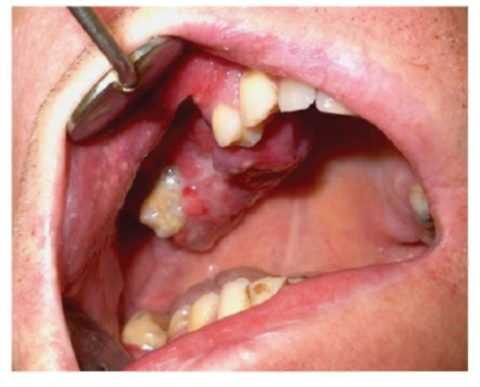
Остеогенная саркома челюсти, симптомы которой указывают на ее злокачественную природу, составляет около 20% первичных раковых новообразований. Заболевание, примерно, с одинаковой частотой поражает верхнюю и нижнюю челюсть.
Наиболее подверженной категорией пациентов при этом считаются мужчины в возрасте 40-60 лет. Опухоль на верхней челюсти преимущественно локализируется в тканях альвеолярного отростка, а нижней - в теле челюсти.
Остеогенная злокачественная опухоль челюстных тканей в сравнении с саркомой других костей тела имеет следующие отличительные черты:
- более старший возраст пациентов;
- редкие явления метастазирования новообразования;
- высокие показатели пятилетней выживаемости.
Клиническая картина болезни
Остеосаркома челюсти, признаки которой свидетельствуют о ее злокачественном течении, проявляется такими симптомами:
- отек и резкое увеличение объема мягких и твердых тканей ротовой полости;
- периодические болевые приступы, интенсивность которых зависит от стадии онкологии;
- нарушение поверхностной чувствительности кожных покровов лица;
- постепенное нарастание признаков раковой интоксикации организма в виде ночной потливости, снижения аппетита, резкого падения массы тела, снижения работоспособности и чувство хронической усталости.
В большинстве клинических случаев длительность субъективных ощущений у пациента до момента установления диагноза может продолжать 1-72 месяца. При этом достоверный диагноз специалист на первом визите установить не может.
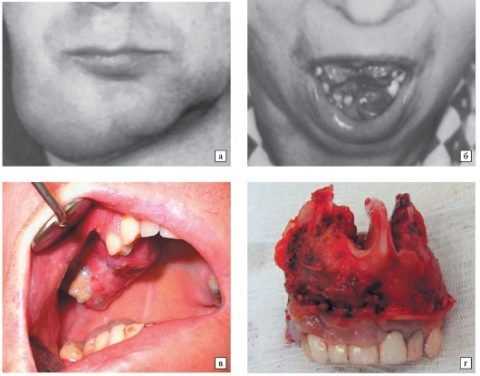
Диагностика заболевания
Стоматологическая инструкция по проведению онкологической диагностики требует проведения следующих мероприятий:
- сбор анамнеза болезни и выяснение основных жалоб пациента;
- визуальный и инструментальный осмотр челюстно-лицевой области;
- рентгенография костных тканей челюстей;
- пальпация региональных лимфатических узлов;
- общий и развернутый анализ крови;
- биопсия или гистологический анализ.
Ключевым способом исследования пациентов с остеосаркомой является рентгенография. На рентгенологических снимках врач определяет отдельные участки растворения кости или замещения ее соединительной тканью.
В последнее время стоматологи-онкологи начали активно применять компьютерную томографию, которая позволяет обнаружить участки атипичного окостенения за пределами челюсти. С помощью этой методики специалист также оценивает размер, форму и точное расположение злокачественного новообразования.
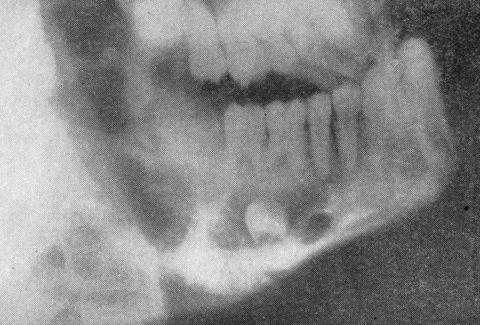
Окончательный диагноз устанавливается только по результатам гистологического и цитологического анализа. Для этого хирург удаляет небольшой участок патологической ткани и отправляет ее в лабораторию для микроскопического анализа. По результатам биопсии формируется план лечения и реабилитации онкобольного.
Методы лечения остеогенной саркомы челюстей
Лечение злокачественного новообразования челюстей исключительно хирургическое. В стоматологической литературе описаны способы комбинированной терапии остеосаркомы, которые включают совместное применение хирургической операции, химиотерапии и лучевого лечения.
Цена и форма хирургической операции зависят от локализации опухоли и ее стадии роста.
Современные результаты исследований показали, что радикальное вмешательство остается наиболее эффективным методом удаления опухоли. Хирургическая операция выполняется в нескольких вариантах
Резекция нижней челюсти
Таким образом, хирург приступает к иссечению части или половины нижней челюсти. Следует учитывать, что при злокачественном поражении костной ткани хирург-онколог часто дополнительно удаляет региональные лимфатические узлы шейной и поднижнечелюстной области.
Оптимальный результат такого лечения наблюдается при наиболее обширных способах резекции челюстных тканей.
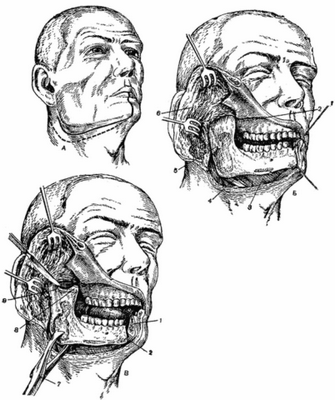
Половинное вычленение челюсти
В предоперационном периоде стоматолог изготовляет пациенту фиксирующую шину, которая предназначена для удерживания в стабильном состоянии частей челюсти или трансплантата.
Сама хирургическая операция проводится под общим наркозом. Затем врач выполняет дугообразный разрез кожных покровов, который соответствует очертаниям челюсти. Следующий этап - это хирургическое выделение ракового очага из мягких тканей и его полное удаление.
После иссечения кости и ракового новообразования хирургическую рану промывают раствором антисептика и зашивают кетгутом.
Резекция верхней челюсти
Удаление участков верхнечелюстной кости осуществляется под эндотрахеальным наркозом. Часто доступ к операционному полю формируется со стороны ротовой полости, что повышает его эстетические характеристики. Но, к сожалению, такой вид оперирования доступен только для пациентов на начальных стадиях онкологии.
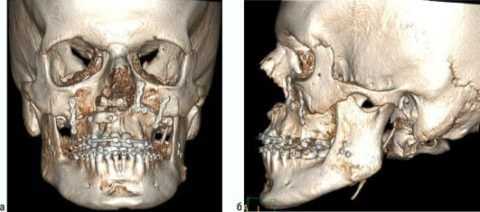
Осложнения оперативных вмешательств
Большинство осложнений возникают после хирургического удаления метастазов и региональных лимфатических узлов.
Они бывают следующих видов:
- Травматическое повреждение лицевого, язычного, блуждающего или поязычного нервов. В таких случаях у больного наблюдается нарушение функции глотания и пережевывания пищи. В отдельных пациентов парализуются мимические мышцы лица.
- Повреждение лимфатического протока груди. У таких пациентов, преимущественно, страдают системные и местные защитные свойства организма.
- Воздушная эмболия и эмфизема средостения. Эти тяжелые нарушения могут привести к летальному исходу.
- Вторичны венозные кровотечения и расстройства, которые сопряжены с высоким риском смертности.
Прогноз заболевания
Прогноз заболевания является неблагоприятным с высокой частотой смертельных случаев. А вот, предупредить образование опухоли может своевременное прохождение плановых стоматологических осмотров и санация ротовой полости.
Читайте также:
