Пептидные нейромедиаторы. Опиоиды и тахикинины - субстанция Р, нейрокинин
Добавил пользователь Alex Обновлено: 22.01.2026
На классификацию нейропетидов повлияла история их открытия. По своей функции, месту синтеза. мишеней и структуре все нейропептиды, включая медиаторы и гормоны, подразделяются на 18 семейств. В некоторых из этих семейств по 20-30 различных нейропептидов. Эти вещества отнесены к нейропептидам потому, что все они образуются также определенными нейронами мозга или ,как эндорфины, в гипофизе , выступая затем в качестве нейромодуляторов, и оказывая то или иное нейротропное или даже психотропное действие. Можно выделить несколько классикационных подходов.
Гипоталамические рилизинг-факторы
Гипоталамус - это область мозга, которая содержит несколько типов нейронов, ответственных за выделение различных гормонов. Гипоталамус расположен ниже таламуса, но чуть выше ствола мозга, размером примерно с миндаль.
Гипоталамус отвечает за некоторые метаболические процессы и аналогичные действия вегетативной нервной системы и синтезирует и секретирует нейрогормоны или нейропептиды. Эти типы пептидов часто называют высвобождающими ( релизинг ) гормонами или гормонами гипоталамуса, которые в свою очередь стимулируют или ингибируют секрецию гормонов гипофиза.
Гипоталамус контролирует температуру тела, голод и важные аспекты поведения родителей и привязанности, жажду, усталость, сон и циркадные ритмы. Все секретируемые пептиды высвобождаются в кровь в капиллярах и немедленно перемещаются в воротные вены во второе капиллярное русло в передней доле гипофиза, где они оказывают свое влияние. Нейропептиды высвобождаются в виде периодических "всплесков" ( выбросах) , поэтому заместительная гормональная терапия этими гормонами не работает, если замены не вводятся также в "всплесках".
- GHRH: гормон, высвобождающий гормон роста ; также известный как фактор, высвобождающий гормон роста (GRF, GHRF), соматолиберин или соматокринин; GHRH представляет собой смесь двух пептидов, один из которых содержит 40 аминокислот, а другой 44; GHRH стимулирует клетки в передней доле гипофиза секретировать гормон роста (GH) и высвобождать путем связывания с рецептором GHRH (GHRHR) на клетках в передней части гипофиза.
- CRH: кортикотропин-рилизинг-гормон; также известный как кортикотропин-рилизинг-фактор (CRF) или кортиколиберин; CRH представляет собой пептид из 41 аминокислоты. CRH действует на клетки в передней доле гипофиза, высвобождая адренокортикотропный гормон . CRH также синтезируется плацентой и, по-видимому, определяет продолжительность беременности. Он также может играть роль в предотвращении иммунной атаки против плода на Т-клетки матери. Портальная система переносит CRH к передней доле гипофиза, где стимулирует кортикотропы к выделению адренокортикотропного гормона ( ACTH) и других биологически активных веществ (β-эндорфин). АCTH стимулирует синтез кортизола, глюкокортикоидов, минералокортикоидов и DEHA. CRH может подавлять аппетит, усиливать субъективные ощущения тревоги и выполнять другие функции, такие как повышение концентрации внимания
- GnRH: гонадотропин-рилизинг-гормон (pyro Glu-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-Gly-NH) ( также известный как гормон, высвобождающий лютеинизирующий гормон - HRH и люлиберин) - cекреция гонадотропин релизинг гормона в начале полового созревания вызывает половое развитие, и с тех пор она необходима для нормальной сексуальной физиологии как у мужчин, так и у женщин; у обоих полов его секреция происходит в периодических импульсах, обычно происходящих каждые 1-2 часа.
- TRH: тиреотропин-рилизинг гормон (трипептид: pGlu-His-Pro-NH2) - стимулирует выброс тиреотропного гормона и пролактина, когда он достигает передней доли гипофиза
- Соматостатин (смесь двух пептидов, одна из 14 аминокислот, другая из 28); соматостатин действует на переднюю долю гипофиза и ингибирует выброс гормона роста (GH) и выброс тиреотропного гормона (TSH); соматостатин также секретируется клетками поджелудочной железы и кишечника, где он ингибирует секрецию множества других гормонов.
- Дофамин ( дофамин является производным аминокислоты тирозина); в гипоталамусе ингибирует выброс пролактина (PRL) из передней доли гипофиза..
· Гормоны гипофиза
ACTH: адренокортикотропный гормон
aMSH: а-меланоциты стимулирующий гормон
GH: гормон роста
FSH: фолликулостимулирующий гормон
LH: лютеинизирующий гормон
TSH: тиреотропин [тиреотропный гормон]
· Опиатные пептиды
· Нейрогипофизарные пептиды
· Нейрональные и эндокринные пептиды
- ANF: предсердный натрийуретический пептид
- BNP представляет собой полипептид из 32 аминокислот, который секретируется желудочками сердца в ответ на растяжение сердечной мышцы, пептид относится к семейству натрийуретических пептидов, которые содержат три структурно связанных паракринных фактора: натрийуретические пептиды предсердия, мозга и С-типа; как предсердные, так и мозговые натрийуретические пептиды секретируются в предсердиях и желудочках сердца, тогда как пептид С-типа секретируется в кости; BNP совместно секретируется вместе с N-концевым фрагментом из 76 аминокислот (NT-proBNP), который является биологически неактивным; BNP представляет собой подковообразный пептид из 32 аминокислот, который связан дисульфидным мостиком, образованным между аминокислотами 10 и 26 и полученным путем расщепления крупных предшественников - препро и прогормонов; BNP активирует трансмембранную гуанилилциклазу, рецептор натрийуретического пептида-A (NPR-A); Активированный NPR-A, в свою очередь, производит второй мессенджер cGMP, который запускает эффекторы, которые опосредуют его сердечные функции.
- CGRP: пептид, связанный с геном кальцитонина - представляет собой нейропептид из 37 аминокислот с сильными сосудорасширяющими и кардиоэкситаторными свойствами, опосредованными рецептором. α-CGRP представляет собой пептид из 37 аминокислот, образованный из альтернативного сплайсинга гена кальцитонина / CGRP, расположенного в хромосоме 11. Менее изученный β-CGRP отличается тремя аминокислотами (у человека) и кодируется в отдельном гене. Это было обнаружено, когда было показано, что альтернативный процессинг РНК-транскриптов из гена кальцитонина приводит к образованию отдельных мРНК, кодирующих CGRP. Человеческая форма CGRP была выделена из ткани щитовидной железы пациентов с медуллярным раком щитовидной железы. CGRP принадлежит к семейству регуляторных пептидов, которое также включает адреномедуллин и амилин. CGRP состоит из амино-концевой дисульфидной мостиковой петли между аминокислотами 2 и 7, за которой следует альфа-спираль между аминокислотами 8 и 18 и плохо определенный поворот между остатками 19 и 21. Карбоксильные и амино-концы CGRP могут независимо взаимодействовать с его рецепторы. Функции CGRP связываются с двумя рецепторами, связанными с G-белком, CGRP1 и CGRP2. Одной из основных функций CGRP является расширение сосудов сердечной мышцы. Чтобы достичь этого, CGRP сначала связывается с рецептором CGRP1, что приводит к выработке цАМФ, который, в свою очередь, активирует протеинкиназу A (PKA). PKA фосфорилирует и открывает калиевые каналы, которые вызывают расслабление мышц. CGRP широко распространен в центральной и периферической нервной системе. Он вызывает расслабление сосудов посредством связывания с рецептором CGRP1 и может играть роль в контроле артериального давления. CGRP также защищает повреждение тканей посредством своих сосудорасширяющих функций, влияет на активность воспалительных клеток, привлекая больше клеток в месте воспаления, играет роль вгенезе мигрени во время болезненных фаз заболевания и играет защитную роль в сердечной ткани.
- VIP: вазоактивный кишечный пептид содержит 28 аминокислотных остатков; этот нейропептид принадлежит к суперсемейству глюкагонов / секретинов, которые являются лигандами рецепторов, связанных с белками класса G G. VIP вырабатывается во многих тканях позвоночных, включая кишечник, поджелудочную железу и супрахиазматические ядра гипоталамуса в головном мозге; стимулирует сократительную способность сердца, вызывает расширение сосудов, повышает гликогенолиз, снижает артериальное давление и расслабляет гладкие мышцы трахеи, желудка и желчного пузыря; пептид имеет период полураспада (t½) около двух минут в крови.
· Циркулирующие пептиды
· Гастроинтестинальные и нейропептиды
- CCK: холецитокинин - также называемый панкреозимином, представляет собой пептидный гормон, обнаруживаемый в тонкой кишке, который составляет классическую триаду гормонов кишечника вместе с гастрином и секретином. CCK секретируется в кровь после приема пищи и играет важную роль в проглатывании, всасывании, подвижности кишечника , передаче сигналов сытости, ингибировании секреции желудочной кислоты и переваривании пищи. Стимулирует переваривание жиров и белков. CCK синтезируется I-клетками в эпителии слизистой оболочки тонкой кишки и секретируется в двенадцатиперстную кишку, первый сегмент тонкой кишки, где он вызывает выделение пищеварительных ферментов и желчи из поджелудочной железы и желчного пузыря. Он также действует как ингибитор голода. Считается, что он также играет важную роль в стимулировании лекарственной толерантности к опиоидам, таким как морфин и героин, и частично участвует в переживаниях гиперчувствительности боли во время отмены опиоидов. CCK был открыт в 1928 году из-за его способности вызывать сокращение желчного пузыря. CCK - это нейропептид, который принадлежит к семейству гормонов, идентифицированных по количеству аминокислот, например, CCK58 и CCK33. Prepro-CCK, аминокислотный пептид a115, сначала расщепляется на pro-CCK, что, в свою очередь, приводит к CCK58, основной обработанной форме CCK, которая предполагает конфигурация спираль - поворот - спираль . CCK связывается с рецепторами CCK на клеточной мембране, которые при активации увеличивают оборот фосфатидилинозита, что приводит к высвобождению внутриклеточного кальция. Высвобождаемый кальций вызывает повышенную секрецию фермента либо непосредственно, либо через активацию протеинкиназы С.
GRP: пептид, высвобождающий гастрин
Субстанция K; Субстанция Р (тахикинины)
Пептиды тахикининов относятся к большому семейству нейропептидов, обнаруженных у широкого спектра видов, от амфибий до млекопитающих. Название этого семейства пептидов происходит от их способности быстро вызывать сокращение кишечной ткани. Семейство тахикининов характеризуется общей С-концевой последовательностью Phe-X-Gly-Leu-Met-NH 2где X представляет собой либо ароматическую, либо алифатическую аминокислоту.
Все тахикининовые пептиды вызывают гипотензию, сокращение гладких мышц кишечника и мочевого пузыря и секрецию слюны у млекопитающих. Гены, которые кодируют белки-предшественники, называемые препротахикининами, дифференцированно сплайсированы для получения различных наборов пептидов, а белки-предшественники подвергаются посттрансляционной обработке с помощью протеаз для получения меньших пептидов.
Нейрокинины являются частью семейства тахикининовых пептидов и включают в себя нейрокинины B, субстанцию P, Физалаемин и Эледоизин. Нейрокинины ( субстанция P, нейрокинин A, нейрокинин B) и рецепторы нейрокининов - NK1 и NK3 - в значительной степени экспрессируются в ядре одиночного тракта (NST), где они участвуют в центральной регуляции висцеральной функции. Нейрокинин А участвует в регуляции кроветворения, в то время как нейрокинин В известен своей ролью медиатора передачи боли. Нейрокинин A также очень похож по своей структуре на субстанцию P и производит некоторые из тех же биологических воздействий, что и субстанция P. Нейрокинин A является мощным бронхоконстриктором. В кишечнике Нейрокинин А вырабатывается внутренней кишечной нервной системой.
· Гастроинтестинальные и пептиды поджелудочной железы
PP: полипептид поджелудочной железы
· Только нейрональные пептиды (?)
- NPY: нейропептид Y - нейропептидный нейротрансмиттер из 36 аминокислот, обнаруженный в мозге и вегетативной нервной системе человека; пептид в основном вырабатывается нейронами симпатической нервной системы и служит сильным вазоконстриктором, а также вызывает рост жировой ткани. В мозге он экспрессируется в различных структурах , включая гипоталамус; считается, что он выполняет несколько функций, таких как увеличение потребления пищи и накопление энергии в виде жира, уменьшение беспокойства и стресса, уменьшение восприятия боли, влияние на циркадный ритм, уменьшение добровольного потребления алкоголя, снижение артериального давления и контроль эпилептических припадков.
- PYY: пептид YY - также известен как пептид тирозин тирозин или пептид поджелудочной железы YY3-36, кодируется геном PPY; пептид YY представляет собой короткий пептид из 36 аминокислот, который выделяется клетками в подвздошной кишке и толстой кишке в ответ на кормление, по - видимому , для того, чтобы уменьшить аппетит .
· Только эндокринные пептиды (?)
Паратиреоидный гормон
Примечание : (?) Указывает на то, что классификационный подход еще не определен и возможны изменения в будущем.
Последние усовершенствования в технологиях, используемых в геномике и протеомике, позволяющие открывать и изучать нейропептиды, привели к множеству вновь обнаруженных функциональных пептидов, присутствующих в нейросистеме различных видов, включая людей. В частности, использование наноразмерной хроматографии в сочетании с масс-спектрометрией позволило провести структурное определение нейропептидов у различных видов на более низких уровнях, чем это было возможно ранее .Поскольку пептиды, синтезируемые в нервной системе, служат мессенджерами и модуляторами многочисленных биологических процессов, важно понимать, как эти пептиды продуцируются и как они действуют. Поскольку неточный синтез нейропептидов или трансдукция сигнала могут привести к дисфункции или гибели организма, знание структуры встречающихся в природе нейропептидов необходимо для расшифровки того, как обрабатываются предшественники нейропептидов и как они функционируют. Ниже приведен список некоторых новых нейропептидов.
- Агути-родственный белок (AGRP) или Агути-родственный пептид (AgRP).
- Регулируемый транскриптом пептид кокаина и амфетамина (CART)
- Эндоморфин-1 и -2
- Ноцицептин/ орфанин FQ - нейропептид из 17 аминокислот, эндогенный лиганд для рецептора ноцицептина (NOP, ORL-1), происходит из белка препроноцицептина, а также из 2 других пептидов, ноцистатина и ноцилла. Ген, кодирующий препроноцицептин, находится у человека на Ch8p21. Ноцицептин, связанный с опиоидом , не действует на классические опиоидные рецепторы mu, каппа и дельта-опиоидные рецепторы, и его действия не противодействуют опиоидному антагонисту налоксону. Ноцицептин является сильным противоболевым средством. Ноцицептин широко распространен в ЦНС и обнаруживается во многих областях гипоталамуса, ствола головного мозга и переднего мозга, а также в вентральном и дорсальных рогах спинного мозга. Ноцицептин действует на рецептор ноцицептина (NOP1), ранее известный как ORL-1. Рецептор также широко распространен в мозге, в том числе в коре, переднем обонятельном ядре, латеральной перегородке, гипоталамусе, гиппокампе, миндалевидном теле, центральном сером ядре, ядрах понтина, межпеданкулярном ядре, черной субстанции, рафовом комплексе, locus coeruleus и спинном мозге. Ноцицептин ослабляет боль, вызванную простагландином Е2. Ноцицептин относится к динорфину А, пептидному 17-мерному лиганду -опиоидного рецептора. Динорфин А также связывает ORL1, но с аффинностью в 100 раз ниже, чем ноцицептин. Орфанин FQ2 представляет собой другой биологически активный пептид 17-мер, полученный из того же предшественника ноцицептина, как преноцицептин.Ноцицептин ослабляет боль, вызванную простагландином Е2.
- Ноцистатин - представляет собой нейропептид, кодируемый геном для предшественника ноцицептина / орфанина FQ. Ноцистатин блокирует вызванную ноцицептином аллодинию и гипералгезию и ослабляет боль, вызванную простагландином Е2. Ноцистатин представляет собой карбоксиконцевой гексапептид ноцистатина (Glu-Gln-Lys-Gln-Leu-Gln), который консервативен у бычьих, человеческих и мышиных видов, которые обладают активностью, блокирующей аллодинию. Ноцистатин - это новый биологически активный пептид, полученный из того же предшественника, что и ноцицептин. Ноцистатин не связывается с рецептором ноцицептина. Ноцицептин и ноцистатин могут играть противоположную роль в передаче боли.
- Секретоневрин - представляет собой нейропептид из 33 аминокислот, полученный из секретогранина II (хромогранин C, CHGC). Пептид представляет собой фрагмент секретогранина II, содержащий аминокислоты с 154 по 186. Он участвует в хемотаксисе моноцитов и эозинофилов (сравнимых по эффективности с IL8) и эндотелиальных клеток и в регуляции пролиферации эндотелиальных клеток. Самые высокие уровни секретоневрина обнаруживаются в передней части гипофиза, за ним следует мозговое вещество надпочечников и гипоталамус задней доли гипофиза (в 2-6 раз более низкие уровни в других исследованных областях мозга). Было показано, что секретоневрин обладает мощной ангиогенной активностью in vivo на модели роговицы мыши и in vitro в трехмерном геле, а также стимулирует высвобождение дофамина из центральных полосатых нейронов и базальных ганглиев. Secretoneurin - это нейропептид, вырабатываемый в мозге, мозговом веществе надпочечника и других эндокринных тканей путем протеолитической обработки секретогранином II. Секретоневрин действует как прямой ангиогенный цитокин, ингибирует апоптоз эндотелиальных клеток (EC), стимулирует пролиферацию EC и активирует систему митоген-активируемой протеинкиназы (MAPK) и путь Akt
- Урокортин - представляет собой пептид из 40 аминокислот, который у людей кодируется геном UCN, членом семейства саувагин / кортикотропин-рилизинг-фактора / уротензина I.Он структурно связан с геном кортикотропин-рилизинг-фактора (CRF), а кодируемый продукт является эндогенным лигандом для рецепторов CRF типа 2. Считается, что он отвечает за влияние стресса на аппетит. Урокортин является сильным анорексигенным пептидом, который вызывает двигательную активность, подобную питанию, при центральном или периферическом введении голодным животным. Урокортин относится к семейству кортикотропин-рилизинг-факторов (CRF), которое включает в себя CRF, уротензин I, саувагин, урокортин II и урокортин III.
- Пролактин - релизинг пептид (PrRP ) - представляет собой пептидный гормон, который у людей кодируется геном PRLH. PrRP стимулирует высвобождение пролактина (PRL) и регулирует экспрессию пролактина посредством связывания с пролактин-высвобождающим пептидным рецептором (GPR10).
Субстанция Р
Субстанция P ( SP , для «порошка»), идентифицированное как тахикинин в кишечнике в 1931 году ( SP был первым известным нейропептидом Von Euler , Gaddum изолировали его из экстрактов кишечника и мозга как одно из многих веществ) и участвующее в контроле множества других вегетативных функций, особенно передачи боли, является предметом интенсивных фундаментальных и клинических психиатрических исследований в качестве центрального нейромедиатора, нейромодулятора и иммуномодулятора наряду с нейрокининами A и B (NKA и NKB), открытыми в 1984 году.
В первых экспериментах SP стимулировал сокращения подвздошной кишки кролика атропин-устойчивым способом. В 1953 году SP был признан сенсорным нейротрансмиттером Lembeck et al. Еще 10 лет спустя были обнаружены два других тахикинина млекопитающих: катионный пептид нейрокинин А (NKA, ранее назывался веществом К) и анионный пептид нейрокинин В . Тахикинины (tachys = swift) вызывают резкое сокращение гладких мышц кишечника. Эти тахикинины участвуют во множественных физиологических процессах, о чем свидетельствует их широкое распространение. На периферии они функционируют как потенциальные регуляторы кровотока, проницаемости сосудов, слюноотделения, моторики желудочно-кишечного тракта, кишечной секреции, мочеиспускания и активности лейкоцитов. Более того, они действуют как переносчики боли с периферии. В центральной нервной системе (ЦНС) тахикинины действуют как нейромедиаторы и нейромодуляторы.
Существует два гена, кодирующих синтез трех тахикининов SP, NKA и NKB: ген препротахикинина I (PPTI) кодирует SP и NKA, а ген PPTII кодирует NKB . Посредством альтернативного сплайсинга ген PPTI может экспрессировать четыре различные формы (α β, γ и δ) мРНК. Все эти формы являются предшественниками субстанция P, но только формы β и γ также кодируют для синтеза NKA и его удлиненных форм нейропептид K и нейропептид γ. Трансляция мРНК генерирует так называемый препропептид. Ферментативное расщепление до «отцовского» пропептида происходит внутри эндоплазматического ретикулума. Последний этап генерации активного пептида осуществляется путем превращения ферментов в цитоплазматические везикулы. После высвобождения нейропептидов они инактивируются катаболическими пептидазами. Тахикинины разлагаются множественными пептидазами в ткани, включая ангиотензинпревращающий фермент (АПФ). Не существует механизма обратного захвата, как известно для моноаминовых нейротрансмиттеров.
SP широко распространен по всей ЦНС, а также по мицеллярным и подслизистым нервным сплетениям кишечника. В головном мозге SP обнаруживается в периакведуктуальной серости среднего мозга, в ядре Raphe Magnus и в ядре reticularis gigantocellularis pars a, которые являются важными структурами в эндогенной системе контроля боли. Большое количество SP-содержащих нейронов было обнаружено в заднем гипоталамусе человека и базальном переднем мозге, что указывает на участие SP в функциях гипоталамуса, таких как сексуальное поведение или высвобождение гормонов гипофиза. SP также обнаруживается в базальных ганглиях, прилежащем ядре и - на более низких уровнях - в коре головного мозга. Более того, есть доказательства того, что SP взаимодействует с дофаминергическими нейронами ядер нигростриатального, лимбического и переднего мозга. NKB нейронов присутствуют в переднем гипоталамусе и базальном переднем мозге, что указывает на комплементарное распределение от SP нейронов. Все три тахикинины представлены в полосатом теле.
В человеческом мозге 5-НТ и SP сосуществуют в значительной части клеточной популяции ядра дорсального шва, что является современной мишенью для лечения антидепрессантами. Почти 50% серотонинергических нейронов в ядре дорсального шва, проецирующихся на передний мозг, и 25% серотонинергических нейронов в ядре срединного шва экспрессируют мРНК SP. SP и 5-HT локализуются в вентральных медуллярных нейронах кошек и в серотонинергических нейрональных афферентах к гипоглоссальному ядру крысы. Кроме того, SP экспрессируется с подтипами серотониновых рецепторов 5-HT 2A , 5-HT 2C и 5-HT 6 в полосатом теле крысы.
Примечательно, что экспрессия SP в полосатом теле, черной субстанции и миндалине снижается после хронического лечения антидепрессантами препаратами имипрамин, дезипрамин, кломипрамин, амоксапин и миансерин. Имипрамин и дезипрамин также уменьшают количество SP в гиппокампе, в то время как его уменьшение в перегородке индуцируется только миансерином.
Субстанция P широко распространено по всей центральной нервной системе, где его часто колокализуют с серотонином, норэпинефрином и дофамином. Многие антагонисты и агонисты рецепторов нейрокинина (NK) были синтезированы и некоторые клинически протестированы. Двойное слепое исследование MK869, селективного антагониста рецептора NK1, который блокирует действие субстанции P, показало значительную активность по сравнению с плацебо и меньшим количеством сексуальных побочных эффектов, чем пароксетин, у амбулаторных пациентов с большой депрессией и умеренной тревогой. Субстанция Р , которое разлагается ангиотензинпревращающим ферментом (АПФ), может опосредовать модуляцию терапевтического результата при аффективных расстройствах функциональным полиморфизмом в гене АПФ: аллель D связан с более высокими уровнями АПФ и повышенной деградацией нейропептидов, что приводит к тому , что пациенты с большой депрессией, которые несут аллель D, имеют более низкие показатели депрессии и более короткую госпитализацию.
В 60-х годах прошлого века были обнаружены первые трициклические антидепрессанты, блокирующие обратный захват классических нейротрансмиттеров серотонина (5-гидрокситриптамина (5-НТ) и норэпинефрина (NE). С тех пор эти два моноаминных нейротрансмиттера были в центре внимания исследований антидепрессантов, и наиболее распространенные патогенетические концепции большой депрессии основаны на этом профиле действия антидепрессантов. Исследования показывают, что модуляция моноаминов не является единственным механизмом действия антидепрессантов. Нейропептиды, которые колокализуются с моноаминами, также могут быть вовлечены в патогенез депрессии.
Колокализация SP и NE демонстрируется наличием SP-содержащих аксонных терминалов в локусе cerulcus. Прямое нанесение SP на локус церулеус оказывает возбуждающее действие через рецептор нейрокинина NK1. SP также локализуется с дофаминергическими нейронами в прилежащем ядре. 32 SP находится под стимулирующим контролем дофаминергических нейронов, выступающих на компактную черную субстанцию и на внутренний сегмент бледного шара. Блокада дофаминергической передачи резерпином снижает уровни мРНК SP, поскольку она находится под стимулирующим контролем дофамина. Хронический лечение с амфетамином было обнаружено, что без влияния на уровень дофаминовых рецепторов в полосатом теле, но заметно увеличились уровни мРНК ИП.Некоторые исследования показывают, что система подавления боли, включающая активацию мезолимбических дофаминергических нейронов, естественным образом вызывается воздействием стресса, посредством эндогенного выброса опиоидов и SP в среднем мозге. SP также экспрессируется с широким спектром других нейропептидов и нейротрансмиттеров, и даже с нейрональной синтазой оксида азота.
Рецепторы нейрокинина
Известны три различных рецептора нейрокинина: NK1, NK2 и NK3. SP является наиболее мощным тахикинином для рецептора NK1, тогда как NKA проявляет наибольшее сродство к рецептору NK2 и NKB для рецептора NK. Недавно было показано, что рецептор NK4, который первоначально был атипичным опиоидным рецептором, мог эффективно реагировать на NKB у крысы, но его обнаружение в тканях человека до настоящего времени не было возможным. Однако следует отметить, что все тахикинины млекопитающих имеют ограниченную селективность в отношении определенного рецептора нейрокинина. Это связано с общей С-концевой аминокислотной последовательностью, которая важна для биологической активности тахикининов.
Нейрокининовые рецепторы представляют собой рецепторы, связанные с G-белком, с характерными семимембранными доменами. В целом, некоторые механизмы предотвращают неконтролируемую стимуляцию клеток нейротрансмиттерами, которые взаимодействуют с рецепторами, связанными с G-белком: (i) удаление агониста из внеклеточной жидкости путем деградации или обратного захвата (последний не относится к тахикининам);(ii) десенсибилизация рецептора путем отсоединения от G-белков для прекращения каскада сигнальной трансдукции; и (iii) эндоцитоз агонист-стимулированного рецептора, истощающий плазматическую мембрану высокоаффинных рецепторов. NK1-рецептор, по-видимому, десенсибилизируется путем фосфорилирования, независимо от интернализации рецептора, в то время как для ресенсибилизации требуется эндоцитоз, рециркуляция и дефосфорилирование. Быстрая тахифилаксия рецептора NK1 после воздействия агониста, однако, связана с быстрой интернализацией рецептора.
Анатомическое распределение рецепторов нейрокининов
Широкий спектр областей мозга экспрессирует рецептор NK1. Примечательно, что ядра шва ( raphe nucleus ) , locus ceruleus, striatum, прилежащее ядро ( nucleus accumbens) , гиппокамп, латеральное ядро гипоталамуса, habenula, интерпедункулярное ядро ( interpeduncular nucleus) , ядро солитарного тракта ( tractus solitarius) и черная субстанция богаты рецепторами NK1. Таким образом, существует значительное несоответствие между SP-содержащими областями мозга и NK1-экспрессирующими участками мозга, что может быть связано с вышеупомянутой ограниченной селективностью тахикининов. Рецепторы NK2 редко распространяются в ЦНС. Их можно найти в небольших количествах в разных регионах, таких как стриатум. Третий тип рецепторов нейрокинина, рецептор NK3, поразительно преобладает в срединных кортикальных слоях по всей коре.
Следовательно, паттерны экспрессии сильно различаются между рецепторами NK1, NK2 и NK3.МРНК рецептора NK4 широко экспрессируется в нейронах ЦНС крыс, включая кору головного мозга, гиппокамп и гипоталамус. Рецептор NK1 также экспрессируется с синтазой оксида азота в полосатых интернейронах у крыс. В спинном мозге рецепторы NK1 локализуются на сенсорных нейронах второго порядка, получая ноцицептивные сигналы. Сигнал рецептора NK1 индуцирует медленно развивающуюся устойчивую деполяризацию, в то время как быстрый ввод в сенсорные нейроны второго порядка опосредуется глутаматом возбуждающей аминокислоты через рецептор N-метил-D-аспартата (NMDA).
Специфические эффекты рецепторов нейрокинина
Elliott и Iversen описали различные эффекты SP после интрацеребровентрикулярного (ICV) введения или непосредственного применения в вентрально-сегментарной области среднего мозга головного мозга крысы, что вызывало повышенную двигательную активность, груминг и тремор. SP вызывает не только простые движения. Даже сложное поведение на животных моделях тревоги и депрессии может модулироваться активацией рецептора NK. Было обнаружено, что инфузия TCV аналога SP, диметил-C7, вызывает отвращение в парадигме кондиционирования места. Более того, введение ICV SP, NKA и NK1- и NK2-селективных агонистов вызывает анксиогенный эффект в тесте плюс-лабиринт, мышиной модели тревожного поведения. Напротив, синтетический агонист NK3 сенктид обладает анксиолитическим эффектом. Это еще раз демонстрирует дифференциальную роль трех рецепторов NK. Однако сложность тахикининовой системы также представлена дифференциальными эффектами в пределах одного подтипа рецептора NK, так как один и тот же рецептор может оказывать противоположные эффекты при стимуляции в разных областях мозга.
Агонисты нейрокининового рецептора
Первые пептидергические антагонисты рецептора NK1 были синтезированы в начале 1980-х годов в качестве полезных инструментов для исследования эндогенных лигандов NK1. Сегодня стало доступно большое количество непептидных антагонистов рецепторов NK1, NK2 и NK3. Рецептор NK3, по-видимому, играет дифференцированную роль в поведении, подобном депрессии: другое недавнее исследование, использующее тест принудительного плавания в качестве мышиной модели депрессии, показало положительный эффект агониста NK3-рецептора аминосенктида.
Антагонисты нейрокининового рецептора
В 1998 году Марк Крамер и его коллеги опубликовали первый отчет о клиническом исследовании, в котором проверялась антидепрессивная эффективность антагониста рецептора NK1. Этот антагонист рецептора NK1 также продемонстрировал значительную анксиолитическую эффективность у пациентов с депрессией. MK869 хорошо переносился и, в частности, частота половой дисфункции была на 23% ниже, чем у пациентов, получавших пароксетин. Третий антагонист рецептора NK1, NKP608, в настоящее время проходит фазу 2 клинических испытаний в качестве антидепрессанта, но на сегодняшний день не опубликовано никаких данных о его эффективности.
Вещества, проявляющие свойства нейротрансмиттеров
Помимо широко известных нейротрансмиттеров и нейромодуляторов к веществам проявляющим эти свойства относятся: энкефалины, нейрокинины, нейротензин , холицистокинин , кортикотропин - релизинг фактор , соматостатин , орексины А и В , эндоканнабиоиды , нейроактивные стероиды и мозговой нейротрофическаий фактор ( brain - derived neurotrophic factor - BDNF).
Энкефалины ( лей- энкефалин и мет- энкефалин) относятся к бета - эндорфину и динорфину, они по своей структуре тесно связаны с пептидамии проявляют действие подобно эндогенным лигандам для мю - дельта - и каппа опиоидным рецепторам. широко распространненым в структурах мозга. Эти вещества играют важную роль в восприятии боли , аддиктивном поведении и эмоциоанльных реакциях.
Нейрокинины субстанция Р ( нейрокинин - 1) , субстанция К ( нейрокинин - 2 или нейрокинин - А ) , нейромедин К ( нейрокинин В) представляют собой группу пептидов которые действуют на NK1, NK2, NK3 рецепторы. Эти вещества могут выполнять функции , как нейротрансмиттеров , так и нейромодуляторов, волвеченных , как правило, в процессы воспаления. Антагонисты NK1 и NK3 рецепторов применяются для лечения депрессии, шизофрении и нейродегенеративных заболеваний.
Холицистокинины ( ССК) - семейство нейропептидов , которое частично концентрируется в миндалине и сером веществе вокруг водопровода ( PAG) , впрочем , как и в других структурах мозга , принимающих участие в генезе тревоги и фобий. В структурах мозга действие ССК опосредуется CCR2 ( CCRD) рецепторами. Хотя тетрапептиды ССК, ССК4 индуцируют появление панических атак , причем, антагонисты рецепторов CCK неэффективны при панических атаках , возможно, в связи с их плохим проникновением через гемато - энцефалический барьер.
Кортикотропин - релизинг фактор ( CRF) действует на CRF1 и CRF2 рецепторы гипофиза, вызывая секрецию адренокортикотропного гормона и кортизола , а также такие структуры мозга , как миндалина , серое пятно и гиппокмп. CRF вовлечен в реакции стресса и изменения настроения , а также проявляет влияние на когнитивную сферу. Антагонисты CRF могут проявлять свойства антидепрессантов , анксиолитиков и используются для лечения алкогольной зависимости.
Соматостатин является пептидным гормоном , который действует на G - протеин - связанные соматостатиновые рецепторы. Он тормозит выделение гормона роста и тироид - стимулирующего гормона из передней доле гипофиза. Соматостатин действует также как модулятор нейротрансмиссии и клеточной пролиферации . Соматостатин вовлечен в патогенез аффективных расстройств.
Орексины А и В ( гипокретины) по своей генетике связаны между собой и относятся к нейропептидом. Они влияют на OX1 и OX2 рецепторы в большом количестве представленные в латеральном гипоталамусе и других структурах мозга, вовлеченных в реакции стресса ( регуляция стресса) . Орексины первоначально были идентифицированы как важные регуляторы питания , но также и в циркадианные ритмы , процессы , связанны со сном и реакции стресса , включая эндокринный контроль.
Нейромедиаторы

Нейромедиаторы, перечисленные в табл. 8.3 и табл. 8.10, найдены в определенных областях нервной системы и вместе со сложным анатомическим устройством обеспечивают сложную функцию головного мозга человека.
Глутамат — главный возбуждающий нейромедиатор в ЦНС
Глутамат — аминокислота, действующая на NMDA-рецепторы и He-NMDA-рецепторы. Это первичный неиромедиатор в таламокортикальнои, пирамидальной клетке, кортикостриарных путях и важный нейромедиатор в гипоталамусе. Когда обнаружили, что некоторые лекарства, воздействующие на NMDA-рецепторы, вызывают психические симптомы, было высказано предположение, что в основе психических заболеваний могут лежать нарушения глутаматной системы.
Таблица 8.10 Классификация главных пептидных нейромедиаторов центральной нервной системы
Эндорфины, энкефалины, динорфины
Субстанция Р, нейрокинин
Нейропептид Y, субстанция Р, нейротензин, галанин
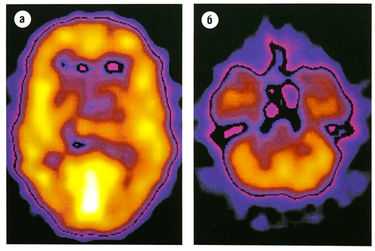
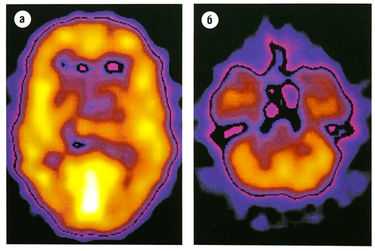
Рис. 8.25 Кортикальное распределение ГАМКд-рецепторных комплексов. Изображение получено с помощью радиоактивно меченного аналога бензодиазепина ломазенила и однофотонной эмиссионной компьютерной томографии. Самые светлые области имеют наивысшую плотность рецепторов, (а) Изображение на уровне среднезатылочной коры, (б) Изображение на уровне мозжечка.
ГАМК — главный тормозной нейромедиатор в ЦНС
ГАМК — аминокислота, действующая прежде всего на ГАМКд- и ГАМКв-рецепторы. ГАМКА-рецепторы присутствуют на 40% нейронов. Кортикальное распределение ГАМКд изображено на рис. 8.25. С1'-канал зависит от ГАМКА-рецептора, в то время как ГАМКв-рецепторы соединены с G-белками.
Бензодиазепины и большинство антиконвульсантов действуют через ГАМК-рецепторы:
- бензодиазепины связываются с определенными бензодиазепиновыми рецепторами, расположенными на соответствующем участке ГАМК-рецепторного комплекса, что увеличивает эффекты ГАМК;
- некоторые антиконвульсанты имеют схожие эффекты с бензодиазепинами, но большинство действуют непосредственно на ГАМК-рецептор.
С нарушениями ГАМК-системы, как полагают,могут быть связаны невротические расстройства. По результатам недавних исследований было высказано предположение о роли ГАМК в этиологии шизофрении.
Глицин — необходимый нейромедиатор для действия глутамата
Глицин необходим для реализации эффектов глутамата. Кроме того, глицин действует на собственные рецепторы, связанные с С1"-каналом и ингибирующие нервные функции.
- Симптомы болезни Паркинсона — результат дисбаланса между ацетилхолиновой и дофаминовой активностями в базальных ганглиях
- Антихолинергические средства используют для лечения паркинсоноподобных неблагоприятных эффектов, связанных с использованием антипсихотических средств, и в лечении идиопатической болезни Паркинсона
- Никотиновые и мускариновые агонисты так же, как лекарственные средства, увеличивающие эндогенный ацетилхолин, оказывают благоприятное действие при лечении болезни Альцгеймера
Ацетилхолин — главный периферический нейромедиатор
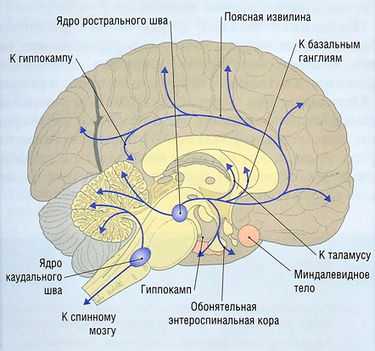
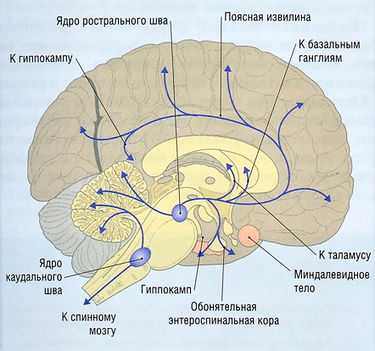
Рис. 8.26 5-Гидрокситриптаминовые пути. 5-НТ-содержащие нейроны найдены в ядрах медиального и дорсального шва, хвостатом и голубоватом пятнах, межножковой области.
АХ действует как нейромедиатор в ЦНС так же, как и на периферии.
Центральное первичное АХ-содержащее ядро -базальное ядро, которое расположено в переднем мозге и идет к коре головного мозга и лимбической системе. Холинергические волокна в ретикулярной системе поступают к коре головного мозга, лимбической системе, гипоталамусу и таламусу.
Идентифицировано девять различных 5-НТ-рецепторов
Наиболее изучены подтипы 5-НТ1А, 5-НТ2В, 5-НТ2с и 5-НТ3. Серотонинергические клеточные тельца в основном локализуются в области верхнего варолиевого моста и среднего мозга. Классические области для 5-НТ-содержащих нейронов — ядра медиального и дорсального шва. Нейроны от ядер шва идут к базальным ганглиям и различным частям лимбической системы и имеют широкое распределение по всей коре головного мозга в дополнение к связям с мозжечком (рис. 8.26).
Все 5-НТ-рецепторы идентифицированы как рецепторы, соединенные с G-белком, кроме подтипа 5-НТ3, который расположен на рецептор-опосредуемом №+/К+-канале.
5-НТ синтезируется из триптофана при участии триптофангидроксилазы, и поступление триптофана лимитирует его синтез. 5-НТ прежде всего метаболизируется моноаминоксидазой А в 5-гидроксииндолацетиловую кислоту (5-ГИАК) .
Норэпинефрин широко распространен в ЦНС
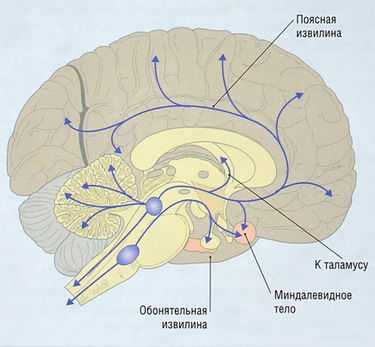
Норэпинефрин действует как нейромедиатор в ЦНС и ВНС (см. ранее). Норэпинефрин действует в нескольких типах адренорецепторов: a1, a2, β1-3. Большинство нейронов, содержащих норэпинефрин, в ЦНС расположены в голубоватом пятне в варолиевом мосту и среднем мозге. Их пути в других областях мозга показаны на рис. 8.27.
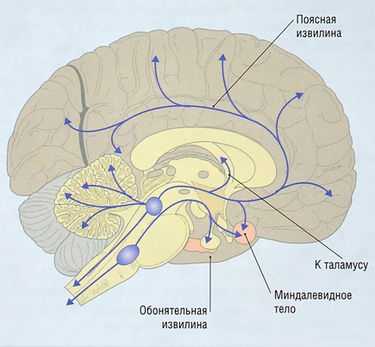
Рис. 8.27 Норэпинефрин в центральной нервной системе. Большая часть НЭ-содержащих нейронов в центральной нервной системе расположены в голубоватом пятне варолиевого моста и среднего мозга. Эти нейроны идут через связку средней части переднего мозга в лимбической системе к коре, таламусу и гипоталамусу. Вторая группа НЭ-содержащих нейронов в вентральной покрышечной области имеет отростки к гипоталамусу и миндалевидному телу.
5-гидрокситриптамин, депрессия и тревожное состояние
- Большинство антидепрессантов ингибируют обратный захват 5-НТ из синаптической щели
- Буспирон — частичный агонист пресинаптических 5-НТ1д-рецепторов — эффективное средство для лечения беспокойства, тревожного состояния и депрессии
- 5-НТ2А- и 5-НТ2С-рецепторы играют определенную роль при депрессивных заболеваниях, негативных симптомах шизофрении и профилактике последствий длительного приема нейролептиков
- Имеется относительное увеличение числа 5-НТ2А-рецепторов в лобной доле коры самоубийц
- С некоторым успехом антагонисты 5-НТ2А-рецепторов применяют для лечения негативных симптомов шизофрении
- Нейролептики, действующие как селективные антагонисты 5-НТ2А-рецепторов (атипичные нейролептики), более эффективны при лечении шизофрении, чем типичные нейролептики, и меньше вызывают неблагоприятные двигательные эффекты при аналогичном уровне блокады дофамина
- Антагонисты 5-НТ3-рецепторов используют для лечения рвоты
Норэпинефрин и аффективные и тревожные состояния
- Норэпинефрин, как полагают, играет критическую роль при аффективных нарушениях и в меньшей степени при тревожных состояниях
- Патология НЭ-содержащих нейронов — часть моноаминовой теории депрессии
- Наиболее традиционные трициклические антидепрессанты ингибируют обратный захват НЭ из синаптической щели и увеличивают доступность синаптического НЭ
- Ингибиторы моноаминоксидазы угнетают расщепление НЭ
- Полагают, что влияние антидепрессанта на превращения НЭ регулируется контролем в постсинаптических рецепторах
- постсинаптические агрецепторы связаны со стимуляцией инозитолфосфатного обмена; *а2-рецепторы ингибируют образование цАМФ;
- β-рецепторы стимулируют образование цАМФ.
В нервной системе человека были идентифицированы пять типов дофаминовых рецепторов (D1-D5)
D1 D5-рецепторы стимулируют образование цАМФ, активизируя стимулирующий G-белок, в то время как D2-, D3- и 04-рецепторы ингибируют образование цАМФ, активизируя ингибирующий G-белок. D2-рецепторы более распространены, чем D3- и D4-рецепторы. D3-рецепторы преимущественно расположены в хвостатом ядре (одно из септальных ядер в лимбической системе), а D4-рецепторы сконцентрированы в медиальной лобной коре.
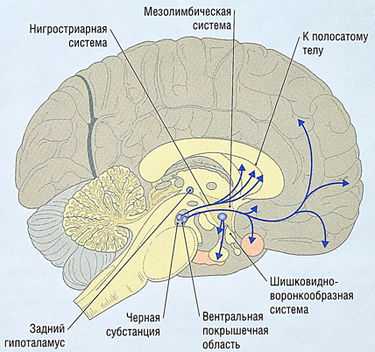
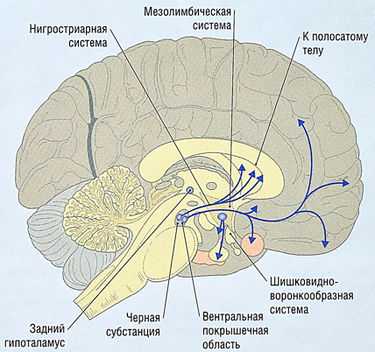
Рис. 8.28 Дофамин в центральной нервной системе. Дофаминергические тракты — нигростриарный, мезолимбический/мезокортикальный и шишковидно-воронкообразный.
Варианты дофаминергических трактов представлены на рис. 8.28:
- нигростриарный тракт идет от черной субстанции в среднем мозге к полосатому телу и играет определенную роль в мотоконтроле;
- мезолимбический/мезокортикальный тракт имеет тела клеток в вентральной области покрышек среднего мозга, прилегающей к черной субстанции, и идет к лимбической системе и новой коре головного мозга в дополнение к полосатому телу (стриатуму). Они подводят волокна к медиальной поверхности фронтальных долей и к парагиппокампу и поясной коре (поясная извилина медиальной и нижней поверхностей полушария большого мозга);
- третий большой путь — это шишковидно-воронкообразный. Тела клеток находятся в извитом ядре и перивентрикулярной области гипоталамуса и проходят в воронке гипоталамуса и переднем гипофизе. Дофамин ингибирует высвобождение пролактина в пределах этого тракта.
Дофамин синтезируется как часть обычного пути для катехоламинов и метаболизируется двумя ферментами: МАОв, которая является интранейрональным ферментом, и катехол-O-метилтрансферазой, которая является экстранейрональным ферментом. Первичный метаболит дофамина — гомованиловая кислота.
Считается, что D2-рецепторы — наиболее важные дофаминовые рецепторы, которые вовлечены в развитие психоза, т.к. эффективность антипсихотических препаратов коррелирует с их сродством к D2-рецепторам. Однако появление нетипичных нейролептиков с равной эффективностью, но с относительно низким сродством к D2-рецептору повышает вероятность, что и другие подтипы дофаминовых рецепторов могут играть важную роль в этиологии и лечении психоза.
Постоянная блокада дофаминовых рецепторов ведет к их дезрегулированию, которое может вносить вклад в нарушения движения, обнаруживаемые при длительной нейролептической терапии.
Очевидно, что мезолимбический и мезокортикальный тракты играют важную роль в регулировании поведения, управляемого положительным подкреплением, и эти находки могут вести к созданию новых лекарственных средств для терапии физической зависимости.
Дофамин, болезнь Паркинсона и психоз
- Идиопатическая болезнь Паркинсона возникает из-за дегенерации клеток в черной субстанции
- Эффекты типа паркинсонических, связанные с типичными нейролептиками (например, галоперидолом, хлорпромазином), — следствие блокирования дофаминовых рецепторов в пределах нигростриарного тракта
- Антипсихотические средства проявляют свои положительные эффекты через действие на мезолимбический и мезокортикальный тракты
- Ингибирование высвобождения пролактина устраняется за счет блокады дофаминового рецептора нейролептиками в пределах шишковидно-воронкообразного пути и ведет к пролактинемии (галакторее)
Известно около 300 пептидных нейромедиаторов в ЦНС
Пептиды имеют менее 100 аминокислот. Наиболее хорошо изученные нейропептиды перечислены в табл. 8.10. Часто эти пептиды синтезируются как часть больших молекул, названных предпрогормонами. Они расщепляются в нейрональной цитоплазме на прогормоны, которые затем собираются в пузырьки. В пределах пузырьков прогормоны далее расщепляются на нейроактивные пептиды. Большинство пептидных нейромедиаторов сосуществует с другими нейромедиаторами.
Считают, что опиоиды регулируют стресс, боль и настроение
Три эндогенные опиоидные группы, т.е. эндорфины, энкефалины и динорфины (см. табл. 8.10), синтезируются из больших молекул-предшественников. Эндорфин обнаружен в норадренергических и серотонинергических нейронах. Опиоиды действуют на три типа рецепторов:
- μ-рецепторы; эффект опиоидов приводит к уменьшению образование цАМФ и увеличению проницаемости для К+;
- δ-рецепторы; эффекты опиоидов аналогичны подобным на μ-рецепторы;
- μ-рецепторы; эффекты опиоидов уменьшают проницаемость для К+.
Нейрогипофизарные нейроактивные пептиды вазопрессин и окситоцин могут быть вовлечены в регуляцию настроения
Два нейрогипофизарных гормона — вазопрессин и окситоцин — синтезируются в гипоталамусе и выделяются (секретируются) в заднюю долю гипофиза. Существуют три рецептора к вазопрессину, и его эффекты связаны с изменениями в фосфолипидах мембран или увеличением содержания цАМФ.
Тахикинины включают субстанцию Р и нейрокинин
Субстанция Р — первичный нейромедиатор в большинстве первичных афферентных чувствительных нейронов, присутствующий в нигростриарном тракте. Субстанция Р связана с АХ и 5-НТ и вовлечена в развитие хореи Хантингтона, болезни Альцгеймера и эмоциональных нарушений.
Холецистокинин может играть определенную роль в развитии шизофрении, панических расстройств, пищевых нарушений и некоторых расстройств движения
Холецистокинин (ХЦК) сосуществует в нейронах с дофамином и ГАМК. Он действует на два подтипа рецептора: ХЦКА и ХЦКВ. Подтип ХЦКА активирует эффект мембранных фосфолипидов. Механизмы сигнальной трансдукции ХЦКв-рецептора пока не выяснены.
Нейротензин может играть определенную роль в развитии шизофрении
Нейротензин сосуществует в нейронах с НЭ и дофамином. Нейротензин действует на G-белок, связанный с высокоаффинными рецепторами, находящимися в областях, богатых дофамином, и энтеро-обонятельной зоне коры, вовлеченных в развитие шизофрении.

Читайте также:
