Примеры внутриглазного абсцесса симулирующего ретинобластому
Добавил пользователь Валентин П. Обновлено: 28.01.2026
ФГБУ «Московский НИИ глазных болезней им. Гельмгольца» Минздрава России, Москва
ФГБУ "Московский НИИ глазных болезней им. Гельмгольца" Минздрава РФ
ФГБУ "Московский НИИ глазных болезней им. Гельмгольца" Минздрава России
ФГБУ "Московский НИИ глазных болезней им. Гельмгольца" Минздравсоцразвития России
Ретинобластома и "псевдоретинобластома" у детей: клинические, томографические и серологические особенности
Журнал: Вестник офтальмологии. 2014;130(1): 18‑24
Саакян С.В., Мякошина Е.Б., Кричевская Г.И., Слепова О.С. Ретинобластома и "псевдоретинобластома" у детей: клинические, томографические и серологические особенности. Вестник офтальмологии. 2014;130(1):18‑24.
Saakian SV, Miakoshina EB, Krichevskaia GI, Slepova OS. Retinoblastoma and "pseudoretinoblastoma" in children: clinical, tomographic and serological features. Vestnik Oftalmologii. 2014;130(1):18‑24. (In Russ.).
Определены клинические, томографические особенности и инфекционный статус, характерные для ретинобластомы и воспалительной гранулемы заднего полюса глаза ("псевдоретинобластомы"), у 16 детей (32 глаза), позволяющие провести дифференциальную диагностику между опухолевым и воспалительным процессом с проведением в дальнейшем адекватного лечения.
Ретинобластома (РБ) - злокачественная опухоль сетчатки у детей раннего возраста. В большинстве случаев диагностика РБ основана на визуализации определенных клинических признаков и результатах различных методов обследования: биомикроскопии, офтальмоскопии, ультразвуковой эхографии, оптической когерентной томографии (ОКТ), флюоресцентной ангиографии, компьютерной томографии, молекулярно-генетического анализа, тонкоигольной аспирационной биопсии, иммунологических исследований [1, 4-6, 16-18].
Однако в некоторых ситуациях атипичное клиническое течение может затруднить выявление злокачественной опухоли [5, 6, 11, 13, 14]. Существует ряд заболеваний глазного дна, симулирующих по своей клинической картине РБ, названных в современной мировой литературе «псевдоретинобластомами» [7-9, 20], частота встречаемости которых, по мнению разных авторов, варьирует от 42 до 53%.
Цель исследования - анализ дифференциально-диагностических особенностей клинической, томографической картины и инфекционного статуса детей с РБ и воспалительными гранулемами заднего отрезка глаза.
Материал и методы
Проанализированы результаты комплексного обследования (общеофтальмологического, офтальмоскопии с использованием непрямого офтальмоскопа и ретинальной педиатрической камеры Ret Cam, ультразвуковой эхографии на ультразвуковом сканере Е-100 фирмы «Topcon» (Япония), ОКТ 16 детей (19 глаз) в возрасте 4 до 74 (в среднем 38±1,2) мес с проминирующими очагами на глазном дне.
Пациенты разделены на две группы: 1-я - 7 больных (10 глаз) с диагнозом РБ, 2-я - 9 пациентов (9 глаз) с диагнозом воспалительная гранулема.
При офтальмоскопии оценивали цвет очага, локализацию, форму, границы, степень пигментации, характер поверхности, наличие локальных зон отложения пигмента, кальцификатов, отслойки сетчатки, шварт, кровоизлияний.
ОКТ проводили на спектральном оптическом когерентном томографе (SOCT Copernicus HR фирмы «Optopol Technology S.A.», Польша). Обследование выполняли с использованием программы 3D-сканирования.
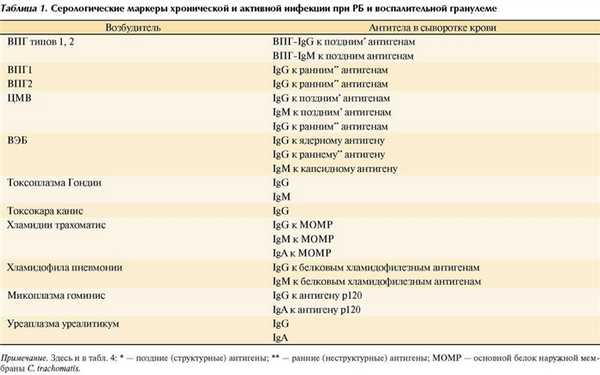
Для определения инфекционного статуса всех больных обследовали на широкий спектр офтальмотропных возбудителей. В сыворотке крови определяли наличие маркеров хронической и активной фазы инфекций. Наличие инфицированности и фазу инфекции диагностировали по характеру серологического ответа, учитывали антигенную специфичность антител и класс иммуноглобулинов (IgM, IgG, IgA), к которому они относятся (табл. 1).
IgM-антитела к структурным антигенам ряда возбудителей, IgG-антитела к неструктурным (ранним) антигенам герпесвирусов рассматривали как маркеры активной инфекции (первичной или реактивации хронической). Антитела определяли в твердофазном иммуноферментном анализе (ИФА) на автоматическом ИФА-анализаторе Лазурит (США) с диагностическими наборами ЗАО «Вектор-Бест» (Кольцово).
Результаты и обсуждение
В 1-й группе у 3 (6 глаз) из 7 больных диагностировали бинокулярную, у 4 (4 глаза) - монокулярную форму РБ с экзофитным солитарным характером роста.
Офтальмоскопически в 2 глазах в стадии А (по международной АВС-классификации, 2001 г.) определяли проминирующий беспигментный узел серо-белого цвета с неровными, нечеткими границами, с гладкой поверхностью (табл. 2). Сосуды сетчатки дифференцированы (рис. 1). Рисунок 1. Рис. 1. Офтальмоскопия экзофитной РБ. Стадия А Эхографически проминенция опухоли составила: 2,3 мм - один глаз и
0,8 мм - второй глаз, диаметр основания: 5,0 мм - в первом случае и 3,0 мм - во втором.
ОКТ при начальной стадии РБ показала наличие признаков, характерных для экзофитного роста опухоли: отграниченной гиперрефлективной гомогенной ткани на уровне наружных слоев сетчатки, истончения внутренних слоев сетчатки над новообразованием при относительной сохранности их дифференцировки и элевации в стекловидное тело, отслойки нейроэпителия в сопредельных с опухолью зонах, ровного хориоидального профиля (рис. 2; табл. 3). Рисунок 2. Рис. 2. Оптическая когерентная томограмма экзофитной формы РБ. Стадия А. Объяснения в тексте.
Данные об использовании ОКТ в диагностике сетчатки при РБ впервые приведены C. Shields и соавт. [17], которые обследовали только макулярную зону 10 глаз с РБ и выявили отслойку задней гиалоидной мембраны, ретинальный отек, субфовеолярное скопление жидкости. Исследование самой опухоли с дифференцировкой ее роста, характерными томографическими признаками впервые проведено авторами данной статьи. При диагностике начальной РБ у значительного числа больных выявлены томографические признаки, характерные для различных форм РБ на ранних этапах ее развития (при эндофитной форме опухоль манифестирует во внутренних слоях сетчатки, формируя гомогенный узел, при экзофитной - в наружных ретинальных отделах с первыми признаками отслойки нейроэпителия в сопредельной зоне и компрессионным истончением прилежащей сетчатки) [4].
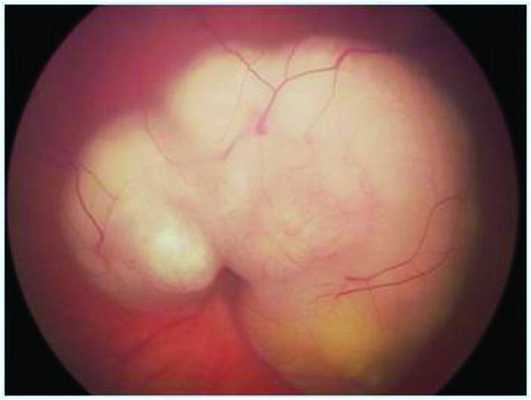
В стадии С опухолевого процесса (1 глаз) определяли притуморальную отслойку сетчатки и беспигментный опухолевый узел серо-белого цвета с неровными, нечеткими границами, гладкой поверхностью и наличием единичных кальцинатов (рис. 3). Рисунок 3. Рис. 3. Офтальмоскопия экзофитной РБ. Стадия С. При ультразвуковом исследовании элевация очага составила 4,3 мм, диаметр основания - 12,0 мм.
Стадию Е РБ диагностировали в 7 глазах. В 6 из них 2/3 глазного яблока было заполнено опухолевой тканью серовато-беловатого цвета, над которой дифференцировали отслойку сетчатки (рис. 4). Рисунок 4. Рис. 4. Офтальмоскопия экзофитной РБ. Группа Е. У 1 ребенка при офтальмоскопии на глазном дне выявили папиллярный очаг, распространяющийся в нижние отделы глазного дна, на поверхности которого наблюдались мелкие кровоизлияния, а в строме - единичные кальцинаты (рис. 5). Рисунок 5. Рис. 5. Офтальмоскопия эндофитной РБ. Группа Е. Проминенция опухоли в среднем составила 10,6±2,7 мм, диаметр основания - 18,0±1,3 мм. Неоваскуляризация радужки и опухолевые клоны в стекловидном теле выявлены в 2 из 7 глаз, а вторичную гипертензию в 7 глазах, в связи с чем все 7 глаз были энуклеированы. Гистологически подтверждена недифференцированная форма РБ.
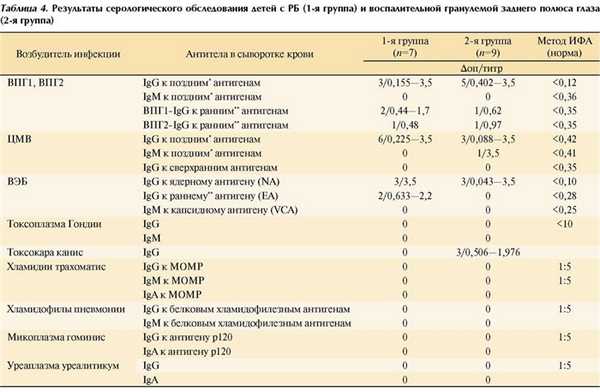
Инфекционный статус в 1-й группе имел следующие особенности (табл. 4) : у 6 детей выявлены IgG-антитела к структурным антигенам цитомегаловируса (ЦМВ) в разных уровнях (0,225-3,5 Δоп), что свидетельствовало о перенесенной или хронической инфекции.
Инфицированность вирусом простого герпеса (ВПГ) отмечена у 2 из 7 больных: у одного выявлены антитела - маркеры активности ВПГ1-инфекции (0,44 Δоп) и ВПГ2-инфекции (0,48 Δоп), у другого - только ВПГ1-инфекции (1,7 Δоп).
Серопозитивны к вирусу Эпштейна-Барр (ВЭБ) оказались 3 детей (высокий уровень Ig-антител к ядерному антигену - выше 3,5 Δоп), у 2 из них одновременно определены антитела к раннему ВЭБ (умеренный (0,633 Δоп) и высокий (2,2 Δоп уровень), что свидетельствовало об активности инфекции (атипичной реактивации или ранней паст-инфекции ВЭБ).
Отмечено и сочетанное вирусное поражение детей с РБ, когда в сыворотке крови выявляли два возбудителя и более: у одного ребенка выявлены ВПГ, ЦМВ и ВЭБ, у другого - ВПГ и ЦМВ, у третьего - ВПГ- и ВЭБ-антитела.
Антитела к остальным исследуемым возбудителям у детей с РБ не обнаружены.
Онкогенное действие вирусов предполагали давно, однако только в последние годы получены прямые доказательства этиологической роли некоторых из них в генезе опухолей разной локализации. Среди возможных механизмов онкогенного действия вирусов выделяют нарушение клеточного цикла, ингибирование апоптоза [10, 15, 19].
Развитие ВЭБ-ассоциированной карциномы желудка связывают с супрессивным влиянием вируса на белок РБ. Последний играет важную регуляторную роль в клеточном росте и дифференцировке, его подавление - существенный, хотя и не единственный фактор в развитии опухоли. Нарушение в транскрипции или экспрессии этого белка тесно коррелирует с возникновением и развитием опухоли желудка [19].
Риск развития РБ у детей с мутацией в гене RB1 повышается более чем на 90%. В последние годы высказана гипотеза о роли онкопротеина вируса папилломы человека Е7 в инактивации белка РБ и развитии спонтанной односторонней РБ [15]. Известна роль ВЭБ в этиопатогенезе ряда лимфом, саркомы Капоши [10], однако связь ВЭБ-инфекции с развитием спонтанной РБ требует дальнейшего изучения.
Во 2-й группе (больные с воспалительной гранулемой заднего отрезка глаза) при офтальмоскопии у девяти больных выявлены проминирующие субретинальные узлы макулярной (4) и парамакулярной (5) локализации беловато-сероватого цвета с неровными нечеткими контурами и бугристой поверхностью. Кроме того, диагностированы отслойка сетчатки и шварты, распространяющиеся от диска зрительного нерва к задней гиалоидной мембране стекловидного тела и проминирующему очагу. В стекловидном теле визуализированы фиброзные тяжи (рис. 6, а, б). Рисунок 6. Рис. 6а. Воспалительная гранулема заднего полюса глаза токсокарозной этиологии. Рисунок 6. Рис. 6б. Воспалительная гранулема заднего полюса глаза цитомегаловирусной этиологии.
Указанная клиническая картина отличалась от таковой при РБ наличием шварт, фиброзных тяжей в сторону стекловидного тела, бугристой поверхностью и серым цветом. Эхографические параметры гранулем составили в среднем 2,4±0,7 мм, диаметр основания - 7,9±1,7 мм.
По мнению C. Shields [18], при офтальмоскопии токсокарозная гранулема выглядит как проминирующий субретинальный беловатый очаг в заднем полюсе глаза и сходный с экзофитной формой РБ; но отличительной особенностью такой формы воспаления сетчатки являются шварты от патологического очага к диску зрительного нерва; для ЦМВ-ретинита характерно наличие кровоизлияний, что согласуется с полученными нами результатами. Кроме того, отсутствие кальцификатов при воспалительном ретините является также отличительной особенностью последнего в сравнении с РБ.
По данным литературы [2, 3], для воспалительных внутриглазных гранулем характерно наличие проминирующего внутриглазного очага с кровоизлияниями, отслойкой сетчатки, швартами и тяжами к диску зрительного нерва при цитомегаловирусном заднем увеите и макулярного фокуса с темно-серым центром, связанным с диском зрительного нерва преретинальным тяжем, при токсокарозной гранулеме. Ранее установлено, что клинически экзофитная форма РБ представляет собой серовато-беловатый узел с гладкой поверхностью и притуморальной отслойкой сетчатки без шварт и тяжей к диску зрительного нерва [6], что отличало злокачественную опухоль от воспалительного процесса при офтальмоскопии.
При ОКТ у больных 2-й группы выявлен ретинальный патологический очаг, локализующийся во внутренних слоях сетчатки с плотными гиперрефлективными включениями без эффекта «тени», ровным хориоидальным профилем, швартами, распространяющимися в стекловидное тело (рис. 7, а, б). Рисунок 7. Рис. 7а. Оптическая когерентная томограмма воспалительной гранулемы заднего полюса глаза токсокарозной этиологии. Рисунок 7. Рис. 7б. Оптическая когерентная томограмма воспалительной гранулемы заднего полюса глаза цитомегаловирусной этиологии. при ОКТ гранулемы отличались от экзофитной формы РБ гетерогенностью структуры с отсутствием эффекта «тени», указывающего на кальцинаты, наличием шварт.
В литературе имеются сведения о томографических изменениях в сетчатке при задних увеитах разной этиологии. Так, в макулярной зоне отмечали кистовидный ретинальный отек; при мультифокальном ЦМВ-ретините - мелкофокусные гиперрефлективные изменения в слое ретинального пигментного эпителия; при старых ретинитах - гиперрефлективность сетчатки, а при свежих воспалениях сетчатки - ее отек [12]. Однако до настоящего времени сравнение томографических признаков РБ и воспалительной гранулемы заднего полюса глаза у детей не проводили.
В результате анализа инфекционного статуса у больных 2-й группы выявлена инфицированность ВПГ с высоким уровнем IgG-антител к структурным антигенам (выше 3,5 Δоп) у 5 из 9 детей, что свидетельствовало об установившейся хронической ВПГ-инфекции (ВПГИ). Реактивация ВПГИ обнаружена у двух детей: низкие показатели активности ВПГ1-инфекции (0,62 Δоп) выявлены у ребенка с последствием перенесенного одностороннего нейрохориоретинита, умеренные показатели активности ВПГ2-инфекции (0,97 Δоп) - у ребенка с частичной атрофией зрительного нерва правого глаза и увеитом неясной этиологии левого глаза (см. табл. 2).
При сравнении зараженности ВПГ больных с опухолью и воспалением можно отметить, что количество инфицированных детей во 2-й группе превышает таковое в 1-й, однако активация ВПГ сравнима в обеих группах.
Антитела ЦМВ IgM в отличие от IgG-антител не передаются трансплацентарно, поэтому их наличие в крови подтверждает факт активной первичной инфекции у ребенка. Низкие уровни IgG-антител к структурным антигенам свидетельствуют против их материнского происхождения и отражают характерную динамику синтеза IgG и IgM-антител при первичной ЦМВ-инфекции.
Зараженность токсокарой обнаружена у 3 из 9 детей с максимальным титром 1,976 Δоп (см. табл. 2), тогда как в 1-й группе зараженность токсокарой не выявлена.
Ни в одном случае не выявлены маркеры активности ВЭБ, токсоплазмы и других инфекций при воспалительных гранулемах. При РБ диагностировали значительную инфицированность онкогенным вирусом ВЭБ.
Иммунологические исследования по дифференциальной диагностике РБ и ретинита Коатса показали высокий уровень эритропоэтина (до 90% при стадии Т3) в сыворотке крови у больных с опухолью и отсутствие цитокина при ретините Коатса и у здоровых детей [6], что позволило провести дифференциальную диагностику опухолевого и псевдотуморозного процесса. Однако до настоящего времени сравнительный анализ инфекционного статуса у детей с РБ и воспалительной гранулемой заднего полюса глаза не проводили.
Таким образом, диагностика некоторых заболеваний глазного дна, по клинической картине сходных с РБ и названных в литературе «псевдоретинобластомами», в некоторых случаях вызывает трудности. Зачастую воспалительные гранулемы заднего полюса глаза симулируют злокачественную опухоль у детей [1, 5, 6, 11, 13, 14, 17, 18].
Полученные нами результаты обследования детей с РБ и воспалительными гранулемами заднего полюса глаза показали значимость комплексного подхода к диагностике внутриглазных новообразований с тщательным исследованием клинической картины, проведением ОКТ и исследованием инфекционного статуса.
Выводы
1. Офтальмоскопическая картина «псевдоретинобластомы» (воспалительной гранулемы заднего полюса глаза) отличается от таковой РБ наличием кровоизлияний и шварт от очага к диску зрительного нерва.
2. ОКТ позволяет выявить отличительные признаки экзофитой формы РБ (отграниченная гиперрефлективная гомогенная ткань на уровне наружных слоев сетчатки с отслойкой нейроэпителия в сопредельных зонах) и воспалительной гранулемы (ретинальный патологический очаг во внутренних слоях сетчатки с плотными гиперрефлективными включениями, швартами в стекловидное тело).
3. В развитии воспалительных заболеваний заднего отрезка глаза, протекающих по типу «псевдоопухолей», важную роль играет токсокара канис, а у детей до года - внутриутробные герпес-вирусные инфекции, не выявляемые у больных с РБ.
4. Распространенность ВПГ, ЦМВ и ВЭБ не различалась в обеих группах. Активность онкогенного ВЭБ выявлена только у трети детей с РБ.
Эндофтальмит
Эндофтальмит - это абсцедирующее воспаление внутренних структур глаза, приводящее к скоплению гнойного экссудата в стекловидном теле. При эндофтальмите отмечаются боли в глазном яблоке, отек и покраснение век и конъюнктивы, значительное понижение остроты зрения, гипопион. В диагностике эндофтальмита используется визометрия, исследование полей зрения, биомикроскопия глаза, диафаноскопия, офтальмоскопия, электроретинография, УЗИ глаза. Комплексное лечение эндофтальмита включает антибиотикотерапию, дезинтоксикационную, противовоспалительную, рассасывающую терапию; интравитреальные, парабульбарные или субконъюнктивальные инъекции, парацентез и промывание передней камеры; при тяжелом течении эндофтальмита - витрэктомию.
МКБ-10
Общие сведения
Гнойные воспаления тканей глазного яблока относятся к числу грозных состояний в офтальмологии, требующих оказания специализированной неотложной помощи. Гнойный процесс при эндофтальмите прогрессирует стремительно, иногда в течение нескольких часов приводя к развитию панофтальмита - тотального воспаления и расплавления всех оболочек глазного яблока и тканей орбиты. По различным данным, частота слепоты, функциональной и анатомической гибели глаза, приводящей к энуклеации, у пациентов с внутриглазной инфекцией достигает 28 - 89%. Данные обстоятельства ставят перед офтальмологами задачу своевременной профилактики, раннего выявления и адекватного лечения инфекций глазного яблока.
Причины эндофтальмита
Экзогенные причины
Экзогенные случаи инфицирования внутриглазных тканей преимущественно связаны со следующими факторами:
- проникающими ранениями глаз (95-97 %),
- операциями на глазном яблоке (2-4%),
- прободными гнойными язвами роговицы,
- инфицированными ожогами глаз.
В структуре механических повреждений глаз, сопровождающихся развитием эндофтальмита, преобладает детский травматизм (40 %), производственные (30%) и сельскохозяйственные (25-50%) травмы. Проникновение в глаз инородного тела значительно повышает риски возникновения эндофтальмита. Послеоперационный эндофтальмит чаще развивается вследствие экстракции катаракты с имплантацией заднекамерной ИОЛ.
При экзогенном инфицировании глаза выделяют первичную и вторичную микробную инвазию. В первом случае микробы попадают в глубокие структуры глаза в момент проникающего ранения или инвазивного вмешательства, а воспалительная реакция развивается уже в первые 2-3 суток. При вторичной микробной инвазии инфицирование развивается в поздние сроки вследствие неадекватной первичной обработки раны, ее зияния, размозжения краев и т. п.
Эндогенные причины
Эндогенный механизм развития эндофтальмита встречается в 1-2 % случаев и связан с гематогенным заносом микробных возбудителей в капилляры радужки и ресничного тела из отдаленных воспалительных очагов в организме при:
- фурункулах, абсцессах, флегмонах,
- синуситах, тонзиллите,
- пневмонии,
- остеомиелите,
- сепсисе,
- менингите,
- септическом эндокардите и др.
Возбудители экзогенного и эндогенного эндофтальмита многообразны. Наиболее часто при бактериологическом исследовании выявляются стафилококки, стрептококки, коринебактерии, протей, гемофильная палочка, синегнойная палочка, нейссерии, энтеробактерии, клебсиелла, пневмококки и различные полимикробные ассоциации. Опасную разновидность представляет грибковый эндофтальмит, который может вызываться более чем двадцатью разновидностями грибков (рода акремониум, кандида, аспергилл, цефалоспориум, нейроспора и др.).
Патогенез
Патогенез эндофтальмита при экзогенном инфицировании многоплановый. В случае нарушения целостности роговицы или склеры микроорганизмы проникают внутрь стекловидного тела, где беспрепятственно размножаются. Образуется внутриглазной очаг инфекции, который быстро распространяется на все оболочки глаза. В свою очередь, нарушение иммунологической изолированности глаза сопровождается аутоиммунной воспалительной реакцией, способствующей ослаблению сопротивляемости инфекции, и агрессивному течению эндофтальмита и панофтальмита.
Образующийся гнойный экссудат приводит к увеиту, расплавлению сосудистой и сетчатой оболочек, инкапсуляции с образованием шварт. Швартообразование в последующем вызывает тракции и отслойку сетчатки с исходом в гипотензию и атрофию глазного яблока.
Симптомы эндофтальмита
Эндофтальмит может протекать по типу отграниченного очага в глазу (абсцесса стекловидного тела) либо диффузного процесса; иногда встречается смешанная форма. По степени тяжести симптоматики выделяют легкую, среднюю и тяжелую степени эндофтальмита.
Экзогенный эндофтальмит развивается на 2-3 сутки после механического повреждения глаза. Прогрессирующее течение заболевания сопровождается болью в глазном яблоке, нарастающим снижением остроты зрения иногда до светоощущения, плавающими помутнениями в поле зрения. Внешние изменения глаза характеризуются умеренным отеком век и конъюнктивы, резкой смешанной инъекцией глазного яблока. Могут развиваться признаки иридоциклита. Характерной чертой эндофтальмита является формирование абсцесса в стекловидном теле, который просвечивает через зрачок желтоватым свечением.
Осложнения
При эндофтальмите тяжелой степени развивается выраженный хемоз, гипопион и гноетечение. Эндогенные эндофтальмиты, протекающие на фоне иммунодефицита или интоксикации, могут носить двусторонний характер. Прогрессирование эндофтальмита приводит к переходу в панофтальмит, что угрожает анатомической и функциональной гибелью глаза, риском развития менингита.
Диагностика
Комплексное офтальмологическое обследование при эндофтальмите позволяет оценить тяжесть процесса и выработать лечебную тактику. При подозрении на эндофтальмит проводится:
- Визометрия. Типичная офтальмологическая картина при эндоофтальмите характеризуется снижением остроты зрения: при легкой степени - частичным, при средней - выраженным, при тяжелой - значительным снижением или отсутствием зрения.
- Исследование полей зрения. Поле зрения сужено или отсутствует.
- Биомикроскопия. Проведение биомикроскопии выявляет смешанную инъекцию глазного яблока, наличие преципитатов на поверхности роговицы, гипопиона, гиперемию и инфильтрацию радужки, образование задних синехий
- Диафаноскопия глаза. Диафаноскопия глаза в проходящем свете позволяет обнаружить желтовато-серый зрачковый рефлекс, свидетельствующий об образовании абсцесса в стекловидном теле. При обратном развитии эндофтальмита ввиду формирования на месте гнойника соединительной ткани рефлекс приобретает молочно-белый оттенок.
- Офтальмоскопия. Проведение прямой и обратной офтальмоскопии при эндофтальмите затруднено и частично возможно только при легкой степени тяжести заболевания.
- Измерение ВГД. Внутриглазное давление при эндофтальмите обычно снижено.
- УЗИ глаза. Выявляет ограниченные или тотальные помутнения в стекловидном теле. Для верификации возбудителя проводится посев культуры из стекловидного тела и водянистой влаги.
- Элекрофизиологические исследования. Показатели электроретинографии могут соответствовать или быть близкими к норме (при очаговом эндофтальмите), значительно снижаться вплоть до исчезновения (при диффузном или смешанном эндофтальмите).
Последствия эндофтальмита у детей необходимо дифференцировать от злокачественной опухоли сетчатки - ретинобластомы.
Лечение эндофтальмита
Лечение эндофтальмита проводится в условиях отделения хирургической офтальмологии. Сразу же после установления диагноза назначается:
- Системная терапия: ударные дозы антибиотиков широкого спектра действия, сульфаниламиды, антимикотические средства, противовоспалительные препараты (НПВП, кортикостероиды), мощная дезинтоксикационная терапия, общеукрепляющая терапия (витаминотерапия, аутогемотерапия), рассасывающая терапия (ферменты).
- Внутриглазные инъекции. Для достижения максимальной концентрации антибактериальных препаратов внутри глаза проводится их внутривенное, внутримышечное, субконъюнктивальное, ретробульбарное, парабульбарное, супрахориоидальное, интравитреальное введение. Одновременно назначаются инстилляции противомикробных глазных капель и аппликации мазей.
- Пункция стекловидного тела. При витреите или гипопионе производится лечебно-диагностическая пункция стекловидного тела с забором экссудата для бактериального посева и введением антибиотика в стекловидное тело. При эндофтальмите возможно проведение внутриартериальной офтальмоперфузии лекарственных препаратов через надглазничную артерию. Для лечения эндофтальмита используются цефалоспорины, гликопептиды, пенициллины, аминогликозиды, фторхинолоны, макролиды и др.
При неэффективности интенсивной консервативной терапии эндофтальмита возникает необходимость хирургического удаления части стекловидного тела - витрэктомии. В послеоперационном периоде антибиотикотерапия должна быть продолжена.
Прогноз и профилактика
Своевременное комплексное лечение эндофтальмита, начатое в легкой стадии, позволяет сохранить зрительные функции. В более поздних стадиях зачастую удается сохранить глаз как анатомический орган, но спасти зрение практически невозможно. Исходом эндофтальмита чаще всего является субатрофия и атрофия глазного яблока. При прогрессировании эндофтальмита в панофтальмит приходится прибегать к энуклеации глазного яблока.
Профилактика экзогенного инфекционного эндофтальмита требует предупреждения травм глаза, проведения адекватной ПХО раны при проникающих ранениях, своевременного удаления инородных тел конъюнктивы и роговицы, грамотного проведения операций на структурах глаза. Для исключения развития эндогенного эндофтальмита необходима санация фокальных гнойных очагов и лечение общих септических состояний.
Ретинобластома
Ретинобластома - злокачественное внутриглазное новообразование, развивающееся из нейроэктодермы сетчатки и встречающееся преимущественно у детей раннего возраста. Для клиники ретинобластомы характерна потеря центрального и бинокулярного зрения, боль, лейкокория, развитие косоглазия, экзофтальма, вторичного воспаления и глаукомы. Обследование при подозрении на ретинобластому включает исследование зрения, измерение внутриглазного давления, осмотр глазного дна, проведение УЗИ глаза, рентгенографии орбиты и придаточных пазух носа, КТ головного мозга, люмбальной пункции. Пациентам с ретинобластомой выполняется фотокоагуляция, криотерапия опухоли; при невозможности сохранения органа зрения - энуклеация пораженного глаза с последующим глазопротезированием.
Ретинобластома - злокачественное новообразование детского возраста, поражающее сетчатку, сосудистую оболочку глаза, орбиту и часто дающее отдаленные метастазы. На долю ретинобластомы приходится 2,5-4,5% случаев всех злокачественных новообразований у детей до 15 лет. В большинстве случаев ретинобластома развивается в возрасте до 5 лет, пик заболеваемости приходится на 2-3 года. В офтальмологии опухоль с одинаковой частотой встречается у девочек и мальчиков.
Причины ретинобластомы
В 50-60% случаев ретинобластомы имеют генетическое (врожденное) происхождение. Более половины детей с ретинобластомой рождается от родителей, имевших в детстве аналогичное заболевание. Врожденная ретинобластома обычно выявляется у детей в возрасте до 30 месяцев. В этом случае ретинобластома, как правило, сочетается с другими врожденными аномалиями - пороками сердца, расщелинами неба («волчьей пастью»), кортикальным детским гиперостозом и др. У больных с генетической формой ретинобластомы имеется повышенный риск развития злокачественных новообразований другой локализации.
Спорадические случаи ретинобластомы встречаются реже и возникают по неизвестным причинам. К числу факторов риска негенетической формы ретинобластомы принято относить высокий возраст родителей, их занятость на металлургических производствах, неблагоприятные экологические и алиментарные факторы, вызывающие аберрации в хромосомах ретинальных и половых клеток. Данная форма опухоли проявляется у детей более старшего возраста и крайне редко - у взрослых.
Современные воззрения на гистогенез ретинобластомы позволяют ее отнести к опухолям нейроэктодермального происхождения. Ретинобластома может исходить из клеток любого ядерного (зернистого) слоя сетчатки. При микроскопическом исследовании определяются отсутствие стромы, очаги некроза и кальцификаты, разная степень дифференцировки опухолевых клеток.
Для ретинобластомы характерен быстрый рост, метастазирование по зрительному нерву в головной мозг, а также гематогенное распространение в костный мозг и трубчатые кости.
Классификация ретинобластомы
По происхождению ретинобластомы делятся на наследственные и спорадические. Наследственные ретинобластомы обычно поражают одновременно оба глаза. Спорадические ретинобластомы, как правило, поражают один глаз и развиваются локально, с образованием единичного (унилатерального) опухолевого узла.
По степени дифференцировки опухолевых клеток различают дифференцированную форму опухоли - ретиноцитому и недифференцированную форму - ретинобластому, которая встречается чаще и является более злокачественной.
Ретинобластома может иметь эндофитный тип роста в направлении центра глазного яблока: при этом происходит разрушение слоев сетчатки и стекловидного тела. При другом варианте роста - экзофитном, ретинобластома инфильтрирует сетчатку, распространяясь в субретинальное пространство. Экзофитные опухоли могут вызывать отслойку сетчатки и скопление транссудата в субретинальном пространстве. В редких случаях (1-2%) встречается инфильтративная форма ретинобластомы, которая ведет к диффузному истончению сетчатки, накоплению экссудата в передних отделах глаза, развитию передних спаек и псевдогипопиона.
Согласно клинической классификации ретинобластомы по системе TNM, выделяют степени развития первичной опухоли:
- Т1 - ретинобластома занимает до 25% глазного дна
- Т2 - ретинобластома распространяется на площадь более 25%, но менее 50% поверхности сетчатки
- ТЗ - ретинобластома распространяется более чем на половину сетчатки или выходит за ее пределы, но сохраняет интраокулярное расположение
- Т4 - ретинобластома выходит за пределы орбиты.
- N1 - имеются метастазы в регионарных (околоушных, подчелюстных, шейных) лимфоузлах.
- Ml - определяются отдаленные метастазы ретинобластомы в головном мозге, костном мозге, костях, печени и др. органах.
Симптомы ретинобластомы
В клиническом течении ретинобластомы различают четыре последовательные стадии.
I - стадия покоя. В этом периоде субъективные симптомы отсутствуют. При осмотре пораженного глаза выявляется лейкокория (симптом «кошачьего глаза») - белый зрачковый рефлекс, обусловленный просвечиванием опухолевой массы через зрачок. К ранним признакам ретинобластомы относят потерю центрального и бинокулярного зрения, вследствие чего может развиваться косоглазие.
II - стадия глаукомы. Сопровождается воспалительными явлениями в глазу - гиперемией, светобоязнью, слезотечением, развитием иридоциклита и увеита. На фоне опухолевой инвазии отмечается локальный болевой синдром. Разрушение ретинобластомой трабекулярного аппарата приводит к затруднению оттока ВГЖ, увеличению внутриглазного давления и возникновению вторичной глаукомы.
III - стадия прорастания. Характеризуется развитием экзофтальма различной степени выраженности, инвазией мягких тканей орбиты и разрушением ее стенок, прорастанием ретинобластомы в придаточные пазухи и субарахноидальное пространство.
IV - стадия метастазирования. Протекает с выявлением отдаленных диссеминированных очагов в костном мозге, печени, трубчатых костях, головном мозге, костях черепа. Распространение ретинобластомы происходит по мягкой мозговой оболочке, зрительному нерву, лимфогенным и гематогенным путем. На этой стадии страдает общее состояние пациента: развивается интоксикация, слабость, мозговые симптомы (тошнота, рвота, головная боль).
Диагностика ретинобластомы
Дети с семейным анамнезом ретинобластомы должны находиться под постоянным наблюдением офтальмолога. На развитие ретинобластомы обычно указывает триада симптомов: лейкокория, косоглазие, расширение зрачка с ослаблением его реакции на свет. При появлении данных признаков проводится тщательное офтальмологическое обследование ребенка, включающее биомикроскопию, прямую и обратную офтальмоскопию, визометрию, тонометрию, гониоскопию, исследование бинокулярного зрения, экзофтальмометрию, измерение угла косоглазия. При помутнении оптических сред важная роль в выявлении ретинобластомы принадлежит УЗИ глаза.
Интраокулярная биопсия может привести к диссеминации злокачественных клеток внутри глаза, поэтому к ее проведению прибегают только при наличии абсолютных показаний. Для оценки распространенности ретинобластомы используются рентгенография орбиты, рентгенография околоносовых пазух, КТ и МРТ головного мозга, сцинтиграфия печени, остеосцинтиграфия. Для оценки возможного отдаленного метастазирования прибегают к выполнению люмбальной пункции с исследованием цереброспинальной жидкости; пункции костного мозга и исследованию миелограммы.
В процессе диагностики ретинобластому следует дифференцировать от рубцовой ретинопатии, дисплазии сетчатки, гамартом, мягкотканных сарком, метастазов нейробластомы, поражений орбиты при лимфоме и лейкемии.
Дети с ретинобластомой должны быть проконсультированы неврологом и отоларингологом.
Лечение ретинобластомы
Лечение ретинобластомы проводится с учетом стадии опухолевого поражения. При этом может использоваться хирургическое вмешательство, лучевая и лекарственная химиотерапия, лазеркоагуляция, криотерапия, термотерапия. Правильное сочетание этих методов во многих случаях позволяет сохранить глаз и зрение. В случает двусторонней ретинобластомы, в отношении каждого глаза определяется дифференцированная тактика в зависимости от степени его поражения опухолью.
В настоящее время офтальмохирурги и офтальмоонкологи стремятся придерживаться максимально консервативного ведения ретинобластомы. При поражениях переднего участка сетчатки и диаметре опухоли до 7 мм прибегают к криодеструкции ретинобластомы; при поражении задних отделов и размерах опухоли до 4 мм показана фотокоагуляция. Возможно проведение термотерапии - комплексного воздействия на опухоль с помощью микроволновой терапии, ультразвукового и инфракрасного излучения.
При массивном внутриглазном поражении, развитии глаукомы, утрате и невозможности восстановления зрения прибегают к энуклеации глаза с последующим глазопротезированием. При экстраокулярном распространении ретинобластомы показана экзентерация глазницы.
Ретинобластома чрезвычайно чувствительна к лучевому лечению. Лучевая терапия при ретинобластоме позволяет добиться хороших результатов в сочетании с органосохраняющими и хирургическими методами лечения. При этом возможно как наружное дистанционное, так и контактное облучение с помощью аппликаций радиоактивных веществ. Осложнением лучевой терапии может являться развитие постлучевой катаракты, лучевого кератита, ксероза.
Химиотерапия в лечении ретинобластомы используется при массивном внутриглазном поражении, опухолевой инвазии зрительного нерва, региональных метастазах. Наиболее эффективным признано сочетание нескольких цитостатиков (винкристина, этопозида, карбоплатина).
Прогноз и профилактика ретинобластомы
При своевременной диагностике и выявлении ретинобластомы на ранней стадии возможно стойкое излечение пациента с помощью органосохраняющих методов - фотокоагуляции, криотерапии, лучевой терапии. При энуклеации глаза также наблюдается высокая выживаемость, однако данная операция сопровождается потерей глаза как органа зрения и образованием косметического дефекта. Факторами неблагоприятного прогноза ретинобластомы служат прорастание опухоли в зрительный нерв, инвазия хориоидальной оболочки, экстрасклеральное распространение опухоли, двустороннее поражение.
Для профилактики ретинобластомы необходимо медико-генетическое консультирование семей с наследственными случаями рака сетчатки, обследование детей раннего возраста из групп риска.
Панофтальмит
Панофтальмит - тотальное гнойное воспаление и расплавление всех структур и оболочек глазного яблока. При панофтальмите возникает резкая боль в глазнице и в голове на стороне поражения, слезотечение, светобоязнь, отек и хемоз конъюнктивы, блефароспазм, озноб, лихорадка, падение зрения. Диагностика панофтальмита основана на данных диафаноскопии, биомикроскопии, офтальмоскопии, УЗИ глаза, бактериологического посева. Лечение панофтальмита требует проведения активной местной и системной антибиотикотерапии; в некоторых случаях - эвисцерации или энуклеации глазного яблока.
Панофтальмит является крайней и наиболее тяжелой формой воспаления органа зрения, при которой в гнойный процесс вовлекаются все оболочки глаза и окружающие мягкие ткани (веки, клетчатка, мышцы). Серьезность проблемы заключается в том, что панофтальмит нередко приводит к гибели и последующей атрофии глаза. Защитные механизмы концентрируются в придаточном аппарате глаза (веках, слезных железах), поэтому проникновение инфекции внутрь глазного яблока сопровождается бурным и беспрепятственным размножением микроорганизмов. В итоге, при панофтальмите гнойному воспалению и расплавлению подвергаются все слои глазного яблока.
Причины панофтальмита
Панофтальмит может быть обусловлен экзогенным или эндогенным проникновением инфекции внутрь глазного яблока. При этом возбудителями обычно выступают стрептококки, стафилококки, пневмококки, синегнойная и кишечная палочки, микобактерии туберкулеза.
В офтальмологии к панофтальмиту чаще всего приводят проникающие ранения глаза (механические повреждения, инородные тела, ожоги). В этом случае гнойная инфекция проникает вглубь глазного яблока через раневой канал. Также панофтальмит может являться следствием бактериального кератита, прободения гнойной язвы роговицы, тяжелого течения увеита, бленнореи, трахомы, абсцесса век, флегмоны глазницы, эндофтальмита.
Эндогенное инфицирование структур глаза встречается реже и может быть связано с метастатическим заносом бактериальной инфекции из отдаленных гнойных очагов. Возникновение панофтальмита возможно вследствие пневмонии, туберкулеза, фурункулеза, послеоперационного или послеродового сепсиса, менингита, тифа, синуситов.
Симптомы панофтальмита
При проникающих ранениях глазного яблока панофтальмит развивается стремительно, в течение 2-3 дней. Гнойное поражение структур глаза сопровождается сильными болями в глазном яблоке, слезотечением, светобоязнью, рефлекторным блефароспазмом, быстрым и значительным снижением зрения. Объективные изменения характеризуются резкой гиперемией, отеком конъюнктивы и век, который может приводить к хемозу - ущемлению веками слизистой глаза. Роговица становится мутной и отечной; радужка расплавляется; в передней камере глаза скапливается гной; гнойный экссудат также обнаруживается в стекловидном теле. При панофтальмите происходит быстрое и существенное снижение зрения вплоть до светоощущения или слепоты.
При дальнейшем прогрессировании панофтальмита гной проникает под конъюнктиву, инфильтрирует перибульбарные ткани, распространяется в тенонову капсулу, усиливая отек тканей и приводя к развитию воспалительного экзофтальма. Подвижность глазного яблока резко ограничивается. Может произойти перфорация склеры с выделением гноя наружу. В дальнейшем, через 6-8 недель, глаз сморщивается и атрофируется.
При анаэробном панофтальмите гнойный процесс развивается бурно: из передней камеры появляется отделяемое кофейного цвета с пузырьками газа, слепота наступает уже в день ранения глаза.
Кроме местных изменений, панофтальмит сопровождается общими симптомами: явлениями интоксикации, головной болью, лихорадочным состоянием с ознобом, рвотой. Гнойные процесс может перейти на мозговые оболочки с развитием менингита, формированием абсцесса головного мозга.
Диагностика панофтальмита
Для диагностики панфотальмита первостепенное значение имеет наличие в анамнезе проникающих ранений глаза и инфекционных очагов в организме.
Объективные признаки панофтальмита (изменения конъюнктивы, радужки, скопление гнойного экссудата в передней камере глаза и стекловидном теле) обнаруживаются офтальмологом при осмотре структур глаза (диафаноскопии, биомикроскопии). При возможности осмотра глазного дна с помощью офтальмоскопии определяются расширенные вены сетчатки. УЗИ-сканирование позволяет выявить очаги деструкции глубоких структур глаза.
Для определения микробной флоры, вызвавшей развитие панофтальмита, проводится парацентез роговицы для получения гнойного экссудата и его бактериологического посева.
Дифференциальная диагностика панофтальмита проводится с эндофтальмитом, который протекает не так бурно.
Лечение панофтальмита
Панофтальмит требует раннего и интенсивного лечения. Основу патогенетической терапии панофтальмита составляет назначение массивных доз антибиотиков (бензилпенициллина, стрептомицина, мономицина, гентамицина и др.). Антибиотики вводятся внутримышечно, внутривенно, в виде ретробульбарных, субконъюнктивальных инъекций. В ряде случаев прибегают к витрэктомии и интравитреальному введению противомикробных средств. Показаны инстилляции и ванночки с раствором трипсина. Для устранения явлений общей интоксикации проводятся внутривенные инфузии солевых растворов.
Консервативное лечение панофтальмита не всегда бывает успешным, поэтому нередко приходится прибегать к эвисцерации или энуклеации глазного яблока с последующим глазопротезированием.
Прогноз и профилактика панофтальмита
При своевременно начатом комплексном лечении панофтальмита в ряде случаев удается сохранить глазное яблоко и остаточное зрение. Чаще всего исходом панофтальмита служит гибель глаза с его последующей атрофией. Прогноз для зрительной функции и жизни при панофтальмите всегда крайне серьезный.
Основная роль в профилактике панофтальмита принадлежит предупреждению травм глаза, санации инфекционных очагов в организме, лечению воспалений структур глаза и его придаточного аппарата. В случае ранений глаза необходимо проведение превентивной местной и общей антибиотикотерапии уже в первые часы после травмы.
Примеры внутриглазного абсцесса симулирующего ретинобластому
ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России, Москва, Россия
ФГБУ «Московский НИИ глазных болезней им. Гельмгольца» Минздрава России, ул. Садовая-Черногрязская, 14/19, Москва, 105062, Российская Федерация
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» РАМН, 115478 Москва, Каширское шоссе, д. 23
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» Минздрава России, Каширское ш., 23, Москва, 115478, Российская Федерация
. Злокачественная медуллоэпителиома, симулирующая ретинобластому — клинико-гистологический анализ случая и опыт получения клеточной культуры
Журнал: Вестник офтальмологии. 2016;132(6): 64‑69
В работе представлен клинико-морфологический анализ случая первичной внутриглазной злокачественной медуллоэпителиомы редкой локализации — центрального отдела сетчатки с вовлечением диска зрительного нерва, — симулирующей ретинобластому, у ребенка 2 лет. Подробно приведены гистологические особенности опухоли (трубчатые и сетчатые структуры опухоли, розетки, ленточные образования, клетки с гиперхромными ядрами, клеточный полиморфизм). Описан единственный на сегодняшний день в Российской Федерации опыт создания первичной культуры внутриглазной злокачественной медуллоэпителиомы с последующей оценкой чувствительности (МТТ-тест) к четырем препаратам (оксалиплатин, иринотекан, ифосфамид, аскорбиновая кислота) в различных концентрациях. Из четырех исследованных препаратов IC50 (3,3 мг/мл) получена только для раствора аскорбиновой кислоты. Несмотря на относительную редкость первичной внутриглазной злокачественной медуллоэпителиомы, необходимо проводить дифференциальный диагноз с другими внутриглазными образованиями, прежде всего ретинобластомой. Полученные данные об эффективности раствора аскорбиновой кислоты в отношении клеток внутриглазной злокачественной медуллоэпителиомы могут быть использованы для дополнения существующих химиотерапевтических протоколов в детской нейро- и офтальмоонкологии.
Внутриглазная медуллоэпителиома (диктиома) — редкая врожденная эмбриональная опухоль, растущая из эпителия цилиарного тела, ресничной части сетчатки и зрительного нерва, которая встречается как у взрослых, так и у детей [1, 2]. Опухоль состоит из тубулярных структур, выстланных псевдомногослойным нейроэпителием. Данная опухоль чаще всего выявляется в первой декаде жизни. Диагностика медуллоэпителиомы не всегда очевидна. Эхографическая локализация зачастую затруднена в связи с плоскостным характером роста, что объясняет позднюю (послеоперационную) диагностику [3].
В литературе за последние 30 лет доступны лишь 10 работ, посвященных первичной внутриглазной медуллоэпителиоме диска зрительного нерва (ДЗН) [2, 4, 5]. В работе Pastora-Salvador и соавторов описан случай медуллоэпителиомы зрительного нерва у мальчика 12 лет. Пациенту провели локальную резекцию опухоли, при этом безрецидивный период наблюдения составил 25 лет [5].
Медуллоэпителиомы классифицируются на тератогенные и нетератогенные варианты, подразделяемые в свою очередь на доброкачественные и злокачественные типы. Основной признак нетератогенного типа опухолей — множественность слоев и полос низкодифференцированных нейроэпителиальных клеток, внешне схожих с эмбриональной сетчаткой или цилиарным эпителием [6].
Дифференциальный диагноз следует проводить с ретинобластомой и другими редкими внутриглазными опухолями, включая беспигментную меланому, шванному и аденокарциному ретинального пигментного эпителия, а также неопухолевыми процессами, такими как воспалительная гранулема [7, 8]. Несмотря на то что медуллоэпителиомы могут выглядеть в виде крупных нейробластных псевдорозеток, для них характерны трубчатые конгломераты клеток, а не рост в виде «перчаток» или «рукоятки», что типично для ретинобластом. Дифференциальными признаками могут служить также тесная взаимосвязь с подлежащими тканями и отсутствие псевдофоторецепторов, в отличие от розеток Флекснера—Винтерштайнера [6]. Иммуногистохимические исследования медуллоэпителиом с псевдорозетками Флекснера—Винтерштайнера выявляют положительный результат на нейронспецифичную енолазу и синаптофизин во всех случаях [6].
В некоторых случаях исход заболевания неблагоприятен. Такое развитие новообразования чаще всего связано с распространением за пределы глаза, но также описаны отдаленные метастазы в лимфатические узлы, околоушные железы, легкие и средостение [9]. Медуллобластома как примитивная нейроэктодермальная опухоль центральной нервной системы у детей поражает преимущественно мозжечок и встречается значительно чаще первичной опухоли внутри глаза [10]. На сегодняшний день доступны несколько химиотерапевтических протоколов для лечения данного заболевания [11]. Первичная внутриглазная медуллоэпителиома, несмотря на низкую частоту встречаемости, представляет интерес для офтальмологов в связи со сложностью ее дифференциальной диагностики с другими внутриглазными новообразованиями, а также единичными данными о возможном химиотерапевтическом лечении.
Цель настоящей работы — клинико-гистологический анализ случая злокачественной медуллоэпителиомы у ребенка, а также описание опыта получения клеточной культуры опухоли и проведения МТТ-теста.
Клинические данные. Мальчик в возрасте 2 лет и 3 мес поступил на обследование и лечение в стационар. Из анамнеза известно, что в возрасте 2 лет родители заметили изменение «окраски» зрачка левого глаза на фотографии, а через 2 мес обратились к врачу по месту жительства, диагноз — подозрение на ретинобластому группы D. До появления первых симптомов ребенка осматривали в 1 год и 7 мес, но без мидриаза. При поступлении острота зрения на левом глазу соответствовала правильной проекции света, передний отрезок глаза без изменений. На глазном дне, по данным осмотра на RetCam, — ДЗН и макула не определяются, прикрыты серо-белой опухолевой тканью с неровными границами и бугристой поверхностью (рис. 1). На правом глазу изменений не выявлено.
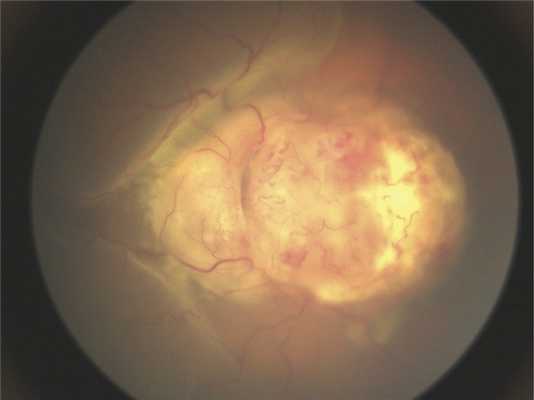
Рис. 1. Клиническая картина опухоли при осмотре на RetCam.
Согласно данным ультразвукового исследования, у заднего полюса выявлены плюс-ткань гетерогенной эхоструктуры с единичными кальцинатами, размером 6,4×13,3 мм, вторичная отслойка сетчатки (рис. 2). Учитывая локализацию опухоли (солитарный опухолевый узел, полностью перекрывающий ДЗН), отсутствие шансов на зрение, размеры образования и высокий риск экстрабульбарного распространения опухоли, выполнена энуклеация левого глаза с пластикой культи. После получения патогистологического заключения (злокачественная медуллоэпителиома) ребенок направлен на консультацию к детскому онкологу с целью возможного выявления новообразования в головном мозге. По данным магнитно-резонансной томографии, опухолевых очагов в ЦНС не выявлено, однако в связи с прорастанием опухоли за laminacribrosa пациенту назначен курс лучевой и химиотерапии (циклофосфан, вепезид, карбоплатин).
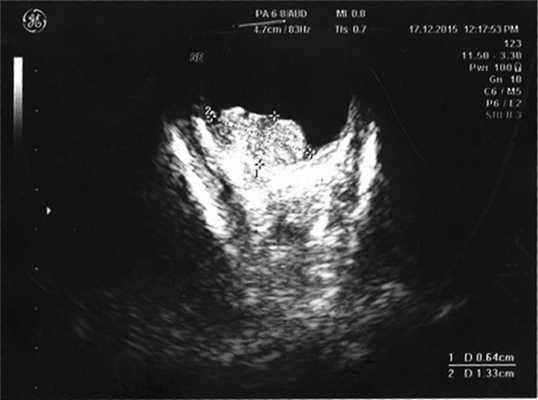
Рис. 2. Результат эхографии левого глаза у ребенка с подозрением на монокулярную форму ретинобластомы.
Патоморфологическое исследование. При морфологическом исследовании кусочка новообразования из боковой колодки выявлена опухоль, состоящая из кубических эпителиальных клеток, которые формировали единичные розетковидные структуры и небольшие участки солидного роста. Поставлен предварительный диагноз — недифференцированная ретинобластома без опухолевых комплексов в дистальном отрезке зрительного нерва. Далее при изучении срезов всего глазного яблока выявлен большой опухолевый узел в центральных отделах глазного дна, тесно связанный со зрительным нервом. Узел состоял преимущественно из трубчатых и сетчатых структур, розеток, ленточных образований, что придавало опухоли местами вид «кружева» (рис. 3).
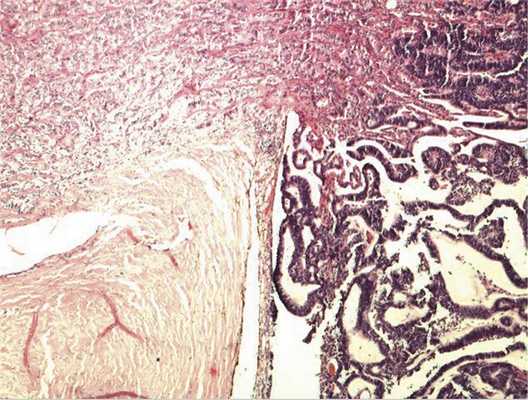
Рис. 3. Часть узла опухоли снаружи от ДЗН, имеющая вид «кружева». Окраска гематоксилином и эозином. Ув. 100.
Отмечалось наличие ленточных структур из низкодифференцированных эпителиальных клеток (рис. 4). Параллельно встречались участки солидного строения из клеток с гиперхромными ядрами с признаками клеточного и ядерного полиморфизма. В них почти исчезает строма, появляются митозы, встречаются участки дистрофии и некроза (рис. 5). Опухоль врастает в ткань ДЗН с переходом за laminacribrosa, но не достигает линии отсечения (рис. 6). В таком виде опухоль обладает местнодеструирующим характером роста и может давать метастазы, глубоко инфильтрируя прилежащую к ДЗН ткань хориоидеи. Окончательный гистологический диагноз: злокачественная медуллоэпителиома центрального отдела сетчатки с вовлечением ДЗН и инвазией перипапиллярной хориоидеи, с глубоким прорастанием по зрительному нерву, не достигая линии отсечения.
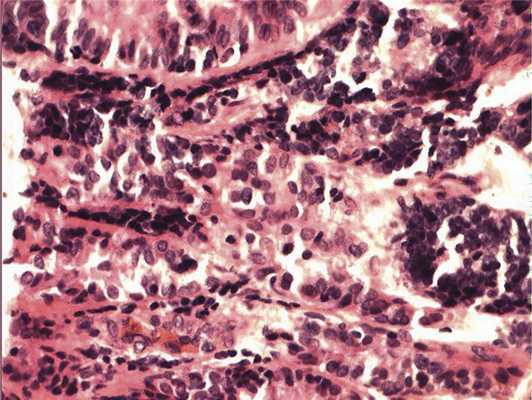
Рис. 4. Формирование полос из низкодифференцированных нейроэпителиальных клеток. Окраска гематоксилином и эозином. Ув. 400.
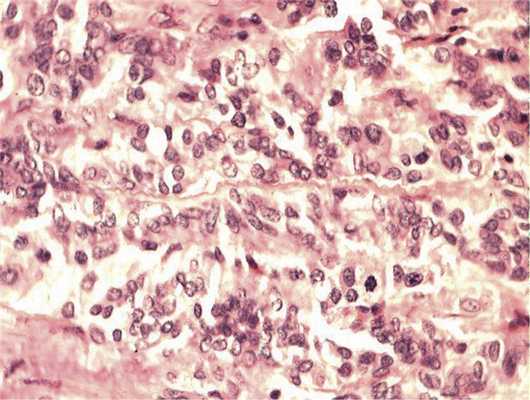
Рис. 5. Зоны солидного роста опухоли. Клеточный полиморфизм с фигурами митозов. Окраска гематоксилином и эозином. Ув. 400.
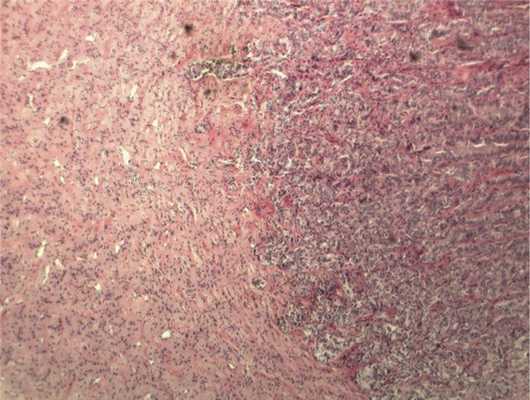
Рис. 6. Врастание опухоли в ткань ДЗН с ростом по ходу пучков нервных волокон. Окраска гематоксилином и эозином. Ув. 100.
Получение первичной культуры опухоли. После вскрытия глазного яблока взят образец опухолевой ткани для получения клеточной культуры с последующим исследованием лекарственной устойчивости (МТТ-тест). Опухолевый образец транспортировали в лабораторию генетики опухолевых клеток РОНЦ им. Н.Н. Блохина в течение 2—3 ч в бессывороточной среде RPMI («ПанЭко», Россия) с добавлением 100 мкг/мл гентамицина («Микроген», Россия). Далее полученную ткань обрабатывали механически (измельчали стерильными ножницами) и ферментативно (0,25% трипсин—0,04% ЭДТА; «ПанЭко», Россия) до получения клеточной суспензии, которую переносили в культуральные флаконы («Corning—Costar», США) со средой RPMI c добавлением 10% эмбриональной сыворотки коров («PAALaboratories», Австрия) и гентамицина 50 мкг/мл. Центрифугировали транспортировочную среду, полученный осадок клеток высевали на флаконы, которые помещали в термостат («Memmert», Германия) при температуре 37 °C и содержанием 5% СО2. Далее в течение 1 мес культивировали полученные клетки, по мере необходимости закисленную среду с погибшими клетками заменяли на новую питательную среду, при достижении клетками 60—80% уровня конфлюэнтности производили рассев клеток на новые культуральные флаконы. В течение культивирования клетки прошли 2—4 пассажа.
МТТ-тест. Метод основан на способности митохондриальных дегидрогеназ живых клеток метаболизировать желтый тетразол-реагент МТТ-3-(4,5-диметилтиазол-2)-2,5-дифенилтетразол-бромид в синий формазан. По интенсивности окраски конечного раствора судят о количестве живых клеток в лунке.
Клетки первичной культуры медуллоэпителиомы MB1 рассевали на 96-луночное плато по 1,5∙10 3 клеток в лунку в объеме 90 мкл культуральной среды RPMI. Препараты (иринотекан, ифосфамид, оксалиплатин и аскорбиновую кислоту) в объеме 10 мкл добавляли в различных концентрациях на следующий день. В контрольные лунки добавляли 10 мкл бессывороточной среды. Клетки культивировали в присутствии химиопрепаратов в течение 3 сут. Затем в лунки добавляли реагент МТТ в концентрации 5 мг/мл в объеме 20 мкл на лунку (рис. 7). Через 1,5—2 ч среду с реагентом удаляли и осадок растворяли в 60 мкл ДМСО. Уровень оптической плотности растворов в каждой лунке определяли с помощью спектрофотометра (планшетного ридера) Multiskan FC («ThermoScientific», EС) при длине волны 594 нм.

Рис. 7. 96-луночное плато с клетками первичной культуры злокачественной медуллоэпителиомы и исследуемыми препаратами.
Далее в «Программе для расчета IC50 химиотерапевтических веществ», написанной в лаборатории генетики опухолевых клеток, строили график зависимости уровня оптической плотности (проценты от контроля) от концентрации вещества и рассчитывали искомую концентрацию IC50 (полумаксимальное ингибирование). Использованы следующие химиопрепараты:
а) Иринотекан («Actavis», Исландия) в концентрациях 0,25; 0,5; 1,0 и 2,0 мг/мл;
б) Ифосфамид («Верофарм», Россия) в концентрациях 0,25; 0,5; 1,0 и 5,0 мг/мл;
в) Оксалиплатин («Medac», Германия) в концентрациях 0,1; 0,2; 0,38; 0,75 и 1,5 мг/мл;
г) Аскорбиновая кислота («Alvils», Россия—Китай) в концентрациях 0,6; 1,25; 2,5 и 5 мг/мл.
Результаты МТТ-теста представлены на рис. 8, а—г. Для аскорбиновой кислоты получена IC50 3,3 мг/мл. Результаты данного теста показывают, что с повышением концентрации препарата выживаемость клеток увеличивается.
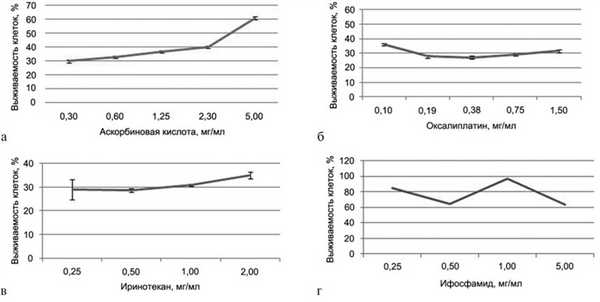
Рис. 8. IC50 (полумаксимальное ингибирование). а — для аскорбиновой кислоты; б — для оксалиплатина; в — для иринотекана; г — для ифосфамида.
IC50 для оксалиплатина, иринотекана и ифосфамида не получена. Для оксалиплатина при минимальной используемой концентрации 0,1 мг/мл выживаемость клеток составила 36%, для иринотекана при минимальной используемой концентрации 0,25 мг/мл — 29%, а для ифосфамида при максимальной используемой концентрации 5 мг/мл — 64%. Таким образом, из четырех исследованных препаратов IC50 (3,3 мг/мл) получена только для раствора аскорбиновой кислоты.
Заключение
К настоящему времени патогномоничные симптомы, свидетельствующие о первичной внутриглазной злокачественной медуллоэпителиоме, не описаны, а диагноз ставится на основании патогистологического заключения. Вместе с тем ряд симптомов, включая наличие кальцификатов и нехарактерные рентгенографические признаки, затрудняют дифференциальную диагностику с другими внутриглазными опухолями детского возраста, прежде всего ретинобластомой. К характерным патоморфологическим особенностям ретинобластомы, отличающим ее от медуллоэпителиомы, относят наличие «истинных» розеток, состоящих из цилиндрической формы нейроэпителиальных клеток эмбрионального типа [12]. Для медуллоэпителиомы, напротив, характерно наличие псевдорозеток, располагающихся диффузно или вокруг сосудов [2]. Несмотря на относительную редкость опухоли, необходимо проводить дифференциальный диагноз с другими внутриглазными образованиями, особенно при наличии сопутствующих длительно существующих глазных симптомов. Полученные данные об эффективности раствора аскорбиновой кислоты в отношении клеток внутриглазной злокачественной медуллоэпителиомы могут быть использованы для дополнения существующих химиотерапевтических протоколов в детской нейро- и офтальмоонкологии. Клеточная культура медуллоэпителиомы и возможная животная модель опухоли являются потенциальными объектами для изучения как экспрессии генов, так и специфических мутаций в ткани опухоли, что в свою очередь представляет интерес в перспективе для селективной химиотерапии опухоли и сохранения глаза.
Читайте также:
