Синдром Биндера (Binder) - синонимы, авторы, клиника
Добавил пользователь Евгений Кузнецов Обновлено: 02.02.2026
Биндер — фамилия. Известные носители: Биндер, Авраам Вольф (1895 1967) американский композитор, автор песен, дирижёр и музыкальный педагог. Биндер, Александру (1902 1981) румынский писатель и поэт авангардист, издатель, известный под псевдонимом Саша Панэ … Википедия
Биндер — англ. binder предварительное соглашение о намерениях между страхователем и страховщиком, фиксирующее желание сторон заключить в последующем полномасштабный договор страхования, после чего биндер заменяется на страховой полис. Б. заключается в… … Словарь бизнес-терминов
БИНДЕР (Binder) Людвиг — (1881 1958) немецкий электротехник. Труды по изучению теплообмена в электрических машинах, преобразованию электрического тока, защите от перенапряжений, диэлектрической прочности изоляционных материалов … Большой Энциклопедический словарь
Биндер Людвиг — Биндер (Binder) Людвиг (26.5.1881, Ингольштадт, ‒ 12.9.1958, Дрезден), немецкий электротехник, член Саксонской АН (1948), член Немецкой АН (Берлин, 1949). С 1919 профессор Высшей технической школы в Дармштадте и Высшей технической школы в… … Большая советская энциклопедия
БИНДЕР Людвиг — БИНДЕР (Binder) Людвиг (1881 1958), немецкий электротехник. Труды по изучению теплообмена в электрических машинах, преобразованию электрического тока, защите от перенапряжений, диэлектрической прочности изоляционных материалов … Энциклопедический словарь
Биндер, Франц — В Википедии есть статьи о других людях с такой фамилией, см. Биндер. Франц Бинде … Википедия
Биндер, Аранка — Аранка Биндер Личная информация Пол: женский Полное имя: Аранка Биндер Оригинальное имя: серб. Аранка Биндер / Aranka Binder Гражданство … Википедия
Биндер, Ханс — Ханс Биндер Гражданство Австрия Дата рождения … Википедия
Биндер, Курт — Курт Биндер Kurt Binder Дата рождения: 10 февраля 1944(1944 02 10) (68 лет) Место рождения: Корнойбург, Австрия Страна … Википедия
Биндер, Авраам-Вольф — Авраам Вольф Биндер (1895 1967) американский композитор, аранжировщик, автор песен, дирижер и музыкальный педагог. Авраам Вольф Биндер родился в Бронксе, Нью Йорк, в большой религиозной семье, у него было пять братьев и сестер Рая,… … Википедия
Синдром Биндера - Binder's syndrome
Синдром Биндера / синдром Биндера (челюстно-носовая дисплазия) - это нарушение развития, в первую очередь затрагивающее переднюю часть верхней челюсти и носовой комплекс (нос и челюсть). Это редкое заболевание, причины которого неясны.
Характеристики синдрома обычно видны. Синдром включает гипоплазию различной степени выраженности хрящевой перегородки носа и предчелюстной кости. Он включает полное полное отсутствие передней носовой ости. Также имеются связанные аномалии прикрепления мышц верхней губы, дна носа и шейного отдела позвоночника. У больных обычно бывает необычно плоская недоразвитая средняя часть лица (гипоплазия средней зоны лица), аномально короткий нос и плоская переносица. У них недоразвитая верхняя челюсть, относительно выступающая нижняя челюсть с превышением по вертикали передней нижней челюсти и скелетно-дентальный профиль класса III (обратный оверджет). У них небольшая лобная пазуха и глобальный дисбаланс лица.
Лечение рекомендуется как можно раньше с задне-передней тракцией верхней челюсти и, примерно, в возрасте 8 лет, повторным введением носогубных мышц на переднюю границу хрящевой системы. Многие люди, страдающие тяжелым заболеванием, подвергаются пластической хирургии или ортодонтическому лечению по косметическим причинам.
Современные подходы к изучению плодового фенотипа в эру генетического ультразвука
Медико-генетическое отделение Московского областного НИИ акушерства и гинекологии, Москва.
Курс пренатальной диагностики, ФГБОУ ДПО РМАПО Минздрава России, Москва.

УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Настоящая работа посвящена изучению плодового фенотипа при ультразвуковом исследовании в различные сроки беременности при помощи новейших технологий Samsung, оптимизирующих диагностику многих врожденных пороков развития, аномалий, нарушений строения, особенностей развития с оценкой значимости отдельных ультразвуковых патологических маркеров в качестве потенциальных признаков генетических синдромов и ассоциаций.
Одной из ведущих причин детской и младенческой смертности являются врожденные пороки развития (ВПР), среди которых в 20% случаев встречаются множественные ВПР (МВПР) с установленной частотой 1:250 новорожденных [1]. Особое значение в профилактике МВПР имеет пренатальная диагностика - современный и высокоэффективный метод диспансеризации плода, направленный на своевременное выявление патологии, впоследствии определяющий выбор адекватной акушерской тактики при данной беременности и специфических мер профилактики болезни в данной семье в дальнейшем [2]. Современные ее возможности позволяют из комплекса патологических нарушений у плода выделить достоверно значимые ультразвуковые маркеры для постановки диагноза генетических синдромов различной этиологии. Сегодня пренатальная синдромология активно развивается, как в плане расширения спектра возможных лабораторных исследований, так и описания значимых, ключевых, таргетных ультразвуковых признаков многих наследственных синдромов различного происхождения.
Группа МВПР включает сотни нозологических форм, различных по этиологии, фенотипическим проявлениям и прогнозу. В силу огромной гетерогенности МВПР представляют собой сложную проблему для постановки окончательного диагноза. Основными этиологическими факторами, приводящими к возникновению синдромов с множественными пороками развития, являются генные, хромосомные мутации и действие на плод неблагоприятных факторов внешней среды [3, 4].
Любые наследственные или врожденные генетические болезни являются результатом повреждения генетической информации на геномном, хромосомном или генном уровне. В 60% всех случаев МВПР встречаются хромосомные синдромы, достаточно широко изученные и хорошо диагностируемые. Для лабораторной диагностики этих повреждений разработаны разнообразные и хорошо известные методы: цитогенетический, молекулярно-цитогенетический и молекулярно-генетический. МВПР нехромосомного генеза встречаются в 40% случаев. Среди них выделяют синдромы, ассоциации и неклассифицированные комплексы. Применительно к нехромосомным синдромам цитогенетическое исследование позволяет лишь отвергнуть хромосомную природу данного комплекса пороков развития, но не установить диагноз.
Сегодня имеется определенное количество публикаций о выявлении некоторых синдромов и ассоциаций при пренатальной эхографии [6, 7]. Однако дородовая идентификация нозологических форм нехромосомных синдромов пока не вошла в рутинную практику врачей в области пренатальной диагностики и носит случайный характер. В литературе отсутствуют четкие рекомендации о системном подходе к диагностике наследственных синдромов различной этиологии, нет диагностических алгоритмов и определенных схем взаимодействия врачей ультразвуковой пренатальной диагностики, генетиков, акушеров-гинекологов.
Использование эхографии делает возможным пренатальное выявление не менее 80% врожденных дефектов во II, III триместрах беременности и свыше 50% значимых нарушений анатомии плода уже в I триместре начиная со сроков 11-12 нед. Весь комплекс диагностированных пороков развития и различных микроаномалий в совокупности составляет фенотипический спектр синдрома, который состоит из «ядерных» (главных, ключевых) признаков и дополнительных аномалий, наличие которых не является обязательным для диагностики клинической нозологии синдрома.
Революцией в пренатальной ультразвуковой диагностике явилось появление объемной эхографии, которая, обладая такими качествами, как неинвазивность, безопасность и возможность многократного применения у одной пациентки, имеет высокую информативность в исследовании анатомии плода и изучении его фенотипа. При применении различных режимов объемной эхографии абсолютно очевидно их преимущество по сравнению с обычным сканированием. Детально можно изучить лицо плода (рис. 1-4) в различные сроки беременности, начиная со сроков первого пренатального скрининга в 11-14 нед, конечности плода, причем не только их наличие и положение (рис. 5, 6), но и состояние и количество пальцев (рис. 7-9) как на руках, так и на ногах. Также можно изучить позвонки плода (рис. 10), состояние твердого нёба (рис. 11, 12), строение наружного уха (ушной раковины) (рис. 13), состояние основных швов черепа и родничков, исключая их преждевременное закрытие при кранисиностозах (рис. 14, 15).
Есть ли жизнь после родов? Ботулотоксин и беременность. Как быть врачу и пациенту?
Эмансипация достигла своих максимальных возможностей, казалось бы, женщинам разрешили голосовать, носить брюки, ездить в седле по-мужски и работать полный день - важные достижения XX столетия. Но наряду с правами появились и обязанности.
Обучение, постоянное повышение профессиональных навыков, ключевые управленческие посты - все это приводит девушек к безусловному успеху, но и отодвигает время наступления беременности и родов.
Если в Советском Союзе в возрасте 28 лет уже писали в карту «старая первородящая», в XXI веке первые роды в 38 лет уже никого не удивляют, и все радуются осознанному выбору.
После первой радости всплывает список вопросов. Что можно делать из ранее разрешенного списка? Процедуры эстетической медицины попадают в этот список важных дел.
Каждая третья женщина после 35 лет делает инъекции ботулотоксина.
«Ботокс беременным», «Диспорт и беременность», «Ксеомин как самый мягкий во время беременности?», «Что делать, если я забеременела и сделала Ботокс?» - поиск в Google выдает миллион запросов. Давайте разбираться вместе с экспертами.
Я в своей практике использую три препарата - Ботокс, Диспорт и Ксеомин. У всех трех в инструкции четко написано, что абсолютным противопоказанием к введению является беременность и лактация. Но несмотря на это своей практике я не видела негативных влияний, хотя, конечно, были пациентки, которые спрашивали, что им делать, если они узнали о беременности уже после коррекции БТА. Я всегда девушек успокаиваю, потому что в литературе описано много случаев, которые показали абсолютную безопасность этих препаратов во время беременности и рождения здоровых детей. Ботулопротеин имеет большой размер молекулы, он не проникает через плацентарный барьер, кроме того, при корректном введении и дозах значительных системных концентраций не наблюдается. Хочу отметить, что мы используем препараты на основе ботулотоксина типа А не только в эстетической медицине, но и в других направлениях. Пациентам по медицинским показаниям проводятся инъекции во время беременности для лечения ахалазии, мигреней, цервикальной дистонии на разных сроках, и ни у кого из пациентов не наблюдалось негативных последствий в связи с лечением. Также были проведены опросы пациентов (400 пациентов), им во время беременности была проведена коррекция в эстетических целях, они об этом не знали, а потом наблюдали течение беременности и родов - все было нормально. В 2016 году компания Аллерган проводила исследование, которое установило, что беременность протекала нормально, и никакого влияния БТА не оказывал на ее течение.
Конечно, если пациентка знает, что она беременна, то ни в коем случае не надо проводить коррекцию, но если процедура была выполнена у пациентки, узнавшей о беременности уже после инъекции, то и беспокоиться ей не надо.
Недавно в журнале Expert Opinion On Drug Safety была опубликована статья гинекологов из Тайваня, которые сделали обзор применения БТА у беременных женщин, причем дозы ботулотоксинов были терапевтическими и применялись у пациенток для лечения неврологических заболеваний 1 .
Все эти состояния успешно лечились и до, и во время беременности инъекциями БТА, что позволило врачам проследить влияние ботулотоксина на течение беременности и воздействие на плод. Ученые утверждают, что инъекции БТА показали относительную безопасность во время беременности.
Ниже мы приводим выдержки из материала.
Ботулотоксин в системном кровотоке
Для начала следует вспомнить: чтобы воздействовать на миометрий или достичь плаценты и негативно повлиять на плод, действующее вещество должно попасть в системный кровоток.
В некоторых отчетах указывалось, что в высоких дозах БТА мог диффундировать из мышечной ткани лица на руку, по результатам однофибровой электромиографии (ЭМГ) 2, 3 . Однако этот эффект оказался субклиническим, потому что у пострадавших не было обнаружено слабости мышц. Если доза препарата не превышала рекомендуемой, то при внутримышечной инъекции БТА не попадал в системный кровоток 4 .
БТА классифицируется FDA как препарат категории С, это означает, что исследования на животных выявили отрицательное воздействие лекарства на плод, а надлежащих исследований у беременных женщин не проводилось, однако потенциальная польза, связанная с применением данного лекарства у беременных, может оправдать его использование, несмотря на имеющийся риск.
Кроме того, исследования показали, что молекулы больше 500 Дальтон не могут проникать сквозь плаценту 5 . Молекулярная масса БТА превышает 500 D, поэтому вряд ли БТА пересечет плацентарный барьер и вряд ли будет присутствовать в крови плода.
До настоящего времени исследования на животных не нашли доказательств для передачи токсинов плоду. У кроликов БТА не обнаруживался в плаценте или у эмбрионов при внутривенном введении высоких (летальных) доз токсина. Пороки развития и выкидыш регистрировались только если кролики получали инъекции БТА в высоких дозах ежедневно; и наоборот, беременные мыши, получавшие БТА не показали аналогичных неблагоприятных исходов 6 .
Дистонии
Дистонией называют синдром, при котором происходит постоянное спазматическое сокращение мышц, спазмы часто непредсказуемы, изменяют нормальное положение тела, могут носить хронический характер и вызывать значительное неудобство, боль и потерю трудоспособности.
В статье 1 рассматривалось применение БТА в лечении идиопатической торсионной дистонии, оромандибулярной дистонии, спастической дистонии (табл. 1).
Как правило, болезнь начинается до начала репродуктивного возраста и сохраняется на протяжении жизни. Распространена у беременных женщин. В настоящее время инъекции БТА являются предпочтительным вариантом лечения. При этом у 10 % пациентов болезнь начиналось внезапно в связи с беременностью и родами. Анкола показал (исследование 350 пациентов), что беременность или связанные с беременностью гормональные изменения могут быть фактором риска заболевания 7 . Морган обнаружил, что в опросе 396 врачей девять беременных женщин получили инъекцию БТА во время беременности. У одной пациентки случился спонтанный аборт, но остальные восемь пациенток родили здоровых детей 8 . Блитцер 11 суммировал данные 1300 пациентов с такими дистониями, как дисфонии аддукторного и абдукторного типов, и за 24 года, по его данным, эффективность БТА составила 91,2 % и 70,3 %.
Таблица 1. Применение БТА для лечения дистонии во время беременности (по Wu Li, Min Tang 1 )
15 недель / 200 ед.
БТА улучшил симптомы, которые повторялись примерно каждые 3-4 месяца.
В последующие 9 лет пациентка забеременела три раза, и получила БТА несколько раз в течение каждой беременности.
Инъекции дали хорошие результаты во всех трех беременностях, пациентка родила здоровых детей
1 раз во втором и третьем триместрах
Место инъекции и доза были идентичны тем, которые использовались до беременности: 40 МЕ в левую грудинно-сосцевидную мышцу, 150 МЕ, и дополнительные 60 МЕ разделены между трапециевидной и правой элеваторной мышцей лопатки. Общая доза на протяжении беременности - 500 МЕ
На 40-й неделе пациентка родила здорового ребенка (вес 3400 г).
У пациентки отмечалось облегчение симптомов, она родила здорового ребенка 20 .
Косоглазие
Отклонение зрительных осей от направления на рассматриваемый объект, при котором нарушается скоординированная работа глаз и затрудняется фиксация обоих глаз на объекте зрения. БТА считается альтернативой хирургии.
Два пациента с косоглазием получили БТА во время беременности
Терапевтическое действие не вызвало осложнений или аномалий плода
17-летняя женщина. Препарат был введен до того, как пациентка узнала о беременности
Родился здоровый ребенок
Ахалазия пищевода
Функциональная непроходимость пищевода. Характеризуется потерей активности нижнего пищеводного сфинктера (LES), и перистальтики пищевода; основными симптомами являются дисфагия, боль в груди и рефлюкс.
Варианты лечения включают диету, введение блокаторов кальциевых каналов, миотомию Геллера. БТА может вводиться местно в область желудка. Процедура не требует глубокой анестезии, и может расслабить LES и облегчить непроходимость пищевода.
Wataganara et al., 2009 13
Здоровый младенец родился на 36-й неделе беременности, не отмечалось нарушения глотания до 6 недель после родов
БТА на 14-й неделе беременности
Холлидей 2016 15
БТА на 31-й + 3 недели беременности
Эклампсия и роды в 37 + 4 недели беременности
Спазм жевательных мышц
Характеризуется пароксизмальным непроизвольным сокращением мышцы нижней челюсти, связанным с гипертрофией височных мышц.
Хроническая тазовая боль (CPP)
Распространенный синдром с различными причинами: основным и единственным симптомом является боль, иногда сопровождаемая расстройствами дефекации. В дополнение к ежедневной боли, пациенты часто жалуются на диспареунию и дисменорею. У женщин после инъекций БТA боль значительно снижалась.
Две женщины забеременели через 4 и 5 месяцев после инъекции;
У одной женщины (41 год; сложная история болезни) в 40 недель сделали плановое кесарево сечение, и у ребенка был дефект межжелудочковой перегородки, который требовал хирургической коррекции. Однако неясно, был ли он вызван введением БТА.
Два случая во время беременности
У обеих матерей были хорошие результаты.
Мигрень
Некоторые лекарства от мигрени считаются небезопасными для беременных 18 .
В 2000 году Биндер и другие первыми сообщили, что БТА успешно применялся у пациентов с головной болью 19 . В метаанализе 17 исследований с участием 3646 пациентов с хронической мигренью Брюла и коллеги обнаружили, что БТА значительно снизил симптомы хронической мигрени через 3 месяца лечения по сравнению с плацебо; следовательно, БТА считался безопасным и хорошо переносимым 20 .
Статистика осложнений
Выводы Wu Li, Min Tang 1 по осложнениям показали, что показатели самопроизвольных абортов и пороков развития плода у беременных женщин, получавших лечение БТА, были похожи на те, о которых сообщалось для населения в целом.
Тан сообщил о 28 случаях, произошедших до 2013 года у пациентов, которые получали БТА во время беременности; в том числе 25 нормальных рождений, 1 терапевтический аборт и 2 самопроизвольных аборта 21 .
В 2016 году Brin et al. сообщили результаты у беременных женщин, которые получили местные инъекции БТА в течение предыдущих 24 лет. Из 137 родов (139 плодов), 110 (79,1%) - живорождение, 29 (20,9%) - потеря плода (21 самопроизвольный аборт) и 8 абортов 22 . Среди живорождений 106 (96,4%) были нормальными, только у 4 пациенток регистрировался плохой исход, у двух - незначительные пороки развития плода и одно врожденное осложнение; общая частота пороков развития плода составила 2,7 %. Возможно, они не были связаны с лечением БТА.
Отравление ботулином
В литературе отмечены случаи, когда высокие дозы БТА могли вызывать симптомы системного отравления ботулином.
Однако в отчете Brin et al. (2016) говорится, что клинический ботулизм не имеет побочных эффектов, связанных с беременностью или плодом 22 . Баделл изучил исходы для матери и плода, связанные с отравлением ботулином: у 16 женщин во время беременности (11 случаев на поздних сроках беременности) и у 1 женщины после инъекции 23 . Хотя беременные женщины показали признаки отравления, все дети родились здоровыми и только у шести пациенток случились преждевременные роды. Анализы крови новорожденных не показали присутствия БТА в системном кровотоке; эти выводы также подтвердили гипотезу о том, что БТА не попадает в систему кровообращения плода 24, 25 .
Если такая ситуация случилась, это не повод для паники. Нейропротеин после введения в ткани существует в активной форме не больше одного часа. В течение этого времени происходит его взаимодействие с аксоном нервного окончания, и разделение тяжелой цепи от легкой. Затем нейротоксин переходит в неактивную форму. Пациентке нужно объяснить принцип работы препарата и успокоить.
Синдром Пьера Робена
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Синдром Пьера Робена, также известный в медицине под названием аномалия Робена, является врожденной патологией развития челюстной части лица. Свое название заболевание получило в честь французского стоматолога П. Робена, который впервые описал все его признаки. Lannelongue и Menard впервые описали синдром Пьера Робина в 1891 г. в своем докладе на примере 2-х пациентов с микрогнатией, расщелиной нёба и ретроглоссоптозом. В 1926 году Пьер-Робин опубликовал случай заболеввания у младенца с признаками классического синдромом. До 1974 года триада признаков была известна как синдром Робена-Пьера. Тем не менее, этот синдром сейчас используется для описания пороков формообразования при одновременном наличии множественных аномалий.
Код по МКБ-10
Эпидемиология
Это гетерогенный врожденный дефект, который имеет распространенность 1 на 8500 живорожденных. Соотношение мужчин к женщинам составляет 1:1, за исключением Х-хромосомой формы.
Среди этих больных, у 50% младенцев расщелина на мягком небе является неполной, остальные рождаются с дугообразным и необычайно высоким небом, но без расщелины.
Причины Синдрома Пьера Робена
Рассматривается возможность аутосомно-рецессивного наследования болезни. Различают два вида синдрома в зависимости от этиологии: изолированный и генетически детерминированный. Изолированный вид развивается из-за компрессии нижней части челюсти во период эмбрионального развития. Компрессия может развиваться вследствие:
- Наличие в матке локальных уплотнений (кисты, рубцы, опухоли).
- Многоплодная беременность.
Также развитие челюсти у плода может нарушаться при:
- Вирусных инфекциях, которые перенесла будущая мать во время беременности.
- Нейротрофических нарушениях.
- Недостаточном количестве фолиевой кислоты в организме беременной женщины.
Патогенез
Синдром Пьера Робена проявляется из-за эмбриональных нарушений, которые вызываются самыми разнообразными патологиями в дородовом периоде.
Существует три патофизиологические теории, которые могут объяснить возникновение синдрома Пьера Робена.
Механическая теория: Эта теория наиболее вероятная. Недоразвитие нижнечелюстного аппарата происходит между 7-й и 11-й неделями беременности. Высокое стояние языка в ротовой полости приводит к образования расщелин в небе, из-за этого не происходит закрытие небных пластинок. Эта теория объясняет классическую перевернутую U-образную расселину и отсутствие связанной с ней заячьей губы. В этиологии определенную роль может играть олигогидрамнион, так как отсутствие амниотической жидкости может привести к деформации подбородка и последующего сдавление языка между небных пластинок.
Неврологическое теория: Задержка в неврологическом развитии была отмечена при проведении электромиографии мышц язычка и глоточных столбов, и вкуса из-за задержки проводимости в подъязычном нерве.
Теория диснейрорегуляции ромбовидного мозга: Эта теория основана на нарушении развития ромбовидного мозга в процессе онтогенеза.
Недостаточное развитие нижней части челюсти ребенка приводит к тому, что ротовая полость значительно уменьшается. Это, в свою очередь, вызывает так называемую псевдомакроглоссию, то есть язык смещается к задней части стенки глотки. Такая патология приводит к развитию обструкции дыхательного пути.
Пока младенец плачет или двигается, проходимость дыхательного пути остается нормальной, но как только он засыпает, снова возникает обструкция.
Из-за респираторных нарушений процесс кормления младенца сильно затруднен. В это время практически всегда возникает обструкция дыхательного пути. Если не применять лечебную коррекцию, то такая патология может привести к сильному истощению всего организма и даже к летальному исходу.
Симптомы Синдрома Пьера Робена
Заболевание отличается трема основными признаками:
- Нижняя микрогнатия (недостаточное развитие нижней части челюсти, встречается в 91,7% случаев заболевания). Она характеризуется втягиванием нижней зубной дуги на 10-12 мм позади верхней арки. Нижняя челюсть имеет небольшое тело, тупой угол. Ребенок достигает нормального развития приблизительно в возрасте 5-6 лет.
- Глоссоптоз (западание языка по причине его недостаточного развития, отмечается в 70-85% случаев).
- Макроглоссия и анкилоглоссия относительно редкие признаки, отмечаются в 10-15% случаев.
- На небе появляется расщелина.
- Брадипноэ и диспноэ.
- Легкий цианоз.
- Асфиксия, которая чаще всего проявляется во время попыток покормить младенца.
- Глотание невозможно или сильно затруднено.
- Позывы к рвоте.
- Аурикулярные аномалии в 75% случаев.
- Потеря слуха проводящего характера встречается у 60% больных, в то время как атрезия наружного слухового канала встречается только у 5% пациентов, недостаточная пневматизация сосцевидного полости височной кости.
- Аномалии внутреннего уха (аплазия боковых полукруглых каналов, большого вестибулярного акведука, потеря волосковых клеток улитки).
- Носовые пороки развития являются нечастыми и представлены в основном из аномалий корня носа.
- Стоматологические пороки развития встречаются в 30% случаев. Ларингомаляция и небно-глоточная недостаточность наблюдаются приблизительно у 10-15% пациентов с синдромом Пьера Робина.
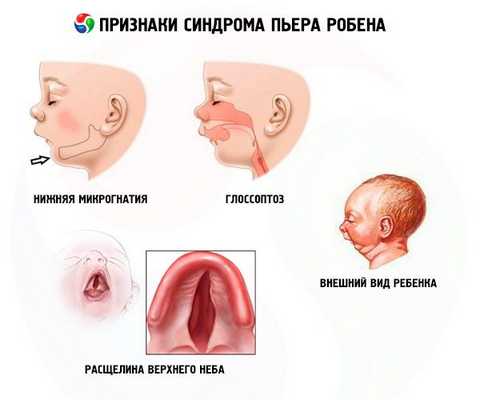
Системные признаки синдрома Пьера Робина
Глазные аномалии встречаются в 10-30% пациентов. Могут встречаться: дальнозоркость, близорукость, астигматизм, склероз роговицы и стеноз носослезного протока.
Сердечно-сосудистые патологии: доброкачественные сердечные шумы, стеноз легочной артерии, открытый артериальный проток, овальное окно, дефект межпредсердной перегородки и легочная гипертензия. Их распространенность варьирует в от 5-58%.
Аномалии, связанные с опорно-двигательным аппаратом (70-80% случаев): синдактилия, диспластические фаланги, полидактилия, клинодактилия, гиперподвижность суставов и олигодактилия верхних конечностей. Аномалии развития нижних конечностей: аномалии стоп (косолапость, аддукция плюсны), бедренные пороки развития (вальгусный или варусный таз, короткие бедра), аномалии бедра (врожденный вывих, контрактуры), аномалии коленного сустава (GENU VALGUS, синхондроз). Пороки развития позвоночного столба: сколиоз, кифоз, лордоз, позвоночная дисплазии, агенезия крестца и копчиковой пазухи.
Патология центральной нервной системы: эпилепсия, задержки развития нервной системы, гидроцефалия. Частота дефектов ЦНС составляет около 50%.
Мочеполовые аномалии: не опустившиеся семенники (25%), гидронефроз (15%), а также водянка яичка (10%).
Ассоциированные синдромы и состояния: синдром Стиклера, синдром трисомии 11q, трисомии 18, синдром удаления 4q, ревматоидная артропатия, гипохондроплазия, синдром Мебиуса.
Стадии
Существует три стадии тяжести заболевания, которые зависят от состояния дыхательных путей ребенка:
- Легкая - есть небольшие проблемы с кормлением, но дыхание почти не затруднено. Лечение проводят в амбулаторно.
- Средняя - дыхание умеренно затруднено, кормление ребенка умеренно трудное. Лечение проводят в стационаре.
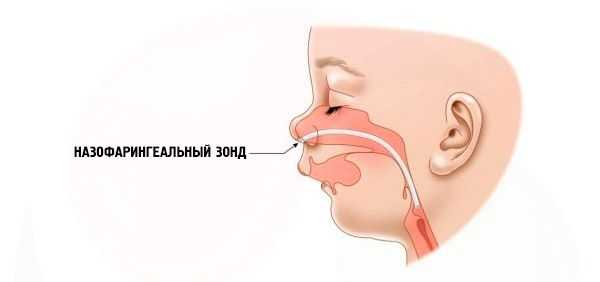
- Тяжелая - дыхание очень затруднено, ребенка невозможно нормально кормить. Необходимо использовать специальные приспособления (интраназальный зонд).
Осложнения и последствия
Сочетание микрогнатии и глоссоптоза может привести к тяжелым респираторным осложнениям и проблемам во время кормления ребенка.
Синдром Пьера Робена вызывает следующие осложнения:
- Стридозное дыхание из-за обструкции дыхательного пути. Ларингомаляция или даже асфиксия во сне.
- Психомоторное развитие ребенка сильно отстает от сверстников.
- Физическое развитие также отстает.
- Речь у больных нарушена.
- Частые инфекционные заболевания уха, которые становятся хроническими и приводят к нарушениям слуха.
- Синдром обструктивного апноэ, наступление смерти во сне варьирует в 14-91% случаев.
- Проблемы с зубами.
Диагностика Синдрома Пьера Робена
Диагностика синдрома Пьера Робена трудностей не вызывает. Она основывается на клинических проявлениях. Чтобы исключить другие патологии, очень важно проконсультироваться у генетика.
У детей с врожденной аномалией Робена с самого рождения нарушено дыхание из-за постоянного западания языка. Младенец беспокойно себя ведет, кожные покровы его синюшные, при вдохах из грудной клетки вырывается хрип. В процессе кормления могут наступать удушья. Диагноз можно поставить также по необычному внешнему виду ребенка - «птичьему лицу». Часто у больных развиваются и другие пороки: миопия, катаракта, патология мочеполовой системы, патология сердца, аномалии развития позвоночника.
По этим клиническим проявлениям поставить правильный диагноз специалисту не составит труда.
К кому обратиться?
Лечение Синдрома Пьера Робена
Лечение проводят сразу же после рождения ребенка с синдромом Пьера Робена. Если заболевание носит легкий характер, то для улучшения состояния больного необходимо постоянно держать ребенка вертикально или лежа на животике. Голову младенца нужно наклонять к груди. В процессе кормления не рекомендовано держать ребенка в горизонтальном положении, чтобы пища не попадала в дыхательные пути.
Если недостаточное развитие нижней части челюсти выражено довольно сильно, применяется оперативное вмешательство для выведения западающего языка в нормальное физиологическое положение. При тяжелых случаях язык подтягивают и фиксируют на нижней губе. При очень тяжелых случаях необходимо проведения трахеостомии, глоссопексии, дистракционного остеогенеза нижней челюсти.
Также применяется и консервативное лечение.
Лекарства
Фенобарбитал. Снотворный и седативный препарат, отличается противосудорожным эффектом. В каждой таблетке находится 100 мл фенобарбитала. Дозировка является индивидуальной, так как зависит от степени тяжести болезни и состояния ребенка. Пациентам с печеночной недостаточностью, гиперкинезом, анемией, миастенией, порфирией, сахарным диабетом, депрессией, непереносимостью компонентов препарат запрещен. При приеме возможны следующие симптомы: головокружение, астения, галлюцинации, агранулоцитоз, тошнота, пониженное артериальное давление, аллергия.
Клоназепам. Препарат, который назначается для лечения эпилепсии. В лекарстве находится активное вещество клоназепам, которое является производным бензодиазепина. Отличается противосудорожным, анксиолитическим и миорелаксирующим эффектом. Доза устанавливается лечащим врачом, но не должна превышать максимальной - 250 мкг в день. Не принимать при бессоннице, мышечном гипертонусе, психомоторном возбуждении, панических расстройствах. При приеме возможны следующие симптомы: заторможенность, тошнота, дисменорея, головная боль, лейкопения, задержка или недержание мочи, алопеция, аллергия.
Сибазон. Выпускается в форме раствора и ректальных таблеток. Активным веществом является производным бензодиазепина (сибазон). Отличается седативным, анксиолитическим, противосудорожным эффектом. Дозировка является индивидуальной. Пациентам с хронической гиперкапнией, миастенией, непереносимостью бензодиазепинов принимать препарат запрещено. При употреблении средства возможно развитие таких симптомов: тошнота, запоры, головная боль, головокружение, икота, недержание мочеиспускания, аллергия.
Кортексин лиофилизат. Препарат с ноотропным действием. В лекарстве находится комплекс полипептидных фракций растворимых в воде и глицин. Дозировка является индивидуальной и назначается лечащим врачом в соответствии с состоянием больного. Пациентам с непереносимостью кортексина принимать препарат запрещено. Средство может вызывать аллергические реакции.
Физиотерапевтическое лечение
Как правило, при легких стадиях синдрома проводится позиционная терапия, когда ребенка укладывают на живот в вертикальном положении до тех пор, пока сила тяжести не заставит нижнюю часть челюсти расти правильно.
Оперативное лечение
Оперативное лечение используется, в первую очередь, для коррекции глоссоптоза. Существует несколько методов:
Читайте также:
