Синдром Герена-Стерна (Guerin-Stern) - синонимы, авторы, клиника
Добавил пользователь Дмитрий К. Обновлено: 22.01.2026
Впервые описал заболевание в 1885 году Жиль де ла Туретт (Gilles de la Tourette), работавший в парижской клинике под руководством учителя Зигмунда Фрейда, врача-психиатра Жана-Мартена Шарко. Бытующие в наше время представления о нем были сформированы благодаря исследованиям экспертов в области психиатрии Артуру и Элейн Шапиро.
Причины появления
Главные «виновники», которые отвечают за синдром Жиля де ла Туретта - гены. Они точно пока не установлены, но если таковые имеются в организме, то существует риск развития данной болезни. Часто родители страдающего синдромом ребенка, отвечая на вопросы специалиста о здоровье членов семьи, с удивлением понимают, что похожие симптомы были у них или у родственников, просто тогда болезнь не была диагностирована.
Кроме наследственной природы, развитие синдрома может быть спровоцировано следующими факторами:
- Будущая мать пила алкоголь, много кофе и курила во время беременности. Также возможно у нее был серьезный токсикоз, стресс.
- Родился ребенок с малым весом, имел повреждения мозга.
- При родах недоставало кислорода.
- У новорожденного наличествовали аномальные результаты по шкале Апгар.
- Стрептококковая инфекция.
Синдром Туретта: симптомы
Вокальные и моторные тики у детей, страдающих данным заболеванием, могут быть как шаблонными, так и уникальными, простыми и сложными. Они проходят приступообразно и множественно в течение дня, ежедневно или с перерывами. Голосовые и двигательные тики бывают одновременно и по отдельности, их частота, количество и сложность постоянно меняется. Они могут обостряться при стрессе, возникать в процессе сна, подавляться произвольно.
Голосовые тики обладают взрывчатой вокализацией, иногда звучат непристойные слова и целые фразы, что получило название «копроламия». Это может сопровождаться и соответствующими неприличными жестами, и такое явление тоже имеет свое наименование «копропраксия». Такое, к счастью, встречаются у небольшого количества больных.
Важно знать следующее:
- наличие тиков не оказывает влияние на умственное развитие ребенка и не свидетельствует о низком интеллекте;
- тики не связаны с энцефалитами, двигательными расстройствами, интоксикациями;
- ребенок быстрее справится с синдромом, если его будут поддерживать в семье, школе и в обществе;
- самые тяжелые тики не являются явным индикатором умения ребенка справляться с разными ситуациями и качеством учебы в школе.
Следует также понимать, что не все тики - признак синдрома.
Детская болезнь в жизни взрослых
Раньше синдром Жиля де ла Туретта считался странным и достаточно редким заболеванием. Страдающих им людей называли бесноватыми, ассоциировались они с выкрикиванием ругательств и нецензурных слов.
В наше время данная болезнь встречается часто, но диагностировать ее тяжело, потому что, в основном, протекает она в легкой форме. Первые симптомы появляются у детей 4-8 лет, но иногда может быть и позже. Частота тиков и их интенсивность с возрастом меняется и к 18 годам должна исчезнуть. Половина больных вступает «во взрослость» уже полностью избавившись от этого синдрома, а другой ничего не остается делать, кроме как на всей протяжении жизни как-то с ней сосуществовать. Полный синдром Туретта, то есть его тяжелая форма, бывает крайне редко.
Легкая степень данной болезни была у писателя Сэмюэля Джонсона, анализ исторических документов доказывает ее наличие у императоров Клавдия, Петра Первого, Наполеона, драматурга Мольера, композитора Моцарта.
Сейчас демонстрируют синдром Туретта известные люди, среди которых есть два знаменитейших футболиста. Скорее всего, нет такого человека, который бы не знал футболиста Дэвида Бекхэма. Он часто без повода выкрикивает бранные слова, ничего не в состоянии с этим поделать. Такая же проблема имеется и у другого футболиста - вратаря Тима Хаварда, у которого время от времени руки двигаются помимо его желания. Однако такая проблема не мешает ему поставить рекорд - у него самое большое количество «сухих» матчей в Англии.
Лечение обязательно
Родители должны понимать, что синдром Туретта - болезнь, на которую нельзя не обращать внимание. Лечения не требует только самая легкая форма заболевания. Но у большого количества больных синдром Туретта сочетается с СГДВ, агрессивностью, тревожностью. У детей могут возникнуть трудности в обучении, так как даже слабые тики их смущают и не дают сосредоточиться. Это сказывается на качестве жизни и взаимоотношениях с друзьями и одноклассниками. Именно поэтому стоит обратиться к специалисту.
Синдром Туретта лечение предполагает следующее:
- психотерапия - поведенческая, рациональная, групповая и индивидуальная, семейная;
- тренировка сдерживания - устранение тика ему же подобным, управление им;
- прием лекарственных препаратов.
Полное излечение на данный момент невозможно. Рядом с ребенком, имеющим такое заболевание, должны находиться люди, хорошо знающие о синдроме (родители, близкие, воспитатели, учителя), которые создают ему поддерживающую обстановку в доме, детском саду, школе. Окружающие должны привыкнуть к тикам, не заострять на них внимания, и они, как правило, со временем уйдут.
Синдром Гийена — Барре - симптомы и лечение
Что такое синдром Гийена — Барре? Причины возникновения, диагностику и методы лечения разберем в статье доктора Жуйкова Александра Вячеславовича, невролога со стажем в 21 год.
Над статьей доктора Жуйкова Александра Вячеславовича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
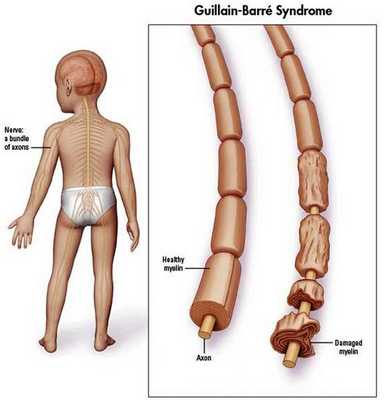
Синдром Гийена — Барре (ГБС) — острое аутоиммунное заболевание, которое охватывает группу острых нарушений периферической нервной системы. Характеризуется мышечной слабостью, а также болью и ползанием мурашек в начале болезни из-за поражения чувствительных волокон. Каждый вариант нарушений характеризуется особенностями патофизиологии и клинического распределения слабости в конечностях и черепных нервах.
Распространённость синдрома Гийена — Барре
Синдром Гийена — Барре встречается в 1-2 случаях на 100 000 населения в год. [10]
Причины синдрома Гийена — Барре
Точная причина синдрома Гийена — Барре неизвестна. Но у 70% пациентов с ГБС наблюдались предшествующие инфекционные заболевания: респираторные, желудочно-кишечные инфекции, вирус Зика. Также синдром Гийена — Барре может развиться после заражения коронавирусом. [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Гийена — Барре
Симптомы ОРВИ или расстройства желудочно-кишечного тракта отмечаются у 2/3 пациентов. Первыми симптомами ГБС являются парестезии пальцев конечностей, за которыми следует прогрессирующая слабость мышц нижних конечностей и нарушения походки. Болезнь прогрессирует в течение нескольких часов или дней, возникает слабость верхних конечностей и развиваются паралич черепных нервов. Параличи обычно симметричны и носят, конечно, периферический характер. У половины пациентов боль может быть первоначальной жалобой, что затрудняет диагноз. Атаксия и боль чаще встречаются у детей, чем у взрослых. Задержка мочи наблюдается у 10%-15% больных. Поражение вегетативных нервов проявляются головокружениями, гипертонией, чрезмерным потоотделением и тахикардией.
При объективном обследовании выявляется восходящая мышечная слабость, а также арефлексия. Сухожильные рефлексы нижних конечностей отсутствуют, но рефлексы верхней конечности могут вызываться. Мышечная слабость может задействовать и респираторные мышцы. Поражение черепных нервов отмечается в 35-50%, вегетативная нестабильность в 26%-50%, атаксия — в 23%, дизестезия — в 20% случаев. [1]
Наиболее распространенными признаками вегетативной дисфункции являются синусовая тахикардия или брадикардия и артериальная гипертония. У пациентов с тяжелой вегетативной дисфункцией наблюдаются изменения периферического вазомоторного тонуса с гипотензией и лабильностью артериального давления.
Нечастые варианты клинического течения болезни включают лихорадку в начале неврологических симптомов, тяжелую сенсорную недостаточность с болью (миалгии и артралгии, менингизм, корешковая боль), дисфункции сфинктеров.
Возможность ГБС должна рассматриваться у любого пациента с быстрым развитием острой нервно-мышечной слабости. На ранней стадии ГБС следует отличать от других заболеваний с прогрессирующей симметричной мышечной слабостью, включая поперечный миелит и миелопатию, острую токсическую или дифтеритическую полиневропатию, порфирию, миастению и нарушения электролитного обмена (например, гипокалиемия).
Патогенез синдрома Гийена — Барре
Нейрофизиологические процессы, лежащие в основе ГБС, подразделяются на несколько подтипов. Наиболее распространенные подтипы включают:
- острую воспалительную демиелинизирующую полирадикулопатию;
- острую двигательную аксональную невропатию;
- острую моторную и сенсорную аксональную нейропатию;
- синдром Миллера-Фишера, как вариант ГБС, характеризуется триадой признаков: офтальмоплегия, атаксия и арефлексия.
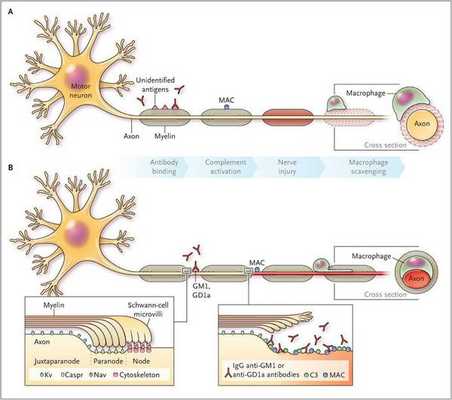
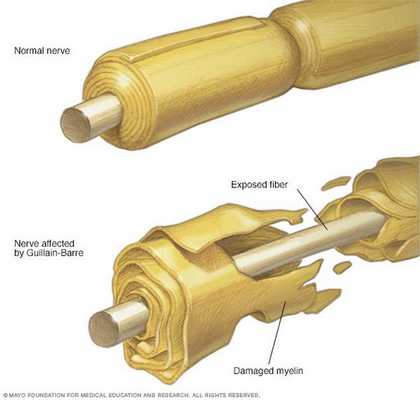
Считается, что ГБС развивается вследствие выработки антител против белка инфекционного агента, которые перекрестно реагируют с ганглиозидами нервных волокон человека. Аутоантитела связываются с миелиновыми антигенами и активируют комплемент, с формированием мембранно-атакующего комплекса на внешней поверхности клеток Шванна. Повреждение оболочек нервных стволов приводит к нарушениям проводимости и мышечной слабости (на поздней стадии может происходить и аксональная дегенерация). Демиелинизирующее поражение наблюдается по всей длине периферического нерва, включая нервные корешки.
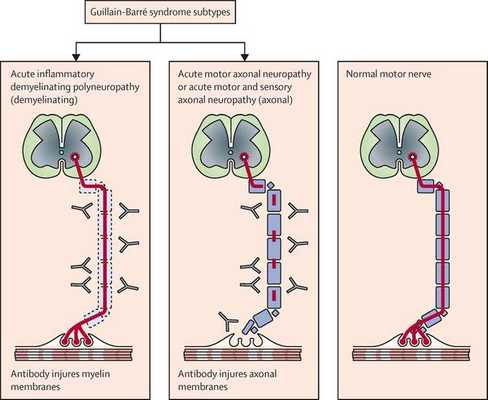
Поражаются все типы нервов, в том числе вегетативные, моторные и сенсорные волокна. Вовлечение двигательных нервов происходит значительно чаще, чем сенсорных.
Классификация и стадии развития синдрома Гийена — Барре
В Международной классификации болезней (МКБ-10) синдром Гийена — Барре кодируется как G61.0.
Основные виды синдрома Гийена — Барре:
- Острая воспалительная демиелинизирующая полирадикулоневропатия (ОВДП) — самая распространённая форма в Северной Америке и Европе. Основным признаком ОВДП является мышечная слабость, которая сперва возникает в нижней части тела, а затем распространяется вверх.
- Синдром Миллера Фишера — проявляется параличом глаз и неустойчивостью походки. Эта форма более распространена в Азии.
- Острая моторная аксональная невропатия (ОМАН) и острая моторно-сенсорная аксональная невропатия (ОМСАН) — чаще встречаются в Китае, Японии и Мексике. [8]
Осложнения синдрома Гийена — Барре
Пациенты с ГБС подвержены риску опасных для жизни респираторных осложнений и вегетативных нарушений.
Показания для перевода в отделение интенсивной терапии включают:
- быстрое прогрессирование моторной слабости с поражением респираторных мышц;
- вентиляционную дыхательную недостаточность;
- пневмонию;
- бульбарные расстройства;
- тяжелую вегетативную недостаточность.
Осложнения проводимого лечения, требующие интенсивной терапии, включают перегрузку жидкостью, анафилаксию на введение внутривенного иммуноглобулина или гемодинамические нарушения при проведении плазмафереза.
У 15%-25% детей с ГБС развивается декомпенсированная дыхательная недостаточность, которая требует механической вентиляции легких. [2] Респираторные нарушения чаще встречается у детей с быстрым прогрессированием заболевания, слабостью верхних конечностей, вегетативной дисфункцией и поражениями черепных нервов. Интубация трахеи может потребоваться у больных для защиты дыхательных путей, проведения механической вентиляции легких. При ГБС быстрое прогрессирование, двусторонний паралич лицевого нерва и вегетативная дисфункция предопределяют повышенную вероятность интубации. Необходимо планирование ранней интубации для минимизации риска осложнений и необходимости проведения экстренной интубации.
Вегетативная дисфункция повышает риск эндотрахеальной интубации. С другой стороны, дисавтономия может увеличить риск гемодинамических реакций на препараты, используемые для индукции анестезии во время интубации.
Признаки, указывающие на необходимость механической вентиляции легких: [4]
- вентиляционная дыхательная недостаточность;
- увеличение потребности в кислороде для поддержания SpO2 выше 92%;
- признаки альвеолярной гиповентиляции (PCO2 выше 50 мм. рт. ст.);
- быстрое снижение жизненной емкости на 50% по сравнению с исходным уровнем;
- невозможность кашля
Вегетативная дисфункция является основным фактором смертности при ГБС. Фатальный сердечно-сосудистый коллапс из-за вегетативной дисфункции наблюдается у 2%-10% тяжелобольных пациентов. [3] Мониторинг частоты сердечных сокращений, артериального давления и электрокардиограммы следует продолжать до тех пор, пока пациенты нуждаются в респираторной поддержке. Чрескожная кардиостимуляция может потребоваться при выраженной брадикардии. Гипотония корректируется восполнением объема циркулирующей крови (ОЦК), и, если пациент невосприимчив к восполнению ОЦК, применяются α-агонисты, такие как норадреналин, мезатон, адреналин.
При нестабильной гемодинамике непрерывная регистрация артериального и центрального венозного давления должна проводиться для контроля объема инфузионной терапии.
Артериальная гипертензия может возникать, но это осложнение не требует специального лечения, если оно не осложняется отеком легких, энцефалопатией или субарахноидальным кровоизлиянием.
Диагностика синдрома Гийена — Барре
Сбор жалоб и анамнеза
На приёме врач в первую очередь обратит внимание на скорость распространения паралича и нарушение дыхания. Если эти признаки выражены, больному может потребоваться экстренная помощь.
Как правило, пациенты с синдромом Гийена — Барре жалуются на нарушение походки, онемение и зябкость ног, а затем и рук. Нередко пациенты рассказывают, что недавно перенесли ОРВИ.
Осмотр
Объективный неврологический осмотр — это основа диагностики при синдроме Гийена — Барре. Врач оценивает рефлексы, координацию движений, походку, чувствительность и мышечную силу.
Лабораторная диагностика
Основным видом лабораторной диагностики при синдроме Гийена — Барре является исследование спинномозговой жидкости, которую получают с помощью люмбальной пункции.
Инструментальная диагностика
ЭНМГ (Электронейромиография) — единственный инструментальный метод диагностики, позволяющий подтвердить диагноз ГБС и уточнить характер патологических изменений (демиелинизирующий или аксональный) и их распространенность. [3]
Игольчатая электромиография характеризуется наличием признаков текущего денервационно-реиннервационного процесса при полинейропатии. Исследуют дистальные мышцы верхних и нижних конечностей (например, переднюю большеберцовую мышцу, общий разгибатель пальцев), а при необходимости и проксимальные мышцы (например, четырёхглавую мышцу бедра).
ЭНМГ-исследование у больных с ГБС зависит от клинических проявлений:
- при дистальных парезах исследуются длинные нервы на руках и ногах: не менее четырех двигательных и четырех чувствительных (двигательные и чувствительные порции срединного и локтевого нервов; малоберцовый, большеберцовый, поверхностный малоберцовый и икроножный нервы с одной стороны).
Оценка основных ЭНМГ- параметров:
Первые признаки денервационного процесса появляются через две-три недели после начала заболевания, признаки реиннервационного процесса — через месяц.
Дифференциальная диагностика
Синдром Гийена — Барре следует отличать от следующих заболеваний:
- и клещевого энцефалита (чувствительность не нарушена, поражены преимущественно черепные нервы); (отягощённый эпидемиологический анамнез, например посещение эндемичных стран); (чувствительность не нарушена, рефлексы снижены незначительно);
- обменно-метаболических полиневропатий (течение хроническое).
Лечение синдрома Гийена — Барре
Показания для госпитализации
Практически во всех случаях требуется госпитализация. Экстренная госпитализация необходима пациентам с нарушениями дыхания — в таких случаях лечение проводят в условиях реанимации.
Общие принципы лечения синдрома Гийена — Барре
Лечение острой демиелинизирующей полирадикулоневропатии комплексное. Основа — плазмаферез, иммуноглобулины и кортикостероиды. В ряде случаев требуется искусственная вентиляция лёгких, коррекция нарушений кровообращения, профилактика инфекционных и тромбоэмболических осложнений. Обязательным условием успешного лечения является уход.
Общее поддерживающее лечение и уход
Пациенты, требующие интенсивной терапии, требуют тщательного общего ухода. Запор наблюдается более чем в 50% случаев пациентов с ГБС в результате динамической непроходимости кишечника. Может потребоваться искусственное питание.
Медикаментозное лечение и плазмаферез
В лечении ГБС предпринимаются различные виды иммуномодулирующей терапии. [1] [2]
Внутривенный иммуноглобулин назначают в виде ежедневной инфузии (в дозе 0,4 гр/кг/день) в течение 5 дней в первые 2 недели болезни. Второй курс иммуноглобулина может потребоваться 5%-10% пациентов, при отрицательной динамике после первоначального улучшения. Механизм действия внутривенного иммуноглобулина, вероятно, многофакторный и, как полагают, включает модуляцию активации комплемента, нейтрализацию идиотипических антител, подавление воспалительных медиаторов (цитокины, хемокины).
Побочные эффекты иммуноглобулина включают головную боль, миалгию и артралгию, гриппоподобные симптомы, лихорадку. У пациентов с дефицитом IgA может развиться анафилаксия после первого курса внутривенного иммуноглобулина.
Плазмаферез способствует удалению антител, вовлеченных в патогенез ГБС. В течение каждого сеанса 40-50 мл/кг плазмы заменяют смесью 0,9% раствора хлорида натрия и альбумина. Проведение плазмафереза приводит к сокращению времени выздоровления и снижению потребности в искусственной вентиляции. Эти преимущества очевидны, если плазмаферез проводится в течение первых двух недель после начала болезни. Осложнения, связанные с плазмаферезом, включают гематому в области венопункции, пневмоторакс после катетеризации подключичной вены и сепсис. Плазмаферез противопоказан пациентам с тяжелой гемодинамической нестабильностью, кровотечением и сепсисом. Комбинация плазмафереза и иммуноглобулина не показала клинических преимуществ.
Симптоматическое лечение синдрома Гийена — Барре:
- при боли применяют парацетамол;
- катадолон и трамадол применяют при выраженном болевом синдроме;
- при нейропатической боли эффективны карбамазепин и габапентин.
Оперативное лечение
При тяжёлом течении может потребоваться длительная респираторная поддержка и наложение трахеостомы. Если пациент находится на искусственном питании, то накладывают гастростому.
Прогноз. Профилактика
ГБС остается серьезным заболеванием, несмотря на улучшение результатов лечения. По сравнению со взрослыми, у детей чаще отмечается более благоприятное течение заболевания, с полным, а не частичным выздоровлением. Причинами неблагоприятного исхода при ГБС являются дыхательная недостаточность, осложнения искусственной вентиляции легких (пневмония, сепсис, острый респираторный дистресс-синдром и тромбоэмболические осложнения), остановка сердца, вторичная по отношению к дисавтономии.
Восстановление обычно начинается через две-четыре недели после прекращения прогрессирования симптомов. Среднее время от начала заболевания до полного выздоровления составляет 60 дней. Данные относительно долгосрочного исхода ГБС ограничены. 75% - 80% пациентов полностью выздоравливают. Около 20% пациентов не могут ходить через полгода.
Младшая возрастная группа (менее 9 лет), быстрое прогрессирование и максимальная мышечная слабость, потребность в искусственной вентиляции легких являются важными предикторами длительного двигательного дефицита. [4]
Синдром Герстмана-Штраусслера-Шейнкера

Синдром (болезнь) Герстмана-Штраусслера-Шейнкера, или синдром ГШШ - нейродегенеративное прионное заболевание. За этим исчерпывающим и сугубо специальным определением скрывается тяжелая, редкая, в некоторых отношениях уникальная патология, и хотя бы поэтому каждое слово заслуживает более подробного рассмотрения.
Дегенерацией, - применительно к единичному организму, - называют патологический процесс перерождения (вырождения) на клеточном уровне, в ходе которого та или иная ткань постепенно утрачивает нормальную, естественную для нее структуру, становясь все более примитивной по строению и все хуже справляясь с возложенными на нее функциями. Как правило, такие процессы обусловлены нарушениями клеточного метаболизма (дистрофия) и/или дефицитом кровоснабжения (ишемия), конечным результатом чего является полная деградация, сокращение в объеме и отмирание (атрофия, некроз, инфаркт) паренхиматозной, т.е. функциональной, узкоспециализированной ткани какого-либо органа. Соответственно, термином «нейродегенеративные заболевания» обозначают большую группу болезней, обычно наследственных и на сегодняшний день неизлечимых, при которых дегенерирует сложнейшая паренхима центральной нервной системы, т.е. нейронное вещество спинного и/или головного мозга, а также нервных узлов и сплетений периферической нервной системы. Начинаясь, как правило, с незначительных нарушений памяти, речи, моторных функций, большинство таких заболеваний в терминальной стадии обусловливают тотальную деменцию (органическое слабоумие) и сугубо вегетативное существование пациента. К наиболее известным нейродегенеративным процессам относятся болезни Альцгеймера, Пика, Паркинсона, амиотрофический боковой и рассеянный склероз, и пр.
Прионные же заболевания, или спонгиоформные (губчатые) энцефалопатии - совершенно особый вид нейродегенерации, причиной которого является недавно открытые (1982) белки-прионы, до сих пор остающиеся предметом интенсивных научных дискуссий: некоторые исследователи склонны считать прионы особой формой жизни, другие рассматривают их исключительно как биохимический феномен. Так или иначе, но прионные молекулы способны in vivo модифицировать другие белки таким образом, что те превращаются в идентичные прионы; в результате клетка погибает, а ткань в целом вырождается в пористую биомассу, не имеющую никакого отношения к первоначальной специализации. Поскольку этот процесс прогрессирует в веществе головного мозга (причем значительно быстрее, чем другие виды нейродегенерации), его проявления и последствия трудно назвать иначе, как катастрофическими. Широкую огласку получили прионные эпизоотии сельскохозяйственного скота (овечья почесуха, коровье бешенство), однако прионными оказались и некоторые заболевания человека, ранее приписываемые неизвестным вирусам, - болезнь Крейтцфельдта-Якоба, куру, фатальная семейная инсомния.
Что касается синдрома Герстмана-Штраусслера-Шейнкера, то как самостоятельная нозологическая единица он выделен и описан еще в 1936 году, однако этиопатогенез этой специфической нейродегенерации стал ясен лишь с открытием прионов и осуществлением хромосомных исследований. К счастью, эта патология не просто редка, а встречается исключительно редко: примерно в одном случае на 10 млн населения.
2. Причины
Наряду с фатальной семейной бессонницей и генетическим вариантом болезни Крейтцфельдта-Якоба, синдром ГШШ является не трансмиссивным (заразным), а наследственным заболеванием. Дефектный ген PRPN запускает «цепную реакцию» воспроизводства белков-прионов в мозговой ткани. Как правило, это происходит в возрастном интервале от 20 до 60 лет, однако о реальной распространенности, о возрастных закономерностях, о влиянии фактора пола и других характеристиках процесса трудно судить с уверенностью, поскольку накопленный объем наблюдений, по статистическим меркам, совершенно недостаточен.
3. Симптоматика, диагностика
Некоторые клинические и патоморфологические особенности синдрома ГШШ роднят его с болезнью Альцгеймера, другие - с различными нейродегенеративными формами атаксии (неупорядоченности, двигательной дискоординации). Это дополнительно осложняет диагностику и, видимо, нередко приводит к диагностическим ошибкам, которые могут быть однозначно устранены только при посмертном патоморфологическом исследовании.
В симптоматике выявляются феномены, характерные как для органического поражения мозжечка (нарушения координации движения, способности к пространственной ориентации), так и т.н. бульбарная симптоматика, специфическая для поражений продолговатого мозга: ослабление и постепенное отмирание глотательного рефлекса, прогрессирующие нарушения артикуляторных составляющих речи и т.д. В терминальной стадии клиническая картина носит столь же тотальный и катастрофический характер, как и при других видах нейродегенерации. Однако от сходных заболеваний именно прионного генеза синдром ГШШ отличается более медленным течением: усредненный период от манифестации до летального исхода составляет примерно 5-6 лет (в разбросе от 3 месяцев до 13 лет).
4. Лечение
Синдром Туретта - симптомы и лечение
Что такое синдром Туретта? Причины возникновения, диагностику и методы лечения разберем в статье доктора Диордиева Максима Борисовича, психиатра со стажем в 8 лет.
Над статьей доктора Диордиева Максима Борисовича работали литературный редактор Вера Васина , научный редактор Владимир Вожжов и шеф-редактор Маргарита Тихонова
Синдром Туретта (Tourette's syndrome) — это заболевание нервной системы, при котором возникают множественные двигательные и вокальные тики. Для постановки диагноза они должны присутствовать дольше года.

Впервые заболевание, похожее на синдром Туретта, было описано в 1486 году в книге «Молот ведьм». Там упоминался священник с моторными и вокальными тиками, считавшийся одержимым. В конце XIX века симптомы заболевания на примере нескольких пациентов описал вместе с коллегами французский невролог Жорж Жиль де ла Туретт, в честь которого и назван синдром [1] .
Обычно синдром Туретта проявляется уже в детстве, но часто заболевание выявляют поздно или не диагностируют вовсе, так как родители не обращают на тики должного внимания. Из-за этого маленькие пациенты не получают своевременной помощи и могут страдать не только от самих тиков, но и от психологических проблем, связанных с заболеванием. В Европе от возникновения первых симптомов синдрома Туретта до постановки диагноза проходит в среднем более 5 лет [2] .
Распространённость синдрома Туретта
Синдром Туретта очень распространён — он встречается примерно у 10 из 1000 детей. В России его диагностируют у 8 человек на 10 000 населения, им могут страдать до 5 % школьников [3] . Мужчины болеют чаще, чем женщины: соотношение между ними составляет примерно 3 к 1.
Причины синдрома Туретта
Синдром Туретта — это генетическое расстройство, которое передаётся от родителей. Однако точный механизм наследования и ген, ответственный за болезнь, не известны. Риск передачи заболевания ребёнку составляет около 50 %. В прошлом, в начале XX века, тики считались следствием психотравм, но современная медицина это отвергает, так как такое предположение не удалось доказать [4] . Психосоциальные факторы и аутоиммунные заболевания не являются причиной синдрома Туретта, но могут влиять на тяжесть течения болезни.
Существует теория, что недостаток магния в организме и связанные с ним нарушения обмена веществ могут влиять на развитие синдрома Туретта. Косвенным доказательством этого служит то, что препараты с некоторыми соединениями магния могут улучшать состояние больных. Однако большие исследования на эту тему не проводились [5] .
Симптомы синдрома Туретта
Синдром Туретта проявляется тиками — быстрыми, внезапными, повторяющимися навязчивыми движениями или произнесением звуков. Чаще всего они возникают у мальчиков в возрасте от 4 до 11 лет. Тяжесть тиков доходит до пика примерно в 10-12 лет и ослабляется в подростковом возрасте. Большинство тиков исчезают спонтанно, но примерно у 1 % детей они сохраняются во взрослой жизни [7] .
Выделяют две основные группы тиков:
- Моторные тики — это непроизвольные движения частей тела. Самый распространённый из них — усиленное моргание. Также могут возникать подпрыгивания, постукивания по себе, развороты и повороты тела, гримасы, плевки, нецензурная жестикуляция и повторения чужих движений (копропраксия и эхопраксия).
- Вокальные, или звуковые, тики — это навязчивое произношение звуков, реже слов. Может проявляться кашлем, покашливанием, кряхтением. Иногда таких детей ошибочно лечат от бронхитов, трахеитов и бронхиальной астмы. Синдром Туретта часто ассоциируется с копролалией — внезапным высказыванием нецензурных фраз или слов, которое зачастую сопровождается копропраксией. Однако копролалия возникает только у 10 % пациентов [6] . Помимо копролалии, они могут повторять чужие слова, собственное слово или фразу (эхолалия и палилалия).
При синдроме Туретта моторные тики обязательно сочетаются с вокальными. Если присутствуют моторные тики, но нет вокальных, то стоит заподозрить другие заболевания: органическое поражение головного мозга, эпилепсию, синдром дефицита внимания (СДВГ), обсессивно-компульсивное расстройство (ОКР).
У многих детей и подростков с синдромом Туретта также отмечается СДВГ, ОКР, повышенная агрессивность, тревожность и склонность к депрессиям.
При синдроме Туретта интеллектуальные способности не нарушаются. Дети с этим заболеванием могут сильно расстраиваться от подшучиваний своих сверстников. При эмоциональном напряжении, вызванном пристальным вниманием или насмешками окружающих, тики могут усиливаться.
Форма тиков при синдроме Туретта может меняться в течение суток или недели, например от лёгких единичных моторных тиков утром или в начале недели до сложных и множественных по вечерам или под конец учебной недели. Видимо, их выраженность зависит в том числе от психоэмоциональных нагрузок.
Иногда дети пытаются сдерживать тики, но такой контроль возможен лишь в некоторой степени. Когда ребёнок старается подавить тики, симптомы могут усилиться. Попытка сдержать тик вызывает выраженный дискомфорт, из-за чего возрастает тревога — тикозные движения, наоборот, немного успокаивают. Из-за стресса, тревожных состояний и усталости тики могут учащаться и усиливаться.
Патогенез синдрома Туретта
Патогенез синдрома Туретта до конца не изучен. Известно лишь, что расстройство вызвано генетическими причинами. Скорее всего, при определённых генетических факторах нарушается работа нейромедиаторных систем в подкорковых образованиях и лобной коре.
Помимо генетических факторов, в патогенезе может участвовать и органическое повреждение головного мозга, например при патологии беременности и родов, черепно-мозговых травмах или нейроинфекциях.
Основная роль в патогенезе заболевания, вероятно, принадлежит дисфункции лобных долей. Считается, что большую роль в развитии синдрома Туретта играет правая лобно-височная область, сенсомоторные отделы орбитофронтальной коры, моторная область, базальные ганглии и поясная извилина. Также важное значение имеют нарушения в кортико-стрио-таламо-кортикальном контуре — нейронных цепях, связывающих кору, базальные ганглии и таламус.

Нарушения в работе этих структур также характерны для детей с ОКР и СДВГ — эти заболевания часто сопутствуют синдрому Туретта. Даже известны генетически связанные с синдромом Туретта формы ОКР (преимущественно ОКР с навязчивыми действиями — F42.1).
Предположительно, при синдроме Туретта нарушается работа дофаминергической системы. Изменения, вероятно, затрагивают серотонин-, норадреналин-, глутамат-, холин-, ГАМКергическую и опиоидную системы. Косвенно на связь синдрома Туретта с дофамином указывает то, что тики уменьшаются при лечении препаратами, которые воздействуют на передачу нервного импульса, вызванную дофамином ( например, путём блокады постсинаптических D2-рецепторов) [2] .
Классификация и стадии развития синдрома Туретта
Синдром Туретта — это разновидность хронических тиковых (или тикозных) нарушений. В Международной классификации болезней (МКБ-10) заболевание кодируется как F95.2 Комбинированные голосовые и множественные двигательные тики.
В следующей Международной классификации болезней (МКБ-11) тики и синдром Туретта из психических расстройств перенесены в неврологические [1] .
Согласно классификации Американской психиатрической ассоциации (DSM-IV), тики подразделяются на следующие группы:
- по виду — двигательные или голосовые;
- по продолжительности — преходящие или хронические.
Преходящее тиковое расстройство — это множественные двигательные, голосовые или тики обоих видов, которые длятся от 1 до 12 месяцев. Хронические тиковые расстройства присутствуют больше года. Они могут быть одиночными или множественными, двигательными или голосовыми, но не оба вида сразу. Синдром Туретта относится к хроническому тиковому расстройству. Для постановки диагноза необходимо, чтобы множественные двигательные тики и хотя бы один голосовой тик наблюдались более года.
Стадии синдрома Туретта не выделяют. Но обычно расстройство начинается с преходящих двигательных тиков, как правило подёргивания лица, которые длятся до года. Часто это гримасничание, затем покашливание и шипение. Постепенно тики распространяются на руки, ноги и мышцы шеи. Затем, обычно через год, присоединяются вокальные тики, которые осложняют картину болезни.
Осложнения синдрома Туретта
Синдром Туретта может сопровождаться депрессией, тревожным расстройством, ОКР и СДВГ, что осложняет прогноз. Депрессия возникает из-за того, что детей с этим синдромом часто обижают и унижают. В результате у них формируется чувство одиночества и может развиться аутоагрессия, вплоть до попытки суицида. Поэтому важно не оставлять ребёнка один на один с этим расстройством: ему особенно необходима поддержка родителей и друзей.
При симптоме копролалии дети выкрикивают нецензурную брань, из-за чего могут подвергаться агрессии со стороны окружающих. Поэтому для таких пациентов очень важно организовать правильную социальную среду [7] .
Диагностика синдрома Туретта
Синдром Туретта диагностирует врач-психиатр или невролог, основываясь на наблюдении и сборе сведений об истории болезни, условиях жизни и перенесённых заболеваниях. Сейчас разрабатываются генетические карты, которые позволят с самого рождения определять совокупность генов, характерных для синдрома Туретта, но пока этот метод недоступен.
Чтобы установить диагноз «синдром Туретта», состояние должно соответствовать следующим критериям:
- присутствуют множественные двигательные тики и как минимум один голосовой тик;
- тики возникают много раз в день, почти ежедневно;
- расстройство длится более года, но необязательно непрерывно, ремиссии продолжаются меньше двух месяцев;
- симптомы появились в возрасте до 18 лет [8] .
Очень важно отличать тики при синдроме Туретта от вторичных тиков, которые появились на фоне инфекций или черепно-мозговых травм при беременности, родах или в раннем детстве. Их различают только на основе анамнеза и физикального обследования. Другие методы, например магнитно-резонансная томография и анализы крови, для диагностики синдрома Туретта не используются.
Лечение синдрома Туретта
Перед врачом всегда стоит выбор — назначать ли препараты при синдроме Туретта. При этом важно ориентироваться на состояние пациента, так как более чем в половине случаев симптомы исчезают без приёма медикаментов.
Психологическая помощь
Если тики не мешают человеку общаться, учиться и работать, то, скорее всего, принимать препараты не нужно. В такой ситуации будет полезно психологическое консультирование ребёнка и родителей. Важно рассказать родителям, что от ребёнка ни в коем случае нельзя требовать, чтобы он перестал кашлять и гримасничать, — это только усилит эмоциональное напряжение и, соответственно, тики.
В зарубежных странах, особенно в США, хорошо зарекомендовал себя метод под названием «Habit reversal training», т. е. тренировка отмены привычки [10] . Пациента учат отслеживать ощущение, предшествующее тикам, и пытаться заменить их на более приемлемые действия. Метод не избавляет от тиков, но заметно уменьшает их проявления.
Также для коррекции поведения используется когнитивно-поведенческая психотерапия [12] .
Медикаментозное лечение
Для лечения синдрома Туретта могут применяться антипсихотики (нейролептики) в невысоких дозировках, которые воздействуют на дофаминэргическую активность. Наиболее эффективны Арипипразол, Рисперидон и Галоперидол. Из них лучше всего переносится Арипипразол. Однако в российских инструкциях по лечению синдрома Туретта это лекарство не упоминается, хотя в США оно одобрено Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) и активно используется в терапии. В России назначают Галоперидол и Рисперидон, а также ряд ноотропов (чаще всего гопантеновую и аминофенилмасляную кислоту) без достаточной доказательной базы.
Есть данные об эффективности Клонидина, но этот препарат опасен при передозировке. Среди возможных побочных эффектов — коллаптоидные состояния, т. е. резкое падение артериального давления, которое может привести к развитию обморока.
Существуют не подтверждённые данные об эффективности инъекции ботулотоксина в мышцы лица.
При возникновении сопутствующих заболеваний, таких как тревожно-депрессивное расстройство и ОКР, применяются селективные ингибиторы обратного захвата серотонина: Сертралин, Пароксетин, Эсциталопрам. При выраженной агрессии, направленной на себя или окружающих, назначаются нормотимики (препараты лития и другие) [12] .
Транскраниальная магнитная стимуляция
В настоящее время изучается влияние транскраниальной магнитной стимуляции на синдром Туретта как у детей, так и у взрослых, но пока недостаточно данных об эффективности этого метода [11] .
Нейрохирургическое лечение
При тяжёлом течении заболевания и выраженной устойчивости к медикаментам может применяться нейрохирургический подход — глубокая стимуляция подкорковых структур головного мозга (бледного шара и таламуса). Её используют для взрослых пациентов.
Прогноз благоприятнее и заболевание чаще заканчивается ремиссией или выздоровлением, если тики появились в возрасте до 7 лет.
Синдром Туретта часто вызывает у людей страх и ассоциации, что эта особенность мешает нормально общаться с другими. Но если грамотно подойти к терапии и исключить провоцирующие факторы, расстройство может протекать вполне благоприятно. Примером служит певица Билли Айлиш. Из-за тяжести заболевания она не ходила в школу и обучалась дома. Это не помешало певице в 2019 году записать сингл, завоевавший первые места в мировых хит-парадах, а в 2021 году войти в список 100 наиболее влиятельных людей года по версии журнала Time. Также синдромом Туретта, предположительно, страдал Вольфганг Моцарт [13] .
Синдром Туретта — это генетическое заболевание, поэтому предупредить его развитие нельзя. Однако если своевременно обратиться к врачу, можно снизить тяжесть болезни и предотвратить развитие депрессии, аутоагрессии и обсессивно-компульсивного расстройства.
При сильных тиках, не поддающихся лечению и мешающих общаться, учиться или работать, пациент может пройти медико-социальную экспертизу: специалисты оценят тяжесть состояния и, при необходимости, определят группу инвалидности.
Синдром Мея-Тернера
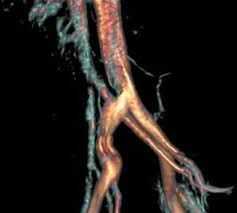
Синдром Мея-Тёрнера - патологическое состояние, которое характеризуется передавливанием левой подвздошной вены малого таза подвздошной артерией. Специалисты считают его сложно диагностируемым, провоцирующим целый ряд серьёзных заболеваний у мужчин и у женщин в виде варикоцеле и варикоза вен малого таза.
Где лечат синдром Мея-Тёрнера? Если Вы столкнулись с этим опасным заболеванием или имеете подозрения на его развитие, обращайтесь в отделение флебологии ЦЭЛТ. Наша клиника является многопрофильной и располагает мощной диагностической и лечебной базой, которая позволяет точно ставить диагноз и проводить лечение синдрома Мея-Тёрнера в Москве в соответствии с международными стандартами.
Причины синдрома Мэя-Тёрнера
Подвздошные вены - это общие парные кровеносные вены, расположенные на уровне крестцово-подвздошного сустава и обеспечивающие отток крови от ног в тазовую область. Они разделяются на правую и левую от брюшной вены и аорты в области крестца и расходятся на внешние и внутренние. Внешние переходят в бедренные вены, внутренние призваны обеспечивать отток крови из тазовых органов.
Синдром Мэя-Тёрнера у мужчин и женщин развивается вследствие придавливания общей подвздошной вены, расположенной с левой стороны, правой артерией к позвоночнику. Он провоцирует нарушения оттока крови из левой ноги и таза и может протекать на фоне атеросклероза стенок кровеносных сосудов. В результате в ноге и половых органах происходит застой крови - и развивается варикоз.
Клинические проявления синдрома Мея-Тёрнера
К сожалению, синдром недостаточно хорошо изучен, поскольку является редким. Специалисты выделяют три стадии его развития:
- Первая - клинические проявления отсутствуют;
- Вторая - просвет подвздошной вены сужается, появляются симптомы венозной недостаточности;
- Третья - развиваются тромбозы.
Симптоматика синдрома - следующая:
- Отёчность левой ноги, нередко - с изменением цвета кожного покрова на синюшний или багровый;
- Интенсивная болевая симптоматика в поражённой области, которую невозможно устранить обезболивающими средствами;
- Заметные невооружённым глазом варикозные узлы на бедре, яичке (у мужчин) или половых губах (у женщин) с поражённой стороны;
- Усиление неприятных ощущений после физических нагрузок, в том числе и несущественных;
- Появление геморроидальных узлов.
И у мужчин и женщин, страдающих от синдрома, возникают проблемы с сексуальными контактами. Так, в первом случае появляются боли тянущего характера в мошонке, которые иррадиируют в мочеиспускательный канал и головку члена и становятся более интенсивными после полового акта. Во втором случае сексуальные контакты становятся и вовсе невозможными из-за болезненности узла.
Диагностика синдрома Мея-Тёрнера
Перед тем, как назначить лечение синдрома Мея-Тёрнера, флебологи ЦЭЛТ проводят комплексные исследования, направленные на постановку правильного диагноза. Для этого пациенту назначают:
Читайте также:
