Синдром Хайльмейера-Шенера (Heilmeyer-Shoner) - синонимы, авторы, клиника
Добавил пользователь Morpheus Обновлено: 28.01.2026
ТЕСТ «У.Д.А.Р.» ПОМОЖЕТ РАСПОЗНАТЬ ИНСУЛЬТ!
Сегодня, 29 октября - всемирный день борьбы с инсультом! Многие знают не понаслышке, насколько это грозное заболевание. До 80% перенесших инсульт становятся инвалидами.
Показать полностью.
Во всех регионах нашей страны открываются и работают сосудистые отделения и региональные сосудистые центры, а значит становится возможным проводить патогенетическую терапию больным с инсультом - тромболизис и тем самым минимизировать возможные тяжелые последствия. Важным моментом является своевременность обращения пациентов с симптомами инсульта в пределах так называемого терапевтического окна - 4,5 часов. К сожалению, многие с опозданием понимают, что случился инсульт.
В мировой практике существует весьма эффективная методика диагностики FAST (face, arm, speech, time), которая позволяет самостоятельно с вероятностью 88% поставить диагноз полушарного инсульта. В нашей стране эта диагностика была известна как УДАР (улыбка, движение, артикуляция, решение).
Для этого не обязательно иметь медицинское образование! В видеоролике дети показывают, как это сделать.
Медицинские консультации запись закреплена
Смартфарма
Лекарственные поражения печени - разнородная группа клинико-морфологических вариантов повреждения печени, причиной развития которых явилось применение лекарственных средств.
Preparatum

Александр Моисеенко
Согласно данным, открыто опубликованным на сайте Посольства США в Украине, в 11 городах страны в период с сентября 2009 по апрель 2013 года за счет средств Министерства обороны США (Пентагона) были открыты 14 лабораторий. Якобы для предотвращения распространения технологий, патогенов и знаний, которые могут быть использованы в ходе разработки биологического оружия».
Показать полностью.
По одной лаборатории было открыто в Киеве, Одессе, Херсоне, Симферополе, Тернополе, Ужгороде, Виннице, Харькове и Луганске. Две лаборатории появились в Днепропетровске и сразу три во Львове.
Интегрирующим подрядчиком строительства всех лабораторий выступила американская компания «Блэк энд Витч» (Black & Veatch). Поставку оборудования и мебели осуществляли 3 украинские компании: «Билобтех», «Макрохим», «Медиамакс». Строили лаборатории 5 украинских компаний: «Одесса Invest», «Проектно-Техничной центр», «РK-Центр», «Project Development Center», «Технопроект», «ЖК - Центр».
Общая стоимость всех лабораторий составляет 26 млн. долларов.
Во всех лабораториях (кроме одесской) более половины затрат составляет строительство. У лабораторий, стоимостью от 1,5 до 1,9 млн. долларов, затраты на оборудование составляют по 400 с лишним тысяч долларов.
В одесской наоборот - на строительство пошло 613 тыс., а на закупку оборудования - 2 млн. долларов!
Примечательно также, что полное совпадение (до одного доллара) затраченных сумм на закупку оборудования значится у лабораторий в Днепропетровске, Львове и Ужгороде: 404 тысячи 078 долларов. И 442 тысячи 977 долларов у херсонской и харьковской лабораториях, построенных к тому же в одном месяце - декабре 2012 года.
Читаем статью Роджерса
Под прикрытием лаборатории для исследования особо опасных патогенов и разработки вакцин США намерено создать военную базу биологической направленности. Ранее аналогичная лаборатория была создана в Грузии.
В 2009 году, в разгар предвыборной кампании на Украине, а заодно в разгар нагнетаемой Тимошенко и её партией паники относительно «атипичного гриппа», я с группой коллег проводил расследование, которое касалось этой эпидемии.
И мы тогда накопали очень много всего интересного. В частности, информацию про фармакологическую корпорацию «Baxter [1]», которая проводила в Украине испытания каких-то таинственных препаратов.
Ту самую корпорацию «Baxter», которая несколько лет назад присылала в африканские страны донорскую кровь, зараженную СПИДом, и которая в 2009 году присылала [2] смесь «птичьего» и «свиного» гриппа вместо вакцины в страны Европы (в частности, в Австрию). По собранной нами информации, эта корпорация занималась испытаниями биологического оружия.
Лаборатории корпорации «Baxter» располагались в районе Тернополя, где как раз было больше всего заболевших «птичьим гриппом», то есть в самом эпицентре эпидемии. И правительству Тимошенко было прекрасно известно про деятельность этой корпорации на территории Украины.
Тогда после придания этой информации огласке деятельность лабораторий по разработке бактериологического оружия была оперативно свёрнута (или перенесена в другие места), а все концы тщательно обрублены.
Но с тех пор у меня сохранились определённые связи. И эти люди недавно передали мне новую информацию, по сравнению с которой прежняя — уже не кажется такой зловещей.
В городе Мерефа Харьковской области некоторое время назад запущен проект по строительству депозитария для исследования и хранения особо опасных патогенов животных и болезнетворных микроорганизмов, разработанный американской компанией «Black and Veatch Special project corp» и финансируемый Министерством обороны США.
Буквально пару месяцев назад на базе «Института экспериментальной и клинической ветеринарной медицины [3]» (ИЭКВМ) в Харькове создана закрытая лаборатория, организованная в подвальном помещении института. Персонал лаборатории состоит из англоязычных иностранцев, преимущественно граждан США. Рядовые сотрудники из числа граждан Украины с ними не общаются и не имеют доступа в помещения лаборатории, куда можно попасть только после нескольких фильтрационных этапов.
ИЭКВМ активно сотрудничает с «Украинским научно-технологическим центром» (УНТЦ), который вопреки названию является иностранной и межправительственной организацией, среди учредителей которой кроме Украины числятся США, Канада и Швеция. А руководителем этой конторы является гражданин США Майкл Зает.
Этот центр поддерживает деятельность украинских учёных и инженеров, ранее вовлечённых в разработку и производство оружия массового уничтожения, а также осуществляет помощь другим высококвалифицированным кадрам, работавшим в оборонной промышленности СССР (в том числе и в других странах СНГ).
В конце 2014 года УНТЦ получил от США и ЕС значительные финансовые средства, часть из которых расходуется на деятельность, осуществляемую в ИЭКВМ.
Прежде, чем остановить свой выбор на Харькове, УНТЦ активно изучал деятельность Симферопольской противочумной станции (к счастью, теперь недоступной для американских интересов), а также проводил семинары в Одессе.
УНТЦ также взаимодействует с многими западными военными организациями, в частности с Польским военным институтом гигиены и эпидемиологии (задействованным во время войны в Афганистане в 2002 году, также занимавшимся эпидемией гриппа в Украине в 2009 году, а также входящим в программу по изучению вируса Эбола), американской лабораторией «Pacific Northwest National Laboratory» (PNNL), занимающейся глобальными вопросами борьбы с терроризмом, и американским же агентством «Defence Threat Reduction Agency» (DTRA), также исследующим лихорадку Эбола и находящимся в подчинении Министерства обороны США.
В январе 2015 года DTRA получило от Минобороны США значительное финансирование на некий неназванный проект, цели и задачи которого засекречены.
«Racoon-city» из фильма «Обитель зла», конечно, переводится с английского не как Харьков, а как Енотов, но это уже такие незначительные тонкости. Если всё это вырвется наружу, то и ощущать иронию момента, и переводить уже будет некому.
Александр Роджерс, специально для «Украина.Ру»
Свиной грипп: геноцид от коммерческой науки
Уже все уши прожужжали про новую гадость - «свиной грипп из Мексики»: руководство повыше отдаёт команды не допустить её в Россию, начальство пониже боязливо отчитывается, что жертв не избежать и у нас. Обсуждать тут было бы нечего, если бы не получил письмо от[info]vladmradio:
«…Добрый день, коллега. Не знаю, входит ли данная тема в круг интересных для Вас, но ввиду последних вирусных мировых событий, возможно, что материалы, о которых я напомню, сегодня достойны внимания. Прошу прощения, если зря отнял время.
Теперь мы наблюдаем некий "свиной" грипп и компанию Бакстер, которая героически с ним борется на переднем крае вирусной войны - в Мексике. Не хочется фантазировать на тему разработки бактериологического оружия. Просто, всё это очень похоже на ещё один способ хорошо заработать на искусственно созданной болезни. Филиалы компании Бакстер представлены на территории России и Украины - вот, именно это и вызывает тревогу…»
А если серьёзно, то, например, версии о появлении того же ВИЧ аналогично восходят к американским медицинским опытам: тренировались на обезьянах - может, хотели сделать такую фигню, которая торкала бы исключительно любителей коммунизма (как версия), а фигня оказалась всеядной и быстренько побежала колошматить обычных граждан, начав, понятно дело, с «продвинутых» - с гомосексуалистов.
Вопрос стоит много шире, нежели просто очередной смертельный вирус - вопрос стоит о том, чтобы запретить коммерческим лабораториям заниматься исследованиями в тех областях, которые касаются искусственного создания болезней. Ведь что сделали в упомянутой конторе: там болезнь человека соединили с болезнью свиньи, и таким образом только свиные, грубо говоря, антибиотики на неё не действуют - равно как и только человеческие. Получился универсальный убийца, справятся с которым нескоро, потому что автор никогда открыто не скажет, что он и создал эту мерзость.
Фактически речь идёт о том, что фармацевтические гиганты могут создавать новый виток глобальной «наркомании»: чтобы вы купили таблетки или ампулы с обычной наркотой, в вашем окружении должен нарисоваться дилер, а в вашей жизни - наступить «чёрная полоса». Обычный дилер может подождать такого стечения обстоятельств, а вот корпорации - нет: им нужен тот, кому жизненно необходимы «наркотики» прямо сейчас! Идеальный вариант - сделать человека зависимым при помощи вируса, болезни, которая уничтожается тем эксклюзивным, запатентованным средством, что есть только у этой корпорации. Конечно, для создания ажиотажа в аптеках нескольким тысячам придётся сдохнуть, но разве велика эта цена за миллионные партии лекарства от искусственной болезни?!
Удивляться такому цинизму уже не приходится - жизнь ничего не стоит, потому что у типового потребителя она и смысла особого не имеет. Если ты живёшь для того, чтобы работать, а работаешь, чтобы жить, то смешна цена такому прозябанию. Впрочем, и у таких животных есть право на жизнь: власти обязаны серьёзно разобраться с коммерческим научным миром и с коммерческими лабораториями, чтобы отобрать у них саму возможность креативить новую заразу.
Конечно, если только коммерческие лаборатории не являются просто неким «научным оффшором», местом, свободным для любых опытов, где спецслужбы занимаются антигуманными исследованиями, прикрываясь брендом. Этакие доктора Менгеле 21-го века. Думаю, как вариант - вполне жизнеспособная версия.
Болезнь Шейермана-Мау ( Юношеский кифоз )
Болезнь Шейермана-Мау - это заболевание, при котором наблюдается прогрессирующее кифотическое искривление позвоночного столба. Возникает в пубертатном возрасте, одинаково часто встречается у мальчиков и девочек. На ранних стадиях симптоматика стертая. В последующем появляются боли и видимая деформация позвоночника - сутулая круглая спина, в тяжелых случаях возможен горб. В отдельных случаях развиваются неврологические осложнения. Для подтверждения диагноза выполняют рентгенографию, КТ и МРТ. Лечение обычно консервативное, при тяжелых деформациях проводятся хирургические вмешательства.
МКБ-10
Общие сведения
Причины
Точные причины болезни Шейермана-Мау неизвестны. Большинство специалистов считают, что существует генетическая предрасположенность к развитию этого заболевания. Наряду с этим, в качестве пусковых моментов рассматриваются травмы в период интенсивного роста, остеопороз позвонков, избыточное развитие костной ткани в заднем отделе позвонков, некроз замыкательных пластинок позвонков и нарушение развития мышц спины. Предрасполагающим фактором являются неравномерные сдвиги гормонального баланса и обмена веществ в пубертатном периоде.
Патанатомия
Человеческий позвоночник имеет четыре естественных изгиба: поясничный и шейный отделы изогнуты вперед (лордозы), крестцовый и грудной - назад (кифозы). Эти изгибы появились в результате приспособления к вертикальному положению тела. Они превращают позвоночник в своеобразную пружину и позволяют ему без вреда переносить разнообразные динамические и статические нагрузки. Углы изгибов в норме составляют 20-40 градусов. Позвоночник состоит из множества отдельных костей (позвонков), между которыми расположены эластичные межпозвонковые диски. Позвонки состоят из тела, дужки и отростков. Массивное тело берет на себя нагрузку, дужка участвует в образовании позвоночного канала, а отростки соединяют позвонки между собой.
В норме тела позвонков имеют почти прямоугольную форму, их задние и передние отделы примерно равны по высоте. При болезни Шейермана-Мау несколько грудных позвонков уменьшаются по высоте в передних отделах, приобретают клиновидную форму. Угол грудного изгиба увеличивается до 45-75 градусов. Спина становится круглой. Нагрузка на позвоночник перераспределяется. Ткань межпозвонкового диска «продавливает» замыкательную пластинку и выпячивается в тело ниже- или вышележащего позвонка, образуются грыжи Шморля. Связки, удерживающие позвонки, компенсаторно утолщаются, что еще больше затрудняет восстановление и дальнейший нормальный рост позвонков. Форма грудной клетки меняется, что может приводить к сдавливанию внутренних органов.
Классификация
В травматологии и ортопедии различают следующие стадии болезни Шейермана-Мау:
С учетом уровня поражения различают:
- Грудную форму. Выявляется поражение нижних и средних грудных позвонков.
- Пояснично-грудную форму. Поражаются верхние поясничные и нижние грудные позвонки.
Симптомы
Первые проявления болезни Шейермана-Мау появляются в период полового созревания. Как правило, пациент в этот период жалоб не предъявляет. Патология обнаруживается случайно, когда родители замечают, что ребенок начал сутулиться и у него ухудшилась осанка. Примерно в это время больной начинает отмечать неприятные ощущения в спине, возникающие после продолжительного пребывания в положении сидя. Иногда возникают неинтенсивные боли между лопатками. Подвижность позвоночника постепенно ограничивается.
Со временем деформация позвоночника становится все более заметной. Возникает выраженная сутулость, в тяжелых случаях образуется горб. Интенсивность болевого синдрома возрастает, ребенок отмечает постоянную тяжесть и быструю утомляемость спины при нагрузках. Боли усиливаются под вечер и при поднятии тяжестей. При значительном искривлении позвоночника возможно нарушение функций легких и сердца. В отдельных случаях возникает подострое или острое сдавление спинного мозга, сопровождающееся парестезиями, нарушениями чувствительности и движений конечностей.
Диагностика
Врач опрашивает пациента с подозрением на болезнь Шейермана-Мау, выясняя жалобы, историю развития патологии и семейный анамнез (были ли случаи заболевания в семье). Ведущим методом инструментальной диагностики является рентгенография позвоночника. На рентгенограммах определяется характерная картина: увеличение угла грудного кифоза более 45 градусов, клиновидная деформация трех и более грудных позвонков и грыжи Шморля. Для выявления неврологических нарушений назначают консультацию невролога. При наличии таких нарушений пациента направляют на МРТ позвоночника и КТ позвоночника для более точной оценки состояния костных и мягкотканных структур. Также может быть назначена электромиография. Межпозвонковая грыжа является показанием к консультации нейрохирурга. При подозрении на нарушения функции органов грудной клетки необходима консультация пульмонолога и кардиолога.
Лечение болезни Шейермана-Мау
Лечением занимаются врачи-ортопеды и вертебрологи. Терапия длительная, комплексная, включает в себя ЛФК, массаж и физиотерапевтические мероприятия. При этом решающее значение в восстановлении нормальной осанки имеет специальная лечебная гимнастика. В течение первых 2-3 месяцев упражнения нужно делать ежедневно, в последующем - через день. Выполнение комплекса упражнений занимает от 40 мин. до 1,5 часов. Необходимо помнить, что при нерегулярных занятиях лечебный эффект резко снижается.
ЛФК для устранения кифоза и восстановления осанки включает в себя 5 блоков: укрепление мышц грудного отдела позвоночника, укрепление мышц ягодиц, расслабление мышц поясницы и шеи (при кифозе эти мышцы постоянно находятся в состоянии повышенного тонуса), растяжение грудных мышц, дыхательные упражнения. Занятия обычной физкультурой также полезны, однако физическая активность должна быть целенаправленной, продуманной с учетом противопоказаний и возможных последствий.
Так, при болезни Шейермана-Мау противопоказаны занятия с отягощениями более 3 кг для женщин и более 5 кг для мужчин. Не рекомендуется накачивать грудные мышцы, поскольку они начинают «стягивать» плечи вперед. Нельзя заниматься «прыжковыми» видами спорта (баскетбол, волейбол, прыжки в длину и т. д.), поскольку интенсивная одномоментная нагрузка на позвоночник может спровоцировать образование грыж Шморля. Плавание полезно при правильной технике (когда задействуются мышцы не только груди, но и спины), поэтому лучше взять несколько уроков у инструктора.
Кроме того, пациентам с болезнью Шейермана-Мау рекомендуют подобрать правильную мебель для работы, сна и отдыха. Иногда необходимо носить корсет. Медикаментозное лечение обычно не требуется. Прием препаратов для укрепления скелета (кальцитонин) показан в крайних случаях - при выраженной деформации позвонков и крупных грыжах Шморля. Нужно учитывать, что подобные препараты имеют достаточно большой список противопоказаний (в том числе по возрасту), могут провоцировать кальцификацию связок и образование камней в почках, поэтому их следует принимать только по назначению врача.
Показаниями к хирургическим вмешательствам при болезни Шейермана-Мау являются угол кифоза более 75 градусов, стойкие боли, нарушение работы органов дыхания и кровообращения. В ходе операции в позвонки имплантируются металлические конструкции (винты, крючки), позволяющие выравнивать позвоночник при помощи специальных стержней.
1. Болезнь Шейермана. Клинические рекомендации/ Общероссийская общественная организация Ассоциация травматологов-ортопедов России - 2015
Синдром Хайнера ( Аллергический первичный гемосидероз легких )
Синдром Хайнера - это редкое аллергическое заболевание детского возраста, характеризующееся аномальной реакцией организма на белки коровьего молока. Симптоматика включает поражение дыхательной системы (кашель, одышку, кровохарканье), недобор массы тела у младенцев и другие признаки отставания в физическом развитии, диспепсические расстройства. Диагностику производят путем микроскопического изучения мокроты и кала, лабораторных анализов крови, элиминационных и провокационных проб. Лечение основывается на исключении из рациона молока коров, а также продуктов на его основе (включая смеси для детского питания) и симптоматической терапии.
Синдром Хайнера (аллергический первичный гемосидероз легких) является очень редкой формой аллергической энтеропатии, спровоцированной белками молока - главным образом, коровьего, но описаны случаи аналогичных реакций на козьи и даже соевые молочные продукты. Патология возникает у детей в возрасте от 3 месяцев до 2-3 лет, с одинаковой частотой поражает мальчиков и девочек. Особенности клинического течения (бронхиты и бронхопневмонии неясного генеза, анемия, рвота и диарея) часто приводят к неправильной диагностике и последующему некорректному лечению. Предполагается, что значительная часть случаев (от трети до половины) остается не диагностированной - количество молока в рационе детей уменьшается с переходом на обычное питание, симптоматика самопроизвольно исчезает.
Существует научная дискуссия, считать ли заболевание простым вариантом энтеропатической аллергии или полноценным аутоиммунным состоянием детского возраста. Сторонники аллергической версии указывают на наличие основного провоцирующего фактора - молока крупного рогатого скота, при исключении которого проявления сразу уменьшаются и практически исчезают. С другой стороны, выраженность и активность поражения собственных тканей является нехарактерной для простой аллергии. Недостаточность данных относительно сохранения непереносимости молока в старшем возрасте не дает возможности точно доказать справедливость той или иной точки зрения. Поэтому исследования состояния продолжаются с целью более точного определения его причин.
Патогенез
Как и этиология, патогенез синдрома Хайнера изучен очень слабо, многие его проявления объясняются предположениями и теоретическими представлениями. Считается, что при попадании в желудочно-кишечный тракт коровьего молока его белки распознаются иммунной системой ребенка как чужеродные, сильно иммуногенные агенты. Возникающая реакция сопровождается выделением антител против данных протеинов, вызывает их связывание и последующую элиминацию. Поскольку при поступлении молока в организм оно первоначально находится в органах ЖКТ, первые проявления патологии затрагивают именно их - изменяется стул, возникают боли, расстройства перистальтики. Нарушается всасывание других нутриентов, в частности - железосодержащих веществ, что оказывает свое влияние на последующих этапах патогенеза синдрома.
На определенном этапе развития патологии возникает перекрестная реакция - антитела против белков молока начинают присоединяться к некоторым клеткам легких и других органов, маркируя их как чужеродные и, тем самым, стимулируя клеточные и гуморальные иммунологические реакции. Развивается инфильтрация легочной ткани с повреждением сосудов малого круга кровообращения, что клинически проявляется симптомами бронхопневмонии. Происходит потеря эритроцитов за счет их выхода из сосудов и поглощения макрофагами с образованием сидерофагов. Этот процесс в сочетании с недостаточным поступлением железа из ЖКТ приводит к гипохромной анемии, иногда принимающей угрожающий характер. В тяжелых случаях возникает гепатоспленомегалия. При продолжающемся поступлении молока сочетание легочных, желудочно-кишечных и гематологических нарушений становится причиной замедления физического развития ребенка.
Проявления патологии возникают в раннем возрасте, начиная с третьего месяца жизни, их развитию предшествует введение в рацион ребенка цельного коровьего молока либо содержащих его смесей. Первоначально могут определяться неспецифические желудочно-кишечные нарушения - колики, метеоризм, диарея, изредка рвота. Затем присоединяются признаки поражения легких - кашель, свистящие хрипы, затрудненное дыхание. Наблюдаемое на этом фоне повышение температуры тела, кровохарканье создает картину, сходную с пневмонией или другой формой легочной инфекции, что зачастую ведет к ошибочной диагностике и лечению.
Хрипы в легких, боли в животе, диарея и иные проявления усиливаются при продолжении употребления продуктов на основе молочного белка. Реакция на прием антибиотиков и других средств против пневмонии и желудочно-кишечной инфекции отсутствует. Это служит одним из важных диагностических признаков синдрома Хайнера. У некоторых больных возникают кожные проявления - сыпь, крапивница, зуд. Частым симптомом является поражение ЛОР-органов - регистрируется заложенность носа, боль в ушах, обусловленная отитом. Характер кала меняется по мере прогрессирования патологии - из простого жидкого он может становиться кровянистым, включающим сначала тонкие прожилки крови, а затем все большее ее количество.
Потеря гемоглобина по причине кровохарканья и выделения крови с калом сочетается с нарушением всасывания железа в ЖКТ, что ведет к сильной анемии, имеющей гипохромный характер. Это, в свою очередь, провоцирует увеличение размеров печени и селезенки (гепатоспленомегалию). Кислородное голодание тканей, особенно головного мозга, развивающееся из-за нарушения работы респираторной системы и уменьшения концентрации гемоглобина, приводит к замедлению развития ребенка. При длительном потреблении молока и его продуктов это может привести к вегетативным нарушениям, проблемам с концентрацией внимания и обучаемостью.
Осложнения
В острый период синдрома Хайнера особенную угрозу представляют легочные нарушения, способные осложняться вторичной бактериальной инфекцией с развитием жизнеугрожающих пневмоний с дыхательной недостаточностью. Анемия, дисфункция кишечника и связанное с этим нарушение всасывания нутриентов, витаминов и микроэлементов в целом снижает сопротивляемость организма инфекционным агентам. Инфильтрация тканей легких иммунокомпетентными клетками на протяжении длительного времени может переходить в ее замещение рубцовыми элементами (пневмосклероз). Это снижает емкость легких, затрудняет поступление кислорода в организм. По некоторым данным, у больных старшего возраста наблюдается повышенная частота развития бронхиальной астмы, пищевых аллергий, заболеваний ЛОР-органов.
Определение синдрома Хайнера в современной педиатрии сопряжено с рядом трудностей. Основную роль играет редкость патологии, из-за чего специалисты не всегда могут своевременно распознать ее наличие по причине отсутствия соответствующего опыта. Проблемы также создает неспецифичность проявлений заболевания, их схожесть с инфекционными поражениями легких, органов пищеварительной системы, анемией. Эти факторы приводят к неправильному определению диагноза, что затрудняет лечение и повышает риски возникновения осложнений. Поэтому в процессе определения патологии следует обращать внимание на детали анамнеза и клинической картины. Алгоритм диагностики имеет следующий вид:
- Сбор анамнеза и анализ симптомов. Сочетание легочных нарушений (хрипов, кашля, выделения мокроты с прожилками крови) с диареей, рвотой и анемическими проявлениями должно вызвать подозрения в наличии данной патологии. Дополнительным доводом в пользу заболевания является недавний перевод ребенка на искусственное вскармливание, включение в рацион продуктов из коровьего молока. Частые простуды, отиты, анемия в анамнезе также подтверждают наличие синдрома.
- Рентгенологические исследования.Рентгенография органов грудной клетки выявляет усиление выраженности легочного рисунка, наличие инфильтратов в виде облаковидных теней.
- Лабораторные анализы. В общем анализе крови отмечается гипохромная микроцитарная анемия, выраженность которой зависит от тяжести состояния больного. Характерным признаком синдрома Хайнера является эозинофилия, особенно увеличивающаяся после употребления молочных продуктов, также возможна лейкопения и значительное увеличение СОЭ. Иммунологическое изучение сыворотки обнаруживает наличие антител к белкам молока.
- Микроскопические исследования. Микроскопия мокроты подтверждает значительное количество сидерофагов - моноцитов, содержащих в себе коричневые зерна гемосидерина. Также отмечается наличие эритроцитов, небольшого количества эозинофилов и кристаллов Шарко-Лейдена. Микроскопическое изучение кала (копрограмма) обнаруживает наличие эозинофилов.
- Иммунологические пробы. При подозрении на непереносимость коровьего молока назначают элиминационную пробу - исключение провоцирующих продуктов из рациона при контроле клинических показателей. Улучшение состояния регистрируется уже через 7-10 дней после отмены, что свидетельствует в пользу наличия заболевания. В случае удовлетворительного состояния больного могут использоваться провокационные пробы, связанные с введением аллергена в организм - при этом показатели будут ухудшаться.
Косвенными признаками синдрома может являться отсутствие эффекта при лечении пневмонии антибиотиками, ухудшение состояние пациента при несоблюдении безмолочной диеты. Дифференциальную диагностику производят с бронхопневмонией, желудочно-кишечной токсикоинфекцией, гематологическими нарушениями. Главной отличительной характеристикой заболевания от вышеперечисленных патологий является отсутствие возбудителя при микроскопическом изучении слизи кала и мокроты.
Лечение синдрома Хайнера
Центральным звеном лечения патологии является исключение поступления в организм белков коровьего молока - в ряде случаев только эти меры позволяют достичь полного выздоровления больного. Если у пациентов старшего возраста (более 1,5-2 лет) это сделать достаточно просто, то при терапии грудных младенцев могут возникнуть сложности. Требуется отмена кормления искусственными смесями, которые в большинстве случаев производятся на основе молока коров, и переход на естественное вскармливание либо использование донорского грудного молока. Применение аналогов (например, соевого молочка) неоднозначно, у ряда больных синдромом Хайнера возникают негативные реакции и при их использовании. Вспомогательные и симптоматические методики лечения включают в себя следующие мероприятия:
- Снижение аллергических и воспалительных проявлений. Часто отмечается положительный эффект от применения антигистаминных средств - происходит улучшение работы ЖКТ, быстрее исчезают инфильтраты в легких. Тяжелые случаи могут потребовать использования кортикостероидов для снижения выраженности воспаления.
- Улучшение показателей крови. Борьба с анемией включает назначение железосодержащих препаратов, введение белков и витаминов в рацион. При грудном вскармливании необходима аналогичная коррекция питания матери.
- Симптоматическая терапия. Сильный кашель может быть ослаблен ингаляциями, постуральным дренажом - назначение отхаркивающих средств противопоказано, так как это может усилить кровоизлияния в легких. Лечение диспепсических расстройств, воспалений ЛОР-органов, вторичных инфекций производится различными группами препаратов согласно показаниям.
Нередко в рамках лечения патологии осуществляется коррекция побочных эффектов от предшествовавших терапевтических мероприятий, назначенных на основе неверной диагностики синдрома. Чаще всего сюда включают коррекцию кишечной микрофлоры, нарушенной в результате приема антибиотиков, применяемых для лечения бронхопневмонии. Другим частым следствием неправильного подхода к терапии является задержка физического развития, возникающая при длительном употреблении коровьего молока. Ее компенсируют санаторно-курортными мероприятиями, лечебной гимнастикой, занятиями с детским психологом.
Прогноз и профилактика
Среди врачей-педиатров синдром Хайнера считается состоянием с относительно благоприятным прогнозом - простое исключение молочных продуктов само по себе обеспечивает успех лечения. Потенциальную угрозу здоровью и жизни ребенка представляет вероятность неверного определения заболевания и, как следствие, неправильного лечения. Оно грозит развитием побочных эффектов (например, дисбактериоза), которые еще больше усугубляют состояние пациента, но большую угрозу представляет дальнейшее поступление молочных белков в организм и обусловленное этим нарастание патологических процессов. Специфической профилактики заболевания не существует, для уменьшения риска осложнений родителям рекомендуется запоминать, когда и какие продукты были использованы при кормлении ребенка. В дальнейшем это помогает связать развитие симптомокомплекса с определенными компонентами рациона и быстрее определить диагноз.
1. Клинический случай синдрома Хейнера/ Клименко В.А. Ащеулов А.М. Синдеева Н.Т.// Здоровье ребенка. - 2014.
2. Пищевая аллергия у детей первых месяцев жизни в клинической практике педиатра/ Филатова Т.А., Ипатова М.Г.// Практика педиатра. - 2016 - №9.
3. Гастроинтестинальные проявления пищевой аллергии у детей/ Г.А. Новик, М.А. Ткаченко// Лечащий врач. - 2012.
Болезнь Меньера: клинико-диагностические критерии, лечебная тактика
Рассмотрены клиническая картина болезни Меньера, описаны стадии заболевания и подходы к лечению. Несмотря на множество средств и способов, используемых при лечении болезни Меньера, до настоящего времени не существует единой лечебной тактики, поиски идеаль
Clinical representation of Meniere's disease was considered, stages of the disease and approaches to the treatment were described. Inspite of the number of means and ways used , in Menier's disease treatment, until now there is no universal strategy of treatment, searching for a perfect method is going on.
Болезнь Меньера — негнойное заболевание внутреннего уха, характеризующееся увеличением объема эндолимфы (лабиринтной жидкости) и повышением внутрилабиринтного давления, в результате чего возникают рецидивирующие приступы прогрессирующей глухоты (чаще односторонней), шума в ушах, системного головокружения, нарушения равновесия и вегетативных расстройств.
Впервые симптомокомплекс, характеризующийся тугоухостью, шумом в ушах и периодически возникающим головокружением, был подробно описан Проспером Меньером (Prosper Meniere) в 1861 г. в докладе «Об особом виде тяжелой глухоты, зависящей от поражения внутреннего уха» на заседании французской Академии медицинских наук. Тогда же это состояние получило название «болезнь Меньера». На основании четырнадцатилетнего опыта обследования больных с подобным симптомокомплексом, результатов аутопсий и данных экспериментов по перерезке полукружных каналов у голубей, опубликованных в 1824 г. физиологом Пьером Флурансом (Jean Pierre Marie Flourens), П. Меньер высказал предположение, что это заболевание связано с внутренним ухом [1]. Позднее, в 1938 г., Hallpike и Cairns доказали, что в основе болезни Меньера лежит эндолимфатический гидропс [2].
Болезнью Меньера страдают преимущественно представители европеоидной расы независимо от пола. Средний возраст больных колеблется от 20 до 50 лет, но болезнь может встречаться и у детей. Несколько чаще заболевание встречается у лиц интеллектуального труда и у жителей крупных городов.
Несмотря на неугасающий многие годы интерес ученых-медиков к данной проблеме, этиология заболевания до конца не выяснена. Существуют несколько теорий развития болезни Меньера. Так, по анатомической теории, болезнь Меньера может быть связана с патологией строения височной кости, в частности, с пониженной пневматизацией клеток сосцевидного отростка и гипоплазией вестибулярного канала, при этом малых размеров эндолимфатический мешок неправильно расположен позади лабиринта.
Согласно генетической теории, наследственная передача болезни Меньера была выявлена более полувека назад, причем результаты последних исследований (М. Verstreken, Бельгия) свидетельствуют об аутосомно-доминантном типе наследования. Полагают, что особую роль играет участок DFNA9 гена СОСН.
Иммунологическая теория подтверждается обнаружением иммунных комплексов в эндолимфатическом мешке у пациентов с болезнью Меньера.
В пользу сосудистой теории свидетельствует частое сочетание болезни Меньера с мигренью, что было замечено еще самим П. Меньером.
Согласно аллергической теории, частота аллергических реакций у больных болезнью Меньера выше, чем среди населения в целом. Так, из 734 больных болезнью Меньера, обследованных M. J. Derebery (США), 59% заявили, что они страдают установленной или предполагаемой аллергией на агенты, переносимые по воздуху, а 40% — установленной или предполагаемой аллергией к пищевым продуктам (тогда как частота аллергических реакций среди всего населения США составляет примерно 20%).
По метаболической теории при болезни Меньера в эндолимфатическом пространстве происходит задержка калия. Это вызывает калиевую интоксикацию волосковых клеток и вестибулярного нейроэпителия, в результате чего развиваются тугоухость и головокружение. Многие авторы склоняются к полиэтиологичности данного заболевания и выделяют «факторы вызывающие» и «факторы предрасполагающие» [3].
Клиническая картина болезни Меньера в подавляющем большинстве случаев (80-90%) характеризуется односторонним поражением с возможным «вовлечением в патологический процесс» и второго лабиринта. В этом случае следует говорить о «двустороннем заболевании» [4, 5].
Дебютировать болезнь Меньера может как с вестибулярных, так и со слуховых (снижение слуха, заложенность уха, ушной шум) симптомов. В первые 2-3 года заболевания тугоухость может быть флюктуирующей (преходящей) с практически полным восстановлением слуха в межприступном периоде. С годами слух постепенно снижается, вплоть до полной глухоты.
Головокружение при болезни Меньера тягостное — системное, сопровождающееся спонтанным нистагмом, атаксией, координаторными расстройствами, выраженными вегетативными проявлениями (гиперсаливация, гипергидроз, флюктуации артериального давления, диспептические расстройства). Продолжительность приступа продолжается от нескольких минут до дней (status meniericus). Выраженность головокружения также может быть различной: от легких «предвестников» до бурной реакции, во время которой больные принимают вынужденное положение на боку, соответствующему больному уху (или направлению быстрого компонента спонтанного нистагма). Атаксия и координаторные нарушения могут сохраняться в течение нескольких дней после приступа. В первые годы заболевания (до 3 лет) между приступами при проведении вестибулометрии, как правило, регистрируется экспериментальная вестибулярная норморефлексия. Позднее, в период ремиссии, регистрируется вестибулярная гипорефлексия на пораженной, а затем и на противоположной стороне. Обычно через 10 и более лет выраженность вестибулярных проявлений уменьшается.
При классическом течении болезни Меньера выделяют три стадии заболевания:
I — преобладающим симптомом является головокружение, нередко сопровождающееся тошнотой и рвотой. Могут наблюдаться бледность и потливость. Обычно приступу головокружения предшествует чувство давления в ухе или соответствующей половине головы, длящееся от 20 мин до нескольких часов. Между приступами слух нормальный.
II — развивается сенсоневральная тугоухость с преимущественным понижением звуковосприятия на низких частотах. Приступы головокружения достигают максимальной выраженности с последующей тенденцией к уменьшению тяжести проявлений.
III — отмечается прогрессивное понижение слуха с развитием двусторонней глухоты. Эпизоды головокружения уменьшаются и затем полностью исчезают; тем не менее может сохраняться атаксия, особенно в темноте.
Американская академия отоларингологии и хирургии головы и шеи (AAO-HNS) (1995 год) определяет «очевидную» болезнь Меньера следующим образом:
- два или более возникающих самопроизвольно приступа головокружения продолжительностью 20 мин и более;
- потеря слуха, подтвержденная данными аудиологических исследований, по меньшей мере в одном случае;
- шум в ушах или ощущение заложенности в причинном ухе;
- другие причины исключены [6].
Диагностика классической формы болезни Меньера основывается на характерных клинических проявлениях и данных аудиометрии. Трудности в постановке диагноза могут быть связаны с тем, что многие пациенты, у которых болезнь начинается с приступов головокружения, не могут четко описать свои жалобы. Кроме того, существует ряд заболеваний и состояний, сопровождающихся вестибулярными расстройствами [7]:
- доброкачественное пароксизмальное позиционное головокружение;
- вертебробазилярная недостаточность;
- вестибулярный нейронит;
- черепно-мозговая травма;
- фистула лабиринта;
- инфекционный лабиринтит;
- последствия отохирургических вмешательств;
- отосклероз;
- мостомозжечковые опухоли;
- рассеянный склероз;
- побочные проявления лекарственных препаратов;
- острый гнойный средний отит;
- гипервентиляция.
Расстройства, которые могут проявляться головокружением и слуховыми симптомами, представлены в таблице.
Окончательный диагноз болезни Меньера ставят на основании результатов дегидратационных тестов (в ответ на медикаментозную дегидратацию понижаются пороги звуковосприятия на низких частотах и улучшается слуховое восприятие речи), экстра- и транстимпанальной электрокохлеографии (характерная для эндолимфатического гидропса кривая) [9]. Регистрируется суммационный потенциал (СП) и потенциал действия (ПД). Нарушение соотношения значений амплитуд СП/ПД (р > 0,3) является характерным признаком гидропса лабиринта, записи вестибулярных вызванных миогенных потенциалов (характерно отсутствие пиков Р13, N23 — график в виде прямой).
Обследование больных с болезнью Меньера должно включать ряд обязательных тестов. К традиционным равновесным тестам, диагностически довольно надежным, относятся проба Ромберга, проба Унтербергера, проба Бабинского-Вейля, указательная проба Барани. Перечисленные исследования в последние годы несколько утратили свое значение, поскольку в специализированных клиниках используют специальное оборудование для вестибулометрии и усложненные тесты. Кроме того, в «батарею тестов» входят: выявление спонтанной отоневрологической симптоматики, калорические тесты (тепловой и холодовой), вращательный тест Барани, тест плавного слежения, тест саккад, исследование оптокинетического нистагма.
Лечение болезни Меньера является эмпирическим, поскольку нет единого взгляда на этиопатогенез данного заболевания. Все существующие в настоящее время способы и методы лечения направлены на облегчение переносимости больными приступов головокружения, но не изменяют значительно течение процесса и не предотвращают развитие тугоухости [7]. Однако индивидуальная, подбираемая с учетом сопутствующих заболеваний терапия может замедлить развитие тугоухости, уменьшить выраженность ушного шума, уменьшить частоту и выраженность головокружения [5].
При лечении острого приступа болезни Меньера применяют в основном медикаментозную и, при наличии условий, карбогено- или оксигенотерапию. Используют седативные препараты и средства, улучшающие мозговое кровообращение (прохлорперазин, прометазин, циннаризин, диазепам) [7], дегидратационные средства. В остром периоде целесообразно вводить препараты парентерально или в свечах. Целесообразно проведение заушных новокаиновых блокад [4].
Одной из наиболее известных схем купирования острого приступа болезни Меньера является схема, разработанная И. Б. Солдатовым и Н. С. Храппо (1977): глюкоза 40% — 20,0 в/в, Пипольфен 2,5% — 2,0 в/м (или Аминазин 2,5% — 1,0 в/м), атропина сульфат 0,1% — 1,0 п/к (или платифиллина гидротартрат 0,2% — 2,0 п/к), кофеин-бензоат натрия 10% — 1,0 п/к; горчичники на шейно-затылочную область, грелка к ногам [9]. Иногда к означенной схеме добавляют ксантинола никотинат 15% — 2,0 в/м или циннаризин, либо винпоцетин [4]. Лечение в межприступном периоде (поддерживающая терапия) должно быть комплексным и довольно активным. Показаны средства, предотвращающие развитие или уменьшающие эндолимфатический гидропс: диуретики (фуросемид, амилорид, гидрохлортиазид), вазодилататоры (аналог гистамина — бетагистина дигидрохлорид), препараты, улучшающие мозговое кровообращение (циннаризин, пропранолол), кортикостероиды, а также немедикаментозное лечение — вестибулярная реабилитация, иглорефлексотерапия.
По современным представлениям, бетагистина дигидрохлорид имеет три уровня действия:
- на кохлеарный кровоток;
- на центральный вестибулярный аппарат;
- на периферический вестибулярный аппарат.
Являясь слабым агонистом Н1-рецепторов и активным блокатором Н3-рецепторов, данный препарат стимулирует постсинаптические гистаминовые рецепторы. Именно Н3-антагонистическим эффектом бетагистина дигидрохлорида объясняют эффект нормализации возбуждения вестибулярных ядер в подкорковых структурах центральной нервной системы и вазоактивную составляющую действия этого препарата [11, 12]. Следует подчеркнуть избирательность вазоактивного действия бетагистина дигидрохлорида [11], который улучшает микроциркуляцию внутреннего уха и проницаемость капилляров, а также нормализует давление эндолимфы в лабиринте, не приводя к выраженному снижению артериального давления. Препарат также положительно влияет на передачу нервного импульса в медиальных и латеральных вестибулярных ядрах и периферических вестибулярных рецепторных образованиях [13]. Опыт многих клиницистов свидетельствует о том, что бетагистина дигидрохлорид уменьшает интенсивность головокружений, сокращает длительность эпизодов головокружений, делает их более редкими. Препарат эффективен как для купирования приступов головокружений и профилактики их рецидивов, так и для уменьшения субъективного ушного шума.
Следует отметить целесообразность использования бетагистина дигидрохлорида у пациентов с болезнью Меньера и в постоперационном периоде — головокружение, как правило, исчезает на 3-4 день после операции [5].
Особняком стоит использование аминогликозидов, обладающих токсическим действием в отношении клеток нейроэпителия внутреннего уха. Метод может использоваться на поздних стадиях БМ при двустороннем поражении и применяется у лиц, которым противопоказано хирургическое лечение. Интратимпанальное введение аминогликозидов достаточно эффективно и возможно при одностороннем поражении [14].
При явной неэффективности консервативного лечения целесообразны различные хирургические вмешательства, как щадящие (слухосохраняющие), так и деструктивные. Деструктивные методы показаны при тяжелых инвалидизирующих формах болезни Меньера. Выделяют 5 групп:
1 — вмешательства на автономной нервной системе (хорд- и хордплексусэктомия);
2 — перерезка сухожилий мышц барабанной полости;
3 — декомпрессивные операции на внутреннем ухе;
4 — деструктивные операции на лабиринте;
5 — деструктивные операции на преддверно-улитковом нерве [5].
К слухосохраняющим операциям относятся:
- шунтирование эндолимфатического мешка — наиболее распространенное хирургическое вмешательство при БМ;
- саккулотомия — декомпрессивная операция на сферическом мешочке;
- пересечение вестибулярного нерва с целью прекращения афферентной импульсации, что способствует исчезновению вестибулярных расстройств.
При безуспешности щадящих видов хирургических вмешательств проводят деструктивные операции:
- лабиринтэктомия;
- кохлеосаккулотомия;
- вестибулярная нейрэктомия.
Следует отметить, что операции на автономной нервной системе и перерезка сухожилий мышц барабанной полости малоэффективны, а декомпрессивные и деструктивные хирургические вмешательства, как правило, приводят к глухоте на оперированное ухо и возобновлению приступов головокружений в отдаленные сроки в связи с фиброзным заращением созданных соустий; деструктивные операции на преддверно-улитковом нерве выполняются в отделениях нейрохирургии.
В настоящее время применяется такой метод хирургического лечения, как лазеродеструкция горизонтального полукружного канала, которая позволяет добиться избавления от приступов головокружения в ближайшие и отдаленные сроки, сохранить слух и задержать развитие гидропического процесса в другом ухе при одностороннем процессе.
Однако, несмотря на обилие научных работ, посвященных болезни Меньера, множество средств и способов, используемых при ее лечении, проблема, по существу, остается нерешенной, поскольку до настоящего времени не существует единой, признанной всеми ведущими специалистами лечебной тактики. Поиски идеального метода лечения болезни Меньера продолжаются.
Литература
- Meniere M. P. Pathologie auriculare. Maladies de l’orielle interne offrant les symptomes de la congestion cerebrale apoplectiforme // Gaz. Med. de Paris. 1861. T. 16. P. 88-89.
- Hallpike C. S., Cairns H. Observation on the pathology of Meniere’s syndrome // J. Laryngol. Otol. 1938. Vol. 53. P. 625-655.
- Сагалович Б. М., Пальчун В. Т. Болезнь Меньера. М.: ООО «Медицинское информационное агентство», 1999. 525 с.
- Бабияк В. И., Ланцов А. А., Базаров В. Г. Клиническая вестибулология. СПб: «Гиппократ», 1996. 336 с.
- Патякина О. К. Лечебная тактика при вестибулогенном головокружении // Consilium medicum. Приложение. 2001. С. 9-12.
- Monsell E. M. New and revised reporting guidelines from the Committee on Hearing and Equilibrium. American Academy of Otolaryngology — Head and Neck Surgery Foundation, Inc. Otolaryngology — Head and Neck Surgery. 1995. 113 (3). Р. 176-8.
- Нурмухаметова Е. Диагностика и лечение болезни Меньера // Русский медицинский журнал. 1998. № 20. С. 1346-1347.
- Bronsteind A. M., Lempert Th. Dizzines. Cambridge University Press, 2007. P. 215.
- Gibson W. P. R, Prasher D. K., Kilkenny G. P. G. Diagnostic significance of transtympanic electrocochleography in Meniere’s diseas // Ann. Otol. Rhinol. Laryngol. 1983. Vol. 92. P. 155-159.
- Солдатов И. Б., Храппо Н. С. Методы лечения болезни Меньера // Журн. ушн., нос. и горл. бол. 1977. № 6. с. 8-14.
- Timmerman H. Рharmakoterapy of vertigo: any news to be expected? // Acta Otolaryngol. 1994, Suppl 513, 28-32.
- Van Cauwenberge P. B., De Moor S. E. G. Physiopathology of H 3-receptors and pharmacology of betahistine // Acta Otolaryngol. 1997. Suppl. 526. P. 43-46.
- Arrang J. M., Garbarg M., Quach T. T., Toung M. D. T., Yeramian E., Schwarts J. C. Actions of betahistine at histamine receptors in the brain // Eur Pharmacol. 1985. Vol. 11. P. 73-84.
- Pfleiderer A. G. The current role of local intratympanic Gentamicin therapy in the management of unilateral Meniere’s disease // Clin Otolaryngol. 1998. Vol. 23 (1). P. 34-41.
О. В. Зайцева, кандидат медицинских наук
ФГБУ НКЦ оториноларингологии ФМБА России, Москва
Синдром Ашермана - симптомы и лечение
Что такое синдром Ашермана? Причины возникновения, диагностику и методы лечения разберем в статье доктора Дурасова Владимира Владимировича, гинеколога со стажем в 34 года.
Над статьей доктора Дурасова Владимира Владимировича работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Синдром Ашермана — это заболевание, при котором происходит сращение стенок матки между собой и возникают внутриматочные спайки (синехии).
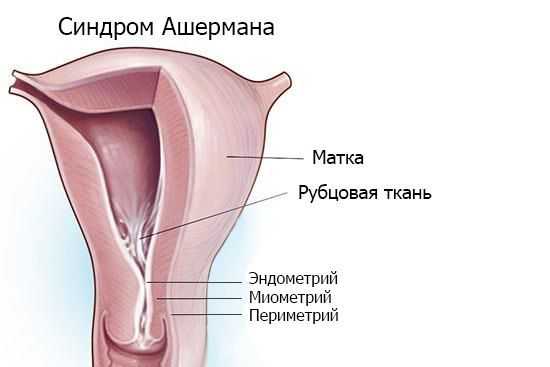
Основная причина патологии — травма эндометрия , особенно на фоне инфекции, которая ведёт к воспалению в полости матки и формированию спаек. Наиболее опасны выскабливания между второй и четвёртой неделей после родов.
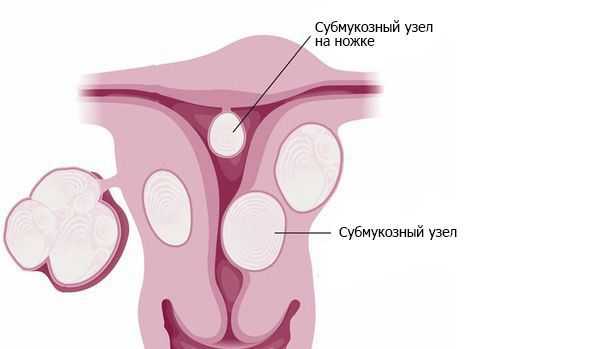
Примерно в 90 % случаев синдром Ашермана возникает в результате постабортных или послеродовых вмешательств [4] . В 40 % случаев спайки образуются п осле повторных выскабливаний при неполном аборте и удалении остатков плацентарной ткани [5] . Нередко сращения возникают после гистероскопических вмешательств по удалению субмукозных узлов — доброкачественных образований в подслизистом слое матки. Удаление сразу нескольких узлов повышает вероятность образования спаек [6] .
Синдром Ашермана иногда встречается после наложения шва Линча (процедура для остановки послеродового кровотечения) и после эмболизации маточных артерий (операции по искусственной закупорке сосудов). К редким причинам относят воспаление половых органов при использовании внутриматочной спирали, генитальном туберкулёзе и шистоматозе (токсико-аллергическом заболевании, вызванном гельминтами).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Ашермана
Как правило, женщины самостоятельно замечают заболевание, когда после медицинского аборта или другой внутриматочной процедуры менструации стали скудными ( гипоменоррея ) или исчезли совсем ( аменорея ) [8] . Вместо них внизу живота возникают схваткообразные интенсивные боли, вызванные затруднением оттока менструальной крови. Эти боли появляются каждый месяц, соответствуя фазе менструального цикла, однако выделений при этом нет. К другим симптомам синдрома относят:
- бесплодие;
- выкидыши;
- нарушение плацентации (врастание плаценты и её предлежание ) [9] ;
При патологии кровь скапливается главным образом не в матке (поскольку там нет свободного пространства из-за сращения), а в маточных трубах. Всасывание менструальной крови может приводить к повышению температуры до субфебрильных величин (чуть больше 37 ° ).
Патогенез синдрома Ашермана
Внутриматочные сращения возникают в ответ на травму или удаление эндометрия противоположных стенок полости матки. После травмы в считаные минуты начинается острое воспаление . Воспалительный процесс активирует комплекс биохимических реакций, похожих на те, которые возникают при кровотечении:
- Тромбоциты прилипают к повреждённой поверхности.
- Местный кровоток усиливается, расширяются мелкие сосуды, по которым течёт артериальная кровь (артериолы).
- Клетки, которые помогают организму бороться с воспалением (нейтрофилы и макрофаги), перемещаются к месту травмы.
- Формируется фибриновая плёнка. Поначалу она тонкая, как паутинка, и располагается в зонах, поверхность которых наиболее повреждена, чаще в месте перехода шейки в тело матки (область внутреннего зева), хотя может покрывать и всю полость матки.
- На третий день после травмы начинают расти клетки, формирующие соединительнотканный рубец, а на пятый в фибриновой плёнке развивается сосудистая сеть, что неотвратимо ведёт к образованию сращений в полости матки [7] .
Таким образом, сращения можно обнаружить на пятый день после вмешательства. Следует отметить, что фибриновая плёнка появляется после травмы у всех пациентов — это защитная реакция организма для ограничения повреждённого участка. У многих женщин к пятому дню плёнка рассасывается, и они выздоравливают, но у части запускается процесс образования спаек.
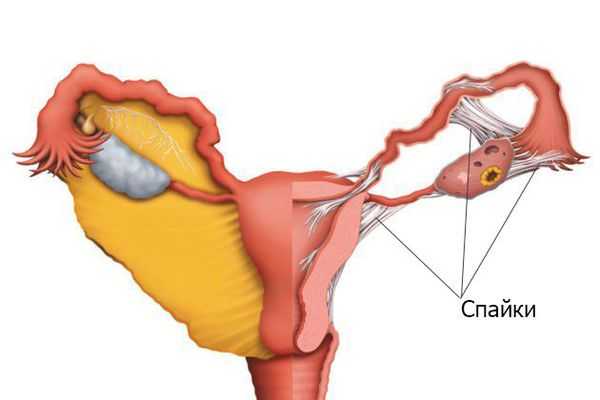
Формирование спаек зависит от степени травмы, состояния иммунной системы, врождённых особенностей и других факторов, многие из которых непонятны до сих пор. Развитию патологии способствуют:
- наличие сгустков крови или остатков плодного яйца в полости матки, что является хорошей питательной средой для микробов;
- заболевания, передающиеся преимущественно половым путём;
- ослабленный иммунитет;
- перенесённое в прошлом вмешательство на шейке матки, ухудшившее её барьерную функцию и другие факторы.
Классификация и стадии развития синдрома Ашермана
Существует несколько классификаций синдрома Ашермана. Одна из самых простых и удобных — классификация по March (2011), который разделял внутриматочные сращения на 3 группы:
- Умеренные — нежные и тонкие спайки, которые занимают менее 25 % полости матки. Устья маточных труб и дно матки свободны или минимально вовлечены.
- Средние — спайками покрыто от 25 до 75 % полости матки, устья маточных труб и дно частично заращены;
- Выраженные — дно и устья маточных труб полностью заращены, спайками покрыто более 75 % полости матки [10] .
Степени развития заболевания более подробно рассмотрены в классификации European Society of Gynecological Endoscopy (1995) [11] .
| Степень | Распространённость внутриматочных спаек |
|---|---|
| 1 | - тонкие и/или плоскостные спайки в устьях маточных труб, которые легко разрушаются тубусом гистероскопа; |
| 2а | - единичные плотные сращения соединяют противоположные зоны полости матки; - устья маточных труб визуализируются; - спайки не могут быть разделены тубусом гистероскопа. |
| 2б | - полное заращение внутреннего зева, при этом верхняя часть полости матки выглядит нормально; |
| 3 | - множественные плотные сращения соединяют противоположные зоны полости матки; - устье одной маточной трубы полностью заращено; |
| 4 | - выраженные плотные сращения с частичным заращением полости матки и устьев обеих маточных труб; |
| 5а | -выраженное рубцевание и разрастание или замещение плотной соединительной тканью внутреннего слоя матки в сочетании со спайками 1 или 2 степени; - аменорея или выраженная гипоменорея; |
| 5б | - выраженное рубцевание и фиброз эндометрия в комбинации со спайками 3 или 4 степени; - аменорея. |
По классификации Американского Общества Репродуктивной Медицины оцениваются данные рентгенодиагностики маточных труб (гистеросальпингографии), гистероскопии, тип спаек, степень нарушений менструальной функции и формируется долгосрочный прогноз по возможности зачать и выносить ребёнка [12] .
| Степень вовлечения полости матки | Менее 1/3 - 1 балл | 1/3-2/3 - 2 балла | 2/3 - 4 балла |
|---|---|---|---|
| Тип спаек | Нежные - 1 балл | Нежные и плотные - 2 балла | Плотные - 4 балла |
| Нарушение менструаций | Норма - 0 баллов | Гипоменоррея - 2 балла | Аменорея - 4 балла |
Суммируя баллы, выделяют 3 стадии:
- слабая — 1-4 балла;
- средняя — 5-8 баллов;
- тяжёлая — 9-12 баллов.
Осложнения синдрома Ашермана
Заболевание может вызывать следующие осложнения:
1. Бесплодие . Беременность возможна только после удачно проведённой операции, при которой удаётся восстановить полноценный объём полости матки и освободить устья маточных труб.
2. Циклические ежемесячные боли. Возникают при заращивании внутреннего зева и нижней трети полости матки.
3. Эндометриоз. Выражается в том, что клетки эндометрия (внутреннего слоя стенки матки) разрастаются за пределами этого слоя . Согласно имплантационной теории, заболевание вызвано тем, что большое количество менструальной крови через маточные трубы попадает в брюшную полость. Отток во влагалище при этом затруднён. Обилие крови в брюшной полости приводит к тому, что защитные силы организма не успевают подавлять активность и разрушать клетки эндометрия.
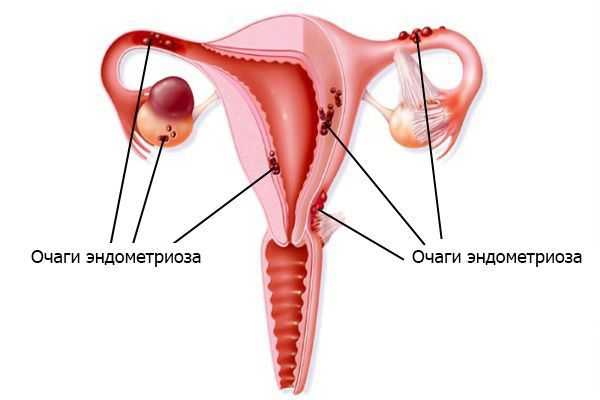
4. Невынашивание беременности, выкидыши . Основная причина состоит в том, что сращения ограничивают функциональный объём полости матки и не дают ей растягиваться.
5. Гипоменструальный синдром (скудные менструации — 1-2 дня, меньше 25 мл, а порой несколько дней в виде "мазни"). Возникает при частичном заращении полости матки.
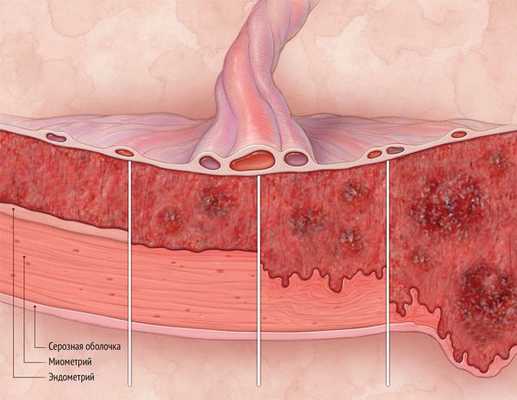
6. Неправильное прикрепление (врастание в стенку матки) плаценты . Осложнение проявляется, когда плацента не отделяется после родов. Это может вызвать кровотечение и в ряде случаев приводит к удалению матки.
Диагностика синдрома Ашермана
Основные методы диагностики:
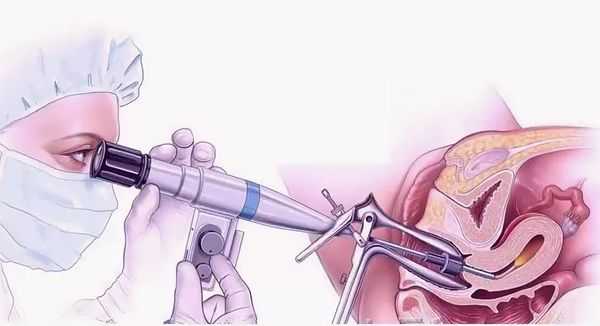
- Диагностическая гистероскопия . Метод позволяет визуально оценить степень поражения эндометрия и является золотым стандартом выявления синдрома Ашермана [13] .
- Гистеросальпингография — исследование, при котором в полость матки вводят рентгеноконтрастный раствор и выполняют рентгеновские снимки для получения изображения полости матки и просвета маточных труб. Имеет лишь историческое значение, потому что точность метода невелика, а лучевая нагрузка на гениталии существенна. Облучение может спровоцировать злокачественные заболевания половых органов или ухудшить работу яичников.
- Зондирование полости матки — метод гинекологического исследования, который проводят с помощью специального маточного зонда.
- Ультразвуковое исследование. Если есть спайки, то на снимках видны эхогенные, нерегулярные эксцентричные линейные сигналы — беловатые плотные участки рубцовой ткани или локальное истончение эндометрия. Исследование проводят в лютеиновую фазу (период с момента овуляции и до начала менструаций).
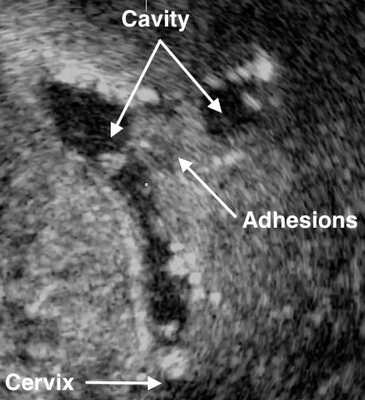
- Соногистерография — ультразвуковое исследование, во время которого в полость матки вводят физиологический раствор.
- Допплеровское исследование— ультразвуковая оценка органических изменений, нарушающих кровоток. Метод позволяет оценить функциональное состояние эндометрия.
- Магнитно-резонансная томография — применяется в случаях тотального поражения полости матки при невозможности провести гистероскопию.
Гистероскопия является самым точным и надёжным методом диагностики синдрома Ашермана . Другие техники выполняют вспомогательное значение и часто дают противоречивые результаты при субмукозных миомах (узлах, растущих в полость матки) и при гиперпластических процессах эндометрия.
Лечение синдрома Ашермана
Операция показана при бесплодии, невынашивании беременности и циклические болях, возникающих из-за затруднения оттока менструальной крови. В последнем случае цель операции состоит в удалении жидкого содержимого из полости матки.
Первые попытки лечить синдром Ашермана заключались в проведении лапаротомии (операции, которая производится путем рассечения передней брюшной стенки скальпелем), утеротомии ( рассечении стенки матки) и пальцевом разрушении спаек. Данные методики имеют лишь историческое значение, поскольку появление гистероскопии значительно улучшило результаты терапии.
Перед операцией, как правило, проводят профилактическое лечение антибиотиками широкого спектра действия. Цель операции — полностью восстановить полость матки. К сожалению, при обширном поражении часто невозможно обнаружить устья маточных труб и найти правильное направление для рассечения сращений. Тогда задача состоит в создании объёма полости матки, достаточного для применения методов вспомогательной репродукции.

Важные аспекты хирургического вмешательства:
- За несколько минут до операции проводят трансвлагалищное УЗИ, чтобы чётко представлять изгиб полости матки. Для навигации в сложных случаях используют ультразвук и лапароскопию, хотя эти методы не могут гарантированно предотвратить разрыв стенок матки, если хирург потеряет правильное направление при рассечении сращений.
- Рассечение сращений производят от центра полости матки латерально (в боковую сторону) и в сторону устьев маточных труб. Рубцовая ткань, в отличие от миометрия, не кровоточит — это является критерием правильности выбранного курса.
- Часто достаточно рассечь плотные сращения в области внутреннего зева и нижней трети полости матки. Это поможет получить доступ ко дну матки, где сращения обычно не очень плотные, и без затруднений освободить устья маточных труб.
Если операция прошла удачно и пациентка чувствует себя хорошо, то уже вечером она может быть выписана. Если процедура была сложной или потребовалось проведение лапароскопии, придётся провести ночь в стационаре.
Прогноз. Профилактика
Прогноз не всегда благоприятен, поэтому особое внимание следует обратить на профилактические меры. Их можно разделить на две группы:
1. Методы первичной профилактики развития спаек в полости матки:
- Бережное отношение к матке при выскабливании, снижение числа повторных вмешательств. Этого можно добиться применением гемостатиков (препаратов, останавливающих кровотечение) после абортов, что уменьшит риск повторного выскабливания. При наличии остатков плодного яйца в полости матки не следует торопиться с выскабливанием, так как 95 % плацентарных полипов (остатков беременности) спонтанно разрушаются в течение трёх месяцев на фоне приёма оральных контрацептивов. Если же повторное опорожнение полости матки необходимо, то выполнить это можно деликатно: методом вакуум-аспирации при ультразвуковой навигации.
- Чтобы предотвратить развитие спаек после внутриматочной хирургии следует ограничить использование электрохирургии в пользу методики Cold Loop ("Холодная петля") . Технология заключается в том, что при удалении субмукозных узлов 1 и 2 типов (когда часть узла находится в полости матки, а часть в стенке) часть узла в матке постепенно удаляется по кусочкам с помощью высокотемпературной петли. Далее узел извлекается из стенки матки с помощью специальных механических устройств, при этом миометрий сокращается и выталкивает остатки узла в просвет полости матки. Очень важно при этом находиться в правильном слое — между псевдокапсулой (растянутыми тканями матки, покрывающими миоматозный узел) и самой миомой. Это позволяет бескровно выделить узел из ложа и обойтись без прижигания тканей, либо использовать её в минимальном объёме на последнем этапе [15] . Это очень важно, поскольку на обожжённой поверхности полости матки легко образуются спайки, а эндометрий восстанавливается очень медленно, да и высокая температура может повредить нижележащий слой миометрия и возникает риск разрыва матки при последующей беременности.
2. Вторичная профилактика — комплекс мер, направленных на снижение риска повторного появления спаек в полости матки после их рассечения:
- После рассечения спаек для стимуляции роста эндометрия следует принимать эстрогены и ввести в полость матки гелевый противоспаечный агент [16][17] . Гель позволяет временно, на пять суток, разобщить противоположные стенки матки и не дать им срастись.
- Применение катетера Фолея (трубки для выведения мочи из мочевого пузыря) — заполненный катетер разобщает стенки матки, он может находиться в полости матки до двух недель. С этой же целью применяют различные пластиковые устройства и внутриматочные спирали. Вероятность повторного образования спаек снижается, но остаётся риск инфицирования [18] .
- Согласно последним исследованиям, для регенерации эндометрия перспективно применение стволовых клеток[20] .
Несмотря на профилактику спаек, они повторно образуются у 25 % женщин с умеренной степенью синдрома Ашермана и у 75 % с тяжёлой. Беременность наступает у 25-75 % оперированных женщин, доношенные дети рождаются в 26-79 % случаях . Разница в данных связана с тем, что не существует общепризнанной классификации синдрома и единого подхода ко вторичной профилактике заболевания.
В дополнение к вышеперечисленным методикам в послеоперационном периоде используют программируемую газовую дистензию . Метод заключается в том, что для разобщения стенок полость матки заполняют углекислым газом. Под давлением газа полость матки растягивается, что приводит к разрушению нежных спаек. Процедуру проводят последовательно на 3, 7 и 10 день после операции. Дополнительным преимуществом является то, что газ, в отличие от жидкости, не переносит в полость матки микроорганизмы, находящиеся на шейке, это делает процедуру более безопасной.
Читайте также:
- Сердечно-легочная реанимация. Пути развития отечественной сердечно-легочной реанимации
- Принципы тренинговой терапии при легастении у детей и подростков
- Рекомендации по анализу рентгенограммы проксимального отдела бедренной кости в ПЗ проекции
- Выбор цемента для цементировки коронок зубов. Рекомендации
- Синдром Вилларе (Villaret)
