Социальные факторы инфаркта миокарда. Стресс и депрессия как причина инфаркта миокарда
Добавил пользователь Дмитрий К. Обновлено: 21.01.2026
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Инфаркт миокарда: причины появления, симптомы, диагностика и способы лечения.
Определение
Инфаркт миокарда (ИМ) - это омертвление участка сердечной мышцы вследствие недостаточного ее кровоснабжения с развитием характерной клинической картины.
Причины появления инфаркта миокарда
Сердце - полый мышечный орган, имеющий форму конуса. Стенки сердца состоят из трех слоев. Внутренний слой - эндокард - выстилает полости сердца изнутри, и его выросты образуют клапаны сердца. Средний слой - миокард - состоит из сердечной мышечной ткани. Наружный слой - перикард. Сердце человека имеет четыре камеры: два предсердия и два желудочка. В правое предсердие поступает кровь из тканей самого сердца и всех частей тела (по верхней и нижней полым венам). В левое предсердие впадают четыре легочные вены, несущие артериальную кровь из легких. Из правого желудочка выходит легочный ствол, по которому венозная кровь поступает в легкие. Из левого желудочка выходит аорта, несущая артериальную кровь в сосуды большого круга кровообращения. Кислород к миокарду сердца доставляется по коронарным артериям.
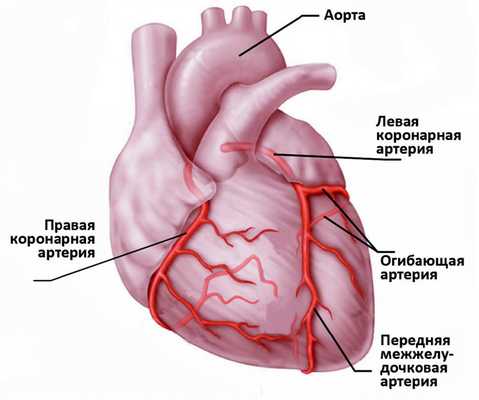
Сердце очень чувствительно к недостатку кровоснабжения (дефициту кислорода). В случае закупорки крупной коронарной артерии и при отсутствии эффективного альтернативного кровообращения по другим сосудам уже через 30 минут в пораженном участке начинается гибель кардиомиоцитов (мышечных клеток сердца).
Нарушение кровообращения вследствие атеросклеротического поражения коронарных артерий в 97-98% случаев имеет основное значение в возникновении инфаркта миокарда.
Атеросклерозом может поражаться как одна коронарная артерия, так и все три. Степень и протяженность сужения артерии могут быть различными. При повышении артериального давления склерозированный внутренний слой сосуда (эндотелий) легко повреждается, кровь проникает внутрь бляшки, активируется процесс свертывания крови и формируется тромб, который может частично или полностью закупорить сосуд.
Где может формироваться тромб:
- на месте разрыва уязвимой (нестабильной) атеросклеротической бляшки;
- на дефекте (эрозии) эндотелия коронарной артерии, не обязательно локализованном на поверхности атеросклеротической бляшки;
- в месте гемодинамически незначимого сужения коронарной артерии.
Развивающийся некроз миокарда может быть различных размеров, а некроз, проходящий через все слои сердца (трансмуральный) может стать причиной разрыва миокарда.
Образование очагов некроза в миокарде сопровождается изменением размера, формы и толщины стенки сердца, а сохранившийся миокард испытывает повышенную нагрузку и подвергается гипертрофии с увеличением объема и массы.
Такие сопутствующие состояния как: анемия, воспаление, инфекция, лихорадка, метаболические или эндокринные расстройства (в частности, гипертиреоз) могут спровоцировать или утяжелить ишемию миокарда.
К факторам риска развития инфаркта миокарда относятся:
- гиперлипидемия (нарушение нормального соотношения липидов крови);
- курение,
- сахарный диабет,
- артериальная гипертензия,
- абдоминальное ожирение,
- психосоциальные причины (стресс, депрессия и т.д.),
- низкая физическая активность,
- несбалансированное питание и потребление алкоголя.
Классификация инфаркта миокарда
I. Острый инфаркт миокарда.
- Острый трансмуральный инфаркт передней стенки миокарда.
- Острый трансмуральный инфаркт нижней стенки миокарда.
- Острый трансмуральный инфаркт миокарда других уточненных локализаций.
- Острый трансмуральный инфаркт миокарда неуточненной локализации.
- Острый инфаркт миокарда неуточненный.
- Повторный инфаркт передней стенки миокарда.
- Повторный инфаркт нижней стенки миокарда.
- Повторный инфаркт миокарда другой уточненной локализации.
- Повторный инфаркт миокарда неуточненной локализации.
- Гемоперикард.
- Дефект межпредсердной перегородки.
- Дефект межжелудочковой перегородки.
- Разрыв сердечной стенки без гемоперикарда.
- Разрыв сухожильной хорды.
- Разрыв сосочковой мышцы.
- Тромбоз предсердия, ушка предсердия и желудочка сердца.
- Другие текущие осложнения острого инфаркта миокарда.
- Коронарный тромбоз, не приводящий к инфаркту миокарда.
- Синдром Дресслера - постинфарктный склероз.
- Другие формы острой ишемической болезни сердца.
- Острая ишемическая болезнь сердца неуточненная.
Симптомы инфаркта миокарда
При инфаркте миокарда в результате нарушения кровообращения в пораженном участке сердца накапливаются продукты обмена, которые раздражают рецепторы миокарда и коронарных сосудов, что проявляется острой болью. Болевой приступ приводит к выбросу адреналина и норадреналина корой надпочечников.
Боль при типичном течении инфаркта миокарда является основным его признаком. Она возникает за грудиной, иногда может отдавать в левую руку, левое плечо, горло, нижнюю челюсть, в подложечную область.
По интенсивности и длительности такая боль в значительной степени превосходит обычный приступ стенокардии. Боль не снимается приемом нитроглицерина. Длительность болевого синдрома может быть различной - от 1 часа до нескольких суток. Иногда инфаркт миокарда сопровождается резкой слабостью, головокружением, головной болью, рвотой, потерей сознания. Больной выглядит бледным, губы синеют, наблюдается потливость.
В первые сутки развития инфаркта миокарда может регистрироваться тахикардия (учащенное сердцебиение), нарушение ритма, повышение температуры до 37-38℃.
Выделяют следующие клинические варианты:
- астматический - протекает как приступ бронхиальной астмы (присутствуют одышка, затрудненное дыхание, чувство нехватки воздуха);
- гастралгический - характеризуется болями в области желудка с распространением в загрудинное пространство, может быть отрыжка, икота, тошнота, многократная рвота, вздутие живота;
- аритмический - возникают нарушения ритма сердца, угрожающие жизни;
- церебральная - характеризуется нарушением мозгового кровообращения (наблюдаются тошнота, головокружение, нарушение сознания с развитием обморока);
- бессимптомный - инфаркт миокарда без типичного болевого приступа. В связи с несоблюдением постельного режима и отсутствием должного лечения протекает неблагоприятно.
Существуют четкие критерии диагностики инфаркта миокарда:
- клиническая картина инфаркта миокарда;
- картина инфаркта миокарда по данным ЭКГ;
- наличие новых участков миокарда со сниженным кровообращением или нарушение сократимости миокарда по данным инструментальных исследований;
- выявление тромбоза коронарных артерий по данным ангиографии.
- определение уровня биохимических маркеров повреждения кардиомиоцитов в крови;
Синонимы: Тн I вч; сердечный Тн I вч; сТн I вч. Tn I hs; cardiac-specific troponin I, high sensitivity; cTn I hs. Краткая характеристика определяемого вещества (Тропонин) Тропонины - небольши�.
Психосоматический порочный круг инфаркта миокарда
Резюме. Представлен обзор исследований, демонстрирующих соматические изменения при психологических процессах, принятых как факторы риска острого инфаркта миокарда: депрессия, стресс, тревога. На основании метафорического обозначения “идеальный шторм” показаны воспалительные, иммунологические, нейрогуморальные предпосылки развития инфаркта миокарда, а равно таковые изменения, являющиеся соматическим субстратом психологических состояний, способствующих развитию инфаркта миокарда посредством поведенческих и биологических факторов риска: “болезненное поведение”, “депрессионная болезнь”. Два эти процесса входят в психосоматический “порочный круг”. В статье делается акцент на важности индивидуализации подхода к реабилитации и вторичной профилактике инфаркта миокарда, поскольку с биопсихосоциальной точки зрения восходящие и нисходящие психосоматические связи у каждого пациента уникальны.
Российский кардиологический журнал 2018, 1 (153): 83-88
Ключевые слова: пациент-центрированная медицина, биопсихосоциальный, психосоматика, соматизация, биопсихокультуральный, инфаркт миокарда.
Авторы
ФГБОУ ВО Российский национальный исследовательский медицинский университет им. Н. И. Пирогова Минздрава России, Москва, Россия.
Таратухин Е. О.* — к. м.н., магистр психологии, доцент кафедры госпитальной терапии № 1 л/ф, Гордеев И. Г. — д. м.н., профессор, зав. кафедрой, Лебедева А. Ю. — д. м.н., профессор кафедры.
Инфаркт миокарда
Социальные факторы инфаркта миокарда. Стресс и депрессия как причина инфаркта миокарда
Кардиология:
Острый психоэмоциональный стресс как причина ИБС (инфаркта миокарда)
Острый психоэмоциональный стресс оказывает отрицательное воздействие на сердечно-сосудистую систему. Сердечно-сосудистая смертность увеличивается в течение месяца после смерти близкого человека, частота сердечно-сосудистых событий возрастает сразу после стихийных бедствий, а также среди гражданских лиц, подвергшихся военному нападению.
Прямые сердечно-сосудистые эффекты психоэмоционального стресса изучали как в условиях реальной повседневной жизни, так и в эксперименте. Экспериментальный стресс (вызванный, например, публичным выступлением либо выполнением трудных интеллектуальных задач в условиях нехватки времени или в сложной обстановке) достоверно увеличивает ЧСС, АД и потребность миокарда в кислороде.
Воздействие острого психоэмоционального стресса на сердечно-сосудистую систему больных с уже имеющейся ИБС было изучено с помощью относительно чувствительных индикаторов ишемии миокарда — регионарной миокардиальной перфузии и нарушения кинетики миокарда желудочков. Было установлено, что у больных ИБС частота ишемии, индуцированной острым психоэмоциональным стрессом, широко варьирует — от 20 до 70%.
Ишемия, вызванная острым психоэмоциональным стрессом, возникает при более низкой ЧСС и более низком уровне работы сердца, чем ишемия, индуцированная физической нагрузкой. Это означает, что в развитии ишемии, вызванной острым психоэмоциональным стрессом, может играть роль снижение миокардиальной перфузии. В исследовании с участием 58 пациентов с ИБС, разделенных на 3 группы в соответствии с ФВ ЛЖ (нормальная, умеренно сниженная — 30-50% и значительно сниженная — < 30%), ишемию в ответ на психоэмоциональный стресс у больных с выраженной дисфункцией ЛЖ выявляли чаще, чем у лиц с нормальной ФВ (50 и 9% соответственно).
Ишемия, вызванная психоэмоциональным стрессом, может иметь важное клиническое значение именно для пациентов с дисфункцией ЛЖ.
Ишемия, вызванная психоэмоциональным стрессом, чаще бывает «немой» (или бессимптомной), чем ишемия, спровоцированная физической нагрузкой. В одном из исследований было показано, что 83% эпизодов ишемии, индуцированной психоэмоциональным стрессом, были бессимптомными. У 30% пациентов с ИБС, у которых отсутствовали признаки ишемии миокарда во время физической нагрузки, была ишемия, спровоцированная психоэмоциональным стрессом. Это позволило предположить, что психоэмоциональный стресс и физическая нагрузка вызывают ишемию различными, но связанными друг с другом механизмами.
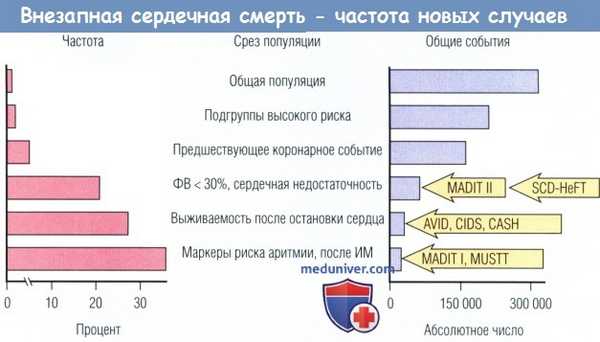
Влияние популяционных подгрупп и времени событий на клиническую эпидемиологию внезапной серденной смерти (ВСС).
Определение частоты возникновения новых случаев (%/год) и общего числа событий в год среди взрослого населения США и среди популяционных подгрупп высокого риска.
Общей численности взрослого населения соответствует 0,1-0,2% ВС в год, что составляет более 300 тыс. событий в год.
При выявлении более мощных факторов риска частота прогрессивно увеличивается, что сопровождается прогрессивным снижением общего числа событий в каждой представленной группе.
Обратную зависимость между частотой распространения и общим количеством событий объясняют постепенным уменьшением пула деноминатора в высших подгрупповых категориях.
Для успешных мероприятий в больших популяционных подгруппах необходимо определить специфические маркеры, чтобы увеличить выявление пациентов с особенно высоким риском
(горизонтальная ось для частоты не является линейной, ее следует интерпретировать соответствующим образом).
При мониторировании больных ИБС в условиях повседневной жизни установлено, что умственное напряжение, не сопряженное с физической нагрузкой, часто вызывает транзиторную ишемию миокарда. Такая ишемия наблюдается, например, во время управления автомобилем или публичного выступления. Большинство эпизодов ишемии в повседневной жизни не индуцированы психологическим или умственным напряжением, но некоторые из них (возможно, 25%) связаны.
Пациенты с ИБС, у которых отмечается ишемия, индуцированная психоэмоциональным стрессом, имеют повышенный риск нефатальных и фатальных кардиальных событий в будущем. Эта связь сохраняется и после учета других ФР (включая возраст, функцию ЛЖ и ИМ в анамнезе).
Острый стресс может способствовать развитию ИБС посредством многих механизмов. Во-первых, при стрессе возрастает потребность миокарда в кислороде вследствие гемодинамических эффектов. Во-вторых, вазоспазм может уменьшить коронарный кровоток, особенно в наиболее пораженных сосудах. В-третьих, в ответ на стресс увеличивается выделение кортизола и катехоламинов, которые активируют тромбоциты и провоцируют их агрегацию, а также повышают уровень ХС и снижают уровень ЛВП.
Все эти механизмы приводят к повышению потребности миокарда в кислороде при одновременном ограничении коронарного кровотока, способствуют разрыву бляшки и формированию тромба.
Внезапные эмоции. Исследования гнева, депрессии и тревоги имеют отношение к отдаленным последствиям подверженности человека устойчивым эмоциям. Вместе с тем существует большое количество работ, посвященных острым эффектам внезапных интенсивных отрицательных эмоций. Поскольку большая часть этих работ касается аритмий и ВСС, они будут рассмотрены в следующем разделе. Однако умственная деятельность, приводящая к сильному гневу или фрустрации и, в меньшей степени, к тревоге и пониженному настроению, может способствовать развитию ишемии миокарда. В течение 1-2 час, следующих за эпизодом сильного гнева, относительный риск ИМ колеблется между 2,3 и 9. Поскольку интенсивные отрицательные эмоциональные переживания вызывают активацию СНС, они могут вызывать спазм КА, разрыв атеросклеротических бляшек и повышение агрегации тромбоцитов.
Гнев и враждебность особенно тесно связаны с увеличением агрегации тромбоцитов. По данным амбулаторного мониторирования, враждебность также ассоциирована со снижением парасимпатического тонуса. При экспериментально вызванном гневе у пациентов с повышенным уровнем враждебности ответ сердечно-сосудистой системы, опосредованный активацией СНС, был сильнее, чем у пациентов с более низким уровнем враждебности.
Депрессивные расстройства у пациентов с ИБС: возможности диагностики и лечения в кардиологическом стационаре
В работе второго съезда Евразийской аритмологической ассоциации и восьмого съезда кардиологов, кардиохирургов и рентгенэндоваскулярных хирургов Республики Беларусь принял участие заведующий отделением общеклинической кардиологии и эпидемиологии сердечно-сосудистых заболеваний НИИ кардиологии Томского НИМЦ РАН, доктор мед. наук, профессор Алексей Репин.
Он обратил внимание на проблему депрессивных расстройств у пациентов с ишемической болезнью сердца, поделился опытом диагностики и лечения в кардиологическом отделении.
Болезни сердца и депрессия
Актуальность проблемы

О тесной взаимосвязи депрессии и заболеваний сердечно-сосудистой системы известно давно, тем не менее эта проблема часто недооценивается. Депрессия является основным психосоциальным фактором риска развития кардиоваскулярных заболеваний.
Среди пациентов с ишемической болезнью сердца (ИБС) депрессия встречается в 3 раза чаще, чем в общей популяции. Частота встречаемости депрессивных расстройств (ДР) в кардиологическом стационаре составляет 23-29 %, встречаемость ДР при перенесенном инфаркте миокарда — 30-38 %, а после инсульта достигает 70 %. Всего же в мире от депрессии страдает от 2,5 % до 10 % населения.
В Беларуси, отмечают на кафедре кардиологии и внутренних болезней БГМУ, исследований по распространенности депрессии среди пациентов кардиологического профиля не проводилось, однако можно предположить, что ее уровень соответствует общемировым показателям.
Негативное влияние ДР на течение ИБС обусловлено двумя механизмами: патофизиологическим и поведенческим. Патофизиологический механизм реализуется через активацию гипоталамо-гипофизарной и симпатоадреналовой систем, подавление активности серотонинергической системы, активацию цитокинов, простагландинов, тромбоцитов. Поведенческий механизм определяет гиподинамию, социальную изоляцию, переедание и несоблюдение диеты, курение, алкоголизацию, некомплаентность. На всех этапах лечения и реабилитации пациентов с ИБС и сочетанными ДР необходимо учитывать каждый из этих механизмов.
Алексей Репин отметил, что Европейское общество кардиологов с 2016 года указывает на необходимость раннего выявления психосоциальных факторов риска ИБС и перенесенного инфаркта миокарда, т. к. они препятствуют повышению приверженности к терапии, усилиям по улучшению образа жизни у пациентов. Оценку психосоциальных факторов риска важно проводить для определения возможных барьеров к изменению образа жизни или соблюдению назначений у пациентов с высоким риском ССЗ или с установленным ССЗ.
Психосоциальные факторы риска ИБС и перенесенного инфаркта миокарда включают низкий социально-экономический статус, социальную изоляцию и низкую социальную поддержку, хронический стресс на работе и в семейной жизни, депрессию, тревогу, враждебность (как черту характера) и гнев, тип личности D (с постоянной склонностью испытывать широкий спектр отрицательных эмоций).
Депрессия и ИБС:
- аффективные расстройства коррелируют с 3-кратным увеличением риска развития инфаркта миокарда и смертности от ИБС, а также более тяжелым течением ИБС, особенно при коморбидности с тревогой;
- ассоциация остается достоверной даже после учета факторов риска, а лечение антидепрессантами снижает риск развития ИБС и утяжеления ее течения.
Алексей Репин:
Согласно российскому закону о психиатрической помощи окончательный диагноз психического расстройства ставится врачом-психиатром или врачом- психотерапевтом. При этом врачи общей практики, терапевты, кардиологи имеют право диагностировать психическое расстройство (диагноз носит предварительный характер), а также назначать лекарственные средства с целью коррекции депрессивного расстройства с обоснованием и в соответствии с протоколами лечения после подтверждения диагноза психиатром или психотерапевтом.
Почему в команде с кардиологом должен работать психиатр или психотерапевт? Для подтверждения диагноза пациента направляют на прием к психиатру или психотерапевту, куда в итоге 85 % не доходят. Кроме того, все чаще наблюдаются скрытые, маскированные депрессии, трудные для диагностики и лечения. В клинической картине маскированной депрессии преобладает соматическая и вегетативная симптоматика, а типичных депрессивных жалоб может и не быть.
В Беларуси принят такой же подход к установлению диагноза и лечению психических расстройств (Прим. ред.).
Исследование: тревожно-депрессивные расстройства и ИБС
Мультидисциплинарная команда, включающая врачей-кардиологов и врачей-психиатров, провела исследование с целью оценки частоты встречаемости тревожно-депрессивных расстройств у разных групп пациентов с ИБС, возможности и эффективности комплексной терапии и реабилитации таких пациентов при динамическом наблюдении.
Критерии включения в исследование:
- информированное согласие пациента,
- возраст старше 18 лет,
- ИБС, диагностированная в соответствии с Национальными рекомендациями ВНОК (стабильная стенокардия II-III функционального класса, перенесенный инфаркт миокарда),
- выявленные аффективные (депрессивные) расстройства (рубрика F3 по МКБ-10).
Критерии исключения:
- отказ пациента от исследования,
- умеренная и тяжелая деменция,
- другие тяжелые органические заболевания головного мозга с выраженными когнитивными нарушениями (энцефалиты, менингиты, последствия ЧМТ),
- психические заболевания (шизофрения, алкогольная зависимость в период употребления и др.),
- острый ИМ или нестабильная стенокардия,
- пароксизмальные нарушения ритма,
- хроническая почечная и/или печеночная недостаточность.
Методы:
- общеклиническое и лабораторное обследование, ЭхоКГ, ТШХ, ВЭМ с ТФН;
- скрининг с использованием госпитальной шкалы тревоги и депрессии (HADS), шкалы самооценки социального функционирования, шкалы депрессии Бека и шкалы самооценки тревоги Шихана (при выявлении повышенного уровня тревоги и депрессии);
- консультация психиатра (при наличии симптомов психических расстройств и информированном согласии пациента с целью уточнения диагноза и выбора лечения), шкала Монтгомери — Асберга для оценки депрессии (MADRS), шкала тревоги Гамильтона (HARS), шкала глобального клинического впечатления (CGI), шкалы оценки побочных эффектов (UCU) (для оценки психического состояния).
Для лечения ДР врач-психиатр назначал антидепрессанты (предпочтительной была монотерапия), предлагались сеансы краткосрочной психотерапии, всем пациентам проводили общепринятую консервативную терапию ИБС.
К сожалению, часто на практике на этапе самооценки депрессии пациентом многие коллеги останавливаются. Так это не работает. В данном случае выявляется только категория высокого риска. Обязателен следующий шаг — консультация психиатра, чтобы верифицировать диагноз.
В нашем исследовании пациенты с выявленным повышением баллов по шкалам направлялись на консультацию к психиатру для уточнения диагноза и выбора способа терапии. При необходимости использовались антидепрессанты. Несколько месяцев мы совместно наблюдали пациентов.
В исследовании участвовал 1 331 человек. Тревога выявлена в 49,6 % случаев, депрессия — в 41,6 % (по шкале HADS).
У 75 % пациентов, имеющих симптомы депрессии и тревоги по данным самоопросников, диагноз был подтвержден клинически.
В 58,3 % случаев потребовалась антидепрессивная терапия.
Результаты
Особенности пациентов с ИБС с ДР:
- рефрактерность артериальной гипертензии (3 и более препаратов),
- низкая эффективность терапии ИБС,
- стенокардия значимо тяжелее,
- в 2 раза чаще переносили инфаркт миокарда,
- почти в 2 раза реже проводилась АКШ,
- в 3 раза реже проводилась ЧКВ.
Клинико-психопатологические особенности ДР у пациентов с хронической ИБС:
- первичность предъявления соматоформных жалоб на кардиалгию, одышку, аритмию, слабость,
- высокий удельный вес атипичной депрессии (42 %),
- наличие второго клинически значимого компонента (92 %), чаще тревожного, в структуре депрессивного синдрома,
- скрытые (социально приемлемые) варианты суицидального поведения — ситуация, когда пациент подвергает себя чрезмерной физической нагрузке в условиях ограничения возможности оказания помощи,
- коморбидность с алкогольной (22,1 %) и никотиновой (28,6 %) зависимостью.
Алексей Репин назвал также рекомендованные для использования в кардиологии антидепрессанты.
Препараты первого ряда:
- флуоксетин, флувоксамин, пароксетин, сертралин, эсциталопрам,
- тразодон,
- агомелатин.
Препараты второго ряда:
В списке отсутствуют трициклические антидепрессанты (ТЦА). Почему? ТЦА оказывают выраженный антидепрессивный эффект и по эффективности при тяжелой депрессии превосходят некоторые более новые группы лекарственных средств, в частности селективные ингибиторы обратного захвата серотонина (СИОЗС). Однако ТЦА значительно уступают антидепрессантам последующих поколений по безопасности и переносимости. В последние годы появляется все больше данных о том, что у пациентов с ИБС ТЦА могут повышать риск смерти и развития инфаркта миокарда.
С учетом высокого риска развития побочных эффектов при приеме ТЦА и наличия более безопасных альтернативных препаратов в настоящее время рекомендуют применять ТЦА только для терапии тяжелых, рефрактерных случаев депрессии, лечением которых должны заниматься исключительно врачи-психиатры. ТЦА в сравнении с СИОЗС никаких преимуществ у наших пациентов не имеют.
В рамках исследования антидепрессанты назначались минимум на 6 месяцев. Удержать пациентов на терапии удавалось от 2 до 5 месяцев. Затем, поясняет эксперт, больные отменяли себе лечение. Тем не менее препараты показали свой эффект.
Динамика симптомов на фоне терапии антидепрессантами:
- Значимое улучшение по синдрому стенокардии — 72 %.
- Уменьшение степени выраженности и продолжительности ангинозных приступов (>50 %).
- Увеличение активности, работоспособности и переносимости физических нагрузок, уменьшение усталости.
- Улучшение способности пациентов различать ангинозную и неангинозную боль, а также изменение отношения к боли.
Эффективность антидепрессивной терапии
Побочные эффекты были выражены слабо и не нарушали повседневное функционирование пациентов (тошнота — 8 %, сонливость — 8,5 %, половая дисфункция — 4 %). Признаков суицидального поведения не отмечалось. На фоне длительной антидепрессивной терапии также не выявлено значимых изменений показателей билирубина, трансаминаз, глюкозы, холестерина, креатинина, коагулограммы, а при суточном мониторировании ЭКГ — проаритмогенного эффекта, отсутствовало удлинение QT.
Специалисты отметили, что у исследуемых пациентов сначала манифестировало ДР, а уже потом возникала симптоматика ИБС.
Группы различались по функции мгновенных рисков: больные ИБС с ДР имели высокий риск смерти в течение первого года после выявления аффективной симптоматики (т. е. в период течения депрессивного эпизода), а в группе без ДР он увеличивался со временем наблюдения, к 6-7-му году.
Однако спустя время обнаружены статистически значимые различия в отдаленной летальности. Выживаемость в группе больных, получавших терапию современными антидепрессантами с низким риском кардиоваскулярных побочных эффектов, была на порядок выше, чем в группе с естественным течением аффективного расстройства. Худшие показатели выживаемости выявлены у пациентов с рекуррентной (рецидивирующей) депрессией.
Таким образом, оптимальная антидепрессивная терапия может увеличивать выживаемость больных хронической ИБС. Пациенты с коронарной болезнью сердца и аффективными расстройствами нуждаются в комплексной дифференцированной помощи (в т. ч. в информировании, психотерапии, психофармакотерапии). Необходимо назначение антидепрессантов психиатром совместно с кардиологом с обсуждением возможных рисков и выгоды на фоне терапии ИБС.
Читайте также:
