Т-лимфомы. Классификация Т-клеточных лимфом.
Добавил пользователь Morpheus Обновлено: 01.02.2026
Т-клеточная лимфома кожи (ТКЛК) — это разнородная группа заболеваний, относящихся к неходжкинским лимфомам, основной чертой которых является инфильтрация кожи злокачественными моноклональными Т-лимфоцитами.
Почему развивается Т-клеточная лимфома кожи
Возникновение Т-клеточной лимфомы связано с мутацией зрелых Т-лимфоцитов, что приводит к их бесконтрольному размножению, миграции в кожу и ее инфильтрации. Что именно вызывает мутацию, неизвестно. Предполагается, что она может быть спровоцирована стимуляцией антигенами в результате сбоя работы иммунной системы.
Спровоцировать сбой иммунной системы могут следующие факторы:
- Вирусные инфекции: вирус Эпштейн-Барра, цитомегаловирус, вирус простого герпеса, ретровирусы, лимфотропный вирус человека и др.
- Некоторые химические вещества, которые используются в промышленности, сельском хозяйстве, строительстве и др.
- Ионизирующее излучение, в том числе лучевая терапия в анамнезе.
- Избыточное воздействие УФ-лучей на кожу.
Т-клеточная лимфома кожи может быть первичной и вторичной. Первичные формы начинаются с поражения кожи. При вторичных сначала поражается лимфоидный орган (например, лимфоузлы), в результате чего в нем происходит размножение и накопление лимфоцитов, потом они мигрируют в кожу и инфильтрируют ее.
Виды Т-клеточных лимфом кожи и их стадии
Выделяют следующие виды Т-клеточной лимфомы кожи:
- Грибовидный микоз.
- Синдром Сезари.
- CD30+ Т-клеточные лимфомы — лимфатоидный папулез (ЛП) и кожная анапластическая крупноклеточная лимфома (КАКЛ).
- Панникулитоподобная Т-клеточная лимфома подкожной клетчатки.
- Первичная кожная агрессивная эпидермотропная CD8+ Т-клеточная лимфома.
- Первичная кожная мелко/среднеклеточная CD4+ Т-клеточная лимфома.
Наиболее часто встречаемые первые 2 типа опухоли. При их стадировании заболевания учитываются следующие факторы:
- Степень поражения кожных покровов.
- Вовлеченность в процесс лимфатических узлов.
- Лимфоидное поражение внутренних органов.
- Поражение системы кроветворения.
Их стадирование происходит согласно следующей схеме:
- 1А стадия. Имеются кожные поражения в виде пятен, которые занимают менее 10% кожного покрова, лимфоузлы не увеличены, в крови обнаруживается незначительное количество атипичных клеток Сезари.
- 1В стадия. Помимо пятен на коже, образуются бляшки, но объем высыпаний не превышает 10% от кожного покрова. Остальные признаки такие же, как на 1А стадии.
- 2А стадия. К вышеперечисленным симптомам добавляется поражение лимфатических узлов.
- 2В стадия. На коже появляются узлы.
- 3 стадия. Кожные проявления генерализуются, образуют сливающуюся эритему и покрывают более 90% поверхности тела.
- При 4 стадии, в крови обнаруживается большое количество атипичных клеток Сезари (более 1000 на микролитр), плюс присоединяется лимфоидное поражение внутренних органов.

Пациентов с синдромом Сезари изначально относят к 4 стадии заболевания, поскольку у них имеется обширная эритродермия и большое количество атипичных лимфоцитов в крови.
Остальные нозологии Т-клеточных лимфом, не являющиеся грибовидным микозом и синдромом Сезари, стадируются на основании следующих признаков:
- Т1А — имеется единичный очаг поражения не превышающий 5 см.
- Т1В — единичный очаг поражения, превышающий 5 см.
- Т2 — имеются множественные высыпания кожи, не выходящие за пределы 1-2 зон
- Т2А — зона поражения не превышает 15 см.
- Т2В — зона поражения не превышает 30 см.
- Т2С — высыпания распространяются более чем на 30 см.
- Т3 — имеется поражение кожи, затрагивающее не рядом расположенные зоны, либо высыпания занимают более 3 зон.
Поражение лимфатических узлов:
- N0 — нет увеличения лимфоузлов, ни центральных, ни периферических.
- N1 — поражена 1 группа периферических ЛУ, которые осуществляют лимфодренаж от пораженного участка кожи.
- N2 — поражено более 1 группы ЛУ, липо есть признаки поражения ЛУ, не осуществляющих дренаж вовлеченной области кожи.
- N3 имеются данные за поражение центральных ЛУ.
Поражение внутренних органов:
- М0 — поражения внутренних органов не обнаружено.
- М1 — есть данные за поражение внутренних органов (требуется морфологическое подтверждение).
Как проявляется лимфома кожи, симптомы
Симптоматические проявления будут зависеть от типа Т-клеточной лимфомы.
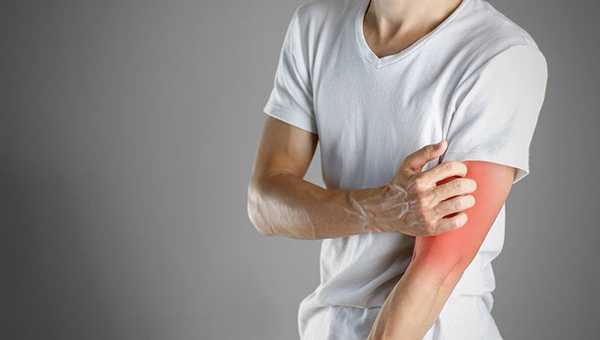
Симптомы грибовидного микоза:
- Высыпания в виде пятен и бляшек различной формы и цвета. Они носят множественный характер и располагаются на участках кожи, не подвергающихся инсоляции (зона купальника).
- Феномен одновременного прогрессирования и регресса разных элементов сыпи.
- Пойкилодермия — в зоне клеточных высыпаний имеется пятнистая пигментация, расширение кровеносных сосудов и атрофические изменения кожи.
- Наличие зуда.
В зависимости от стадии заболевания, грибовидный микоз будет иметь следующие особенности. На начальном этапе (1 стадия) отмечается наличие множественных или единичных пятен, которые могут достигать размеров в 20 см. Пятна зудят и могут шелушиться. Внешне они напоминают псориаз или экзему. На этой стадии заболевание может существовать годами и даже десятилетиями. Пятна могут спонтанно регрессировать и образовываться снова. Учитывая то, что клиническая картина сходна с другими дерматологическими нозологиями, правильный диагноз сразу поставить сложно, как правило, на это занимает достаточно длительное время.
Для второй стадии пятна начинают трансформироваться в бляшки — пораженная кожа утолщается и как бы приподнимается над здоровой, ее цвет становится красно-синюшным. Бляшки могут спонтанно регрессировать, или, наоборот, увеличиваться в размерах и сливаться друг с другом. На их поверхности может быть шелушение.
На 3 стадии образуются кожные опухоли в виде куполообразных красно-синюшных узлов, с гладкой поверхностью. Узлы увеличиваются в размерах и распадаются, при этом образуются язвы с кровянисто-гнойным отделяемым.
Панникулитоподобная Т-клеточная лимфома подкожной клетчатки проявляется множественными плотными бляшками, либо узлами различного цвета, которые преимущественно располагаются на нижних конечностях. Клинически напоминают панникулит (воспаление подкожной клетчатки).
Первичная CD4+кожная лимфома из мелких/крупных клеток проявляется единичными или множественными узлами синюшно-багрового цвета. В отличие от грибовидного микоза, узлы появляются сразу, без этапа пятна и бляшки.
Клиническим проявлением синдрома Сезари является наличие обширной эритемы (покраснения кожи), которая распространяется не менее чем на 80% покровов тела. Эритема может шелушится, но не обязательно. Характерно увеличение лимфоузлов до размеров ореха. Чаще всего, поражаются паховые и подмышечные ЛУ.
CD30+ Т-клеточная лимфома проявляется рецидивирующими сгруппированными или диссеминированными папулезными высыпаниями. Отдельные элементы могут спонтанно регрессировать в течение нескольких недель, причем на данном фоне могут образовываться новые папулы. В ряде случаев элементы сыпи могут некротизироваться с образованием некротических язв размером от 1 до 4 см, которые самопроизвольно разрешаются с формированием рубца.
Диагностика Т-клеточной лимфомы кожи
Для постановки диагноза необходимо комплексное обследование:
- Осмотр кожных высыпаний.
- Морфологическое и иммунотипическое исследование биоптатов кожи из очагов поражения. Чтобы результаты биопсии были более информативным, необходима отмена всех наружных препаратов, а также системных глюкокортикостероидов за две недели до забора материала. В сомнительных случаях проводят повторную биопсию через 2-4 недели после предыдущей и материал берут из разных очагов.
- Молекулярно-генетические исследования для определения характерных генетических мутаций.
При подозрении на синдром Сезари проводят такое же обследование, как и при грибовидном микозе (ГМ), плюс добавляют следующие данные:
- Определение площади поражения кожи. Если есть узлы, определяют их количество и размер наибольшего из них.
- Производят определение количества клеток Сезари с помощью проточной цитометрии.
Как проводится лечение лимфомы кожи
Для лечения лимфомы кожи используется химиотерапия. Схемы будут определяться типом заболевания и его стадией.
Лечение грибовидного микоза
При 1А стадии возможна тактика наблюдения — «наблюдай и жди». При прогрессировании до 1В и 2А стадии проводится наружная терапия, при этом используются следующие средства:
- Топические кортикостероиды. Их необходимо наносить на поверхность пятен и бляшек.
- УФО спектра В — узковолоконное ультрафиолетовое облучение лучами спектра В. Может применяться для пятен и тонких бляшек.
- ПУВА-терапия — псорален + УФО лучами спектра А. Данный вид лечения эффективен при толстых бляшках и фолликулярной форме ГМ.
- Локальная лучевая терапия в СОД 10-20 Гр. Применяется при единичных высыпаниях.
- Тотальная лучевая терапия (ТЛК). Проводится при наличии распространенных высыпаний, которые не реагируют на топические стероиды. Облучение проводится в суммарной очаговой дозе 30-40 Гр с фракционированием разовой очаговой дозы 1,2-1,5Гр. В качестве поддерживающего лечения после ТЛК применяется ПУВА-терапия. Т-клеточная лимфома кожи является чувствительной к облучению опухолью, поэтому лучевая терапия может применяться, как терапия первой линии при лечении ранних и поздних лимфом, так и для лечения рецидивов.

Если наружная терапия лимфомы кожи не оказала эффекта, добавляют вторую линию терапии, в рамках которой могут использоваться следующие системно действующие препараты:
- Ретиноиды.
- Интерфероны.
- Вериностат — ингибитор гистондеацетилазы. метотрексат или проспидин.
Лечение поздних стадий (2В-4В) лимфомы кожи
На поздних стадиях лимфомы кожи используется химиотерапия и электронно-лучевая терапия. Химиотерапия проводится с помощью вориностата. Его необходимо принимать перорально до достижения контроля заболевания (критериями контроля является отсутствие признаков прогрессирования). В случае развития неприемлемых токсических реакций препарат отменяют.
Лечение синдрома Сезари
Лечение СС базируется на следующих принципах:
- Комбинированное лечение (наружное и системное) является более эффективным, чем монотерапия.
- По возможности, следует избегать назначения цитостатиков, поскольку они подавляют иммунитет.
- Необходима своевременная диагностика и лечение инфекционных осложнений.
- Поскольку одним из основных симптомов, снижающих качество жизни пациентов, является зуд. Необходимо его эффективное устранение.
Терапия первой линии
Наилучшую эффективность в рамках терапии первой линии у больных с СС показал экстракорпоральный фотоферез (ЭКФ). Из цельной крови выделяют лейкоциты, которые обрабатывают фотосенсибилизирующим веществом и затем обрабатывают светом с заданной длиной волны. Это приводит к их гибели. За одну процедуру можно удалить только часть клеток, поэтому сеансы повторяют с определенной периодичностью — 1 раз в день в течение 2-х дней с последующим 4-х недельным перерывом.
Также может использоваться альфа-интерферон, только в более высоких дозах, чем при лечении ГМ, или метотрексат в низких дозах, при недоступности других видов терапии.
Для достижения лучшего эффекта, эти методы лечения комбинируют с методами наружной терапии, которые используются при ГМ, например:
- Альфа-интерферон + ПУВА.
- Метотрексат + наружные глюкокортикостероиды.
- ЭКФ + ТОК и др.
Терапия второй линии
При отсутствии эффекта от лечения первой линии, переходят ко второй. Здесь уже используются цитостатические препараты:
- Хлорамбуцил.
- Доксорубицин.
- Вориностат.
- Гемцитабин.
- Пентостатин.
- Флударабин+циклофосфамид.

Устранение зуда
Часто больных кожной лимфомой беспокоит зуд. Он может иметь ярко выраженный характер и существенно снижать качество жизни таких людей. Для борьбы с этим симптомом используются следующие препараты и методы терапии:
- Увлажняющие кремы.
- Антигистамины.
- Антибиотики. Доказано, что кожа больных СС обширно колонизирована золотистым стафилококком, поэтому назначение антибактериальных препаратов благоприятно сказывается не только на выраженности зуда, но и на общем течении заболевания.
Если зуд носит нестерпимый характер, назначается габапентин, который используется для лечения боли при нейропатиях. Начинают с дозировки 900 мг/сут, постепенно увеличивая ее до 3600 мг/сут. Для улучшения сна могут назначаться снотворные препараты.
Лечение лимфоматоидного папулеза
В настоящее время нет методов лечения, способных изменить ход течения заболевания или предотвратить его трансформацию в лимфому. Сам лимфоматоидный папулез не влияет на продолжительность жизни, поэтому тактика воздержания является предпочтительной — «наблюдай и жди».
Если имеются многочисленные генерализованные высыпания, используется ПУВА-терапия и низкие дозы метотрексата. Во время терапии наблюдается частичное исчезновение высыпаний, но после отмены лечения, они образуются снова. Полной ремиссии удается достичь редко.
В связи с этим, для контроля лечения необходима поддерживающая терапия с помощью данных методов, но необходимо помнить о возможных осложнениях. Например, ПУВА может спровоцировать развитие рака кожи, а метотрексат — фиброз печени.
Если имеются крупноузелковые элементы (более 2 см), которые не разрешаются самопроизвольно или под действием терапии, их можно удалить хирургически. Тем более при их наличии необходима биопсия для исключения вторичной анапластичной крупноклеточной лимфомы. Альтернативой может стать локальная лучевая терапия. В целом пациенты с ЛП должны пожизненно наблюдаться у врача, поскольку есть вероятность трансформации их заболевания в другие формы лимфом.
Лечение АКЛК
При одиночных или сгруппированных высыпаниях показано их хирургическое удаление или локальное облучение. Такая тактика позволяет добиться полной ремиссии у 95% пациентов. Но независимо от применяемого метода лечения, у 40% больных возникают рецидивы. Если они ограничены только кожными проявлениями, без затрагивания лимфатических узлов и внутренних органов, других методов лечения не требуется, можно использовать предыдущую тактику.
Для больных с множественными высыпаниями рекомендованы низкие дозы метотрексата (5-25 мг/нед). Если желаемый эффект не наступает, добавляют терапию альфа-интерфероном. При наличии очагов внекожного проявления необходима системная химиотерапия по протоколу CHOP.
Трансплантация костного мозга и стволовых клеток
При неэффективности других методов лечения, молодым пациентам с поздними стадиями заболевания может быть рекомендована химиотерапия с последующей аллогенной трансплантацией гемопоэтических стволовых клеток (ГСК). Процедура проводится следующим образом.
Первый этап — это химиотерапия, которая призвана уничтожить клон злокачественных Т-лимфоцитов. Этот этап называется кондиционирование. В рамках химиотерапии используются следующие препараты и режимы:
- CHOP — циклофосфамид, доксорубицин, винкристин, преднизолон
- EPOCH — этопозид, циклофосфамид, доксорубицин, винкристин, преднизолон.
- Пентостатин.
- Флурадабин+ интерферон альфа или циклофосфамид.
- Гемцитабин.
Вторым этапом является пересадка гемопоэтических клеток донора. Для реципиента эта процедура не представляет проблем и выглядит как обычное переливание крови. В течение последующих 3-4 недель трансплантат начинает приживаться в костном мозге, о чем свидетельствует повышение уровня лейкоцитов в крови. Генетически, это лейкоциты донора, и они должны полностью заменить иммунную системы больного. Весь этот процесс занимает от нескольких месяцев до года.
Процесс восстановления после лечения
Первый год после аллогенной трансплантации можно сравнить с периодом новорожденности — человек получает полностью новую иммунную систему, которая никогда раньше не сталкивалась с инфекционными заболеваниями. На ее «обучение» нужно время, и в этот период рекомендуется соблюдать ряд правил, которые помогут предотвратить инфицирование. Более подробно о них расскажут в больнице.
После того как иммунная система восстановится, необходимо будет заново пройти полный курс вакцинации, который выполняется в детском возрасте.
Прогноз
Прогноз заболевания зависит от клинической формы Т-клеточной лимфомы и ее стадии. Для пациентов с ранней стадией ГМ прогноз благоприятный, поскольку эта лимфома кожи очень редко прогрессирует до более серьезных стадий, и средняя продолжительность жизни таких больных составляет 12 лет.
Для пациентов с изначально более поздними стадиями Т-клеточной лимфомы (2В и больше) без признаков поражения внутренних органов, средняя продолжительность жизни составляет 5 лет, при этом для больных с поражением лимфоузлов прогноз несколько хуже, чем при системном обширном поражении кожи. Для больных, у которых лимфома кожи поразила внутренние органы, средняя продолжительность жизни составляет 2,5 года.
CD 30+ Т-клеточные лимфомы характеризуются относительно доброкачественным течением. В частности, лимфоматоидный папулез не влияет на продолжительность жизни больных, за исключением случаев трансформации в другие виды лимфом, в том числе грибовидный микоз, лимфому Ходжкина и др. Трансформация возникает у 4-25% больных и может возникнуть в период дебюта ЛП, после его излечения и даже предшествовать ему. Кожная анапластическая крупноклеточная лимфома также характеризуется благоприятным прогнозом, пятилетней выживаемости достигают 96% больных.
Периферические Т-клеточные лимфомы (ПТКЛ)
Периферические Т-клеточные лимфомы (ПТКЛ) представляют собой лимфомы, происходящие из зрелых (посттимических) Т-лимфоцитов и NK-клеток с первичными нодальными или экстранодальными манифестациями. ПТКЛ составляют более 10% всех диагностируемых неходжкинских лимфом.
Цель первичной системной терапии куративная. Однако примерно в 30% случаев может возникать рефракция на терапию. Ответ на последующую терапию, как правило, хуже, поэтому терапии второй линии рекомендовано проводить в рамках исследовательских программ.
Факторы риска
Причины возникновения неходжкинских лимфом, в том числе периферических Т-клеточных лимфом до конца не изучены. Согласно исследованиям, к факторам риска развития заболевания можно отнести длительный прием иммуносупресивных препаратов, а также наличие глютеновой энтеропатии (целиакии).
Заболевание может возникнуть в любом возрасте, однако чаще поражает людей старше 60 лет. Мужчины заболевают чаще женщин, соотношение составляет 3:2.
Симптомы заболевания
Как и при других видах лимфом, начальными признаками заболевания часто являются увеличенные безболезненные лимфатические узлы и/или экстранодальные манифестации. При Т-клеточных лимфомах, ассоциированных с энтеропатией и мономорфной эпителиотропной Т-клеточной лимфоме экстранодальные манифестации возникают, как правило, в области гастроинтестинального тракта, при экстранодальной NK-T-клеточной лимфоме носового типа, в области носа и его придаточных пазух. Панникулитоподобная Т-клеточная лимфома проявляется в виде подкожных уплотнений.
Типичной для периферических Т-клеточных лимфом является В-симптоматика (потеря веса, ночное потоотделение, сильная слабость) и высокая подверженность инфекциям. При ангиоиммунобластной Т-клеточной лимфоме часто наблюдаются поликлональная гипергаммаглобулинемия, кумбс-положительная гемолитическая анемия или Эппштейн-Барр ассоциированные и клональные В-клеточные пролифирации.
Классификация периферических Т-клеточных лимфом
Всемирная организация здравоохранения классифицирует следующие формы периферических Т-клеточных лимфом:
Т-клеточный пролимфоцитарный лейкоз (T-PLL)
Т-клеточный лейкоз из больших гранулярных лимфоцитов (Z-LGL)
Хроническое лимфопролиферативное нарушение NK-клеток (CLPD-NK)
Агрессивный NK-клеточный лейкоз (ANKL)
Эппштейн-Барр ассоциированная + T-клеточная лимфома детского возраста (EBVT)
Гидроа-вакциниформное лимфопролиферативное заболевание (HV-подобная LPD)
Взрослый Т-клеточный лейкоз/лимфома (ATLL)
Экстранодальная NK/T-клеточная лимфома носового типа (ENKTL)
Т-клеточная лимфома ассоциированная с энтеропатией (EATL)
Мономорфная эпителиотропная интестинальная Т-клеточная лимфома (MEITL)
Индолентное Т-клеточное лимфопролиферативное заболевание ЖКТ (ITCLD-GT)
Гепатолиенальная Т-клеточная лимфома (HSTL)
Подкожная панникулитоподобная Т-клеточная лимфома (SPTCL)
Грибовидный (фунгоидный) микоз (MF)
Синдром Сезари (SS)
Первичные кожные CD30+Т-клеточные лимфопролиферативные заболевания (PCTPD)
- Лимфоматоидный папулез (LyP);
- Первичная кожная анапластическая крупноклеточная лимфома (PCALCL).
Первичная кожная yo-Т-клеточная лимфома (PCGDTCL)
Первичная кожная агрессивная эпидермотропная CD8+ цитотоксическая Т-клеточная лимфома (PCACETL)
Первичная кожная акральная CD8+ Т-клеточная лимфома (PCATCL)
Первичная кожная CD4+ у мелко-/среднеклеточные Т-клеточные лимфопролиферативные нарушения (PCSM-LPD)
Периферическая Т-клеточная лимфома, NOS (PTCL, NOS)
Ангиоиммунобластная Т-клеточная лимфома (AITL)
Фолликулярная Т-клеточная лимфома (FTCL)
Нодальная периферическая Т-клеточная лимфома с TFH-фенотипом (PTCLTFH)
Анапластическая крупноклеточная лимфома, ALK+ (ALCL, ALK+)
Анапластическая крупноклеточная лимфома, ALK- (ALCL, ALK-)
Ассоциированная с грудным имплантом анапластическая крупноклеточная лимфома (BIA-ALCL)
Диагностика периферических Т-клеточных лимфом
Диагноз Т-клеточная лимфома ставится на основании патологического исследования тканей (например, анализа удаленного лимфатического узла, или биопсии других тканей). Очень часто необходимыми являются иммунологические или молекулярно-биологические исследования. Во многих случаях целесообразно проведение второго пересмотра заключения патологоанатомами, специализирующимися на диагностике лимфом.
Пункция костного мозга
Во время проведения пункции (биопсии) осуществляется забор клеток и тканей костного мозга. Это, как правило, является частью контроля за состоянием пациентов при патологиях крови.
Для определения распространения заболевания и его стадии проводятся такие обследования как:
- Компьютерная томография (КТ), при необходимости в комбинации с позитронно-эмиссионной томографией (ПЭТ), шеи, грудной клетки, живота и малого таза;
- Магнитно-резонансная томография (МРТ);
- При поражении костного мозга проводят пункцию костного мозга;
- При неврологических жалобах возможно проведение люмбальной пункции.
Многочисленные анализы крови позволяют сделать заключение об активности заболевания и наличии сопровождающих заболеваний, например вирусной инфекции. Кроме этого, проводятся обследования функции органов, например, ЭКГ и эхокардиография.
Первичный Т-клеточный лейкоз поражает, в первую очередь, органы лимфатической системы — лимфатические узлы и селезенку, но также костный мозг и другие органы, такие как кожа. Подтверждение диагноза в данном случае основывается преимущественно на анализе клеток крови, например, микроскопически и с помощью так называемой проточной цитофлуориметрии, для исследования картины признаков поверхностей клеток, а также на основе биопсии поврежденных тканей.
Неходжкинские лимфомы
Неходжкинские лимфомы (НХЛ) - это гетерогенная группа злокачественных лимфопролиферативных опухолей, различающихся по биологическим свойствам, морфологическому строению, клиническим проявлениям, ответу на терапию и прогнозу (ВОЗ, 2001 г.).
С 82.1. Фолликулярная неходжкинская лимфома, смешанная, мелкоклеточная с расщепленными ядрами и крупноклеточная фолликулярная.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Диагноз должен быть установлен согласно Классификации опухолей лимфатической системы (ВОЗ, 2001 г.). В скобках указаны иммунофенотипические характеристики соответствующего гистологического варианта.
(CD5 + CD10- CD19 + CD20 +/- CD21+ CD22-/+ CD23 + CD24+ CD103 - FMC-7- cCD38-; иммуноглобулины: sIg(M+/-D) - слабо; cIg - обычно отсутствуют).
(CD5 - CD10 - CD20 + CD21+ CD22 + CD23 -/+ CD24 + CD103 - FMC-7+ cCD38 -; имуноглобулины sIg+ярко; cIg-отсутствуют).
(CD5 - CD10 - CD19 + CD20 + CD21+ CD22 + CD23 - CD24 + CD103- FMC-7+ cCD38 +; иммуноглобулины: sIgM+; cIg + присутствуют).
(CD5 - CD10 - CD19 + CD20 + CD21 + CD22 + CD23 - CD24+ CD103+ FMC-7+ cCD38 -; иммуноглобулины sIg(M+/-D, реже G или A); cIg-обычно отсутствуют)
(CD5 - CD10 - CD19 - CD20 - CD21 - CD22 - CD23 - CD24 - CD103 - FMC-7 - cCD38++; иммуноглобулины: sIg отсутсвуют; cIG присутсвуют (G, A, редко D, E L-цепи).
Экстранодальные В-клеточные лимфомы маргинальной зоны мукозо-ассоциированной лимфоидной ткани (MALT-ома).
(CD5 - CD10 - Cd19 + CD20 + CD21 - Cd22 + CD23 - CD24 - CD103 - FMC-7 + cCD38 - bcl1 -; иммуноглобулины: sIg(M>G>A), cIg присутсвуют (~40%))
(CD5 - CD10 +/- CD19 + CD20 + CD21 + CD22 + CD23 +/- CD24 + CD103 - FMC-7 + cCD38 -; иммуноглобулины: sIg (A, G), не всегда; cIg. BCL2+)
(CD5 + CD10 - CD19 + CD20 + CD21+ CD22 + C23 - CD24 + CD103 - FMC-7+ cCD38 -; иммуноглобулины: sIg(M+/-D), λ>κ; cIg обычно отсутствуют. BCL1+).
(CD5 - CD10 -/+ CD19 + CD20 + Cd21 + CD22+ Cd23 +/- CD24 + CD103 - FMC-7 + cCd38 - BCL6 + BCL-2 -/+; иммуноглобулины sIg чаще положительные, cIg - чаще отрицательные).
Медиастинальная (тимическая) В-крупноклеточная лимфома.
(CD5 - CD10 + CD19 + CD20 + CD21 +/- CD22 + CD23 - CD24 + CD103 - FMC-7(?) cCD38 - BCL6 + BCL2 -; иммуноглобулины: sIgM+; cIg отсутствуют).
Т-лимфобластная лимфома/лейкоз из клеток-предшественников (острый лимфобластный лейкоз из Т-клеток предшественников).
(CD2 + CD3 + CD4 + CD5 + CD7 + CD8 -/+ CD16 - CD30 - CC56 - CD57 - CD25 - TCRαβ + (CD1a - TdT - CD4 + CD8 + в 25% случаев)).
(CD2 + CD3 + CD4 - CD5 - CD7 - CD8 + CD16 + CD30 - CD56 +/- CD57 +/- CD25 - TCRαβ +/- TCRγδ -; редкие варианты CD4 +; CD4 + CD8 +; TCRγδ +).
(CD2 + CD3ε + CD4 - CD5 - CD7 - CD8 +/- CD16 +/- CD30 - CD56 + CD57 -/+ CD25 - TCRαβ -; присутствуют молекулы цитотоксических гранул: гранзим В, перфорин).
(CD2 +/- CD3 + CD4 - CD5 - CD7 + CD8 -/+ CD16 - CD30 +/- CD56 -/+ CD57 - CD25 +/- CD103 + TCRβγ +; присутствуют молекулы цитотоксических гранул: гранзим В, перфорин).
(CD2 + CD3 + CD4 - CD5 - CD7 - CD8 - CD16 - CD30 - CD56 +/- CD57 - CD25(?)TCRαβ - TCRγδ +; присутствуют молекулы цитотоксических гранул: гранзим В, перфорин).
(CD2 +/- CD3 +/- CD4 + CD5 +/- CD7 -/+ CD8 -/+ CD16 - CD30 - CD56 - CD57 - CD25 +/- TCRαβ +/-; особенность: крупные кластеры ФДК (CD21; CD23) вокруг пролиферирующих венул).
Диагностика специфических вариантов Т-лимфом является в большей степени морфологической, нежели иммунологической.
1. Т-лимфобластная лимфома/лейкоз из клеток-предшественников (острый лимфобластный лейкоз из Т-клеток предшественников).
Распределение НХЛ по стадиям осуществляется по классификации Ann Arbor (1971), разработанной для лимфомы Ходжкина.
Стадия I - поражение одной лимфатической зоны или структуры (I) или локализованное поражение одного экстралимфатического органа или ткани (IE) в пределах одного сегмента.
Стадия II - поражение двух или более лимфатических областей по одну сторону диафрагмы, либо локализованное поражение одного экстралимфатического органа или ткани и их регионарных лимфатических узлов с (или без) поражением других лимфатических областей по ту же сторону диафрагмы или без него (IIE). Для II стадии следует указывать число пораженных лимфатических зон.
Стадия III - поражение лимфатических узлов или структур по обе стороны диафрагмы, которое может сочетаться с локализованным поражением одного экстралимфатического органа или ткани (IIIE) либо с поражением селезенки (IIIS) или с поражением того и другого (III I+S).
Стадия IV - диссеминированное поражение одного или нескольких экстралимфатических органов, с поражением лимфатических узлов или без него, либо изолированное поражение экстралимфатического органа с поражением отдаленных (не регионарных) лимфатических узлов. Метастазы в печень или костный мозг - всегда IV стадия.
Отдельно обозначают симптомы интоксикации:
1. В - наличие одного или нескольких из следующих симптомов: ночной профузный пот, температура тела выше 38 о С не менее трех дней подряд без признаков воспалительного процесса, снижение массы тела на 10% за последние 6 мес.
2. А - отсутствие указанных симптомов.
Диагностика
Диагностические критерии*** (Описание достоверных признаков заболевания в зависимости от степени тяжести процесса)
Жалобы обусловлены расположением опухолевых очагов. При поражении лимфатических узлов шеи и средостения - часто сухой кашель, если есть сдавление крупных сосудов грудной полости - цианоз и отечность верхней половины тела и лица с нарушениями дыхания и тахикардией. При поражении лимфатических узлов брюшной полости и забрюшинного пространства - может быть развитие кишечной непроходимости, отеки нижних конечностей, желтуха, нарушение мочеотделения.
При поражении носоглотки - затруднение носового дыхания. При поражении молочной железы - диффузное уплотнение молочной железы. При поражении ЦНС - резкая головная боль, тошнота, рвота. При поражении ЖКТ - похудание, тошнота, рвота, снижение аппетита.
Детальный сбор анамнеза с особым вниманием к наличию симптомов интоксикации и темпу роста лимфатических узлов.
Тщательное пальпаторное обследование всех групп периферических лимфатических узлов (подчелюстных, шейно-надключичных, подключичных, подмышечных, подвздошных, паховых, бедренных, локтевых, затылочных), печени, селезенки. Осмотр ЛОР-врача (небные миндалины, носоглотка).
1. Клинический анализ крови, включая содержание эритроцитов, гемоглобина, тромбоцитов, лейкоцитарную формулу, СОЭ.
2. Биохимический анализ крови, включая исследование креатинина, мочевины, билирубина, общего белка, трансаминаз, ЛДГ, щелочной фосфатазы.
1. УЗИ:
- всех групп периферических лимфатических узлов, включая шейные, над- и подключичные, подмышечные, паховые, бедренные, парааортальных, подвздошных;
4. Рентгенография костей при наличии жалоб у больного на боли, а также при выявлении изменений на сцинтиграммах.
2. Биохимический анализ крови, включая исследование общего белка, креатинина, мочевины, билирубина, трансаминаз, ЛДГ, щелочной фосфатазы.
Эксцизионная биопсия. Для исследования берется самый ранний из появившихся лимфатических узлов, который удаляется полностью. При удалении узел не должен быть поврежден механически. Нежелательно для гистологического исследования использовать паховые лимфатические узлы, если имеются вовлеченные в процесс другие группы лимфатических узлов. Пункционная биопсия для начальной диагностики недостаточна.
Соскоб с кожи для цитологического исследования, а также гистологическое исследования участка кожного покрова при подозрении на поражение кожи.
Трансторакальная биопсия медиастинальных лимфатических узлов, эновидеоторакоскопическая биопсия медиастинальных лимфатических узлов.
Гистологическое исследование ткани лимфатического узла должно сопровождаться иммуногистохимическим исследованием.
1. УЗИ:
- всех групп периферических лимфатических узлов, включая шейные, над- и подключичные, подмышечные, паховые, бедренные, парааортальных, подвздошных;
3. Рентгенография костей при наличии жалоб у больного на боли, а также при выявлении изменений на сцинтиграммах.
4. Клинический анализ крови, включая содержание эритроцитов, гемоглобина, тромбоцитов, лейкоцитарную формулу, СОЭ.
5. Биохимический анализ крови, включая исследование креатинина, мочевины, билирубина, общего белка, трансаминаз, ЛДГ, щелочной фосфатазы.
6. Биопсия костного мозга (трепанобиопсия крыла подвздошной кости). Цитологического исследования недостаточно.
5. Люмбальная пункция (при лимфобластных лимфомах или при подозрении на поражение ЦНС) для исследования спинномозговой жидкости.
Дифференциальный диагноз
Лечение
Цели лечения - уменьшение размеров лимфоузлов, печени и селезенки, исчезновение (или уменьшение) симптомов опухолевой интоксикации.
Немедикаментозное лечение: режим и диета в зависимости от тяжести состояния пациента и наличия сопутствующей патологии.
Лечение больных проводится с учетом иммуноморфологического варианта лимфомы (лимфоидное преобладание или нет), стадии заболевания и наличия или отсутствия тех или иных факторов риска.
В I стадии лимфом НСЗ до и после лучевой терапии проводятся 2 цикла ПХТ по схеме флюдарабин 25 мг/м 2 в/в, ежедневно, 5 дней или схема СОР. В случае CD 20+ вариантов, рекомендовано сочетанное применение ритуксимаба (375 мг/м 2 - 6 введений) вместе с ПХТ по схеме R-СОР. Альтернативным вариантом могут быть 3 цикла ПХТ с последующей лучевой терапией без дополнительной химиотерапии после облучения, если к моменту начала лучевой терапии была достигнута полная ремиссия.
Больным с опухолями ВСЗ в I стадии до начала лучевой терапии и после нее требуется провести по 3 цикла ПХТ. В комбинацию препаратов должны быть включены антрациклины (R-CHOP, СНОР).
Во IIА стадии всем больным независимо от степени злокачественности следует проводить 6 курсов ПХТ: 3 до и 3 после лучевой терапии. Облучению подлежат только исходные зоны поражения (традиционный режим гамма-терапии до СОД 32-36 Грей). Профилактическое облучение всех групп лимфатических узлов нецелесообразно.
Для значительной части пациентов с лимфомами НСЗ в III-IV стадии процесса не существует излечивающей терапии.
2. R-FCМ* - ритуксимаб 375 мг/м 2 в 0-й день, флударабин 25 мг/м 2 в/в, в 1-3-й день и циклофосфамид 200 мг/м 2 в 1-3 день, митоксантрон - 8 мг/м 2 в 1-й день.
4. R-FМD* - ритуксимаб 375 мг/м 2 в 0-й день, флударабин 25 мг/м 2 в/в, в 1-3-й день и митоксантрон 10 мг/ м 2 в 1-й день, дексаметазон - 20 мг в сутки, в таблетках, в 1-5-й день.
5. R-CHOP* - ритуксимаб 375 мг/м 2 в 0-й день, циклофосфан 750 мг/м 2 в 1-й день, адриабластин 50 мг/м 2 в 1-й день, винкристин 1,4 мг/м 2 в 1-й день и преднизолон 40 мг/м 2 внутрь, в 1-5-й дни. Курсы повторяются каждый 21-й или 14-й день, всего 6- 8 курсов.
* Добавление к схемам ритуксимаба (375 мг/м 2 - в 0-й день, 6 введений) показано в случае CD 20+ вариантов (также см. таблицу «Рекомендованные схемы лечения с ритуксимабом при В-клеточных лимфомах»).
При достижении полной или частичной ремиссии (в том числе после индукционной терапии с включением ритуксимаба), показано проведение поддерживающей терапии ритуксимабом в течение 2-х лет: по 375 мг/м 2 ритуксимаба в виде в/в инфузии, каждые 2 месяца. Целесообразность поддерживающей терапии ритуксимабом убедительно доказана: использование современных терапевтических подходов позволило впервые продемонстрировать увеличение показателя общей выживаемости больных при фолликулярной лимфоме.
При рецидиве лимфомы мантийной зоны эффективно применение бортезомиба (велкейда) в дозе 1,3 мг/м 2 в/в, в 1, 4, 8 и 11 дни, перерыв 10 дней (с 12 по 21 день), всего 4 введения за цикл. Рекомендуется проводить лечение до достижения полной ремиссии с проведением 2-х консолидирующих циклов после достижения полной ремиссии (в среднем до 17 циклов).
При В-клеточных, CD20+ НХЛ НСЗ, фолликулярных или трансформирующихся НХЛ, в том числе рефрактерные, к ритуксимабу применяют зевалин.
Завершающим этапом лечения у больных с III стадией является лучевая терапия. Облучению подвергаются очаги исходного поражения в суммарной дозе 36 Гр. При IV стадии болезни лучевая терапия не является обязательным компонентом лечения, хотя проведение ее не исключено.
У больных с III-IV стадиями НХЛ при полной ремиссии в результате химиолучевого лечения, целесообразно применять поддерживающую терапию интерфероном α-2β в режиме 3 млн МЕ, подкожно, 3 раза в неделю, на протяжении 18 месяцев.
Основным лечебным подходом при III-IV стадии лимфом ВСЗ является ПХТ. Первой линией является схема R-CHOP - ритуксимаб 375 мг/м 2 в 0-й день, циклофосфан 750 мг/м 2 в 1-й день, адриабластин 50 мг/м 2 в 1-й день, винкристин 1,4 мг/м 2 в 1-й день и преднизолон 40 мг/м 2 внутрь, в 1-5-й дни. Курсы повторяются каждый 21-й или 14-й день, всего 6- 8 курсов. Добавление к схемам ритуксимаба ( 375 мг/м 2 - в 0-й день, 6 введений) показано в случае CD 20+ вариантов.
В III стадии после ПХТ следует лучевая терапия в СОД 36-40 Гр на зоны исходного поражения. Облучению подлежат зоны первичного поражения: общая доза на зоны с полной регрессией опухоли после химиотерапии - 36 Гр, при частичной регрессии - 40 Гр. У больных с IV стадией проведение лучевой терапии необязательно, но целесообразно облучить очаги с большой исходной массой опухоли. Облучению подлежат зоны первичного поражения: общая доза на зоны с полной регрессией опухоли после химиотерапии - 36 Гр, при частичной регрессии - 40 Гр. У больных с IV стадией проведение лучевой терапии необязательно.
Лечение лимфобластных лимфом и лимфом из мелких клеток с нерасщепленными ядрами (лимфома Беркитта и типа Беркитта) проводится по программам лечения острых лимфобластных лейкозов.
При химиотерапии агрессивных НХЛ следует стремиться к достижению полной ремиссии. Необходимо избегать снижения доз цитостатических препаратов и удлинения интервалов между курсами. При склонности к нейтропении оправдано назначение с профилактической целью гемопоэтических ростовых факторов.
Для лечения рецидивов предложен ряд схем ПХТ, включающих препараты, которые редко используют на первых этапах лечения: цитозар, цисплатин, метил-гаг, митоксантрон. Эффективность повторного лечения заметно ниже первичного.
В случаях второго, третьего рецидивов, а также первичной рефрактерности, назначение стандартных доз химиопрепаратов бесперспективно. Основным видом лечения в этом случае должна быть высокодозная химиотерапия в условиях специализированных клиник.
Неходжкинские лимфомы ( Лимфосаркома )
Неходжкинские лимфомы - опухолевые заболевания лимфатической системы, представленные злокачественными B- и T-клеточными лимфомами. Первичный очаг может возникать в лимфатических узлах либо других органах и в дальнейшем метастазировать лимфогенным или гематогенным путем. Клиника лимфом характеризуется лимфаденопатией, симптомами поражения того или иного органа, лихорадочно-интоксикационным синдромом. Диагностика основывается на клинико-рентгенологических данных, результатах исследования гемограммы, биоптата лимфоузлов и костного мозга. Противоопухолевое лечение включает курсы полихимиотерапии и лучевой терапии.
МКБ-10



Общие сведения
Неходжкинские лимфомы (НХЛ, лимфосаркомы) - различные по морфологии, клиническим признакам и течению злокачественные лимфопролиферативные опухоли, отличные по своим характеристикам от лимфомы Ходжкина (лимфогранулематоза). В зависимости от места возникновения первичного очага гемобластозы делятся на лейкозы (опухолевые поражения костного мозга) и лимфомы (опухоли лимфоидной ткани с первичной внекостномозговой локализацией). На основании отличительных морфологических признаков лимфомы, в свою очередь, подразделяются на ходжкинские и неходжкинские; к числу последних в гематологии относят В- и Т-клеточные лимфомы. Неходжкинские лимфомы встречаются во всех возрастных группах, однако более половины случаев лимфосарком диагностируется у лиц старше 60 лет. Средний показатель заболеваемости среди мужчин составляет 2-7 случая, среди женщин - 1-5 случаев на 100 000 населения. В течение последних лет прослеживается тенденция к прогрессирующему увеличению заболеваемости.

Причины
Этиология лимфосарком достоверно неизвестна. Более того, причины лимфом различных гистологических типов и локализаций существенно варьируются. В настоящее время правильнее говорить о факторах риска, повышающих вероятность развития лимфомы, которые на данный момент хорошо изучены. Влияние одних этиофакторов выражено значительно, вклад других в этиологию лимфом весьма несущественен. К такого рода неблагоприятным предпосылкам относятся:
- Инфекции. Наибольшим цитопатогенным эффектом на лимфоидные клетки обладает вирус иммунодефицита человека (ВИЧ), гепатита С, Т-лимфотропный вирус 1 типа. Доказана связь инфицирования вирусом Эпштейна-Барр с развитием лимфомы Беркитта. Известно, что инфекция Helicobacter pylori, ассоциированная с язвенной болезнью желудка, может вызывать развитие лимфомы той же локализации.
- Дефекты иммунитета. Риск возникновения лимфом повышается при врожденных и приобретенных иммунодефицитах (СПИДе, синдроме Вискотта-Олдрича, Луи-Бар, Х-сцепленном лимфопролиферативном синдроме и др.). У пациентов, получающих иммуносупрессивную терапию по поводу трансплантации костного мозга или органов, вероятность развития НХЛ увеличивается в 30-50 раз.
- Сопутствующие заболевания. Повышенный риск заболеваемости НХЛ отмечается среди пациентов с ревматоидным артритом, красной волчанкой, что может быть объяснено как иммунными нарушениями, так и использованием иммуносупрессивных препаратов для лечения данных состояний. Лимфома щитовидной железы обычно развивается на фоне аутоиммунного тиреоидита.
- Токсическое воздействие. Прослеживается причинно-следственная связь между лимфосаркомами и предшествующим контактом с химическими канцерогенами (бензолом, инсектицидами, гербицидами), УФ-излучением, проведением лучевой терапии по поводу онкологического заболевания. Прямое цитопатическое действие оказывают цитостатические препараты, применяемые для химиотерапии.
Патогенез
Патологический лимфогенез инициируется тем или иным онкогенным событием, вызывающим нарушение нормального клеточного цикла. В этом могут быть задействованы два механизма - активация онкогенов либо подавление опухолевых супрессоров (антионкогенов). Опухолевый клон при НХЛ в 90% случаев формируется из В-лимфоцитов, крайне редко - из Т-лимфоцитов, NK- клеток или недифференцированных клеток.
Для различных типов лимфом характерны определенные хромосомные транслокации, которые приводят к подавлению апоптоза, утрате контроля над пролиферацией и дифференцировкой лимфоцитов на любом этапе. Это сопровождается появлением клона бластных клеток в лимфатических органах. Лимфоузлы (периферические, медиастинальные, мезентериальные и др.) увеличиваются в размерах и могут нарушать функцию близлежащих органов. При инфильтрации костного мозга развивается цитопения. Разрастание и метастазирование опухолевой массы сопровождается кахексией.
Лимфосаркомы, первично развивающиеся в лимфоузлах называются нодальными, в других органах (небной и глоточных миндалинах, слюнных железах, желудке, селезенке, кишечнике, головном мозге, легких, коже, щитовидной железе и др.) - экстранодальными. По структуре опухолевой ткани НХЛ делятся на фолликулярные (нодулярные) и диффузные. По темпам прогрессирования лимфомы классифицируются на индолентные (с медленным, относительно благоприятным течением), агрессивные и высоко агрессивные (с бурным развитием и генерализацией). При отсутствии лечения больные с индолентными лимфомами живут в среднем 7 - 10 лет, с агрессивными - от нескольких месяцев до 1,5-2 лет.
Современная классификация насчитывает свыше 30 различных видов лимфосарком. Большая часть опухолей (85%) происходит из В-лимфоцитов (В-клеточные лимфомы), остальные из Т-лимфоцитов (Т-клеточные лимфомы). Внутри этих групп существуют различные подтипы неходжкинских лимфом. Группа В-клеточных опухолей включает:
- диффузную В-крупноклеточную лимфому - самый распространенный гистологический тип лимфосарком (31%). Характеризуется агрессивным ростом, несмотря на это почти в половине случаев поддается полному излечению.
- фолликулярную лимфому - ее частота составляет 22% от числа НХЛ. Течение индолентное, однако возможна трансформация в агрессивную диффузную лимфому. Прогноз 5-летней выживаемости - 60-70%.
- мелкоклеточную лимфоцитарную лимфомуи хронический лимфоцитарный лейкоз - близкие типы НХЛ, на долю которых приходится 7% от их числа. Течение медленное, но плохо поддающееся терапии. Прогноз вариабелен: в одних случаях лимфосаркома развивается в течение 10 лет, в других - на определенном этапе превращается в быстрорастущую лимфому.
- лимфому из мантийных клеток- в структуре НХЛ составляет 6%. Пятилетний рубеж выживаемости преодолевает лишь 20% больных.
- В-клеточные лимфомы из клеток маргинальной зоны - делятся на экстранодальные (могут развиваться в желудке, щитовидной, слюнных, молочных железах), нодальные (развиваются в лимфоузлах), селезеночную (с локализацией в селезенке). Отличаются медленным локальным ростом; на ранних стадиях хорошо поддаются излечению.
- В-клеточную медиастинальную лимфому - встречается редко (в 2% случаев), однако в отличие от других типов поражает преимущественно молодых женщин 30-40 лет. В связи с быстрым ростом вызывает компрессию органов средостения; излечивается в 50% случаев.
- макроглобулинемию Вальденстрема (лимфоплазмоцитарную лимфому) - диагностируется у 1% больных с НХЛ. Характеризуется гиперпродукцией IgM опухолевыми клетками, что приводит к повышению вязкости крови, сосудистым тромбозам, разрывам капилляров. Может иметь как относительно доброкачественное (с выживаемостью до 20 лет), так и скоротечное развитие (с гибелью пациента в течение 1-2 лет).
- волосатоклеточный лейкоз- очень редкий тип лимфомы, встречающийся у лиц пожилого возраста. Течение опухоли медленное, не всегда требующее лечения.
- лимфому Беркитта - на ее долю приходится около 2% НХЛ. В 90% случаев опухоль поражает молодых мужчин до 30 лет. Рост лимфомы Беркитта агрессивный; интенсивная химиотерапия позволяет добиться излечение половины больных.
- лимфому центральной нервной системы - первичное поражение ЦНС может затрагивать головной или спинной мозг. Чаще ассоциируется с ВИЧ-инфекцией. Пятилетняя выживаемость составляет 30%.
Неходжкинские лимфомы Т-клеточного происхождения представлены:
- Т-лимфобластной лимфомой или лейкозом из клеток-предшественников - встречается с частотой 2%. Различаются между собой количеством бластных клеток в костном мозге: при 25% - как лейкоз. Диагностируется преимущественно у молодых людей, средний возраст заболевших - 25 лет. Худший прогноз имеет Т-лимфобластный лейкоз, показатель излечения при котором не превышает 20%.
- периферическими Т-клеточными лимфомами, включающими кожную лимфому (синдром Сезари, грибовидный микоз), ангиоиммунобластную лимфому, экстранодальную лимфому из естественных киллеров, лимфому с энтеропатией, панникулитоподобную лимфому подкожной клетчатки, крупноклеточную анапластическую лимфому. Течение большей части Т-клеточных лимфом быстрое, а исход неблагоприятный.

Симптомы
Варианты клинических проявлений НХЛ сильно варьируются в зависимости от локализации первичного очага, распространенности опухолевого процесса, гистологического типа опухоли и пр. Все проявления лимфосарком укладываются в три синдрома: лимфаденопатии, лихорадки и интоксикации, экстранодального поражения. В большинстве случаев первым признаком НХЛ служит увеличение периферических лимфоузлов. Вначале они остаются эластичными и подвижными, позднее сливаются в обширные конгломераты. Одновременно могут поражаться лимфоузлы одной или многих областей. При образовании свищевых ходов необходимо исключить актиномикоз и туберкулез.
Такие неспецифические симптомы лимфосарком, как лихорадка без очевидных причин, ночная потливость, потеря веса, астения в большинстве случаев указывают на генерализованный характер заболевания. Среди экстранодальных поражений доминируют неходжкинские лимфомы кольца Пирогова-Вальдейера, ЖКТ, головного мозга, реже поражаются молочная железа, кости, паренхима легких и др. органы. Лимфома носоглотки при эндоскопическом исследовании имеет вид опухоли бледно-розового цвета с бугристыми контурами. Часто прорастает верхнечелюстную и решетчатую пазуху, орбиту, вызывая затруднение носового дыхания, ринофонию, снижение слуха, экзофтальм.
Первичная лимфосаркома яичка может иметь гладкую или бугристую поверхность, эластическую или каменистую плотность. В некоторых случаях развивается отек мошонки, изъязвление кожи над опухолью, увеличение пахово-подвздошных лимфоузлов. Лимфомы яичка предрасположены к ранней диссеминации с поражением второго яичка, ЦНС и др.
Лимфома молочной железы при пальпации определяется как четкий опухолевый узел или диффузное уплотнение груди; втяжение соска нехарактерно. При поражении желудка клиническая картина напоминает рак желудка, сопровождаясь болями, тошнотой, потерей аппетита, снижением веса. Абдоминальные лимфосаркомы могут проявлять себя частичной или полной кишечной непроходимостью, перитонитом, синдромом мальабсорбции, болями в животе, асцитом. Лимфома кожи проявляется зудом, узелками и уплотнением красновато-багрового цвета. Первичное поражение ЦНС более характерно для больных СПИДом - течение лимфомы данной локализации сопровождаются очаговой или менингеальной симптоматикой.
Осложнения
Наличие значительной опухолевой массы может вызывать сдавление органов с развитием жизнеугрожащих состояний. При поражении медиастинальных лимфоузлов развивается компрессия пищевода и трахеи, синдром сдавления ВПВ. Увеличенные внутрибрюшные и забрюшинные лимфатические узлы могут вызвать явления кишечной непроходимости, лимфостаза в нижней половине туловища, механической желтухи, компрессии мочеточника. Прорастание стенок желудка или кишечника опасно возникновением кровотечения (в случае аррозии сосудов) или перитонита (при выходе содержимого в брюшную полость). Иммуносупрессия обусловливает подверженность пациентов инфекционным заболеваниям, представляющим угрозу для жизни. Для лимфом высокой степени злокачественности характерно раннее лимфогенное и гематогенное метастазирование в головной и спинной мозг, печень, кости.
Вопросы диагностики неходжкинских лимфом находятся в компетенции онкогематологов. Клиническими критериями лимфосаркомы служат увеличение одной или нескольких групп лимфоузлов, явления интоксикации, экстранодальные поражения. Для подтверждения предполагаемого диагноза необходимо проведение морфологической верификации опухоли и инструментальной диагностики:
- Исследование клеточного субстрата опухоли. Выполняются диагностические операции: пункционная или эксцизионная биопсия лимфоузлов, лапароскопия, торакоскопия, аспирационная пункция костного мозга с последующими иммуногистохимическими, цитологическими, цитогенетическими и другими исследованиями диагностического материала. Кроме диагностики, установление структуры НХЛ важно для выбора тактики лечения и определения прогноза.
- Методы визуализации. Увеличение медиастинальных и внутрибрюшных лимфоузлов обнаруживается с помощью УЗИ средостения, рентгенографии и КТ грудной клетки, брюшной полости. В алгоритм обследования по показаниям входят УЗИ лимфатических узлов, печени, селезенки, молочных желез, щитовидной железы, органов мошонки, гастроскопия. С целью стадирования опухоли проводится МРТ внутренних органов; в выявлении метастазов информативны лимфосцинтиграфия, сцинтиграфия костей.
- Лабораторная диагностика. Направлена на оценку факторов риска и функции внутренних органов при лимфомах различных локализаций. В группе риска производится определение ВИЧ-антигена, анти-HCV. Изменение периферической крови (лимфоцитоз) характерно для лейкемизации. Во всех случаях исследуется биохимический комплекс, включающий печеночные ферменты, ЛДГ, мочевую кислоту, креатинин и др. показатели. Своеобразным онкомаркером НХЛ может служить b2-микроглобулин.
Дифференцировать неходжкинские лимфомы приходится с лимфогранулематозом, метастатическим раком, лимфаденитами, возникающими при туляремии, бруцеллезе, сифилисе, туберкулезе, токсоплазмозе, инфекционном мононуклеозе, гриппе, СКВ и др. При лимфомах конкретных локализаций проводятся консультации профильных специалистов: оториноларинголога, гастроэнтеролога, маммолога и т.д.

Варианты лечения неходжкинских лимфом включают оперативный метод, лучевую терапию и химиотерапию. Выбор методики определяется морфологическим типом, распространенностью, локализацией опухоли, сохранностью и возрастом больного. В современной онкогематологии приняты протоколы лечения лимфосарком, базирующиеся на использовании:
- Химиотерапии. Наиболее часто лечение лимфом начинают с курса полихимиотерапии. Этот метод может являться самостоятельным или сочетаться с лучевой терапией. Комбинированная химиолучевая терапия позволяет достичь более длительных ремиссий. Лечение продолжается до достижения полной ремиссии, после чего необходимо проведение еще 2-3 консолидирующих курсов. Возможно включение в циклы лечения гормонотерапии.
- Хирургических вмешательств. Обычно применяется при изолированном поражении какого-либо органа, чаще - ЖКТ. По возможности операции носят радикальный характер - выполняются расширенные и комбинированные резекции. В запущенных случаях, при угрозе перфорации полых органов, кровотечения, непроходимости кишечника могут выполняться циторедуктивные вмешательства. Хирургическое лечение обязательно дополняется химиотерапией.
- Лучевой терапии. В качестве монотерапии лимфом применяется только при локализованных формах и низкой степени злокачественности опухоли. Кроме этого, облучение может быть использовано и в качестве паллиативного метода при невозможности проведения других вариантов лечения.
- Дополнительных схем лечения. Из альтернативных методов хорошо себя зарекомендовала иммунохимиотерапия с применением интерферона, моноклональных антител. С целью консолидации ремиссии применяется трансплантация аутологичного или аллогенного костного мозга и введение периферических стволовых клеток.
Прогноз и профилактика
Прогноз при неходжкинских лимфомах различен, зависит, главным образом, от гистологического типа опухоли и стадии выявления. При местнораспространенных формах долгосрочная выживаемость в среднем составляет 50-60%, при генерализованных - всего 10-15%. Неблагоприятными прогностическими факторами служат возраст старше 60 лет, III-IV стадии онкопроцесса, вовлечение костного мозга, наличие нескольких экстранодальных очагов. Вместе с тем, современные протоколы ПХТ во многих случаях позволяют добиться долгосрочной ремиссии. Профилактика лимфом коррелирует с известными причинами: рекомендуется избегать инфицирования цитопатогенными вирусами, токсических воздействий, чрезмерной инсоляции. При наличии факторов риска необходимо проходить регулярное обследование.
2. Эпидемиология и биология неходжкинских лимфом/ Хансон К.П., Имянитов Е.Н.// Практическая онкология. - 2004 - Т.5, №3.
4. Современные подходы к терапии неходжкинских лимфом/ Поддубная И. В.// Русский медицинский журнал. - 2011. - №22.
Читайте также:
