Техника операции при чрез- и надмыщелковом переломе плечевой кости
Добавил пользователь Валентин П. Обновлено: 21.01.2026
Центральный научно-исследовательский институт травматологии и ортопедии им. Н.Н. Приорова Министерства здравоохранения и социального развития РФ, Москва
ФГАОУ ВО «Российский Университет Дружбы Народов», Москва, Россия
ФГБУ «НМИЦ ТО им. Н.Н. Приорова» Минздрава России, Москва, Россия
Тактика хирургического лечения посттравматических ложных суставов и дефектов диафиза плечевой кости
Журнал: Вестник травматологии и ортопедии им Н.Н. Приорова. 2019;(1): 35‑41
Актуальность. Переломы плечевой кости составляют от 5 до 8% от всех переломов костей скелета. Несращения их встречаются нечасто, однако в случае наличия инфекции, нарушенного кровоснабжения, при открытых, многооскольчатых переломах вторичное костное сращение может быть затруднено. В случае нарушенного местного репаративного потенциала выбор в пользу становится практически неизбежным. Цель исследования: определение показаний к кровоснабжаемой костной пластике при ложных суставах и дефектах плечевой кости и анализ ее эффективности. Пациенты и методы. В отделении микрохирургии и травмы кисти ФГБУ «НМИЦ ТО им. Н.Н. Приорова» в период с 2010 по 2017 г. было проведено оперативное лечение с использованием васкуляризованных костных трансплантатов 41 пациента с ложными суставами и дефектами плечевой кости. У 38 пациентов использовался васкуляризованный трансплантат из малоберцовой кости, у 3 — из медиального мыщелка бедренной кости. Во всех случаях применялся накостный остеосинтез пластиной. Оценка результатов проводилась на основании рентгенологического исследования и компьютерной томографии. Результаты. Консолидация перелома при кровоснабжаемой костной пластике была достигнута в 36 (88%) случаях в течение 4-6 мес: в группе с применением малоберцового трансплантата — в 33 случаях, в группе с применением трансплантата из мыщелка бедренной кости — у 3 пациентов. Заключение. Каждый ложный сустав плечевой кости имеет уникальный комплекс причин возникновения и требует индивидуализированного подхода. При длительно существующих посттравматических ложных суставах и дефектах плечевой кости кровоснабжаемая костная пластика является эффективным способом лечения. Конфликт интересов: не заявлен Источник финансирования: исследование проведено без спонсорской поддержки
Введение. Переломы плечевой кости составляют от 5 до 8% от всех переломов костей скелета [1]. Несращения их встречаются нечасто: накостный остеосинтез — в 5,5-8,7% случаев, блокируемый интрамедуллярный остеосинтез — в 3-5,6% [15]. Однако, несмотря на редкую встречаемость, они могут представлять значительные трудности для травматолога-ортопеда.
Существуют различные факторы, которые могут предрасполагать к несращению плечевой кости у пациента. Ожирение, остеопороз, алкоголизм, курение, сопутствующие заболевания могут увеличить частоту несращения, однако их невозможно скорректировать перед выполнением ревизионной хирургии [1]. Тем более что обычно у пациента имеется более одного фактора, приводящего к слабости репаративного потенциала при переломе плечевой кости [14].
Плохое качество кости, связанное с наличием у пациента остеоартрита или остеопороза может в дальнейшем компрометировать среду, необходимую для заживления перелома. В дополнение — рубцовые ткани, оставшиеся от предыдущих хирургических вмешательств, и близость сосудисто-нервных образований к медиальной стенке плечевой кости могут осложнить хирургический доступ к зоне несращения даже для опытного травматолога-ортопеда 7.
Описано много способов лечения ложных суставов плечевой кости, дающих различную вероятность успеха. Применяются открытая репозиция и внутренняя фиксация, интрамедуллярный остеосинтез, аппараты наружной фиксации, однако выбор оптимальной методики до настоящего времени остается предметом научных дебатов.
Частота сращения ложных суставов плечевой кости при использовании традиционных методик остеосинтеза в комбинации с использованием костных трансплантатов варьирует от 70 до 92% 2, однако в случае наличия инфекции, нарушенного кровоснабжения, при открытых, сегментарных или многооскольчатых переломах вторичное костное сращение может быть затруднено [7].
Распространенность костной консолидации при открытой репозиции и внутренней фиксации неинфицированного ложного сустава плечевой кости варьирует от 64 до 100% [11]. Присутствие инфекции часто ассоциировано со значительно более низкой вероятностью достижения костного сращения, ограничивает возможности хирургического лечения и приводит к ухудшению функциональных результатов [1, 4]. Лечение инфицированных ложных суставов, ложных суставов у пациентов с множеством предшествующих неудавшихся попыток оперативного лечения в анамнезе должно быть комплексным [15]. В таких ситуациях использование васкуляризованного костного трансплантата становится практически неизбежным, так как оно обусловливает большую вероятность успеха и ускорения репаративного процесса 16.
Дополнительным преимуществом васкуляризованного костного трансплантата является возможность его применения в сочетании с кожно-мышечным лоскутом для реконструкции сопутствующего мягкотканного дефекта.
Цель настоящего исследования — определение показаний к кровоснабжаемой костной пластике при ложных суставах и дефектах плечевой кости и анализ ее эффективности.
Материал и методы
В отделении микрохирургии и травмы кисти ФГБУ «НМИЦ ТО им. Н.Н. Приорова» в период с 2010 по 2017 г. было проведено оперативное лечение 41 пациента (19 мужчин, 22 женщины) с ложными суставами и дефектами плечевой кости с использованием васкуляризованных костных трансплантатов. Средний возраст пациентов составил 41 год (18-65 лет), средний период времени с момента травмы — 2 года и 4 мес (1-8 лет).
До поступления в НМИЦ ТО им. Н.Н. Приорова некоторые пациенты уже были оперированы с применением различных методик наружного и погружного остеосинтеза: среднее количество операций — 2,2 (2-7).
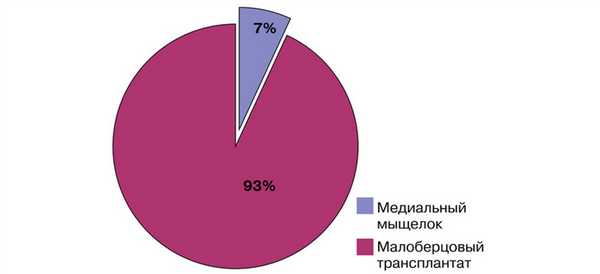
Кровоснабжаемый трансплантат из малоберцовой кости использовался у 38 (93%) пациентов, васкуляризованный трансплантат из медиального мыщелка бедренной кости — у 3 (7%) пациентов (рис. 1). Рис. 1. Распределение пациентов по типу васкуляризованного трансплантата.
Во всех случаях применялся накостный остеосинтез пластиной без контакта пластины с трансплантатом (мостовидная костная пластика).
Перед использованием лоскута из малоберцовой кости проводился тщательный костный и мягкотканный дебридмент.
При наличии показаний в раннем послеоперационном периоде проводилась ранняя хирургическая ревизия трансплантата, чтобы избежать нарушения в нем микроциркуляции.
Оценка результатов проводилась на основании данных рентгенологического исследования и компьютерной томографии.
Результаты
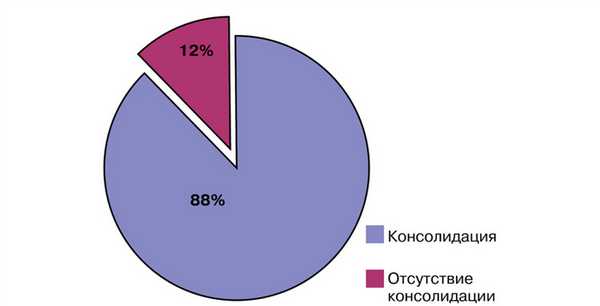
Консолидация перелома при кровоснабжаемой костной пластике была достигнута в 36 (88%) случаях в течение 4-6 мес (рис. 2): Рис. 2. Результаты оперативного лечения с использованием кровоснабжаемой костной пластикой. в группе применения малоберцового трансплантата консолидация была достигнута в 33 случаях, в группе трансплантата из мыщелка бедренной кости — в 3 случаях.
Клинический пример 1
Пациентка И., 34 лет.
Диагноз: последствия минно-взрывного ранения левого плеча с дефектом плечевой кости, мягких тканей, лучевого нерва. Остеомиелит.
На рис. 3-9 Рис. 3. Пациентка И., 34 лет. Внешний вид до операции. Рис. 9. Внешний вид и функция через год после операции. представлены все этапы обследования и лечения пациентки И.
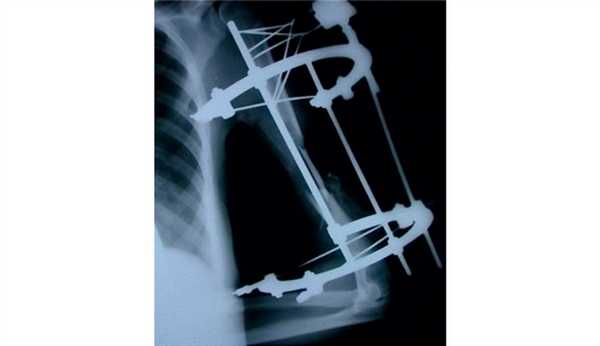
Рис. 4. Рентгенограмма пациентки И. до операции.
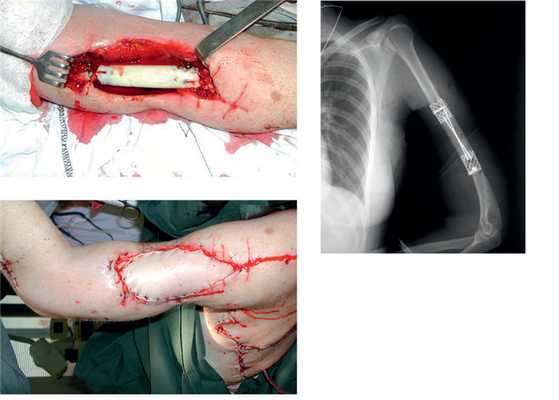
Рис. 5. Пациентка И. Этапное оперативное вмешательство. а — замещение дефекта плечевой кости цементным спейсером; б — транспозиция торакодорсального лоскута в область мягкотканного дефекта плеча; в — послеоперационная рентгенограмма.
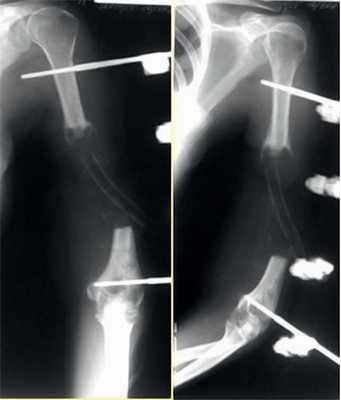
Рис. 6. Рентгенограммы пациентки И. после удаления цементного спейсера.
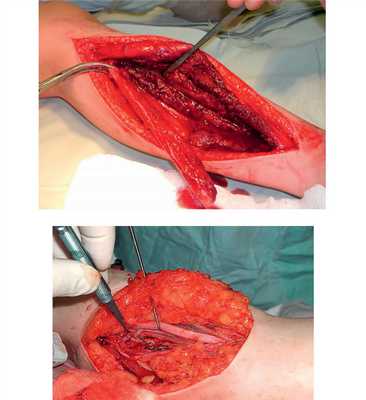
Рис. 7. Оперативное лечение пациентки И.: пластика левой плечевой кости свободным кровоснабжаемым трансплантатом из малоберцовой кости.
Клинический пример 2
Пациентка Н., 41 года.
Диагноз: ложный сустав левой плечевой кости.
На рис. 10-14 Рис. 10. Рентгенограмма пациентки Н. до операции. Рис. 14. Внешний вид и функция пациентки Н. через 8 мес после операции. представлены этапы обследования и лечения пациентки Н.
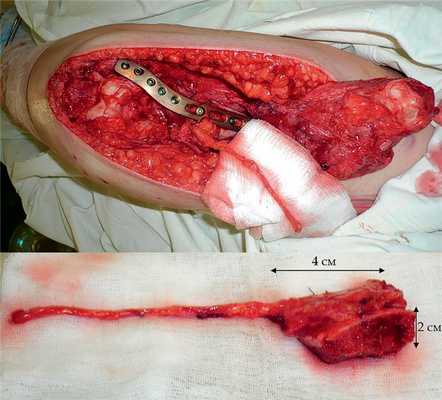
Рис. 11. Пациентка Н. Оперативное лечение: резекция зоны ложного сустава левой плечевой кости, остеосинтез пластиной и винтами. Пластика свободным кровоснабжаемым трансплантатом из внутреннего мыщелка бедренной кости.
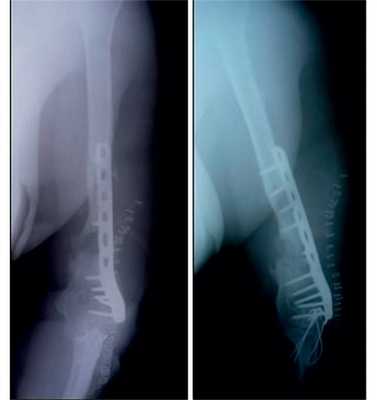
Рис. 12. Рентгенограммы пациентки Н. после операции.
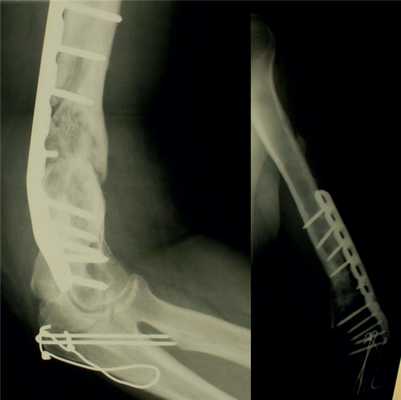
Рис. 13. Рентгенограммы пациентки Н. через 8 мес после операции.
Васкуляризованные костные трансплантаты могут быть использованы при лечении посттравматических ложных суставов, аваскулярных некрозов, некрозов кости после лучевого поражения, остеомиелита, для реконструкции костного дефекта. Выбор вида костного трансплантата остается до настоящего времени неопределенным.
В последнее время трансплантат из мыщелков бедра используется для лечения тяжелых ложных суставов конечностей, не поддающихся другому лечению [15].
В противоположность васкуляризованному трансплантату из малоберцовой кости, трансплантат из медиального мыщелка бедренной кости меньше в размерах, более гибкий и может быть с легкостью встроен в дефект неправильной формы. Эластичность трансплантата допускает его более тугую укладку вокруг трубчатой кости. Это особенно удобно при малом размере дефекта, когда использование аутокости из крыла подвздошной кости или малоберцового трансплантата может быть проблематичным [13].
A. King и соавт. [13] достигли успехов в лечении 5 пациентов с ложными суставами плечевой кости с помощью васкуляризованного кортикопериостального трансплантата из медиального мыщелка бедренной кости. Средний срок достижения костной консолидации составил 7,5 мес, ревизионное вмешательство не потребовалось ни в одном случае. Все пациенты имели отличную функцию локтевого и плечевого суставов. Эти данные совпадают с нашими наблюдениями, однако показания к выбору методики требуют уточнения в дальнейших исследованиях.
Атрофические ложные суставы без значительного костного дефекта могут быть эффективно скорректированы при помощи васкуляризованного кортикопериостального трансплантата из медиального мыщелка бедренной кости [15].
Васкуляризованный трансплантат из малоберцовой кости имеет преимущества в случае больших костных дефектов, при нестабильности и инфицированности ложного сустава, особенно при наличии множественных неудавшихся попыток получить сращение другими способами, при атрофии костной ткани и повреждении окружающих мягких тканей. Использование васкуляризованного трансплантата из малоберцовой кости, как правило, приводит к заживлению перелома с хорошим восстановлением мягких тканей и разрешением хронической инфекции [15].
Заключение. Таким образом, при длительно существующих посттравматических ложных суставах и дефектах плечевой кости, при наличии двух и более оперативных вмешательств с неудовлетворительным результатом в анамнезе кровоснабжаемая костная пластика является эффективным способом лечения.
Каждый ложный сустав плечевой кости имеет уникальный комплекс причин возникновения и требует индивидуализированного подхода.
Техника операции при чрез- и надмыщелковом переломе плечевой кости
Переломы плечевой кости, по данным разных авторов, составляют 7-12% общего числа всех переломов костей [2]. Оперативное лечение данных переломов является приоритетным, так как прерывает патологическую цепь и создает условия для полноценного восстановления анатомических структур сегмента и функций суставов.
Появление фиксаторов нового поколения расширило показания к оперативному лечению, нивелируя определенный хирургический нигилизм при лечении сложных переломов, особенно в случае остеопороза, околосуставных, многооскольчатых и перипротезных переломов [1]. С одной стороны, это позволяет расширить показания к оперативному вмешательству, с другой - возникают новые дополнительные проблемы в тактике лечения больных с переломами длинных трубчатых костей [3].
До настоящего времени количество неудовлетворительных исходов лечения остается высоким (от 7 до 26%). Среди них несросшиеся и неправильно сросшиеся переломы, ложные суставы, в том числе осложненные хроническим остеомиелитом [6].
Проблема лечения больных с осложнениями переломов плечевой кости имеет не только медицинское, но и социальное значение. Большинство пациентов этой группы составляют лица трудоспособного возраста. Основной задачей лечения данного контингента больных является максимально возможное восстановление трудоспособности. Добиться этого можно только при использовании реконструктивно-восстановительных методов оперативного лечения. Такой радикальный подход к лечению данной категории пациентов с применением оптимальной оперативной методики в каждом конкретном наблюдении считаем оправданным.
Целью нашего исследования было определение причин ошибок и осложнений при лечении переломов плечевой кости и изучение результатов оперативного лечения данного контингента больных.
Материал и методы
Анализ материала показал, что основные причины осложнений при лечении переломов плечевой кости можно разделить на 3 группы:
1. Несостоятельность остеосинтеза:
использование неадекватного фиксатора.
2. Недооценка характера и локализации повреждения:
нарушение кровоснабжения костных отломков и мягких тканей;
неправильно избранный способ лечения;
нарушение биомеханики сегмента.
3. Неадекватные лечебно-тактические действия:
несоблюдение оптимальных сроков лечения;
необоснованный отказ от оперативного вмешательства;
ранняя отмена иммобилизации или необоснованный отказ от ее применения.
В основу исследования положен анализ результатов лечения 55 больных с последствиями переломов плечевой кости. Возраст пациентов варьировал от 19 до 77 лет, большинство (38 человек) составили лица трудоспособного возраста (от 22 до 55 лет). Преобладали пациенты женского пола - 37, мужчин было 18.
В зависимости от характера рентгенологических и анатомо-функциональных изменений конечности применяли дифференцированный подход к хирургическому лечению больных с последствиями переломов плечевой кости. Всех больных разделили на
3 группы: 1-я - с несросшимися переломами, 2-я - с неинфицированными ложными суставами; 3-я - с инфицированными ложными суставами. Такое разделение позволяет оценить тяжесть последствий переломов и является основой для планирования лечебного процесса.
У 26 пациентов выявлено несращение или формирование ложного сустава из-за несостоятельности накостного остеосинтеза, у 2 - интрамедуллярного остеосинтеза с блокированием, у 1 пациента - наружного чрескостного остеосинтеза спице-стержневым аппаратом Илизарова.
До поступления 16 больных перенесли две и более операций с применением интрамедуллярного и накостного остеосинтеза. У 21 пациента закрытая репозиция и фиксация перелома гипсовой повязкой оказались несостоятельными.
В 1-ю группу включено 17 пациентов в возрасте от 19 до 62 лет (средний возраст 41,7 года).
Всем пациентам выполнено реконструктивное оперативное вмешательство. У одного пациента с несостоятельностью наружного чрескостного остеосинтеза аппарат внешней фиксации предварительно удален и проведена подготовка кожных покровов.
У остальных пациентов 1-й группы внутренние фиксаторы и фиброзные ткани между фрагментами удаляли во время операции, производили адаптацию костных фрагментов с восстановлением оси сегмента и выполняли накостный остеосинтез (или реостеосинтез).
Основная концепция реконструктивной операции - хорошая биологическая совместимость имплантата и хирургическая техника, обеспечивающая бережное отношение к мягким тканям и костным фрагментам. Для остеосинтеза (или реостеосинтеза) использовали оригинальные накостные пластины: динамические компрессирующие (DCP), динамические компрессирующие ограниченного контакта (LC-DCP) и пластины с угловой стабильностью (LCP).
В одном наблюдении произошел перелом фиксатора с формированием ложного сустава. У всех остальных пациентов достигнута полная консолидация перелома с хорошим функциональным результатом.
Приводим клинические примеры.
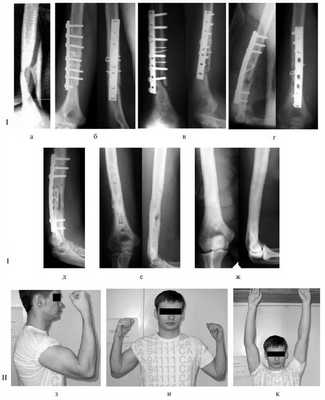
1. Больной Г., 19 лет, поступил через 4 мес после травмы и операции с диагнозом: несрастающийся перелом нижней трети диафиза правой плечевой кости после остеосинтеза пластиной; нестабильность металлофиксатора (рис. 1). Рисунок 1. Рентгенограммы больного Г., 19 лет (I), и функция конечности через 2,5 года после реконструктивной операции (II). I: а - оскольчатый перелом плечевой кости, б - накостный остеосинтез пластиной, в - через 4 мес после травмы (отсутствие консолидации, несостоятельность остеосинтеза), г - после реконструктивной операции, д - через 3 мес после операции, е - удаление имплантата, ж - восстановление структуры плечевой кости в отдаленном периоде; II: з - состояние мягких тканей плеча, и, к - полное восстановление функции конечности.
Ко 2-й группе отнесен 31 пациент в возрасте от 34 до 77 лет (средний возраст 53,6 года).
У 17 пациентов наблюдали гипертрофический ложный сустав плечевой кости. В таких ситуациях оперативное лечение имело целью восстановление механической конструкции (жесткости) сегмента.
В ходе операции вскрывали костномозговые каналы, концы фрагментов освежали и фиксировали в анатомически правильном положении без полного удаления фиброзно-хрящевой ткани.
У 14 пациентов отмечали гипотрофический (или атрофический) ложный сустав. Для оптимизации условий процесса сращения таким пациентам выполняли декортикацию или аутотрансплантацию костной ткани в дополнение к стабильной внутренней фиксации.
У 6 пациентов с атрофическими ложными суставами, ранее неоднократно оперированных, наряду со стабильной внутренней фиксацией для поддержки остеогенеза применяли свободные реваскуляризируемые или ротированные на сосудистой ножке надкостнично-кортикальные аутотрансплантаты.
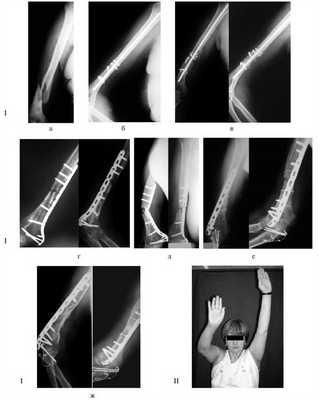
2. Больная В., 47 лет, поступила через 2 года после автотравмы с диагнозом: атрофический ложный сустав правой плечевой кости, перелом фиксатора (рис. 2). Рисунок 2. Рентгенограммы больной В., 47 лет (I), и функция конечности через 2 нед после операции (II). I: а - многооскольчатый перелом правой плечевой кости, б - интрамедуллярный остеосинтез, в - несостоятельность фиксатора через 3 мес, г - реостеосинтез пластиной с угловой стабильностью, д - перелом накостного фиксатора спустя 18 мес, е - реконструкция плечевой кости - накостный остеосинтез метафизарной пластиной с применением ротированного на сосудистой ножке надкостнично-кортикального аутотрансплантата, ж - консолидация ложного сустава через 5 мес; II - функция конечности через 2 нед после операции.
В 3-ю группу вошли 7 пациентов в возрасте от 26 до 70 лет (средний возраст 48 лет).
У 2 пациентов 3-й группы с хроническим остеомиелитом в стадии ремиссии выявлен ложный сустав плечевой кости. Им выполнена реконструктивная операция с применением ротированных надкостнично-кортикальных аутотрансплантатов для поддержки остеогенеза в условиях наружного чрескостного остеосинтеза по Илизарову.
В 5 наблюдениях при инфицированных ложных суставах и несросшихся переломах выполнены удаление металлоконструкций, некрэктомия концов костных фрагментов и наружный чрескостный остеосинтез по Илизарову. 3 пациентам операция дополнена пластикой костной раны фрагментами трехглавой (2) и плечелучевой (1) мышц.
Результаты
Ближайшие результаты лечения изучены у всех больных. Наблюдавшиеся осложнения разделены нами на две группы - ранние и поздние. Из ранних осложнений поверхностное нагноение раны выявлено в 2 наблюдениях, воспаление мягких тканей вокруг спиц аппарата наружной фиксации - в 2 наблюдениях.
Поздние осложнения, потребовавшие повторных операций, распределились следующим образом. Отсутствие консолидации выявлено у 4 больных. Повторное вмешательство у 2 пациентов выполнено с применением ротированных на сосудистой ножке надкостнично-кортикальных аутотрансплантатов.
Позднее нагноение (через 2,5 мес после операции), потребовавшее преждевременного удаления накостного фиксатора, наблюдали у одного пациента. Полной консолидации удалось достичь с использованием ортеза.
Раннее снятие аппарата Илизарова из-за нагноения мягких тканей вокруг спиц имело место у одного больного. В последующем сращение достигнуто после повторного наружного остеосинтеза по заживлении ран.
Отдаленные результаты лечения (в сроки от 1 года до 6 лет) прослежены у 38 больных. Оценка результатов проводилась с использованием системы Н.А. Любошица и Э.Р. Маттиса [4], а также И.Л. Шварцберга [5]. Хорошим результат лечения признан в 27 наблюдениях, удовлетворительным - в 7, неудовлетворительным - в 4. Неудовлетворительным результатом считали отсутствие консолидации костных отломков, что требовало повторного оперативного вмешательства.
Лечение последствий переломов длинных трубчатых костей требует индивидуального подхода в каждом наблюдении и должно быть направлено на создание условий для регенерации костной ткани на основе законов биомеханики, физиологии и патофизиологии.
Распределение больных на группы для оценки тяжести последствий способствовало правильному выбору лечебно-тактических действий.
При замедленной консолидации (несростающихся переломах) перелома плечевой кости (1-я группа) своевременно и технически грамотно выполненный остеосинтез (или реостеосинтез) позволяет сохранить условия репаративной регенерации и восстановить функцию конечности в целом.
Гипертрофические ложные суставы (2-я группа) плеча обладали достаточным объемом костной и мягких тканей. Наша задача заключалась в грамотном использовании этого ресурса.
Использование современных методик и фиксаторов позволило добиться положительных результатов.
С увеличением количества предшествующих обращению внутренних фиксаций наблюдали увеличение частоты возникновения гипотрофических (аваскулярных) ложных суставов (2-я группа). Принято считать, что причиной формирования атрофических и гипотрофических ложных суставов у таких пациентов является нарушение кровоснабжения концов фрагментов в результате тяжелых повреждений и хирургических вмешательств.
У этих пациентов наряду со стабильной внутренней фиксацией считаем оптимальным применение свободных реваскуляризируемых или ротированных на сосудистой ножке надкостнично-кортикальных аутотрансплантатов для поддержки остеогенеза.
Цели и хирургическая тактика у пациентов c инфицированными ложными суставами (3-я группа) зависели от активности остеомиелитического процесса, сопутствующих анатомических изменений.
Свободные реваскуляризируемые или ротированные на сосудистой ножке надкостнично-кортикальные аутотрансплантаты применяли для поддержки остеогенеза у пациентов с ложными суставами и хроническим остеомиелитом в стадии ремиссии в условиях выраженного фиброза тканей, патологических изменений тканей сегмента конечности, нарушения кровоснабжения концов костных фрагментов.
В стадии обострения или при вялотекущей хронической гнойной инфекции в области ложного сустава выполняли удаление металлофиксаторов, традиционную санацию гнойного очага и остеосинтез аппаратом внешней фиксации. Дополнительное применение ротированных мышечных лоскутов позволило осуществить тампонаду остеомиелитической полости или укрыть костные фрагменты хорошо снабжаемыми кровью, устойчивыми к инфекции тканями, способными создать благоприятные условия для остеорепарации.
Таким образом, разделение больных на группы не только позволяет оценить тяжесть последствий переломов плечевой кости, но и отражает необходимость дифференцированного подхода к лечению данного контингента больных.
При замедленной консолидации и гипертрофических ложных суставах плечевой кости правильный выбор метода остеосинтеза ( или реостеосинтеза) и технически грамотное выполнение оперативного вмешательства дают возможность сохранить условия репаративной регенерации и восстановить функцию конечности в целом.
Применение свободных реваскуляризируемых и ротированных на сосудистой ножке надкостнично-кортикальных аутотрансплантатов наряду со стабильной внутренней фиксацией при гипотрофических (аваскулярных) ложных суставах является высокоэффективным методом лечения.
У пациентов с инфицированными ложными суставами плечевой кости создание благоприятных условий для остеорепарации возможно с применением хорошо снабжаемых кровью, устойчивых к инфекции тканей.
Переломы мыщелков плечевой кости в структуре ежегодной заболеваемости составляют, по разным оценкам, от 5,7 до 34 на 100 000 населения в год [5, 7]. Распределение имеет бимодальный характер с первым пиком заболеваемости у молодых мужчин в возрасте до 19 лет, как правило, в результате высокоэнергетических травм и вторым пиком у женщин пожилого возраста с сопутствующим остеопорозом и нарушениями процесса ремоделирования костной ткани [6].
Цель настоящего исследования - улучшить результаты хирургического лечения внутрисуставных оскольчатых переломов мыщелков плечевой кости с помощью чрескостного остеосинтеза аппаратом внешней фиксации.
С 1998 по 2013 г. в клиниках травматологии и ортопедии Управления делами Президента РФ оперированы 55 пациентов с внутрисуставными оскольчатыми переломами мыщелков плечевой кости, которым был выполнен чрескостный остеосинтез аппаратом внешней фиксации конструкции А.И. Городниченко.
Хирургическое лечение переломов мыщелков плечевой кости осуществляли методом чрескостного остеосинтеза с применением спице-стержневого аппарата, основными преимуществами которого являлись стабильность достигаемого остеосинтеза на весь период лечения, элементы аппарата, изготовленные из высокопрочного рентгенопрозрачного углепластика, что позволяло контролировать точность закрытой репозиции во всех проекциях, одностороннее расположение, компактные размеры и незначительная масса всей конструкции, а также «плавающие» держатели стержней, не препятствующие устранению всех видов смещения костных отломков [2]. Наш опыт наглядно показал простоту и безопасность остеосинтеза данным аппаратом, минимальную травматичность операции и высокую стабильность фиксации костных отломков даже у больных с остеопорозом.
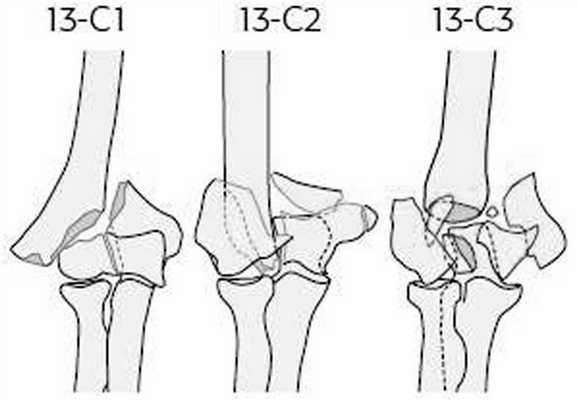
Показаниями к чрескостному остеосинтезу аппаратом внешней фиксации являлись открытые и закрытые оскольчатые внутрисуставные переломы мыщелков плечевой кости типов 13-С1,2,3 по классификации АО [4] (рис. 1). Рисунок 1. Классификация АО внутрисуставных оскольчатых переломов мыщелков плечевой кости (тип 13-С1,2,3). Среди повреждений преобладали открытые и закрытые переломы типов 13-C1,2 по классификации AO. В случае открытых повреждений подобного типа больные были оперированы в течение первых 6 ч с момента поступления. Переломы 13-С1 встречались в 26 (47,2%) наших наблюдениях, переломы 13-С2 - в 20 (36,4%) и переломы 13-С3 - в 9 (16,4%) наблюдениях.
Все оперативные вмешательства проводили на ортопедическом столе под контролем электронно-оптического преобразователя. Методом анестезии являлась либо проводниковая анестезия - блок плечевого сплетения, либо внутривенный наркоз. Репозицию перелома, как правило, проводили закрыто, и только при многооскольчатых внутрисуставных переломах типа 13-С3 выполняли открытую репозицию с целью наиболее точного восстановления конгруэнтности суставных поверхностей. Количество вводимых стержней зависело от характера перелома и наличия сопутствующего остеопороза. В область дистального метаэпифиза плечевой кости вводили 1 или 2 стержня и 1 или 2 спицы с упорными площадками, которые крепили с наружной стороны в аппарате внешней фиксации. В диафиз плечевой кости вводили 1 или 2 кортикальных стержня. Все стержни вводили через разрезы кожи длиной до 5 мм, что позволяло сократить интраоперационную кровопотерю до 10-30 мл, а продолжительность операции до 30-45 мин. Окончательной репозиции достигали на операционном столе с помощью средств ручной репозиции, чему в значительной мере способствовало то обстоятельство, что основные элементы аппарата были выполнены из рентгенопрозрачного углепластика.
Результаты и обсуждение
Консолидация перелома наступила во всех наблюдениях. Вторичного смещения отломков в аппарате нами не отмечено. Средний срок фиксации составил 78 дней (от 65 до 98 дней). Ближайшие результаты оценивали через 2,5-3 мес после операции при демонтаже аппарата, отдаленные - через 10-12 мес после остеосинтеза на основании клинико-рентгенологических данных.
Отличным считали результат, при котором наступала консолидация перелома, объем движений восстанавливался более чем на 80% исходного (110° и более), субъективная оценка больным функции очень хорошая, пациент вернулся к предыдущей работе.
Результат расценивали как хороший, если наступала консолидация перелома, объем движений восстанавливался более чем на 65% исходного (от 90° до 109°), субъективная оценка больным функции хорошая, пациент вернулся к некоторым видам работы.
Удовлетворительным считали результат, при котором наступала консолидация перелома, объем движений восстанавливался более чем на 50% исходного (от 70° до 89°), субъективная оценка больным функции удовлетворительная, пациент полностью пригоден к облегченному труду.
Как неудовлетворительный оценивали результат при восстановлении объема движений менее чем на 50% исходного (менее 70°), субъективной оценке больным функции как неудовлетворительной, пациент нетрудоспособен.
Демонтаж аппаратов производили в амбулаторных условиях либо пациентов госпитализировали в стационар на один день. Через 1 год после остеосинтеза из 51 (92,7%) обследованного у 9 (17,6%) отмечены отличные результаты, у 24 (47,1%) - хорошие и у 18 (35,3%) - удовлетворительные. Неудовлетворительных результатов не было. Из осложнений у 4 (7,3%) пациентов отмечалось воспаление мягких тканей вокруг стержней, которое было купировано в стационаре и не потребовало демонтажа аппарата.
С целью иллюстрации полученных результатов приводим клинический пример.
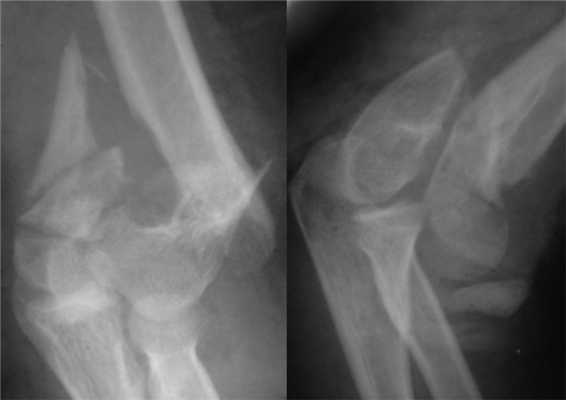
Больная П., 25 лет, поступила в стационар с жалобами на боли в левом локтевом суставе через 2 ч после травмы в результате падения на улице. При осмотре отмечены отек левого локтевого сустава, болезненность при пальпации, невозможность движений в суставе из-за боли. После клинико-рентгенологического обследования установлен диагноз: закрытый внутрисуставной оскольчатый чрезмежмыщелковый перелом левой плечевой кости со смещением отломков тип 13-С2 (рис. 2). Рисунок 2. Рентгенограммы больной П. с внутрисуставным оскольчатым чрезмежмыщелковым переломом левой плечевой кости со смещением отломков тип 13-С2.
Сосудистых и неврологических расстройств в дистальных отделах левой верхней конечности выявлено не было. При поступлении произведена анестезия места перелома, внешняя иммобилизация гипсовой лонгетной повязкой.
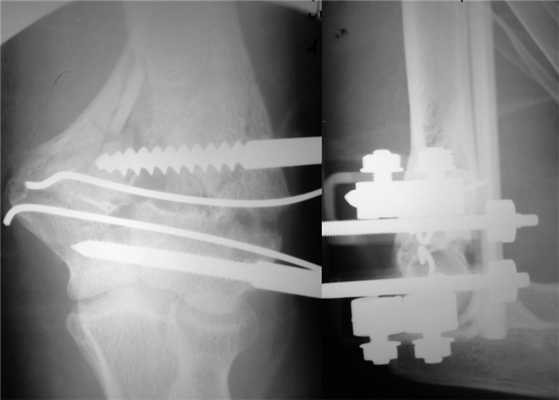
На следующий день под новокаиновым блоком плечевого сплетения произведена операция: закрытая репозиция и чрескостный остеосинтез левой плечевой кости спице-стержневым аппаратом внешней фиксации конструкции А.И. Городниченко. Через разрезы кожи и мягких тканей по наружной поверхности левого плеча длиной до 5 мм введено 2 кортикальных стержня в диафиз плечевой кости, один кортикальный и один спонгиозный стержень и 2 спицы с упорной площадкой в мыщелки и надмыщелки плечевой кости. После фиксации проксимальных стержней в аппарате под контролем электронно-оптического преобразователя произведена закрытая репозиция с помощью съемных рукояток с последующей стабилизацией дистальных стержней и спиц (рис. 3). Рисунок 3. Рентгенограммы больной П. после остеосинтеза левой плечевой кости спице-стержневым аппаратом. Кожа вокруг стержней ушита одиночными швами. Кровопотеря в ходе операции 20 мл. Продолжительность операции 40 мин.

Послеоперационное течение без осложнений, проводили регулярные перевязки с обработкой кожи вокруг стержней и спиц растворами антисептиков и сменой асептических повязок. Швы вокруг стержней сняты через 8 дней после операции, пациентка выписана на амбулаторное лечение с рекомендациями по дальнейшему восстановительному лечению. Движения в левом локтевом суставе перед выпиской из стационара показаны на рис. 4. Рисунок 4. Рентгенограммы больной П. после остеосинтеза левой плечевой кости спице-стержневым аппаратом.
После консолидации перелома через 71 день произведен демонтаж аппарата (рис. 5). Рисунок 5. Рентгенограммы больной П. после остеосинтеза левой плечевой кости спице-стержневым аппаратом. Движения в левом локтевом суставе после демонтажа аппарата от 0 до 128° (рис. 6). Рисунок 6. Внешний вид больной П. после демонтажа аппарата (объем движений в левом локтевом суставе от 0 до 128°).
Таким образом, полученные нами результаты лечения оскольчатых внутрисуставных переломов мыщелков плечевой кости (тип С по классификации АО) с применением чрескостного остеосинтеза аппаратом внешней фиксации конструкции А.И. Городниченко свидетельствуют о его высокой эффективности по созданию стабильного остеосинтеза, позволяющего сохранить функцию поврежденного сустава на протяжении всего периода лечения, что при регулярных занятиях лечебной физкультурой обеспечивает восстановление объема движений в поврежденном суставе и создает условия для восстановления трудоспособности пациентов. Применение малотравматичного чрескостного остеосинтеза дает возможность избежать значительной кровопотери в ходе оперативного вмешательства, а конструктивные особенности аппарата - сократить продолжительность операции.
Многократность использования в сочетании с меньшей стоимостью фиксатора по сравнению с пластинами с угловой стабильностью гарантируют достижение значительного экономического эффекта. Одностороннее расположение и компактные размеры создают условия для улучшения качества жизни пациентов в послеоперационном периоде. Применение аппарата внешней фиксации конструкции А.И. Городниченко позволяет улучшить функциональные результаты хирургического лечения оскольчатых внутрисуставных переломов мыщелков плечевой кости и избежать неудовлетворительных результатов. Применение аппарата обеспечивает сокращение сроков стационарного лечения, реабилитации и временной нетрудоспособности пациентов. Предложенный метод лечения переломов дистального отдела плечевой кости можно рекомендовать для широкого практического применения.
Чрезмыщелковый перелом плеча со смещением
Чрезмыщелковый перелом плеча - нарушение целостности костной ткани мыщелка плечевой кости в результате травмы или патологического процесса.
Цель этапа:
- своевременная диагностика чрезмыщелкового перелома плеча;
- определение терапевтической тактики (консервативная, оперативная);
- профилактика возможных осложнений;
- проведение реабилитационных мероприятий;
- восстановление функции конечности.
Период протекания
Длительность лечения (дней): 9

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
1. Открытый (инфицированный перелом).
2. Закрытый перелом.
Классификация АО:
- А - внесуставной перелом;
- В - неполный внутрисуставной перелом;
- С - полный внутрисуставной перелом;
Каждый пункт имеет разделение по характеру перелома (например: А1 - перелом латерального надмыщелка, или С3 - полный внутрисуставной оскольчатый метафизарный сложный перелом плечевой кости).
Факторы и группы риска
Диагностика
Критерии диагностики:
1. Болевой синдром в травмированной конечности.
2. Ограничение или отсутствие движений в локтевом суставе.
3. Изменения мягких тканей над участком перелома (отек, гематома, деформация и др.).
4. Крепитация костных отломков при пальпации предполагаемого травмированного участка плеча.
5. Рентгенологические признаки перелома диафиза плеча со смещением.
Лечение
Любой метод лечения проводится с применением адекватного обезболивания. Анальгетические и нестероидные противовоспалительные препараты используются в течение 2 недель.
Консервативное лечение:
1. Переломы без смещения подлежат консервативному лечению с наложением гипсовой лонгеты сроком на 3-6 недель.
2. Рентгенографический контроль после репозиции и через неделю после репозиции.
Перед проведением оперативного лечения при открытых переломах обязательно введение противостолбнячного анатоксина.
Оперативное лечение: показано при чрезмыщелковых переломах со смещением (металлоостеосинтез плечевой кости с помощью Y-образной пластины, спицами Киршнера, болтом-стяжкой и др.).
Основной целью является стабилизация перелома и обеспечение движений в локтевом суставе уже на начальных стадиях. Раннее возобновление движений следует предусматривать у пожилых пациентов, несмотря на наличие тяжелых оскольчатых переломов остеопоротической кости. Иногда в таких случаях показано первичное эндопротезирование сустава. Контроль консолидации перелома проводится рентгенологическим методом через 21 день после репозиции, затем ежемесячно.
Результаты многоцентровых исследований установили, что при использовании антибиотикопрофилактики у пациентов с открытыми переломами значительно уменьшается риск развития гнойно-воспалительных осложнений.
Пациентов можно разделить на 3 группы риска:
1. Открытый перелом с повреждением кожи и мягких тканей длиной менее 1 см, рана чистая.
2. Открытый перелом с повреждением кожи длиной более 1 см при отсутствии выраженных повреждений подлежащих тканей или значительных смещений.
3. Любые сегментарные переломы, открытые переломы с выраженным повреждением подлежащих тканей или травматической ампутацией.
Пациентам 1-2 групп риска необходимо введение предоперационной дозы антибиотиков (как можно раньше после травмы), в основном с действием на грамположительные микроорганизмы.
Для пациентов группы риска 3 дополнительно назначают антибиотики, действующие на грамотрицательные микроорганизмы.
Схемы антибиотикопрофилактики:
1. Пациентам 1-2 групп риска - цефалоспорины 3-4 поколения в\м 1,0-2,0.
2. Пациентам 3 группы риска - цефалоспорины 3-4 поколения в\м 1,0-2,0 через 12 часов (2 раза в сутки) 7 дней + метронидазол 100 мл в/в через 8 часов (3 раза в сутки) 3-5 дней.
Перечень основных медикаментов:
1. *Метронидазол таблетка 250 мг, раствор для инфузий 0,5 во флаконе 100 мл
2. *Цефтриаксон порошок для приготовления инъекционного раствора 250 мг, 500 мг, 1000 мг во флаконе
3. *Цефазолин порошок для приготовления инъекционного раствора 1000 мг
Перелом плечевой кости
- доставить пострадавшего в стационар травматологического профиля при наличии или отсутствии осложнений.
4. Повреждение магистральных сосудов с формированием напряженной гематомы или наружным кровотечением.
Переломы хирургической шейки - аддукционные и абдукционные (встречаются очень часто, особенно в пожилом возрасте)
Аддукционный перелом является результатом падения на согнутую и приведенную в локтевом суставе руку. Центральный отломок смещается кпереди и кнаружи. Периферический отломок отклоняется кнаружи и смещается кверху. Между отломками образуется угол, открытый кнутри.
Абдукционный перелом возникает при падении на отведенную руку. Центральный отломок отклоняется кпереди и книзу. Периферический отломок располагается от центрального, образуя угол, открытый кнаружи.
Косвенный механизм: падение на кисть или локтевой сустав отведенной рукой; чрезмерное ротационное вращение по оси плеча.
Тип 1. Линия излома проходит выше места прикрепления большой грудной мышцы. Центральный отломок занимает положение отведения кнаружи и кпереди с ротацией кнаружи. Периферический отломок приведен кнутри сокращением большой грудной мышцы, подтянут кверху и ротирован кнутри.
Тип 2. Линия излома проходит ниже прикрепления большой грудной мышцы, но выше прикрепления дельтовидной. Центральный отломок сокращением большой грудной мышцы приведен и умеренно ротирован кнутри. Периферический отломок умеренно отведен кнаружи и подтянут кверху за счет сокращения дельтовидной мышцы.
Тип 3. Линия излома проходит ниже прикрепления дельтовидной мышцы, которая отводит центральный отломок кнаружи и кпереди. Периферический отломок подтянут кверху вследствие сокращения мышечного футляра плеча.
Читайте также:
