Техника рассечения кожи, подкожной клетчатки и поверхностной фасции. Разрезание кожи, подкожной жировой клетчатки и фасции.
Добавил пользователь Alex Обновлено: 21.01.2026
И.Е. МИКУСЕВ, Г.И. МИКУСЕВ, Р.Ф. ХАБИБУЛЛИН
Казанская государственная медицинская академия
Республиканская клиническая больница МЗ РТ, г. Казань
Микусев Глеб Иванович
кандидат медицинских наук, врач-травматолог
Статья посвящена одному из тяжелых и относительно редких повреждений, встречающихся в практике хирургов и травматологов — травматической отслойке кожи. Описание этого вида патологии в хирургических руководствах и учебниках не отличается особой полнотой. Поверхностное знакомство хирургов и травматологов с травматической отслойкой кожи иногда способствует просмотру этого повреждения. Даны четкие рекомендации по диагностике и лечению травматической отслойки кожи.
Ключевые слова: травматическая отслойка кожи, диагностика, лечение.
I.E. MIKUSEV, G.I. MIKUSEV, R.PH. KHABIBULLIN
Kazan State Medical Academy
Republican Clinical Hospital of the Ministry of Health of the Republic of Tatarstan, Kazan
Traumatic skin detachment: diagnostic and treatment
The article considers one of the severe and relatively rare damages which occur in the practice of surgeons and traumatologists — traumatic skin detachment. The description of this type of pathology in textbooks and work manuals is not full. Sketchy knowledge of surgeons and traumatologists of traumatic skin detachment sometimes leads to omitting such an injury. Clear guidelines for the diagnosis and treatment of traumatic skin detachment are given.
Key words: traumatic skin detachment, diagnostic, treatment.
Травматическая отслойка кожи возникает вследствие грубого механического воздействия различных движущихся предметов, большей частью вращающимся колесом. Из 53 случаев в наших наблюдениях у 18 больных травматическая отслойка кожи возникла при наезде колеса автобуса, троллейбуса, грузовой и легковой автомашины. Падение с лестницы или крыши, удар тяжелым предметом, касательное соскальзывание тяжелого предмета или прижатия им, сдавливание движущимся вагоном, автомобилем, протаскивание тела по земле трамваем и т.д. — все эти факторы могут привести к травматической отслойке кожи.
По нашим наблюдениям, отслоение кожи не всегда проходит одинаково, на что также указывал и В.К. Красовитов (1947) [4]. Практически можно выделить три основных типа травматической отслойки кожи.
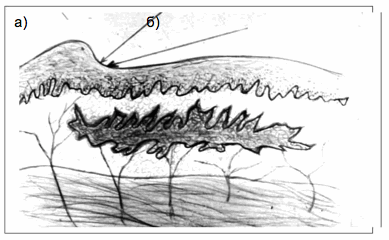
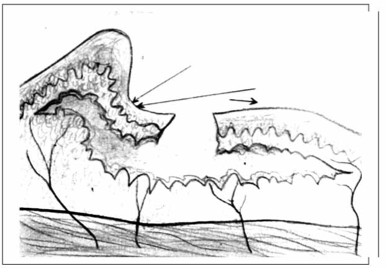
Первый тип: превалирует размозжение подкожной жировой клетчатки в зоне отслойки с разделением ее на участки, связанные с кожей, а оставшаяся часть — с фасцией (рис. 1 — закрытая травматическая отслойка кожи по 1-му типу и рядом открытая травматическая отслойка кожи по 1-му типу). При этом происходит полное нарушение кровоснабжения кожи из-за повреждения питающих сосудов.
Травматическая отслойка кожи по I типу: а — закрытая травматическая отслойка кожи по I типу; б — открытая травматическая отслойка кожи по I типу
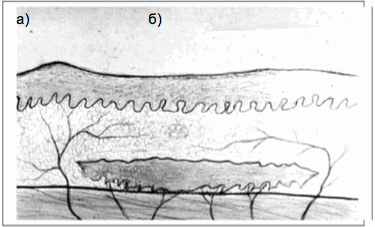
Второй тип: на первое место выдвигается подкожный разрыв жировой клетчатки, не сопровождающийся грубым нарушением ее и глубжележащих тканей, при этом большая часть подкожно-жировой клетчатки отходит вместе с кожей, образуя довольно толстый пласт, содержащий достаточное количество питающих сосудов (рис. 2 — закрытая травматическая отслойка кожи по 2-му типу и рядом открытая травматическая отслойка кожи по 2-му типу).
Рисунок 2.
Травматическая отслойка кожи по II типу: а — закрытая травматическая отслойка кожи по II типу; б — открытая травматическая отслойка кожи по II типу
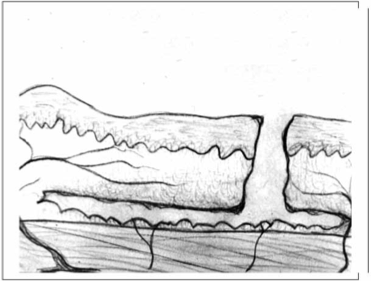
Третий (смешанный, комбинированный) тип: участки размозжения подкожно-жировой клетчатки чередуются с участками, где сохранилась большая часть этой клетчатки вместе с кожей в виде пласта (рис. 3 — смешанная, комбинированная закрытая отслойка кожи).
Смешанная, комбинированная закрытая отслойка кожи
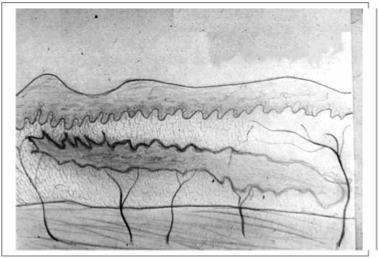
По-видимому, тип отслойки кожи зависит от механизма травмы, в основном от быстроты перемещения повреждающего предмета по отношению к области тела, от физических свойств тканей на поврежденном участке и от возраста пострадавшего.
Клинически, как по нашим наблюдениям, так и по данным других авторов [5, 6], могут быть выделены закрытые и открытые травматические отслойки кожи. Среди наблюдаемых больных закрытая отслойка кожи встретилась у 13 больных.
Все отслойки кожи еще со времен Morel-Lavallee принято разделять на три группы: малые, средние и большие, но, к сожалению, без уточнения размеров участка повреждения.
При травматической отслойке кожи всегда образуется щелевидное пространство («карман»), чаще всего между кожей и первой фасцией. В момент травмы одновременно с разрушением жировой ткани разрываются кровеносные и лимфатические сосуды, и «карман» начинает заполняться изливающейся кровью и лимфой, появляется ощущение зыбления (ундуляция).
Для установления правильного диагноза травматической отслойки кожи очень важным является уточнение механизма травмы, т.к. механизм возникновения отслойки — это грубое механическое воздействие различных движущихся предметов и при этом приложение силы под некоторым углом.
При повреждениях, где имеется сильный ущерб мягких тканей, особенно при повреждениях колесом движущегося транспорта и т.п., надо всегда помнить об отслоениях кожи. Тем не менее, по нашим наблюдениям, диагностические ошибки при этом виде повреждения, особенно в случае закрытой отслойки кожи, допускаются. Мы полагаем, это связано с тем, что практические врачи хирургического профиля с травматической отслойкой кожи мало знакомы. При поступлении подобных больных, особенно при закрытых травматических отслойках кожи, как правило, выставляется диагноз ушиб мягких тканей и подкожная гематома травмированной области, которая достоверно подтверждается пункциями с удалением кровянистого содержимого. При сочетании повреждения конечностей на разных уровнях (особенно при дорожно-транспортных травмах) основное внимание в первую очередь уделяется открытым повреждениям, не предполагая о возможном тяжелом закрытом повреждении, таком как травматическая отслойка кожи.
Вышеизложенное наглядно показывает следующее клиническое наблюдение.
Больная И., 16 лет, для дальнейшего лечения поступила в КазНИИТО 06.02.1985 г., через 4 месяца после травмы — переднее колесо автобуса проехало через правую голень, а затем наехало (но не переехало!) и на левое бедро. После травмы больная доставлена в травматологическое отделение БСМП г. Набережные Челны, где был установлен диагноз: открытый перелом костей правой голени с обширным повреждением мягких тканей, разрыв наружно-боковой связки левого коленного сустава с гемартрозом. Травматический шок II ст. При обследовании больной на левом бедре четко были видны следы от протектора колеса с участками кровоподтеков без повреждения кожного покрова.
При поступлении больной на фоне противошоковых мероприятий выполнена первичная хирургическая обработка открытого повреждения костей правой голени с восстановлением кожного покрова. Только через сутки после госпитализации выявлена травматическая отслойка кожи левого бедра от верхней трети его до уровня коленного сустава (по-видимому, по первому типу). В дальнейшем наступил полный некроз кожи циркулярно на левом бедре на участках травматической отслойки кожи, что осложняло лечение пострадавшей в связи с тяжелым повреждением и правой голени. К сожалению, подобные диагностические ошибки в наших наблюдениях встретились в 6 случаях, что связано с недостаточным вниманием при обследовании и выяснением механизма травмы у пострадавших.
Лечение больных с травматической отслойкой кожи представляет определенные трудности, и шаблонного подхода при этом не должно быть. Как показали наши наблюдения, способы лечения прежде всего зависят от типа и площади отслойки.
Отслойки кожи малой и средней величины могут лечиться пункциями с последующим наложением давящей повязки. Если же после пункции опорожнения образовавшегося «кармана» кожи не наступает, а клинически в нем определяется содержимое, то показано рассечение кожи на 2-3 см для удаления сгустков крови и поврежденной подкожной жировой клетчатки. Наложение продолжительной давящей повязки после введения в ранку резинового выпускника также обязательно. А.Г. Гугуцидзе [7] для лечения травматической отслойки кожи малой и средней величины с успехом применял активный дренаж.
При обширных закрытых отслойках кожи возможны два способа лечения, в зависимости от типа отслоения. Как показали наши наблюдения, при первом типе закрытой травматической отслойки, когда превалирует размозжение подкожно-жировой клетчатки в зоне повреждения, необходима обработка кожи по В.К. Красовитову, когда с кожного лоскута и фасции полностью удаляется подкожно-жировая клетчатка. При втором типе отслойки обработка кожи по типу свободного полнослойного трансплантата является излишней, так как в толще кожно-подкожного лоскута содержится достаточное количество питающих сосудов. В случае смешанной (комбинированной) отслойки показана частичная обработка кожных лоскутов по Красовитову.
Однако до операции практически невозможно установить в каждом отдельном случае закрытой травматической отслойки кожи тип повреждения. Поэтому мы предлагаем очень простую методику уточнения типа отслоения до начала основного оперативного вмешательства.
При установленном диагнозе отслойки кожи или даже при подозрении на отслойку с учетом механизма травмы на нижних конечностях, а также на других участках тела после соответствующей обработки кожи больного и рук хирурга (в перчатках), проделывали «диагностические» насечки длиной до 3 см по наружной и внутренней поверхностям голени и бедра. Из этих разрезов проводится пальцевое обследование кожно-подкожных лоскутов кпереди и кзади и делаются дополнительные насечки над концом пальца. При отслойке по второму типу выявляется довольно равномерный на всех участках толстый пласт подкожно-жировой клетчатки, тогда как при первом типе участки пласта равномерной толщины почти не встречаются. А при смешанном (комбинированном) варианте отслойки кожи, наоборот, выявляются участки толстых равномерных пластов и участки кожи с незначительным слоем жировой ткани (или вообще без нее). Из этих же насечек легко установить наличие повреждения фасции и мышц, а также при показаниях произвести фасциотомию.
Очень важным диагностическим признаком при этой манипуляции является наличие в «кармане» размозженной подкожно-жировой клетчатки. При первом типе вместе с кровью и лимфой отходит значительное количество жировой ткани, тогда как при втором типе в жидком содержимом выделяются в основном капельки жира с единичными кусочками жировой ткани. При первом типе травматической отслойки насечки по наружной и внутренней поверхностям голени, а также бедра соединяются между собой по типу лампасного разреза и проводится обработка двух лоскутов (переднего и заднего) по Красовитову. Ранее проведенные насечки на этих лоскутах оставляются для оттока лимфы, крови и наносятся дополнительные насечки для лучшего приживления полнослойного кожного трансплантата.
Больная К., 15 лет, доставлена в КазНИИТО 30/Х1 1982 г. Диагноз: закрытый перелом костей правой голени и правой стопы. Больная попала под машину, и по правой ноге проехало колесо грузовой машины «МАЗ». У больной клинически выявлена циркулярная закрытая травматическая отслойка кожи с подкожной клетчаткой от средней трети правого бедра до области лодыжек с переходом на тыльную поверхность правой стопы. На рентгенограммах повреждений костей не выявлено. Обследование отслоенных участков кожи через диагностические насечки на голени и бедре показало, что имеется первый тип отслойки с размозжением подкожно-жировой клетчатки. Последняя в большом количестве отходила через насечки вместе с кровью и лимфой. Насечки соединены между собой по типу лампасных разрезов, начиная от лодыжек до средней трети бедра. Передний и задний лоскуты обработаны по Красовитову (под наркозом при переливании крови и полиглюкина). Операция продолжалась 5 часов.
Если при проведении «диагностических» насечек выявляется второй тип отслойки, то операция на этом завершается.
Больной Т., 33 года, доставлен 8/Ш 1983 г. с диагнозом закрытого перелома костей правой голени; находился в состоянии алкогольного опьянения. Со слов жены, правая нижняя конечность пострадавшего попала под колесо троллейбуса. Рентгенологически выявлен перелом дистального метафиза правой малоберцовой кости без смещения. Под наркозом проведена ревизия отслоенного лоскута через диагностические насечки на голени и бедре. Выделилось около 700-800 мл кровянистого отделяемого с капельками жира (но без жировой ткани!). Выявлен второй тип закрытой отслойки кожи с подкожной клетчаткой, а начиная от уровня головки малоберцовой кости до средней трети правой голени, через насечки установлено повреждение фасции этой зоны с частичным повреждением малоберцовых мышц. Поэтому насечки на этом участке соединены между собой по типу лампасного разреза и мышцы подшиты на свое место кетгутом. Швы на рану. В насечки введены резиновые выпускники, наложены циркулярная повязка стерильным бинтом, смоченным раствором риванола. Фиксация задней гипсовой лонгетой.
В случаях обширной открытой отслойки, когда имеется лишь одна питающая ножка, должна проводиться обработка кожи по Красовитову. Однако здесь допустимо частичное использование отслоенного кожно-подкожного лоскута при относительной целости клетчатки, начиная от питающей ножки, для местной пластики по типу реплантации при равной длине и ширине ножки (1:1), а вся остальная отслоенная ткань должна обрабатываться по типу полнослойного кожного трансплантата.
Лишь в случае отслойки кожно-подкожных лоскутов в размерах 1:1 или 1:1,5 возможно пришивание их без обработки по Красовитову. Однако и здесь хирургу необходимо убедиться в целости питающей ножки, т.е. в толщине ножки лоскута.
Отслоенные цилиндрические трубки кожи с подкожной клетчаткой с проксимальной питающей ножкой снабжаются кровью гораздо лучше, чем лоскут с дистальной ножкой. Поэтому, убедившись в жизнеспособности такого цилиндрического лоскута, последний после нанесения насечек может быть подшит на прежнее место. Естественно, и в этих случаях жизнеспособность лоскута будет зависеть от типа травматической отслойки.
Как показали наши клинические наблюдения, независимо от того, как была обработана отслоенная кожа: вручную скальпелем, или ножницами по типу полнослойного перфорированного лоскута, или по типу толстого расщепленного кожного лоскута дерматомом, или даже совсем не было обработки кожи при втором типе отслойки — наиболее поврежденные участки кожи (осаднение, ушиб, имбибиция на всю толщину кровью) в послеоперационном периоде некротизируются.
Возникает вопрос о целесообразности иссечения явно нежизнеспособных участков травмированной отслоенной кожи. К сожалению, не всегда имея под рукой готовый стерильный дерматом, щадя пострадавшего и боясь причинить ему дополнительную травму при взятии расщепленных кожных лоскутов, большинство хирургов стараются на время (как биологическую повязку) реплантировать явно нежизнеспособные кожные лоскуты (после обработки по Красовитову укладывают их на свое прежнее место). По нашему твердому убеждению, эту тактику следует признать неправильной, что подтверждается и другими авторами [8].
В заключение следует указать, что обширное повреждение кожного покрова конечности должно считаться столь же серьезной травмой для конечности, как, например, повреждение магистральных сосудов и нервных стволов. Правильная тактика хирурга с проведением первичной кожной пластики по показаниям является единственной мерой, которая, возможно, в некоторых случаях спасает не только конечность, но и жизнь пострадавшего. Лечение больных с указанными повреждениями должно начинаться с обязательного переливания крови, кровезаменителей, назначения комплекса витаминов, метилурацила и т. д.
Успех оперативного вмешательства при обширных повреждениях кожного покрова зависит от радикальности хирургической обработки раны, правильного выбора метода кожной пластики с безукоризненным его осуществлением и от надлежащего послеоперационного ухода.
1. Кодзаев К.К. Травматическая отслойка кожи // Вестн. хир. — 1936. — Т. 42, кн. 117-118. — С. 11-18.
2. Алексеев В.В. 2 случая decollement de la peau // Вестн. хир. — 1930. — Т. 21, кн. 62-63. — С. 212-213.
3. Paul D. Zur Versorgung von Skalpierungsverletzungen // Beitr. Orthop. Traumatol. — 1975. — Vol. 3. — S. 190-192.
4. Красовитов В.К. Первичная пластика отторгнутыми лоскутами кожи // Краснодар, 1947. — 236 с.
5. Рубашев С.М. К вопросу о лечении травматической отслойки кожи // Вестн. хир. — 1936. — Т. 47, кн. 127. — С. 87-88.
6. Элькин М.А. К вопросу о лечении травматической отслойки кожи // Хирургия. — 1939. — № 1. — С. 60-62.
7. Гугуцидзе А.Г. Травматическая отслойка кожи // Труды НИИТО МЗ Грузинской ССР. — Тбилиси, 1972. — Т. XI. — С. 233-237.
8. Schiefer R. Die Ablederungsverletzung (Ein Beitrag zur Anwendung des grossen Vollhautlappens) // Zbl Chir. — 1966. — Vol. 24. — S. 869-874.
ПОЛИТРАВМА / POLYTRAUMA
Муниципальное автономное учреждение здравоохранения Ордена Знак Почета «Городская клиническая больница № 8», г. Челябинск, Россия,
Федеральное государственное бюджетное учреждение «Российский научный центр «Восстановительная травматология и ортопедия» им. акад. Г.А. Илизарова» Министерства здравоохранения Российской Федерации, г. Курган, Россия
КЛИНИЧЕСКИЙ ПРИМЕР ЛЕЧЕНИЯ ПАЦИЕНТКИ С ОБШИРНОЙ ТРАВМАТИЧЕСКОЙ ОТСЛОЙКОЙ МЯГКИХ ТКАНЕЙ
Обширная отслойка мягких тканей (ООМТ) часто является серьезной хирургической патологией, характеризующейся отслоением кожи и подкожной клетчатки от нижележащих мышц и фасций, возникающей в результате внезапного сдвига, приложенного к поверхности кожи [1, 2].
Основные локализации обширных отслоек кожи - это нижние конечности, туловище, скальп и лицо 6. Отслойки можно классифицировать как закрытые/внутренние или открытые/внешние поражения 9. Как результат такой травмы может быть полный некроз отслоенных тканей из-за нарушения в них кровообращения [10]. Кроме того, из-за неправильного ведения ран у пациентов с обширными размозжениями тканей под отслоенной кожей часто развивается инфекционный процесс, некротический фасциит, приводящие к еще более тяжелому состоянию и летальному исходу [7, 11].
Однако различие между жизнеспособными и нежизнеспособными тканями может быть затруднено при раннем лечении ООМТ в обоих типах травм [7]. И поскольку каждая травма уникальна по разнообразию поражений, трудно разработать соответствующий алгоритм принятия решений для лечения; поэтому исход ООМТ часто остается недооцененным [1, 6]. На результат лечения оказывают свое влияние множество факторов: локализация, площадь и глубина повреждения тканей, сопутствующие травмы и патологии, лабораторные данные, а также выбор метода лечения: качество первичной хирургической обработки тканей, первичное наложение швов, первоначальное консервативное лечение, последовательное этапное удаление размозженных тканей, применение вакуумного лечения ран (VAC), первичная пластика по Красовитову 14. При подобных травмах также важен способ фиксации конечности. Создание благоприятных условий для заживления ран оптимальнее всего происходит в условиях чрескостного остеосинтеза по Илизарову [15, 16].
При этом необходимо подчеркнуть, что до настоящего времени лечение таких больных проходит с наличием ряда организационных и лечебно-тактических проблем, начиная с того, что существуют сложности с кодировкой данной патологии в системе МКБ 10. Для травмы нижних конечностей подходит код Т04.3 (Размозжение нескольких областей нижней (их) конечности (ей)). При этом в перечне нозологий ОМС по травматологии отдельно данный вид травмы не выделяется. Соответственно, медицинские карты этих больных учитываются по другим кодам: в лучшем случае как политравма, в худшем - как скальпированная рана. Нет утвержденного объема обследования мягких тканей, необходимых методов лечения, критериев выполнения стандарта для данной патологии. Нет клинических рекомендаций и стандартов лечения пациентов с данной патологией, утвержденных Министерством здравоохранения РФ.
КЛИНИЧЕСКИЙ ПРИМЕР
Работа была выполнена в соответствии с этическими нормами Хельсинкской декларации Всемирной медицинской ассоциации «Этические принципы проведения научных медицинских исследований с участием человека» с поправками 2013 г. и «Правилами клинической практики в Российской Федерации», утвержденными приказом Минздрава РФ от 19.06.2003 г. № 266. Пациент подписал информированное согласие на проведение хирургического вмешательства и публикацию полученных данных без идентификации личности.
В качестве клинического примера хотим представить опыт лечения больной К. 55 лет, которая получила травму 17.04.2012 во время дорожно-транспортного происшествия. При посадке в автобус она оступилась, упала на землю, после чего автобус проехал по ее левой нижней конечности. Бригадой скорой медицинской помощи в тяжелом состоянии, обусловленном травматическим шоком 2 степени и продолжающимся кровотечением, была доставлена в приемное отделение ближайшей к месту травмы МБУЗ ГКБ № 8 г. Челябинска с диагнозом: «Политравма, геморрагический шок 2 степени (табл.), обширная открытая отслойка мягких тканей левой нижней конечности (стопа, голень, бедро), продолжающееся кровотечение из левой паховой области».
Таблица. Динамика лабораторных показателей у пациентки К. 55 лет
Эритроциты, ×10 12 /л
Лейкоциты, ×10 9 /л
Тромбоциты (10 9 /л)
Прокальцитониновый тест, нг/мл
Общий билирубин, мкмоль/л
Прямой билирубин, мкмоль/л
При поступлении собран анамнез, проведены клинические и лабораторные исследования, выполнена рентгенография левой нижней конечности, таза. При поступлении на фоне проведения инфузии артериальное давление 90/60 мм рт. ст., пульс 80 в 1 мин, частота дыхательных движений 20 в 1 мин. Общая площадь выявленных отслоенных тканей 19 % поверхности тела. Выявлен открытый перелом проксимальной фланги 1-го пальца левой стопы без смещения. Таким образом была установлена степень тяжести травмы по шкале Injury Severity Score (ISS) (Baker S.P. et al., 1974) - тяжелая, индекс травмы (Kirkpatric J.R., Youmans R.L., 1971) - 12 (тяжелое повреждение) [17, 18]. По классификации отслоек по Arnez Z.M. с соавторами (2009) полученная травма относится ко второй группе (нециркулярная рана, зона повреждения ограничена одним слоем (как правило, между глубокой фасцией и подкожно-жировой клетчаткой)) [19].
На фоне проводимой противошоковой терапии травматологами-ортопедами была выполнена операция: первичная хирургическая обработка ран левой нижней конечности, остановка кровотечения левой паховой области. Проведена ревизия ран на протяжении всей левой нижней конечности, выявлен отрыв кожи с подкожно-жировой клетчаткой от поверхностной фасции на бедре и голени полуциркулярного характера, в области коленного сустава - по задней полуокружности, на стопе - циркулярно.
Пульс на тыльной артерии стопы и задней большеберцовой артерии ритмичный, ослабленный. Нарушений чувствительности на пальцах стопы нет. Снижена чувствительность на отслоенных кожных лоскутах. Первый палец на левой стопе бледный, прохладный. Другие пальцы телесного цвета, теплые, но прохладнее, чем на здоровой стопе. Под общей анестезией ткани левой нижней конечности были отмыты растворами антисептиков, выполнена остановка кровотечения, покровные ткани были уложены на свое место и фиксированы швами, установлены активные дренажи, конечность с учетом обширности повреждения мягких тканей была фиксирована аппаратом Илизарова. С учетом тяжести общего состояния больная после операции доставлена в реанимационном отделении.
19.04.2012 выполнена трахеостомия. Несмотря на выполненные манипуляции, кровотечение из поврежденных тканей сохранялось. В течение следующих суток по дренажам было получено около 400 мл геморрагического отделяемого (источник - область задней поверхности коленного сустава). В связи с этим на вторые сутки после травмы пострадавшая была взята опять в операционную, где выполнена повторная хирургическая обработка. Попытка найти поврежденные магистральные сосуды не увенчалась успехом. Вмешательство закончилось установкой дренажей и ушиванием раны.
В послеоперационном периоде состояние больной продолжало оставаться тяжелым. В последующие 10 дней больная оставалась в отделении реанимации, где проводились перевязки. Общее состояние пострадавшей постепенно ухудшалось, что выражалось в клинической картине локального и общего статуса и подтверждалось данными инструментальных и лабораторных исследований. Тяжелое состояние было обусловлено явлениями перенесенного травматического и геморрагического шока, неблагоприятным течением обширного раневого процесса, токсикоза, являющегося следствием всасывания в микроциркуляторное русло продуктов распада тканей. Температура имела гектический характер.
К 11-м суткам после травмы отмечалась церебральная, дыхательная, сердечно-сосудистая недостаточность, имелась острая печеночная и нутритивная недостаточность. По шкале Глазго - 10 баллов, RASS - 2 балла. Локально отмечалось увеличение конечности в объеме, покраснение кожных покровов, обширные участки некроза кожи и подкожно-жировой клетчатки. Были удалены швы, раскрыты раны, из которых получено мутное серозно-гнойное отделяемое. В анализах крови выраженный сдвиг лейкоцитарной формулы, гиповолемия, прокальцитониновый тест резко положительный (табл.). По результатам клинического и лабораторного обследования был диагностирован ранний посттравматический сепсис, по шкале SOFA (Sequential Organ Failure Assessment) - 6, по шкале APACHE - 22 балла. Из ран были высеяны Pseudomonas aeruginosa в 10 5 , Acinetobacter baumannii 10 6 , Aeromonas 10 6 , Klebsiella pneumonia 10 6 ; из крови был высеян Enterococcus faecium 10 4 и Acinetobacter baumannii 10 2 .
На совместном консилиуме с привлечением пластического хирурга из ожогового центра г. Челябинска (03.05.2012) было решено выполнить в срочном порядке повторную хирургическую обработку ран с их ревизией, иссечением нежизнеспособных тканей, при этом пациентка уже находилась в состоянии септического шока.
При очередной ревизии ран выявлено, что у больной имелась недиагносцированная обширная отслойка покровных тканей не только левой нижней конечности, но и левой ягодичной области, передней брюшной стенки в подвздошной, паховой и левой боковой областях (рис. 1, 2). При этом под поврежденными кожными покровами находились напряженные гематомы общим объемом до 300 мл. В результате общая площадь поражения составила 30 % поверхности тела. При ревизии ран выявлен разрыв большой ягодичной мышцы, что было закрыто разволокненной широкой фасцией правого бедра (рис. 3), размозжение части мышц голени и бедра. Такие повреждения тканей (некробиоз) неизбежно вызывали эндогенную интоксикацию и развитие гнойно-септических осложнений.
Рисунок 1. Фотография левой нижней конечности пациентки К. 55 лет на 15-е сутки после травмы перед ревизией отслоенных тканей. Видны формирующиеся зоны некроза покровных тканей левого бедра, серая подкожно-жировая клетчатка раны, коленного сустава и стопы, кровоизлияния в покровные ткани проксимальнее раны
Рисунок 2. Фотография левой стопы пациентки К. 55 лет на 15-е сутки после травмы. Видны поврежденные покровные ткани, характер и тяжесть повреждения определить сложно из-за наличия типичной для хирургии ошибки. Окружающие рану покровные ткани широко и густо окрашены раствором бриллиантового зеленого, под которым сложно определить особенности кожных покровов (цианоз, некроз, гиперемия)
Рисунок 3. Фотография пациентки К. 55 лет. Во время ревизии раны на бедре выявлено наличие отслойки покровных тканей между поверхностной фасции бедра и подкожно-жировой клетчаткой, доходящей до лонного сочленения и линии пупка
Во время операции было произведено широкое раскрытие «карманов», иссечены некротические и резко ишемизированные ткани. Общая площадь удаленных покровных тканей составила 15 % поверхности тела. Однако половину из удаленных кожных покровов удалось обработать по Красовитову и подготовить для последующей реплантации (рис. 4). Установлены активные дренажи, наложены наводящие швы для фиксации лоскутов. В конце операции раны частично закрыты полнослойными кожными аутотрансплантатами. На глубокую рану передней поверхности правого бедра уложена вакуумная повязка VivanоMed c переменным разряжением (производитель медицинского изделия «Пауль Хартманн АГ». Место нахождения организации - Германия, 'Paul Hartmann AG', Paul-Hartmann-Str.12, 89522, Heidenheim, Germany. ФСЗ 2012/12770. Дата государственной регистрации медицинского изделия: 20.08.2012. Срок действия регистрационного удостоверения: бессрочно).
Рисунок 4. Фотографии левой нижней конечности пациентки К. 55 лет во время операции на 15-е сутки после травмы
После этой операции пациентка продолжала лечение в отделении реанимации на аппарате искусственного дыхания. Состояние пациентки стабилизировалось в течение трех суток. В послеоперационном периоде регулярно проводились перевязки и хирургические обработки под общей анестезией, общая инфузионная и антибактериальная терапия. Показательна динамика изменений прокальцитонинового теста, которая говорит о купировании системной воспалительной реакции организма (табл.).
11, 21, 25 мая выполнялись этапные некрэктомии и пластики ран левой нижней конечности расщепленными кожными трансплантатами (рис. 5). 22.05.2012 больная экстубирована, 25.05.2012 переведена в общую палату, где продолжено медикаментозное лечение и перевязки. С 28.05.2012 больная начала вставать, постепенно увеличивая физическую нагрузку. Переведена из хирургического стационара в отделение реабилитации 30.05.2012, срок лечения острой травмы составил 33 дня.
Рисунок 5. Этап реконструктивно-восстановительного лечения пациентки К. 55 лет через 1 месяц после травмы
При выписке пациентки отмечалось благоприятное заживление всех ран, сохранялась мозаичная гипестезия кожи в зонах отслойки. За время нахождения на реабилитации больная была вертикализирована, она снова научилась ходить.
После выписки из стационара больная продолжила курс реабилитации в амбулаторных условиях. Самостоятельно она начала ходить через 2 месяца после травмы, через два года вернулась к обычной трудовой деятельности в качестве преподавателя кафедры физкультуры. На контрольном осмотре через 6 лет больная жалоб не предъявляет, ран нет, трофических язв нет, занимается спортом, носит обычную обувь (рис. 6).
Рисунок 6. Отдаленный результат лечения пациентки К. 55 лет через 6 лет
Рассмотренное клиническое наблюдение демонстрирует следующее:
1. При отсутствии серьезных повреждений внутренних органов и минимальной скелетной травмы на фоне обширной отслойки мягких тканей развивается угрожающее жизни состояние, требующее длительной интенсивной терапии и неотложных хирургических вмешательств.
2. Использование современных диагностических процедур (УЗИ, КТ с контрастированием сосудов, МРТ левой нижней конечности, передней брюшной стенки, ягодичной области) у данной пациентки в ближайшее время после травмы позволило бы точнее и раньше установить диагноз, определить тяжесть повреждения тканей и выбрать более правильную хирургическую тактику лечения.
3. Своевременное участие пластического хирурга в процессе лечения необходимо для установки точного диагноза, оказания специализированной помощи при обширных отслойках покровных тканей.
4. Обработка кожных покровов раствором бриллиантового зеленого (или иными красящими антисептиками) затрудняет визуальную оценку состояния покровных тканей (гиперемию, цианоз, сосудистую реакцию) и должна быть исключена из арсенала лечебных мероприятий.
5. Выявленные на начальном этапе лечения данной больной организационные и тактические ошибки являются достаточно характерными при оказании медицинской помощи пострадавшим с подобными травмами. В связи с этим необходимо проведение большой информационной и организационной работы с целью разработки и практического внедрения алгоритма ведения больных с обширными отслойками мягких тканей.
Информация о финансировании и конфликте интересов
Исследование не имело спонсорской поддержки.
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Техника рассечения кожи, подкожной клетчатки и поверхностной фасции. Разрезание кожи, подкожной жировой клетчатки и фасции.
БУ «Городская клиническая больница №1» Минздрава Чувашии, Чебоксары, Россия
ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», Чебоксары, Россия;
БУ «Больница скорой медицинской помощи» Минздрава Чувашии, Чебоксары, Россия
ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова» Чебоксары, Россия, БУ «Республиканская клиническая больница» Минздрава Чувашии, Чебоксары, Россия
ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова» Чебоксары, Россия
ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», Чебоксары, Россия;
АУ «Республиканский клинический онкологический диспансер» Минздрава Чувашии, Чебоксары, Россия
Значимость фасциальных структур передней брюшной стенки при проведении оперативного доступа и развитии послеоперационных осложнений
Журнал: Оперативная хирургия и клиническая анатомия. 2019;3(1): 8‑12
Введение. В последние годы кесарево сечение становится все более распространенным методом родоразрешения, однако хирурги недостаточно осведомлены о наличии и расположении фасциальных структур. Цель исследования. Изучить топографоанатомические особенности фасциальных структур передней брюшной стенки для обеспечения адекватного оперативного доступа при проведении суправезикального экстраперитонеального кесарева сечения по методике Г.Л. Драндрова (1988). Материал и методы. Исследование выполнено с использованием трупного (50 образцов) и биопсийного (150 биоптатов) материала. Методы исследования: диссекция, интраоперационное наблюдение, микроскопия срезов, окрашенных гематоксилином и эозином. Результаты. На основании полученных данных можно предположить, что забрюшинная фасция, как и внутрибрюшная, распространяется по окружности, ее производными на передней брюшной стенке являются пред- и позадипузырная фасции. Заключение. Суправезикальное экстраперитонеальное кесарево сечение — операция выбора при высоком риске гнойно-септических осложнений.
В последние годы кесарево сечение становится все более распространенным методом родоразрешения. Причиной тому стали как объективные факторы (увеличение среднего возраста первородящих и, как следствие, увеличение числа беременностей на фоне экстрагенитальной патологии после применения вспомогательных репродуктивных технологий; возрастание количества беременных с рубцом на матке и др.), так и ряд субъективных факторов (желание матери избежать родовой деятельности, предпочтения акушера) [1].
Лидерами по частоте проведения оперативных родов среди стран признаны Бразилия (около 56% всех родов) и Турция (более 40% родов) [2]. По данным Росстата, за последние 10 лет в России доля абдоминальных родов также возросла более чем в 1,5 раза — с 17,9% в 2005 г. до 28% в 2016 г. [3].
Столь широкое внедрение кесарева сечения в повседневную практику требует от современного акушера-гинеколога умения владеть различными его методиками на высоком уровне и выбирать предпочтительный оперативный доступ в зависимости от клинической ситуации. Длительный безводный период и высокий риск инфекционных осложнений являются прямыми показаниями для выполнения кесарева сечения внебрюшинным доступом [4]. Однако частота применения подобных операций в настоящее время низка [5], что объясняется наличием эффективных антибактериальных препаратов, препятствующих развитию гнойно-септических осложнений, и высоким риском ранения мочевого пузыря и сосудов при выполнении оперативного вмешательства [6].
Однако, по нашему мнению, высокая частота подобных осложнений связана не с технической сложностью операции, а с неполной осведомленностью хирургов о наличии и расположении фасциальных структур, рассекаемых во время оперативного доступа.
Цель исследования — изучить топографоанатомические особенности фасциальных структур передней брюшной стенки для обеспечения адекватного оперативного доступа при проведении суправезикального экстраперитонеального кесарева сечения по методике Г.Л. Драндрова (1988).
Исследование выполнено с использованием трупного (50 образцов) и биопсийного (150 биоптатов) материала. Биопсийный материал получен во время проведения суправезикального экстраперитонеального кесарева сечения по методике Г.Л. Драндрова (1988), а также интраперитонеального кесарева сечения.
Методы исследования: диссекция, интраоперационное наблюдение, микроскопия срезов, окрашенных гематоксилином и эозином. Материал фиксировали в 10% нейтральном забуференном формалине в течение 48 ч, после чего выполняли стандартную гистологическую проводку в гистопроцессоре Leica ASP200 (Германия). Парафиновые срезы толщиной 4 мкм окрашивали гематоксилином и эозином.
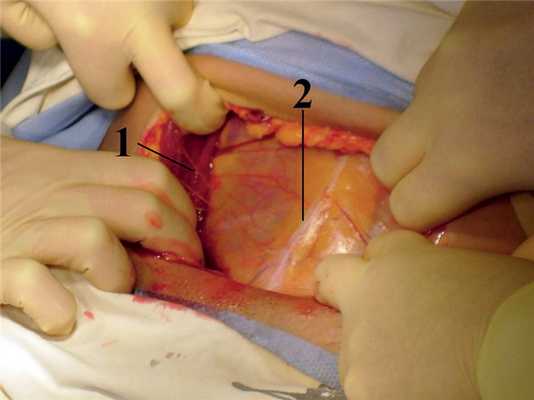
При осуществлении экстраперитонеального оперативного доступа к нижнему сегменту матки после рассечения кожи, подкожной жировой клетчатки и апоневроза широких мышц живота и разведения прямых мышц живота тупым путем обнажается поперечная фасция (рис. 1). Рис. 1. Поперечный надлобковый разрез по Пфанненштилю.
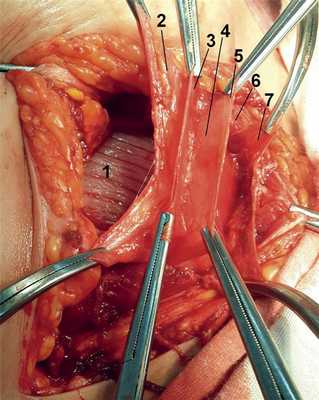
При вскрытии поперечной фасции визуализируется еще 2 тонких пласта ткани, покрывающих спереди и сзади мочевой пузырь (рис. 2). Рис. 2. Интраперитонеальный оперативный доступ. Полость брюшины вскрыта. Кзади от последнего располагается брюшина.
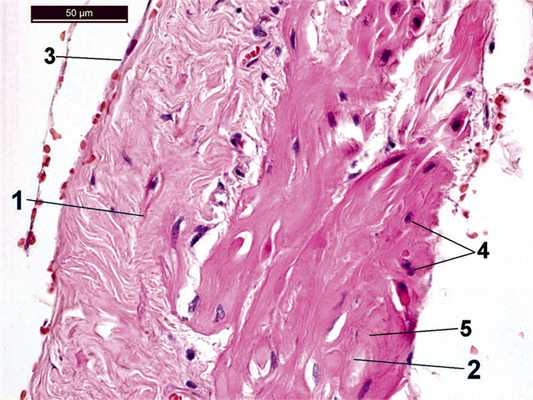
При микроскопии срезов данных тканей, окрашенных гематоксилином и эозином, выявлено, что они образованы оформленной соединительной тканью и представляют собой фасциальные структуры (рис. 3). Рис. 3. Позадипузырная фасция (2) и брюшина (1). И если первое образование (предпузырная фасция) упоминается во многих литературных источниках начиная с середины прошлого века, то наличие фасциальной структуры позади мочевого пузыря (позадипузырной фасции) не отражено в известной нам литературе. Некоторые авторы упоминают о существовании висцеральной фасции мочевого пузыря [7], а также fasc. vesico umbilicalis, которая покрывает мочевой пузырь со всех сторон [8].
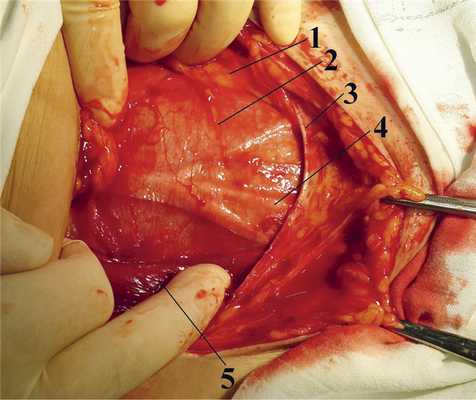
При выполнении диссекции на трупном материале выявлено, что листки пред- и позадипузырной фасций, охватывая мочевой пузырь спереди и сзади, по бокам и выше пупка сливаются в общий листок с поперечной фасцией. От верхушки мочевого пузыря к пупку между предпузырной и позадипузырной фасциями следует урахус (рис. 4). Рис. 4. Поперечный надлобковый разрез по Пфанненштилю. Поперечная фасция (1) вскрыта.
Посредством фасций малый таз разделен на фасциальные клетчаточные пространства. Непосредственно за поперечной фасцией расположено собственно предпузырное клетчаточное пространство. Между листками пред- и позадипузырной фасций и стенкой мочевого пузыря расположено околопузырное пространство. Между брюшиной и позадипузырной фасцией располагается позадипузырное клетчаточное пространство. При наличии в нем хорошо выраженной жировой клетчатки брюшина довольно легко отслаивается от задней стенки мочевого пузыря, что позволяет создать суправезикальный экстраперитонеальный доступ к нижнему сегменту матки. Однако в большинстве случаев это весьма затруднительно, и попытка разделения может осложниться травмой мочевого пузыря. Отпрепаровка брюшины значительно облегчается, если предварительно ножницами рассечь позадипузырную фасцию в поперечном направлении над мочевым пузырем, которая достаточно прочно фиксирует к нему брюшину.
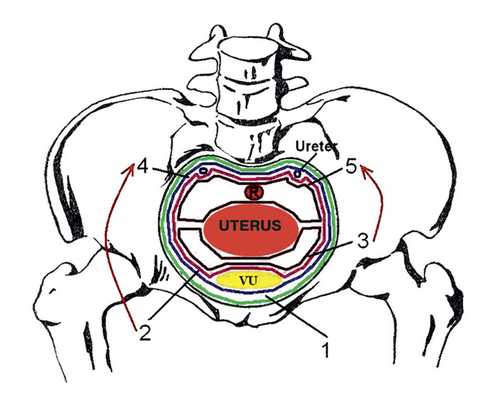
Анализ 20 клинических случаев послеоперационных осложнений показал, что гнойные затеки и гематомы из околопузырного клетчаточного пространства могут распространяться по ходу мочеточников в околопочечную клетчатку, а также через запирательный канал на бедро; при повреждении брюшины и поперечной фасции — во влагалище прямых мышц живота и в область пупка. Из позадипузырного клетчаточного пространства патологическое содержимое может затечь в забрюшинное клетчаточное пространство (рис. 5). Рис. 5. Схема возможного распространения гнойных затеков и гематом по клетчаточным пространствам таза.
На основании полученных данных можно предположить, что забрюшинная фасция, как и внутрибрюшная, распространяется по окружности, ее производными на передней брюшной стенке являются пред- и позадипузырная фасции, а кзади она расщепляется на пред- и позадипочечный листки. Это, по нашему мнению, является закономерностью и подтверждает футлярную теорию Н.И. Пирогова.
Суправезикальное экстраперитонеальное кесарево сечение — операция выбора при высоком риске гнойно-септических осложнений. С наступлением эры антибиотиков экстраперитонеальный доступ, к сожалению, несколько утратил свою популярность. Однако, кроме очевидного преимущества в профилактике перитонитов, он имеет и массу других достоинств: отсутствие перитонеальных болей в послеоперационном периоде, уменьшение сроков реабилитации женщины, профилактика спаечного процесса [9, 10].
Кроме того, необходимо помнить, что эра антибиотикорезистентности не за горами, поэтому, на наш взгляд, весьма вероятно, что суправезикальный экстраперитонеальный доступ к нижнему сегменту матки найдет свое место в современном акушерстве. А знание о существовании и ходе пред- и позадипузырной фасций поможет докторам выполнять хирургические вмешательства на органах малого таза с меньшей травматичностью и позволит определять наиболее вероятные пути распространения гноя и гематом в случае возникновения послеоперационных осложнений.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Драндров Д.Г. — ординатор кафедры акушерства и гинекологии ФГБОУ ВО «ЧГУ им. И.Н. Ульянова»; 428015, Чувашская Республика, Чебоксары, Московский пр., 15
Москвичев Е.В. — д.м.н., проф. кафедры нормальной и топографической анатомии с оперативной хирургией ФГБОУ ВО «ЧГУ им. И.Н. Ульянова»; 428015, Чувашская Республика, Чебоксары, Московский пр., д. 15. Зав. патологоанатомическим отделением АУ «Республиканский клинический онкологический диспансер» МЗ ЧР; 428020, Чувашская Республика, Чебоксары, ул. Гладкова, 31
Миопластический способ ампутации голени по Митишу—Светухину (модификация метода Бюржеса).
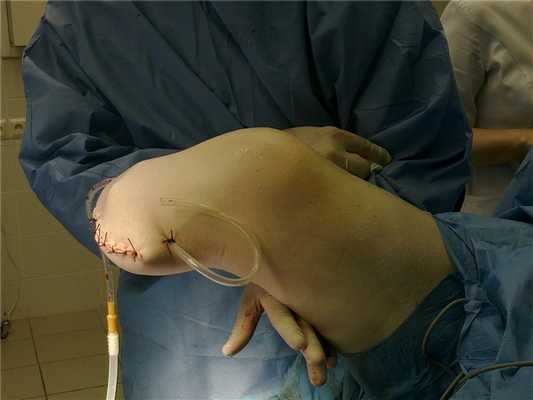
Данный способ миопластической ампутации голени разработан в Институте хирургии им. А.В. Вишневского РАМН для пациентов с хронической критической ишемией нижних конечностей.
При окклюзионном поражении артерий голени, поверхностной бедренной и подколенной артерий у больных с сохраненным кровотоком по глубокой артерии бедра развивается коллатеральная сеть на уровне коленного сустава. Через коллатерали происходит питание тканей верхней трети голени. В этой ситуации наиболее хорошо кровоснабжается икроножная мышца, так как ее питающая артерия отходит выше щели коленного сустава, что позволяет сформировать хорошо кровоснабжаемый икроножный кожно-мышечный лоскут при ампутации на уровне верхней трети голени. Однако, кровоснабжение камбаловидной мышцы существенно страдает, так как осуществляется из бассейна заднеберцовой артерии, которая в большей степени подвержена окклюзионно-стенотическому поражению.
В.А.Митиш и А.М.Светухин (1997 г.) предложили во время ампутации голени полностью удалять камбаловидную мышцу, а при необходимости также и мышцы передней и наружной групп и формировать культю голени за счет икроножного кожно-мышечного.
Преимущества данного метода:
- формирование культи голени из тканей с сохраненным или развитым коллатеральным кровотоком;
- возможность атравматичной обработки сосудисто-нервного пучка на проксимальном уровне;
- уменьшение рисков местных раневых осложнений в послеоперационном периоде;
- формирование культи правильной цилиндрической формы;
- лучшая адаптация культи в условия протезирования в позднем послеоперационном периоде;
- гемодинамически значимое окклюзионно-стенотическое поражение магистральных артерий пораженной конечности на проксимальном уровне, включая глубокую артерию бедра;
- значимые нарушение микроциркуляторного звена на уровне предполагаемой ампутации (уровень TcP02 < 28—30 мм рт. ст.)
По данным авторов, разработавших и успешно применяющих метод ампутации голени у больных с критической ишемией с 1993 г., положительный результат получен в 98,7 % случаев.
Продольным разрезом до уровня слияния сухожильного растяжения икроножной мышцы с камбаловидной, по границы наружной и задней групп мышц латеральной м медиальной поверхности голени рассекают кожу, подкожную жировую клетчатку и собственную фасцию голени. Дополнительным критерием дистального уровня разреза служит уровень, расположенный на 3—4 см выше границы отека и гиперемии тканей. Далее, после рассечения собственной фасции голени выделяют икроножную и камбаловидную мышцы и тупо разделяют их друг от друга на всем протяжении. Дистальную ножку заднего мягко-тканного комплекса рассекают (с пересечением сухожилия икроножной мышцы) и формируют задний икроножный кожно-мышечный лоскут. Затем выделяют верхнюю часть камбаловидной мышцы и отсекают ее от проксимальных точек прикрепления, благодаря чему широко обнажается сосудисто-нервный пучок в верхней трети голени, что, в свою очередь, позволяет максимально атравматично обработать сосудисто-нервный пучок на необходимом уровне. Поперечным полуовальным разрезом на 1,0 см ниже предполагаемого уровня пересечения большеберцовой кости рассекают кожу, подкожную клетчатку и фасцию. На протяжении 1,5-2 см мобилизуют от надкостницы большеберцовой кости кожно-фасциальный лоскут. В косопоперечном направлении рассекают переднюю и наружную группы мышц с обработкой сосудов и нерва. Последовательно выполняют транспериостальную остеотомию малой и большой берцовых костей, при этом малоберцовую кость перепиливают на 1,5—2 см выше уровня пересечения большеберцовой кости. Гребень большеберцовой кости резецируют в косом направлении. Поперечно рассекают оставшиеся мышцы задней группы. Таким образом культя голени условно разделяется на переднюю часть — передний кожно-фасциальный лоскут и культи берцовых костей с окружающими мышцами и заднюю часть — икроножный кожно-мышечный лоскут. Икроножный кожно-мышечный лоскут должен быть длиннее остальных частей на значение, равное сагиттальному поперечнику торца формируемой культи. Образовавшееся пространство кзади от берцовых костей дренируют перфорированной силиконовой трубкой, выведенной на кожу через отдельные разрезы, и ликвидируют, подшивая заднюю часть культи к передней синтетическими рассасывающимися нитями. Опилы берцовых костей закрывают задним кожно-мышечным лоскутом, после чего избыточную часть икроножного лоскута иссекают. Края раны адаптируют друг к другу и ушивают. После операции проводят аспирационное дренирование в течение 1—3 дней.
Строение кожи и ее придатков - Официальный сайт Санкт-Петербургского общества дерматовенерологов

Кожа состоит из трех слоев: эпидермиса, дермы (собственно кожи) и гиподермы (подкожной клетчатки).
Эпидермис - самый верхний, наружный слой кожи - состоит из клеток многослойного плоского ороговевающего эпителия, которые по мере дифференцировки продвигаются от базальной мембраны по направлению к поверхности кожи. Эпидермис, в свою очередь, состоит из 5 слоев: базального, шиповатого, зернистого, блестящего и рогового.
Основа эпидермиса - самый нижний, внутренний базальный слой (stratum basale, germinativum), состоит из 1 ряда мелких клеток цилиндрической формы - базальных кератиноцитов. Непосредственно над базальным слоем кератиноциты увеличиваются в размере и формируют шиповатый слой (stratum spinosum), состоящий из 3—6 (до 15) рядов шиповатых кератиноцитов, постепенно уплощающихся к поверхности кожи. Из-за высокой митотической активности (частого деления клеток) базальный и шиповатый слои называют ростковым слоем Мальпиги, за счет него происходят формирование и регенерация эпидермиса.
Зернистый слой (stratum granulosum) состоит из 2—3 рядов клеток, имеющих вблизи шиповатого слоя цилиндрическую или кубическую форму, а ближе к поверхности кожи - ромбовидную.
Блестящий слой (stratum lucidum) выражен в участках наиболее развитого эпидермиса, т. е. на ладонях и подошвах, где состоит из 3—4 рядов вытянутых по форме слабо контурированных клеток.
Роговой слой (stratum corneum) образован полностью ороговевшими безъядерными клетками - корнеоцитами (роговыми пластинками), которые содержат нерастворимый белок - кератин. Наиболее развит роговой слой там, где кожа подвергается наибольшему механическому воздействию (ладони, подошвы).
Кроме вышеперечисленных клеток в эпидермисе также обнаруживаются меланоциты (клетки, вырабатывающие основной пигмент кожи), а также клетки иммунной системы кожи: клетки Лангерганса (эпидермальные макрофаги) и клетки Гринстейна (тканевые макрофаги).
Эпидермис отделен от дермы базальной мембраной, которая является эластической опорой, прочно связывающей эпителий с дермой и препятствующей прорастанию клеток эпидермиса в дерму.
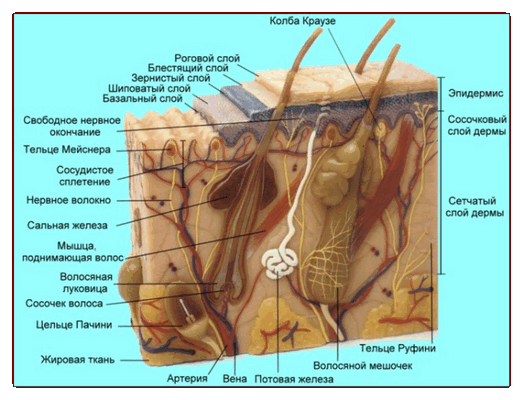
Дерма - соединительнотканная часть кожи - является опорой для придатков кожи (волос, ногтей, потовых и сальных желез), сосудов и нервов. Она состоит из двух слоев: сосочкового и сетчатого.
Тонкий верхний сосочковый слой (stratum papillare) состоит из бесструктурного вещества и тонких соединительнотканных (коллагеновых, эластических и ретикулярных) волокон и образует сосочки, залегающие между эпителиальными гребнями шиповатых клеток. Более толстый сетчатый слой (stratum reticulare) распространяется от основания сосочкового слоя до подкожной жировой клетчатки; основу его составляют пучки толстых коллагеновых волокон, расположенные параллельно поверхности кожи. В дерме располагается поверхностная сосудистая сеть, и две сети лимфатических сосудов - поверхностная и глубокая. В дерме же сосредоточена основная часть нервного аппарата кожи: два нервных сплетения - глубокое и поверхностное и множественные кожные рецепторы (свободные и инкапсулированные: колбы Краузе,тельца Фатера—Пачини, тельца Мейснера, диски Меркеля). В некоторых участках сосочкового слоя дермы располагаются мышечные волокна, связанные с волосяными луковицами - мышцы, поднимающие волос.
Гиподерма - подкожная жировая клетчатка - состоит из сети коллагеновых, эластических и ретикулярных волокон, между которыми располагаются дольки жировой ткани - скопления крупных жировых клеток-липоцитов. Толщина гиподермы варьирует от 2 мм (на черепе) до 10 см и более (на ягодицах). Гиподерма толще на дорсальных и разгибательных, тоньше на вентральных и сгибательных поверхностях конечностей. Местами (на веках, под ногтевыми пластинками, на крайней плоти, малых половых губах и мошонке) она отсутствует. В подкожной жировой клетчатке залегают крупные сосуды и нервные стволы.
Придатки кожи
К придаткам кожи относят волосы, ногти, сальные и потовые железы.
Волосы. В каждом волосе (pilus) различают две части: стержень и корень. Стержень - часть волоса, выступающая над поверхностью кожи. Корень волоса заложен в дерме и иногда доходит до подкожной жировой клетчатки. Корень волоса погружен в дермальное влагалище (соединительнотканную сумку) и формирует вместе с ним волосяной фолликул. Волосяной фолликул имеет цилиндрическую форму и открывается на поверхности кожи своеобразным расширением - воронкой, в которую погружается стержень волоса. На границе верхней и средней трети фолликула в него открывается выводной проток сальной железы. Самая глубокая расширенная часть корня волоса называется волосяной луковицей; нижняя часть луковицы - матрикс - состоит из клеток, отличающихся очень высокой митотической активностью и обеспечивающих рост волоса.
Читайте также:
