УЗИ при тромбозе воротной вены
Добавил пользователь Алексей Ф. Обновлено: 21.01.2026
Тромбоз селезеночной вены — это закупорка просвета сосуда тромбом, которая сопровождается увеличением селезенки и расширением сети коллатералей. Острый тромбоз проявляется болями в животе, кровавой рвотой и кишечным кровотечением. Для хронического варианта характерны дискомфорт и тяжесть в области левого подреберья, периодические кровотечения из носа и ЖКТ, анемия. Диагностика включает инвазивные (спленопортография, эндоскопическое УЗИ, лапароскопия) и неинвазивные исследования (КТ или МРТ брюшной полости, УЗИ-допплерография). Показано консервативное лечение либо хирургическое вмешательство (шунтирование, спленэктомия).
МКБ-10

Общие сведения
Тромбоз селезеночных вен — один из вариантов предпеченочной портальной гипертензии, на долю которого приходится около 5-10% всех патологий системы воротной вены. Распространенность в популяции составляет примерно 0,5%. Опасность сосудистого поражения заключается в геморрагических осложнениях и развитии гиперспленизма. Чаще всего тромбоз вен селезенки выявляется у страдающих циррозом печени (до 25%). Существенных возрастных и гендерных различий среди пациентов не выявлено.

Причины
Венозный тромбоз считается полиэтиологическим заболеванием, поскольку на его возникновение влияют локальные и системные факторы. У половины больных точную причину патологии не удается установить даже после тщательного инструментального обследования. Наиболее известный этиологический фактор — цирроз печени, который сопровождается вторичными изменениями селезеночной вены. В практической флебологии выделяют другие причины тромбоза:
- Интраабдоминальные факторы. Наиболее обширная категория причин, которая вызывает до 70% случаев заболевания. К обструкции селезеночной вены приводит хронический панкреатит и панкреонекроз, кисты и псевдокисты поджелудочной железы. Тромбозу способствуют воспалительные процессы в кишечнике, вирусные гепатиты.
- Врожденные предпосылки. Тромбообразование в просвете вен селезенки наблюдается у людей с генетически обусловленными тромбофилиями, гиперкоагуляционными состояниями. Предрасполагающим фактором тромбоза являются структурные аномалии селезеночной и воротной вен, которые способствуют задержке тромбоцитарных масс.
- Злокачественные новообразования. Заболевание встречается при опухолях головки поджелудочной железы или гепатоцеллюлярной карциноме и связано с механическим сдавлением венозных сосудов. У 3% пациентов тромбоз служит первым проявлением миелопролиферативной болезни.
- Системные поражения вен. Рецидивирующие тромбозы селезеночной вены являются частыми спутниками мигрирующего тромбофлебита. Воспалительный процесс в венозной стенке сочетается с повышенным притоком и агрегацией тромбоцитов. Некоторые случаи тромбоза обусловлены облитерирующим тромбангиитом (болезнью Бюргера).
- Механические повреждения. Появление тромбоза ожидаемо после тупой травмы живота, удара в область поясницы. Крайне редко закупорка селезеночной вены происходит как ятрогенное осложнение — при проведении хирургических вмешательств на печени или поджелудочной железе.
Факторы риска
Среди факторов риска исследователи выделяют системные или локальные инфекционные процессы (эндокардит, сепсис, туберкулез), которые сопровождаются повышением свертывающей активности крови. Вероятность обструкции возрастает у женщин во время беременности и в послеродовом периоде, у пациенток, которые принимают оральные контрацептивы. Частота тромбозов увеличивается при длительном соблюдении строгого постельного режима, в периоде реабилитации после обширных хирургических вмешательств.
Патогенез
В основе развития заболевания лежит триада Вирхова: гиперкоагуляция, деструкция клеток эндотелия сосудов и локальное замедление кровотока. При этом возникают благоприятные условия для скопления тромбоцитов в вене, которые затем прикрепляются к поврежденной венозной стенке. В селезеночных венах формируются красные тромбы, которые состоят из тромбоцитов, фибрина и эритроцитов.
При благоприятных условиях возможен асептический аутолиз или реканализация тромба с частичным восстановлением кровотока в селезеночной вене. Чаще наблюдается постепенный рост тромба и прогрессирующие расстройства гемодинамики в системе воротной вены. Одновременно активируется сеть коллатеральных венозных сосудов. При остром тромбозе коллатерали не успевают сформироваться.
Классификация
По локализации существуют тромботические процессы, которые поражают небольшие вены, отходящие от селезенки, а также тромбозы селезеночной вены, образованной слиянием мелких венозных сосудов. Тромбы подразделяются на пристеночные, при которых часть венозного просвета свободна, и обтурирующие. Обструкцию селезеночной вены систематизируют по характеру течения, согласно которому выделяют 2 разновидности тромбозов:
- Острые. Клинические проявления манифестируют в течение нескольких часов или дней. Характерно тяжелое состояние и высокий риск осложнений.
- Хронические. Заболевание развивается 2-3 года и более, протекает малосимптомно. По этиологии хронические тромбозы бывают первичными, когда патологический процесс сразу же локализован в вене селезёнки, и вторичными.
Симптомы
Острый тромбоз
Течение острого тромбоза напоминает хирургические заболевания органов брюшной полости. Внезапно ощущается резкая боль в животе, которая локализована слева в подреберье или в эпигастрии. Боли не связаны с приемом пищи или физическими нагрузками. Одновременно с болевым синдромом появляется рвота. В рвотных массах обнаруживаются примеси алой крови. После кровавой рвоты больные чувствуют облегчение. Через несколько часов отходит дегтеобразный стул.
Хронический тромбоз
Хронический тромбоз селезеночной вены длительное время протекает бессимптомно или малосимптомно. Первым признаком становится чувство тяжести и дискомфорта в левых отделах живота. При неловких движениях, резких поворотах в левом подреберье беспокоят тупые боли. При присоединении воспалительного процесса возникают эпизоды повышения температуры тела, сочетающийся с интенсивным болевым синдромом.
Спустя несколько лет после манифестации тромбоза появляются носовые или желудочно-кишечные кровотечения (рвота с кровью, черный кал). Наблюдается периодическое увеличение объема живота вследствие асцита. Асцит характеризуется быстрым прогрессированием и самостоятельным рассасыванием. Вследствие повторных кровотечений развивается анемия. Больные жалуются на головокружения, слабость, непереносимость физических нагрузок.
Осложнения
Типичное последствие тромбоза, которое встречается у 90% пациентов — профузные кровотечения из ЖКТ. Для тромбов в венах селезенки характерно поражение сосудов желудка, а не нижней трети пищевода, как при классической портальной гипертензии. Различия в локализации кровотечений обусловлены особенностями анастомозирования сосудов селезенки. При отсутствии медицинской помощи массивное кровотечение заканчивается смертью.
При хроническом варианте патологии тромбы распространяются на брыжеечные вены и кишечные аркады. Нарушается кровоснабжение тонкого кишечника, происходит рефлекторный спазм артериол. Возникает интестинальная ишемия, которая в 5% случаев заканчивается инфарктом кишечника. При компенсаторном расширении венозных коллатералей происходит сдавление внепеченочных желчных протоков, что вызывает механическую желтуху и холангит.
Диагностика
Постановкой диагноза тромбоза селезеночной вены чаще занимаются врачи-хирурги, реже — гастроэнтерологи или узкоспециализированные гепатологи. Физикальные данные не отличаются от таковых при классических формах портальной гипертензии. Пациенту назначают комплекс лабораторно-инструментальных исследований:
- Анализы крови. В клиническом анализе выявляют анемию или панцитопению, которая характерна для гиперспленизма. Коагулограмма проводится для исключения врожденных коагулопатий. У больных с циррозом печени обнаруживают снижение протромбинового индекса.
- УЗИ брюшной полости. Классическая чрескожная сонография недостаточно информативна, поэтому рекомендовано эндоскопическое УЗИ, обладающее специфичностью 99%. Метод выявляет наличие тромбов в просвете селезеночной вены, спленоренальные и портосистемные шунты. Для оценки кровотока проводится ультразвуковая допплерография.
- КТ брюшной полости. Применяется не только для обнаружения тромба, но и с целью верификации причин тромбоза. Чаще используется КТ с контрастированием. Альтернативой рентгенологическому методу является МРТ органов живота, при которой отсутствует лучевая нагрузка.
- Спленопортография. Инвазивное исследование сосудов бассейна воротной вены показано на этапе подготовки к хирургической коррекции заболевания. С помощью рентгеноконтрастного метода визуализируют все венозные сосуды и их коллатерали, выясняют размеры, протяженность и локализацию тромбоза.
- Лапароскопия. Современная малоинвазивная методика рекомендована для выявления этиологии болезни. При поражении селезеночных сосудов хирурги видят неизмененную или пораженную циррозом печень на фоне хорошо развитых коллатералей и резко увеличенной селезенки.
Лечение тромбоза селезеночной вены
Консервативная терапия
Лечебная тактика при тромбозах предполагает устранение обструкции кровотока и компенсацию возникших нарушений. Из-за высокого риска кровотечения лечение проводится в стационаре. При продолжающемся кровотечении вводят гемостатики, выполняют эндоскопическую коагуляцию сосудов. Базовая терапия включает 3 группы препаратов:
- Тромболитики. Ферментные лекарственные средства, разрушающие тромбы, применяются только в случае острого тромбоза, с момента появления которого прошло не более 5 дней. Для целенаправленного введения лекарств выбирают внутривенный или катетерный способ.
- Антикоагулянты. Низкомолекулярные гепарины показаны для предотвращения распространения тромба. Современные препараты безопасны и не требуют постоянного контроля коагулограммы. Непрямые антикоагулянты добавляют спустя неделю после начала гепаринотерапии.
- Дезагреганты. Препараты назначаются для длительного приема. Их действие преимущественно направлено на профилактику вторичного тромбоза, если не получается устранить этиологические факторы. Вместо ацетилсалициловой кислоты предпочитают использовать производные тиенопиридинов.
Для предупреждения пилефлебита необходима парентеральная антибактериальная терапия в комбинации с противогрибковым препаратом. По показаниям больные принимают обезболивающие средства — анальгетики из группы нестероидных противовоспалительных средств, спазмолитики. Чтобы улучшить реологические свойства и электролитный состав крови, проводится инфузионная терапия. Дальнейшее лечение подбирается с учетом причины тромбоза.
Хирургическое лечение
Среди оперативных вмешательств распространено спленоренальное или мезокавальное шунтирование, которое предназначено для разгрузки венозной сети и профилактики кровотечений из расширенных вен. При невозможности создать сосудистые анастомозы рекомендована спленэктомия. Удаление селезенки решает проблему гиперспленизма и панцитопении, но является независимым фактором риска повторного тромбоза.
Прогноз и профилактика
У 90-95% пациентов с тромбозом селезеночной вены консервативные методики позволяют купировать обострение и нормализовать венозный кровоток. Для полного излечения требуется устранение причины тромбоза, поэтому при онкологических процессах прогноз сомнительный. Профилактика состоит в своевременном лечении болезней печени и поджелудочной железы, назначении дезагрегантов больным с гиперкоагуляционными нарушениями.
1. Тромбоз воротной вены: современный взгляд на вопросы этиопатогенеза, профилактики и лечения/ И.Г. Бакулин, Н.В. Шаликиани// Эффективная фармакотерапия. Гастроэнтерология. — 2015.
2. Тромбоз воротной и селезеночной вен — предпеченочная портальная гипертензия/ Е.В. Онучина// Клиническая медицина. — 2005.
3. Диагностика и профилактика тромбоза селезеночной вены у больных инфицированным панкреонекрозом/ А.И. Андреев, А.Ю. Анисимов// Вестник современной клинической медицины. — 2014.
4. Тромбоз вен портальной системы у больных острым панкреатитом/ С.М. Чуклин, Б.Я. Подгорный// Госпитальная хирургия. — 2015.
Тромбоз воротной вены ( Пилетромбоз )
Тромбоз воротной вены - это полная или частичная окклюзия ствола воротной вены и ее ветвей тромботическими массами. Патология проявляется абдоминальным синдромом, рвотой, диареей, признаками портальной гипертензии (асцит, спленомегалия, расширение венозных коллатералей), осложняется кровотечением из верхних отделов пищеварительного тракта, инфарктом кишечника и другими состояниями. Основу диагностики составляют методы визуализации - УЗДС, МР- и КТ-ангиография, венография пораженных участков. Лечебная тактика предполагает антикоагулянтную терапию, тромболизис, хирургическую коррекцию.

Тромбоз воротной вены (пилетромбоз) считается достаточно редким явлением, риск возникновения которого не превышает 1% в общей популяции. Его распространенность среди пациентов с циррозом печени варьируется от 0,6 до 26%, что, по-видимому, связано с различием в критериях выборки и диагностических методах. Заболевание называют причиной 5-10% случаев портальной гипертензии у жителей развитых стран и до 40% - в азиатском регионе (из-за более высокой частоты инфекционной патологии). Распространенность первичного тромбоза у взрослых и детей одинакова. Гендерных отличий в развитии болезни не выявлено, кроме цирротической обструкции, чаще диагностируемой у мужчин.

Заболевание имеет мультифакторную природу. Тромбоз развивается под влиянием системных и локальных нарушений, участвующих в повреждении сосудистой стенки, усилении коагуляции, замедлении венозного кровотока. Среди наиболее значимых причин отмечают следующие:
- Цирроз печени. Является основным этиологическим фактором, составляя 24-32% случаев тромботической окклюзии. Вероятность тромбоза повышается на поздних стадиях болезни, при необходимости трансплантации органа. Переход цирроза в гепатоцеллюлярную карциному увеличивает частоту внепеченочных пилетромбозов.
- Новообразования. Злокачественные новообразования печеночного или панкреатического происхождения являются причиной 21-24% случаев тромбоза. Развитие патологии опосредовано компрессией или прямой опухолевой инвазией, сопутствующей гиперкоагуляцией, гормональными сдвигами.
- Тромбофилии. Системные нарушения вызваны врожденными дефектами коагуляции - генетическими мутациями (фактора V Лейдена, протромбина, ингибитора активатора плазминогена), дефицитом протеинов C и S, антитромбиновой недостаточностью. К приобретенным факторам относят хроническую миелопролиферативную патологию, антифосфолипидный синдром, пароксизмальную ночную гемоглобинурию.
- Воспалительные заболевания. Патологический процесс может возникать на фоне абдоминальной воспалительной патологии (панкреатита, холецистита, гепатита), инфекционных заболеваний (малярии, брюшного тифа, амебиаза). У детей и новорожденных половина случаев тромбоза приходится на долю омфалита, пупочного сепсиса, аппендицита.
- Травмы и оперативные вмешательства. Воротная вена подвергается повреждению при травмах живота и хирургических вмешательствах на органах брюшной полости (спленэктомии, холецистэктомии, трансплантациии печени). Патология возникает после портосистемного шунтирования, тонкоигольной аспирационной биопсии печени, склеротерапии вен пищевода.
К другим факторам риска тромбоза воротной вены относят беременность, прием пероральных контрацептивов, гиперхолестеринемию. Отмечена роль внутрибрюшной аденопатии, синдрома системного воспалительного ответа. В детском возрасте окклюзия возникает при врожденных аномалиях сосудистой системы (дефектах межжелудочковой и межпредсердной перегородок, деформации полой вены) и желчевыводящих путей. Причина 10-30% тромботических стенозов остается невыясненной.
Исходя из современных представлений, пилетромбоз является результатом системных коагулопатий (наследственных, приобретенных) и действия локальных факторов. Повреждение стенки сосуда опухолью, инвазивными процедурами или травмами характеризуется выработкой цитокинов, активацией тромбоксана A2 и тромбина, усилением адгезии и агрегации тромбоцитов. Венозный застой при наружной компрессии сопровождается гипоксией эндотелия, накоплением активированных факторов свертывания. Все это запускает формирование пристеночного кровяного сгустка с дальнейшим его увеличением.
Сосудистая окклюзия сопровождается портальной гипертензией, что ведет к изменению системной и внутриорганной гемодинамики. Печень теряет около 2/3 своего кровоснабжения, но это компенсируется дилатацией печеночной артерии и быстрым развитием сети коллатералей. Вокруг тромбированной вены формируется кавернома, а сама она превращается в фиброзный тяж. Новообразованные сосуды расположены в пределах желчных протоков и пузыря, поджелудочной железы, антрального отдела желудка, двенадцатиперстной кишки.
Патогенез тромбоза при печеночном циррозе до конца не ясен. Важное значение отводят портальной гипертензии с замедлением кровотока по воротной вене, периферическому лимфангииту, перипортальному фиброзу. Системное шунтирование крови провоцирует гемосидероз, гепатоциты в зонах гипоперфузии подвергаются апоптозу. В тонком и толстом кишечнике выше уровня окклюзии определяются застойные явления, в желудке - гастропатия. Брыжеечная ишемия может привести к переходу тромботического процесса на мезентериальные сегменты.
Формальной классификации тромбоза воротной вены не существует. Согласно клиническим рекомендациям по портальной гипертензии, при постановке диагноза учитывают участок тромбоза и его проявления, наличие и характер основного заболевания, степень окклюзии (частичную, полную), вовлеченность внепеченочных сегментов. В зависимости от локализации тромба различают несколько форм патологии:
- Стволовая (трункулярная). Участок окклюзии расположен в стволе воротной вены, дистальнее слияния селезеночной и верхней мезентериальной. Возникает первично или путем распространения из корешкового сегмента.
- Радикулярная (корешковая). Характеризуется поражением корешковых ветвей - селезеночной вены и брыжеечных сосудов.
- Терминальная. Пилетромбоз распространяется на внутрипеченочные разветвления и капилляры, сопровождаясь мелкими или развитыми коллатералями.
Представленная классификация позволяет оценить последствия тромботической обструкции и трудоспособность пациента. При поражении сначала интерстициальных сосудов, а затем крупных стволов констатируют восходящий (первичный) процесс. Мезентериальный тромбоз, возникающий из-за обструкции воротной или селезеночной вен, называют нисходящим (вторичным). В клинической флебологии также различают острую, подострую и хроническую стадии, последовательно сменяющие друг друга.
Клиническая картина тромбоза воротной вены определяется происхождением, степенью, протяженностью, локализацией, темпами нарастания окклюзии, выраженностью коллатералей. Частичное тромбирование протекает бессимптомно, выявляясь лишь при инструментальной диагностике, полной обструкции (90-100% просвета) присуще бурное развитие за несколько суток. Подострая форма прогрессирует на протяжении 4-6 недель, а хронический процесс характеризуется медленным нарастанием симптоматики (от нескольких месяцев до года).
Стволовой тромбоз
Острый стволовой пилетромбоз проявляется резкими болями в правом подреберье и эпигастрии, сочетающимися с метеоризмом, частой рвотой, диареей (нередко с примесью крови). Быстро нарастают признаки портальной гипертензии - расширение подкожных, пищеводных, геморроидальных вен, асцит. Зачастую выявляют желтуху, недостаточность печеночной функции. Общее состояние пациентов быстро становится тяжелым, что в основном обусловлено рецидивирующими кровотечениями из желудочно-кишечного тракта.
Радикулярный тромбоз
Радикулярный тромбоз на уровне селезеночного сегмента начинается остро, с боли в левом подреберье, кровавой рвоты и дегтеобразного стула. Увеличение селезенки и субфебрильная лихорадка сочетаются с обычными размерами печени. В подостром периоде постепенно нарастают спленомегалия, асцит, расширяется венозная сеть на животе. Терминальная форма патологии выявляется только при распространенном поражении - у таких пациентов обычно определяют увеличенную селезенку, широкие подкожные коллатерали.
Хронический пилетромбоз не имеет специфических проявлений. Отсутствие аппетита и общая слабость - иногда единственные симптомы болезни. У большинства пациентов выявляют подкожные анастомозы, умеренный асцит. В 20-40% случаев патология манифестирует кровотечением из варикозных расширений пищевода. Вялотекущие варианты тромбоза воротной вены характеризуются нерезким болевым синдромом, субфебрилитетом, чувствительностью печении при пальпации. Отмечаются спленомегалия с признаками гиперспленизма, тяжестью в подреберье, исхуданием.
Наиболее опасное следствие острой окклюзии мезентериальных сосудов - инфаркт кишечника с развитием перитонита и полиорганной недостаточности (характерно для 5% случаев). Большинство осложнений длительного пилетромбоза обусловлено портальной гипертензией. Расширение пищеводных вен у многих пациентов сопровождается кровотечением, риск которого в 100 раз выше при циррозе печени. Выраженное портосистемное шунтирование приводит к печеночной энцефалопатии, вторичным изменениям в желчевыводящих путях (портальной билиопатии, холангиопатии). При сохраняющихся факторах риска тромбозы могут рецидивировать, осложняться эмболизацией.
Отсутствие специфических признаков тромбоза, необходимость определения предпосылок, уровня, степени и последствий поражения создают потребность в комплексном обследовании пациента. Основой диагностической программы выступают методы инструментальной визуализации:
- УЗАС воротной вены. Обладая высокой специфичностью (60-100%), признано методом выбора при первичной диагностике. УЗДС определяет неоднородный очаг повышенной эхогенности с нечеткими контурами, частично или полностью перекрывающий сосудистый просвет. Допплеровское картирование дает возможность выявить отсутствие кровотока в вене и ее притоках, наличие портосистемных шунтов, каверноматозную трансформацию.
- КТ и МР-ангиография сосудов.КТ с контрастированием дает точную информацию о состоянии венозных стенок, протяженности тромбированных участков, наличии перивисцеральных коллатералей, варикозных вен в забрюшинном пространстве. Магнитно-резонансную ангиографию используют для выяснения состоятельности портального кровотока, оценки просвета шунтов - ее результаты более надежны, чем УЗДС.
- Портальная венография. Используется в случаях, когда неинвазивными методами подтвердить или исключить тромботическое поражение не удается. Контрастная венография выявляет не только стенозы, но и дефекты наполнения от сдавления извне. Однако при установленной проходимости сосуда в ней нет необходимости.
Проводя диагностику пилетромбоза, врачи-флебологи обращают внимание на показатели коагулограммы (увеличение фибриногена, протромбинового индекса, замедление времени свертывания крови), низкий уровень антитромбина. Выявить варикозно-расширенные вены пищевода позволяет ФГДС, исключить цирроз удается благодаря эластографии и биопсии печени. Дифференциальная диагностика осуществляется с печеночным шистосомозом, тромбозом нижней полой вены, сдавливающим перикардитом, рестриктивной кардиомиопатией.
Лечение тромбоза воротной вены
Задачами лечебной коррекции являются восстановление проходимости сосуда, предотвращение прогрессирования патологии, устранение осложнений венозной гипертензии. Исходя из остроты процесса, возраста пациента, этиологических и прочих факторов, применяют комбинацию консервативных и радикальных методов:
- Антикоагулянтная терапия. Является лучшим способом для реканализации венозного просвета, но единого мнения о ее применении нет. Длительность лечения антикоагулянтами (низкомолекулярными гепаринами, пероральными средствами) у лиц с острым пилетромбозом составляет от 3 до 6 месяцев, а при хроническом решается в индивидуальном порядке.
- Введение тромболитиков.Регионарный тромболизис (введение стрептокиназы, альтеплазы, тенектеплазы) транспеченочным или трансъюгулярным доступом позволяет обеспечить реканализацию, избежав побочных эффектов антикоагулянтной терапии. При острой тотальной или субтотальной окклюзии может выполняться системный тромболизис.
- Хирургические методы. При неэффективности консервативных мероприятий операцией выбора является дистальное спленоренальное шунтирование. В условиях нарушенной проходимости селезеночного участка накладывают мезентерикопортальный или мезентерикокавальный анастомоз с применением сосудистых протезов.
Варикозные расширения пищевода лечат с помощью лигирования, эндоскопической склеротерапии. В ургентных ситуациях при кровотечении могут производить операции азигопортального разобщения (гастротомию с прошиванием нижней трети пищевода, деваскуляризацию желудка). Тяжелый гиперспленизм требует спленэктомии.
В целом прогноз при заболевании относительно благоприятный. Сгустки могут подвергаться асептическому аутолизу, организации, васкуляризации. Десятилетняя выживаемость для взрослых достигает 60%, а общий уровень смертности составляет менее 10%. При наличии цирроза и злокачественных новообразований прогноз ухудшается. Иногда тромбы превращаются в эмболы, становятся источником сепсиса. Но своевременное и интенсивное лечение приводит к реканализации сосуда, что сопровождается полным клиническим выздоровлением. Профилактика рецидивов проводится путем назначения антикоагулянтов.
1. Тромбоз воротной вены в практике гастроэнтеролога/ Подлесских М.Н., Цодиков Г.В., Волчкова Е.В. и др.// Фарматека. — 2010. — № 2.
2. Тромбоз воротной вены: современный взгляд на вопросы этиопатогенеза, профилактики и лечения / Бакулин И.Г., Шаликиани Н.В.// Эффективная фармакотерапия. Гастроэнтерология. - 2014- №2 (43).
3. Тромбоз воротной и селезеночных вен - предпеченочная портальная гипертензия/ Онучина Е.В.// Сибирский медицинский журнал. - 2005.
4. Тромбоз воротной вены у пациента с острым панкреатитом и хроническим алиментарно-токсическим гепатитом/ Карнута Г.Г. , Зиновьева С.Ю., Юркова Т.Е., Костюкевич О.И.// Русский медицинский журнал. - 2016. - №17.
Ультразвуковая диагностика венозных тромбозов, имеющих паранеопластический генез (клинические наблюдения)

Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Частота развития венозного тромбоза изменяется в достаточно широком диапазоне, зависящем от области поражения, а также причины, обусловившей тромбообразование. На аутопсии тромбоз воротной вены диагностируется в 0,14 - 0,6 % случаев, в то же время у пациентов, умерших от цирроза печени, пилетромбоз выявляется значительно чаще и достигает 9%. Частота тромбозов нижней полой вены и/или печеночных вен составляет 0,04 - 0,16 % [1].
Тромбоз воротной вены может быть следствием различных заболеваний: злокачественных новообразований, панкреатита, внутрибрюшного абсцесса, травмы, цирроза печени, воспалительных заболеваний толстого кишечника и т.д.
Пилетромбоз чаще развивается из-за локального нарушения системы свертывания крови и образования сгустка в просвете воротной вены. Эхографическая картина характеризуется появлением в просвете воротной вены неоднородного образования повышенной или смешанной эхогенности с неровными и нечеткими контурами, препятствующего кровотоку, размеры которого могут быть различными - от 0,5 см до полной окклюзии воротной вены и(или) ее ветвей [2].
По локализации различают 3 варианта пилетромбоза: радикулярный (корешковый), терминальный и трункулярный. Радикулярная форма характеризуется образованием тромбов в корешковых ветвях воротной вены - мезентериальных сосудах и селезеночной вене. Терминальный пилетромбоз возникает при наличии тромбов в просвете мелких разветвлений воротной вены внутри печени и в ее капиллярах. Трункулярный тромбоз воротной вены (стволовой пилетромбоз) может развиться первично в самом стволе и нередко вторично вследствие распространения тромботического процесса на ствол воротной вены из ее корешков [1].
Клиническая картина тромбоза воротной вены разнообразна и зависит от скорости формирования тромбов, локализации, степени закупорки сосудов, развития коллатеральных анастомозов. Острый тромбоз воротной вены чаще наблюдается при полицитемии, циррозе печени, после спленэктомии. Внезапно появляются разлитые боли в животе, тошнота, кровавая рвота, коллапс. Хронический пилетромбоз развивается медленно, от нескольких месяцев до нескольких лет. В случае образования кавернозных тромбов в просвете воротной вены больные могут жить годами и даже десятилетиями. Нередко начальным симптомом является желудочно-кишечное кровотечение. В большинстве случаев имеет место спленомегалия, а увеличение печени, кроме случаев цирроза, не является характерным признаком. В развернутой стадии болезни в клинической картине преобладают повторные желудочно-кишечные кровотечения [3, 4]. Изменения показателей функциональных проб печени зависят как от степени поражения сосуда, так и тяжести основного заболевания (цирроз, опухоль печени и др.), на фоне которого развился тромбоз воротной вены.
Тромбоз нижней полой вены и(или) печеночных вен регистрируется в 0,04 - 0,16 % вскрытий [1].
Эхографически тромбоз нижней полой вены проявляется наличием в просвете сосуда образования повышенной или смешанной эхогенности, чаще с неоднородной структурой, в которой могут выявляться мелкие анэхогенные трубчатые образования (участки реканализации) [2].
Клиническая картина тромбоза нижней полой вены зависит от ряда факторов: скорости формирования и распространения тромба; степени окклюзии просвета нижней полой вены; компенсаторных возможностей коллатералей; уровня тромбоза нижней полой вены, для которого принято выделять дистальный, почечный и печеночный сегменты. При локализации поражения в печеночном сегменте и переходе тромбоза на печеночные вены формируется синдром Бадда-Киари [5].
В литературе имеются данные о том, что тромбоз нижней полой вены не всегда сопровождается тяжелыми клиническими проявлениями, а чаще протекает бессимптомно. Последний вариант имеет место при хронической форме заболевания, неокклюзирующем тромбозе нижней полой вены, не имеющем характерных клинических признаков даже при большой распространенности процесса. Начальными симптомами болезни могут быть увеличение печени, боли в правом подреберье, рвота. На развернутой стадии нарастает гепатомегалия, печень становится плотной, в ряде случаев появляются спленомегалия, расширенные вены на передней брюшной стенке и грудной клетке. В терминальной стадии резко выражены симптомы портальной гипертензии. При острой форме заболевания имеют место те же симптомы, но скорость их появления и прогрессирования составляет несколько дней [1]. Нередко изолированный тромбоз печеночного сегмента нижней полой вены возникает при поражении этого отрезка вены опухолевым процессом [5].
Материалы и методы
Больной Х., 71 год, больная Б., 80 лет обследовались в условиях амбулаторного приема в отделении ультразвуковой диагностики МУЗ ГБ N 1 Курска. Сонографическое исследование проводилось по традиционной методике на современном ультразвуковом сканере, оснащенном линейным и секторным датчиками с частотой 3,5 Mгц. Учитывая скрининговый характер обследования больных, подробный сбор анамнеза, оценка функциональных, лабораторных данных не проводилась.
Клиническое наблюдение 1
Больной Х. направлен кардиологом для проведения УЗИ сердца (по поводу ишемической болезни сердца, стабильной стенокардии напряжения III ФК: НIIА) и гепатобилиарной зоны (в связи с жалобами на ноющие боли, чувство тяжести в правом подреберье). При проведении эхографии печени размеры последней соответствовали верхней границе нормы. Паренхима визуализировалась диффузно неоднородной, в ней лоцировались гипо- и изоэхогенные округлые и овальные образования различного размера (от 1,5 до 4,8 см) преимущественно с неоднородной внутренней структурой, несколько нечеткими контурами (рис. 1 а,б).
Возможности ультразвукового исследования с цветовым допплеровским картированием в диагностике тромбоза в системе воротной вены

Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Тромбоз воротной вены (ВВ) - процесс образования тромба вплоть до полной окклюзии просвета сосуда, дренирующего русло органов желудочно-кишечного тракта. Тромбоз воротной вены является редким заболеванием сосудов печени. Он может быть результатом большого количества различных заболеваний и оставаться бессимптомным или проявляться симптомами основного заболевания 2. Диагностика заболевания сложна. Прогноз при тромбозе воротной вены всегда серьезен и неблагоприятен, часто наблюдаются смертельные исходы вследствие кровотечений или печеночной комы.
Цель работы - показать на клинических примерах возможности ультразвукового исследования с цветовым допплеровским картированием (ЦДК) в диагностике тромбоза в системе воротной вены.
Прижизненный диагноз тромбоза основного ствола воротной вены в России впервые поставил С.П. Боткин в 1862 г. В 1934 г. Н.Д. Стражеско впервые в мировой литературе описал прижизненно распознанный тромбоз правой ветви ствола воротной вены и на основании собственных исследований и данных литературы разработал симптоматологию закупорки правой ветви воротной вены.
Достоверных сведений о частоте тромбоза воротной вены нет. По секционным данным, тромбоз выявляют в 0,14-0,34% всех вскрытий (L. Lissauer, 1908; L.Т. Webster, 1921; Е.С. Pallette, 1936). По другим данным (А.И. Грицюк, 1973), при вскрытии умерших от основных сердечно-сосудистых заболеваний (атеросклероза, гипертонической болезни, эндокардитов и пороков сердца) тромбоз воротной вены был обнаружен в 0,56% случаев (у 10 из 1763 умерших), что составляет 0,8% всех тромбоэмболий, развивающихся при этих заболеваниях. Известно, что тромбоз воротной вены поражает до 30% больных гепатоцеллюлярной карциномой и до 5% больных портальной гипертензией на фоне цирроза печени.
- Травма стенки вены во время хирургической операции.
- Снижение скорости потока крови в воротной вене: сдавление сосуда извне опухолью, рубцами, эхинококковой кистой, альвеококком; хроническая сердечная недостаточность; констриктивный перикардит; синдром Бадда - Киари (тромбоз печеночных вен).
- Повышение свертываемости крови либо изменение соотношения ее клеточных элементов: в послеоперационном периоде - особенно у онкологических больных, а также после спленэктомии; при воспалительных процессах - как осложнение острого аппендицита, при гнойных холангите и лимфадените гепатодуоденальной связки, язвенном колите; панкреонекрозе; умбиликальной инфекции в неонатальном периоде (неонатальная септициемия, омфалит, инфицирование при катетеризации пупочной вены с целью обменного переливания крови); при осложнениях беременности (в частности, эклампсии); при некоторых гематологических заболеваниях, обусловливающих повышение свертываемости крови (например, псевдосиндром Банти при висцеральном лейшманиозе).
Клиническая картина зависит от локализации и протяженности тромбоза воротной вены, быстроты его развития и природы предрасполагающего заболевания печени. Наиболее тяжелое проявление заболевания - инфаркт печени либо атрофия ее сегмента. Однако в 1/3 случаев тромбоз формируется медленно, вследствие чего успевает развиться коллатеральный кровоток, а воротная вена со временем реканализируется и происходит ее кавернозная трансформация. Тем не менее даже при относительно благоприятном течении заболевания развивается портальная гипертензия 4.
При диагностике тромбоза воротной вены следует обратить внимание на коагулограмму: повышение содержания фибриногена, появление активированного фибриногена Б, увеличение протромбинового индекса, уменьшение времени свертывания крови [2].
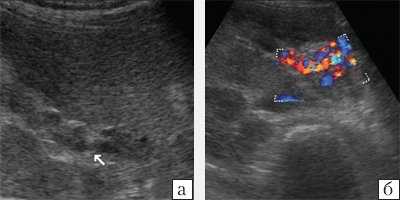
При ультразвуковом исследовании (УЗИ) в серошкальном режиме в просвете воротной вены можно выявить неоднородное образование повышенной или смешанной эхогенности, с неровными, нечеткими контурами, препятствующее кровотоку, размеры которого могут быть различными: от 0,5 см до полной окклюзии воротной вены и/или ее ветвей (рис. 1, а). Эхогенность тромба чаще является более высокой, чем окружающей его крови. Однако на ранних стадиях формирования эхогенность может отличаться настолько незначительно, что визуализация тромба чрезвычайно сложна. Могут определяться увеличение диаметра сосуда с нечеткостью контуров, увеличение печени и снижение ее эхогенности, увеличение селезенки. Могут быть найдены первопричины тромбоза воротной вены: гепатоцеллюлярная карцинома, метастазы, цирроз печени, новообразования поджелудочной железы и др. При пилефлебите обнаруживают абсцессы печени [3].

a) В-режим. Неоднородное образование повышенной эхогенности с неровными, нечеткими контурами в просвете воротной вены (стрелки).
б) Режим ЦДК. Полное отсутствие допплеровских сигналов внутри просвета сосуда; допплеровский сигнал определяется в сети мелких коллатералей.
При ЦДК отмечается полное или частичное отсутствие допплеровских сигналов внутри просвета сосуда; в случае частичного тромбоза сигнал определяется пристеночно вокруг тромба, частично окклюзирующего вену, либо в сети узких коллатералей (рис. 1, б). В случае частичного тромбоза определяется допплеровский сигнал с признаками турбулентности на фоне повышенной скорости кровотока. При опухолевом тромбозе кровоток может быть пульсирующим либо непрерывным [2, 3]. Визуализируются мелкие или крупные коллатерали. При кавернозной трансформации воротной вены в режиме ЦДК в коллатералях определяется сглаженная допплеровская кривая со средней скоростью кровотока меньше 8 см/с [5]. Возможны кавернозные мальформации вены, спонтанные порто-портальные, порто-кавальные и спленоренальные шунты.
При компьютерной томографии (КТ) обнаруживается тромб как дефект наполнения в просвете воротной вены, не усиливающий сигнала.
При магнито-резонансной томографии (МРТ) в просвете воротной вены выявляются участки патологического сигнала, не отличающегося по интенсивности от окружающих тканей на Т1-взвешенных изображениях и имеющие повышенную интенсивность на Т2-взвешенных изображениях.
Ангиография является методом окончательного подтверждения диагноза. Из соображений безопасности чаще исследуется венозная фаза верхнебрыжеечной артериографии, реже выполняется спленопортография. В воротной вене выявляют дефект наполнения, либо она вообще не контрастируется.
В зависимости от локализации тромба различают три вида тромбоза воротной вены: радикулярная форма (тромбоз селезеночной вены и мезентериальных сосудов); терминальная форма (тромбозы мелких разветвлений и капилляров воротной вены в печени); стволовой тромбоз (в самом стволе воротной вены) 3.
Кроме того, тромбоз воротной вены бывает острым (после спленэктомии, при циррозе) и хроническим (развивается долго - от нескольких месяцев до нескольких лет) 1.
Стадии тромбоза
- Острая - эхогенный тромб. Воротная вена может быть увеличена.
- Подострая - визуализируются тромб и мелкие коллатерали. Воротная вена может быть увеличена.
- Хроническая - крупные коллатерали в проекции облитерированной воротной вены (кавернозная трансформация воротной вены). Воротная вена уменьшена или не визуализируется 2.
Приводим несколько клинических наблюдений пациентов с тромбозом воротной вены и ее ветвей.
Пациент Ц., 39 лет. В анамнезе тупая травма живота с последующим развитием геморрагического панкреонекроза. Неоднократные оперативные вмешательства: дренирование сальниковой сумки. Предъявляет жалобы на боли в эпигастральной области.
УЗИ брюшной полости
Печень увеличена в размерах, контуры ее ровные, четкие, структура диффузно неоднородная, смешанной эхогенности, признаков билиарной гипертензии нет. Ствол воротной вены виден как образование неоднородной структуры с множеством эхогенных, параллельно идущих стенкам сосуда перегородок. Наличие гиперэхогенных участков в паравенозной области воротной вены (рис. 2, а). При ЦДК - выраженные коллатерали в проекции воротной вены (рис. 2, б). Желчный пузырь удален. Поджелудочная железа увеличена в размерах, головка - до 40 мм, контуры неровные, нечеткие, структура диффузно неоднородная, отмечается чередование участков повышенной и пониженной эхогенности, проток визуализируется на всем протяжении, на уровне тела поджелудочной железы он расширен до 10 мм. В проекции головки поджелудочной железы - выраженные околоподжелудочные коллатеральные анастомозы (рис. 3). Селезенка нормальных размеров, ее структура однородная, средней эхогенности. Селезеночная вена 7 мм, ход ее извит, деформирован, в проекции ворот селезенки имеются выраженные коллатерали (рис. 4). Заключение: гепатомегалия. Диффузные изменения печени. Картина хронического головчатого панкреатита. Тромбоз воротной вены с последующей реканализацией и кавернозной трансформацией воротной вены, развитием коллатеральных анастомозов.
а) В-режим. Отсутствие типичного трубчатого анэхогенного ствола воротной вены с гиперэхогенными стенками. Ствол воротной вены виден как образование неоднородной структуры с множеством эхогенных, параллельно идущих стенкам сосуда перегородок (стрелка). Наличие гиперэхогенных участков в паравенозной области воротной вены.
б) режим ЦДК - выраженные крупные коллатерали в проекции воротной вены.
Портальная гипертензия
Портальная гипертензия - синдром, развивающийся вследствие нарушения кровотока и повышения кровяного давления в бассейне воротной вены. Портальная гипертензия характеризуется явлениями диспепсии, варикозным расширением вен пищевода и желудка, спленомегалией, асцитом, желудочно-кишечными кровотечениями. В диагностике портальной гипертензии ведущее место занимают рентгеновские методы (рентгенография пищевода и желудка, кавография, портография, мезентерикография, спленопортография, целиакография), чрескожная спленоманометрия, ЭГДС, УЗИ и др. Радикальное лечение портальной гипертензии - оперативное (наложение портокавального анастомоза, селективного спленоренального анастомоза, мезентерико-кавального анастомоза).



Под портальной гипертензией (портальной гипертонией) понимается патологический симптомокомплекс, обусловленный повышением гидростатического давления в русле воротной вены и связанный с нарушением венозного кровотока различной этиологии и локализации (на уровне капилляров или крупных вен портального бассейна, печеночных вен, нижней полой вены). Портальная гипертензия может осложнять течение многих заболеваний в гастроэнтерологии, сосудистой хирургии, кардиологии, гематологии.
Этиологические факторы, приводящие к развитию портальной гипертензии, многообразны. Ведущей причиной выступает массивное повреждение печеночной паренхимы вследствие заболеваний печени:
- острых и хронических гепатитов
- опухолей печени, холедоха
- паразитарных инфекций (шистосоматоза),
- интраоперационном повреждении или перевязке желчных протоков.
Определенную роль играет токсическое поражение печени при отравлениях гепатотропными ядами (лекарствами, грибами и др.). К развитию портальной гипертензии может приводить заболевания сосудистого генеза:
- тромбоз, врожденная атрезия, опухолевое сдавление или стеноз портальной вены
- тромбоз печеночных вен при синдроме Бадда-Киари
- повышение давления в правых отделах сердца при рестриктивной кардиомиопатии, констриктивном перикардите.
В некоторых случаях развитие портальной гипертензии может быть связано с критическими состояниями при операциях, травмах, обширных ожогах, ДВС-синдроме, сепсисе. Непосредственными разрешающими факторами, дающими толчок к развитию клинической картины портальной гипертензии, нередко выступают инфекции, желудочно-кишечные кровотечения, массивная терапия транквилизаторами, диуретиками, злоупотребление алкоголем, избыток животных белков в пище, операции.

КТ ОБП. Портальная гипертензия на фоне обструкции воротной вены опухолью поджелудочной железы (красная стрелка). Опухолевый тромб (зеленая стрелка) в воротной вене. Асцит (белая стрелка).
Основными патогенетическими механизмами портальной гипертензии выступают наличие препятствия для оттока портальной крови, увеличение объема портального кровотока, повышенное сопротивление ветвей воротной и печеночных вен, отток портальной крови через систему коллатералей (потртокавальных анастомозов) в центральные вены.
В клиническом течении портальной гипертензии может быть выделено 4 стадии:
- начальная (функциональная)
- умеренная (компенсированная) - умеренная спленомегалия, незначительное расширение вен пищевода, асцит отсутствует
- выраженная (декомпенсированная) - выраженные геморрагический, отечно-асцитический синдромы, спленомегалия
- портальная гипертензия, осложненная кровотечением из варикозно-расширенных вен пищевода, желудка, прямой кишки, спонтанным перитонитом, печеночной недостаточностью.
В зависимости от распространенности зоны повышенного кровяного давления в портальном русле различают тотальную (охватывающую всю сосудистую сеть портальной системы) и сегментарную портальную гипертензию (ограниченную с нарушением кровотока по селезеночной вене с сохранением нормального кровотока и давления в воротной и брыжеечных венах).
По локализации венозного блока выделяют предпеченочную, внутрипеченочную, постпеченочную и смешанную портальную гипертензию. Различные формы портальной гипертензии имеют свои причины возникновения.
- Развитие предпеченочной портальной гипертензии (3-4 %) связано с нарушением кровотока в портальной и селезеночных венах вследствие их тромбоза, стеноза, сдавления и т. д.
- В структуре внутрипеченочной портальной гипертензии (85-90 %) различают пресинусоидальный, синусоидальный и постсинусоидальный блок. В первом случае препятствие на пути внутрипеченочного кровотока возникает перед капиллярами-синусоидами (встречается при саркоидозе, шистосомозе, альвеококкозе, циррозе, поликистозе, опухолях, узелковой трансформации печени); во втором - в самих печеночных синусоидах (причины - опухоли, гепатиты, цирроз печени); в третьем - за пределами печеночных синусоидов (развивается при алкогольной болезни печени, фиброзе, циррозе, веноокклюзионной болезни печени).
- Постпеченочная портальная гипертензия (10-12%) бывает обусловлена синдромом Бадда-Киари, констриктивным перикардитом, тромбозом и сдавлением нижней полой вены и др. причинами. При смешанной форме портальной гипертензии имеет место нарушение кровотока, как во внепеченочных венах, так и в самой печени, например, при циррозе печени и тромбозе воротной вены.

КТ ОБП. Этот же пациент, расширенный левый долевой ствол воротной вены (синяя стрелка) с периваскулярным отеком (желтая стрелка).
Симптомы портальной гипертензии
Наиболее ранними клиническими проявлениями портальной гипертензии служат диспепсические симптомы: метеоризм, неустойчивый стул, чувство переполнения желудка, тошнота, ухудшение аппетита, боли в эпигастрии, правом подреберье, подвздошных областях. Отмечается появление слабости и быстрой утомляемости, похудание, развитие желтухи.
Иногда первым признаком портальной гипертензии становится спленомегалия, выраженность которой зависит от уровня обструкции и величины давления в портальной системе. При этом размеры селезенки становятся меньше после желудочно-кишечных кровотечений и снижения давления в бассейне портальной вены. Спленомегалия может сочетаться с гиперспленизмом - синдромом, характеризующимся анемией, тромбоцитопенией, лейкопенией и развивающимся в результате повышенного разрушения и частичного депонирования в селезенке форменных элементов крови.
Асцит при портальной гипертензии отличается упорным течением и резистентностью к проводимой терапии. При этом отмечается увеличение объемов живота, отеки лодыжек, при осмотре живота видна сеть расширенных вен передней брюшной стенке в виде «головы медузы».
Характерными и опасными проявлениями портальной гипертензии являются кровотечения из варикозно измененных вен пищевода, желудка, прямой кишки. Желудочно-кишечные кровотечения развиваются внезапно, имеют обильный характер, склонны к рецидивам, быстро приводят к развитию постгеморрагической анемии. При кровотечении из пищевода и желудка появляется кровавая рвота, мелена; при геморроидальном кровотечении - выделение алой крови из прямой кишки. Кровотечения при портальной гипертензии могут провоцироваться ранениями слизистой, увеличением внутрибрюшного давления, снижением свертываемости крови и т. д.
Выявить портальную гипертензию позволяет тщательное изучение анамнеза и клинической картины, а также проведение совокупности инструментальных исследований. При осмотре больного обращают внимание на наличие признаков коллатерального кровообращения: расширения вен брюшной стенки, наличия извитых сосудов около пупка, асцита, геморроя, околопупочной грыжи и др.
- Лабораторный комплекс. Объем лабораторной диагностики при портальной гипертензии включает исследование клинического анализа крови и мочи, коагулограммы, биохимических показателей, АТ к вирусам гепатита, сывороточных иммуноглобулинов (IgA , IgM , IgG).
- Рентгенография. В комплексе рентгеновской диагностики используется кавография, портография, ангиография мезентериальных сосудов, спленопортография, целиакография. Данные исследования позволяют выявить уровень блокировки портального кровотока, оценить возможности наложения сосудистых анастомозов. Состояние печеночного кровотока может быть оценено в ходе статической сцинтиграфии печени.
- Сонография. УЗИ брюшной полости необходимо для выявления спленомегалии, гепатомегалии, асцита. С помощью допплерометрии сосудов печени производится оценка размеров воротной, селезеночной и верхней брыжеечной вен, расширение которых позволяет судить о наличии портальной гипертензии.
- Функциональные исследования. С целью регистрации давления в портальной системе прибегают к проведению чрескожной спленоманометрии. При портальной гипертензии давление в селезеночной вене может достигать 500 мм вод. ст., тогда как в норме оно составляет не более 120 мм вод. ст.
Обследование пациентов с портальной гипертензией предусматривает обязательное проведение эзофагоскопии, ФГДС, ректороманоскопии, позволяющих обнаружить варикозное расширение вен ЖКТ. Иногда вместо эндоскопии проводится рентгенография пищевода и желудка. К биопсии печени и диагностической лапароскопии прибегают в случае необходимости получения морфологических результатов, подтверждающих заболевание, приведшее к портальной гипертензии.

КТ ОБП. Этот же пациент, варикозно расширенные вены как проявление синдрома портальной гипертензии (коричневая стрелка).
Лечение портальной гипертензии
Терапевтические методы лечения портальной гипертензии могут быть применимы только на стадии функциональных изменений внутрипеченочной гемодинамики. В терапии портальной гипертензии используется:
- Фармакотерапия: нитраты (нитроглицерин, изосорбид), β-адреноблокаторы (атенолол, пропранолол), ингибиторы АПФ (эналаприл, фозиноприл), гликозаминогликаны (сулодексид) и др.
- Эндоскопические манипуляции. При остро развившихся кровотечениях из варикозно-расширенных вен пищевода или желудка прибегают к их эндоскопическому лигированию или склерозированию. При неэффективности консервативных вмешательств показано прошивание варикозно-измененных вен через слизистую оболочку.
- Оперативное лечение. Основными показаниями к хирургическому лечению портальной гипертензии служат желудочно-кишечные кровотечения, асцит, гиперспленизм. Операция заключается в наложении сосудистого портокавального анастомоза, позволяющего создать обходное соустье между воротной веной или ее притоками (верхней брыжеечной, селезеночной венами) и нижней полой веной или почечной веной. В зависимости от формы портальной гипертензии могут быть выполнены операции прямого портокавального шунтирования, мезентерикокавального шунтирования, селективного спленоренального шунтирования, трансъюгулярного внутрипечёночного портосистемного шунтирования, редукции селезеночного артериального кровотока, спленэктомия.
- Паллиативные вмешательства. Паллиативными мерами при декомпенсированной или осложненной портальной гипертензии, могут являться дренирование брюшной полости, лапароцентез.
Прогноз
Прогноз при портальной гипертензии, обусловлен характером и течением основного заболевания. При внутрипеченочной форме портальной гипертензии исход, в большинстве случаев, неблагоприятный: гибель пациентов наступает от массивного желудочно-кишечного кровотечения и печеночной недостаточности. Внепеченочная портальная гипертензия имеет более доброкачественное течение. Наложение сосудистых портокавальных анастомозов может продлить жизнь иногда на 10—15 лет.
Читайте также:
- Показания к неотложной терапии нарушений ритма. Показания к госпитализации больных с нарушениями ритма.
- Введение в лучевую диагностику паравертебрального пространства: лучевая анатомия, методы исследования
- Влияние аборта на течение рака молочной железы
- Факторы эпидемического процесса. Эпидемиологические проблемы современности
- Гистиоцитарная реакция при пневмониях. Типы пневмонических процессов
