Влияние альдостерона на обмен калия. Зависимость секреции калия от альдостерона
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Важно помнить! Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Другие названия: Aldosterone.
Код услуги для заказа 9004 Альдостерон в медицинской лаборатории Синэво.
Альдостерон — стероидный гормон, синтезирующийся из холестерина в клетках клубочкового слоя коры надпочечников - это основной и самый важный минералокортикоид. Альдостерон вызывает увеличение реабсорбции натрия и хлора в почечных канальцах таким образом задерживает натрий и хлор в организме, уменьшает выделение жидкости с мочой, усиливает выделения калия, тем самым альдостерон участвует в регуляции баланса электролитов, поддержании объёма крови и артериального давления.
Нормальная секреция альдостерона зависит от многих факторов: содержания калия (гиперкалиемия стимулирует, а гипокалиемия подавляет продукцию альдостерона), уровня АКТГ, магния и натрия в крови, активности ренин-ангиотензиновой системы. Ренин высвобождается из почек, когда снижается кровяное давление, уменьшается концентрация натрия в крови или повышается концентрация калия. Он расщепляет белок ангиотензиноген, содержащийся в крови, с образованием ангиотензина I, который под воздействием фермента преобразуется в ангиотензин II. Ангиотензин II, в свою очередь, способствует сокращению кровеносных сосудов и стимулирует образование альдостерона. В итоге данных преобразований поднимается кровяное давление и содержание натрия и калия поддерживается на необходимом уровне.
Повышенный уровень альдостерона клинически проявляется артериальной гипертензией, мышечной слабостью, судорогами и парестезиями, аритмиями. При первичном гиперальдостеронизме (синдром Конна) наблюдается повышение секреции альдостерона, причиной которого чаще всего является аденома клубочковой зоны коры надпочечников. Вторичный гиперальдостеронизм связан с застойной сердечной недостаточностью, циррозом печени с образованием асцита, определёнными заболеваниями почек, избытком калия, низконатриевой диетой, токсикозом беременных, стенозом почечных артерий (2-3% всех случаев артериальной гипертензии). Для первичного гиперальдостеронизма характерно повышение уровня альдостерона, сочетающееся с низкой активностью ренина плазмы, для вторичного гиперальдостеронизма — повышение концентрации альдостерона сочетается с высокой активностью ренина плазмы.
Пониженный уровень альдостерона обычно сопровождается гипонатриемией, гиперкалиемией, снижением выведения калия с мочой и повышением выведения натрия, метаболическим ацидозом и гипотонией. Наиболее частой причиной этого состояния является сниженная продукция ренина вследствие повреждения почек (гипоренинемический гипоальдостеронизм), особенно у пациентов с сахарным диабетом. Хроническая недостаточность коры надпочечников (болезнь Аддисона), вследствие её первичного повреждения при туберкулёзе, аутоиммунной патологии надпочечников, амилоидозе сопровождается снижением уровня альдостерона и повышением уровня ренина плазмы.
Показания к назначению:
- артериальная гипертензия и выявленная низкая концентрация калия.
- диагностика первичного гиперальдостеронизма, вызванного аденомой надпочечников и адреналовой гиперплазией;
- артериальная гипертензия, в том числе резистентные формы;
- артериальная гипертензия в молодом возрасте;
- ортостатическая гипотензия;
- подозрение на недостаточность надпочечников
Метод: иммуноферментный (ИФА)
Анализатор: полуавтоматический иммуноферментный анализатор IMark, США
Единицы измерения: пг/мл:
Материал для исследования: сыворотка венозной крови
Подготовка:
- Важным условием обеспечения качества лабораторного исследования крови является взятие материала натощак, в утреннее время (до 12:00).
- За 12 часов до исследования следует исключить прием алкоголя, курение, прием пищи, ограничить физическую активность.
- Утром в день взятия крови на исследование можно выпить воду.
- Исключить прием лекарств; если отменить прием лекарств невозможно, необходимо проинформировать об этом лабораторию.
- Взятие материала желательно проводить до проведения любых медицинских диагностических манипуляций.
- Ограничить потребление углеводов в течение 14-30 дней до исследования.
- В течение 14-30 дней до исследования отменить (по согласованию с врачом) мочегонные, антигипертензивные препараты, стероиды, пероральные контрацептивы и эстрогены.
- Исключить (по согласованию с врачом) прием ингибиторов ренина в течение 7 дней до исследования.
Интерпретация результатов:
Результат лабораторных исследований не является достаточным основанием для постановки диагноза. Интерпретация результатов и постановка диагноза осуществляется только лечащим врачом.
Референтные значения:
Пг/мл
Горизонтальное положение: 12,0-157,5
Вертикальное положение: 13,3-231,4
Повышение уровня:
- синдром Конна (первичный гиперальдостеронизм);
- альдостерома;
- гиперплазия надпочечников.
- вторичный гиперальдостеронизм:
- сердечная недостаточность;
- цирроз печени с образованием асцита;
- нефротический синдром;
- синдром Барттера;
- послеоперационный период у больных с гиповолемией, вызванной кровотечением;
- злокачественная ренальная гипертензия;
- гемангиоперицитома почки, продуцирующая ренин;
- транссудаты;
- синдром периодических отёков;
- псевдогиперальдостеронизм
Понижение уровня:
- болезнь Аддисона;
- гипоальдостеронизм.
- избыточная секреция дезоксикортикостерона, кортикостерона;
- синдром Шерешевского-Тернера (в 25% случаев);
- сахарный диабет;
- острая алкогольная интоксикация.
- синдром Лиддла.
- пожилой возраст
Факторы, влияющие на результат:
Повышение:
Диуретики, слабительные (хроническое злоупотребление с развитием дегидратации), эстрогены, пероральные контрацептивы, калий, ангиотензин.
Понижение:
Бета-блокаторы, центральные альфа 2 миметики, НПВС, ИАПФ, Са2+-блокаторы (группа дигидропиридинов), блокаторы АТ рецепторов, ингибиторы ренина, кортикостероиды, продолжительное лечение гепарином, продукты из корня лакрицы (солодки), аминоглютетимид, дезоксикортикостерон, этомидат.
Где сдать анализ Альдостерон (Aldosterone)
Сдать анализ Альдостерон (Aldosterone) можно в любом пункте Синэво в Минске, Барановичах, Бобруйске, Борисове, Бресте, Витебске, Ганцевичах, Гомеле, Гродно, Жлобине, Лиде, Могилеве, Мозыре, Молодечно, Новогрудке, Новополоцке, Орше, Пинске, Полоцке, Речице, Светлогорске, Слуцке, Сморгони, Солигорске.
Подробную информацию по ценам и срокам выполнения анализов Вы можете получить в разделе "Анализы" или по телефонам:
7766 звонок бесплатный для абонентов МТС и life:) звонок платный для абонентов A1 (по тарифам оператора) +375 (17) 338 88 88 звонок платный, тарифицируется как исходящий вызов на фиксированную сеть
Режим работы колл-центра понедельник-пятница: с 07:00 до 19:00 суббота: с 07:30 до 16:00 воскресенье: с 8:00 до 16:00
Анализ на альдостерон - гормон надпочечников
Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 20.06.2020
- Reading time: 3 минут чтения
Альдостерон - это стероидный гормон (минералокортикостероид), вырабатываемый надпочечниками в клубочковом слое. Он участвует в регуляции водного и минерального обмена, отвечает за выведение адекватного количества калия с мочой, реабсорбцию ионов натрия в почках, предотвращая их выведение и чрезмерную потерю, что будет связано с дегидратацией и снижением артериального давления.
Особенности выработки альдостерона в организме
Альдостерон является компонентом системы ренин-ангиотензин-альдостерон (система РАА). Этот гормон напрямую определяет удержание натрия (соли) в почках и косвенно влияет на выведение калия. Он играет важную роль в контроле объема крови и артериального давления.
Альдостерон синтезируется в коре надпочечников под влиянием целой цепи событий. Почка, реагируя на падение артериального давления или натрия (часто свидетельствует о дегидратации), начинает выделять ренин - фермент, катализирующий реакцию, продуктом которой является гормон ангиотензин.
Ренин превращает ангиотензиноген (белоксинтезируется печенью) в ангиотензин I. Затем ангиотензинпревращающий фермент превращает ангиотензин I в ангиотензин II. Ангиотензин II влияет на сужение кровеносных сосудов и стимулирует синтез альдостерона. У здоровых людей повышение активности ренина сопровождается увеличением концентрации альдостерона; когда активность ренина низкая, уровни альдостерона также снижаются.
Нормальная концентрация альдостерона в крови: 140-560 пмоль / л.
Показания к исследованию
Тест проводится для оценки нарушений секреции альдостерона или ренина. Это полезно при диагностике гиперальдостеронизма (чрезмерное производство альдостерона) или гипоальдостеронизма (недостаточный синтез альдостерона).
Анализ на альдостерон в крови или мочи и сывороточный ренин могут быть назначены, когда у пациента высокое кровяное давление и низкий уровень калия. Анализ иногда назначается вместе с другими тестами, когда врач подозревает у пациента надпочечниковую недостаточность.
Поскольку первичный гиперальдостеронизм является потенциально излечимой причиной гипертонии, которая часто не поддается обычному антигипертензивному лечению, некоторые врачи назначают тест на альдостерон и ренин, чтобы определить тип лечения, который может быть эффективным у пациентов с очень высоким кровяным давлением.
Симптомы, указывающие на повышенный уровень альдостерона - гиперальдостеронизм:
- В результате чрезмерно высокого уровня натрия и чрезмерного увлажнения: рефрактерная тяжелая гипертония, полиурия, жажда;
- В результате снижения уровня калия: слабость, онемение и спазмы мышц, аритмии.
Симптомы, указывающие на пониженный уровень альдостерона - гипоальдостеронизм:
- Из-за низкого уровня натрия и обезвоживания: сильная слабость, низкое кровяное давление.
- В результате повышения уровня калия: слабость, аритмии.
Противопоказания для проведения анализа на альдостерон
Для определения альдостерона достаточно собрать небольшое количество крови, поэтому противопоказаний для проведения этого теста нет.
Как проводится анализ на альдостерон
Образец крови берут из вены на руке. Некоторые врачи предпочитают оценивать секрецию альдостерона, основываясь на результатах теста на концентрацию этого гормона в образце мочи.
Уровень альдостерона изменяется в течение дня из-за его чувствительности к ряду факторов, включая положение тела. Поэтому для оценки уровней альдостерона врач может попросить пациента стоять или лежать в течение 15-30 минут до взятия крови. Лучше всего, если кровь собирается лежа утром, прежде чем пациент встанет с постели.
Расшифровка анализа
Высокие уровни альдостерона в сыворотке и моче, сопровождающиеся низким уровнем ренина, указывают на первичный гиперальдостеронизм. Напротив, вторичный гиперальдостеронизм характеризуется высоким уровнем альдостерона и ренина.
Низкие уровни альдостерона обычно возникают при недостаточности надпочечников или болезни Аддисона. Причиной снижения синтеза альдостерона у некоторых новорожденных с врожденной гиперплазией надпочечников является отсутствие фермента, необходимого для синтеза кортизола. Врожденная гиперплазия надпочечников считается редкой причиной гипоальдостеронизма.
Причины повышения альдостерона
Вторичный гиперальдостеронизм - повышение концентрации альдостерона происходит из-за наличия других заболеваний, таких как:
- Обезвоживание.
- Стеноз почечной артерии. Когда почечная артерия сужается, нарушается кровоснабжение почек. Почка воспринимает это как сигнал об обезвоживании и падении кровяного давления.
- Цирроз печени. Больная печень не может производить достаточно альбумина - белков плазмы, ответственных за онкотическое кровяное давление. В этой ситуации вода покидает кровеносные сосуды, мигрирует во внеклеточное пространство и происходит обезвоживание. Кроме того, печень не может метаболизировать альдостерон с соответствующей скоростью, поэтому происходит дополнительное повышение его концентрации.
- Нефротический синдром.
- Сердечная недостаточность. В этом случае сердце не может обеспечить адекватный кровоток через почки, которые получают это как сигнал об обезвоживании.
- Ренин-секретирующая опухоль - очень редко.
- Первичный гиперальдостеронизм (синдром Конны). Это синдром редкого заболевания, вызванный наличием аденокарциномы надпочечников (обычно доброкачественной) или гипертрофией клубочкового слоя коры надпочечников.
Причины снижения уровня альдостерона
- Дисфункция почек (чаще всего как осложнение длительного диабета) - почки не выделяют ренин в достаточных количествах.
- Первичная недостаточность надпочечников (болезнь Аддисона). Может быть вызвана аутоиммунной реакцией (чаще всего), туберкулезом или другими инфекциями или врожденным дефицитом ферментов, ответственных за синтез гормонов надпочечников (врожденная гиперплазия надпочечников).
- Применение лекарств - ингибиторов ангиотензинпревращающего фермента (АПФ-I), антагонистов рецептора ангиотензина II (препятствует стимуляции ангиотензина II надпочечниками для выделения альдостерона), нестероидных противовоспалительных препаратов (НПВП), ß-блокаторов.
Что может повлиять на результат анализа
На результаты теста на альдостерон может влиять:
- содержание соли в рационе;
- солодка, имитирующая свойства альдостерона;
- лекарства, особенно безрецептурные - нестероидные противовоспалительные болеутоляющие средства (такие как ибупрофен), диуретики, бета-блокаторы, стероиды, ингибиторы конвертирующих ферментов (АПФ) и оральные контрацептивы. Многие из этих препаратов используются для лечения высокого кровяного давления.
Уровень альдостерона снижается до очень низкого уровня во время тяжелой болезни, поэтому его не следует измерять в период обострения заболеваний. Увеличивать результаты альдостерона могут стресс и интенсивная физическая активность.
Перед обследованием врач должен проинформировать пациента о возможной необходимости изменения содержания натрия (соли) в рационе, отказа от диуретиков и других лекарств и о снижении физической активности.
Водно-электролитный обмен в организме здорового человека: принципы регуляции

Регуляция водно-солевого обмена, как и большинство физиологических регуляций, включает афферентное, центральное и эфферентное звенья. Афферентное звено представлено массой рецепторных аппаратов сосудистого русла, тканей и органов, воспринимающих сдвиги осмотического давления, объема жидкостей и их ионного состава. В результате, в центральной нервной системе создается интегрированная картина состояния водно-солевого баланса в организме. Так, при увеличении концентрации электролитов и уменьшении объема циркулирующей жидкости (гиповолемии) появляется чувство жажды, а при увеличении объема циркулирующей жидкости (гиперволемии) оно уменьшается. Следствием центрального анализа является изменение питьевого и пищевого поведения, перестройка работы желудочно-кишечного тракта и системы выделения (прежде всего функции почек), реализуемая через эфферентные звенья регуляции. Последние представлены нервными и, в большей мере, гормональными влияниями. Увеличение объема циркулирующей жидкости за счет повышенного содержания воды в крови (гидремия) может быть компенсаторным, возникающим, например, после массивной кровопотери. Гидремия с аутогемодиллюцией представляет собой один из механизмов восстановления соответствия объема циркулирующей жидкости емкости сосудистого русла. Патологическая гидремия является следствием нарушения водно-солевого обмена, например при почечной недостаточности и др. У здорового человека может развиться кратковременная физиологическая гидремия после приема больших количеств жидкости.
Помимо перманентного обмена водой между организмом и окружающей средой важное значение имеет обмен водой между внутриклеточным, внеклеточным сектором и плазмой крови. Следует отметить, что механизмы водно-электролитного обмена между секторами не могут быть сведены только к физико-химическим процессам, так как распределение воды и электролитов связано также с особенностями функционирования мембран клеток. Наиболее динамичным является интерстициальный сектор, на котором прежде всего отражаются потеря, накопление и перераспределения воды и сдвиги электролитного баланса. Важными факторами, влияющими на распределение воды между сосудистым и интерстициальным секторами является степень проницаемости сосудистой стенки, а также соотношение и взаимодействие гидродинамических давлений секторов. В плазме содержание белков равна 65-80 г/л, а в интерстициальном секторе только 4 г\л. Это создает постоянную разность коллоидно-осмотического давления между секторами, обеспечивающую удержание воды в сосудистом русле. Роль гидродинамического и онкотического факторов в обмене воды между секторами была показана еще в 1896г. американским физиологом Э. Старлингом: переход жидкой части крови в межтканевое пространство и обратно обусловлен тем, что в артериальном капиллярном русле эффективное гидростатическое давление выше, чем эффективное онкотическое давление, а в венозном капилляре - наоборот.
Гуморальная регуляция водно-электролитного баланса в организме осуществляется следующими гормонами:
- антидиуретический гормон (АДГ, вазопрессин), воздействует на собирательные трубочки и дистальные канальцы почек, увеличивая реабсорбцию воды;
- натриуретический гормон (предсердный натриуретический фактор, ПНФ, атриопептин), расширяет приносящие артериолы в почках, что увеличивает почечный кровоток, скорость фильтрации и экскрецию Na+; ингибирует выделение ренина, альдостерона и АДГ;
- ренин-ангиотензин-альдостероновая система стимулирует реабсорбцию Na+ в почках, что вызывает задержку NaCl в организме и повышает осмотическое давление плазмы, что определяет задержку выведения жидкости.
- паратиреоидный гормон увеличивает абсорбцию калия почками и кишечником и выведение фосфатов и увеличение реабсорбции кальция.
Содержание натрия и организме регулируется в основном почками под контролем ЦНС через специфические натриорецепторы. реагирующие на изменение содержания натрия в жидкостях тела, а также волюморецепторы и осморецепторы, реагирующие на изменение объема циркулирующей жидкости и осмотического давления внеклеточной жидкости соответственно. Содержание натрия в организме контролируется ренин-ангиотензинной системой, альдостероном, натрийуретическими факторами. При уменьшении содержания воды в организме и повышении осмотического давления крови усиливается секреция вазопрессина (антидиуретического гормона), который вызывает увеличение обратною всасывания воды в почечных канальцах. Увеличение задержки натрия почками вызывает альдостерон, а усиление выведения натрия — натрийуретические гормоны, или натрийуретические факторы (атриопептиды, простагландины, уабаинподобное вещество).
Состояние водно-солевого обмена в значительной степени определяет содержание ионов Cl- во внеклеточной жидкости. Из организма ионы хлора выводятся в основном с мочой, желудочным соком, потом. Количество экскретируемого хлорида натрия зависит от режима питания, активной реабсорбции натрия, состояния канальцевого аппарата почек, кислотно-щелочного состояния. Обмен хлора в организме пассивно связан с обменом натрия и регулируется теми же нейрогуморальными факторами. Обмен хлоридов тесно связан с обменом воды: уменьшение отеков, рассасывание транссудата, многократная рвота, повышенное потоотделение и др. сопровождаются увеличением выведения ионов хлора из организма.
Баланс калия в организме поддерживается двумя способами:
изменением распределения калия между внутри- и внеклеточным компартментами, регуляцией почечной и внепочечной экскреции ионов калия.
Распределение внутриклеточного калия по отношению к внеклеточному поддерживается прежде всего Na-K-АТФазой, являющейся структурным компонентом мембран всех клеток организма. Поглощения калия клетками против градиента концентрации инициируют инсулин, катехоламины , альдостерон. Известно, что ацидоз способствует выходу калия из клеток, алкалоз — перемещению калия внутрь клеток.
Экскретируемая почками фракция калия обычно составляет приблизительно 10-15 % от всего фильтруемого калия плазмы. Задержка в организме или выделение калия почкой определяется тем, каково направление транспорта калия в связующем канальце и собирательной трубке коры почек. При высоком содержании калия в пище эти структуры секретируют его, а при низком - секреция калия отсутствует. Помимо почек калий выводится желудочно-кишечным трактом и при потоотделении. При обычном уровне ежедневного потребления калия (50-100 ммоль/сут) приблизительно 10 % удаляются со стулом.
Главные регуляторы обмена кальция и фосфора в организме: витамин D, паратгормон и кальцитонин. Витамин D (в результате преобразований в печени образуется витамин D3, в почках — кальцитриол) увеличивает всасывание кальция в пищеварительном тракте и транспорт кальция и фосфора к костям. Паратгормон выделяется при снижении уровня кальция в сыворотке крови, высокий же уровень кальция тормозит образование паратгормона. Паратгормон способствует повышению содержания кальция и снижению концентрации фосфора в сыворотке крови. Кальций резорбируется из костей, также увеличивается его всасывание в пищеварительном тракте, а фосфор удаляется из организма с мочой. Паратгормон также необходим для образования активной формы витамина D в почках. Увеличение уровня кальция в сыворотке крови способствует выработке кальцитонина. В противоположность паратгормону он вызывает накопление кальция в костях и снижает его уровень в сыворотке крови, уменьшая образование активной формы витамина D в почках. Увеличивает выделение фосфора с мочой и снижает его уровень в сыворотке крови.
Первичный гиперальдостеронизм: симптомы, диагностика, лечение синдрома Конна

Врач гинеколог-эндокринолог. Стаж 23+ лет. Принимает в Университетской клинике в Санкт-Петербурге. Стоимость приема 2000 руб.
- Запись опубликована: 19.09.2022
- Reading time: 6 минут чтения
Гиперальдостеронизм — одна из наиболее распространенных причин вторичной гипертензии. Это патологическое состояние вызвано чрезмерной выработкой гормона альдостерона надпочечниками. При первичном гиперальдостеронизме увеличение секреции альдостерона связано с аномалиями, расположенными внутри самих надпочечников. При вторичном гиперальдостеронизме аномалии, вызывающие повышение концентрации альдостерона, возникают вне надпочечников.
Альдостерон влияет на поддержание натриевого и калиевого баланса. Избыток альдостерона вызывает задержку натрия и воды в организме, что приводит к повышению артериального давления. Повышенное кровяное давление вызывает повышенный риск инсульта, инфаркта, сердечной и почечной недостаточности.
Что такое гиперальдостеронизм
Первичный гиперальдостеронизм - это ренин-независимый синдром перепроизводства альдостерона, характеризующийся повышенной концентрацией альдостерона, снижением активности ренина плазмы, повышением артериального артериального давления, гипокалиемией и метаболическим алкалозом. Проблема связана с органической патологией надпочечников, например, аденомой или гиперплазией.
Классические симптомы первичного гиперальдостеронизма - гипертония и гипокалиемия, но уровень калия также может находиться в пределах нормы.
Патология была впервые описана в 1954 г. доктором Конном, который диагностировал у пациента резистентную гипертензию, гипокалиемию и альдостерон-продуцирующий аденому надпочечников. Поэтому гиперальдостеронизм, развившийся из-за аденомы, продуцирующей альдостерон, называется синдром Конна.
Статистика распространенности заболевания
Точная распространенность первичного гиперальдостеронизма неизвестна, но последние исследования показывают, что проблема затрагивает 10-13% случаев артериальной гипертензии. Наиболее частая причина - реципрокная гиперплазия надпочечников. Такая патология чаще диагностируется у мужчин после 50 лет. У женщин обычно выявляется альдостерома. Классический возраст больных - 30-30 лет.
Таблица 1. Наиболее распространенные причины и классификация первичного гиперальдостеронизма
| Причина ПГ | Случаи, % |
| Односторонняя или двусторонняя альдостерон-продуцирующая аденома надпочечников | до 40 |
| Идиопатический гиперальдостеронизм и гиперплазия обоих надпочечников | 25-60 |
| Первичная гиперплазия одного надпочечника | 2 |
| Альдостерон-продуцирующая карцинома | 1 |
| Семейный гиперальдостеронизм:Тип I - глюкокортикоид-зависимый гиперальдостеронизм, Тип II - односторонняя или двусторонняя альдостерон-продуцирующая аденома или идиопатический гиперальдостеронизм и гиперплазия обоих надпочечников | |
| Эктопическая альдостерон-продуцирующая аденома или карцинома (может присутствовать при наличии опухолей яичников и почек) |
Патофизиология ПГ
При первичном гиперальдостеронизме надпочечники автономно выделяют альдостерон, что приводит к ингибированию (подавлению) эндогенной системы ренина и ангиотензина. Альдостерон вызывает задержку соли в почках и потерю калия, результатом чего становится повышение содержания натрия в организме, что приводит к угнетению синтеза ренина в почках.
Прямое влияние альдостерона на дистальный нефрон приводит к задержке натрия и потере ионов водорода и калия, что приводит к развитию гипокалимического алкалоза, хотя концентрации калия в плазме могут сохраняться и существенно не снижаться или соответствовать норме у каждого второго больного.
Кроме того, альдостерон оказывает патофизиологическое действие на многие другие ткани, например, может привести к фиброзу сердца, дисфункции эндотелия сосудов и нефросклерозу.
Клинические признаки первичного гиперальдостеронизма
Наиболее важный первичный клинический признак ПГ - гипертония, обычно умеренная или высокая (>180/110 мм рт.ст.), устойчивая к обычному лечению, требующая применения 3-х и более препаратов, снижающих артериальное давление. Гипертония, вызванная альдостерон-продуцирующей аденомой надпочечников, характеризуется более тяжелой гипертензией и более частым выявлением гипокалиемии, а при идиопатической гиперплазии надпочечников клинические признаки могут быть менее выраженными. К сожалению, эти клинические признаки не считаются надежными в плане дифференциации альдостерон-продуцирующей аденомы от идиопатической гиперплазии надпочечников.
Повышенное артериальное давление может проявляться головными болями, нарушениями зрения, болями в груди. Плохо контролируемая гипертония может привести к опасным для жизни осложнениям, поэтому важно определить причину повышенного артериального давления и быстро начать лечение.
Второй признак первичного гиперальдостеронизма - гипокалиемия, обычно бессимптомная. Гипокалиемия может привести к аритмии, мышечной слабости, болезненным мышечным спазмам, повышенной жажде и усилению мочеиспускания. Ранее гипокалиемия считалась одним из наиболее важных клинических признаков ПГ, но затем исследования показали, что этот симптом есть менее, чем у 40% больных.
Иногда из-за выраженной гипокалиемии у пациентов могут наблюдаться:
- тетания - болезненные и непроизвольные сокращения мышц;
- миопатия - хронические нервные заболевания с первичным поражением мышц;
- полиурия - чрезмерная выработка мочи; - активный ночной диурез (гипокалиемический нефрогенный несахарный диабет).
Также возможна ассоциация с остеопорозом. Снижение концентрации калия в плазме крови сопровождается метаболическим алкалозом.
Пациенты с первичным гиперальдостеронизмом имеют более высокую частоту и смертность от сердечно-сосудистых заболеваний по сравнению с больными с первичной артериальной гипертензией с таким же увеличением артериального давления. Влияние гиперальдостеронизма на сердечно-сосудистую систему не зависит от концентрации калия в плазме. Пациенты с диагнозом гиперальдостеронизм имеют большие размеры левого желудочка. Из-за повышенного риска сердечно-сосудистых патологий повышается риск развития инсульта, инфаркта миокарда и фибрилляции предсердий.
Возможны и другие клинические признаки, такие как гипернатриемия (концентрация натрия в плазме крови у пациентов с ЛГ составляет 143-147 ммоль/л), гипомагниемия.
Что делать при появлении симптомов гиперальдостеронизма?
При появлении симптомов следует обратиться к эндокринологу, который после сбора анамнеза, осмотра и измерения артериального давления назначит анализы на концентрации электролитов в сыворотке крови. В случае выявления отклонений и подозрения на первичный гиперальдостеронизм он направит пациента на дальнейшую диагностику.
Диагностика первичного гиперальдостеронизма
В 2016 г. Европейское Общество эндокринологов обновило клинические рекомендации по диагностике и лечению первичного гиперальдостеронизма. Ранее рекомендовалось обследование на гиперальдостеронизм всем пациентам с умеренной и тяжелой гипертензией (>160/100 мм рт.ст.), независимо от уровня калия в крови.
Новые руководящие принципы расширили этот список. В него включили больных с постоянно повышенным артериальным давлением (>150 мм рт.ст. (систолическое) и >100 мм рт.ст. (диастолическое)) и пациентов с гипертонией и апноэ сна.
Рекомендуемый в Европе алгоритм диагностики первичного гиперальдостеронизма включает 4 этапа.
Таблица 2. Этапы диагностики ЛГ первичного гиперальдостеронизма
| Этап | Диагностика |
| 1 | Выявление симптомов, дающих основание подозревать гиперальдостеронизм. Пациента нужно обследовать, если у него есть хотя бы 1 из 5 состояний (см. таблицу 3) |
| 2 | Первичный скрининговый тест - изучаются концентрация альдостерона в плазме и прямая концентрация ренина, затем рассчитывается отношение альдостерона к ренину |
| 3 | Анализы для подтверждения диагноза |
| 4 | Определение подтипа патологии |
Таблица 3. Признаки, требующие диагностики первичного гиперальдостеронизма
| Состояние | |
| 1 | Лечение устойчивой артериальной гипертензии (АКС >140/90 мм рт.ст. при лечении 3 группами антигипертензивных препаратов) |
| 2 | Артериальная гипертензия и спонтанная или мочегонная гипокалиемия |
| 3 | Артериальная гипертензия и эпизодиома |
| 4 | Раннее начало артериальной гипертензии и/или инсульта ( |
| 5 | Все пациенты с артериальной гипертензией с родственниками первой линии с диагнозом гиперальдостеронизм |
Результаты исследования могут быть искажены многими факторами и лекарствами, поэтому анализы проводятся в стандартизированных условиях. Перед проведением лабораторных исследований необходимо скорректировать уровень калия и натрия, прекратить прием препаратов (временная отмена некоторых препаратов, обычно за 4-6 недель до теста), способных повлиять на результаты исследования. В их числе:
- спиронолактон;
- ингибиторы ангиотензинпревращающего фермента;
- блокаторы рецепторов ангиотензина II;
- ингибиторы ренина, бета-адреноблокаторы; ;
- дигидропиридины;
- агонисты центрального действия α-2 (клонидин, α-метилдопа); .
Для коррекции артериальной гипертензии препаратами с минимальным воздействием на соотношение ПАК/ТРК рекомендуемый препарат первого выбора - не дигидропиридиновый блокатор кальциевых каналов, например, верапамил. При персистенции неконтролируемой гипертензии могут добавляться альфа-адреноблокаторы, например, доксазозин.
У пациентов с первичным альдостеронизмом обычно наблюдается снижение концентрации калия в крови, повышение концентрации альдостерона, снижение активности ренина плазмы и повышение альдостерон-ренинового индекса, обусловленное коэффициентом двух предыдущих значений. Первичный гиперальдостеронизм подозревается, если концентрация альдостерона в плазме (ng/dl)/прямая концентрация ренина (ng/l) составляет >5,7. Пределы соотношения могут варьироваться в зависимости от системы единиц измерения, используемой в лабораториях.
Обнаружив вышеперечисленные отклонения, врач примет решение о необходимости проведения дальнейших тестов, оценивающих гормональную функцию надпочечников, так называемых функциональных проб.
Третий этап представляет собой тест на подтверждение диагноза, направленный на подтверждение автономной выработки альдостерона. Рекомендуется проводить 1 из 4 проб: с пероральным прием соли, с 0,9% раствором NaCl, супрессионный тест на флудрокортизон, провокацию каптоприлом. Наиболее часто используемый тест с NaCl. Концентрация альдостерона после введения NaCl не снижается ниже 10 нг/дл, а у здоровых людей составляет менее 5 нг/дл.
Пациентам с неконтролируемой гипертензией, сердечной недостаточностью, почечной недостаточностью, аритмией, гипокалиемией рекомендуется пройти тест с провокацией каптоприлом, измеряющим изменение уровней ренина в плазме в ответ на препарат каптоприл.
После подтверждения диагноза проводится компьютерная томография (КТ) органов брюшной полости для определения подтипа патологии. КТ проводится для определения причины гиперальдостеронизма - аденомы надпочечников, гиперплазии или карциномы (подозревается при обнаружении односторонней опухоли >4 см). Магнитно-резонансная томография (МРТ) не имеет преимуществ перед КТ, поэтому не рекомендуется в качестве стандартного метода обследования. Чувствительность КТ - 78%, специфичность - 75%.
Данные КТ надпочечников определяют дальнейшую тактику обследования и лечения. Например, если при КТ обнаружен односторонний гиподенсный узел (участок, отличающийся по плотности или цвету и четкими границами на изображении) и пациенту более 35 лет, следующий диагностический этап - исследование венозной крови надпочечников. Для уточнения того, где происходит перепроизводство альдостерона, проводят катетеризацию надпочечниковых вен и тест на венозную кровь надпочечников. Это золотой стандарт оценки латерализации первичного гиперальдостеронизма, с чувствительностью - 95% и специфичностью - 100%.
Если патология выявлена у больного в возрасте до 20 лет с положительным семейным анамнезом или инсультом до 40 лет, необходима консультация генетика.
Лечение первичного гиперальдостеронизма
Цель лечения гиперальдостеронизма - нормализация артериального давления и концентрации калия в крови.
Тактика лечения зависит от причины патологии. При одностороннем гиперальдостеронизме, когда причина первичного альдостеронизма - опухоль надпочечников, секретирующая альдостерон, лечение выбора заключается в хирургическом удалении надпочечников вместе с опухолью лапароскопическим методом - лапароскопическая адреналэктомия. Важная предоперационная подготовка - коррекция гипокалиемии и гипертонической болезни. Лекарства первого выбора - антагонисты минералкортикоидных рецепторов. Рекомендуемая продолжительность лечения - до 5 недель.
После операции необходимо наблюдать за уровнем калия, так как из-за временного гипоальдостеронизма, вызванного контраллатеральной супрессией надпочечников, может возникнуть гиперкалиемия. По возможности следует уменьшить дозы антигипертензивных препаратов.
На следующий день после операции следует проверить активность альдостерона и ренина в плазме крови - это ранний биохимический показатель операционного успеха.
Первые несколько недель после операции не следует уменьшать количество поваренной соли в еде.
Важно понимать, что операция помогает снять давление не всем больным. После хирургического лечения артериальная гипертензия сохраняется примерно в половине случаев.
Пациентам после односторонней адреналэктомии требуется длительное наблюдение. Каждые 6-12 месяцев придется сдавать анализы на альдостерон, ренин, электролиты, и ежедневно измерять давление. Через год после операции нужно сделать КТ органов брюшной полости с последующим повторением КТ каждые 1-3 года.
При диагностике двусторонней гиперплазии надпочечников терапия включает фармакологическое лечение и модификацию образа жизни (рекомендуется поддерживать нормальную массу тела, умеренные физические нагрузки и диету с ограничением потребления соли
Для медикаментозного лечения используются диуретики, которые снижают действие альдостерона и повышают концентрацию калия в крови (спиронолактон и эплеренон). Эти препараты также применяются у пациентов с аденомой надпочечников, секретирующих альдостерон перед операцией или в случае противопоказаний к процедуре.
В случае семейного гиперальдостеронизма также назначается медикаментозное лечение.
- Антагонисты минералокортикоидных рецепторов. Это препараты первого выбора. Первым назначается спиронолактон. Начальная доза 12,5-25 мг 1 к./сут, постепенно дозу увеличивают до 100 мг. При персистенции неконтролируемого артериального давления, гипокалиемии доза может быть увеличена до 400 мг. Основные нежелательные эффекты после приема этого препарата: у мужчин - гинекомастия, у женщин - нарушения менструального цикла, болезненность груди. При плохой переносимости спиронолактона назначают эплеренон, не обладающий антиандрогенным действием прогестерона. Начальная доза - 25 мг 2 к./сут, стандартная доза - 50-200 мг/сут.
- Калийсберегающие диуретики. Например, триамтерен или амилорид. Препараты второй линии назначаются, когда не переносятся антагонисты минералокортикоидных рецепторов. В большинстве случаев требуется повышенная доза амилорида (до 40 мг/сут). При его приеме необходимо контролировать уровень калия в крови.
- Блокаторы кальциевых каналов. Например, нифедипин. Могут быть полезны, потому что, блокируя диффузию кальция в адренокортикальную клетку, они уменьшают выработку альдостерона. При наследственном гиперальдостеронизме требуется длительное наблюдение за больными - каждые 3-6 месяцев нужно проводить анализы на концентрацию калия, креатинина в крови, ежедневно измерять давление, при наличии опухолей и др. изменений повторять КТ надпочечников каждые 3-4 года.
- Глюкокортикоиды. Могут назначаться небольшие дозы для лечения глюкокортикоид-зависимого гиперальдостеронизма. Например, может быть выписан дексаметазон 0,25-0,5 мг перед сном.
При лечении глюкокортикоидами необходимо каждые 2-3 года проходить обследование на минеральную плотность костей на предмет возможного остеопороза.
Можно ли полностью вылечить гиперальдостеронизм?
Хирургическое лечение альдостеронсекрецирующей аденомы приводит к полному разрешению симптомов гиперальдостеронизма у 35-70% больных. Пациентам с двусторонней гиперплазией надпочечников рекомендуется постоянно соблюдать ограниченную солью диету и поддерживать пожизненное фармакологическое лечение, направленное на нормализацию концентрации калия в крови и контроль артериального давления. Только хорошо контролируемое артериальное давление позволит избежать органных осложнений (инсульт, инфаркт).
Что нужно сделать после окончания лечения гиперальдостеронизма?
После хирургического лечения альдостерон-секретирующей аденомы надпочечников некоторым пациентам требуется продолжение лечения гипертонической болезни. После хирургического лечения требуется оценка концентрации кортизола в крови, что обусловлено возможным риском развития надпочечниковой недостаточности. Рекомендуется регулярный контроль артериального давления.
Также нужно вести здоровый образ жизни, положительно влияющий на контроль артериального давления, в том числе: снижение соли в рационе, поддержание здоровой массы тела, регулярные физические упражнения, ограничение количества потребляемого алкоголя и отказ от курения.
Что делать, чтобы не заболеть гиперальдостеронизмом?
Способов предотвратить возникновение первичного гиперальдостеронизма пока не разработано. Однако ранняя диагностика и применение соответствующего лечения, направленного на надлежащий контроль артериального давления, позволяет уменьшить сердечно-сосудистые осложнения и, таким образом, снизить смертность.
Выводы
Первичный гиперальдостеронизм приводит более чем к каждому десятому случаю гипертонии - это одна из самых распространенных причин вторичной гипертонии. У пациентов с гиперальдостеронизмом заболеваемость и смертность от сердечно-сосудистых заболеваний выше по сравнению с пациентами с первичной артериальной гипертензией, которые имеют такой же порог артериального давления.
Поэтому первичный гиперальдостеронизм следует подозревать, если больной соответствует хотя бы 1 из 5 критериев. Перед проведением скринингового теста необходимо скорректировать уровень калия и натрия в крови, прекратить прием лекарств, способных повлиять на результаты исследования. После подтверждения диагноза проводится КТ органов брюшной полости, данные которой определяют дальнейшую тактику обследования и лечения.
Гиперальдостеронизм - симптомы и лечение
Что такое гиперальдостеронизм? Причины возникновения, диагностику и методы лечения разберем в статье доктора Матвеева М. А., эндокринолога со стажем в 11 лет.
Над статьей доктора Матвеева М. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Гиперальдостеронизм — это синдром, при котором кора надпочечников вырабатывает повышенное количество гормона альдостерона. Он сопровождается развитием артериальной гипертензии и поражением сердечно-сосудистой системы [1] . Нередко артериальная гипертензия, развившаяся на фоне повышенного уровня альдостерона, носит злокачественный характер: крайне плохо поддаётся медикаментозной коррекции и приводит к ранним и серьёзным осложнениям, таким как ранний инсульт, инфаркт миокарда, фибрилляция предсердий, внезапная сердечная смерть и др.
Гиперальдостеронизм является одной из самых частых причин артериальной гипертензии. По некоторым данным, он выявляется в 15-20 % всех случаев [5] .
В силу стёртой клинической картины данный синдром диагностируется редко. Однако его выявление имеет огромное значение как из-за своей распространённости, так и в связи с возможным своевременным лечением причины артериальной гипертензии и предотвращением тяжёлых сердечно-сосудистых осложнений, улучшая прогноз и качество жизни пациентов.
Кора надпочечников выделяет большое количество альдостерона либо автономно, либо в ответ на стимулы вне надпочечников.
Причинами автономной секреции альдостерона являются заболевания надпочечников:
- аденома (доброкачественная опухоль) надпочечника, продуцирующая альдостерон (синдром Крона);
- двусторонний идиопатический гиперальдостеронизм (точна причина неизвестна);
- односторонняя гиперплазия надпочечника (развивается в результате микро- или макронодулярного разрастания клубочковой зоны коры одного надпочечника);
- семейный гиперальдостеронизм (наследственное заболевание, встречается крайне редко);
- карцинома (злокачественная опухоль) надпочечника, вырабатывающая альдостерон.
Самой частой причиной гиперальдостеронизма является аденома (обычно односторонняя), состоящая из клеток клубочковой зоны. У детей аденомы встречаются редко. Как правило, это состояние у них вызвано раком или гиперплазией (разрастанием) одного надпочечника. У пожилых пациентов аденома встречается реже. Она связана с двусторонней гиперплазией надпочечников [4] [10] .
Вненадпочечниковыми причинами синдрома являются:
- стеноз (сужение) почечной артерии, приводящий к снижению почечного кровотока и, как следствие, гиперсекреции альдостерона;
- почечная вазоконстрикция (сужение любых сосудов почки), в том числе из-за опухолевого процесса;
- застойная сердечная недостаточность, цирроз печени с асцитом (скоплением жидкости в брюшной полости) и др., т. е. состояния, которые приводят к повышению альдостерона за счёт снижения печеночного кровотока и скорости метаболизма альдостерона [10] .
Крайне редко возможно развитие псевдогиперальдостеронизма — артериальной гипертензии и низкого уровня калия в крови, имитирующих симптомы гиперальдостеронизма. Причиной тому является существенная передозировка солодки или жевательного табака, которые влияют на метаболизм гормонов в надпочечниках.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гиперальдостеронизма
Клинические проявления гиперальдостеронизма чаще встречаются в возрасте 30-50 лет, однако описаны случаи выявления синдрома и в детском возрасте [1] .
Основным и постоянным симптомом гиперальдостеронизма является артериальная гипертензия. В 10-15 % она носит злокачественный характер [3] . Клинически гипертония проявляется головокружением, головными болями, мельканием "мушек" перед глазами, перебоями в работе сердца, в особо тяжёлых случаях — даже временной потерей зрения. Систолическое артериальное давление достигает 200-240 мм рт. ст.
Обычно гипертония при данном синдроме устойчива к препаратам, нормализующим давление. Однако этот признак гиперальдостеронизма далеко не всегда становится определяющим, поэтому его отсутствие не исключает диагноз и может привести к диагностической ошибке. Течение артериальной гипертензии при наличии синдрома может быть умеренным и даже мягким, поддающимся коррекции небольшими дозами препаратов. В редких случаях артериальная гипертензия носит кризовый характер, что требует дифференциальной диагностики и тщательного клинического разбора.
Второй признак гиперальдостеронизма — нейромышечный синдром. Он встречается довольно часто. Его основные проявления включают мышечную слабость, судороги, ползанье "мурашек" по ногам, особенно в ночные часы. В тяжёлых случаях могут быть временные параличи, которые внезапно начинаются и исчезают. Они могут длиться от нескольких минут до суток [3] [4] .
Третий признак гиперальдостеронизма, встречающийся не менее чем в 50-70 % случаев, — почечный синдром. Он представлен, как правило, невыраженной жаждой и учащённым мочеиспусканием (часто в ночное время).
Выраженность всех вышеперечисленных проявлений напрямую связана с концентрацией альдостерона: чем выше уровень этого гормона, тем выраженнее и тяжелее проявления гиперальдостеронизма.
Патогенез гиперальдостеронизма
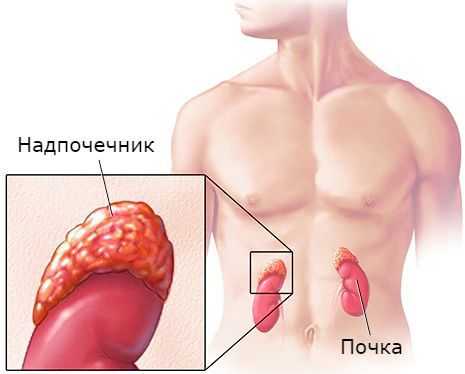
Надпочечники — это парные эндокринные железы, расположенные над верхними полюсами почек. Они являются жизненно необходимой структурой. Так, удаление надпочечников у экспериментальных животных приводило к смерти через несколько суток [2] .
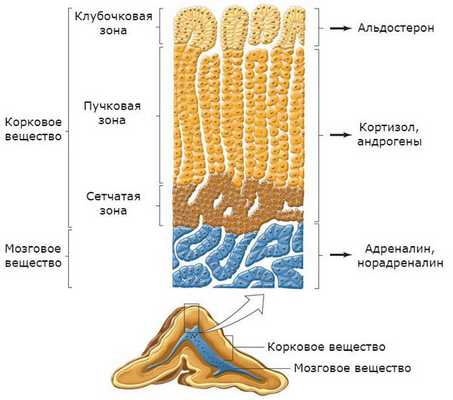
Надпочечники состоят из коркового и мозгового вещества. В корковом веществе, которое составляет до 90 % всей ткани надпочечника, выделяют три зоны:
- клубочковая;
- пучковая;
- сетчатая.
В клубочковой зоне синтезируются минералокортикоиды — подкласс кортикостероидных гормонов коры надпочечников, к коим относится альдостерон. К ней прилежит пучковая зона, вырабатывающая глюкокортикоиды (кортизол). Самая внутренняя зона — сетчатая — секретирует половые гормоны (андрогены) [2] .
Главным органом-мишенью для альдостерона являются почки. Именно там данный гормон усиливает всасывание натрия, стимулируя выделение фермента Na + /K + АТФазы, таким образом повышая его уровень в плазме крови. Второй эффект воздействия альдостерона — выделение почками калия, снижая его концентрацию в плазме крови.
При гиперальдостеронизме, т.е. при повышенной альдостерона, натрия в плазме крови становится чрезмерно много. Это приводит к повышению осмотического давления плазмы, задержке жидкости, гиперволемию (увеличение объёма жидкости или крови в сосудистом русле), в связи с чем развивается артериальная гипертензия.
Дополнительно высокий уровень натрия повышает чувствительность стенок сосудов к их утолщению, воздействию веществ, повышающих артериальное давление (адреналин, серотонин, кальций и др.) и развитию фиброза (разрастанию и рубцеванию) вокруг сосудов. Низкий уровень калия в крови в свою очередь вызывает поражение почечных канальцев, что приводит к снижению концентрационной функции почек. В результате этого довольно быстро развивается полиурия (увеличение объёма выделяемой мочи), жажда и никтурия (ночное мочеиспускание). Также при низком уровне калия нарушается нейромышечная проводимость и pH крови [1] [3] . Сходным образом альдостерон влияет на потовые, слюнные и кишечные железы [2] .
Из всего выше сказанного можно сделать вывод о том, что основная жизненно важная функция альдостерона — это поддержание физиологической осмолярности внутренней среды, т. е. баланса суммарной концентрации растворённых частиц (натрия, калия, глюкозы, мочевины, белка).
Классификация и стадии развития гиперальдостеронизма
В зависимости от причин гиперсекреции альдостерона выделяют первичный и вторичный гиперальдостеронизм. Подавляющее большинство случаев данного синдрома являются именно первичными.
Первичный гиперальдостеронизм — это повышенная секреция альдостерона, независящая от гормональной системы, которая контролирует объём крови и кровяное давление. Он возникает из-за заболеваний надпочечников.
Вторичный гиперальдостеронизм — это повышенная секреция альдостерона, вызванная вненадпочечниковыми стимулами (заболеваниями почек, застойной сердечной недостаточностью).
Отличительные клинические признаки этих двух типов гиперальдостеронизма указаны в таблице ниже [10] .
Осложнения гиперальдостеронизма
У пациентов с гиперальдостеронизмом крайне часто наступают сердечно-сосудистые поражения и смерть в сравнении с людьми с аналогичной степенью артериальной гипертензии, но вызванной другими причинами [11] [12] . Такие пациенты имеют очень высокий риск развития инфаркта и нарушение ритма сердца, в частности фибрилляции предсердий, что потенциально является фатальным состоянием. Риск внезапной сердечной смерти у пациентов с гиперальдостеронизмом увеличивается в 10-12 раз [13] .
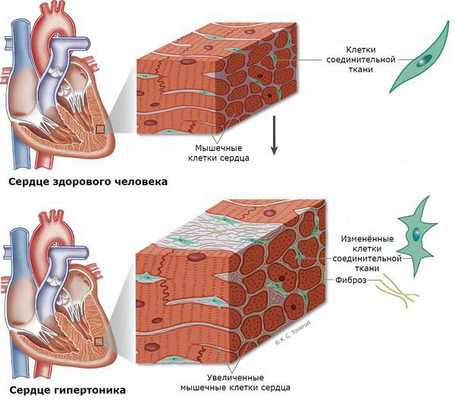
Нередко у пациентов выявляются вызванные гиперальдостеронизмом кардиосклероз, гипертрофия левого желудочка и дисфункция эндотелия (внутреннего слоя сосудов) [3] . Это объясняется прямым повреждающим влиянием альдостерона на миокард и сосудистую стенку. Доказано, что увеличение массы миокарда при гиперальдостеронизме развивается раньше и достигает больших размеров [1] .
При развитии почечного синдрома (из-за интенсивного выведения почками калия) нарушается выведение ионов водорода. Это приводит к защелачиванию мочи и предрасполагает к развитию пиелита и пиелонефрита (воспаления почек), микроальбуминурии и протеинурии (выделения повышенного уровня альбумина и белка с мочой). У 15-20 % больных развивается почечная недостаточность с необратимыми изменениями работы почек. В 60 % случаев выявляется поликистоз почек [12] [13] .
Неотложным состоянием, связанным с гиперальдостеронизмом, является гипертонический криз. Его клинические проявления могут ничем не отличаться от обычных гипертонических кризов, проявляющихся головными болями, тошнотой, болями в области сердца, одышкой и т. д. Заподозрить нетипичный гипертонический криз в такой ситуации поможет наличие брадикардии (редкого пульса) и отсутствие периферических отёков. Эти данные в корне изменят тактику лечения и направят диагностический поиск в правильном направлении.
Диагностика гиперальдостеронизма
Для того чтобы не пропустить гиперальдостеронизм, вначале крайне важно выделить основные факторы риска, которые помогут заподозрить это заболевание. К ним относятся:
- артериальная гипертония II степени, т. е. стабильное повышение систолического (верхнего) артериального давления более 160/179 мм рт. ст., диастолического (нижнего) — более 100/109 мм рт. ст.;
- артериальная гипертония, устойчивая и/или плохо контролируемая препаратами (хотя этот признак далеко не всегда указывает на патологию);
- сочетание артериальной гипертонии с низким уровнем калия в крови (независимо от приёма мочегонных средств);
- артериальная гипертония и случайно выявленное (при УЗИ и/или КТ) образование надпочечника;
- отягощённый семейный анамнез: развитие артериальной гипертонии и/или острых сердечно-сосудистых катастроф до 40 лет, а также родственники, у которых уже был диагностирован гиперальдостеронизм [1][5] .
Следующий этап диагностики — лабораторное подтверждение. Для этого исследуется альдостерон-рениновое соотношение (АРС). Данное исследование является наиболее надёжным, информативным и доступным. Оно должно проводиться в ранние утренние часы: в идеале не позднее чем через два часа после пробуждения. Перед забором крови необходимо спокойно посидеть 5-10 минут.
ВАЖНО: некоторые препараты могут повлиять на концентрацию альдостерона и активность ренина плазмы, что, в свою очередь, изменит АРС. Поэтому за две недели до сдачи данного анализа важно отменить такие препараты, как спиронолактон, эплеренон, триамтерен, тиазидные диуретики, препараты из группы ингибиторов АПФ, БРА (блокаторов рецепторов ангиотензина) и другие. Врач должен проинформировать об этом пациента и временно назначить другую схему лечения гипертонии.
При положительном АРС необходимо провести подтверждающий тест с физиологическим раствором. Он проводится в условиях стационара, т. к. имеет ряд ограничений и требует исследование уровня альдостерона, калия и кортизола исходно и после 4-часового вливания двух литров физиологического раствора. В норме в ответ на большое количество вводимой жидкости выработка альдостерона подавляется, однако при гиперальдостеронизме подавить гормон таким способом не удаётся.
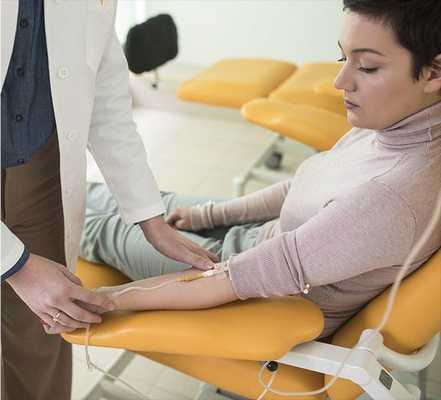
Низкий уровень калия в крови отмечается лишь в 40 % случаев синдрома, поэтому он не может быть надёжным критерием диагностики. А вот щелочная реакция мочи (вследствие повышенного выведения калия почками) является довольно характерным признаком патологии.
При подозрении на семейные формы гиперальдостеронизма проводится генетическое типирование (исследование на предрасположенность) с консультацией генетика [3] [6] .
Третий этап диагностики — топическая диагностика. Она направлена на поиски очага заболевания. Для этого используются различные способы визуализации внутренних органов.
УЗИ надпочечников — низкочувствительный метод диагностики. Предпочтительнее проводить КТ: она помогает выявить как макро- и микроаденомы надпочечников, так и утолщения ножек надпочечников, гиперплазии и другие изменения [14] .
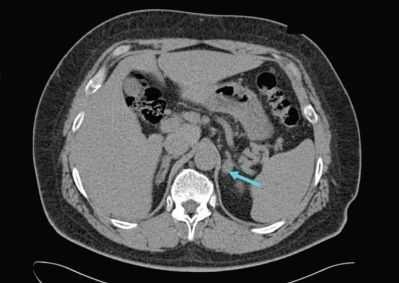
Для уточнения формы гиперальдостеронизма (одностороннего и двустороннего поражения) проводится селективный забор крови из вен надпочечников в специализированных центрах [9] . Это исследование эффективно снижает риск необоснованного удаления надпочечника только по данным КТ [4] .
Лечение гиперальдостеронизма
Оперативное лечение
Методом выбора при аденоме надпочечника, синтезирующей альдостерон, и односторонней гиперплазии надпочечника является эндоскопическая адреналэктомия — удаление одного или двух надпочечников через небольшие разрезы.
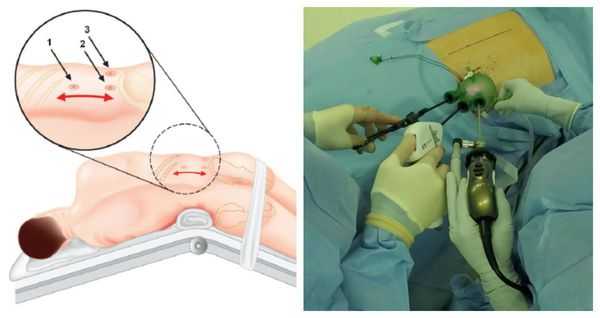
Данная операция выравнивает концентрацию калия в крови и улучшает течение артериальной гипертонии почти у 100 % больных. Полное излечение без использования антигипертензивной терапии достигается примерно у 50 %, шанс контроля артериального давления на фоне адекватной терапии увеличивается до 77 % [1] . В ряде исследований продемонстрировано уменьшение массы миокарда левого желудочка и устранение альбуминурии, что значительно повышает качество жизни таких пациентов.
Однако если гиперальдостеронизм не был диагностирован долгое время, то и после операции артериальная гипертония может сохраняться, а развившиеся сосудистые осложнения могут стать необратимыми, как и поражение почек. Поэтому крайне важно выявлять и лечить гиперальдостеронизм как можно раньше [7] .
Противопоказания к удалению надпочечника:
- возраст пациента;
- небольшая ожидаемая продолжительность жизни;
- тяжёлая сопутствующая патология;
- двусторонняя гиперплазия надпочечников (когда нет возможности провести селективный забор крови из вен надпочечников);
- гормонально-неактивная опухоль надпочечника, ошибочно принятая за источник выработки альдостерона.
Консервативное лечение
При наличии этих противопоказаний, высоком риске операции или отказе от хирургического вмешательства показано консервативное лечение специальными препаратами — антагонистами минералокортикоидных рецепторов (АМКР). Они эффективно снижают артериальное давление и защищают органы от избытка минералокортикоидов [7] [12] .
К этой группе препаратов относится калийсберегающий диуретик спиронолактон, который блокирует минералокортикоидные рецепторы и препятствует развитию фиброза миокарда, связанного с альдостероном. Однако он обладает рядом побочных эффектов, воздействуя ещё и на рецепторы андрогенов и прогестерона: может привести к гинекомастии у мужчин, снижению либидо, вагинальным кровотечениям у женщин. Все эти эффекты зависят от дозы препарата: чем больше доза препарата и длительность его применения, тем побочные эффекты более выражены.
Также существует относительно новый селективный препарат из группы АМКР — эплеренон. Он не воздействует на стероидные рецепторы в отличие от его предшественника, поэтому число неблагоприятных побочных эффектов будет меньше [9] .
При двусторонней гиперпродукции альдостерона показано длительное консервативное лечение. При вторичном гиперальдостеронизме следует лечить основное заболевание и корректировать артериальную гипертонию также с помощью препаратов группы АМКР [12] .
Прогноз. Профилактика
Выявление и адекватное лечение гиперальдостеронизма в большинстве случаев позволяет устранить артериальную гипертонию и связанные с ней осложнения или значительно смягчить её течение. Причём чем раньше синдром будет диагностирован и пролечен, тем благоприятнее прогноз: улучшается качество жизни, снижается вероятность инвалидизации и фатальных исходов [4] . Рецидивы после своевременной односторонней адреналэктомии, выполненной по показаниям, не возникают.
При запоздалой диагностике гипертония и осложнения могут сохраняться даже после терапии.
Гиперальдостеронизм может довольно долго протекать только с симптомами гипертонии.
Постоянно высокие цифры артериального давления (более 200/120 мм рт. ст.), нечувствительность к антигипертензивным препаратам, низкий уровень калия в крови — далеко не обязательные признаки синдрома. А ведь именно на это, зачастую, ориентируются врачи, чтобы заподозрить заболевание, "пропуская" гиперальдостеронизм с относительно "мягким" течением на ранних этапах.
Чтобы решить эту проблему, врачам, которые работают с пациентами с артериальной гипертензией, необходимо выявлять группы высокого риска и прицельно обследовать их на предмет наличия гиперальдостеронизма.
Читайте также:
