Внесосудистая и внутрисосудистая пурпуры у ребенка
Добавил пользователь Skiper Обновлено: 21.01.2026
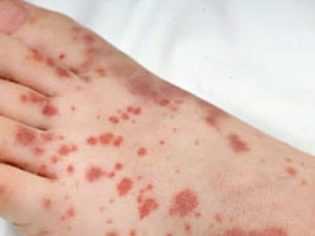
Петехии - точечные геморрагии, имеющие округлую форму и возникающие при разрыве мелких кровеносных сосудов под кожей. Красные, пурпурные и фиолетовые пятна появляются в результате выхода эритроцитов из кровеносного русла в межтканевое пространство. Петехии — как крошечные ушибы, достигающие в диаметре 1 или 2 мм. Они не пальпируются и не выделяются над поверхностью кожи. Петехиальные кровоизлияния бывают единичными и множественными. Одномоментно появляется сразу несколько плоских пятен, которые не изменяют свой цвет и не исчезают при нажатии пальцем или растягивании кожи.
Петехии — симптом целого ряда патологий, среди которых преобладают болезни крови, системные аутоиммунные заболевания, некоторые инфекции.
У здоровых людей высыпания могут появляться из-за чрезмерного напряжения. Со временем пятнышки бледнеют и исчезают, оставляя после себя небольшую пигментацию.Локализация петехий различна: кожа рук, ног, туловища, лица, слизистая оболочка ротовой полости, конъюнктива глаз.
Этиология
Перед тем, как приступить к лечению петехий, необходимо выявить и исключить причины их появления!
Физиологические причины
- Наиболее распространенной причиной образования петехиальной сыпи у здоровых людей является травма — сильное физическое воздействие на кожу. Капилляры разрываются, кровь вытекает под кожу. У взрослых петехии чаще образуются после удара, а у детей - во время игр или падения. На слизистой оболочке полости рта геморрагии появляются при употреблении твердой пищи.
- Чрезмерное перенапряжение, возникающее во время приступов кашля, эмоционального плача или рвоты, может привести к разрыву капилляров возле глаз и на других участках лица.
- Нередко петехии можно увидеть после родов у женщины и новорожденного. Сильное перенапряжение и стресс оказывают негативное воздействие на кожу матери и ребенка.
- Единичные петехии появляются во время занятий некоторыми видами спорта — тяжелой атлетикой.
- Тесная и неудобная одежда — причина появления петехий.
- Петехии могут появиться при натягивании жгута или в следствие повышенного давления на мягкие ткани. Точечные геморрагии в таких случаях не представляют особой опасности для здоровья и бесследно исчезают через несколько дней.
- Старение кожи.
Патологические причины
В результате большинства гематологических и аутоиммунных заболеваний нарушаются процессы образования и функционирования тромбоцитов, что клинически проявляется появлением на коже петехий. Диссеминированная внутрисосудистая коагуляция также является причиной геморрагической сыпи бактериального происхождения.
- Аутоиммунные заболевания — СКВ, склеродермия, спондилоартрит, тромбоцитопеническая пурпура, геморрагический васкулит;

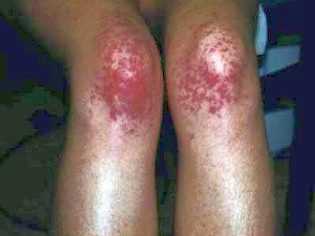
примеры петихий при тромбоцитопенической пурпуре, характерной для детей
Патогенез
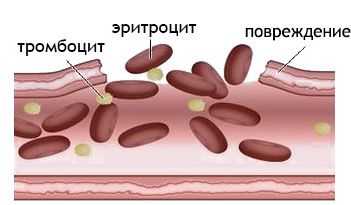
В результате травматического повреждения капилляров тромбоциты собираются вместе, чтобы помочь крови свернуться. Группы тромбоцитов вступают в реакцию с факторами свертывающей системы крови, кровь застаивается в пораженном месте, образуется тромб. У лиц с имеющимися в организме нарушениями свертывающая система крови работает менее эффективно, на коже появляются мелкие кровоподтеки — петехии.
- Первичные петехии — это мелкие точки, которые вначале имеют пурпурную или голубовато-черную окраску, а в последующем изменяют цвет до коричневого или желто-коричневого. Это объясняется образованием гемосидерина в тканях. Постепенно очертания петехий становятся размытыми, а их цвет тускнеет.
- Механизм образования вторичных петехий — просачивание клеток крови в смежные ткани. Такие геморрагии не проходят самостоятельно. Больные нуждаются в оперативном вмешательстве.
Некоторые инфекционные заболевания проявляются появлением петехий на коже. Особенно это касается детей с еще неокрепшим иммунитетом. У ребенка инфекционный синдром проявляется жаром, тахикардией, одышкой. Патогенные микроорганизмы вырабатывают токсины, которые поражают стенки сосудов. Подкожные кровоизлияния или геморрагическая сыпь — характерный признак сепсиса. В тяжелых случаях сыпь быстро распространяется по всему телу, возникают обморочные, судорожные и бредовые состояния.
При системных заболеваниях собственные сосуды воспринимаются организмом как чужеродные. Иммунная система вырабатывает антитела, образуются иммунные комплексы, которые циркулируют в крови, оседают на стенках сосудов и поражают их. У больных появляется общая и специфическая симптоматика: одышка, гипергидроз, кардиалгия, боль в мышцах и суставах.
Если петехии сопровождаются недомоганием и лихорадкой, распространяются по всему телу, приобретая большие размеры, и выглядят, как синяки, необходимо немедленно обратиться к врачу.
Основные виды петехий при различных заболеваниях
Менингит
Менингит проявляется геморрагической сыпью, элементы которой имеют звездчатую форму и бледный цвет. Это ранний симптом заболевания, появляющийся в первые часы и сутки и очень быстро распространяющийся по телу. Петехии локализуются на бедрах, голенях, ягодицах, стопах, нижней части живота. Они имеют в центре везикулу и часто сливаются друг с другом, образуя обширные экхимозы, которые в дальнейшем часто подвергаются некрозу.
Гонорея
При гонорее высыпания локализуются на дистальных отделах конечностей, над крупными суставами. Они напоминают пустулы с геморрагическим содержимым и сочетаются с характерной клинической симптоматикой — признаками поражения мочеполового аппарата, аноректальной области и глотки.
Стафилококковая инфекция
Стафилококковая инфекция проявляется гнойными петехиями, при исследовании которых обнаруживают скопления грамположительных кокков. При стафилококковом сепсисе повышается проницаемость сосудистых стенок под воздействием микробных токсинов. На коже, слизистой рта и склерах появляются геморрагии в виде точечных петехий.
Аутоиммунные заболевания, васкулиты
При аутоиммунных заболеваниях возникает петехиальная экзантема на руках и ногах, а спустя 2—4 дня на ней появляются множественные петехии. Их появление сопровождается признаками интоксикационного синдрома: жаром, малгией, артралгией, недомоганием. Петехии спустя несколько дней исчезают, а на их месте остаются пигментированные участки и зоны шелушения.
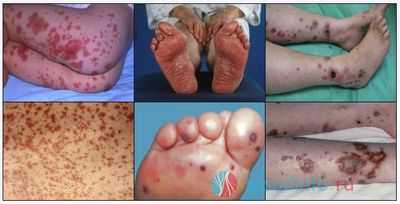
геморрагии при различных васкулитах
Петехиальная сыпь при геморрагическом васкулите сопровождается поражением суставов и болью в животе. Чаще всего воспаляются крупные суставы ног — голеностопный или коленный. Боль в эпигастрии носит умеренный характер без явных признаков диспепсии. В тяжелых случаях внезапная, приступообразная, напоминающая кишечную колику боль в животе сопровождается диареей, рвотой, лихорадкой.
Болезнь Шамберга
Болезнь Шамберга — гемосидероз кожи, возникающий из-за аутоиммунного воспаления кожных капилляров. На коже больных появляются мелкие точки, как от укола иглой. Сначала они имеют бурую или коричневую окраску, а затем светлеют и исчезают на некоторое время. Высыпания располагаются на теле симметрично, но морфологически они разнообразны. Это связано с одновременным возникновением на коже свежих и застарелых элементов. Эта болезнь имеет доброкачественное течение, поскольку поражаются только кожные капилляры. Подвержены патологии в большей степени мужчины. Петехии располагаются на бедрах и голенях, имеют различный размер и неровный контур.
Энтеровирусная инфекция
Энтеровирусная инфекция проявляется лихорадкой, болью в мышцах, воспалением мягких мозговых оболочек, герпетической ангиной, желудочно-кишечной дисфункцией. После появления петехиальной сыпи на коже состояние больных заметно улучшается, температура тела нормализуется. Сыпь появляется в течение одного дня. Она располагается на лице и туловище и исчезает бесследно к концу вторых суток.
Диагностика заболеваний, проявляющихся петехиальной сыпью, включает сбор жалоб, опрос больного, проведение лабораторных испытаний и диагностических тестов:
- Коагулограмма,
- Общий анализ крови,
- Биопсия костного мозга.
Диагностика и лечение
Петехии, возникающие спонтанно и не сопровождающие клинической симптоматикой, проходят самостоятельно и не требуют специального лечения. Но несмотря на это, лицам, не имеющим каких-либо заболеваний, необходимо убедиться в отсутствии скрытых причин кровоизлияний.
Геморрагический васкулит ( Аллергическая пурпура , Болезнь Шенлейн-Геноха , Капилляротоксикоз )
Геморрагический васкулит — системное асептическое воспаление сосудов микроциркуляторного русла с преимущественным поражением кожи, суставов, желудочно-кишечного тракта и почечных клубочков. Протекает с явлениями геморрагической или уртикарной сыпи, артралгиями, абдоминальным болевым синдромом, гематурией и почечной недостаточностью. Диагностика основана на клинических симптомах, лабораторных данных (анализ крови, мочи, коагулограмма), исследовании органов ЖКТ и почек. Основой лечения васкулита является терапия антикоагулянтами, ангиагрегантами. В тяжелых случаях применяется экстракорпоральная гемокоррекция, глюкокортикоидная терапия, противовоспалительное, цитостатическое лечение.
МКБ-10

Общие сведения
Геморрагический васкулит (ГВ, болезнь Шенлейн-Геноха, аллергическая пурпура, капилляротоксикоз) относится к наиболее распространенным на сегодняшний день геморрагическим заболеваниям. По сути своей он является аллергическим васкулитом поверхностного характера с поражением мелких артериол, венул, а также капилляров. В Международной классификации болезней (МКБ) заболевание имеет название "аллергическая пурпура". Болезнь Шенлейн-Геноха встречается в основном в детском возрасте - от 5 до 14 лет. Средняя распространенность среди детей этого возраста составляет 23-25 случая на 10 тыс. Наиболее подвержены заболеванию лица в возрасте 7-12 лет. У детей до 3 лет известны лишь отдельные случаи возникновения пурпуры.

Причины
Этиологические аспекты изучены не до конца, известно лишь, что в большинстве случаев патология носит инфекционно-аллергическую природу. Существует сезонная зависимость ‒ наибольшая заболеваемость регистрируется в сырое и холодное время года. Многолетние наблюдения позволили выявить общие триггерные факторы, предшествующие развитию клинических проявлений. К их числу относят:
Во многих наблюдениях причинный фактор, вызвавший возникновение васкулита, установить не удается. Ряд авторов высказывает предположение, что воздействие провоцирующих факторов приводит к развитию геморрагического васкулита лишь в тех случаях, когда оно осуществляется на фоне генетической предрасположенности организма к гиперергическим иммунным реакциям.
В основе механизма развития геморрагического васкулита лежит образование иммунных комплексов и повышение активности белков системы комплемента. Циркулируя в крови, они откладываются на внутренней поверхности стенки мелких сосудов (венул, артериол, капилляров), вызывая ее повреждение с возникновением асептического воспалительного процесса. Воспаление сосудистой стенки в свою очередь приводит к повышению ее проницаемости, отложению в просвете сосуда фибрина и тромботических масс, что обуславливает основные клинические признаки заболевания — кожно-геморрагический синдром и микротромбирование сосудистого русла с поражением ЖКТ, почек, суставов.
Классификация
В клиническом течении капилляротоксикоза различают острую фазу (начальный период или обострение) и фазу стихания (улучшение). По преобладающим симптомам заболевание классифицируют на следующие клинические формы: простую, ревматоидную (суставную), абдоминальную и молниеносную. В соответствии с характером течения различают острый (до 2-х мес.), затяжной (до полугода) и хронический ГВ. По тяжести клинических проявлений выделяют васкулит:
- Легкой степени. Отмечается удовлетворительное состояние пациентов и необильный характер сыпи, артралгии.
- Средней степени. Состояние больного средней тяжести, высыпания обильные, артралгии сопровождаются изменениями в суставах по типу артрита, отмечаются периодические боли в животе и микрогематурия.
- Тяжелой степени. Имеет место тяжелое состояние больного, сливные обильные высыпания с некротическими участками, ангионевротические отеки, нефротический синдром, наблюдается макрогематурия и желудочно-кишечные кровотечения, возможно развитие острой почечной недостаточности.
Симптомы
Для клиники аллергической пурпуры типично острое начало с повышением температуры до субфебрильных или фебрильных цифр. Однако возможно отсутствие подъема температуры. Кожный синдром отмечается в самом дебюте заболевания и наблюдается у всех больных. Он характеризуются диффузными пятнисто-папулезными геморрагическими элементами различной величины (чаще мелкими), не исчезающими при надавливании. В некоторых случаях наблюдается уртикарная сыпь. Высыпания обычно располагаются симметрично на коже голеней, бедер и ягодиц, в области крупных суставов, реже — на коже рук и туловища. Обильность высыпаний часто коррелирует с тяжестью васкулита. При наиболее тяжелом его течении в центре некоторых элементов сыпи развивается некроз и образуется язва. Разрешение сыпи заканчивается длительно сохраняющейся гиперпигментацией. При хроническом течении ГВ с частыми рецидивами на коже после исчезновения сыпи возникает шелушение.
Суставной синдром развивается у 70% пациентов. Поражения суставов могут носить кратковременный характер в виде легкой артралгии или сохраняться в течение нескольких дней с выраженным болевым синдромом, сопровождающимся другими симптомами артрита (покраснение, отечность) и приводящим к ограничению движений в суставе. Типичным является летучий характер поражения с вовлечением преимущественно крупных суставов, чаще коленных и голеностопных. Суставной синдром может появиться в начальном периоде васкулита или возникнуть позже. Зачастую он имеет преходящий характер и никогда не приводит к стойкой деформации суставов. Абдоминальный синдром может предшествовать кожно-суставным проявлениям или сопутствовать им. Он проявляется болями в животе различной интенсивности - от умеренных до приступообразных по типу кишечной колики. Пациенты часто не могут указать точную локализацию боли, жалуются на нарушения стула, тошноту и рвоту. Абдоминалгии могут появляться несколько раз в течение суток и проходят самопроизвольно или в первые несколько дней лечения.
Почечный синдром возникает у 25-30% пациентов и проявляется признаками хронического или острого гломерулонефрита с различной степенью гематурии. У ряда больных возникает нефротический симптомокомплекс. Поражение других органов при геморрагическом васкулите происходит довольно редко. Это может быть геморрагическая пневмония в виде кашля с прожилками крови в мокроте и одышки, кровоизлияния в эндокард, геморрагический перикардит, миокардит. Поражение сосудов головного мозга проявляется головокружением, раздражительностью, головной болью, эпиприступами и может вызвать развитие геморрагического менингита.
Осложнения
Поражение почек является самым стойким синдромом геморрагического васкулита, может осложняться злокачественным гломерулонефритом и хронической почечной недостаточностью. В тяжелых случаях аллергической пурпуры возникают желудочно-кишечные кровотечения, сопровождающиеся кровавой рвотой и присутствием крови в каловых массах, легочные кровотечения, кровоизлияния в вещество головного мозга (геморрагический инсульт). Массивные кровопотери могут привести к коллапсу и анемической коме. Осложнения абдоминального синдрома встречаются реже и представлены инвагинацией кишечника, перитонитом, тромбозом брыжеечных сосудов, некрозом части тонкого кишечника. Наибольшая частота летальных исходов регистрируется при молниеносной форме ГВ.
Диагностика
Проводя диагностику, ревматолог учитывает возраст пациента, изучает этиофакторы, сопоставляет клинические и лабораторные данные, исключает другие заболевания. При развитии почечного синдрома пациенту необходима консультация нефролога, при наличии абдоминальных болей - консультация гастроэнтеролога и хирурга. Диагностическая панель включает:
- Гематологические тесты. В общем анализе крови, как правило, отмечаются неспецифические признаки умеренного воспаления (лейкоцитоз и небольшое повышение СОЭ), увеличение количества тромбоцитов и эозинофилов. Биохимический анализ крови показывает увеличение иммуноглобулина А и СРБ. Большое диагностическое значение имеют результаты коагулограммы. Отсутствие в ней данных за нарушение свертывания при наличии клинических признаков геморрагического синдрома свидетельствует в пользу ГВ.
- Анализы мочи и кала. В анализе мочи выявляется гематурия, протеинурия, цилиндрурия. Пациентам с почечным синдромом показан мониторинг изменений в анализе мочи, проведение биохимии мочи, пробы Зимницкого, Нечипоренко. Для диагностики скрытого ЖКТ-кровотечения производят анализ кала на скрытую кровь.
- Инструментальную диагностику. С целью оценки состояния органов-мишеней выполняется УЗИ почек, УЗДГ почечных сосудов. Для исключения органических причин кровотечения из пищеварительного тракта и бронхов целесообразно проведение УЗИ брюшной полости, гастроскопии, бронхоскопии.
- Биопсию с гистологией. В тяжелых диагностических случаях показана биопсия кожи или почек. Гистологическое исследование биоптата выявляет характерные изменения: отложения иммуноглобулина А и ЦИК на эндотелии и в толще сосудистой стенки венул, артериол и капилляров; образование микротромбов; выход элементов крови за пределы сосуда.
Абдоминальную форму геморрагического васкулита следует дифференцировать от других причин, обуславливающих появление симптомов «острого живота»: аппендицита, пенетрации язвы желудка, острого холецистита, панкреатита, перфорации кишечника при язвенном колите др. Также необходимо исключить тромбоцитопеническую пурпуру, геморрагический синдром при инфекционных заболеваниях (геморрагических лихорадках, гриппе), лейкоз, ревматоидный артрит, болезнь Стилла, острый гломерулонефрит, системные васкулиты.
Лечение
В острой фазе геморрагического васкулита пациентам необходимо соблюдать постельный режим и гипоаллергенную диету, ограничить употребление жидкости и соли, исключить прием антибиотиков и других медикаментов, которые могут усиливать сенсибилизацию организма. Основные направления терапии зависят от клинических проявлений, поэтому их целесообразно рассматривать посиндромно:
- При любых синдромах. Основу базисной терапии при всех формах ГВ составляет назначение дезагрегантов (дипиридамола, пентоксифиллина) и активаторов фибринолиза (никотиновой кислоты). Препараты этих групп препятствуют агрегации тромбоцитов, улучшают микроциркуляцию и внутритканевую перфузию. Часто в базисную схему включают гепарин и другие антикоагулянты.
- При кожном синдроме. Терапия предполагает применение сульфасалазина, колхицина. Использование преднизолона до сих пор является спорным вопросом среди врачей. Возможно его назначение в тяжелых случаях ГВ. При отсутствии эффекта от терапии кортикостероидами препаратами запаса являются цитостатики.
- При суставном синдроме. Выраженные артралгии купируются проведением противовоспалительной терапии (индометацин, ибупрофен). Дополнительно могут назначаться производные аминохинолина (хлорохин).
- При почечном синдроме. Назначаются высокие дозы глюкокортикоидов, цитостатиков. Возможно использование иАПФ, антагонистов рецепторов ангиотензина II, введение нормального человеческого иммуноглобулина, проведение электрофореза с никотиновой кислотой и гепарином на область почек. В терминальной стадии ХПН требуется гемодиализ или трансплантация почки.
- При абдоминальном синдроме. Интенсивный болевой синдром служит показанием к внутривенному введению преднизолона, реополиглюкина, кристаллоидов. При развитии хирургических осложнений (перфорация, инвагинация кишки) применяется хирургическая тактика.
Тяжелое течение заболевания является показанием для проведения экстракорпоральной гемокоррекции (гемосорбция, иммуносорбция, плазмаферез). Многие авторы отмечают неэффективность антигистаминных препаратов в лечении ГВ. Однако их применение может быть оправдано у пациентов с аллергическим анамнезом. При связи заболевания с пищевой аллергией и наличием абдоминального синдрома дополнительно назначаются энтеросорбенты.
Прогноз и профилктика
Легкие формы геморрагического васкулита склонны к самопроизвольному излечению после первой же атаки заболевания - их прогноз благоприятен. При молниеносной форме смерть пациентов может произойти в первые несколько суток от начала заболевания. Чаще всего это связано с поражением сосудов ЦНС и возникновением внутримозгового кровоизлияния. Другой причиной летального исхода может стать тяжелый почечный синдром, приводящий к развитию уремии. В целях профилактики аллергического васкулита рекомендуется санация хронических инфекционных очагов ЛОР органов, дегельминтизация при глистных инвазиях, исключение контакта с известными аллергенами и бесконтрольного приема медикаментов.
Тромбоцитопеническая пурпура ( Болезнь Верльгофа )
Тромбоцитопеническая пурпура - это разновидность геморрагического диатеза, характеризующаяся дефицитом красных кровяных пластинок - тромбоцитов, чаще вызванным иммунными механизмами. Признаками тромбоцитопенической пурпуры служат самопроизвольные, множественные, полиморфные кровоизлияния в кожу и слизистые оболочки, а также носовые, десневые, маточные и другие кровотечения. При подозрении на тромбоцитопеническую пурпуру оценивают анамнестические и клинические данные, показатели общего анализа крови, коагулограммы, ИФА, микроскопии мазков крови, пункции костного мозга. В лечебных целях больным назначаются кортикостероидные, гемостатические препараты, цитостатическая терапия, проводится спленэктомия.

Тромбоцитопеническая пурпура (болезнь Верльгофа, доброкачественная тромбоцитопения) - гематологическая патология, характеризующаяся количественным дефицитом тромбоцитов в крови, сопровождающаяся наклонностью к кровоточивости, развитию геморрагического синдрома. При тромбоцитопенической пурпуре уровень кровяных пластинок в периферической крови опускается значительно ниже физиологического - 150х10 9 /л при нормальном или несколько увеличенном количестве мегакариоцитов в костном мозге. По частоте встречаемости тромбоцитопеническая пурпура занимает первое место среди прочих геморрагических диатезов. Манифестирует заболевание обычно в детском возрасте (с пиком в раннем и дошкольном периоде). У подростков и взрослых патология в 2-3 раза чаще выявляется среди лиц женского пола.

В 45% случаев имеет место идиопатическая тромбоцитопеническая пурпура, развивающаяся самопроизвольно, без видимых причин. В 40% случаев тромбоцитопении предшествуют различные инфекционные заболевания (вирусные или бактериальные), перенесенные примерно за 2-3 недели до этого. В большинстве случаев это инфекции верхних отделов дыхательного тракта неспецифического генеза, в 20% - специфические (ветряная оспа, корь, краснуха, эпидемический паротит, инфекционный мононуклеоз, коклюш). Тромбоцитопеническая пурпура может осложнять течение малярии, брюшного тифа, лейшманиоза, септического эндокардита. Иногда тромбоцитопеническая пурпура проявляется на фоне иммунизации - активной (вакцинации) или пассивной (введения γ - глобулина). Тромбоцитопеническая пурпура может быть спровоцирована приемом медикаментов (барбитуратов, эстрогенов, препаратов мышьяка, ртути), длительным воздействием рентгеновских лучей (радиоактивных изотопов), обширным хирургическим вмешательством, травмой, избыточной инсоляцией. Отмечаются семейные случаи заболевания.
Большинство вариантов тромбоцитопенической пурпуры имеет иммунную природу и связано с продукцией антитромбоцитарных антител (IgG). Образование иммунных комплексов на поверхности тромбоцитов приводит к быстрому разрушению кровяных пластинок, уменьшению продолжительности их жизни до нескольких часов вместо 7-10 суток в норме.
Изоиммунная форма тромбоцитопенической пурпуры может быть обусловлена поступлением в кровь «чужеродных» тромбоцитов при повторных переливаниях крови или тромбоцитарной массы, а также антигенной несовместимостью тромбоцитов матери и плода. Гетероиммунная форма развивается при повреждении антигенной структуры тромбоцитов различными агентами (вирусами, медикаментами). Аутоиммунный вариант тромбоцитопенической пурпуры вызван появлением антител против собственных неизмененных антигенов тромбоцитов и обычно сочетается с другими заболеваниями такого же генеза (СКВ, аутоиммунной гемолитической анемией). Развитие трансиммунной тромбоцитопении у новорожденных провоцируется проходящими через плаценту антитромбоцитарными аутоантителами матери, больной тромбоцитопенической пурпурой.
Дефицит тромбоцитов при тромбоцитопенической пурпуре может быть связан с функциональным поражением мегакариоцитов, нарушением процесса отшнуровывания кровяных красных пластинок. Например, симптомокомплекс Верльгофа обусловлен неэффективностью гемопоэза при анемии (B-12 дефицитной, апластической), остром и хроническом лейкозах, системных заболеваниях органов кроветворения (ретикулезах), костномозговых метастазах злокачественных опухолей.
При тромбоцитопенической пурпуре происходит нарушение образования тромбопластина и серотонина, снижение сократительной способности и усиление проницаемости стенки капилляров. С этим связаны удлинение времени кровотечения, нарушение процессов тромбообразования и ретракции кровяного сгустка. При геморрагических обострениях количество тромбоцитов снижается вплоть до единичных клеток в препарате, в период ремиссии восстанавливается до уровня ниже нормы.
В классификации тромбоцитопенической пурпуры учитываются ее этиологические, патогенетические и клинические особенности. Различают несколько вариантов - идиопатическую (болезнь Верльгофа), изо-, транс-, гетеро- и аутоиммунную тромбоцитопеническую пурпуру, симптомокомплекс Верльгофа (симптоматическую тромбоцитопению).
По течению выделяют острую, хроническую и рецидивирующую формы. Острая форма более характерна для детского возраста, длится до 6 месяцев с нормализацией уровня тромбоцитов в крови, не имеет рецидивов. Хроническая форма протекает более 6 месяцев, чаще встречается у взрослых пациентов; рецидивирующая - имеет циклическое течение с повторениями эпизодов тромбоцитопении после нормализации уровня тромбоцитов.
Симптомы тромбоцитопенической пурпуры
Тромбоцитопеническая пурпура клинически проявляется при падении уровня тромбоцитов ниже 50х10 9 /л, обычно через 2-3 недели после воздействия этиологического фактора. Характерна кровоточивость по петехиально-пятнистому (синячковому) типу. У больных тромбоцитопенической пурпурой появляются безболезненные множественные кровоизлияния под кожу, в слизистые оболочки («сухой» вариант), а также кровотечения («влажный» вариант). Они развиваются спонтанно (часто в ночное время) и их выраженность не соответствует силе травматического воздействия.
Геморрагические высыпания полиморфны (от незначительных петехий и экхимозов до крупных синяков и кровоподтеков) и полихромны (от ярких багрово-синих до бледных желто-зеленых в зависимости от времени появления). Чаще всего геморрагии возникают на передней поверхности туловища и конечностей, редко - в области лица и шеи. Кровоизлияния определяются и на слизистой оболочке миндалин, мягкого и твердого неба, конъюнктиве и сетчатке, барабанной перепонке, в жировой клетчатке, паренхиматозных органах, серозных оболочках головного мозга.
Патогномоничны интенсивные кровотечения - носовые и десневые, кровотечения после удаления зубов и тонзиллэктомии. Могут появляться кровохарканье, кровавые рвота и понос, кровь в моче. У женщин обычно превалируют маточные кровотечения в виде меноррагий и метроррагий, а также овуляторных кровотечений в брюшную полость с симптомами внематочной беременности. Непосредственно перед менструацией появляются кожные геморрагические элементы, носовые и другие кровотечения. Температура тела остается в норме, возможна тахикардия. При тромбоцитопенической пурпуре имеется умеренная спленомегалия. При профузном кровотечении развивается малокровие внутренних органов, гиперплазия красного костного мозга и мегакариоцитов.
Медикаментозная форма манифестирует вскоре после приема лекарственного препарата, продолжается от 1 недели до 3 месяцев со спонтанным выздоровлением. Радиационная тромбоцитопеническая пурпура отличается тяжелым геморрагическим диатезом с переходом костного мозга в гипо- и апластическое состояние. Инфантильная форма (у детей до 2 лет) имеет острое начало, тяжелый, часто хронический характер и выраженную тромбоцитопению (9/л).
В течении тромбоцитопенической пурпуры выявляют периоды геморрагического криза, клинической и клинико-гематологической ремиссии. При геморрагическом кризе кровоточивость и лабораторные изменения ярко выражены, в период клинической ремиссии на фоне тромбоцитопении геморрагии не проявляются. При полной ремиссии отсутствуют и кровоточивость, и лабораторные сдвиги. При тромбоцитопенической пурпуре с большой кровопотерей наблюдается острая постгеморрагическая анемия, при длительной хронической форме - хроническая железодефицитная анемия.
Наиболее грозное осложнение - кровоизлияние в головной мозг развивается внезапно и быстро прогрессирует, сопровождаясь головокружением, головной болью, рвотой, судорогами, неврологическими нарушениями.

Диагноз тромбоцитопенической пурпуры устанавливается гематологом с учетом анамнеза, особенностей течения и результатов лабораторных исследований (клинического анализа крови и мочи, коагулограммы, ИФА, микроскопии мазков крови, пункции костного мозга).
На тромбоцитопеническую пурпуру указывают резкое снижение числа тромбоцитов в крови (9/л), увеличение времени кровотечения (>30 мин.), протромбинового времени и АЧТВ, снижение степени или отсутствие ретракции сгустка. Число лейкоцитов обычно в пределах нормы, анемия появляется при значительной кровопотере. На высоте геморрагического криза выявляются положительные эндотелиальные пробы (щипка, жгута, уколочная). В мазке крови определяется увеличение размеров и снижение зернистости тромбоцитов. В препаратах красного костного мозга обнаруживается нормальное или повышенное количество мегакариоцитов, присутствие незрелых форм, отшнуровка тромбоцитов в малочисленных точках. Аутоиммунный характер пурпуры подтверждается наличием в крови антитромбоцитарных антител.
Тромбоцитопеническую пурпуру дифференцируют от апластических или инфильтративных процессов костного мозга, острого лейкоза, тромбоцитопатий, СКВ, гемофилии, геморрагического васкулита, гипо- и дисфибриногенемий, ювенильных маточных кровотечений.
Лечение тромбоцитопенической пурпуры
При тромбоцитопенической пурпуре с изолированной тромбоцитопенией (тромбоциты >50х10 9 /л) без геморрагического синдрома лечение не проводится; при среднетяжелой тромбоцитопении (30-50 х10 9 /л) медикаментозная терапия показана в случае повышенного риска развития кровотечений (артериальной гипертензии, язвенной болезни желудка и 12-перстной кишки). При уровне тромбоцитов 9/л лечение осуществляют без дополнительных показаний в условиях стационара.
Кровотечения купируются введением кровоостанавливающих препаратов, местно применяется гемостатическая губка. Для сдерживания иммунных реакций и снижения сосудистой проницаемости назначаются кортикостероиды в понижающей дозе; гипериммунные глобулины. При больших кровопотерях возможны трансфузии плазмы и отмытых эритроцитов. Вливания тромбоцитарной массы при тромбоцитопенической пурпуре не показаны.
У больных хронической формой с рецидивами обильных кровотечений и кровоизлияниями в жизненно важные органы выполняют спленэктомию. Возможно назначение иммунодепрессантов (цитостатиков). Лечение тромбоцитопенической пурпуры при необходимости должно сочетаться с терапией основного заболевания.
Прогноз
В большинстве случаев прогноз тромбоцитопенической пурпуры весьма благоприятный, полное выздоровление возможно в 75% случаев (у детей - в 90%). Осложнения (например, геморрагический инсульт) наблюдаются в острой стадии, создавая риск смертельного исхода. При тромбоцитопенической пурпуре требуется постоянное наблюдение гематолога, исключаются препараты, влияющие на агрегационные свойства тромбоцитов (ацетилсалициловая к-та, кофеин, барбитураты), пищевые аллергены, проявляется осторожность при проведении вакцинации детей, ограничивается инсоляция.
ДВС-синдром
ДВС-синдром - расстройство гемостаза, связанное с гиперстимуляцией и дефицитом резервов свертывающей системы крови, приводящее к развитию тромботических, микроциркуляторных и геморрагических нарушений. При ДВС-синдроме наблюдается петехиально-гематомная сыпь, повышенная кровоточивость, дисфункция органов, а в острых случаях - развитие шока, гипотонии, сильных кровотечений, ОДН и ОПН. Диагноз устанавливают по характерным признакам и лабораторным тестам системы гемостаза. Лечение ДВС-синдрома направлено на коррекцию гемодинамики и нарушений свертывающей системы (антиагреганты, антикоагулянты, ангиопротекторы, гемотрансфузии, плазмаферез и др.).



ДВС-синдром (диссеминированное внутрисосудистое свертывание, тромбогеморрагический синдром) - геморрагический диатез, характеризующийся чрезмерным ускорением внутрисосудистой коагуляции, образованием рыхлых сгустков крови в микроциркуляторной сети с развитием гипоксических и дистрофически-некротических измерений в органах. ДВС-синдром представляет опасность для жизни пациента из-за риска возникновения обширных, плохо купируемых кровотечений и острой дисфункции органов (главным образом, легких, почек, надпочечников, печени, селезенки), имеющих обширную микроциркуляторную сеть.
ДВС-синдром можно рассматривать, как неадекватную защитную реакцию, направленную на ликвидацию кровотечения при повреждении кровеносных сосудов и изоляцию организма от пораженных тканей. Встречаемость ДВС-синдрома в различных отраслях практической медицины (гематологии, реаниматологии, хирургии, акушерстве и гинекологии, травматологии и др.) достаточно велика.

Причины ДВС-синдрома
ДВС-синдром развивается на фоне заболеваний, протекающих с повреждением тканей, эндотелия сосудов и клеток крови, сопровождаемых микрогемодинамическими нарушениями и сдвигом гемостаза в сторону гиперкоагуляции. Основной причиной ДВС-синдрома выступают септические осложнения бактериальных и вирусных инфекций, шок любой природы. ДВС-синдром часто сопутствует акушерской патологии - тяжелому гестозу, предлежанию и преждевременной отслойке плаценты, внутриутробной гибели плода, эмболии амниотической жидкостью, ручному отделению последа, атоническим маточным кровотечениям, а также операции кесарево сечение.
Развитие тромбогеморрагического синдрома могут инициировать метастазирующие злокачественные опухоли (рак легкого, рак желудка), обширные травмы, ожоги, серьезные хирургические вмешательства. Нередко ДВС-синдром сопровождает трансфузию крови и ее компонентов, трансплантацию тканей и органов, протезирование сосудов и клапанов сердца, применение искусственного кровообращения.
Способствовать возникновению ДВС-синдрома могут сердечно-сосудистые заболевания, протекающие с гиперфибриногенемией, увеличением вязкости и снижением текучести крови, механическим препятствием кровотоку атеросклеротической бляшкой. К ДВС-синдрому могут приводить прием медикаментов (ОК, ристомицина, диуретиков), острые отравления (например, ядом змеи) и острые аллергические реакции.
Несостоятельность гемостаза при ДВС-синдроме возникает за счет гиперстимуляции свертывающей и быстрого истощения антикоагулянтной и фибринолитической систем гемостаза.
Развитие ДВС-синдрома обуславливается различными факторами, которые появляются в кровяном русле и напрямую активируют процесс свертывания, либо осуществляют это через медиаторы, воздействующие на эндотелий. В качестве активаторов ДВС-синдрома могут выступать токсины, ферменты бактерий, околоплодные воды, иммунные комплексы, стрессовые катехоламины, фосфолипиды, снижение сердечного выброса и кровотока, ацидоз, гиповолемия и др.
Развитие ДВС-синдрома происходит с последовательной сменой 4-х стадий.
I - начальная стадия гиперкоагуляции и внутрисосудистой агрегации клеток. Обусловлена выбросом в кровь тканевого тромбопластина или веществ, обладающих тромбопластиноподобным действием и запускающих внутренний и внешний пути свертывания. Может продолжаться от нескольких минут и часов (при острой форме) до нескольких дней и месяцев (при хронической).
II - стадия прогрессирующей коагулопатии потребления. Характеризуется дефицитом фибриногена, кровяных пластинок и плазменных факторов вследствие их избыточного расхода на тромбообразование и недостаточного возмещения.
III - критическая стадия вторичного фибринолиза и выраженной гипокоагуляции. Отмечается разбалансировка гемостатического процесса (афибриногенемия, накопление патологических продуктов, разрушение эритроцитов) с замедлением свертывания крови (вплоть до полной неспособности к свертыванию).
IV - стадия восстановления. Наблюдаются либо остаточные очаговые дистрофические и некротические изменения в тканях тех или иных органов и выздоровление, либо осложнения в виде острой органной недостаточности.

Классификация ДВС-синдрома
По выраженности и скорости развития ДВС-синдром может быть острым (в т.ч., молниеносным), подострым, хроническим и рецидивирующим. Острая форма тромбогеморрагического синдрома возникает при массивном выбросе в кровь тромбопластина и ему подобных факторов (при акушерской патологии, обширных операциях, травмах, ожогах, синдроме длительного сдавления тканей). Характеризуется ускоренной сменой стадий ДВС-синдрома, отсутствием нормального защитного антикоагуляционного механизма. Подострая и хроническая формы ДВС-синдрома связаны с обширным изменением поверхности эндотелия сосудов (например, вследствие атеросклеротических отложений), выступающим в роли активирующей субстанции.
ДВС-синдром может проявляться локально (ограниченно, в одном органе) и генерализованно (с поражением нескольких органов или всего организма). По компенсаторному потенциалу организма можно выделить компенсированный, субкомпенсированный и декомпенсированный ДВС-синдром. Компенсированная форма протекает бессимптомно, микросгустки лизируются за счет усиления фибринолиза, факторы свертывания восполняются из резервов и путем биосинтеза. Субкомпенсированная форма проявляется в виде гемосиндрома средней степени тяжести; декомпенсированная - характеризуется каскадными реакциями реактивного фибринолиза, несостоятельностью коагуляционных процессов, несворачиваемостью крови.
ДВС-синдром может протекать с одинаковой активностью прокоагулянтного и сосудисто-тромбоцитарного звеньев гемостаза (смешанный патогенез) или с преобладанием активности одного из них.
Симптомы ДВС-синдрома
Клинические проявления ДВС-синдрома определяются темпом развития и распространенностью поражения, стадией процесса, состоянием компенсаторных механизмов, наслоением симптомов заболевания-индуктора. В основе ДВС-синдрома лежит комплекс тромбогеморрагических реакций и дисфункции органов.
При острой манифестной форме быстро (за несколько часов) развивается генерализованный ДВС-синдром, для которого характерно шоковое состояние с гипотонией, потерей сознания, признаками отека легких и острой дыхательной недостаточности. Гемосиндром выражается нарастающей кровоточивостью, массивными и профузными кровотечениями (легочными, маточными, носовыми, желудочно-кишечными). Характерно развитие очагов ишемической дистрофии миокарда, панкреонекроза, эрозивно-язвенного гастроэнтерита. Молниеносная форма ДВС-синдрома свойственна эмболии околоплодными водами, когда коагулопатия стремительно (в течение нескольких минут) переходит в критическую стадию, сопровождаясь кардиопульмонарным и геморрагическим шоком. Летальность матери и ребенка при этой форме ДВС-синдрома приближается к 80%.
Подострая форма ДВС-синдрома носит локальный характер с более благоприятным течением. Незначительный или умеренный гемосиндром проявляется петехиальной или сливной геморрагической сыпью, синяками и гематомами, усиленной кровоточивостью из мест инъекций и ран, кровотечениями из слизистых оболочек (иногда - «кровавый пот», «кровавые слезы»). Кожа приобретает бледный вид, мраморность, становится холодной на ощупь. В ткани почек, легких, печени, надпочечников, ЖКТ развиваются отек, резкое полнокровие, внутрисосудистая коагуляция, сочетание очагов некроза и множественных кровоизлияний. Самая распространенная - хроническая форма ДВС-синдрома часто имеет бессимптомное течение. Но по мере прогрессирования фонового заболевания нарастают проявления геморрагического диатеза и нарушения функции органов.
ДВС-синдром сопровождается астеническим синдромом, плохим заживлением ран, присоединением гнойной инфекции, развитием келоидных рубцов. К осложнениям ДВС-синдрома относятся гемокоагуляционный шок, острая дыхательная недостаточность, ОПН, некроз печени, язвенная болезнь желудка, инфаркт кишечника, панкреонекроз, ишемический инсульт, острая постгеморрагическая анемия.

Диагностика ДВС-синдрома
Для установления ДВС-синдрома необходимы тщательный сбор анамнеза с поиском этиологического фактора, анализ клинической картины и данных лабораторных исследований (общего анализа крови и мочи, мазка крови, коагулограммы, паракоагуляционных проб, ИФА). Важно оценить характер кровоточивости, уточнить стадию коагулопатии, отражающую глубину нарушений.
Для ДВС-синдрома характерна петехиально-гематомная кровоточивость, геморрагии сразу из нескольких мест. При малосимптомном течении гиперкоагуляция выявляется только лабораторными методами. К обязательным скрининговым тестам относятся определение количества тромбоцитов, фибриногена, АПТВ, протромбинового и тромбинового времени, времени свертывания по Ли-Уайту. Исследование маркеров внутрисосудистого свертывания - РФМК и ПДФ, D-димера методом ИФА и паракоагуляционных проб помогает подтвердить ДВС-синдром.
Критериями ДВС-синдрома являются наличие фрагментированных эритроцитов в мазке крови, дефицит тромбоцитов и фибриногена, повышение концентрации ПДФ, падение активности антитромбина III в сыворотке крови, удлинение АПТВ и тромбинового времени, отсутствие образования или нестабильность сгустка или in vitro. Выполняется оценка функционального состояния «шоковых органов»: легких, почек, печени, сердечно-сосудистой системы, головного мозга. ДВС-синдром необходимо дифференцировать от первичного фибринолиза, других коагулопатических синдромов.
Лечение ДВС-синдрома
Успех лечения ДВС-синдрома возможен при его ранней диагностике. Активные лечебные мероприятия требуются при выраженной симптоматике в виде кровотечений и органной недостаточности. Больных с ДВС-синдромом следует госпитализировать в ОРИТ и при необходимости проводить ИВЛ, активную противошоковую терапию. При малосимптомном ДВС-синдроме основным представляется лечение фоновой патологии, коррекция параметров гемодинамики и функциональных нарушений органов.
Острый ДВС-синдром требует срочного устранения его первопричины, например, экстренного родоразрешения, гистерэктомии - при акушерской патологии или антибиотикотерапии - при септических осложнениях. Для ликвидации гиперкоагуляции показано введение антикоагулянтов (гепарина), дезагрегантов (дипиридамола, пентоксифиллина), фибринолитиков. Больные должны находиться под постоянным динамическим контролем показателей гемостаза.
В качестве заместительной терапии при ДВС-синдроме применяются трансинфузии свежезамороженной плазмы, тромбоцитарной или эритроцитарной массы (при падении уровня тромбоцитов или Hb); криопреципитата (при сердечной недостаточности), физраствора. При кровотечениях, угрожающих жизни, возможно назначение антифибринолитических средств (аминокапроновой к-ты, ингибиторов протеаз). При кожных геморрагиях и ранах накладываются повязки с этамзилатом, гемостатическая губка.
По показаниям применяют кортикостероиды, оксигенотерапию, плазмаферез. Для восстановления микроциркуляции и нарушенных функций органов назначают ангиопротекторы, ноотропные препараты, посиндромную терапию. В случае ОПН проводят гемодиализ, гемодиафильтрацию. При хроническом ДВС-синдроме целесообразно использование дезагрегантов, вазодилататоров, в послеоперационном периоде - гепаринотерапии.
Прогноз и профилактика ДВС-синдрома
Прогноз ДВС-синдрома - вариативный, зависит от основного, этиологически значимого заболевания, тяжести нарушений гемостаза и своевременности начатого лечения. При остром ДВС-синдроме не исключен летальный исход в результате некупируемой большой кровопотери, развития шока, ОПН, острой дыхательной недостаточности, внутренних кровоизлияний. Предупреждение ДВС-синдрома заключается в выявлении пациентов группы риска (особенно, среди беременных и лиц пожилого возраста), лечении фонового заболевания.
Тромбоцитопеническая пурпура у детей

Геморрагические патологии — это специфические заболевания крови. В детской практике они встречаются довольно часто, отличаются достаточно тяжелым течением. Достаточно часто у детей встречается тромбоцитопеническая пурпура.
В настоящее время насчитывается множество геморрагических патологий. К их развитию приводят самые разные причины. Одна из таких болезней — тромбоцитопеническая пурпура. Эта патология возглавляет список геморрагических заболеваний как у детей, так и у взрослых. Если ориентироваться на статистику, можно отметить, что она встречается у 40-70% пациентов, имеющих различные патологии крови.
Данная патология характеризуется сильным снижением в периферическом кровеносном русле общего количества тромбоцитарных клеток. Это обусловлено наличием иммунного конфликта между кровяными пластинками и антигенами. Нужно отметить, что анатомические параметры селезенки при этом остаются нормальными. Врачи отмечают, что ежегодно регистрируется все больше случаев данного геморрагического заболевания.
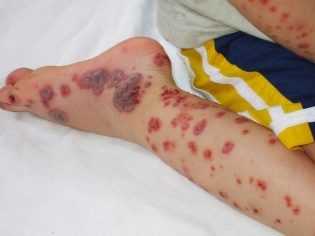
Малышки страдают от этой патологии гораздо чаще, чем мальчики.
Единая причина возникновения заболевания в настоящее время не установлена. Долгое время ученые не могли понять, по каким причинам у малышей возникает данная патология крови. Только современные разработки и научные исследования помогли специалистам получить некоторые ответы на их вопросы.
К развитию тромбоцитопенической пурпуры приводит воздействие самых разных факторов. К самым распространенным и научно обоснованным относятся:
- Длительный прием некоторых видов лекарственных препаратов. Ученые доказали, что более 60 различных лекарств могут спровоцировать у ребенка появление на коже симптомов данного геморрагического заболевания. К таким препаратам относятся хинин, хинидин, сульфаниламиды, гепарин, фуросемид, дипиридамол, дигоксин, метаболиты ацетилсалициловой кислоты, парацетамол, некоторые виды бета-блокаторов, тиазиды, цефалоспорины, ампициллин, левамизол и многие другие. Предсказать развитие геморрагического заболевания у конкретного ребенка — практически невыполнимая задача.
- Генетические дефекты. Многие европейские ученые считают, что в развитии идиопатического варианта заболевания очень важную роль играет наследственность. Сейчас проводятся многочисленные научные эксперименты, которые должны доказать или опровергнуть данную теорию. Имеющиеся генетические нарушения могут приводить к развитию аутоиммунного воспаления и появлению неблагоприятных симптомов геморрагического заболевания.
- Последствия перенесенных инфекционных патологий. Токсическое воздействие продуктов жизнедеятельности болезнетворных микроорганизмов на детский организм приводит к развитию различных воспалительных иммунологических реакций. У малышей, имеющих врожденные иммунодефицитные состояния, риск возникновения тромбоцитопенической пурпуры повышен в несколько раз.

- Внутриутробное заражение. Первые признаки геморрагического заболевания формируются у малыша еще в период нахождения в утробе матери. Женщина, страдающая тромбоцитопенической пурпурой, может передать ребенку через систему плацентарного кровотока ряд аутоиммунных антител. Такая клиническая ситуация приводит к тому, что неблагоприятные симптомы болезни возникают у новорожденного малыша уже в первые месяцы жизни.
Долгое время ученые не могли установить, каков механизм развития тромбоцитопенической пурпуры у детей. В течение многих десятилетий сохранялись различные теории, которые объясняли патогенез данного геморрагического заболевания. В последнее время (в связи с появлением новых лабораторных аппаратов и усовершенствованием методов диагностики) появляются новые знания о механизме возникновения тромбоцитопенической пурпуры у детей.
Во время патологического процесса в детском организме появляется большое количество специфических белковых молекул. Они называются антитромбоцитарными антителами. Эти вещества начинают взаимодействовать с особыми антигенными составляющими клеточных мембран кровяных пластинок (тромбоцитов).
В норме данные клетки крови выполняют ряд очень важных физиологических функций. Они необходимы для обеспечения нормальной вязкости, а также для кровотока.
Результаты последних научных исследований подтверждают то, что структура тромбоцитов при данном геморрагическом заболевании претерпевает ряд изменений. В них появляется выраженный гранулярный аппарат, а также существенно повышается уровень альфа-серотонина. Изменение общего количества тромбоцитов влияет на появление стойких изменений, начинающих происходить в сосудистой стенке. В ответ на данное состояние увеличивается количество тромбоцитарного фактора роста.

Все эти нарушения приводят к гибели эндотелиоцитов — клеток, выстилающих изнутри кровеносные сосуды и придающих им специфическую «гладкость», необходимую для бесперебойного кровотока. В результате таких патологических отклонений у ребенка начинают появляться первые признаки геморрагического синдрома, который существенно ухудшает его самочувствие.
После перенесенных бактериальных или вирусных инфекций антитромбоцитарные антитела обычно появляются спустя ½ -1 месяц. По своей принадлежности они относятся к классу иммуноглобулинов G. Этим обусловлено также стойкое сохранение появившихся антител в крови в дальнейшем. В некоторых случаях они могут сохраняться у ребенка в течение всей жизни. Гибель «отработанных» иммунных комплексов происходит в селезенке.


Последние результаты проведенных научных исследований позволили уточнить, почему у ребенка, страдающего аутоиммунной тромбоцитопенической пурпурой, долгое время остаются симптомы повышенной кровоточивости. Это во многом обусловлено снижением уровня серотонина. В норме данное вещество участвует в образовании кровеносного сгустка.
Врачи выделяют несколько клинических форм данного геморрагического состояния.
К ним относятся:
- иммунная тромбоцитопения;
- идиопатическая.
Доктора также пользуются еще одной классификацией, которая позволяет разделить различные варианты тромбоцитопенической пурпуры на разные иммунные формы. К ним относятся:
- Изоиммунная. Наиболее часто встречается после гемотрансфузий. Может быть врожденной - когда у мамы и будущего малыша есть иммунный конфликт по тромбоцитарным антигенам. Может иметь транзиторный характер. Данная клиническая форма часто постоянно рецидивирующая.
- Аутоиммунная. Возникает вследствие образования в организме большого количества тромбоцитарных антител к собственным кровяным пластинкам.
- Гетероиммунная. К развитию данного иммунного варианта заболевания часто приводит прием некоторых групп лекарственных препаратов. Важную роль в этом играет наличие у заболевшего малыша индивидуальной гиперчувствительности и невосприимчивости отдельных химических веществ. Это способствует развитию специфического признака — пурпурных высыпаний на коже, которые являются следствием множественных кровоизлияний.
- Трансиммунная. Данная иммунная форма болезни развивается, как правило, вследствие возникшего антигенного конфликта и накопления антитромбоцитарных антител у беременной женщины. Они достаточно легко проникают в организм плода через систему плацентарного кровотока, приводя к развитию геморрагического синдрома.


Выраженность неблагоприятных клинических признаков заболевания во многом зависит от того, насколько критично снижение тромбоцитов в периферической крови. Симптомы нарастают при падении уровня кровяных пластинок до 100000/мкл. Снижение до 50000/мкл приводит к появлению выраженных симптомов геморрагического синдрома.
Это патологическое состояние является наиболее специфическим клиническим признаком тромбоцитопенической пурпуры. Оно характеризуется появлением многочисленных и разнообразных кровоизлияний, возникающих в самых разных анатомических зонах.
Довольно часто у заболевшего ребенка появляются носовые и десневые кровотечения, наиболее опасны кровоизлияния в головной мозг и внутренние органы. Это приводит к инвалидизации заболевшего малыша.
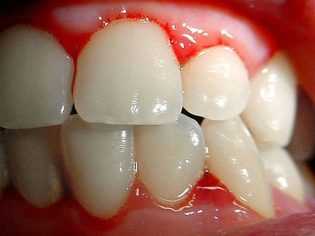
Кровотечения в почках или мочевыводящих путях проявляется у ребенка присутствием примеси крови в моче. При обильных кровотечениях может возникать гематурия — появление большого количества эритроцитов в мочевом осадке. Кровотечения в желудочно-кишечном тракте (особенно в дистальных отделах кишечника) приводят к тому, что у ребенка появляется черный стул (мелена). Эти клинические признаки являются весьма неблагоприятными и требуют обязательного обращения за консультацией к врачу.
Геморрагический синдром при тромбоцитопенической пурпуре имеет несколько особенностей. Он характеризуется несимметричностью возникающих отклонений, а также полной спонтанностью их появления. Степень выраженности признаков, как правило, не соответствует интенсивности оказанного воздействия.
В некоторых случаях неблагоприятные симптомы проявляются у ребенка даже при однократном приеме лекарственного препарата или после перенесения обычной инфекции. Довольно часто тромбоцитопеническая пурпура протекает в острой форме.
Кровоизлияния могут быть множественными и возникать одновременно (в самых разных внутренних органах). Существуют и довольно неблагоприятные локализации внутренних кровотечений. К ним относятся почки, надпочечники, головной, а также спинной мозг, сердце, печень. Кровоизлияния в эти органы приводят к выраженному нарушению жизненно важных функций.
Тромбоцитопеническая пурпура имеет определенные особенности. При проведении пальпации внутренних органов можно отметить, что отсутствует увеличение селезенки и печени. Лимфатические узлы также остаются нормальными по размеру. Эти клинические признаки существенно отличают данную патологию от многих других геморрагических заболеваний. Довольно часто синдром повышенной кровоточивости остается лишь одним проявлением данной болезни.
Как проявляется у новорожденных?
Первые симптомы у малышей, имеющих в крови аутотромбоцитарные антитела, появляются уже в первые месяцы жизни. У грудничков геморрагический синдром может быть выражен по-разному. На появление негативных симптомов влияет исходное состояние малыша, а также наличие у него тяжелых сопутствующих патологий.
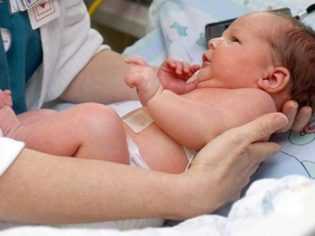
Проявляется тромбоцитопеническая пурпура у малышей возникновением кровоизлияний в кожу, слизистые оболочки, а также во внутренние органы.
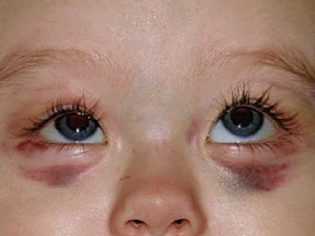
Обычно первыми симптомами, которые родители обнаруживают у заболевшего ребенка, бывают крупные синяки, внезапно появившиеся на кожных покровах. Как правило, никаких предшествующих повреждений или ударов перед появлением на коже таких элементов не бывает. Развитие кровоизлияний в полость крупных суставов носит весьма опасный характер, так как может приводить к нарушению походки и появлению болезненности при совершении активных движений.
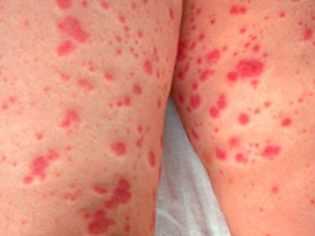
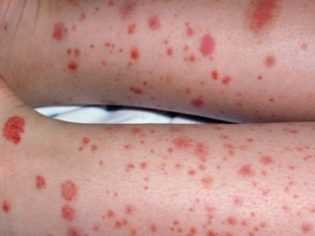
Заподозрить заболевание можно при появлении у ребенка различных кровоизлияний. В норме таких проявлений у малышей нет. Появление синяков на коже без связи с травмой или ударом также должно мотивировать родителей обратиться с малышом на консультацию к педиатру. Более точный диагноз сможет поставить детский гематолог.
Для проведения диагностики требуется выполнение нескольких лабораторных тестов. Эти исследования помогают установить патологический вариант кровоточивости, а также определить степень выраженности имеющихся у ребенка физиологических нарушений.
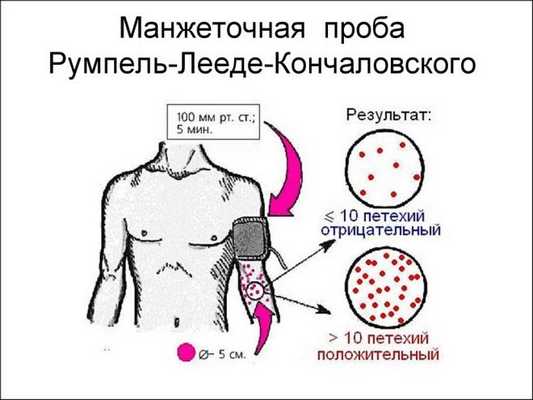
Для выявления излишней кровоточивости проводятся «проба щипка» и манжеточная проба. Исследование с помощью манжетки детского тонометра для измерения артериального давления является обязательным при диагностике тромбоцитопенической пурпуры.
Базовым исследованием, которое проводится для всех без исключения малышей, является общий анализ крови. Данное геморрагическое заболевание характеризуется резким снижением количества тромбоцитов. После перенесенных вирусных инфекций в крови может долгое время присутствовать стойкий лимфоцитоз. Проведение спинномозговой пункции при тромбоцитопенической пурпуре носит лишь вспомогательный характер. Результат миелограммы при этом заболевании покажет, что количество тромбоцитов в норме.
С целью установления имеющихся функциональных нарушений проводится анализ на коагулограмму. Он помогает определить количество фибриногена, протромбиновое время и другие важные критерии оценки внутрисосудистого тромбообразования. Результат оценивает лечащий врач.
В некоторых ситуациях требуется расширение комплекса диагностических мероприятий. Назначение дополнительных исследований проводится по строгим медицинским показаниям.
Появление у малыша признаков выраженного геморрагического синдрома — повод для госпитализации в стационар. Коррекция гематологических нарушений проводится в госпитальных условиях, все процессы контролируют врачи. Во время обострения болезни необходим постельный режим. По мере улучшения самочувствия малыш может вернуться к своему привычному образу жизни. Активные занятия спортом для таких детей обычно ограничиваются.
Одной из важных составляющих лечения является соблюдение диеты.

Больной малыш должен есть 5-6 раз в сутки, небольшими порциями. Очень хорошо, если пища будет предварительно измельчена. Рекомендуется готовить блюда щадящим способом, обжаривание в масле следует исключить. Основу детского рациона должны составлять различные белковые продукты.
Основными лекарственными средствами, которые назначаются врачами для компенсации геморрагического синдрома, являются глюкокортикостероиды. Они оказывают комплексное воздействие, включающее в себя десенсибилизирующий, противовоспалительный, иммуносупрессивный и антиаллергический эффект. Основным препаратом, который назначается в этот период, является преднизолон. Дозировка гормона определяется индивидуально, с учетом возраста и веса малыша.
При приеме преднизолона в крови заболевшего ребенка постепенно увеличивается количество тромбоцитов. Прием гормонов способствует уменьшению количества циркулирующих антитромбоцитарных антител, а также снижению образования иммунных комплексов, которые вызывают появление неблагоприятных симптомов.
О том, что такое тромбоцитопеническая пурпура, смотрите в следующем видео.
Читайте также:
