Желточная (вителлиформная) дистрофия Беста. Пятно вишнево-красного цвета и факомы сетчатки
Добавил пользователь Алексей Ф. Обновлено: 22.01.2026
Болезнью Беста называют детскую дегенерацию желтого пятна. Подобная патология редко встречается с дистрофией сетчатки в зоне макулы и имеет вид отграниченного круга желтоватого цвета. Внешний вид зоны дегенерации стал причиной еще одного названия данной патологии - желточная дистрофия.
Также подобную дегенерацию принято называть детской, так как выявляется она только у детей 5 - 15 лет.
Причины возникновения
Дистрофия Беста по методу наследования отнесена к аутосомно-доминантному типу. К развитию заболевания прямое отношение имеет ген, который находится на длинном плече хромосомы номер одиннадцать.
Заранее выявить заболевание невозможно, оно проходит бессимптомно. В редких случаях пациенты могут жаловаться на проблемы с чтением мелкого шрифта, иногда наступающее затуманивание зрения, а также метаморфопсии. Особенно часто подобную патологию выявляют случайно на очередном офтальмологическом осмотре.
Признаки заболевания
Дистрофия Беста возникает вследствие скопления транссудата под пигментным эпителием. Подобное скопление иногда может достигать трех размеров диаметра диска зрительного нерва и вести к офтальмологическим изменениям в зоне макулы глаза. В зависимости от интенсивности подобных изменений, принято выделять определенные стадии развития заболевания:
- Превителлифомную стадию, когда в макуле обнаруживаются мелкие желтые пятна и минимальное нарушение пигментации;
- Вителлиформную стадию с вителлиформной кистой в макуле;
- Стадию разрыва кисты и резорбции её содержимого;
- Стадию образования фиброглиального рубца.
В своем развитии, болезнь Беста строго проходит стадии не всегда, иногда возможны незначительные вариации проявлений заболевания. Изменения, как правило, имеют двусторонний, асимметричный характер. Острота зрения снижается только к 3-ей стадии, оставаясь в пределах от 0,02 до 1,0D. С течением времени возможна дегенерация внешних составляющих фоторецепторов. Без должного адекватного лечения болезнь Беста может быть осложнена образованием субретинальной мембраны и субретинальными кровоизлияниями. В редких случаях, подобное состояние может привести к отслойке сетчатки, а также хориоидальному склерозу.
Диагностика болезни Беста
Диагностирование детской дегенерации желтого пятна происходит на основании результатов офтальмоскопии, показаний электроретинографии и электроокулографии. Нередко для ее подтверждения применяют и флуорисцентную ангиографию. В сложных ситуациях для помощи в диагностике может понадобиться обследование членов семьи пациента.
В случае четко выраженной желточной кисты поставить диагноз, труда не составляет, но при нечетких границах кисты и резорбции ее содержимого, необходимо провести дифференциальную диагностику. Дифференцировать болезнь Беста необходимо от миопического макулита, болезни Штаргардта, серозного отека макулы, кистозной дистрофии макулярной зоны, хороидита.
Лечение заболевания
Действенного и эффективного лечения болезни Беста в настоящее время не существует. Так как, заболевание обычно бессимптомно, беспокоящих пациента, врачи, как правило, не предпринимают каких-либо особых мер. В случае формирования субретинальной мембраны, которая способна вызывать незначительные дефекты зрения, иногда проводится лазерная коагуляция сетчатки.
В сравнении с болезнью Беста, дегенерация желтого пятна у взрослых не прогрессирует, кроме того, она сопровождается меньшими очагами поражения.
В медицинском центре «Московская Глазная Клиника» все желающие могут пройти обследование на самой современной диагностической аппаратуре, а по результатам - получить консультацию высококлассного специалиста. Мы открыты семь дней в неделю и работаем ежедневно с 9 ч до 21 ч. Наши специалисты помогут выявить причину снижения зрения, и проведут лечение выявленных патологий. Опытные рефракционные хирурги, детальная диагностика и обследование, а также большой профессиональный опыт наших специалистов обеспечивают благоприятный результат для пациента.
Периферическая дистрофия сетчатки
Периферическая дистрофия сетчатки - заболевание, характеризующееся истончением внутренней оболочки глаза в периферических отделах. Длительное время патология имеет бессимптомное течение. При выраженном поражении сетчатой оболочки появляются «мушки» перед глазами, нарушается функция периферического зрения. Диагностика включает в себя офтальмоскопию, периметрию, УЗИ глаза, визометрию и рефрактометрию. При начальных проявлениях дистрофии показана консервативная терапия (ангиопротекторы, антиагреганты, антигипоксанты). Выраженные дегенеративные изменения требуют хирургической тактики (лазерной коагуляции в зонах поражения сетчатки).
Общие сведения
Периферическая дистрофия сетчатки - распространенная патология в современной офтальмологии. В промежуток времени с 1991 по 2010 год число пациентов возросло на 18,2%. В 50-55% случаев заболевание развивается у людей с аномалиями рефракции, среди них 40% - больные миопией. Вероятность дистрофических изменений при нормальной остроте зрения составляет 2-5%. Первые симптомы патологии могут возникать в любом возрасте. Нозология с одинаковой частотой встречается среди лиц мужского и женского пола, однако к решетчатой дистрофии наиболее предрасположены мужчины, что обусловлено генетическими особенностями наследования.
Причины периферической дистрофии сетчатки
Патология может развиваться у лиц с миопическим или гиперметропическим типом рефракции, реже - при отсутствии нарушений зрительных функций. Более подвержены риску больные миопией. Этиология заболевания до конца не изучена. Решетчатая дистрофия наследуется по Х-сцепленному типу. Другие основные причины дистрофии сетчатки:
- Воспалительные заболевания глаз. Локальные поражения сетчатки, вызванные продолжительным течением ретинита или хориоретинита, лежат в основе дегенеративно-дистрофических изменений периферических отделов оболочки.
- Нарушение местного кровоснабжения. Региональные изменения кровотока приводят к трофическим расстройствам и истончению внутренней оболочки глазного яблока. Предрасполагающими факторами выступают артериальная гипертензия, атеросклеротическое поражение сосудов.
- Травматические повреждения. К периферической дистрофии приводит тяжелая черепно-мозговая травма и поражение костных стенок глазницы.
- Ятрогенное влияние. Изменения внутренней оболочки развиваются после витреоретинальных операций или превышения мощности воздействия при лазерной коагуляции сетчатой оболочки.
Патогенез
Пусковой фактор развития периферической дистрофии - расстройства локальной гемодинамики. Наиболее чувствительны к недостатку кислорода периферические отделы оболочки. При длительном нарушении трофики сетчатка истончается по периферии, что часто незаметно при осмотре глазного дна. Первые проявления возникают на фоне перенесенных инфекционных заболеваний, интоксикации или диабета в стадии декомпенсации. Потенцирует прогрессирование дистрофии миопический тип рефракции. Это связано с тем, что при увеличении продольной оси глазного яблока внутренняя оболочка глаза также поддается незначительному растяжению, что приводит к еще большему истончению по периферии. Определенную роль в механизме развития заболевания отводят дегенеративным изменениям стекловидного тела, при котором возникают тракции и вторичное повреждение сетчатки.
Классификация
В зависимости от морфологической картины патологию классифицируют на решетчатый, инееподобный и кистевидный типы. Отдельные варианты дистрофических изменений по внешнему виду напоминают «след улитки» и «булыжную мостовую». С клинической точки зрения выделяют следующие формы заболевания:
- Периферическая хориоретинальная дистрофия (ПХРД). При данном варианте нозологии в патологический процесс вовлечена сетчатка и хориоидеа.
- Периферическая витреохориоретинальная дистрофия (ПВХРД). Характеризуется поражением стекловидного тела, сетчатой и сосудистой оболочки.
Классификация витреохориоретинальных дистрофий по локализации:
- Экваториальные. Это наиболее распространенная зона поражения сетчатки, т. к. область истончения расположена по окружности глаза во фронтальной плоскости.
- Параоральные. При данном типе дистрофические изменения локализируются у зубчатой линии.
- Смешанные. Форма ассоциирована с наибольшим риском разрыва из-за наличия диффузных изменений по всей поверхности сетчатой оболочки.
Симптомы периферической дистрофии сетчатки
Длительное время поражение сетчатой оболочки протекает без клинических проявлений. Для патологии характерно снижение периферического зрения, что ведет к затрудненной ориентации в пространстве. Из-за того, что поле зрения сужается по концентрическому типу, больные могут выполнять только определенные виды зрительной работы (читать, рисовать). Функция центрального зрения при условии отсутствия аномалий рефракции не страдает. В редких случаях пациенты предъявляют жалобы на появление плавающих мушек перед глазами или дефектов зрительного поля в виде скотом. Такие симптомы, как «молнии» или вспышки яркого света свидетельствуют о разрыве сетчатки и требуют немедленного вмешательства. Для периферической дистрофии характерно одностороннее течение, но при решетчатом варианте в большинстве случае поражаются оба глаза.
Осложнения
Наиболее распространенное осложнение периферической дистрофии - разрыв сетчатки. Повреждение внутренней оболочки возникает в участках наибольшего истончения при воздействии таких факторов, как вибрация, погружение под воду, интенсивные физические нагрузки. Стекловидное тело часто фиксировано к краю дистрофии, что ведет к дополнительному возникновению тракции. У пациентов с изменениями периферии сетчатой оболочки также наблюдается высокий риск отслойки сетчатки. Больные более склонны к кровоизлияниям в полость стекловидного тела, реже - в переднюю камеру глаза.
Диагностика
В силу того, что для данной патологии часто характерно бессимптомное течение, тщательное обследованное пациента играет ведущую роль в постановке диагноза. Для визуализации дистрофии по периферии сетчатки необходимо проведение следующих офтальмологических исследований:
- Офтальмоскопия. Зона поражения при решетчатой форме и дистрофии по типу «следа улитки» локализируется в верхне-наружном квадранте у экватора глаза. Из-за зон облитерации сосудов на сетчатке образуются темные и светлые пятна, напоминающие решетку, или перерванные линии, которые называют «следами улитки». Инееподобная дистрофия имеет вид желто-белых включений, расположенных над поверхностью сетчатой оболочки.
- Периметрия. Методика позволяет выявить концентрическое сужение полей зрения. При подозрении на то, что у пациента имеются начальные проявления болезни, рекомендовано применять квантитативный способ периметрии.
- Визометрия. Исследование дает возможность диагностировать нормальное центральное зрение на фоне снижения периферического. Острота зрения снижается в случае возникновения патологии на фоне миопии.
- Рефрактометрия. Методика применяется для изучения клинической рефракции с целью выявления пациентов из группы риска.
- УЗИ глаза. Позволяет визуализировать начальные проявления патологии. При мелкокистозной дистрофии определяются множественные округлые образования разного диаметра. УЗИ используют для диагностики изменений стекловидного тела, выявления спаек и тракций, оценки размеров продольной оси глаза.
Лечение периферической дистрофии сетчатки
Выбор терапевтической тактики зависит от характера течения патологии. Перед началом лечения глазное дно осматривают в условиях максимального мидриаза. Для устранения проявлений периферической дистрофии применяют:
- Консервативную терапию. Используется только при диагностике минимальных проявлений болезни. Пациентам показан пероральный прием лекарственных средств из группы антиагрегантов, ангиопротекторов и антигипоксантов. В качестве вспомогательных препаратов применяются биоактивные добавки, витамины группы С, В.
- Хирургическое вмешательство. Оперативное лечение периферической формы заболевания сводится к проведению лазерной коагуляции сосудов в зонах наибольшего истончения. Цель вмешательства - профилактика возможных разрывов. Операция проводится в амбулаторных условиях. В послеоперационном периоде необходима консервативная терапия, включающая метаболические средства, антигипоксанты и ангиопротекторы.
Прогноз и профилактика
Прогноз для жизни и в отношении зрительных функций благоприятный. Пациентам из группы риска необходимо 1-2 раза в год, а также при появлении новых симптомов патологии проходить обследование у офтальмолога. Неспецифические превентивные меры сводятся к контролю уровня глюкозы крови, артериального и внутриглазного давления. При миопической рефракции необходима коррекция остроты зрения при помощи очков или контактных линз. Выявление у больного объективных признаков дистрофии требует исключения экстремальных видов спорта, тяжелых физических нагрузок.
Болезнь Беста
Болезнь Беста - одна из форм двухсторонней центральной (макулярной) пигментной абиотрофии сетчатки, приводящая к дистрофии фоторецепторов желтого пятна и значительному ухудшению зрения. Характеризуется первоначально бессимптомным течением, со временем падает острота зрения, возникает центральная скотома. Диагностика производится на основании осмотра глазного дна, данных электроокулографии и флюоресцентной ангиографии сосудов сетчатки, генетических исследований. Специфического лечения болезни Беста не существует, используется поддерживающее лечение для замедления прогрессирования проявлений патологии.
Болезнь Беста (центральная пигментная абиотрофия, вителлиформная дистрофия Беста) - генетическое заболевание, характеризующееся развитием кистозных дистрофических изменений в области желтого пятна. Впервые описано в 1905 году Ф. Бестом, который изучил идентичные нарушения зрения у восьми родственников и высказал предположение о наследственной природе патологии. Болезнь Беста с одинаковой частотой поражает как мужчин, так и женщин, встречаемость составляет примерно 3-4:100000. В отличие многих других форм абиотрофии сетчатки болезнь Беста редко приводит к полной слепоте, кроме того, характеризуется длительным многостадийным течением. На первоначальных этапах патологии нарушения зрения не развиваются, и нет практически никаких симптомов, изменения на сетчатке нередко бывают случайной находкой при медицинском осмотре у врача-офтальмолога. Своевременно назначенная поддерживающая терапия может значительно замедлить развитие болезни Беста.
Причины болезни Беста
Причиной дистрофии сетчатки, которая имеет место при болезни Беста, является мутация гена BEST1, локализованного на 11-й хромосоме. Он кодирует белок бестрофин, относящийся к классу анионных каналов пигментного эпителия сетчатой оболочки глаза. Патогенез нарушений при болезни Беста досконально не изучен - выяснено, что при этой патологии происходит медленное разрушение пигментного эпителия в области желтого пятна, и изменяются свойства мембраны Бруха. В результате этого происходит прорастание капилляров в субретинальное пространство, в сетчатке накапливаются гранулы вещества, по своим биохимическим свойствам схожего с липофусцином. Макроскопически при болезни Беста в области желтого пятна медленно нарастают пигментные нарушения, затем возникает киста, которая перекрывает поступление света к большей части фоторецепторов макулярной области. Затем происходит разрыв кисты, ее содержимое резорбируется, на ее месте формируется рубец, который и является причиной стойких нарушений зрения.
Механизм наследования мутаций гена BEST1 - аутосомно-доминантный с достаточно высокой пенетрантностью. Помимо болезни Беста, нарушения структуры этого гена могут быть причиной некоторых других форм пигментной дегенерации сетчатки, бестрофинопатии, вителлиформной дистрофии взрослых. Последняя по своему течению очень похожа на болезнь Беста, но в отличие от нее развивается не в детском, а взрослом возрасте. Это позволяет предположить, что вителлиформная дистрофия взрослых является разновидностью синдрома Беста - современная генетика пока не обнаружила иных мутаций, которые приводили бы именно к этому состоянию.
Симптомы болезни Беста
Первые изменения на глазном дне при болезни Беста возникают в возрасте 2-5 лет, однако субъективных симптомов при этом не наблюдается. Поэтому заболевание диагностируется либо по итогам случайного медицинского обследования, либо в более позднем возрасте, после развития первых нарушений зрения. В целом болезнь Беста характеризуется определенной стадийностью.
Нулевая стадия болезни Беста диагностируется очень редко, так как при ней нет даже незначительных изменений в области желтого пятна. Наблюдается только снижение фовеального рефлекса и изменения электроокулографии. При изучении последней выявляется снижение коэффициента Ардена. Иногда такие проявления регистрируются у взрослых без дальнейшего развития клинической картины болезни Беста - это считается признаком носительства мутации гена BEST1.
В течение первой стадии субъективные симптомы все также не выражены, лишь в некоторых случаях наблюдается незначительное снижение остроты зрения. На глазном дне выявляются несколько желтоватых точек в макулярной области сетчатки. Во время второй стадии точки разрастаются до размеров, сопоставимых с диаметром диска зрительного нерва, и внешне схожи с яичным желтком. Нарушения остроты зрения на этой стадии болезни Беста не соответствуют офтальмологической картине и незначительны - она сохраняется на уровне 0,6-0,9. На третьей стадии болезни Беста происходит разрыв вителлиформных кист, что приводит к резкому снижению остроты зрения. Также распространенными жалобами на этой стадии являются затуманивание зрения, трудности с чтением мелкого текста. Четвертая стадия характеризуется резорбцией продуктов разрыва кист и формированием на их месте рубца. Острота зрения у разных пациентов на этом этапе составляет от 0,02 до 0,7, кроме того, возникает относительная центральная скотома и псевдогипопион. Границы поля зрения, как правило, не изменяются, сохраняется нормальное восприятие цветов.
Длительность каждой стадии у разных больных может колебаться в широких пределах. Кроме того, в некоторых случаях болезнь Беста может развиваться более быстро, поэтому некоторые стадии не диагностируются. Изменения на глазном дне обоих глаз чаще всего имеют асимметричный характер. Как правило, полной слепоты не наступает, одним из осложнений болезни Беста может быть формирование субретинальной неоваскулярной мембраны, значительно снижающей остроту зрения. Кроме того, с возрастом на месте рубцов после вителлиформных кист возможно развитие хориодального склероза.
Диагностика болезни Беста производится при помощи методов современной офтальмологии - осмотра глазного дна, электроокулографии, флюоресцентной ангиографии сосудов сетчатки. При осмотре в зависимости от стадии заболевания выявляются либо желтые точки, либо сформировавшиеся вителлиформные кисты, сконцентрированные в центре. После их разрыва (третья стадия болезни Беста) картина глазного дна напоминает «яичницу-болтушку». Кроме того, на любом этапе заболевания могут возникать ретинальные кровоизлияния, также заметные при осмотре. На последней стадии болезни Беста формируется псевдогипопион, заметны пигментные отложения в области желтого пятна.
Одним из самых первых проявлений заболевания является аномальная картина электроокулографии, которая регистрируется еще до появления первых изменений на глазном дне. Патогномоничный признак болезни Беста - снижение коэффициента Ардена или отношения светового пика к световому спаду, который на конечных этапах развития патологии не превышает 1,5. При флюоресцентной ангиографии на первых стадиях болезни (до образования вителлиформных кист) наблюдаются участки локальной гиперфлюоресценции, соответствующие местам атрофии пигментного эпителия. После образования кист (вторая стадия болезни Беста) в местах их локализации обнаруживают полное отсутствие флюоресценции, а при их разрыве (третья стадия) - гиперфлюоресценцию в верхних частях кист и ее отсутствие в нижних.
Врачом-генетиком может быть произведена и генетическая диагностика болезни Беста, которая сводится к секвенированию последовательности гена BEST1 с целью поиска мутаций. Это исследование относится к достаточно сложным, так как в этой области 11-й хромосомы расположено огромное количество генов, мутации многих из них также способны приводить к наследственным офтальмологическим заболеваниям. Дифференциальную диагностику болезни Беста проводят с синдромом Коатса и отслойкой пигментного эпителия. В отличие от них центральная пигментная абиотрофия всегда имеет двухсторонний характер и характеризуется аномальной электроокулографией.
Лечение и прогноз болезни Беста
Специфического лечения болезни Беста не существует, в связи с чем используют поддерживающую терапию, способную значительно замедлить прогрессирование патологии. К ней относят назначение витаминов А и Е, сосудорасширяющих и улучшающих трофику сетчатки средств - мельдоний, метилэтилпиридинол, этилметилгидроксипиридина сукцинат. Это тормозит развитие и последующий разрыв вителлиформных кист, позволяя сохранять удовлетворительную остроту зрения длительное время. В тех случаях, когда болезнь Беста осложнилась образованием субретинальной неоваскулярной мембраны, показана лазерная коррекция.
Прогноз болезни Беста, как правило, условно благоприятный. Полная потеря зрения наступает в очень редких случаях, обычно все ограничивается снижением остроты зрения и относительной центральной скотомой. Периферическое и сумеречное зрение не страдает, больные в дальнейшем только затрудняются при работе с небольшим шрифтом и мелкими деталями. При вителлиформной дистрофии взрослых нарушения зрения выражены еще слабее, в ряде случаев больные совсем не имеют жалоб, а наличие болезни определяется только офтальмологическими и генетическими исследованиями.
Абиотрофия сетчатки ( Дегенерация сетчатки , Дистрофия сетчатки )
Абиотрофия сетчатки - разнородная группа наследственных заболеваний дистрофического характера, обусловленных постепенным разрушением сетчатки со снижением остроты зрения, а при некоторых формах - полной слепотой. Симптомы вариабельны: может наблюдаться снижение остроты зрения, гемералопия, нарушения цветового восприятия. Диагностика осуществляется офтальмологическими и генетическими методами (офтальмоскопия, электроретинография, флуоресцентная ангиография, изучение семейного анамнеза и выявлением дефектных генов). При большинстве форм абиотрофии сетчатки специфическое лечение отсутствует, симптоматическая и поддерживающая терапия способна ослабить некоторые симптомы и замедлить прогрессирование болезни.
МКБ-10
Абиотрофия сетчатки (дегенерация сетчатки, дистрофия сетчатки) - патология органа зрения, при которой развивается дистрофия сетчатой оболочки глаза. Может быть частью симптомокомплекса некоторых наследственных заболеваний, выступать как самостоятельная патология, в некоторых случаях возможна вторичная дегенерация после травм и других воздействий.
Самостоятельные наследственные формы абиотрофии сетчатки имеют разную распространенность, в среднем она колеблется в пределах 1-10:10000. Механизм наследования различных форм может быть аутосомно-доминантным, аутосомно-рецессивным и сцепленным с полом. По этой причине наблюдаются сильные различия и в половом распределении заболевания - от равной поражаемости лиц обоих полов до практически полного превалирования мужчин среди заболевших (при Х-сцепленном наследовании). Генетически обусловленная абиотрофия сетчатки - наиболее распространенная причина потери зрения наследственного характера.
Причины
Этиология абиотрофии сетчатки различается в зависимости от конкретного типа заболевания. Общий механизм - мутация определенного гена или генов, которые кодируют специфические белки, участвующие в жизнедеятельности сетчатой оболочки глаза. При этом патогенез большинства форм изучен недостаточно.
Пигментная дистрофия сетчатки. Причиной наиболее распространенной формы абиотрофии сетчатки - пигментной дистрофии - могут являться более 150 вариантов мутаций в нескольких десятках генов, большинство из которых наследуются по аутосомно-доминантному типу. Почти четверть всех случаев пигментной абиотрофии сетчатки обусловлена различными мутациями в гене белка опсина. В гене белка фоторецепторов CRB1 мутация имеет рецессивный характер наследования, а в генах RP2 и RPGR - сцепленный с Х-хромосомой.
Существует редчайшая форма пигментной абиотрофии сетчатки с мутацией в митохондриальной ДНК и, следовательно, наследованием от матери потомству. Несмотря на огромное количество разнообразных вариантов первичного нарушения при пигментном ретините, патогенез заболевания в целом одинаков - происходит нарушение утилизации отработанных палочек, в результате чего они становятся источником токсинов в сетчатке. Из-за того, что концентрация палочек растет по направлению к периферии сетчатой оболочки, патологические изменения начинаются именно там, образование новых фоточувствительных клеток замедляется, что и ведет к снижению светочувствительности.
Белоточечная абиотрофия сетчатки ассоциируется с мутациями одного из четырех генов - RHO, PRPH2, RDH5 или RLBP1, при этом наиболее распространена форма, обусловленная изменениями гена PRPH2, кодирующего белок периферин. Заболевание наследуется по аутосомно-рецессивному типу. Предполагается, что периферин участвует в стабилизации мембран фоторецепторов, главным образом палочек, поэтому нарушения в его структуре делают их менее устойчивыми и приводит к их разрушению. Белоточечная абиотрофия сетчатки имеет прогрессирующее течение, при этом первые нарушения (которые заметны при осмотре глазного дна в виде белых точек) образуются на периферии сетчатки.
Желтопятнистая абиотрофия сетчатки (болезнь Штаргардта) также обусловлена мутациями нескольких генов. Наиболее распространенная форма желтопятнистой дегенерации сетчатой оболочки связана с нарушением структуры белка ABCA4, который выполняет транспортные и энергетические функции в мембранах фоторецепторов. Эта форма заболевания наследуется по аутосомно-рецессивному типу. Изменение структуры трансмембранного белка ABCA4 приводит к накоплению в сетчатке токсичных метаболитов (в частности, липофусцина), что и вызывает дистрофию светочувствительного слоя.
Другой вариант болезни Штаргардта с аутосомно-доминантным наследованием обусловлен изменением структуры белка ELOVL4, который контролирует образование длинноцепочных жирных кислот в тканях глаза. В этом случае дегенерация фоторецепторов связана с нарушением синтеза некоторых компонентов их мембран. Еще один тип желтопятнистой абиотрофии сетчатки ассоциируется с мутацией гена PROM1. Патогенез нарушений в этом случае досконально не изучен.
Абиотрофия сетчатки Беста вызвана мутациями гена BEST1, продуктом транскрипции которого является белок бестрофин, относящийся к классу анионных каналов. Наследование аутосомно-доминантное, патогенез дистрофии неизвестен.
Врожденная стационарная ночная слепота является генерализованной абиотрофией сетчатки с преимущественным поражением палочек, она также сопровождается другими нарушениями органа зрения - косоглазием, катарактой. Выделяют полную и неполную формы врожденной стационарной ночной слепоты, обе наследуются по Х-сцепленному механизму.
Полный тип обусловлен мутацией гена NYX, кодирующего белок, обеспечивающий передачу возбуждения от палочек биполярным клеткам. В результате этого передача информации от фоторецепторов нарушается, возникает гемералопия с практически полным отсутствием зрения в темноте, при этом острота и цветовое восприятие обычно не страдают.
Неполная форма связана с мутацией гена CACNA1F, продуктом которого является схожий белок, но он имеется как у палочек, так и у колбочек. При этом, однако, передача импульса не блокируется полностью, поэтому сумеречное зрение только ослаблено, но также страдает острота и цветовое восприятие.
В офтальмологии все наследственные формы дистрофии сетчатой оболочки глаза делят на три группы:
- Периферические, при которых нарушения возникают преимущественно по краям глазного дна, но при некоторых формах абиотрофии они могут прогрессировать и захватывать центральные области, вплоть до желтого пятна. Кроме того, при них сильнее всего страдает периферическое зрение, нарушается адаптация глаза к темноте, часто возникает гемералопия. К ним относят пигментную и белоточечную абиотрофию сетчатки.
- Центральные, которые характеризуются преимущественным поражением желтого пятна и центральных областей глазного дна. При этом нарушается цветовое восприятие, сильно падает острота зрения. Именно такие проявления сопровождают болезнь Штаргардта и болезнь Беста.
- Генерализованные. При некоторых мутациях или их сочетании абиотрофия сетчатки может затрагивать всю сетчатую оболочку глаза, поэтому некоторые исследователи выделяют и третью группу дистрофий - генерализованные. Врожденная стационарная ночная слепота относится именно к такому типу. Генерализованные нарушения сетчатки сопровождают другие наследственные заболевания - например, амавроз Лебера.
При этом из-за большого количества различных мутаций вышеописанное разделение несколько условно. Так, некоторые формы пигментной дистрофии могут приобретать генерализованный характер, а при мутации гена PROM1 (четвертый тип болезни Штаргардта) абиотрофия от центральных областей сетчатки может распространяться на периферию.
Симптомы абиотрофии сетчатки
Симптомы абиотрофии сетчатки довольно вариабельны из-за большого количества различных мутаций, которые приводят к развитию данной патологии. Но в тоже время, между различными вариантами дистрофии в пределах одной группы (периферические, центральные или генерализованные абиотрофии) имеется ряд схожих проявлений.
Периферические абиотрофии сетчатки (пигментная дистрофия, белоточечная абиотрофия) начинаются с преимущественного поражения палочек, поэтому одним из первых симптомов заболевания будет гемералопия. С прогрессированием патологии, при дальнейшем разрушении палочек, снижение ночного зрения может перерасти в его полную потерю - никталопию. Нарушается периферическое зрение, возникает концентрическая скотома, после которой поле зрения сужается настолько, что становится «трубчатым».
При белоточечной абиотрофии сетчатки более тяжелые нарушения чаще всего не развиваются, дневное зрение и цветовосприятие остается без изменений. В ряде случаев пигментной дистрофии в патологический процесс вовлекаются и колбочки, что ведет к падению дневного зрения, снижению его остроты и иногда полной слепоте. Течение заболевания может занимать десятки лет, хотя встречаются и быстротечные, а также ювенильные формы.
Центральные абиотрофии сетчатки характеризуются преимущественным поражением колбочек, концентрация которых наиболее высокая в области желтого пятна - поэтому их также называют макулодистрофиями. На первый план выступает резкое снижение остроты зрения, нарушается восприятие цветов, при полном разрушении фоторецепторов в центре глазного дна развивается центральная скотома.
Если патологический процесс не распространяется на периферические области сетчатки, то периферическое и сумеречное зрение затрагивается слабо. При формах абиотрофии, характеризующихся очаговым поражением фоторецепторов, развиваются слепые пятна в поле зрения. При особо тяжелых формах может возникать атрофия волокон зрительного нерва и полная слепота.
Полная форма врожденной стационарной ночной слепоты характеризуется выраженной никталопией с сохранением дневного зрения и цветового восприятия. При этом прогрессирования заболевания не происходит. Симптомами неполной формы ВСНС является умеренная гемералопия, пониженная острота зрения, аномалии цветового зрения, сложность адаптации к пониженной освещенности.
Пациенты с абиотрофией сетчатки должны быть проконсультированы генетиком и офтальмологом. Определение дистрофических процессов в сетчатой оболочке глаза производится на основании данных осмотра глазного дна, электроретинографии, исследования остроты зрения и цветового восприятия. Немаловажную роль играет изучение наследственного анамнеза, а также генетические исследования на предмет выявления мутаций в генах, ассоциированных с тем или иным типом абиотрофии сетчатки.
При пигментной дистрофии по периферии глазного дна выявляются очаги отложения пигмента, также они могут наблюдаться и на центральных участках при соответствующей форме заболевания. Отмечается сужение артериол сетчатки, а на поздних этапах возникает атрофия капилляров сосудистой оболочки глаза. В ряде случаев выявляется восковидная атрофия диска зрительного нерва. Электроретинография показывает значительное снижение амплитуды всех волн, что свидетельствует о резком уменьшении количества фоторецепторов в сетчатке. Секвенирование ДНК с целью выявления мутаций наиболее часто производится в отношении генов RP1, RHO, RDS, RLBP1, PRPF8 и ряда других.
Белоточечная абиотрофия сетчатки при осмотре глазного дна характеризуется наличием белых, иногда с металлическим оттенком, очагов, расположенных по периферии сетчатки. Артериолы сетчатой оболочки сужены, пигментные отложения представлены в единичном количестве, выявляется побледнение диска зрительного нерва. Изменения на электроретинографии выражены слабо и не являются надежным диагностическим критерием. Генетическая диагностика представлена секвенированием гена PRPH2.
При болезнях Штаргардта и Беста при офтальмоскопии обнаруживаются атрофические очаги светлого оттенка, нередко окруженные отложениями пигмента. Размеры и количество очагов может значительно отличаться и отражает тяжесть поражения сетчатой оболочки глаза. В основном они располагаются в центральных зонах, но могут распространяться и на периферию. На электроретинографии выявляется резкое снижение амплитуды волны А, что свидетельствует о преимущественном разрушении колбочек. Генетическая диагностика сводится к выявлению мутаций в генах ABCA4 и CNGB3 и изучению наследственного анамнеза.
Лечение абиотрофии сетчатки
Специфического этиотропного лечения любой формы абиотрофии сетчатки на сегодняшний момент не существует. В качестве поддерживающего лечения, задерживающего прогрессирование заболевания, используются препараты витаминов А, Е, рибофлавина. Сосудорасширяющие средства позволяют улучшить кровоснабжение сетчатки, что также замедляют дистрофические процессы.
В последние годы появились данные об успешном применении бионических имплантатов сетчатки (Argus, Argus 2), позволивших частично вернуть зрение пациентам, полностью утратившим его из-за абиотрофии. Некоторые наработки в области использования стволовых клеток, генной терапии также преследуют цель найти метод лечения абиотрофии сетчатки.
Прогноз
Из-за большого количества мутаций, которые являются причиной абиотрофии, и различного клинического течения дистрофических процессов в сетчатке прогноз практически всегда неопределенный. Некоторые типы пигментной дистрофии могут ограничиться гемералопией и нарушением периферического зрения, тогда как другие формы этой патологии ведут к полной слепоте. Путем приема препаратов витамина А в ряде случаев удается замедлить прогрессирование абиотрофии сетчатки, по некоторым данным использование солнцезащитных очков также позволяет достичь аналогичного результата.
Болезнь Беста - симптомы и лечение
Что такое болезнь Беста? Причины возникновения, диагностику и методы лечения разберем в статье доктора Рытик Нины Петровны, офтальмолога со стажем в 13 лет.
Над статьей доктора Рытик Нины Петровны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Болезнь Беста — это генетическое заболевание глаз, которое вызывает изменения в центральной области сетчатки, так называемой макуле. Первоначально оно протекает бессимптомно, но постепенно приводит к ухудшению остроты зрения и появлению слепого участка в центре поля зрения.
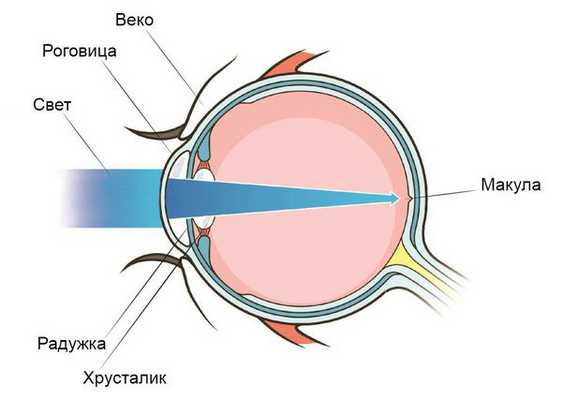
Возникновение и развитие болезни связано с дефектами в наследственном аппарате — мутациями гена VMD2 [3] . Область, в которой локализуется ген VMD2, известна врачам как область скопления генов, отвечающих за развитие большой группы гетерогенных генетических заболеваний с поражением глаз в комплексе с умственной отсталостью , ожирением , тугоухостью и другими патологиями органов и систем [11] .
Болезнь Беста наследуется по аутосомно-доминантному пути, т. е. вероятность возникновения заболевания не зависит от пола и тяжести течения болезни у родителей.
У данного заболевания высокая пенетрантность, т. е. болезнь развивается у большинства людей с патологическим геном. Несмотря на это, выраженность клинических проявлений у родственников варьирует от минимальных изменений и сохранения 100 % зрения до выраженного снижения остроты зрения (вплоть до 0,02) и инвалидизации. Проследить семейную отягощённость удаётся не всегда, даже при комплексном обследовании [2] .
Заболевание считается редким. Его распространённость составляет около 1 случая на 10000 населения [1] . Впервые упоминание о нём в литературе появилось в 1905 году: офтальмолог Ф. Бест описал его как двустороннюю макулодистрофию, которую он наблюдал у восьми членов одной семьи.
Факторов, способствующих манифестации заболевания при наличии наследственной предрасположенности, не выявлено.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
На начальных стадиях заболевание никак не проявляется, поэтому обычно оно диагностируется случайно при медицинском осмотре. Симптомы появляются только на более поздних стадиях патологии.
Манифестирует болезнь в возрасте 5-15 лет. Ребёнок жалуется на прогрессирующее, обязательно двустороннее снижение чёткости зрения: он начинает испытывать затруднение при чтении мелкого шрифта вблизи. Также его беспокоят "вспышки", "мерцание огоньков" и ухудшение цветовосприятия (в основном наблюдается цветослабость на жёлто-зелёный, зелёный, сине-зелёный цвета).
Изменения в большинстве случаев несимметричные, но возникают на обоих глазах. Острота зрения в зависимости от стадии болезни значительно колеблется: от 0,01 до 1,0.
Важно отличать болезнь Беста от вителлиформной макулодистрофии взрослых. Это заболевание также является генетическим, но возникает и прогрессирует оно в зрелом возрасте (около 40-50 лет). Для него характерно двустороннее, как правило, симметричное субретинальное поражение в центральной области сетчатки. Изменения так же, как при болезни Беста, имеют локальную, очерченную, круглую форму, желтоватый оттенок, но их размер всегда значительно меньше и они не прогрессируют [10] .
Патогенез болезни Беста
Патофизиологический механизм болезни Беста на данный момент неизвестен. Предполагается, что при данной патологии происходит аномальное накопление вещества, подобного липофусцину — жёлто-коричневому пигменту гликопротеиновой природы, который встречается во всех тканях и органах человека. Это вещество скапливается между пигментным эпителием сетчатки и слоем светочувствительных клеток — фоторецепторов. В результате нарушается мембрана Бруха (самый внутренний слой сосудистой оболочки глаза) и разрушаются нервные элементы сетчатки.
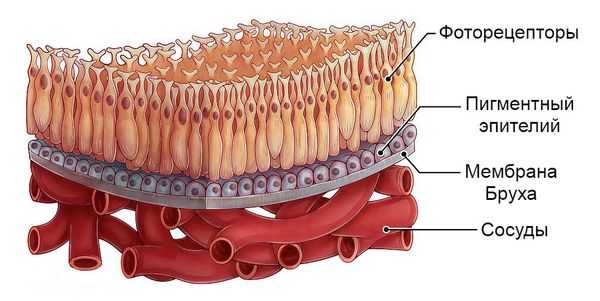
Большинство наружных сегментов фоторецепторов разрушается полностью, при этом во внутренних сегментах светочувствительных клеток скапливаются продукты кислых мукополисахаридов, вызывая изменения в сетчатке. Слой пигментного эпителия отделяется от слоя фоторецепторов, из-за чего формируется немного проминирующее (выбухающее) жёлтоватое образование, т.е. киста, которая локализуется в центральной или околоцентральной области сетчатки [3] .
Классификация и стадии развития болезни Беста
Заболевание относится к наследственным ретинальным дистрофиям. В Международной классификации болезней (МКБ-10) ему присвоен код H35.5.
Болезнь Беста всегда протекает с прохождением четырёх определённых стадий, которые завершаются образованием рубца в центральной области сетчатки [1] .
- Первая стадия — превителлиформная. Она предшествует формированию кисты. В макуле наблюдаются изменения пигментации в виде множества маленьких желтоватых очажков. Во время электроокулографии фиксируются аномальные изменения.
- Вторая стадия — вителлиформная. Формируется классическая вителлиформная киста, которая при осмотре очень похожа на "яичный желток" довольно крупных размеров (до 1 диаметра диска зрительного нерва). Изменения асимметричны и практически всегда поражают оба глаза. Офтальмоскопические изменения не соответствуют высокой остроте зрения: даже у пожилых пациентов этот показатель находится в пределах от 0,4 до 0,9.
- Третья стадия — разрыв кисты и её резорбция, т. е. рассасывание. Острота зрения снижается, пациентам становится трудно читать мелкий текст.
- Четвёртая стадия — формирование фиброглиального рубца на месте кисты. Также на этой стадии возможно развитие субретинальной неоваскуляризации — образование новых сосудов под сетчаткой [3] . Острота зрение падает ещё сильнее, в поле зрения появляются слепые зоны.
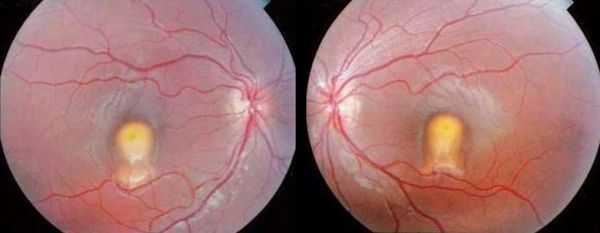
Осложнения болезни Беста
На поздних стадиях заболевания начинают развиваться осложнения. Самые частые — это образование сквозных разрывов в макулярной области, потеря центральной остроты зрения и формирование "пятна перед глазами". Возникновение отслойки сетчатки встречается реже.

Одним из частых осложнений так же является субретинальная неоваскуляризация — образование новых сосудов в зоне глазного дна [11] . Она является одной из причин инвалидизации при болезни Беста, так как приводит к стойкому снижению центральной остроты зрения. При этом полная слепота не развивается.
Для постановки диагноза "болезнь Беста" необходим ряд обследований. В первую очередь нужно зарегистрировать специфическую офтальмоскопическую картину глазного дна, характерную для каждой стадии заболевания. Затем, чтобы оценить состояние сетчатки, следует выполнить электроокулографию (ЭОГ) и электроретинографию (ЭРГ). В последние годы, с развитием генетики, стало обязательным молекулярное генетическое исследование пациента. Вместе с этим производят офтальмологическое и генетическое обследование других членов семьи.
Офтальмоскопия позволяет обнаружить первые признаки болезни Беста на первом и втором десятилетии жизни. На первых стадиях в макуле появляются желтоватые очажки, затем формируются виттелиформные кисты, при разрывах которых глазное дно напоминает картину "яичницы-глазуньи". На последних стадиях в макуле формируется атрофические глиальные рубцы, а при осложнениях — неоваскулярная мембрана и сквозные макулярные отверстия.
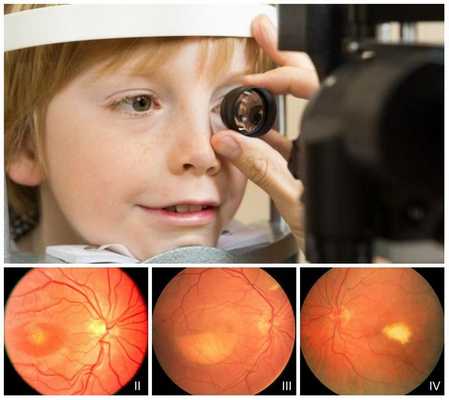
Электроокулография является очень важным методом диагностики при болезни Беста. С её помощью можно выявить такой специфический признак заболевания, как снижение коэффициента Ардена — соотношения биопотенциала глаз в темноте и при свете. Данный показатель будет снижен даже на нулевой стадии болезни при нормальной офтальмоскопической картине. В случае вителлиформной макулодистрофии взрослых электроокулография изменений не выявит.

Флюоресцентная ангиография позволяет диагностировать болезнь Беста даже на доклиническом этапе. Изменения сетчатки зависят от стадии заболевания. На начальном этапе болезни видны мелкие окончатые дефекты и участки с локальной гиперфлюоресценцией (свечением). При наличии сформированной кисты флюоресценция полностью отсутствует. На третьей стадии болезни гиперфлюоресценция наблюдается только в верхней части кисты, а в нижней её части отсутствует [8] .
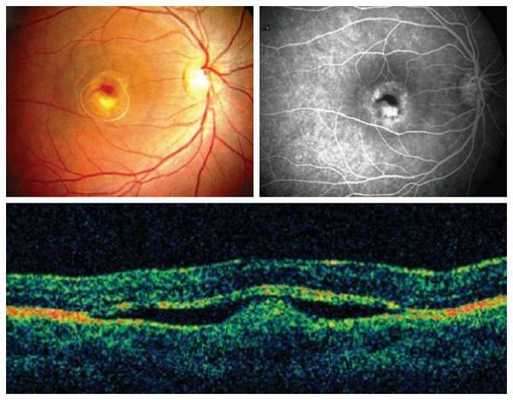
При электроретинографии (общей и ритмичной) наблюдается снижение амплитуды "а" волн, увеличение латентных периодов "а" и "b" волн, а также угнетение ответа от центральных отделов сетчатки [9] .
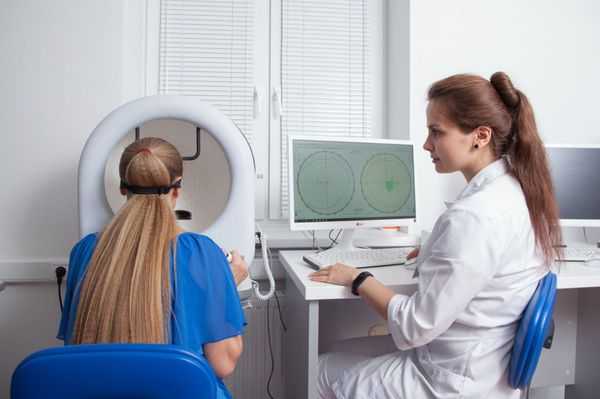
Статическая компьютерная периметрия выявляет снижение чувствительности макулярной области, а при разорвавшейся вителлиформной кисте — центральную абсолютную скотому (слепое пятно) . При этом границы поля зрения по периферии остаются в норме.
Дифференциальная диагностика
Болезнь Беста необходимо отличить от других заболеваний:
- болезни Коатса и других макулярных дистрофий пигментного эпителия сетчатки (Х-образной макулярной дистрофии);
- острого хориоретинита (в первую очередь токсоплазмозной этиологии);
- болезни Штаргардта;
- вителлиформной дистрофии взрослых;
- отслойки пигментного эпителия сетчатки [11] .
Болезнь Коатса — врождённая ненаследственная патология, при котором наблюдаются аномалии сосудов сетчатки глаза. Она может стать причиной частичной или полной слепоты. На первых стадиях болезнь Коатса так же, как и болезнь Беста, течёт без симптомов и в большинстве случаев диагностируется у детей 2-8 лет при случайных профилактических осмотрах, проводимых в детских садах или школах. В отличие от болезни Беста, при болезни Коатса, как правило, в патологический процесс вовлекается только один глаз. Лишь у 5-8 % больных наблюдаются двусторонние изменения. Мальчики заболевают им в 3 раза чаще, чем девочки [9] .
У большинства пациентов с заболеванием Коатса во время первого офтальмологического обследования в центральной области сетчатки выявляют возвышающийся округлый очаг твёрдого желтоватого экссудата, очень похожий на вителлиформные изменения, встречающиеся при болезни Беста. Данные экссудаты в центральной области сетчатки очень часто сочетаются с кровоизлияниями за сетчаткой и образованием новых сосудов, что тоже характерно для болезни Беста.
Диагностика болезни Коатса основывается на результатах осмотра глазного дна (офтальмоскопии), а также центральной области и периферии глазного дна с применением или налобного офтальмоскопа с линзами 20-30 дптр, или офтальмобиомикроскопии с трёхзеркальной линзой Гольдмана. У большинства пациентов с болезнью Коатса во время данного обследования обязательно выявляются аномалии сосудов: микро- и макроаневризмы, телеангиэктазии ( сосудистые звёздочки ), артериовенозные шунты. Чаще всего эти аномалии располагаются в височной половине сетчатки.
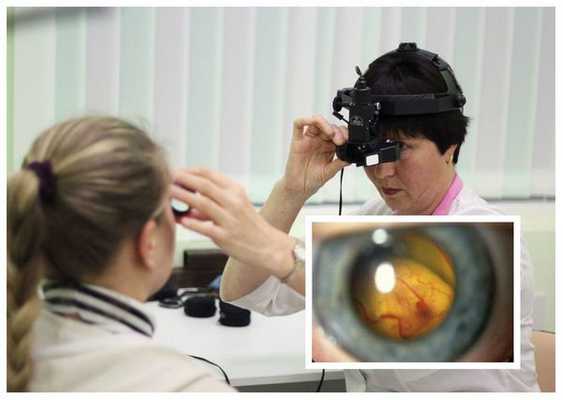
Изменения при электроокулографии в начальной и развитой стадиях заболевания, как и при болезни Беста, не выявляются. Но острота зрения у больных с ретинитом Коатса низкая: при наличии изменений в центральной области сетчатки она не превышает 0,4, а при болезни Беста длительно сохраняются в норме [7] .
Острый токсоплазмозный хориоретинит — это паразитарное заболевание глаз, для которого характерно в основном скрытое или хроническое течение. Как правило, оно поражает только один глаз, в отличие от болезни Беста. При неадекватном и несвоевременном лечении может привести к стабильному снижению остроты зрения.
Трудности при диагностике обычно возникают при обследовании больных с приобретённым токсоплазмозом и экссудативно-геморрагическими изменениями в центральной области сетчатки, которые похожи на вителлиформные очажки с субретинальными геморрагиями, как при болезни Беста. Хориоретинальные поражения при токсоплазмозе сочетаются с выпотом в стекловидное тело различной степени тяжести, а порой и изменениями переднего отрезка глаза.
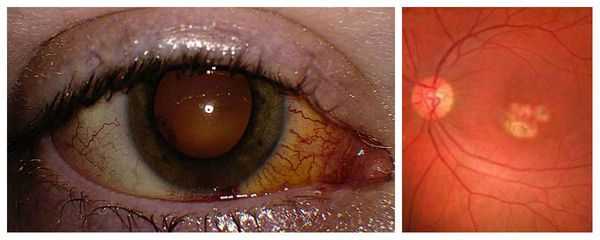
Пациенты, как правило, предъявляют жалобы на внезапное, резкое и значительное снижение центральной остроты зрения, которая в ряде случаев изменяется до 0,01-0,2. При статической периметрии регистрируется повышенный порог яркостной чувствительности, относительная или абсолютная центральная скотома. Электроокулография, как правило, не изменена.
Для подтверждения и верификации токсоплазмоза необходимо выполнить иммунологические исследования, определить антитела к токсоплазме или выделить её методом ПЦР (полимеразной цепной реакции). В 95 % случаев токсосплазмозный хориоретинит хорошо поддаётся лечению, острота зрения может восстановиться до исходных значений [12] .
Болезнь Штаргардта иначе называют ювенильной макулярной дегенерацией. Впервые это заболевание описал немецкий врач-офтальмолог К. Штаргардт как врождённое поражение макулы, которое передавалось по наследству в одной семье.
Как правило, болезнь Штаргардта начинается в молодом (ювенильном) возрасте и сопровождается поражением центральной области сетчатки, как и болезнь Беста. Её отличает быстрое прогрессирование, вплоть до инвалидизации. Медленное ухудшение зрения встречается крайне редко (при доминантном типе наследования) [9] .
Данное заболевание всегда двустороннее и симметричное. Его характерными признаками являются различные процессы: атрофия хориоидеи (сосудистой оболочки глаза), "бычий глаз", очаг дистрофии цвета "битой (кованой) бронзы" и др. При далеко зашедшем процессе фовеолярный рефлекс (центральная ямка макулы) отсутствует. В макулярной области на уровне пигментного эпителия сетчатки наблюдаются скопления коричневатого, тёмного пигмента, который окружён участками гипер- и депигментации. Эти скопления отличаются от вителлиформных жёлтых очагов при болезни Беста.
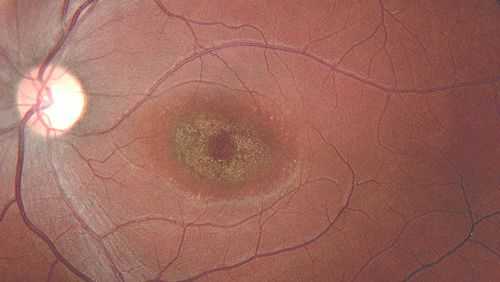
Вителлиформная макулодистрофия взрослых , в отличие от болезни Беста, развивается у людей 40-50 лет. Для неё характерно двустороннее симметричное поражение макулы с локальными изменениями. Очаги патологии, как правило, имеют округлую форму и жёлтый оттенок. Их отличает отсутствие прогрессирования и небольшие размеры: диаметр поражений достигает 0,3-0,5 размера диска зрительного нерва. При этом нарушения зрительных функций минимальны.
Вещества, подобные липофусцину, скапливаются диффузно в различных местах: в пигментном эпителии, внутренней части фоторецепторов, мюллеровских клетках и даже в стекловидном теле.
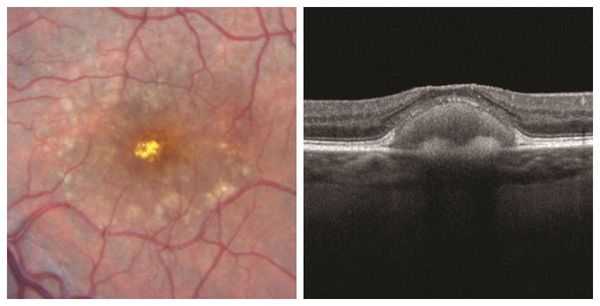
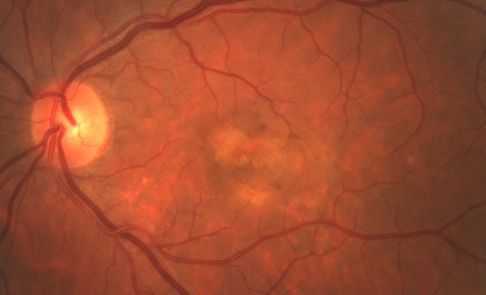
Отслойка пигментного эпителия сетчатки возникает при нарушении нормального соединения пигментного эпителия сетчатки с мембраной Бруха. К причинным факторам относятся сосудистые, воспалительные и дистрофические процессы.
Длительное время болезнь может существовать без какой-либо динамики, спонтанно исчезать, а вследствие инвазии сосудов из хориоидеи трансформироваться в геморрагическую отслойку. Сложности в диагностике могут возникнуть при атипичной клинической картине заболевания и экссудативных изменениях в центральной области сетчатки.
Обычно болезнь поражает только один глаз. Общая электроретинография не меняется, локальная — может быть снижена. Электроокулография, как правило, в норме. При флюоресцентной ангиографии на последней стадии отслойки регистрируется гиперфлюоресценция.
Лечение болезни Беста
Лечения болезни Беста на сегодняшний момент не существует. Можно лишь затормозить формирование кист, предотвратить их разрывы и наступление осложнений, которые сильно влияют на остроту зрения пациента. С этой целью применяется антиоксидантная и вазоактивная терапия, а также витамины С, Е и А. Вазоактивные препараты улучшают кровоснабжение сетчатки, а витамины являются мощными антиоксидантами [5] .
Вероятно, что в будущем при лечении болезни Беста будет применяться генная инженерия или терапия, направленная на нормализацию тока жидкости через пигментный эпителий сетчатки, торможение накопления липофусцина и воздействия на другие этапы патогенеза [13] .
Прогноз. Профилактика
Прогноз для зрения относительно благоприятный. Так как заболевание протекает медленно, острота зрения снижается постепенно, при этом страдает только центральное зрение. Благодаря сохранению периферического зрения человек хорошо адаптируется, часто сохраняя работоспособность и возможность чтения.
При обнаружении заболевания врач должен проинформировать больного о вариабельности течения заболевания, рисках его возникновения у будущих детей и функциональных прогнозах. Желательно проконсультироваться с врачом-генетиком.
Все члены семьи пациента обязательно должны пройти обследование у офтальмолога. Сам пациент должен регулярно наблюдаться у своего лечащего врача [14] .Чтобы дети и подростки не отставали в развитии, необходимо вовремя применять технические средства реабилитации слабовидящих [1] .
Читайте также:
