Очаги гиперфиксации рфп в тазобедренном суставе
Вопрос №2. Что такое радиофармпрепарат?
Радиофармпрепарат (РФП) – это соединение, состоящее из специального вещества и радионуклида (изотопа, радионуклидной метки). Специальное вещество отвечает за то, в каком органе накопится РФП, а радионуклидная метка позволяет врачу-диагносту увидеть это накопление на изображении.
В настоящее время для производства РФП используется очень широкий спектр как специальных веществ, так и радионуклидных меток. Во всем мире самым часто используемым у онкологических больных соединением специального вещества и радионуклидной метки является 18 F-фтордезоксиглюкоза ( 18 F-ФДГ). В данном соединении 18 F выполняет функцию радионуклидной метки, ФДГ – специального вещества.
Вопрос №3. Что такое физиологическое накопление РФП?
Физиологическое накопление (гиперфиксация) РФП – это повышенное накопление РФП, определяющееся в различных органах и системах в норме.
Физиологическое накопление наблюдается при исследованиях со всеми РФП: 18 F-ФДГ, 11 С-холином, 11 С-метионином, 68 Ga-ПСМА и т.д. В зависимости от типа РФП меняется лишь местоположение физиологической гиперфиксации. Например, при ПЭТ и ПЭТ/КТ с самой часто используемой 18 F-ФДГ физиологическое накопление РФП определяется в коре головного мозга, ротоглотке, носоглотке, мышцах гортаноглотки, миокарде левого желудочка, чашечно-лоханочных системах почек, фрагментарно по ходу петель толстой кишки, мочевом пузыре.
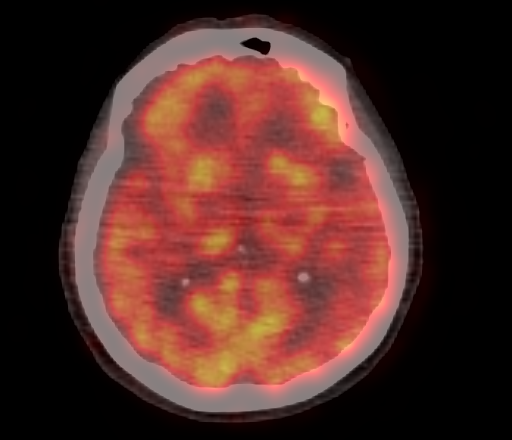 |  |
| Физиологическое накопление 18 F-ФДГ в коре головного мозга. | |
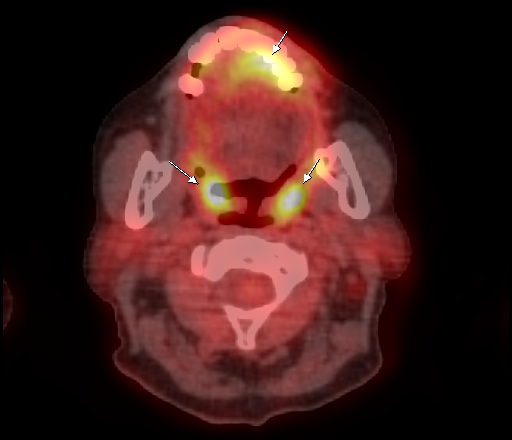 | 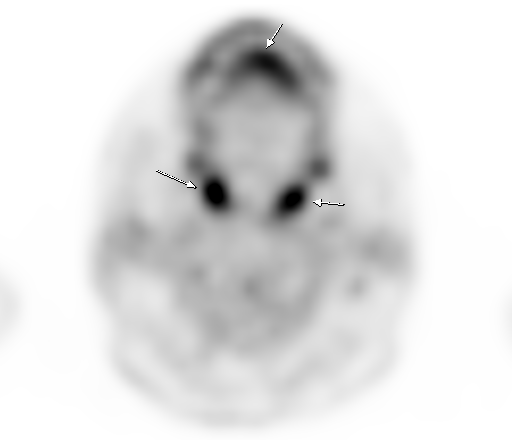 |
| Физиологическое накопление 18 F-ФДГ в ротоглотке. | |
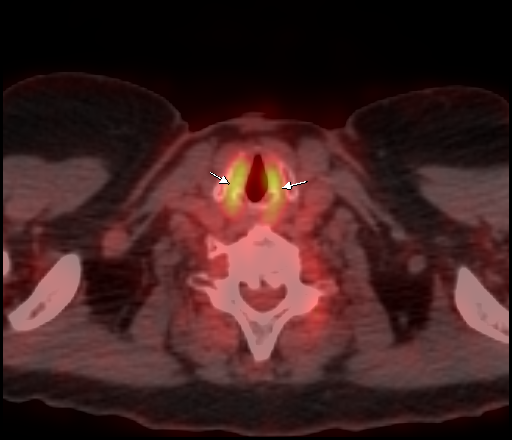 |  |
| Физиологическое накопление 18 F-ФДГ в мышцах гортаноглотки. | |
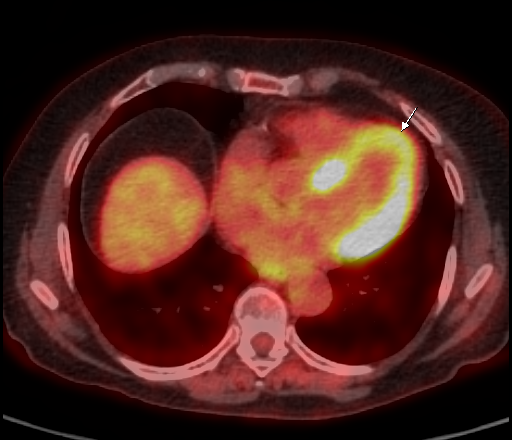 |  |
| Физиологическое накопление 18 F-ФДГ в миокарде левого желудочка. | |
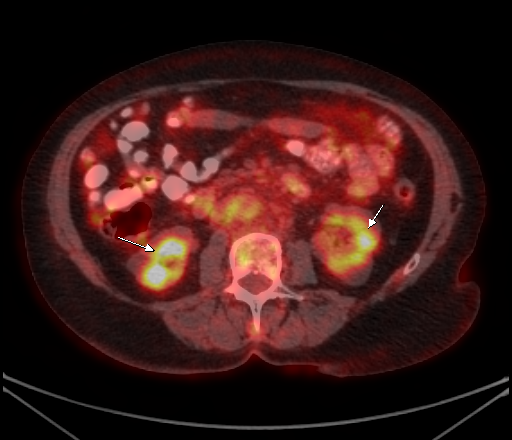 | 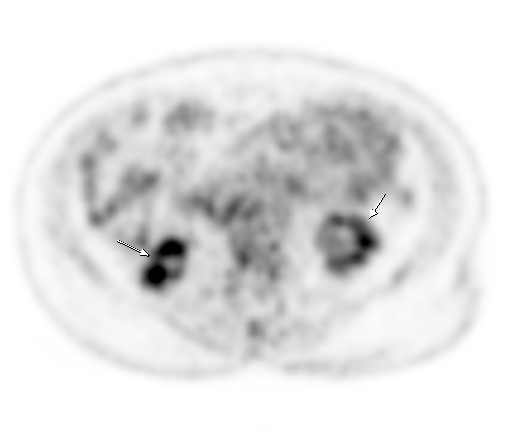 |
| Физиологическое накопление 18 F-ФДГ в чашечно-лоханочных системах почек. | |
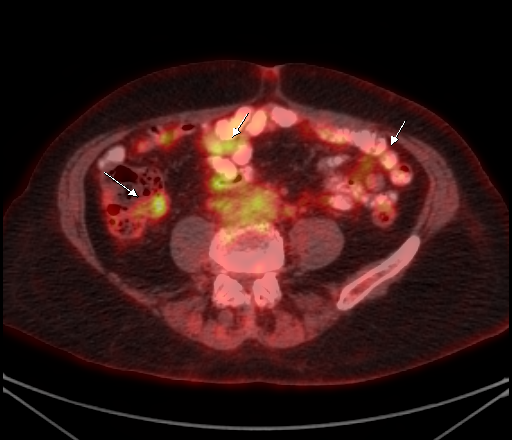 | 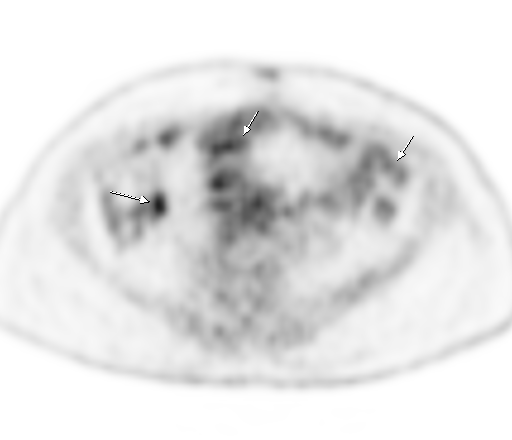 |
| Физиологическое накопление 18 F-ФДГ по ходу петель толстой кишки. | |
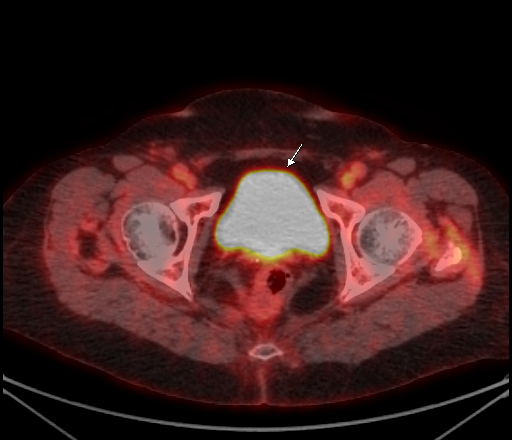 | 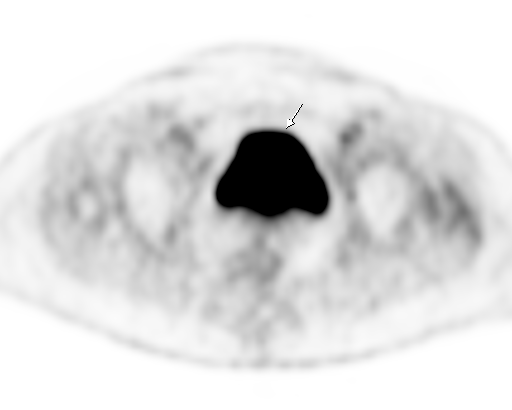 |
| Физиологическое накопление 18 F-ФДГ в мочевом пузыре. | |
Вопрос №4. Что такое патологическое накопление РФП?
Патологическое накопление РФП – это повышенное накопление РФП в органах и тканях, регистрирующееся при заболеваниях, чаще всего в злокачественных опухолях.
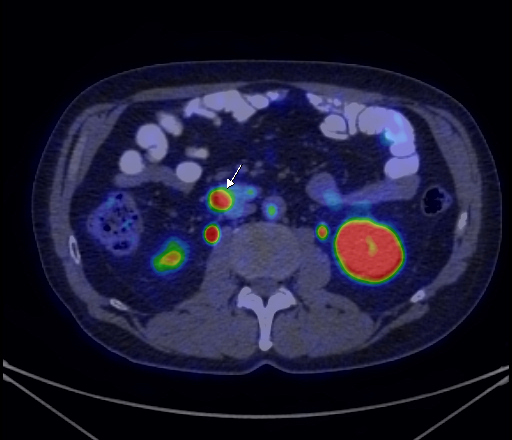 |
| Данные ПЭТ/КТ с 68 Ga-DOTA-TATE у пациента с нейроэндокринной опухолью тощей кишки. В проекции злокачественной опухоли, расположенной в тощей кишке, определяется очаг патологической гиперфиксации РФП. |
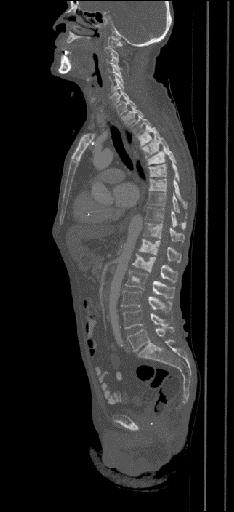 | 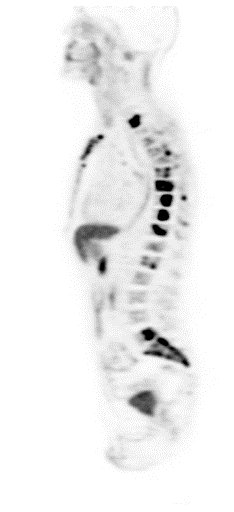 | 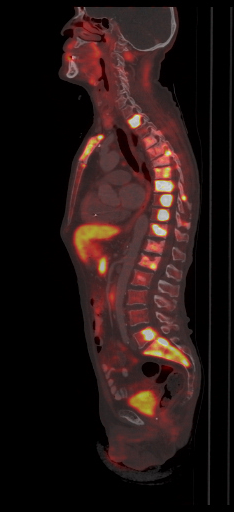 |
| Данные ПЭТ/КТ с 11 С-холином у пациента с раком предстательной железы. Состояние после простатэктомии. В костях скелета визуализируются множественные очаги патологического накопления РФП (метастазы). | ||
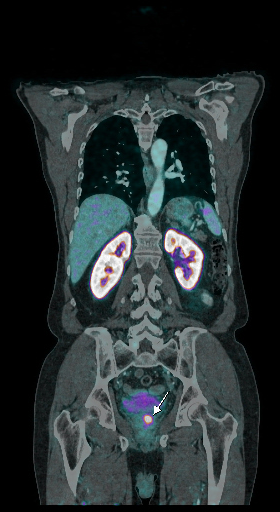 | 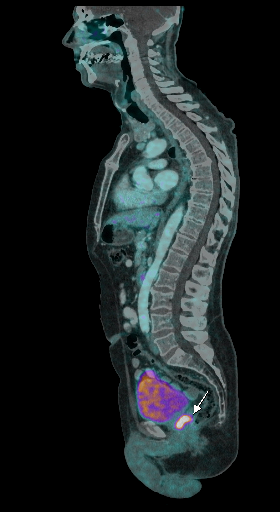 | 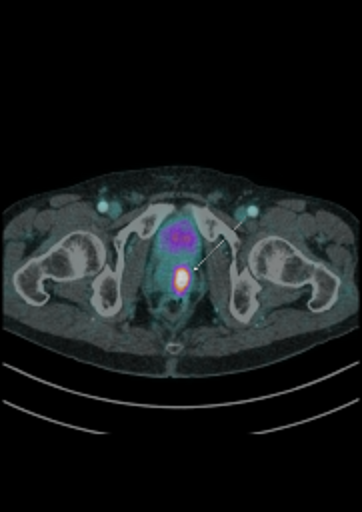 |
| Данные ПЭТ/КТ с 68 Ga-ПСМА у пациента с местным рецидивом рака предстательной железы. Состояние после лучевой терапии. В левых отделах предстательной железы определяется очаг патологического накопления РФП. | ||
Вопрос №5. Что такое метаболически активное и метаболически неактивное образование?
Метаболически неактивное образование – это образование, которое не накопило РФП. Чаще всего отсутствие повышенного накопления РФП в опухоли свидетельствует о ее доброкачественной природе.
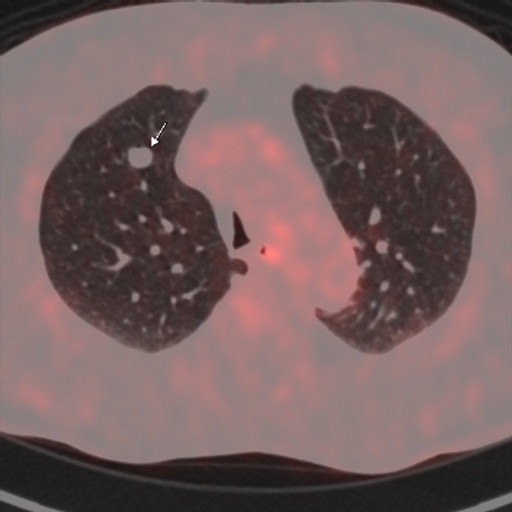 |
| Данные ПЭТ/КТ с 18 F-ФДГ у пациента с метаболически неактивным образованием правого легкого (доброкачественная опухоль - гамартома). |
Метаболически активное образование – это образование, в котором накопился РФП в повышенном количестве. Повышенное накопление РФП в опухоли чаще всего свидетельствует о ее злокачественном характере.
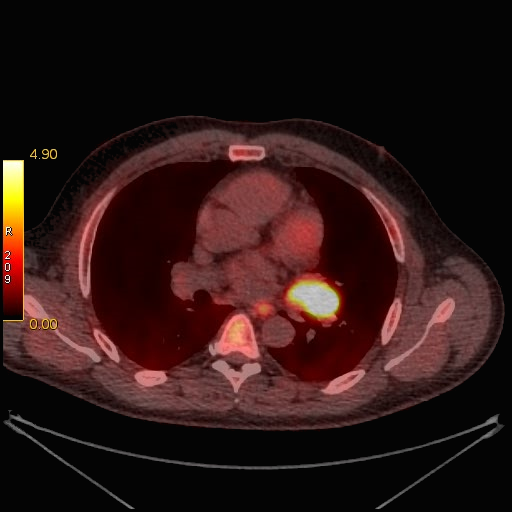 |
| Данные ПЭТ/КТ с 11 С-метионином у больного с метаболически активным образованием корня левого легкого (типичный карциноид). |
Вопрос №6. Что такое SUV?
SUV (Standardized Uptake Value, стандартизированный уровень захвата) – это величина, отражающая интенсивность накопления РФП в зоне интереса, например, в опухоли.
Показатель SUV рассчитывается программным комплексом автоматически и измеряется в различных единицах. В нашем Центре, как и в большинстве отечественных и зарубежных медицинских учреждений, где проводится позитронная эмиссионная томография, в качестве единиц измерения показателя SUV принято использовать г/мл (g/ml).
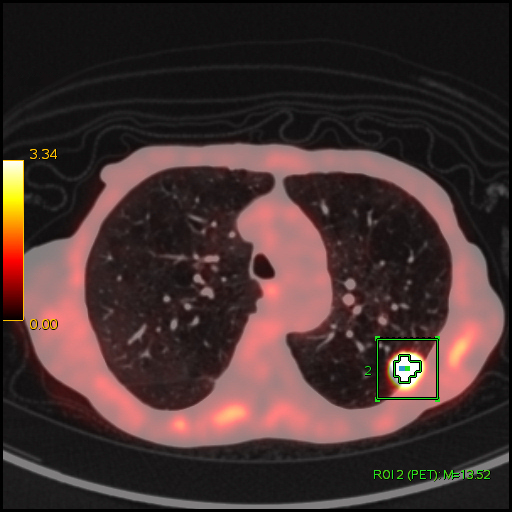 |
| Данные ПЭТ/КТ с 18 F-ФДГ. Оконтуривание метаболически активной злокачественной опухоли левого легкого для измерения показателя SUV. В данном случае величина SUV в опухоли определяется на уровне 13,52 g/ml. |
Вопрос №7. Для чего используется величина SUV?
Величина SUV в основном используется для оценки ответа злокачественной опухоли на проведенное лечение. Важно подчеркнуть, что в ряде клинических ситуаций показатель SUV в опухоли является единственным критерием, позволяющим оперативно получить информацию о чувствительности образования к только что начатой терапии.
Если опухоль чувствительна к лечению, то уровень SUV в ней при повторном ПЭТ-исследовании будет снижаться, если нечувствительна или малочувствительна (резистентна, устойчива) – значение SUV останется без изменений или увеличится. Следует помнить, что своевременная диагностика устойчивости опухоли к лечению позволит скорректировать план лечения, а в некоторых случаях и радикально его изменить.
Как уже было сказано выше, для оценки эффективности терапии врач-радиолог оценивает динамику показателя SUV до и после лечения.
Существует четыре варианта метаболического ответа опухоли на проведенное лечение:
- Частичный метаболический ответ – устанавливается при уменьшении значения SUV в опухоли на 25% и более;
- Полный метаболический ответ – заключается в отсутствии повышенного накопления РФП в опухоли;
- Метаболическое прогрессирование – устанавливается при увеличении SUV на 25% и более и/или при появлении новых очагов патологической гиперфиксации РФП;
- Метаболическая стабилизация – регистрируется при отсутствии достоверных (менее 25%) изменений показателя SUV в опухоли.
 |  |  |
| а | б | в |
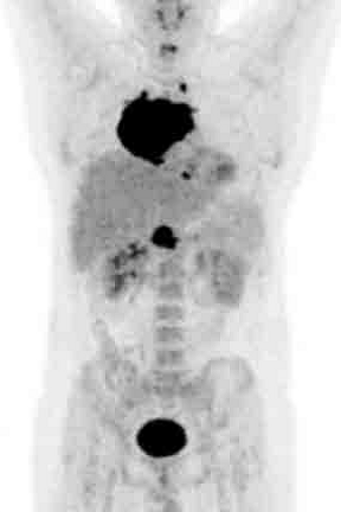
Результаты ПЭТ с 18 F-ФДГ у пациента с диффузной В-клеточной крупноклеточной лимфомой до лечения (а), после 2 курса ПХТ (б) и через 13 месяцев после окончания терапии (в).
а – до лечения в средостении визуализируется массивное метаболически активное образование с уровнем SUV=12,6;
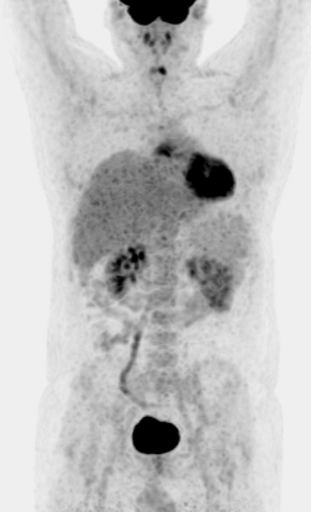
б – после 4 курса ПХТ отмечается значительное уменьшение метаболического объема опухоли и снижение показателя SUV до 3,4 (достигнут частичный метаболический ответ, т.е. опухоль чувствительна к выбранной ПХТ);
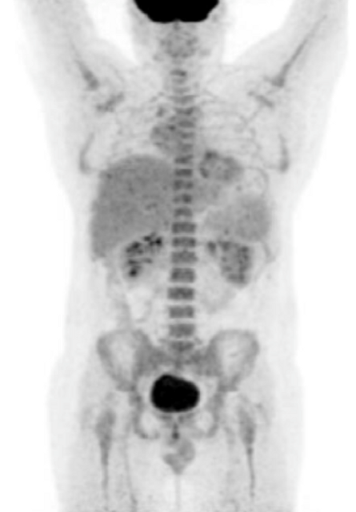
в – через 13 месяцев после окончания ПХТ очагов патологической гиперфиксации РФП в проекции органов средостения не обнаружено (достигнут полный метаболический ответ).
Какой из лучевых методов диагностики костных метастазов при РПЖ является наиболее точным и объективным? Какие дополнительные методы можно использовать в случае затруднения диагностики метастазов? Cреди лучевых методов (рентгено-, остеосцинти-, томограф
Cреди лучевых методов (рентгено-, остеосцинти-, томографии), широко используемых в современной урологической практике для ранней диагностики локализации и стадии течения метастатического процесса в костях, остеосцинтиграфия (ОСГ) в силу своей высокой чувствительности занимает приоритетное положение [3]. Невысокая специфичность данного метода значительно возрастает при дополнительном использовании других инструментальных методов (КТ, УЗИ, МРТ и т. д.), особенно при диагностировании смешанных и остеолитических очагов метастазов, а также когда визуальные рентгенологические признаки метастатического процесса отсутствуют [3].
Нами проведен ретроспективный анализ 8500 сканограмм больных (в возрасте 60-82 лет), полученных в отделении радиоизотопной диагностики ГВКГ им. Н. Н. Бурденко (1990-1998 годы). Из них изучено 450 (подробно 45) больных с подозрением на РПЖ (или с установленным раком простаты в анамнезе).
Все больные с РПЖ (в возрасте 60-82 лет) были разделены на четыре группы:
- Больные с подозрением на РПЖ, которым выполнена ОСГ.
- Больные c неинформативной картиной РПЖ на сканограммах, которые кроме ТР УЗИ и биопсии, подвергались МРТ для уточнения характера процесса.
- Больные с РПЖ, которым требуется уточнение стадии метастатического процесса и его характера.
- Больные, которым провели одновременное комплексное инструментальное обследование по схеме: ОСГ+МРТ+Ro-графия+ТР УЗИ +ПРИ+ ПСА (основная группа) .
В исследуемые группы не включали пациентов с болезнью Педжета, лимфогранулематозом, лейкозом, мраморной болезнью, а также консолидирующими переломами, воспалительными и врожденными деструктивными процессами в костях, симулирующих картину метастатического РПЖ. По показаниям выполняли ТР УЗИ, пункционную биопсию, пальцевое ректальное исследование предстательной железы (ПРИ), проводили серологическое определение уровня сывороточного общего простатспецифического антигена и применяли гистологические методы. Уровень накопления РФП в костной ткани 30% относили к гиперфиксации, патогномоничной для ракового метастатического поражения костей. При наличии метастазов в симметричных отделах скелета (ребра, лопатки, кости таза и др.) уровень фиксации индикатора в данной зоне сравнивали с этим показателем в противоположной (симметричной) зоне (например, 6-е правое ребро — 6-е левое ребро и т. д.). При наличии несимметричных зон (тела позвонков и др.) степень накопления РФП сравнивали с ниже- или вышележащей зоной (позвонком).
 |
| Рисунок 1. При остеосцинтиграфии определяются очаги гиперфиксации РПФ в Th 6-12, L 1-2 позвонках, в углах обеих лопаток, в пояснично-крестцовом сочленении справа, в крыльях таза больше слева спереди, в ребрах |
Статистическая обработка материала осуществлялась стандартными методами. Были получены следующие результаты. Теоретической основой работы послужили широко известные данные о физико-химических особенностях метаболизма фосфатных комплексов, меченных Тс-99m РФП [6]. Данный индикатор интенсивно диффундирует из кровеносного русла и накапливается в остеобластах, а также в матрице вновь формирующейся остеоидной ткани в мета- и эпифизарных участках трубчатых костей, характеризующихся высоким уровнем васкуляризации и активности костного мозга [2, 3, 8].
 |
| Рисунок 2. На сцинтиграммах костей скелета сохраняются множественные очаги гиперфиксации РПФ, более интенсивные по сравнению с предыдущим обследованием |
У больных четвертой группы (n=8) было проведено комплексное инструментальное обследование (ОСГ, МРТ, Rо-графия); подобный алгоритм оказался наиболее эффективным из всех подходов.
Полученные нами данные свидетельствуют о том, что ОСГ скелета позволяет выявить метастатические очаги на 6-12 месяцев раньше, чем это возможно при использовании обычного рентгенологического метода, что соответствовало результатам, полученным другими учеными [7, 9]. Объясняется этот факт тем, что введенные внутривенно радиоактивные атомы Р легко включаются в Са-Р-обмен в раннем периоде формирования неоостеоида. Остеобластическая стадия морфогенеза костного метастаза РПЖ характеризовалась активизированными остеобластами, продукцией атипичного остеоидного вещества, выраженным сосудистым компонентом и комплексами иммунных и раковых клеток. На макроуровне эти процессы были представлены сцинтиграфически признаками костной (остеобластической) перестройки, рентгенологически — признаками костной деструкции (остеолизиса). Практически важной особенностью ОСГ скелета является полная визуализация всего скелета, что недостижимо при использовании рентгенографии. При отсутствии сцинтиграфических признаков РПЖ наиболее эффективные результаты получены у четвертой группы больных. Совпадение данных ЛТ (ОСГ, Ro-графии) и цитогистологических методов исследований составило 70-80%. Совпадения по различным стадиям РПЖ колебались от 65 до 95%, что было связано со степенью злокачественности раковых клеток, их индуктирующим влиянием на остеобласты, активностью остеогенных деструктивно-репаративных и протекторных стромогенных процессов в метастатических очагах, а также гормональным фоном и характером оперативного вмешательства [3, 5, 6]. Точность ранней диагностики метастатической формы РПЖ достигала 80-95% при одновременном с ОСГ изучении сывороточной ПСА, что также отражено в литературе [1].
| Ранняя диагностика локализации и характера метастазов в костях при раке предстательной железы (РПЖ) с помощью лучевых методов — актуальная проблема современной онкоурологии [4, 6, 8]. Гематогенные метастатические очаги в костях при раке предстательной железы (РПЖ) встречаются в 50-70% случаев, а по данным сцинтиграфии (ОСГ) — в 12-62% (при отсутствии рентгенологических признаков) [3] |
1. Вуд Мари Э., Банн Пол А. Секреты гематологии и онкологии /Под ред. Токарева Ю. Н., Бухни А. Е.. М.: Бинон, 1997.
2. Линденбратен Л. Д., Наумов Л. Б. Медицинская рентгенология. М.: Медицина, 1984.
3. Портной А. С., Гродзовская Ф. Л. Рак и аденома предстательной железы. Л.: Медицина, 1984. 272. С. 159-162.
4. Руководство по урологии. В 3-х т. /Под ред. Лопаткина Н. А.. М.: Медицина, 1998.
5. Рукавишников В. А., Сальвицкий Б. Н. К вопросу лучевой диагностики злокачественных новообразований костей // Специализированная медицинская помощь и современные проблемы ее интеграции. Тез. докл. науч. конф. 11.12.1986. ГВКГ им. Н. Н. Бурденко, М. 1986. С. 408-409.
6. Савченко Т., Мечев Д., Романенко В. Руководство по ядерной медицине. Вища школа, Киев, 1991. С. 480-489.
7. Harada K., Tanahashi Y., Igari D., Numata I., Orikasa S. Clinical evaluation of inside echo patterns in gray scale prostatic echography /J. Urology 1980. 124, № 2. Р. 216-220.
8. McKillop J. H., Fogelman I. Benign and malignant bone disease // British Nuclear Medicine Society. 1991. Р. 30-53.
9. Signori G. B., Marini F., Perego S., Valente R. Scintigrafia ossea e puntato midollare nella valutazione del carcinoma prostatico /Urologia (Treviso). 1979. 46, № 3. P. 359-363.
Читайте также:


