Макролиды в лечении туберкулеза
В 2000 г. была собрана и проанализирована информация по туберкулезу из 211 стран мира. К концу 1999 г. было зарегистрировано 8,4 млн случаев патологии, из которых только о 3,7 млн имелось сообщение в ВОЗ. К сожалению, ВОЗ не располагает сведениями о фактической численности больных, выделяющих лекарственно-устойчивые штаммы микобактерий туберкулеза (МБТ). Однако по данным, поступающим из большинства регионов планеты, резистентность МБТ к антибактериальным препаратам (АБП) регистрируется повсеместно, обнаруживая тенденцию к росту. Частота ее варьирует в разных странах. Так, проведенные в 1998-1999 гг. исследования (США) показали, что у больных туберкулезом, проживающих в городах с наибольшей плотностью населения (например, в Нью-Йорке), МБТ оказались устойчивыми к одному препарату и более в 21% случаев, а полирезистентный туберкулез обнаруживался в 8%. По данным экспертов ВОЗ, особенно значительна его доля в республиках бывшего СССР и частично в Китае.
Не обсуждая проблему создания абсолютно новых препаратов, решение которой потребует колоссальных затрат и длительных научных изысканий, рассмотрим результаты исследований, связанные с упомянутыми модификацией и апробацией.
Перспективным представляется применение рифалацила, т.к. он практически не вызывает токсических гепатитов при длительном приеме. Эти свойства препарата объясняют изменением его метаболизма по отношению к цитохромам Р450.
Другим направлением современной фармакологии, связанным с повышением активности рифампицина, является поиск новых лекарственных форм, в состав которых включают липосомы. Использование подобной структуры позволит существенно снизить частоту побочных реакций и повысить бактериостатические свойства препарата.
В последнее десятилетие при резистентных формах туберкулеза начал применяться амикацина сульфат. Это полусинтетический аминогликозид, созданный H. Kawaguchi et al. (1972) посредством ацетилирования 1-аминогруппы 2-дезоксистрептаминовой половины канамицина А. Антибиотик обладает широким спектром действия, преимущественно в отношении грамотрицательных бактерий, подавляет размножение МБТ. Он распределяется в определённых концентрациях в легком, печени, миокарде, селезёнке, других органах, избирательно накапливаясь в корковом слое почек; может проникать через гематоэнцефалический барьер - особенно выражено это свойство при воспалении менингеальных оболочек. Амикацин активен против стрептомицинустойчивых МБТ, однако отмечена перекрестная резистентность к препарату штаммов, не чувствительных к канамицину и частично к полипептиду капреомицину.
В связи с этим внимание фтизиатров привлекает новое поколение макролидов. Эти вещества, так же как и фторхинолоны, способны накапливаться внутриклеточно, особенно в макрофагах, что для лечения туберкулеза имеет принципиальное значение, т.к. возбудитель персистирует в макрофагах; кроме того, новые макролиды стимулируют действие на иммунокомпетентные клетки.
Исследования, посвященные применению полусинтетического макролидного антибиотика кларитромицина (ингибитор трансляции, реагирующий с 505-рибосомальной субъединицей бактериальной клетки), выявили, что в микробиологических тестах он оказался более активным по сравнению с рифампицином. Имеется клинический опыт и по использованию азитромицина (сумамед).
В настоящее время изучается производное эритромицина -кетолид телитромицин, ранее известный под шифром HMR-3647. Так же как и кларитромицин, он подавляет белковый синтез, реагируя с БОБ-рибосомальной субъединицей, но по местам прикрепления к мишени они совпадают лишь частично. Правда, действие телитромицина оценено пока только в отношении быстрорастущих микобактерий, но не М. tuberculosis.
С целью повышения эффективности терапии резистентных форм туберкулеза в режимы лечения начали включать некоторые ГЗ-лактамные антибиотики, в частности амоксициллин с клавулановой кислотой (амоксиклав). Он легко проникает через стенку МБТ, проявляет высокий аффинитет к пенициллинсвязывающему белку и благодаря этому обладает весьма широким спектром действия. К антибиотику умеренно чувствительны М. tuberculosis, М. bovis, а также некоторые атипичные штаммы - М. fortuitum, М. kansasii. Необходимо подчеркнуть, что при сочетании препарата с аминогликозидами in vitro инактивируется действие последних.
По данным Г.Л.Гуревича и Д.А.Ветушко (БелНИИПиФ, 2001), амоксициллин с клавулановой кислотой можно рекомендовать как средство выбора на первых этапах комплексной терапии при остропрогрессирующем специфическом процессе, а также при длительном лечении пациентов с мультирезистентностью к большинству основных и резервных противотуберкулёзных препаратов.
В настоящее время проходят апробацию первые представители нового класса (З-лактамных антибиотиков - карбапенемы (имипен, тиенам). Тиенам ингибирует синтез клеточной стенки бактерий и оказывает бактерицидное действие против широкого спектра грамположительных и грамотрицательных патогенных микроорганизмов - как аэробных, так и анаэробных. Имеются данные о чувствительности к препарату М. fortuitum, M.smegmatis; in vitro показано, что тиенам проявляет синергизм с аминогликозидами в отношении некоторых изолятов Pseudomonas aeruginosa.
МБТ относятся к числу грамположительных хемоорганотропных аэробных бактерий и обладают большими адаптивными способностями к выживанию при низких концентрациях кислорода. Это свойство возбудителя было положено в основу тестирования метронидазола и некоторых нитроимидазолов. Известно, что последние легко проникают в бактериальную клетку и связываясь с ДНК, нарушают процесс репликации, оказывая противопротозойное и противомикробное действие. В настоящее время предлагается назначать метронидазол больным с множественной лекарственной устойчивостью.
Таков небольшой перечень препаратов, сравнительно недавно нашедших применение у пациентов с преимущественно деструктивными и нередко прогрессирующими резистентными формами туберкулеза легких. Одни из них заняли прочное место в комплексных схемах (производные рифампицина, канамицина, фторхинолоны), другие пока внедряются и проходят клиническую апробацию (амоксиклав, азитромицин, карбапенемы и др.), однако она ограничена дефицитом финансовых средств противотуберкулёзных учреждений.
Следует подчеркнуть, что химиотерапия при туберкулезе отличается от общепринятых способов применения различных АБП при других острых и хронических инфекциях. Туберкулостатическое лечение приходится проводить систематически и длительно. Это связано с биологическими характеристиками МБТ, значительной распространенностью и выраженностью специфических и неспецифических тканевых повреждений. Существенную роль играет также низкая скорость репаративных процессов, особенно при хронических формах болезни. Те же причины определяют и другое условие эффективности лечения - необходимость комбинирования туберкулостатиков с различными патогенетическими средствами, способствующими росту сопротивляемости организма инфекции. Здесь во фтизиатрии также наметились новые тенденции. По мнению некоторых авторов, использование интерферонов и особенно уинтерферона, а также интерлейкинов 12 и 2 может оказаться перспективным методом повышения иммунобиологического статуса больного.
Серьёзные исследования в области туберкулеза проводятся в США в Национальном институте аллергии и инфекционных заболеваний и центрах контроля и профилактики заболеваний. Изучается безопасность, микробиологическая и иммунологическая активность рекомбинанта человеческого интерлейкина-2 у ВИЧ-негативных лиц. Совместно с японскими учеными определяется роль пептидореактивных γ, σ-Т-клеток, внутриклеточного иммунитета, а также исследуется оболочка микобактерий как возможный объект действия новых противотуберкулёзных препаратов.
Кроме того, проводится апробация нового орального противотуберкулезного средства рифалазила в сочетании с изониазидом, тестируется безопасность и бактерицидная активность препарата KRM-1648 (рифалацил) у взрослых бацилловыделителей.
Многие эксперименты сегодня сконцентрированы на изучении активности адгезивных молекул, способов передачи генетической информации, молекулярных механизмов развития лекарственной устойчивости. При решении этих задач можно ожидать создания новых высокоэффективных противотуберкулезных препаратов.
(Коровкин В.С., БелМАПО. Журнал "Медицинская панорама" № 9, ноябрь 2002)
Существует три основных метода лечения туберкулеза, как легких, так и других органов. Это медикаментозная и химиотерапия, а также хирургическое вмешательство. В этой статье мы подробно разберем каждый из способов.
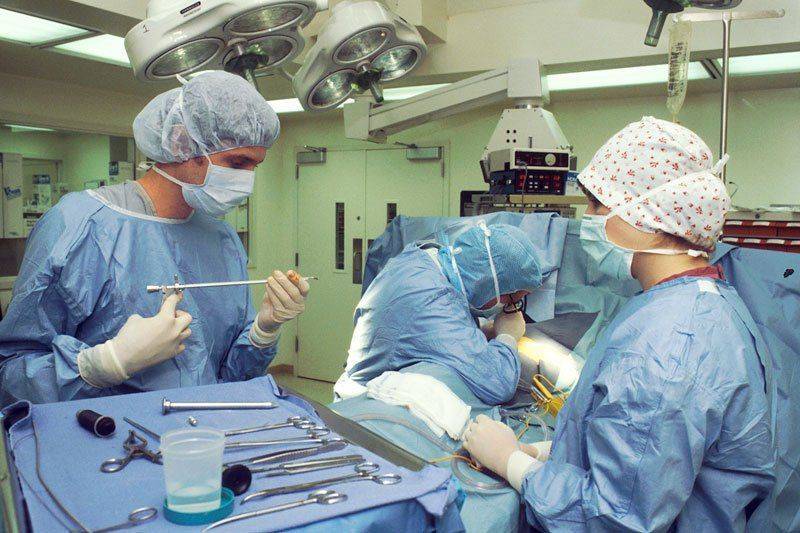
Показания к хирургическому лечению туберкулеза
Хирургическое вмешательство при лечении туберкулеза — одна из крайних мер. Такой вид необходим далеко не в каждом случае.
Выделяют три основных причины, говорящие о необходимости оперативного вмешательства:
- отсутствие положительной динамики остальных способов лечения при ярковыраженной резистентности возбудителя к медикаментам;
- необратимые нарушения, спровоцированные заболеванием легких, плевры, бронхов, лимфатических узлов;
- осложнения опасные для жизни.
Распространенными формами туберкулеза для проведения операций считаются туберкулема, кавернозный и фибро-кавернозный туберкулез. В остальных случаях зачастую помогают безоперационные способы.
Виды оперативных манипуляций:
- резекция легких;
- торакопластика;
- торакостомия;
- удаление плевральных сращений;
- резекция грудинных лимфоузлов;
- инфильтративный туберкулез в стадии распада требует проведения коллапсотерапии — пневмоторакса или пневмоперитонеума;
- легочное кровотечение;
- туберкулез кишечника;
- инфильтративный туберкулез.
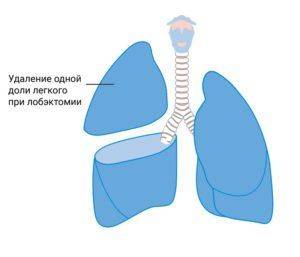
Наибольшая часть оперативных манипуляций проводится в плановом режиме, но бывают случаи, когда возникает экстренная необходимость к проведению вмешательства.
Реабилитация после операции
Процесс реабилитации после хирургического вмешательства проходит тяжело. Высокая температура тела держится около месяца.
В редких случаях в ходе реактивности у пациента может произойти заражение других органов.
Для помощи в восстановительном процессе лечащий врач назначает прием антибиотиков при длительной госпитализации.
После выписки из стационара нужно пройти восстановительный курс в санатории. Далее нужно своевременное лечение и профилактика. Как лечить данный недуг решает фтизиатр.
Препараты для лечения туберкулеза легких
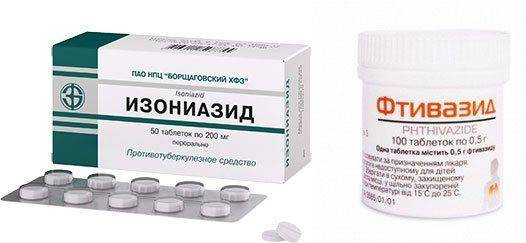
- Изониазид (тубазид). Резистентность возбудителя к медикаменту формируется на протяжении 5 месяцев. Один из комплексных препаратов. Подходит взрослым и детям. Наибольшая эффективность достигается на ранней стадии.
- Фтивазид. Производится в виде порошка и таблетках. Один из комплексных препаратов. Подходит взрослым и детям. Наибольшая эффективность достигается при заболеваниях на начальной стадии.
- Салюзид растворимый. Применяется для инъекций и промываний очагов поражения туберкулезом.
- Метазид. Выпускается в порошке и таблетках. Предотвращает размножение бактерий. Один из комплексных препаратов. Подходит взрослым и детям. Наибольшая эффективность достигается при заболеваниях на начальной стадии.
- Рифампицин. Продается в капсулах и растворе для инъекций. Используется в комплексе с другими средствами. Назначается при отсутствии эффекта от других медикаментов.

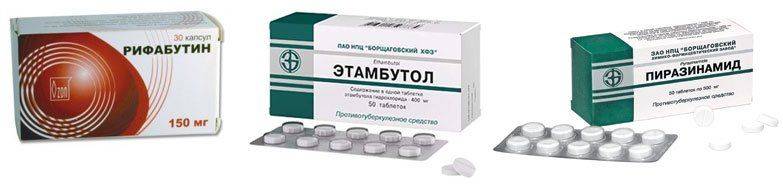
- Рифабутин (Микобутин). Выпускается в капсулах. Рифабутин воздействует на бактерии, которые устойчивы к рифампицину. Возможно использование пациентами с пониженным иммунитетом. Используется в комплексе с другими препаратами. Курс составляет от 6 месяцев.
- Этамбутол (таблетки и капсулы). Оказывает действие непосредственно на возбудителя, резистентного к стрептомицину, изониазиду, ПАСК, канамицину, этионамиду. Использование как самостоятельного средства нецелесообразно из-за быстрого формирования устойчивости бактерий.
- Пиразинамид. Производится в таблетках. Воздействует на бактерии, которые резистентны к другим медикаментам. Используют при казеозыхлимфоаденитах, туберкулемах и казеозно-пневмонических осложнениях. Курс терапии длится от полугода до нескольких лет. Использование как отдельного препарата нецелесообразно, так как быстро возникает резистентность бактерий.
- Этионамид. Выпускается в таблетках, драже, свечах. Назначается при непереносимости и отсутствии эффекта от других медикаментов. Менее активен, чем тубазид и стрептомицин, но воздействует на возбудителя резистентного к этим медикаментам.
- Протионамид. Реализуется в таблетках. Бактерии быстро формируют резистентность к данному медикаменту. Назначается при непереносимости этионамида и прочих медикаментов.
- Стрептомицин. Производится в виде порошка для инъекций. Антибиотик. Рекомендовано использовать в форме аэрозоля.
- Пасомицин. Назначается для терапии. Подходит взрослым и детям.
- Канамицин. Производится в виде таблеток, порошка для инъекций. Антибиотик, подходит взрослым и детям. Используют при отсутствии эффективности других антибиотиков. Возможно использование в форме аэрозоля. Курс длится не более 2 месяцев.
- Амикацин. Производится в виде раствора для инъекций. Уничтожает грамположительные и грамотрицательные бактерии.
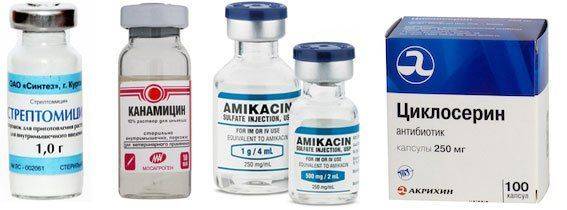
- Флоримицина сульфат. Применяется комплексно в качестве замещающего средства. Используется пациентами при возникновении резистентности возбудителя к другим медикаментам.
Подходит взрослым и детям. - Циклосерин. Производится в форме таблеток, капсул. Воздействует на возбудителя резистентного к стрептомицину, изониазиду, фтивазиду, ПАСК. Используется как замещающее средство. Назначается при отсутствии положительной динамики от предыдущих медикаментов.
- Ципрофлоксацин. Активно воздействует на штамм в период развития колоний. Пациентам с ВИЧ инфекцией применяют ципрофлоксацин, несмотря на низкий результат терапии.
- Офлоксацин. Производится в виде таблеток, раствора для инфузий. Вызывает угнетение деления клеток и гибель бактерий.
- Левофлоксацин (таваник). Назначается пациентам с резистентностью бактерий к большинству медикаментов и бурно протекающей инфекцией. Активен к грамотрицательным микроорганизмам.

Цефалоспорины относят к доказано эффективным средствам в комплексном противотуберкулезном назначении. На практике дают хорошие результаты комбинирования цефотаксима с изониазидом и рифампицином, особенно на начальном этапе терапии.
В наши дни широко используются антибиотики из класса макролидов (азитромицин, кларитромицин, рокситромицин, джозамицин, диритромицин, мидекамицин и др.). Они показаны для комплексной борьбы с патогенной микрофлорой, отягощающей течение болезни.
- Азитромицин, кларитромицин — относятся к лекарствам для терапии простудных осложнений. Применяется при резистентности возбудителя к прочим медикаментам.
- Тиоацетазон. Используется при внелегочных формах туберкулеза. Подходит взрослым и детям.
- Натрия парааминосалицилат (ПАСК). Подходит взрослым и детям.
В наши дни широко используют комбинированные средства, когда в одной капсуле собраны действующие вещества из основного комплекса. Прием средств после выписки из больницы позволяет соблюдать точную дозировку медикаментов.
Существуют комбинированные медикаменты, такие как майрин и майрин-П. В составе находятся: изониазид, рифампицин и этамбутол. Зукокс, Зукокс Е, Зукокс плюс, содержат в одной капсуле рифампицин/изониазид и пиразинамид в разных пропорциях.
Химиотерапия при туберкулезе
Лечение туберкулеза в стационаре подразумевает использование химиотерапии. Она занимает много времени в связи со сложностями к воздействию на палочку Коха. При этом быстро формируется устойчивость бактерии к лекарствам.
Главным условием химиотерапии туберкулеза считается комбинирование 3-4 препаратов с различной активностью для предотвращения устойчивости возбудителя к медикаментам.
Лечение туберкулеза легких у взрослых проводится целым комплексом различных препаратов. Поэтому лечение в стационаре осуществляется под регулярным контролем чувствительности возбудителя к используемым медикаментам.
Пробное лечение следует применять без результатов длительного исследования, чтобы не ухудшать состояние больного. В терапии медикаменты, к которым формируется устойчивость, заменяются другими.
Лечение туберкулеза у детей также проводится путем применения химиотерапии. Схемы лечения подбирает фтизиатр исходя из клинической картины заболевания.
Основные принципы лечения туберкулеза:
- Использование комплекса средств без перерыва на протяжении всегопериода лечения;
- Длительность курса составляет от полугода до нескольких лет. Пациент должен быть готов к длительной терапии;
- После стационарного пребывания необходимо обратиться в реабилитационный санаторий и проводить амбулаторное лечение;
- Дополнительная терапия: помимо химиотерапевтических препаратов необходимо употреблять витамины и иммуномодуляторы;
- Абсолютное соблюдение приема и назначенной дозировки препаратов.
Несвоевременное лечение диссеминированного туберкулеза легких вызывает туберкулез плевры.
По назначению врача проводится дополнительная терапия при туберкулезе: индуктотермия, лазеротерапия, ультразвук, электрофорез, аэрозольные процедуры.
Лечение туберкулеза у детей и подростков выполняют теми же способами, что и у взрослого. Ребенок быстрее идет на поправку, есть шанс вылечить заболевание полностью. Самая высокая смертность от туберкулеза наблюдается у больных с ВИЧ инфекцией.
Лечение туберкулеза народными средствами
В народной медицине для устранения заболевания советуют:
- Совершать пешие прогулки на свежем воздухе (лучше в сосновом бору);
- Каждый день готовить белокочанную капусту, алоэ, чеснок;
- Кушать виноград и пить сок;
- Выпивать до 2л в день молока;
- Отхождению мокроты помогает настой корней алтея;
- Пить отвар мать-и-мачехи и сосновых почек, настой багульника;
- Добавлять рыбий жир;
- Принимать перемолотую смесь из чеснока и лимона.
Важным дополнением является ведение здорового образа жизни и здорового питания. Это позволит укрепить иммунитет для борьбы организма с заболеванием. Лечение туберкулеза в домашних условиях формируется на соблюдении режима, здоровом питании, регулярном осмотре специалистом и проведении анализов.

Патогенетическая терапия
Терапия основывается на поднятии иммунитета и восстановлении защитных сил организма. Лечить туберкулез данным способом следует одновременно с химиотерапией. Схема подбирается индивидуально.
Патогенетическая терапия подразумевает использование следующих средств при туберкулезе:
- противоаллергические;
- гормональные;
- негормональные;
- антиоксиданты и антигипоксанты;
- физиотерапевтические процедуры;
- витамины и микроэлементы;
- анаболические препараты.

Антибиотики при туберкулезе – это одно из основных звеньев курса лечения. Подбирать лекарства должен только врач-фтизиатр, учитывая тяжесть заболевания и индивидуальные особенности организма больного. В результате их использования уничтожается палочка Коха, предотвращаются рецидив и осложнения.
Когда назначают лечение антибиотиками
Антибиотики назначают при открытой форме туберкулеза, если болезнь протекает в скрытом виде, а также при имеющихся симптомах, указывающих на заражение микобактериями. Это должно быть подтверждено:
- положительной реакцией Манту у ребенка;
- наличием в мокроте или мазке пациента палочки Коха.
Антибиотики при туберкулезе легких используют совместно с приемом витаминов.
Виды противотуберкулезных антибактериальных препаратов
Существует следующая классификация антибиотиков для лечения туберкулеза:
- Химические. Предназначены они для уничтожения возбудителя заболевания и предотвращения его распространения. К ним относят: Пиразинамид, Тиамид, ПАСК.
- Полусинтетические. Оказывают комплексное воздействие, уничтожают палочку Коха и предотвращают развитие болезни. Чаще всего используют Циклосерин и медикаменты рифамициновой группы.
- Базовые. С их помощью осуществляется лечение первичной формы туберкулеза. Наиболее эффективное средство – Рифабутин.
- Резервные. Это название препаратов второго уровня, предназначенных для терапии хронической патологии. Они проявляют эффективность, если микобактерии приобрели устойчивость к базовым лекарственным средствам.
Кроме того, выделяют следующие группы антибиотиков против туберкулеза:
- Препараты первого ряда. Они считаются наиболее действенными и могут использоваться для лечения взрослых и детей. Самым сильным противотуберкулезным антибиотиком является Рифампицин. Это мощное средство, поэтому многие врачи назначают его для лечения сторонних заболеваний легких, когда другие лекарства оказываются неэффективными.
- Аминогликозиды. Такие средства являются токсичными, поэтому лечение проводится под контролем врача. Эти медикаменты оказывают пагубное воздействие на почки и провоцируют развитие глухоты. Самый популярный аминогликозид – Стрептомицин.
- Фторхинолоны. Такая категория антибиотиков оказывает губительное воздействие на различные виды патогенных бактерий. Назначают их при прогрессирующей форме заболевания. К ним относят Таваник.
Какие антибиотики принимать
Противотуберкулезные антибиотики эффективно уничтожают палочку Коха. Какой препарат лучше назначить, решает лечащий врач. Отпускаются подобные фармпрепараты только по рецепту.
Это антибиотик, который помогает лечить туберкулез легких. Способен подавлять деятельность кокков и грамположительных бактерий, но оказывается неэффективным в отношении грамотрицательных бактерий и грибков. Препарат уничтожает и палочку Коха. Капсулы принимают утром натощак. Во время лечения туберкулеза легких оказывает наибольшую эффективность в сочетании с другими противотуберкулезными препаратами (например, с Пиразинамидом).
Длительность лечения может составлять до 1 года. Если у пациента другие формы заболевания, например туберкулез кишечника, продолжительность терапии составляет не меньше 9 месяцев.
При исчезновении симптомов болезни препарат следует продолжать принимать, т. к. оставшиеся микобактерии способны вызвать рецидив заболевания.
Противопоказано средство при гепатите печени, болезнях почек, индивидуальной непереносимости, при сердечно-сосудистых заболеваниях, во время беременности.
Это лекарственное средство назначают достаточно редко, т. к. отличается высокой токсичностью. Применяют в виде внутримышечных инъекций. Выводится медикамент почками, поэтому дозировку корректируют в зависимости от почечной функции. Стрептомицин применяют для терапии активной формы туберкулеза в сочетании с Пиразинамидом, Рифампицином и Изониазидом.
Препарат запрещено использовать одновременно с аминогликозидами из-за нефро- или нейротоксичности. Вместе с анестетиками способен привести к развитию паралича. Противопоказан во время беременности, грудного вскармливания, до 1 года. С осторожностью применяют при поражении слухового нерва, нервной системы и болезнях почек.
Такой антибиотик хорошо уничтожает палочку Коха, но для терапии туберкулеза назначается редко из-за высокой токсичности. Вводится препарат внутримышечно, после чего средство сразу проникает в кровоток и оказывает лечебное действие в течение 8-12 часов. Схема лечения следующая: медикамент вводят 6 дней, после чего делают перерыв на 1 день. Длительность терапии зависит от течения и стадии болезни.
К противопоказаниям относят: болезнь Паркинсона, миастению, невриты преддверно-улиткового нерва, чрезмерную чувствительность к составляющим препарата, тяжелые заболевания почек, непроходимость кишечника, беременность, период лактации.
Чтобы вылечить туберкулез, врач может назначить Циклосерин. Это противомикробное средство широкого спектра воздействия снижает или подавляет синтез клеточных стенок микобактерии. Препарат характеризуется бактериостатическими и бактерицидными свойствами. Используют его в комплексном лечении или для терапии хронической патологии, когда другие противотуберкулезные медикаменты оказались неэффективными.
Длительность лечения составляет около 6 месяцев.
Противопоказан препарат при эпилепсии, непереносимости компонентов средства, болезнях нервной системы, алкоголизме, тяжелой почечной недостаточности, психозах, хронической депрессии, беременности и грудном вскармливании.
Это антибиотик, который назначают для лечения туберкулезных больных, если патология протекает в хронической форме. Нередко его применяют, если развилась устойчивость микобактерий к другим противотуберкулезным средствам. Эффективен при лечении туберкулеза кожи, гортани и легких. Нередко сочетают с медикаментами второго ряда: Циклосерином, Пиразинамидом, Этоксидол.
К противопоказаниям относят: болезни вестибулярного аппарата, чрезмерную чувствительность к составляющим средства, первичный туберкулез, нарушение работы печени и почек, неврит слухового нерва.
Педиатры для лечения туберкулеза у детей нередко стали назначать антибиотики. При этом нужно соблюдать назначенную дозировку, чтобы избежать развития устойчивости. Терапию начинают с применения антибиотика первого ряда – Рифампицина, который сочетают с Изониазидом. Иногда в схему лечения включают Стрептомицин. Однако такой медикамент нельзя применять для лечения детей младше 7 лет, т. к. он может привести к потере слуха. При назначении лекарств учитывают имеющиеся противопоказания.
Почему отменяют антибиотик
Антибиотики при лечении туберкулеза отменяют в том случае, если на фоне их приема развились опасные побочные явления, которые могут угрожать не только здоровью, но и жизни пациента. В этом случае назначают прием витаминов и противовоспалительных препаратов.
Содержание
Антимикобактериальные средства [ править | править код ]
В этой статье обсуждаются фармакологические свойства и клиническое применение антимикобактериальных средств, то есть препаратов, применяемых при туберкулёзе, проказе и инфекции, вызванной Mycobacterium avium-intracellulaге. В мире туберкулёз по-прежнему занимает первое место среди причин смерти от инфекционных заболеваний, хотя в США рост числа случаев туберкулёза среди ВИЧ-инфицированных удалось приостановить. Хроническое течение болезни и большая длительность противотуберкулёзной терапии создают дополнительные трудности, связанные с несоблюдением назначений врача, побочными эффектами и лекарственной устойчивостью. Здесь рассматриваются противотуберкулёзные средства первого и второго ряда, а также их применение в условиях распространения устойчивых штаммов микобактерий туберкулёза. Обсуждается также профилактика и лечение инфекции, вызванной Mycobacterium avium-intracellulare, у ВИЧ-инфицированных. Кроме того, даётся представление о клинических формах проказы и средствах, используемых при их лечении.
Противотуберкулёзные средства подразделяют на препараты первого и второго ряда (табл. 48.1). К препаратам первого ряда относятся наиболее эффективные и относительно нетоксичные изониазид, рифампицин, этамбутол, стрептомицин и пиразинамид. Их с успехом применяют у подавляющего большинства больных туберкулёзом. Хорошие результаты даёт 6-месячный курс лечения изониазидом, рифампицином и пиразинамидом (при условии, что возбудитель чувствителен к ним): первые 2 мес используют изониазид, рифампицин и пиразинамид, в следующие 4 мес — изониазид и рифампицин. Эффективен и 9-месячный курс лечения изониазидом и рифампицином; его можно назначать при всех формах туберкулёза, вызванного чувствительными к этим препаратам штаммами (Bass et al., 1994). В районах, где распространена первичная устойчивость к изониазиду, до получения результатов бактериологического исследования в дополнение к рифампицину, изониазиду и пиразинамиду назначают этамбутол или стрептомицин. Если микобактерии устойчивы к препаратам первого ряда, в схему лечения включают препараты второго ряда, так что в целом комбинация состоит из 5—6 противотуберкулёзных средств. К препаратам второго ряда относятся офлоксацин, ципрофлоксацин, этионамид, аминосалициловая кислота, циклосерин, амикацин, канамицин и капреомицин (Iseman, 1993). При лечении ВИЧ-инфицированных нужно помнить о взаимодействии рифамицинов (рифампицин, рифапентин, рифабутин) с ингибиторами протеазы ВИЧ и ненуклеозидными ингибиторами обратной транскриптазы. Приём противотуберкулёзных средств под непосредственным наблюдением медицинского работника улучшает результаты лечения (Havlir and Barnes, 1999).
На Mycobacterium leprae и Mycobacterium avium-intracellulare изониазид не действует. Полимикобактериальную проказу (лепроматозную, погранично-лепроматозную и пограничную) лечат дапсоном, клофазимином и рифампицином не менее 2 лет, олигомикобактериальную (туберкулоидную, погранично-туберкулоидную и неопределенную) — дапсоном и рифампицином в течение 6 мес.
В отношении Mycobacterium avium-intracellulare активны рифабутин, кларитромицин, азитромицин и фторхинолоны. Азитромицин и кларитромицин — более эффективные средства профилактики инфекции, вызванной Mycobacterium avium-intracellulare, чем рифабутин. В сочетании с этамбутолом азитромицин и кларитромицин применяют для лечения этой инфекции у ВИЧ-инфицированных.
Таблица 48.1. Антимикобактериальные средства
Препараты первого ряда
Препараты второго ряда
Изониазид + рифампицин + пиразинамид + этамбутол или стрептомицин
Ципрофлоксацин или офлоксацин; циклосерин; капреомицин; канамицин; амикацин; этионамид; клофазимин; аминосалициловая кислота
Кларитромицин или азитромицин + этамбутол ± рифабутин
Рифабутин; рифампицин; этионамид; циклосерин; спарфлоксацин; офлоксацин; левофлоксацин
Изониазид + рифампицин* + этамбутол
Этионамид; циклосерин; кларитромицин; амикацин; стрептомицин; левофлоксацин
Mycobacterium fortuitum, Mycobacterium chelonae и Mycobacterium abscessus
Цефокситин; рифампицин; сульфаниламиды; ципрофлоксацин; офлоксацин; кларитромицин; триметоприм/сульфаметоксазол; имипенем
Триметоприм/сульфаметоксазол; кларитромицин; миноциклин; доксициклин
Дапсон + рифампицин ± клофазимин
Миноциклин; офлоксацин; кларитромицин; этионамид
Антимикробные средства, действующие на Mycobacterium avium-intracellulare [ править | править код ]
В настоящее время распространённость инфекции, вызванной Mycobacterium avium-intracellulare, среди ВИЧ-инфицированных значительно снизилась (Benson, 1997—1998). До широкого внедрения высокоактивной антиретровирусной терапии и медикаментозной профилактики инфекции, вызванной Mycobacterium avium-intracellulare, диссеминированная форма этой инфекции наблюдалась у 15—40% ВИЧ-инфицированных. Как правило, болезнь развивается на поздних стадиях ВИЧ-инфекции, когда число лимфоцитов CD4 падает ниже 100 мкл-1; появляются лихорадка, потливость по ночам, снижение веса, анемия (Masuret al., 1993). В отсутствие ВИЧ-инфекции Mycobacterium avium-intracellulare обычно поражает только лёгкие: больные жалуются на постоянный кашель с мокротой; на рентгенограмме грудной клетки обнаруживают диффузные или очаговые инфильтраты, иногда с образованием каверн (Havlir and Ellner, 2000). Обычные антимикобактериальные средства малоэффективны. Недавно появились новые препараты, активные в отношении Mycobacterium avium-intracellulare. Их применяют для профилактики и лечения этого заболевания у ВИЧ-инфицированных.
Рифабутин — производное рифамицина S. Рифабутин действует так же, как и рифампицин (ингибирует бактериальную РНК-полимеразу), но in vitro и при экспериментальном туберкулёзе у мышей он эффективнее рифампицина.
Химические свойства. Рифабутин растворим в органических растворителях, а в низких концентрациях (0,19 мг/мл) — в воде. Его структурная формула следующая:
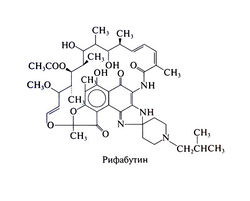
Антимикробная активность. В отношении Mycobacterium avium-intracellulare рифабутин активнее рифампицина. In vitro рифабутин действует как на Mycobacterium avium (основной возбудитель у ВИЧ-инфицированных), так и на Mycobacterium intracellulare, которую выделяют у 40% больных без ВИЧ-инфекции. МПКдля большинства штаммов Mycobacterium avium-intracellulare составляет 0,25—1 мкг/мл, МПК для многих штаммов Mycobacterium tuberculosis не превышает 0,125 мкг/мл.
Устойчивость. И у Mycobacterium tuberculosis, и у Mycobacterium avium-intracellulare иногда встречается перекрёстная устойчивость к рифампицину и рифабутину. Так, из 225 штаммов Муcobacterium avium-intracellulare, устойчивых к рифампицину в концентрации 10 мкг/мл, 20% были устойчивы к рифабутину в г концентрации 1 мкг/мл (Heifetsetal., 1985). Фармакокинетика. После приёма рифабутина внутрь в дозе 300 мг максимальная сывороточная концентрация достигается через 2—3 ч и составляет 0,4 мкг/мл. Рифабутин элиминируется в две фазы; конечный Т1/2 составляет в среднем 45 ч (16—96 ч). Благодаря своей липофильности препарат накапливается в тканях (его концентрация там в 5—10 раз превышает сывороточную). Выводится рифабутин с мочой и желчью. При почечной недостаточности дозу не снижают.
Применение. Рифабутин используют для профилактики инфекции, вызванной Mycobacterium avium-intracellulare, у ВИЧ-инфицированных. При приёме в дозе 300 мг/сут вероятность бактериемии снижается на 50% (Nightingale et al., 1993). Однако азитромицин и кларитромицин эффективнее рифабутина и, в отличие от него, не взаимодействуют с антиретровирусными препаратами. В сочетании с кларитромицином и этамбутолом рифабутин применяют для лечения инфекции, вызванной Mycobacterium avium-intracellulare (Shafran etal., 1996). Кроме того, рифабутин часто назначают ВИЧ-инфицированным больным туберкулёзом вместо рифампицина, так как последний в большей степени усиливает метаболизм антиретровирусных средств (Haas, 2000).
Побочные эффекты. Как правило, ВИЧ-инфицированные хорошо переносят рифабутин. Основные причины отмены препарата — сыпь (4%), желудочно-кишечные нарушения (3%) и нейтропения (2%; Nightingale et al., 1993). На поздних стадиях ВИЧ-инфекции нейтропения возникает в 25% случаев. При приёме рифабутина в д03е более 450 мг/сут в сочетании с кларитромицином или флуконазолом наблюдались увеит и артралгия. Больных предупреждают, что при появлении симптомов поражения глаз (боль в глазах, нечёткость зрения) приём рифабутина следует прекратить. Как и рифампицин, рифабутин окрашивает кожу, мочу, кал, слюну и слёзы в оранжевый цвет. Возможно окрашивание контактных линз К редким побочным эффектам относятся тромбоцитопения, гриппоподобный синдром, гемолиз, миозит, боль в груди и гепатит.
Рифабутин, как и рифампицин, индуцирует микросомальные ферменты печени, ускоряя метаболизм ряда лекарственных средств, в том числе зидовудина, преднизона, дигитоксина, хинидина, кетоконазола, пропранолола, фенитоина, производных сульфанилмочевины, вар-фарина. По сравнению с рифампицином рифабутин в меньшей степени снижает сывороточную концентрацию индинавира и нелфинавира.
Фармакологические свойства макролидов и их клиническое применение подробно рассматриваются в гл. 47. Здесь обсуждается только роль этих препаратов в лечении инфекции, вызванной Mycobacterium avium-intracellulare.
Антимикробная активность. In vitro в отношении Mycobacterium avium-intracellulare кларитромицин примерно в 4 раза активнее азитромицина. Однако in vivo эти различия не столь заметны, поскольку азитромицин очень хорошо проникает внутрь клеток и его концентрации в тканях превышают сывороточную на два порядка. На большинство других атипичных микобактерий (за исключением Mycobacterium simiae) кларитромицин действует в концентрации не более 4 мкг/мл.
Устойчивость. Длительная монотерапия кларитромицином или азитромицином приводит к появлению устойчивых штаммов Mycobacterium avium-intracellulare, поэтому макролиды назначают только в комбинации с другими антимикобактериальными средствами.
Применение. Кларитромицин (500 мг 2 раза в сутки) или азитромицин (500 мг 1 раз в сутки) в сочетании с этамбутолом используют для лечения инфекции, вызванной Mycobacterium avium-intracellulare, у ВИЧ-инфицированных; в некоторых случаях дополнительно назначают рифабутин (Shafran etal., 1996; Masur et al., 1993). Лечение продолжают пожизненно (USPHS, 1999). Побочные эффекты. В высоких дозах, которые необходимы для лечения инфекции, вызванной Mycobacterium avium-intracellulare, макролиды иногда вызывают шум в ушах, головокружение и обратимое снижение слуха.
Фармакологические свойства фторхинолонов и их клиническое применение подробно рассматриваются в Хинолоны. Здесь обсуждается роль этих препаратов в лечении инфекций, вызванных только Mycobacterium avium-intracellulare.
Антимикробная активность. In vitro фторхинолоны (левофлок-сацин, ципрофлоксацин, офлоксацин, флероксацин и cnapj флоксацин) подавляют рост Mycobacterium tuberculosis (МПК: £ 1,3 мкг/мл) и Mycobacterium avium-intracellulare (МПК £1(Ь 100 мкг/мл). МПКдля Mycobacterium fortuitum и Mycobacteri um kansasii не превышает 3 мкг/мл.
Устойчивость. При монотерапии ципрофлоксацином инфекции, вызванной Mycobacterium fortuitum, к нему развивается устойчивость.
Применение. Ципрофлоксацин (750 мг 2 раза в сутки или 500 мг 3 раза в сутки) в сочетании с кларитромицином, рифабутином и амикацином применяют для лечения инфекции, вызванной Mycobacterium avium-intracellulare, у ВИЧ-инфицированных (Havlir and Ellner, 2000). Офлоксацин (300—800 мг/сут) в комбинации с противотуберкулёзными препаратами второго ряда назначают при полирезистентном туберкулёзе.
In vitro клофазимин подавляет рост большинства штаммов Mycobacterium avium-intracellulare в концентрации 1,6—2 мкг/мл, однако результаты его клинического применения в сочетании с другими антимикобактериальными средствами неутешительны. Более подробные сведения о клофазимине приведены в разделе, посвящённом противолепрозным средствам.
Фармакологические свойства амикацина рассмотрены в гл. 46. Дмикацин входит в схему комбинированной терапии инфекции, вызванной Mycobacterium avium-intracellulare, в качестве третьего или четвёртого препарата. МПК для большинства штаммов Mycobacterium avium-intracellulare составляет 8—32 мкг/мл.
Надежда на успешное лечение инфекции, вызванной Mycobacterium avium-intracellulare, появилась благодаря кларитромицину и азитромицину. Оба препарата высокоактивны в отношении многих штаммов этих микобактерий. Даже при монотерапии устраняется бактериемия или уменьшается число микобактерий в крови, исчезают лихорадка и ночная потливость. Однако монотерапия сопровождается развитием лекарственной устойчивости, поэтому большинство врачей в настоящее время комбинируют кларитромицин или азитромицин с этамбутолом (Haas, 2000; Shafran et al., 1996). Иногда к этой схеме добавляют рифабутин, клофазимин или фторхинолоны, хотя преимущества такого лечения не доказаны. Чем больше препаратов назначают одновременно, тем выше риск лекарственных взаимодействий и побочных эффектов. По данным одного исследования, у 46% больных, получавших комбинацию из 4 препаратов, лечение пришлось прекратить (Kemper et al., 1992). Улучшение обычно наступает через 1—2 мес после начала терапии, а посевы становятся отрицательными через 3 мес (Masur et al., 1993). ВИЧ-инфицированным лечение проводят пожизненно (USPHS, 1999). Изониазид и пиразинамид на Mycobacterium avium-intracellulare не действуют.
Профилактика инфекции, вызванной Mycobacterium avium-intracellulare, показана всем ВИЧ-инфицированным с числом лимфоцитов CD4 менее 50 мкл-1. Кларитромицин и азитромицин снижают риск развития этой инфекции и хорошо переносятся. Если на фоне высокоактивной антиретровирусной терапии наблюдается стойкое улучшение — число лимфоцитов CD4 стабилизируется на уровне выше 100 мкгГ1, а концентрация вирусной РНК снижается, — профилактическое лечение можно прекратить (USPHS, 1999).
Перспективы [ править | править код ]
Перспективное направление в лечении микобактериальных инфекций — применение фторхинолонов. Расширение системы контролируемой амбулаторной терапии туберкулёза и успехи высокоактивной антиретровирусной терапии позволяют надеяться на дальнейшее снижение распространенности туберкулёза среди ВИЧ-инфицированных. Расшифровка механизмов устойчивости микобактерий к антимикробным средствам поможет более эффективно бороться с устойчивыми микроорганизмами. Ещё одно важное новое направление в антимикобактериальной терапии — использование иммуномодуляторов (например, интерферона у), стимулирующих фагоцитоз микобактерий макрофагами.
Читайте также:


