Выделение и культивирование вирусов
Вирусы размножаются только в живых клетках, и выделение возбудителя в заражённой культуре клеток — один из основных методов диагностики вирусных инфекций. Поскольку большинство патогенных вирусов отличает тканевая и типовая специфичность, то почти к каждому вирусу можно подобрать соответствующие клеточные или тканевые культуры, а также создать стандартные условия культивирования (наличие клеток одного типа). Размножение вируса обеспечивают чувствительные (пермиссивные) клетки. Поэтому при выделении неизвестного возбудителя проводят одномоментное заражение 3-4 культур клеток, предполагая, что одна из них может оказаться пермиссивной. Культуры клеток получают диспергированием соответствующих органов и тканей, но чаще используют эмбриональные ткани (человека и животных) либо трансформированные опухолевые клетки. При помещении на соответствующую плоскую поверхность клеточные культуры обычно растут в виде монослоя.
Первично-трипсинизированные культуры. Суспензии клеток получают гомогенизированием соответствующих тканей, предварительно обработанных трипсином. Культуры часто представлены клетками смешанного типа и не подлежат повторному культивированию. Жизнеспособность таких культур составляет 2-3 нед.
Полуперевиваемые линии клеток представлены диплоидными клетками человека и животных. Культуры ограниченно пригодны к повторному диспергированию и росту (как правило, не более 20-30 пересевов), сохраняя при этом жизнеспособность и не подвергаясь спонтанной трансформации.
Перевиваемые линии клеток (гетероплоидные культуры) представлены клетками, подвергнутыми длительному культивированию и спонтанным трансформациям. Культуры способны к многократному диспергированию и перевиванию. Работа с ними менее трудоёмка по сравнению с приготовлениями первичных культур; перевиваемые клетки относительно одинаковы по своей морфологии и стабильны по свойствам.
Не все виды клеток способны расти в виде монослоя, в некоторых случаях поддержание дифференцированных клеток возможно только в культуре органа. Обычно это суспензия ткани, обладающей специализированной функцией, также обозначаемая как культура переживающей ткани.
Куриные эмбрионы
Куриные эмбрионы — практически идеальные модели для культивирования некоторых вирусов (например, гриппа и кори). Замкнутая полость эмбриона препятствует проникновению микроорганизмов извне, а также развитию спонтанных вирусных инфекций. Эмбрионы применяют для первичного выделения вирусов из патологического материала; для пассирования и сохранения их, а также для получения необходимых количеств вируса. Некоторые возбудители (например, герпесвирусы) вызывают характерные изменения (по ним можно распознавать заболевание). Заражение проводят на хорион-аллантоисную оболочку, в амниотическую или аллантоисную полость либо в желточный мешок.
Заражение на хорион-аллантоисную мембрану. Обычно используют 10-12-суточные эмбрионы. Яйца просматривают в проходящем свете, отмечают локализацию воздушного мешка и выбирают область без сосудов. Осторожно удаляют фрагмент скорлупы, освобождают наружную оболочку и отслаивают её осторожным надавливанием. Затем делают отверстие у края воздушного мешка. При отсосе через это отверстие хорион-аллантоисная оболочка отслаивается от наружной оболочки. На неё наносят исследуемый материал, свободный от бактерий и простейших (пропущенный через бактериальные фильтры и обработанный бактерицидами).
Заражение в амниотическую полость. Обычно используют 7-14-суточные эмбрионы, у которых после отслоения хорион-аллантоисной оболочки (см. выше) расширяют отверстие, захватывают пинцетом амниотическую оболочку и выводят через хорион-аллантоисную оболочку. Через неё в амниотическую полость вводят исследуемый материал.
Заражение в аллантоисную по лость. 10-суточные эмбрионы заражают через отверстия, сделанные в скорлупе и подлежащих оболочках (см. выше).
Заражение в желточный мешок. Используют 3
8-суточные эмбрионы, у которых в этом возрасте желточный мешок занимает почти всю полость яйца. Заражение проводят через отверстие, сделанное в воздушном мешке
Наблюдение и учёт результатов. В качестве вируссодержащего материала можно использовать содержимое желточного мешка, аллантоисную и амниотическую жидкости либо весь эмбрион, нарезанный вместе с окружающими тканями на кусочки. Для выявления характерных поражений на хорион- развивающегося куриного эмбриона.
аллантоисной мембране удаляют скорлупу и наружную оболочку. Затем мембрану извлекают и помещают в стерильную воду. Характер поражений изучают на тёмном фоне.
При невозможности выделить и идентифицировать вирус стандартными методами in vitroинфекционный материал вводят чувствительным к возбудителю животным, и после развития типичного инфекционного процесса проводят повторное заражение чувствительных клеточных культур. Наиболее часто используют мышей, кроликов и обезьян; для выделения некоторых вирусов (например, вирусов Коксаки) заражают мышат-сосунков. Вследствие дороговизны и сложности содержания лабораторных животных, практически повсеместно их вытеснили клеточные культуры. Тем не менее, животные модели активно используют для изучения особенностей патогенеза и формирования иммунных реакций при вирусных инфекциях.
Идентификация вирусов
Качественное определение
Цитопатические эффекты оценивают при микроскопии клеточных культур. По степени поражения клеток выделяют вирусы с высокой или умеренной цитопатогенностью. Размножение вирусов в культурах клеток сопровождается нарушениями морфологии клеток монослоя. Некоторые вирусы вызывают характерные цитопатические изменения, что (с учётом клинической картины заболевания) позволяет быстро поставить предварительный диагноз. Например, размножение парамиксовирусов (вирусы кори, паротита, PC-вирус) сопровождается появлением характерных гигантских многоядерных клеток; аденовирусы вызывают образование скоплений больших круглых клеток, а при репродукции герпесвирусов клетки округлой формы диффузно располагаются по всему монослою.
Тельца включений. Многие вирусы вызывают появление в заражённых клетках характерных образований — скоплений вирусных белков или частиц, видимых в световой микроскоп. Тельца включений могут располагаться как в цитоплазме (тельца Гварнери при оспе), так и в ядрах клеток (аденовирусы).
Отсутствие цитопатического эффекта. Некоторые вирусы (например, вирус краснухи) не проявляют цитопатического эффекта. Их можно выявлять по интерференции другого вируса, способного вызывать дегенерацию заражённых клеток.
Феномен гемадсорбции. Многие заражённые вирусами клетки приобретают способность сорбировать на своей поверхности различные эритроциты. Феномен гемадсорбции имеет общие механизмы с гемагглютинацией и проявляется на ранних сроках, до проявления цитопатического эффекта, при его отсутствии либо слабой выраженности.
Экспресс-диагностика. Для быстрой идентификации вирусной инфекции разработаны многочисленные методы экспресс-диагностики, основанные на обнаружении вирусных Аг. Например, для ранней диагностики ВИЧ-инфекции широко используют ИФА, выявляющий поверхностные Ar вируса.
Лабораторные исследованияпри проведении идентификации вирусов и диагностике вирусных инфекций включают следующие этапы: выделение, культивирование, индикация (выявление) и идентификация вирусов.
2.3.1 Культивирование вирусов
Вирусы не растут на искусственных питательных средах, а размножаются только внутриклеточно. Крупным достижением было предложение Р. Гудпасчура в 1932 г. использовать для культивирования вирусов куриные эмбрионы. Окончательное решение проблемы культивирования вирусов оказалось возможным лишь после того, как были разработаны основные способы культивирования клеток вне организма.
Использование куриных эмбрионов. Куриные эмбрионы – практически идеальные модели для культивирования некоторых вирусов (например, гриппа и кори). Замкнутая полость эмбриона препятствует проникновению микроорганизмов извне, а также развитию спонтанных вирусных инфекций. Эмбрионы применяют для первичного выделения вирусов из патологического материала; для пассирования и сохранения их, а также для получения необходимых количеств вируса. Некоторые возбудители (например, герпесвирусы) вызывают характерные изменения (по ним можно распознавать заболевание).
Для заражения обычно используют куриные эмбрионы 7–12-дневного возраста. Перед заражением определяют жизнеспособность эмбриона путем овоскопирования (просматривают в проходящем свете). Живые эмбрионы при овоскопировании проявляют двигательную активность, хорошо виден сосудистый рисунок. Простым карандашом очерчивают границы воздушной камеры.
Куриные эмбрионы заражают вируссодержащим материалом в асептических условиях стерильными инструментами, предварительно обработав скорлупу над воздушным пространством йодом и спиртом. Заражение проводят на хорион-аллантоисную оболочку, в амниотическую или аллантоисную полость, либо в желточный мешок (рисунок 29). Выбор метода заражения зависит от биологических свойств вируса.
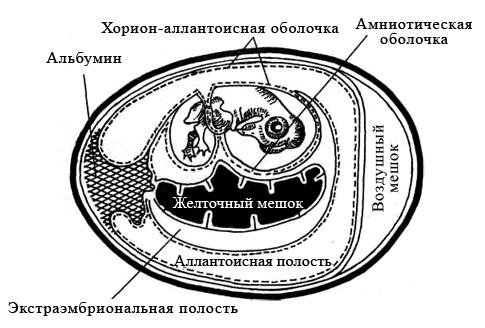
Рисунок 29 – Схематическое изображение развивающегося куриного эмбриона
Культура клеток. Вначале был использован метод переживающих тканей. Он заключался в том, что в колбу, содержащую питательную среду, вносили кусочек ткани. Клетки некоторых тканей в таких условиях могут переживать (но не размножаться) до 30 дней, а в них могут размножаться вирусы. Однако этот способ давал очень небольшой выход вирусов. Необходимо было разработать условия, при которых клетки ткани могли бы свободно размножаться.
Для получения культур клеток необходимо было решить четыре главных задачи:
– получить в необходимом количестве свободные (т. е. изолированные друг от друга) клетки;
– создать такие питательные среды и условия, в которых клетки могли бы активно размножаться;
– обеспечить условия, при которых в культурах клеток не могли бы размножаться бактерии;
– определить методы, с помощью которых можно было бы распознавать рост вируса в культуре клеток и идентифицировать его.
Для выделения изолированных (разобщенных), но жизнеспособных клеток из разрушенных тканей, стали использовать обработку их слабым раствором трипсина, разрушающего межклеточные мостики. Для культивирования клеток были предложены различные среды, содержащие все необходимые для размножения клеток питательные вещества (аминокислоты, основания, витамины и другие), минеральные соли, имеющие оптимальную рН и т. д. К питательным средам добавляли индикатор, по изменению цвета которого можно было судить о метаболизме клеток и их размножении. Было установлено, что в качестве основы, на которой клетки размножаются и образуют монослой, может быть использовано хорошо обработанное стекло пробирок и колб. Для подавления возможного роста бактерий вируссодержащий материал перед посевом его в культуры клеток стали обрабатывать антибиотиками.
В 1949 г. Дж. Эндерс, Т. Веллер и Ф. Роббинс показали, что вирус полиомиелита хорошо размножается в первично-трипсинизированных культурах клеток, полученных из почек обезьян. Основной недостаток первично-трипсинизированных клеток заключается в том, что после нескольких пересевов они перестают размножаться. Поэтому предпочтением стали пользоваться культуры таких клеток, которые способны размножаться in vitro бесконечно долго. Такие перевиваемые культуры клеток (клеточные линии характеризуются бессмертием и гетероплоидным кариотипом) получают из опухолевых тканей (HeLa получена из карциномы шейки матки, НЕр-2 – из карциномы гортани; Детройт-6 – из метастаза рака легкого в костный мозг; RН – из опухоли почки человека) или из мутантных клеток с полиплоидным набором хромосом. Однако опухолевые клетки нельзя применять для получения вакцин. Для этих целей используют только культуры таких клеток, которые не содержат никаких контаминантных вирусов и не обладают злокачественностью. Лучше всего этим требованиям отвечают культуры диплоидных клеток.
Полуперевиваемые (диплоидные) культуры клеток – клетки одного генотипа, способные in vitro выдерживать 50–100 пассажей, сохраняя при этом свой исходный диплоидный набор хромосом. Диплоидные линии фибробластов эмбриона человека используются как для диагностики вирусных инфекций, так и при производстве вирусных вакцин. Как оказалось, вирусы могут размножаться не только в культурах клеток, образующих монослой на стекле пробирок, но и в суспензиях живых клеток.
Для обеспечения жизнедеятельности культивируемых клеток необходимы питательные среды. По назначению они делятся на ростовые и поддерживающие. В ростовых питательных средах должно содержаться больше питательных веществ, обеспечивающих активное размножение клеток и формирование монослоя. Поддерживающие среды обеспечивают переживание клеток в уже сформированном монослое в период размножения в них вирусов.
2.3.2 Выделение вирусов
Выделение вирусов в культурах клеток. При выделении вирусов из различных инфекционных материалов (кровь, моча, слизистые отделяемые, смывы из органов) применяют культуры клеток, обладающих наибольшей чувствительностью к предполагаемому вирусу. Для заражения используют культуры в пробирках с хорошо развитым монослоем клеток. Перед заражением клеток питательную среду удаляют и в каждую пробирку вносят по 0,1–0,2 мл взвеси исследуемого материала, предварительно обработанного антибиотиками для уничтожения бактерий и грибов. После 30-60 мин контакта вируса с монослоем клеток удаляют избыток материала, в культуру вносят поддерживающую среду и пробы оставляют в термостате до выявления признаков размножения вируса.
Выделение вирусов на лабораторных животных. При невозможности выделить и идентифицировать вирус стандартными методами in vitro инфекционный материал вводят чувствительным к возбудителю животным, и после развития типичного инфекционного процесса проводят повторное заражение чувствительных клеточных культур. Наиболее часто используют мышей, кроликов и обезьян; для выделения некоторых вирусов (например, вирусов Коксаки) заражают мышат-сосунков. Вследствие дороговизны и сложности содержания лабораторных животных, практически повсеместно их вытеснили клеточные культуры. Тем не менее животные модели активно используют для изучения особенностей патогенеза и формирования иммунных реакций при вирусных инфекциях.
Таким образом, для выделения чистых культур вирусов в лабораторных условиях в настоящее время используются следующие живые объекты (биологические модели): 1) культура клеток (тканей, органов); 2) куриные эмбрионы; 3) лабораторные животные.
2.3.3 Индикация вирусов
Индикация вирусов в культурах клеток. Индикатором наличия вируса в зараженных культурах клеток может служить:
1) развитие специфической дегенерации клеток – цитопатическое действие вируса (ЦПД), имеющее три основных типа: крупно- или мелкоклеточная дегенерация; образование многоядерных гигантских клеток (симпластов); развитие очагов клеточной пролиферации, состоящих из нескольких слоев клеток (гроздевидная дегенерация клеток).
Различают два механизма гибели клеток, вызываемой вирусами, – некроз и апоптоз. Некроз происходит из-за необратимых нарушений целостности клеточных мембран, апоптоз – вследствие фрагментации ядерной ДНК под действием клеточной эндонуклеазы.
Цитопатические эффектыоценивают при микроскопии клеточных культур. По степени поражения клеток выделяют вирусы с высокой или умеренной цитопатогенностью:
2) обнаружение внутриклеточных включений, располагающихся в цитоплазме и/или в ядрах пораженных клеток;
3) положительная реакция гемагглютинации (РГА) или гемадсорбции (РГАдс). Некоторые вирусы, в частности, вирус гриппа, обладают особыми рецепторами (гемагглютининами), с помощью которых они адсорбируются на эритроцитах и вызывают их склеивание (гемагглютинацию). Такие вирусы легко обнаруживаются с помощью реакции гемагглютинации или гемадсорбции (эритроциты адсорбируются на инфицированных вирусами клетках культуры тканей);
4) феномен бляшкообразования. Широкое распространение получил предложенный в 1952 г. Р. Дюльбекко метод бляшек (негативных колоний), позволяющий производить количественное определение вирусов. Для выделения вирусов монослой клеток после удаления питательной среды заражают вируссодержащим материалом и покрывают слоем агара, содержащего индикатор нейтральный красный. Чашки (флаконы) инкубируют при 37 °С. Через 48–96 ч выявляются пятна – бляшки. Они имеют диаметр 1–3 мм и выглядят неокрашенными на розовом фоне. Пятна возникают за счет цитопатического действия вируса;
5) цветная реакция Солка. О росте вирусов в клетках можно судить с помощью индикатора, добавляемого к питательной среде. Если клетки активно осуществляют метаболизм, рН среды сдвигается в кислую сторону, и среда окрашивается в желтый цвет. В случае размножения вируса клетки погибают, рН среды мало меняется, и она сохраняет первоначальный (малиновый) цвет или (при нейтральной рН) приобретает оранжевый;
6) реакция интерференции (используется при отсутствии ЦПД, гемагглютинации и гемадсорбции): исследуемая культура повторно заражается вирусом, вызывающим ЦПД. В положительном случае ЦПД будет отсутствовать (реакция интерференции положительна). Если в исследуемом материале вируса не было, наблюдается ЦПД.
Кроме того, для обнаружения вируса в культурах клеток могут быть использованы различные серологические реакции.
Индикация вирусов на лабораторных животных. Индикация вируса основана на обнаружении у животных признаков инфекционного заболевания, регистрации их гибели, изучении характера патоморфологических и патогистологических изменений в тканях и органах, выявлении положительной реакции гемагглютинации.
2.3.4 Методы идентификации вирусов
Определение типа вируса (его идентификация) основано на нейтрализации биологической активности вируса с помощью типоспецифических сывороток. Конечный результат ее может быть установлен на основании следующих признаков:
1) нейтрализация цитопатического действия: в культуральную среду, содержащую изучаемый вирус, вносят коммерческую сыворотку (например, к вирусу краснухи при подозрении на неё), инкубируют и заражают вторую культуру; через 1–2 дня в неё вносят известный цитопатогенный вирус. При наличии цитопатогенного эффекта делают вывод о том, что первая культура была заражена вирусом, соответствовавшим антителам примененной сыворотки;
2) нейтрализация реакции гемадсорбции;
3) изменение проявления цветной пробы;
4) задержка (торможение) реакции гемагглютинации: смешивают культуральную среду, содержащую возбудитель, с известной коммерческой антисывороткой и вносят в культуру клеток. После инкубации определяют способность культуры к гемагглютинации и при её отсутствии делают заключение о несоответствии вируса антисыворотке.
5) нейтрализация в опытах на животных.
Таким образом РН (реакция нейтрализации) основана на подавлении соответствующей реакции, феномена, развития инфекционного процесса после внесения в культуру или введения в организм животного смеси вируса со специфичными AT, содержащимися в диагностической сыворотке.
Вопросы для самоконтроля
1 Назовите основные принципы классификации вирусов.
2 Приведите русские и латинские названия основных семейств вирусов человека и животных.
3 Назовите типовых представителей основных семейств вирусов и заболевания, вызываемые ими.
4 Каковы особенности морфологии и ультраструктуры вирусов человека и животных (основных семейств)?
5 Назовите РНК-геномные и ДНК-геномные фитовирусы.
6 Какие этапы включают в себя лабораторные исследования при идентификации вирусов и диагностике вирусных инфекций?
7 Какие биологические модели используются для выделения и культивирования вирусов человека и животных?
8 Как происходит заражение куриных эмбрионов в лабораторных условиях?
9 Какие методы получения культуры клеток вы знаете?
10 Как проводят идентификацию вирусов в курином эмбрионе и на лабораторных животных?
11 Какие существуют методы индикации вирусов на культуре клеток?
12 В чем заключается назначение и сущность реакций нейтрализации вирусов?
13 Назовите способы постановки реакций нейтрализации вирусов.
21-й век - это век, совершающий семимильные шаги в области технологического прогресса, стремительно развиваются наука и медицина. Современный уровень прогресса позволяет претворить в жизнь то, что раньше казалось человеку невозможным. Постиндустриальная стадия развития человечества нацелена на высокие технологии, инновации во всех сферах.
Особенно быстро развивается медицина: большинство болезней, считавшихся ранее неизлечимыми, теперь таковыми не являются. Так, например, культивирование вирусов позволяет создавать профилактические препараты: вакцины и сыворотки, предотвращающие эпидемии чумы, оспы и других смертельно опасных болезней.
Что такое культивирование?
Культивирование (от лат. cultivo – возделывать) представляет собой процесс разведения и выращивания чего-либо в искусственных условиях. В медицине, а точнее в эпизоотологии – частном ответвлении от ветеринарной медицины, культивирование является основным процессом, позволяющим изучать воздействие вируса на живой организм.
На основании полученной информации фармацевты изготавливают противовирусные препараты, создают методики, позволяющие в будущем противодействовать выявленным микроорганизмам. Выделение вирусов из зараженного материала также позволяет сохранять их для дальнейшего использования.

История эпизоотологии
Еще в 1879 году французский ученый В. Гальтье впервые предпринял попытку культивировать вирус. Его выбор пал на такое заболевание, как бешенство: он выделил неклеточный агент этой болезни посредством заражения кролика кровью больной собаки.
В 1919 году у немца А. Левенштейна получилось заразить вирусом герпеса, взятым у человека, кролика. Годом позже его соотечественник В. Грютер подтвердил опыт своего коллеги и доказал, что подобная культивация на кроликах возможна.
В 1925 году двое ученых – Ф. Паркер и Б. Най – доказали, что вирус коровьей оспы в состоянии воспроизводиться в тканях организма животных. 6-ю годами позже Вудрафф и Э. Гудпасчер заявили, что культивация вируса оспы птиц может проводиться на оболочке куриных эмбрионов, тем самым открыв научному миру новый метод репродукции вирусов.
Процесс заражения клетки
Процесс культивирования вируса невозможен без наличия реагирующей на него клетки. Когда клетка найдена (это могут быть клетки куриных эмбрионов, части тканей, органов или даже целые животные), в нее вводится нуклеиновая кислота вируса, которая перепрограммирует генетическую информацию искомой клетки, заменяя ее своей. Обычно вредоносной частице удается поселиться в клетке, даже несмотря на систему противовирусной защиты и вырабатываемые организмом интерфероны.

После того как вирус проник через мембрану клетки, он начинает размножаться, проходя через 3 стадии. Сначала происходит транскрипция генома закрепившегося вируса, что означает перенос информации из системы ДНК в РНК, которая в последующем синтезируется в ускоренном темпе. Следующий этап – образование и созревание белков, которые послужат каркасом для дочерних вирусных тел.
На последней, заключительной стадии новосинтезированные вирусные тела увеличиваются в количестве. Когда их становится слишком много, разрывают мембрану и выходят из клетки, в которой изначально закрепился вирус. Стоит отметить, что образование вирионов (дочерних тел данного микроорганизма) не всегда приводит к гибели клетки-хозяина. Некоторые способны отпочковываться от мембраны, не вызывая ее разрыва, в то время как клетка продолжает производить вирусные тела.
Микробиология и ее методы
С течением времени биология, как наука, развивалась и впитывала в себя новые факты. Постепенно усложняясь, от нее стали отпочковываться разные направления: биомеханика, гидробиология, вирусология, космическая биология и многие другие. Такой раздел, как микробиология, изучает процессы жизнедеятельности микроорганизмов, в том числе и посредством заражения подопытного лабораторного животного вирусом. Таким образом, в микробиологии культивирование вирусов считается одним из основных способов получения информации, являясь ключевым инструментом биологического метода исследования.

Помимо биологического метода, суть которого заключается в исследовании действия вируса на организм животного и последующей его культивации, существуют и некоторые другие. Во многих случаях вредоносными микроорганизмами заражают куриные эмбрионы, поскольку довольно крупная доля вирусов, известных на сегодняшний день науке, способна реплицироваться именно в этой форме жизни. Однако чаще всего биологи в качестве рабочего материала используют тканевые культуры, поскольку они наиболее продуктивны в качестве метода культивирования.
Вирус и тканевые культуры
Тканевая культура представляет собой некую систему клеток в виде суспензии. Это слой определенного размера, обычно в одну клетку, который помещается на стекло сосуда. Чаще других используется первичная монослойная ткань. Добиться монослойности довольно трудно, сначала выбранную ткань (обычно это ткань сердца, плаценты или почек животных) нужно измельчить.
После измельчения биологи применяют расщепляющий белок фермент – трипсин, который разъединяет клетки ткани, уничтожая между ними межклеточную связь. После достижения разъединения клеток необходимо отмыть их от фермента и поместить в питательную среду, чтобы обеспечить рост получившейся клеточной культуры. Данной средой может послужить среда 199, которая характерна высоким содержанием глюкозы, солей и разных витаминов. Меняется питательная среда по прошествии 2–3 дней.

Кроме первичной ткани для культивирования вирусов также применяются так называемые перевариваемые ткани, которые, в свою очередь, делятся на нормальные и опухолевые. Они более стойкие, чем первичные, и способны длительно размножаться. Нормальными тканями могут послужить органы животных: почки барана, сердце обезьяны. В качестве опухолевых тканей обычно берут клетки HeLa, выделенные изначально из рака шейки матки, или клетки Hep-3, взятые из рака лимфы.
Вирус и куриные эмбрионы
Большинство известных науке вирусов можно выращивать в куриных эмбрионах. Они очень жизнеспособны и устойчивы к негативным внешним воздействиям. Срок, на котором заражается эмбрион, зависит от задач исследования и вида вируса, но обычно не превышает двух недель. Так, например, чтобы провести культивирование вируса гриппа, нужен 9-10-дневный эмбрион, а для того чтобы вырастить вирус паротита, достаточно и недельного эмбриона.
При работе с куриным эмбрионом все его зачатки тканей подвергаются заражению. Результативность культивации можно увидеть на финальной стадии: это может быть гибель эмбриона, а также дефекты развития в виде появления на оболочках эмбриона бляшек, состоящих из вирусных частиц – вирионов.
В любом случае данный метод культивирования и индикации вирусов имеет существенный недостаток, заключающийся в необходимости вскрытия эмбриона для захвата воспроизведенного вируса. Также полученная субстанция имеет в себе высокую концентрацию белка, который нужно удалить, чтобы вывести чистый инфекционный агент для дальнейшего производства медикаментов.

Вирус и организмы животных
В настоящее время использование лабораторных животных в качестве биологического материала в силу своей негуманности ограничено с 1986 года Европейской конвенцией о защите позвоночных животных. Несмотря на это, многие виды животных: мыши и крысы, хорьки и кролики, овцы, собаки и обезьяны – все равно используются в лабораторных работах и экспериментах, поскольку некоторые вирусы способы к репликации только в живых организмах.
Культивирование вирусов в организме животных проводится по-разному: для воспроизведения нейротропных вирусов (бешенство, энцефалит) заражается мозг животного, для создания респираторных (грипп) производится интраназальное заражение, для дерматотропных (оспа) – накожное и подкожное инфицирование.
Чаще прочих для культивации используются грызуны: мыши и крысы, сирийские хомячки, свинки. Их заражают нейротропными инфекционными агентами, аденовирусами, лимфоцитарным хориоменингитом посредством введения вредоносного микроорганизма в мозг или брюшную полость.

Некоторые вредоносные микроорганизмы гораздо быстрее развиваются в телах молодых особей, поэтому онкогенными вирусами заражаются в основном новорожденные крысы и сирийские хомячки. Без них также невозможно обойтись при культивации вирусов Коксаки. Стоит отметить, что биологический метод культивирования вирусов в микробиологии тоже имеет свои изъяны. Во-первых, организмы лабораторных животных загрязняются вирусами, в силу чего они испытывают недомогание. Во-вторых, чтобы получить чистый инфекционный агент, нужно провести его через другие культуры клеток, что увеличивает продолжительность исследования.
Показатели успеха заражения
Культивирование и индикация вирусов – два неразрывных процесса. Индикация позволяет понять, смог ли микроорганизм ужиться в зараженной клетке и получилось ли у него развиваться дальше. Говорить о факте репликации можно, если у животного наблюдаются основные признаки заболевания, а также если органы и ткани подверглись патоморфологическим изменениям. Часто в качестве индикации используется реакция гемагглютинации, которая показывает степень распространения вируса на основе выделяемого им белка гемагглютинина.
Современные особенности культивирования вирусов
Прогресс не стоит на месте, во всех научных сферах появляются инновационные методы, технологии. Микробиология и вирусология не являются исключением. Теперь вместо простого размещения клеточной культуры на сосудах применяется роллерный метод, при котором используемый материал находится на нескольких цилиндрических поверхностях, вращающихся по окружности и периодически омываемых питательной средой. Данный метод хорош тем, что он увеличивает число получаемых клеток и требует меньший расход питательного материала.

Общий вывод
Культивировать вирусы, то есть создавать их в искусственных средах, человек начал совсем недавно. Поначалу заражались организмы животных с целью изучения принципа действия инфекционных агентов и выработки препаратов против них. Благодаря микробиологии, вирусологии и эпизоотологии человечество избавилось от таких смертельной опасности таких заболеваний, как чума, туберкулез, бешенство, корь.
Сейчас для культивации вирусов в основном используются отдельные тканевые культуры и куриные эмбрионы. Посредством различных манипуляций живые клетки заражаются, в них происходит созревание вирусных тел, которые потом выходят за клеточное пространство. Созревшие вирусы собираются биологами для дальнейшего изучения.
Читайте также:


