Асцит при инфекционном перитоните
Инфекционный перитонит – вирусное заболевание кошек, характеризующееся перитонитом, лихорадкой, дегидратацией ткани, отеками брюшной полости и анорексией (отказ от корма).
Заболевание у кошек протекает в трех формах — экссудативной ( влажной), пролиферативной (сухой) и у большинства кошек заболевание протекает бессимптомно.
Более часто болеют кошки в возрасте от 6 месяцев до 5 лет .
Возбудитель – РНК – содержащий вирус, принадлежащий к роду Coronavirus, семейству Coronaviridae. Вирионы полиморфны, величиной 80-120 нм. На поверхности вириона имеются характерные булавовидные выступы в виде солнечной короны. Вирус в антигеном отношении однороден и серологически идентичен. Вирус размножается в культуре клеток почек и щитовидной железы, при низких температурах хорошо сохраняется, но очень чувствителен к теплу и свету.
Эпизоотологические данные. Источником возбудителя инфекции являются больные и переболевшие кошки. Вирус выделяется у кошек начиная со второй половины инкубационного периода и в течение 2-3 месяцев после выздоровления с носовыми истечениями, мочой и калом. Заражение инфекционным перитонитом у кошек в основном происходит алиментарным путем, через рот, возможно заражение кошки и воздушно-капельным путем.
К возбудителю чувствительны только кошки, иногда котята.
Патогенез. Коронаровирус, вызывающий инфекционный перитонит, мало тропичны к эпителиальным клеткам кишечника. Первоначально вирус размножается в макрофагах, которые разносят его по всему организму кошки. В результате этого инфекция принимает генерализованный характер.
Попав в организм кошки короновирус сначала размножается в миндалинах или кишечнике и только потом попадает в регионарные лимфатические узлы. В результате этого возникает первичная виремия. С током крови вирус заносится во многие органы и ткани, особенно в те, которые содержат большое количество кровеносных сосудов и в своем составе имеют много макрофагов.
В последующем у больной кошки возникает вторичная виремия, за счет разноса вируса в макрофагах.
В том случае, когда у кошки хорошая резистентность и она способна на полноценный иммунный ответ, размножение короновируса в макрофагах не будет происходить и болезнь у кошки не разовьется.
В случае отсутствия у кошки адекватной иммунной реакции, несмотря на наличие специфических антител, коронаровирус будет продолжать размножаться в макрофагах Макрофаги будут скапливаться вокруг кровеносных сосудов преимущественно под серозными оболочками и интерстиции различных органов, приводя к развитию экссудативной формы инфекционного перитонита. Эта форма перитонита у кошек развивается быстро и вызывает гибель кошки в течение нескольких недель.
В том случае, когда иммунный ответ слабый, то у кошки развивается пролиферативная форма болезни. Инфекционный процесс длится до 6 месяцев.
Симптомы. Симптомы заболевания у кошек зависят от возраста, количества и вирулентности возбудителя и от силы иммунного ответа.
У котят заболевание сопровождается полной потерей аппетита (анорексия), температура тела повышается до 40° С и больше, перитонит, у отдельных животных плеврит.
У взрослых кошек вирусный перитонит протекает в двух формах: экссудативной и неэкссудативной.
Экссудативная форма вирусного перитонита сопровождается скоплением экссудата в брюшной или грудной полости. При проведении клинического осмотра ветеринарный специалист отмечает одышку, при аускультации нарушение сердечного ритма из-за скопления жидкости в сердечной сорочке, шумы в легких. В результате накопления жидкости в брюшной полости (асцит) отмечаем увеличение объема живота и его отвисание.
Неэкссудативная форма вирусного перитонита протекает с поражением глаз (конъюнктивит, поражение сетчатки глаза и радужной оболочки), печени ( печень увеличена, видимые слизистые оболочки анемичны и желтушные), почек (гломерулонефрит), легких (пневмония кошек), центральной нервной системы (парезы конечностей, манежные движения, повышенная кожная чувствительность). Данная форма вирусного перитонита через несколько недель или месяцев заканчивается смертью животного.
При конъюнктивите владельцы отмечают гнойные выделения из глаз. Исследованием при помощи УЗИ на поверхности почек отмечаем гранулемы, печень увеличена, бугристая, с очагами некроза.
Диагноз на инфекционный перитонит в ветеринарной клинике ставят на основании симптомов заболевания, результатов ультразвукового и гематологического исследования, при экссудативной форме исследования асцитной жидкости, результатов рентгенологического исследования грудной и брюшной полостей. Кровь и асцитную жидкость в ветеринарной лаборатории исследуют по ПЦР.
Дифференциальный диагноз. При проведении дифференциальной диагностики экссудативной формы инфекционного перитонита ветеринарные специалисты должны исключить токсоплазмоз, бактериальный перитонит, асциты сердечного и почечного происхождения, опухоли, травмы и сердечную недостаточность, при неэкссудативной форме болезни — токсоплазмоз, туберкулез, лимфосаркоматоз.
Лечение. Лечение заболевания должно быть комплексным. Больной кошке назначают диету, состоящую из легкопереваримых и витаминизированных кормов. Назначается курс антибиотикотерапии из группы цефалоспоринов, сульфаниламидные препараты которые необходимо вводить внутримышечно, подкожно и внутривенно с учетом тяжести животного. При наличии асцита делают пункцию брюшной полости, с целью эвакуации экссудата. Назначают тилозин (160мг/кг) в течение двух дней, преднизолон (2мг/кг), мочегонные (гексаметилентетрамин, лазикс, верошпирон и др.). Проводится симптоматическое лечение — прием болеутоляющих препаратов, для поддержании сердечно сосудистой системы — сердечные препараты( сульфакамфокаин, кофеин). Иногда больной кошке проводят переливание крови. При развитии у кошки острого перитонита в первые часы на область живота прикладываем холод. Иногда в ветеринарных клиниках назначают химиотерапию и гормональные средства.
Профилактика. Профилактика инфекционного перитонита складывается из общих мер профилактики — полноценное, сбалансированное кормление. Периодическая обработка от глист и блох у кошек, клещей. Во время прогулки избегать контакта с бродячими животными. Избегать применения гормональных препаратов. Исходя из того, что вирус малоустойчив и легко уничтожается простыми дезинфицирующими средствами, рекомендуется применять нашатырный спирт или разведенный водой (1:32) отбеливатель, владельцы должны регулярно проводить дезинфекцию помещения для кошек.
Асцит - это состояние, при котором в брюшной полости появляется свободная жидкость в больших количествах.
Асцит является следствием цирроза печени в 75%; злокачественных новообразований - в 10%; сердечной недостаточности в 5% случаев.
В клинической картине у пациентов отмечается вздутие живота и прогрессирующее нарастание веса.
Диагноз основывается на результатах физикального и визуализирующих (рентгенологических, ультразвуковых) методов исследования.
Лечение заключается в назначении бессолевой диеты, диуретиков. Больным может производиться терапевтический лапароцентез, выполняются хирургические вмешательства. Пациенты с асцитом - кандидаты на трансплантацию печени.
Наиболее частым осложнением асцита является спонтанный бактериальный перитонит . Он возникает при инфицировании асцитической жидкости, которое в 90% случаев происходит спонтанно. У больных появляются боли в животе, повышается температура тела.
Для диагностики этого осложнения производится исследование асцитической жидкости. Для лечения спонтанного бактериального перитонита назначаются антибактериальные препараты.
-
Классификация асцита
Асцит классифицируется в зависимости от количества жидкости, наличия инфицирования асцитической жидкости и варианту ответа на медикаментозную терапию.
- По количеству жидкости в брюшной полости:
- Небольшое количество жидкости.
- Умеренное количество жидкости.
- Значительное количество жидкости (напряженный, массивный асцит).
- По инфицированности содержимого:
- Стерильное содержимое.
- Инфицированное содержимое.
- Спонтанный бактериальный перитонит.
- По варианту ответа на медикаментозную терапию:
- Асцит поддающийся медикаментозной терапии.
- Рефрактерный асцит.
Асцит, который не может быть устранен, или ранний рецидив которого не может быть адекватно предотвращен лечением.
- Асцит, резистентный к диуретикам: асцит, рефрактерный к диете с ограничением натрия и интенсивной терапии диуретиками ( спиронолактон 400 мг/день, фуросемид 160 мг/день в течение не менее 1 недели; диета с ограничением поваренной соли менее 5,2 г/день).
- Асцит, не контролированный диуретиками: асцит, рефрактерный к терапии из-за развития вызванных диуретиками осложнений, которые препятствуют применению эффективных дозировок диуретиков.
- Эпидемиология асцита
Асцит является следствием цирроза печени в 75%; злокачественных новообразований - в 10%; сердечной недостаточности - в 5% случаев.
Примерно у половины пациентов с циррозом печени асцит развивается в течение 10 лет от начала заболевания. Он обусловлен нарушениями почечной функции, портального и висцерального кровообращения.
Примерно 50% пациентов с цирротическим асцитом умирают в течение 2 лет от начала заболевания. Показатели однолетней выживаемости у больных с асцитом, резистентным к терапии, составляют 50%.
У здоровых мужчин внутриперитонеальная жидкость обнаруживается в меньших количествах, чем у женщин, у которых ее объем составляет примерно 20 мл (в зависимости от фазы менструального цикла). При асците этот объем значительно увеличивается.
Частота возникновения спонтанного бактериального перитонита составляет 15-20%.
-
Этиология и факторы риска развития асцита
- Факторы риска при отсутствии патологических процессов в брюшине.
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
- Цирроз печени .
- Алкогольный гепатит.
- Фулминантная печеночная недостаточность.
- Метастазы в печень .
- Хроническая сердечная недостаточность .
- Констриктивный перикардит .
- Синдром Бадда-Киари .
- Обструкция нижней полой вены.
- Гипоальбуминемия (градиент концентрации альбумина сыворотка-асцит 11г/л) и другими причинами (градиент концентрации альбумина сыворотка-асцит 225 мЕ/мл (или выше верхней границы нормы для сыворотки крови).
О рефрактерном асците свидетельствует отсутствие эффекта от проводимой терапии, которая заключается в назначении пациенту бессолевой диеты и диуретиков в высоких дозах.
Клинически различают две формы рефрактерного асцита:
- Асцит с ежедневной потерей менее чем 200 г массы тела (несмотря на ограничения натрия) и прием 400 мг спиронолактона (Верошпирон) или 30 мг амилорида (Амипразид, Арумил, Мидамор), а также 160 мг фуросемида (Лазикс) в течение 2 недель.
- Асцит, который невозможно контролировать; рецидивирующий асцит, обострения которого невозможно предупредить, назначая диуретики в дозах, не вызывающих побочных явлений.
- Основные диагностические критерии гепаторенального синдрома:
- Гепаторенальный синдром развивается у пациентов с хроническими или острыми заболеваниями печени, выраженной печеночной недостаточностью, портальной гипертензией и асцитом.
- Существуют два варианта течения гепаторенального синдрома.
- Синдром первого типа характеризуется прогрессирующим течением: быстрым нарастанием симптомов почечной недостаточности. Диагностика синдрома первого типа производится на основании увеличения почти вдвое содержания сывороточного креатинина (более чем 1,5 мг/дл) или 50%-ным снижением суточного клиренса креатинина (менее 40 мл/мин) в течение 2 недель. Пациенты с синдромом первого типа нуждаются в трансплантации печени. В противном случае синдром заканчивается летально у 90% больных.
- Для синдрома второго типа характерно медленно прогрессирующее течение.
- Отсутствие шока, текущей бактериальной инфекции, данных о приеме нефротоксических препаратов, отсутствие диареи и рвоты, потери жидкости с почками (снижение веса более чем на 500 г в течение нескольких дней у пациентов с асцитом без периферических отеков и более 1 кг/сут у больных с периферическими отеками).
- Отсутствие улучшения почечной функции (сохранение уровня сывороточного креатинина более чем 1,5 мг/дл и суточного клиренса креатинина менее 40 мл/мин) после назначения диуретиков и увеличения объема плазмы за счет введения 1,5 л изотонического раствора.
- Протеинурия менее 500 мг/дл и отсутствие ультразвуковых признаков поражения почечной паренхимы или обструктивной уропатии.
- Дополнительные диагностические критерии гепаторенального синдрома:
- Объем суточной мочи менее 500 мл/сут.
- Концентрация натрия в моче менее 10 мЭкв/л.
- Осмолярность мочи выше, чем осмолярность крови.
- Концентрация натрия в сыворотке крови менее 130 мЭкв/л.
- Количество эритроцитов в моче более 50 в поле зрения.
Немедикаментозная терапия асцита заключается в соблюдении определенного режима жизни и ограничений в диете.
Постельный режим и ограничение потребления натрия являются эффективными терапевтическими мероприятиями у 10% пациентов с асцитом.
Ограничения в диете и лечение диуретиками оказывают терапевтический эффект у 90% пациентов с асцитом. При отсутствии эффекта или при выраженном асците необходимо стационарное лечение.
Больные с асцитом, не получающие диуретиков, ежедневно экскретируют почками примерно 20 ммоль/сут натрия.
Отрицательный баланс натрия может быть достигнут благодаря ограничению потребления натрия с пищей до 22 ммоль/сут, что затруднительно для больных. Как правило, удается поддерживать количество натрия в пище в количестве 44 ммоль/сут.
В пищевом рационе пациентов с асцитом должны содержаться низкие количества соли (1-1,5 г/сут или 40-60 ммоль/сут).
Инфекция при циррозе печени – это патологический процесс, который вызывается инвазией в норме стерильных тканей, органов и полостей патогенными и условно-патогенными микроорганизмами. Данное осложнение встречается довольно часто у пациентов с циррозом печени, особенно у тех, кто находится на противовирусной терапии. Основной механизм возникновения инфекции – бактериальная транслокация кишечной микрофлоры через стенки кишечника в кровь вследствие таких причин, как повышение кишечной проницаемости, в той или иной степени выраженной иммунной дисфункции, избыточного бактериального роста.
Избыточный бактериальный рост рассматривается как один из механизмов, способствующих бактериальной транслокации через брыжеечные лимфоузлы с последующей циркуляцией микроорганизмов и их компонентов в крови. Кроме того, у пациентов могут быть отдаленные очаги инфекции (инфекции кожи, мочевого тракта, легких и т. д.), вызванные, к примеру, установкой внутривенного периферического катетера. Возникает бактериемия или бактериоасцит, и в том случае, если активность опсонинов асцитической жидкости удовлетворительна, у такого пациента шанс бактериоасцита незначителен, если же нет – существует большой риск развития спонтанного бактериального перитонита.
В настоящее время инфекции подразделяют на 2 большие группы: внутрибольничные, или нозокомиальные, и внебольничные инфекции. Важность данной классификации очевидна, т. к. в соответствии с принятыми подходами антибактериальной терапии это должно влиять на выбор антибиотика. Если инфекция у пациента развивается более чем через 48 ч после поступления в стационар, она относится к первой группе (нозокомиальная инфекция).
– пациенты ранее находились в медицинских организациях или гемодиализных центрах и получали внутривенно химиопрепараты за 30 дней до госпитализации;
– пациенты были госпитализированы как минимум на 2 дня и прооперированы за 90-180 дней до возникновения инфекции;
– пациенты получали помощь по типу стационара на дому или сестринского ухода.Среди инфекций наиболее часто встречаются спонтанный бактериальный перитонит, инфекции мочевого тракта, пневмонии, инфекции кожи и мягких тканей. У пациентов, получающих двойную противовирусную терапию, на первое место выходят пневмонии, затем – кожные инфекции, инфекции полости рта, урогенитальные, гастроинтестинальные инфекции. Риск развития инфекции в данном случае зависит от длительности получаемой терапии, возраста пациента, наличия фиброза, исходной гипергликемии и ряда других причин.
В данной ситуации очень важны ранняя диагностика и агрессивная терапия. Условно проявления инфекций можно разделить на 2 большие группы: общие симптомы и симптомы локальные, которые связаны с вовлечением в патологический процесс того или иного органа.
Общими симптомами могут быть недомогание, утомляемость, озноб, тошнота, рвота, диарея и нарушения сознания. При осмотре пациента обращают на себя внимание проявление у него таких симптомов, как гипертермия, гипотермия, тахипноэ, тахикардия, артериальная гипертензия, желтуха и нарастающая сыпь. Однако в некоторых случаях симптомы могут отсутствовать, и обнаружить наличие инфекции у пациента можно только по картине крови. Исключить инфекцию необходимо у каждого пациента с циррозом печени в случае появления у него какого-либо нарушения сознания.
Локальными симптомами при спонтанном бактериальном перитоните могут быть боли в животе, болезненность при пальпации, однако данные клинические признаки могут и вовсе отсутствовать; при инфекциях мочевого тракта – дизурия, болевые ощущения; при пневмонии – кашель, боли в груди, локальная болезненность, отек, эритема, изменение сознания и пр.
Лабораторная диагностика при подозрениях на любую инфекцию включает в себя общий анализ крови, определение С-реактивного белка и прокальцитонина (73% чувствительности, 63% специфичности).
Для диагностики инфекций мочевых путей рекомендуется использование высокочувствительного теста – определение лейкоцитарной эстеразы в моче.
Для диагностики пневмонии также недавно появились заслуживающие внимания тесты – исследования антигена пневмококка и легионеллы в моче (чувствительность данного теста – до 80%, специфичность – свыше 90%). Тест занимает около 15 минут и позволяет определять микроорганизмы даже после того, как назначена антибактериальная терапия, что порой бывает критически важным. В случае наличия одного из вышеперечисленных признаков пневмонии пациента следует лечить амбулаторно, при появлении 2 и более признаков необходимы госпитализация и безотлагательное лечение.
В случае бактериального перитонита необходимо дифференцировать спонтанный перитонит от вторичного, т. к. последний является хирургической инфекцией и, соответственно, решение данного вопроса находится в компетенции хирургов. При вторичном бактериальном перитоните, так же как и при спонтанном, отмечается полиморфноядерный лейкоцитоз асцитической жидкости, однако содержание белка, как правило, более 10 г/л, содержание глюкозы 250 (как правило, наблюдается у пациентов после антибактериальной терапии либо в результате допущенных технических погрешностей при взятии жидкости)); мономикробный ненейтрофильный спонтанный бактериальный перитонит, который развивается у 60-80% пациентов (посев выявляет 1 микроорганизм, количество нейтрофилов 250 (развивается, как правило, в результате повреждения кишечника)).
1. Наличие самой инфекции, установленной или предполагаемой.
2. Повышение температуры выше 38°С или ее понижение ниже 36°С;
3. ЧСС >90.
4. Лейкоциты >12 000 илиКаждый ветеринарный врач сталкивается с проблемой асцитов у животных и должен знать все тонкости диагностирования этого состояния.
Асцит
Это патологическое накопление свободной жидкости в брюшной полости. В нормальном состоянии там всегда есть вещество, выделяемое брюшиной и обеспечивающее скольжение брюшинных листков, которые выстилают внутренние органы и ограничивают саму полость; кроме того эта жидкость необходима, чтобы не происходило склеивания органов. При этом жидкость всасывается самой же брюшиной.
Однако при различных заболеваниях жидкость в брюшной полости начинает продуцироваться в слишком большом количестве и при этом перестает всасываться брюшиной. Кроме того параллельно могут образовываться и другие жидкости – кровь в результате внутрибрюшного кровотечения, которое объясняется травмой внутренних органов, гинекологическими заболеваниями и т.д.; гнойно-воспалительная жидкость в результате кишечной непроходимости или прободной язвы желудка. Объем жидкости может достигать от 1 до 10 литров, следствием чего является значительное вздутие живота. Скорость увеличения (от незначительного до очень большого) довольно низкая.
Патогенез развития практически всех асцитов связан с усилением кровотока во внутренних органах и портальной гипертензией. Основным источником формирования асцита является печеночная лимфа, образующаяся вследствие повышенного пропотевания компонентов плазмы через синусоидальный эндотелий.
Виды асцита
Это наиболее часто встречаемый вид асцита (до 80% всех случаев). Он может быть вызван первичными опухолями печени или метастазами из других органов.
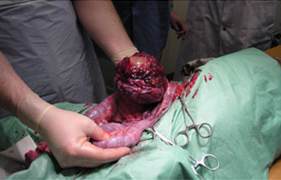
Слева - На фото опухоль яичника, вызвавшая асцит.
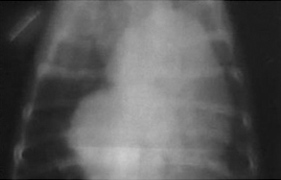
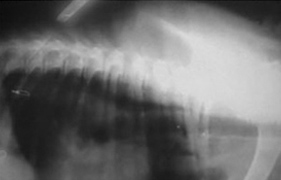
В центре - Асцит, вызванный хондросаркомой в грудной полости у лабрадора.
Справа - После удаления пораженного легкого жидкость из брюшной полости полностью рассосалась.В нашей ветеринарной практике встречался после травм у собак и кошек или при опухолях поджелудочной железы.
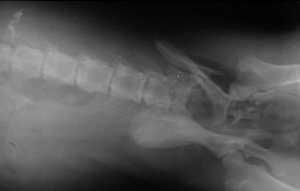
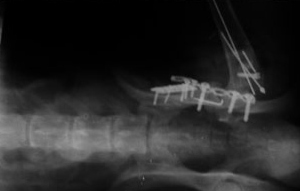
Слева - Асцит при панкреатите. Вызван разрывом поджелудочной железы в результате ДТП.
Справа - После операции жидкость из полости удаленаА также асцит, встречающийся при портокавальных шунтах.
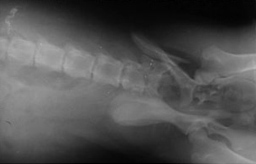
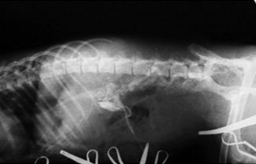
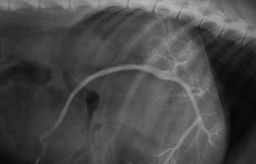
Слева - Портография спаниеля. Портоковальный шунт.
В центре - Повторная портография спаниеля.
Справа - Портография овчарки в начальной стадии цирроза печени. Расширение сосудов.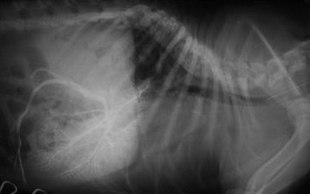
Рис. Французский бульдог. Отсутствие портального кровотока в правой латеральной доли печени. Асцит. Портальное давление 30 см.Нормальное давление в каудальной полой вене составляет 2-7 см водного столба, при повышении давления более 15-20 см возможно развитие асцита.
Спонтанный бактериальный асцит, перитонит связан с проникновением в асцитическую жидкость главным образом грам отрицательной микрофлоры.
- Переполнение мочевого пузыря
- Кисты яичников или предстательной железы
- Беременность
- Патологические изменения матки
Диагностика асцитов
Практика ветеринарной клиники неврологии, травматологии и интенсивной терапии доктора Сотникова показывает, что при асците сначала необходимо провести анализ асцитической жидкости. В 80% случаев этот простой и весьма не дорогостоящий метод дает практически точный диагноз. Результаты лабораторных исследований дают план действий для дальнейшего лечения или продолжения диагностического обследования.
При застойных формах асцита необходимо провести кардиологическое обследование, включающее УЗИ сердца, ЭКГ и рентген грудной полости. Далее необходимо провести ультразвуковое изучение органов брюшной полости.
Параллельно с этими методами диагностики должны проводиться биохимический и клинический анализ крови. При биохимическом анализе обращают внимание на АЛТ, АСТ, щелочную фосфатазу, уровень билирубина и альбумина. По некоторым данным градиент сывороточного и асцитического альбумина, превышающий 1,1г%, указывает на наличие портальной гипертензии. Мочевина может оказаться важным показателем особенно в диагностике циррозов и степени почечной недостаточности.
Если при проведенных лабораторных исследованиях стало ясно, что главной причиной асцита являются изменения в печени, то далее необходимо провести цитологическое, гистологическое исследования именно этого органа.
Очень важным исследованием, а иногда и решающим для постановки диагноза и дальнейшего прогноза лечения, является портография. Снабжение кислородом печени осуществляется на 80% кровью из портальной вены, поэтому вполне закономерно, что при повреждении портального кровотока происходят изменения в структуре печени.
При проведении портографии необходимо также провести измерение давления в портальной вене. Нормальное портальное давление должно быть на уровне 8-13 см водного столба. При повышении давления до 18-20 см возможно развитие асцита. Значимым диагностическим тестом может стать разница давления в полой вене и в воротной вене. Разница должна составлять 4-6 см. Только после постановки основного диагноза возможно проведение лечения.
Ограничение клинических задач коррекцией только асцитического синдрома может ухудшить продолжительность и качество жизни пациента в целом!
Следует отметить, что проведение лапароцентеза с удалением значительного количества жидкости ухудшает течение и прогноз заболевания. Такие действия практически никогда не приводят к излечению пациента и могут применяться только в исключительных случаях. Крайне важно проводить лечение основного заболевания, вызвавшего асцит.
Для определения заболевания следует обратиться в ветеринарную клинику, которая располагает всеми видами диагностики. Причем сделать это необходимо как можно скорее. Даже при незначительном вздутии живота у вашего питомца, обращайтесь к ветеринарным врачам, только так можно вовремя установить причину асцита и сделать все необходимое для скорейшего выздоровления.
Печеночно-почечный синдром определяется как прогрессирующая олигурическая почечная недостаточность на фоне хронических и острых болезней печени при отсутствии других известных клинических или патологических причин для почечной недостаточности. Печеночно-почечный синдром характеризуется острым сужением сосудов наиболее ярко выраженным в корковых областях почек. Печеночно-почечный синдром при циррозе рассматривается как крайняя степень патофизиологического развития болезни, ведущая к удержанию ионов натрия и воды у больных.
Одной из основных причин печеночно-почечного синдрома является дисбаланс между внутрипочечным сужением и расширением сосудов. Его патогенез определяется гемодинамическими изменениями и нарушением прямых печеночно-почечных связей. Последнее включает в себя гепаторенальный рефлекс, который активируется разрушением гепатоцитов, увеличением внутрисинусоидального давления, что ведет к значительному снижению клубочковой фильтрации. Более того, снижение скорости образования в печени мочегонных факторов также может оказывать свое влияние, однако эти факторы пока еще не полностью идентифицированы. Гемодинамические изменения характеризуются периферическим расширением сосудов, что частично происходит в результате увеличения образования оксида азота вследствие эндотоксемии. Для поддержания кровяного давления расширение сосудов балансируется активацией симпатической нервной и различных гуморальных систем, регулирующих давление внутри организма. Все это одновременно является пусковым механизмом задержки ионов натрия и воды. В результате возникает гипердинамическая циркуляция, однако компенсаторные механизмы, очевидно, недостаточно эффективны для того, чтобы противостоять расширению сосудов и поэтому сохраняется ретенция натрия и воды. Таким образом, печеночно-почечный синдром имеет полное сходство с преренальной азотемией.
Печеночно-почечный синдром развивается при дальнейшем прогрессировании ренальной вазоконстрикции в результате уменьшения внутрисосудистого объема после парацентеза, кровотечений, больших доз диуретиков и, например, при длительном применении нестероидных противовоспалительных препаратов. Клинически печеночно-почечный синдром характеризуется олигурией, концентрированной, почти лишенной натрия, мочой на ранних стадиях без нарушений в моче количества элементов седиментации.
Таким образом, печеночно-почечный синдром имеет сходство с преренальной азотемией (уремией) и отличается от последней потерей улучшения функциональной способности почек после восстановления объема плазмы крови. Большинство больных циррозом печени при печеночно-почечного синдрома без экстренного соответствующего лечения погибают.
Стойкая, не исчезающая при коррекции гиповолемии, функциональная почечная недостаточность у больных циррозом печени - гепаторенальный синдром (печеночная нефропатия) - развивается чаще всего на фоне нарастающего и резистентного к лечению асцита, резко нарушенной функции печени, значительно выраженной задержки воды, гипонатриемии и значительного снижения содержания натрия в моче в результате нарушенной его экскреции почками. Печеночно-почечный синдром является следствием остро нарастающей гиповолемии - при кровотечении, рвоте, диарее, септицемии, эвакуации большого объема асцитической жидкости при парацентезе или чрезмерном диурезе при передозировке мочегонных средств. Аналогичный синдром со стойкой азотемией имеет место при фульминантной (молниеносной) печеночной недостаточности у больных с острым и подострым некрозом печени. У этих больных, а не у больных циррозом, целесообразно проводить гемодиализ. Печеночно-почечный синдром следует отличать от частых при циррозе печени эпизодов обратимой преренальной азотемии с метаболическим алкалозом, которые могут повторяться в течение нескольких лет из-за снижения объема крови при рвоте, диарее, полиурии или желудочно-кишечном кровотечении. В терминальной стадии цирроза печени печеночно-почечный синдром развивается у 80% больных, однако основной причиной смерти является не почечная недостаточность, а печеночная кома.
Как уже указывалось, в основе гепаторенального синдрома лежит почечная вазоконстрикция, главным образом в наружном слое корковой зоны почек (наружная кортикальная ишемия). Как следствие этого, возникает резкое снижение почечного кровотока и гломерулярной фильтрации и дальнейшее уменьшение выделения натрия почками при нормальной способности к канальцевой реабсорбции.
Печеночно-почечный синдром проявляется постепенным нарастанием в плазме крови содержания креатинина (> 212 мкмоль/л) и мочевины (> 8,3 мкмоль/л, иногда до 33 мкмоль/л), олигурией ( 40 ммоль, но всегда > 12 ммоль за сут. (соотношение осмолярность мочи и осмолярность плазмы 1:1). Важно также иметь в виду, что у 60-85% больных циррозом печени (чаще алкогольным) развивается нефропатия, обусловленная отложением в мезангии почечных клубочков иммуноглобулинов, в основном за счет IgA, в сочетании с С 3 - компонентом комплемента, так называемая IgA-нефропатия. Это осложнение обычно протекает клинически латентно и не сопровождается хронической почечной недостаточностью или артериальной гипертонией. Однако у 1/4 больных отмечаются изменения мочи, соответствующие изменениям при гломерулонефрите или при нефротическом синдроме, в единичных случаях наблюдается массивная гематурия. Цирроз печени нередко может сочетаться с хроническим пиелонефритом.
Мера профилактики печеночно-почечного синдрома при циррозе печени - тщательное устранение факторов, которые могут способствовать гиповолемии: строгий контроль за применением диуретических препаратов, эвакуацией больших количеств асцитической жидкости при парацентезах, дозой нестероидных противовоспалительных средств, борьба с инфекционными осложнениями и экстренные мероприятия для остановки кровотечений.
При печеночно-почечном синдроме следует ограничить введение белка до 0,5 г/кг (при таком режиме отрицательный азотистый баланс не развивается), ионов натрия и воды до 800-1000 мл/сут., так как для больных с почечной недостаточностью свойственно резкое снижение способности выделять жидкость, вследствие чего развивается гипонатриемия разведения и гипоосмолярность плазмы. Эффективно введение 5% р-ра глюкозы, подавляющей распад белка, особенно при белковом голодании. Рекомендовано сочетать инфузии альбумина по 50 г каждые 2 ч и 20% р-ра маннитола по 150 мл каждые 2 ч и далее - назначение фуросемида и антагонистов альдостерона (спиронолактона). При отсутствии эффекта прибегают к назначению орнитин-вазопрессина (25 ЕД через 12 ч и допамина 100 мг через 12 ч). Если и эти лечебные мероприятия при печеночно-почечном синдроме оказываются неэффективными, необходима трансплантация печени или наложение трансюгулярного (трансшейного) внутрипеченочного портосистемного стент-шунта (TIPS). Ввиду того что аргинин, как составляющий компонент цитраргинина, является донатором оксида азота, его применение может усугубить почечную недостаточность при печеночно-почечном синдроме.
Асцит-перитонит относится к тяжелейшим осложнениям портальной гипертензии с отечно-асцитическим синдромом. Он развивается вследствие спонтанного инфицирования асцитической жидкости возбудителями кишечного происхождения или при парентеральном попадании инфекции в организм.
Бактериальные инфекции являются частыми осложнениями у пациентов с портальной гипертензией, особенно у больных с циррозом. Среди них спонтанный бактериальный перитонит является наиболее известным и часто встречающимся в клинической практике, так как он широко распространен и ассоциируется с высоким уровнем смертности. Патофизиология спонтанного бактериального перитонита не полностью ясна, но скорее всего он возникает в связи с переходом бактерий из кишечного просвета в мезентериальные брыжеечные лимфатические узлы - феномен известный как бактериальная транслокация, системная циркуляция бактерий и в конечном итоге - переход их в асцитическую жидкость.
Асцит-перитонит наблюдается у 7-8% больных декомпенсированным циррозом печени. Летальность при этом осложнении, достигающую 80-100%, можно значительно снизить при своевременном диагнозе и проведении срочной антибактериальной терапии.
При бактериологическом исследовании чаще всего высевают Е. albi, а также стрептококки, Klebsiella, стафилококки и протей. Характерными симптомами являются абдоминальная боль, болезненность при пальпации живота, лихорадка, парез кишок с исчезновением шума кишечной перистальтики, зачастую без симптомов раздражения брюшины, в гемограмме - лейкоцитоз. У больных с асцитом-перитонитом прогрессирующе нарастают явления печеночной энцефалопатии, часто развиваются сепсис, острые кровотечения из вен пищевода и желудка, гепаторенальный синдром. Асцитическая жидкость, полученная при диагностическом парацентезе, более чем у 70% больных мутная, содержит > 400 лейкоцитов в 1 мкл, 15-80% которых представлены полиморфно-ядерными лейкоцитами, повышена концентрация лактата в асцитической жидкости.
При асците-перитоните необходимо экстренное назначение антибиотиков широкого спектра действия после диагностической пункции живота для бактериологического исследования асцитической жидкости.
Спонтанный бактериальный перитонит является мономикробной инфекцией, как правило, вызываемой грамнегативными бактериями. Цефалоспорины третьего поколения являются одним из вариантов лечения для пациентов со спонтанным бактериальным перитонитом, хотя последние исследования дают основание считать, что хинолоны (офлоксацин, ципрофлоксацин) также весьма эффективны при пероральном применении. При употреблении этих антибиотиков излечиваются 80-90% пациентов. Несмотря на высокий уровень излечиваемости, смертность очень высока (20-40%), что оправдывает использование профилактических мер у пациентов, имеющих предрасположенность к этому виду осложнений. Определены несколько подгрупп больных циррозом печени, которые представляют более высокий риск для развития асцита-перитонита:
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
Этиология асцита в 90% случаев связана с хроническими заболеваниями печени: портальной гипертензией (развившейся вследствие цирроза печени ), алкогольным гепатитом, обструкцией печеночной вены (синдром Бадда-Киари).
Непеченочными причинами асцита могут быть: заболевания сердца ( сердечная недостаточность , констриктивный перикардит), злокачественные новообразования (карциноматоз, псевдомиксома брюшины), заболевания брюшины (инфекционный перитонит), выраженная гипоальбуминемия (нефротический синдром), другие болезни (опухоли и кисты яичников, панкреатит , саркоидоз , системная красная волчанка, микседема).
Факторы риска возникновения асцита:
Читайте также:


